Некроз сетчатки глаза на фоне вируса
Обновлено: 18.04.2024
Острый некроз сетчатки, вызванный вирусом опоясывающего герпеса
Журнал: Вестник офтальмологии. 2020;136(6): 236‑241
Заболеваемость опоясывающим герпесом достаточно высока, а herpes zoster ophtalmicus является второй по частоте формой этого заболевания. Некротизирующие герпетические ретинопатии (в частности, острый некроз сетчатки) встречаются относительно редко: в мировой литературе в основном представлены описания отдельных клинических случаев. Однако они способны привести к полной потере зрения. В данном обзоре обобщены современные знания о причинах развития, особенностях диагностики и лечения острого некроза сетчатки. Проанализировано 40 статей за период 2011—2019 гг., находящихся в свободном доступе в базе данных EBSCO. Проведенный анализ данных литературы позволил систематизировать и в сжатой форме изложить современные представления о распространенности, клинических особенностях и тактике ведения больных с острым некрозом сетчатки герпетической этиологии. Выявлены некоторые противоречия, касающиеся диагностических критериев и хирургического лечения острого некроза сетчатки.
Дата принятия в печать:
В мире заболеваемость опоясывающим герпесом составляет 1,2—3,4 случая на 1000 человек, увеличиваясь до 3,9—11,8 на 1000 человек в год в возрастной группе 65 лет и старше[1]. Только в США прямые экономические потери, связанные с опоясывающим герпесом, оцениваются в 1,1 млн долларов в год [2].
Реактивации вируса опоясывающего герпеса (VZV — varicella zoster virus) способствует любое снижение T-клеточного иммунитета, включая возрастную иммуносупрессию, ВИЧ, злокачественные опухоли, химиотерапию, туберкулез, травмы и прием иммуносупрессантов [1].
Реактивацию VZV, персистирующего в сенсорных ганглиях, можно предотвратить с помощью вакцинации. Вакцинация особенно актуальна в возрасте старше 50 лет, когда риск возникновения опоясывающего герпеса многократно возрастает. Вакцина достаточно эффективна и хорошо переносится [3].
Примерно в 20% случаев (VZV) поражает первую ветвь тройничного нерва, вызывая появление характерной болезненной сыпи в области лба, носа и глаза. Подобное поражение носит название herpes zoster ophthalmicus (HZO) [4]. HZO встречается в 20 раз чаще, чем поражение второй и третьей (верхнечелюстная и нижнечелюстная) ветвей тройничного нерва [5], и уступает только локализации на туловище [3].
Клиническими проявлениями HZO являются лихорадка, головная боль, иногда делириозное состояние и очаговая неврологическая симптоматика [6]. Около 60% больных испытывают боль различной выраженности в области дерматома пораженного нерва [1], часто боль возникает или усиливается при причесывании [7].
Появление везикулезной сыпи — необязательный симптом: опоясывающий герпес без кожных проявлений носит название zoster sine herpete [3, 8].
Хотя случаи слепоты в исходе HZO редки, все же значительна частота осложнений с необратимыми повреждениями глаза: легкое снижение зрения регистрируется у 34% пациентов, среднетяжелое — у 5%, тяжелое — также у 5% [7].
Некротизирующие герпетические ретинопатии (НГР) — это группа редких осложнений с локализацией в заднем сегменте глаза, способных вызвать выраженное ухудшение зрения [9, 10].
К НГР относятся острый некроз сетчатки (acute retinal necrosis, ARN), прогрессирующий некроз наружных слоев сетчатки (progressive outer retinal necrosis, PORN) и цитомегаловирусный ретинит (CMV-ретинит) [9, 11].
Некоторые авторы предлагают рассматривать ARN и PORN не как самостоятельные клинические нозологии, а как варианты НГР, проявляющиеся в зависимости от иммунного статуса больного [9].
НГР могут быть вызваны VZV, вирусами простого герпеса (herpes simplex virus, HSV) 1-го и 2-го типов (HSV-1 и HSV-2), цитомегаловирусом и (редко) вирусом Эпштейна—Барр [12].
CMV и другие патогены способны вызывать некроз сетчатки, похожий на ARN [13]. Однако при поражении CMV или токсоплазмами не выполняются диагностические критерии ARN (см. далее) [14].
Спектр клинических проявлений зависит как от этиологии НГР, так и от активности иммунной системы [15]. Например, выраженность воспаления стекловидного тела при НГР зависит от степени иммуносупрессии: от легких преходящих эпизодов при выраженной иммуносупрессии (например, СПИД) до среднетяжелых и тяжелых форм при умеренной иммуносупрессии или нормальном иммунитете [12, 13, 16].
Риск развития CMV-ретинита и PORN особенно высок у пациентов с иммуносупрессией [12]. При системной иммуносупрессии вирусный ретинит развивается вдвое чаще [17].
Диагноз НГР обычно основывается на исчерпывающих клинико-анамнестических данных и результатах исследования глазного дна [19]. Тщательное выяснение иммунного статуса и наличия в недавнем времени опоясывающего лишая или ветряной оспы способствует установлению этиологии [18].
Характерным признаком НГР, выявляемым при исследовании глазного дна, является прогрессирующая атрофия сетчатки, ведущая к вторичной отслойке сетчатки с потерей зрения [9, 18].
Диагноз НГР может быть подтвержден в ранние сроки при исследовании внутриглазной жидкости (ВГЖ) методом полимеразной цепной реакции (ПЦР) [19]. Исследование только стекловидного тела или стекловидного тела и ВГЖ по эффективности диагностики не имеет преимуществ перед исследованием одной только ВГЖ [19, 20]. Высокая вирусная нагрузка является неблагоприятным прогностическим фактором в отношении сохранения зрения [21].
ПЦР ВГЖ может быть использована и для оценки эффективности лечения [21, 22].
Тяжесть НГР обусловлена повышенным риском отслойки сетчатки. При ARN и PORN отслойка сетчатки развивается быстрее, чем при CMV-ретините, что связано с более быстрым распространением повреждений [9].
Из-за редкости НГР универсальной схемы противовирусной терапии для каждого этиологического агента не разработано [9].
Острый некроз сетчатки (ARN) — это редкое неотложное офтальмологическое состояние, угрожающее потерей зрения в связи с некрозом и последующей отслойкой сетчатки. Обычно ARN свойственны быстрое прогрессирование при отсутствии лечения, расширение области поражения, некроз всей толщи сетчатки и сопутствующее воспаление стекловидного тела и передней камеры глаза [12, 23].
В типичных случаях ARN характеризуется периферическим некрозом сетчатки, окклюзионной артериолярной ретинопатией и внутриглазным воспалением разной степени выраженности. Обычно процесс односторонний, но при прогрессировании болезни в 10% случаев поражается и второй глаз [24].
По данным S. Khochtali и соавт. [25], у каждого третьего больного диагноз ARN врачами первичного звена не был установлен; в результате пациенты получали только глюкокортикостероиды (ГКС), что привело к ухудшению зрения. В Великобритании 45,5% больных из-за несвоевременной диагностики ARN получали системные ГКС без противовирусных препаратов [25].
При поздней диагностике ARN вероятна потеря зрения из-за склонности этого заболевания осложняться отслойкой сетчатки [26].
Степень потери зрения после перенесенного ARN зависит от площади пораженной сетчатки [26]. Наименьшие нарушения зрения отмечаются при ретините площадью менее 25%, более выраженные — при площади ретинита 25—50 и 100% [27].
На прогноз сильно влияет то, сколько времени прошло от начала болезни до начала лечения [26].
Впервые ARN был описан A. Urayama и соавторами в 1971 г. [28] как односторонний острый увеит, сопровождающийся артериитом сетчатки и появлением белых инфильтратов на периферии сетчатки с последующей ее отслойкой [14].
Обычно ARN вызывают VZV и HSV, но иногда также вирус Эпштейна—Барр, CMV и др. [26]. По разным оценкам, VZV выявляется при ARN в 25—83,7% случаев [29]. По-видимому, для разных возрастных групп характерна разная этиология ARN [25].
ARN встречается у мужчин и женщин любого возраста [29]. Средний возраст больных можно оценить в 35,7 года [25]. Обычно ARN развивается в возрасте от 20 до 60 лет, мужчины болеют ARN несколько чаще (70% случаев) [26].
Обычно ARN развивается у иммунокомпетентных пациентов [9], редко — у иммунокомпрометированных [26].
Описан случай ARN у 19-летней пациентки с лейкемией в анамнезе (ремиссия после трансплантации костного мозга) [30], у 52-летней женщины с ревматоидным артритом, которой был установлен интравитреальный имплант с дексаметазоном (по поводу резистентного макулярного отека). Известны случаи ARN после интравитреального введения триамцинолона [17].
Механизм развития ARN у ВИЧ-инфицированных принято связывать с нарушениями клеточного иммунитета, VZV-инфекцией и склонностью к гиперкоагуляции [26].
ARN — это редкая патология: 0,8—3,9% увеитов [29, 31]. Двусторонний ARN встречается в 8,7—33% случаев [25, 26, 29], причем глаза не обязательно поражаются одновременно: чаще всего поражение второго глаза происходит в течение 12—14 нед от начала болезни, однако в 3,4 и 13,6% случаев это происходило в течение 2 и 4 лет наблюдения соответственно [25, 32].
При ARN велик риск осложнений (таких как отслойка сетчатки, вовлечение макулы, зрительного нерва или второго глаза) и потери зрения [25]. Отслойка сетчатки регистрируется у 66% больных ARN (по данным C.Lau и соавторов — 60% [33]). Другие исследователи описывают это осложнение реже. Отслойка сетчатки может возникнуть через 32—71 день от манифестации заболевания, а иногда и в более поздние сроки [26].
Риск отслойки сетчатки повышается при вовлечении всех ее квадрантов или большой площади некроза сетчатки [26].
Клиническая картина ARN включает: снижение зрения, высыпания, боль в глазу, светобоязнь. Первоначальным проявлением может быть воспаление передних отделов глаза, поэтому на ранних стадиях ARN можно ошибочно принять за конъюнктивит или увеит. Чаще это процесс односторонний [23].
Диагностические критерии ARN были представлены Американским обществом по изучению увеитов (AUS) в 1994 г. Они основывались на клинических признаках и не включали результаты микробиологического исследования тканей и жидкостей глаза, хотя об этиологической роли герпесвирусов уже было известно [14].
Критерии AUS предполагают наличие всех пяти признаков: как минимум один очаг некроза с четкими границами на периферии сетчатки, быстрое прогрессирование болезни при отсутствии противовирусной терапии, периферическое распространение некроза, окклюзионная васкулопатия с вовлечением артериол и выраженная воспалительная реакция в стекловидном теле и передней камере. Если характеристики болезни с указанными критериями не совпадают, такую патологию называют просто некротизирующей герпетической ретинопатией [14, 34].
В 2015 г. H. Takase и коллегами предложен новый диагностический подход [14]:
I. Базовые понятия
1. Диагноз установлен на основании сочетания ранней глазной симптоматики, характера течения болезни и обнаружения вируса во ВГЖ.
2. Подозрение на ARN обоснованно при наличии ранней глазной симптоматики 1a и 1b (см. ниже); рекомендовано вирусологическое исследование ВГЖ и назначение противовирусных препаратов.
3. Заключительный диагноз определяется дальнейшим течением болезни и результатами вирусологических тестов.
4. ARN обычно регистрируется у иммунокомпетентных пациентов. Следует учитывать, что при наличии иммунодефицита возможно искажение симптоматики.
II. Диагностические критерии
1. Ранняя глазная симптоматика
1b. Беловато-желтые участки (или участок) на периферии сетчатки (гранулярные или пятнистые на ранней стадии, а затем постепенно сливающиеся).
1c. Артериит сетчатки.
1d. Гиперемия зрительного диска.
1e. Непрозрачность стекловидного тела, вызванная воспалением.
1f. Повышенное внутриглазное давление.
2. Характер прогрессирования
2a. Быстрое периферическое распространение очагов поражения сетчатки.
2b. Развитие разрыва или отслойки сетчатки.
2c. Окклюзия сосудов сетчатки.
2d. Атрофия зрительного нерва.
2e. Эффективность противовирусных препаратов.
3. Исследование ВГЖ на наличие вируса.
Положительный результат ПЦР или соответствующий коэффициент Гольдманна—Уитмер (соотношение специфических антител в плазме крови и ВГЖ) в отношении HSV-1, HSV-2 или VZV.
III. Классификация
1. ARN с подтвержденной вирусной этиологией
Наличие ранней глазной симптоматики (пункты 1a и 1b), одного из вариантов течения, представленных в пункте 2, и лабораторное подтверждение.
2. ARN неустановленной этиологии
Наличие 4 из 6 ранних глазных симптомов, включая 1a и 1b; наличие любых двух вариантов прогрессирования, представленных в пункте 2; отрицательный результат лабораторных исследований (или исследования не проводились).
Бляшки Кирилейса считаются проявлением иммунного ответа: они представляют собой скопление в стенках артерий иммунных клеток и продуктов воспалительной реакции [32]. Описан случай HZO, при котором количество бляшек Кирилейса увеличивалось, несмотря на высокие дозы ГКС; процесс распространялся вокруг оптического диска, в то время как воспаление затухало. Исчезновение бляшек началось только через 4 нед [32].
Прогностически неблагоприятными в отношении снижения остроты зрения факторами считаются: начало лечения более чем через 14 дней от появления глазных симптомов, вовлечение макулы или диска зрительного нерва, развитие отслойки сетчатки, вовлечение в процесс 25—50% сетчатки [35].
В настоящее время ПЦР стала более доступным методом, что позволило накопить много новых данных об ARN [13]. Более того, мультиплексная ПЦР-система, позволяющая проводить анализ на множество патогенов в небольшом объеме ВГЖ, показала свою эффективность при разных заболеваниях [36]. Используя эту систему в Японии у больных ARN, S. Sugita и соавторам удалось подтвердить этиологическую роль ВПГ-1, ВПГ-2 и VZV, но не других герпесвирусов и токсоплазмы [36].
Для классического ARN характерны сливной периферический ретинит [38], облитерирующий артериит и витриит. Бляшки Кирилейса при ARN можно видеть в одном глазу или в обоих (при двустороннем ARN) [32]. При обнаружении бляшек Кирилейса необходимо исключить ARN: осмотреть периферические отделы сетчатки, чтобы выявить очаги перенесенного ретинита и васкулита [39].
Хотя оптимального протокола лечения ARN пока не существует, не вызывает сомнений, что ранняя диагностика и своевременное начало лечения улучшают прогноз [14].
Лечение ARN включает внутривенное или интравитреальное введение противовирусных препаратов, ГКС и профилактическую лазерную демаркацию.
Препаратом выбора при лечении ARN является ацикловир для внутривенного введения в дозе 10 мг/кг каждые 8 ч в течение 10 дней с последующим переходом на пероральный прием 800 мг каждые 8 ч в течение 6—14 нед. В течение нескольких дней после начала терапии выраженность ретинита уменьшается. При отсутствии противовирусной терапии продолжительность ретинита составляет 6—12 нед [9]. Внутривенное введение ацикловира улучшает долгосрочный прогноз, снижает риск поражения второго глаза и частоту развития слепоты. При этом не было выявлено связи вовлечения второго глаза с недостаточными дозами ацикловира [26], однако хорошо известна нефротоксичность ацикловира, проявляющаяся у 12—48% больных. В большинстве случаев она обратима при раннем выявлении и прекращении приема препарата [24].
В определенных случаях необходимо введение ганцикловира или фоскарнета в стекловидное тело. Также используются таблетированные препараты с повышенной биодоступностью — валацикловир и фамцикловир [24].
Отслойка сетчатки развивается у 20—50% больных, несмотря на противовирусную терапию (обычно после того, как миновала острая фаза ARN). Витреоретинальные тракции обычно приводят к разрывам на границах пораженной и интактной сетчатки [29].
Для профилактики потери зрения и отслойки сетчатки при ARN успешно применена комбинация системных противовирусных препаратов и интравитреального фоскарнета [40]. Введение фоскарнета в стекловидное тело снижает вероятность отслойки сетчатки [23].
Системное введение ГКС на исход болезни не влияет, но затягивает процесс выздоровления [25].
При тяжелом ARN для снижения риска отслойки сетчатки рекомендуют профилактическую лазеропексию (демаркацию) и раннюю витрэктомию [17, 26], однако эффективность лазерной фотокоагуляции и ранней витрэктомии для профилактики отслойки сетчатки остается спорной [26].
Судить об эффективности лазерной ретинопексии трудно еще и потому, что при более тяжелом ARN воспаление стекловидного тела препятствует выполнению процедуры, т.е. метод применим при более легких формах ARN, при которых прогноз по сохранению зрения и так благоприятный. Лазерная ретинопексия не позволяет предотвратить вторичную отслойку сетчатки и в том случае, если после процедуры площадь некроза продолжает увеличиваться, выходя за пределы выполненной лазером демаркационной линии [26].
Поздние осложнения ARN требуют хирургического лечения; оно требуется в 51,6% случаев. Основным показанием к хирургическому лечению является отслойка сетчатки (96,87%) [26].
Заключение
ARN — это редкое осложнение HZO, способное вызвать выраженное ухудшение зрения. Он может развиваться как при наличии, так и при отсутствии иммуносупрессии и может быть вызван VZV, HSV и иногда вирусом Эпштейна—Барр.
В типичных случаях ARN характеризуется периферическим некрозом всей толщи сетчатки, окклюзионной артериолярной ретинопатией и сопутствующей воспалительной реакцией стекловидного тела и в передней камере глаза. Чаще процесс односторонний. Пациент может жаловаться на снижение зрения, высыпания, боль в глазу, светобоязнь.
Диагноз ARN правомерен при наличии пяти признаков: как минимум один очаг некроза с четкими границами на периферии сетчатки, быстрое прогрессирование болезни при отсутствии противовирусной терапии, периферическое распространение некроза, окклюзионная васкулопатия с вовлечением артериол и выраженная воспалительная реакция в стекловидном теле и передней камере.
Диагноз может быть подтвержден в ранние сроки при исследовании ВГЖ методом ПЦР. При этом высокая вирусная нагрузка является неблагоприятным прогностическим фактором в отношении сохранения зрения.
При отсутствии лечения ARN быстро прогрессирует. Риск отслойки сетчатки повышается при вовлечении всех квадрантов сетчатки или большой площади ее некроза.
Лечение ARN включает внутривенное или интравитреальное введение противовирусных препаратов (ацикловир, валацикловир, фамцикловир, ганцикловир или фоскарнет), местное применение ГКС и профилактическую лазерную коагуляцию.

Острый некроз сетчатки (ОНС) – редкое и крайне тяжелое заболевание, характеризующееся быстро прогрессирующим периферическим некротическим ретинитом, окклюзивным васкулитом, воспалительной реакцией в стекловидном теле и передней камере с последующим развитием отслойки сетчатки у 65%-72% больных Чаще всего причиной развития ОНС являются вирусы varicella-zoster и herpes simplex.
Общепризнанной считается вирусная этиология острого ретинального некроза; однако в качестве воз‑ будителя заболевания дополнительно может выступать другой инфекционный агент, в частности, микобактерия туберкулеза, в таком случае речь идет о так называемой, микст–инфекции.
При остром ретинальном некрозе вовлекаются преимущественно периферические отделы сетчатки, в то время как центральная область сетчатки, как прави‑ ло, остаётся интактной.
Методом ПЦР-диагностики при остром ретиналь‑ ном некрозе не всегда удается идентифицировать ДНКвозбудителя в биоптате стекловидного тела, наиболее ин‑ формативным является исследование биоптата сетчатки.
История открытия заболевания
В 1982 году W.W. Culbertson с соавторами выполнили световую и электронную микроскопию тканей энуклеированного глаза пациента с острым некрозом сетчатки. При этом гистологическое исследование показало наличие эозинофильных внутриядерных включений в клетках сетчатки, а электронная микроскопия — присутствие вирусов группы герпеса во всех слоях пострадавшей сетчатки. В дальнейшем эти же авторы подтвердили вирусную этиологию процесса путем идентификации вируса герпес-зостер иммуногистохимическим методом и сообщили о первом опыте работы с внутривенным использованием ацикловира для лечения острого ретинального некроза.
В 1990 г. Forster D.J. с коллегами впервые описали другую форму некротизирующей герпетической ретинопатии – прогрессирующий некроз наружных слоев сетчатки. Доказательство того, что причиной ретинита может быть цитомегаловирус (ЦМВ), было получено в 1964 г.. ЦМВ-ретиниты описываются главным образом у пациентов с иммунодефицитами, чаще всего больных СПИДом (в том числе ятрогенные) или с врожденной инфекцией, однако встречаются и случаи у здоровых пациентов, с системными заболеваниями соединительной ткани.
- наличие одного или более фокусов ретинального некроза с четкими границами на периферии сетчатки;
- быстрое прогрессирование при отсутствии противовирусной терапии;
- круговое распространение; окклюзионная васкулопатия с вовлечением артериол;
- воспалительная реакция в стекловидном теле и передней камере;
- нейропатия или атрофия зрительного нерва, склерит и боль.
При отсутствии перечисленных выше критериев также предлагаются следующие определения:
Этиология
Отмечено, что возникновение острого ретинального некроза не связано с возрастом, полом и состоянием иммунной системы пациента.
Согласно данным ВОЗ 60–80% населения инфицированы вирусами семейства герпес. По результатам полимеразной цепной реакции (ПЦР) сетчатки, полученной при биопсии, в качестве возбудителей острого ретинального некроза были идентифицированы вирус Эпштейна-Барр, вирус простого герпеса (ВПГ) 1 и 2 типа, ЦМВ. Другие авторы ключом к определению этиологии считают ПЦР-диагностику в отношении влаги передней камеры или стекловидного тела. При этом дифференциальную диагностику проводили с атипичным токсоплазмозом и другими формами ретиноваскулитов, в частности, таких как болезнь Бехчета.
Также в литературе описаны клинические случаи заболевания после вакцинации против herpes zoster. Существуют два вида вакцины для подкожного введения. Первичную вакцинацию проводят препаратом Varivax (две инъекции, малые дозы), а ревакцинацию – препаратом Zostavax (одна инъекция, большая доза).
Синдром ОРН наблюдается относительно редко и, как правило, возникает у взрослых людей молодого возраста, а его развитие у детей описано лишь в единичных случаях, в том числе в период новорожденности. У детей заболевание протекает более агрессивно с тяжелым витриитом и мембранообразованием в стекловидном теле.
Лечение

До сих пор отсутствует единый подход к лечению острого ретинального некроза, неясно, целесообразно ли применение аспирина, кортикостероидов, выполнение барьерной лазеркоагуляции и профилактической витрэктомии.
Но по данным литературы, у пациентов, которым были проведены ранняя витрэктомия, интраоперационное промывание витреальной полости ацикловиром, отграничительная лазеркоагуляция некротических очагов сетчатки с экстрасклеральным пломбированием или без него и тампонадой газом или силиконовым маслом, регматогенная отслойка сетчатки развивается в 2 раза реже и при этом практически отсутствуют случаи субатрофии глазного яблока.
Одни авторы утверждают, что острые ретинальные некрозы, вызванные вирусом варицелла-зостер, носят более серьезный характер и прогрессируют быстрее по сравнению с теми, которые вызваны ВПГ. Поэтому начинать лечение следует более высокими дозами ацикловира до тех пор, пока во внутриглазной жидкости с помощью ПЦР выявлялся вирус-возбудитель. Если результаты ПЦР-диагностики подтверждают наличие ВПГ как вируса-возбудителя, дозировку препарата следует уменьшить до 10 мг/кг 3 раза в день. После внутривенной терапии следуют 6 недель противовирусной терапии per os.
Другие исследователи выступали за дополнительное применение интравитреальной инъекции ганцикловира или фоскарнета при лечении пациентов с тяжелыми случаями острого ретинального некроза.
Лечение ОНС начинают с интенсивной противовирусной и противовоспалительной терапии. Консервативное лечение купирует воспалительный процесс, однако не предотвращает возможность развития разрывов и отслойки сетчатки.
В 1991 году был разработан стандарт лечения пациентов с острым ретинальным некрозом при помощи ацикловира. Рекомендуемым режимом является внутривенное введение ацикловира в дозе 10 мг/кг каждые 8 часов (или 1500 мг/м2 ) в день в течение 5–10 дней, затем пероральный прием ацикловира в дозе от 400 до 800 мг 5 раз в день дополнительно от 6 до 12 недель. В качестве минимального срока терапии был определён полуторамесячный приём противовирусных препаратов per os, так как по данным разных авторов, вовлечение парного глаза в процесс происходит в трети случаев в срок от первых нескольких недель до нескольких месяцев или даже лет.
На сегодняшний день перорально лучше применять препарат Валацикловир — это пролекарство ацикловира, при всасывании превращается в ацикловир, имеет более высокую биодоступность и более длительный Т½, а также, принимается с меньшей кратностью (2 раза в сутки).
Активное динамическое наблюдение за больными, перенесшими ОНС, позволяет своевременно обнаружить изменения, требующие хирургического лечения, что приводит к более высоким функциональным и анатомическим результатам.
Методом хирургического лечения ОНС и его осложнений является витрэктомия, которая проводится при возникновении разрывов и отслойки сетчатки, в случаях выраженного помутнения стекловидного тела, грубых витреоретинальных шварт. Оперативное лечение целесообразно проводить у пациентов до формирования отслойки сетчатки при выраженном тракционном синдроме с разрывами сетчатки или без них.
Достижение хорошего анатомического результата (прилегание отслоенной сетчатки, восстановление прозрачности оптических сред) возможно в большинстве случаев хирургического лечения ОНС, но функциональные результаты лечения ОНС зависят от распространенности зоны некроза на глазном дне, исходного функционального и анатомического состояния сетчатки и стекловидного тела.
Вирус ветрянки-зостер (ВВЗ), как правило, вызывает два разных по своим клиническим проявлениям заболевания — ветряную оспу и Herpes Zoster (опоясывающий лишай).
Из анамнеза жизни: пациентка отмечает наличие периодических вертебралгий и паравертебралгий, патологии коленных суставов (около 8 лет назад проводилась процедура пунктирования правого коленного сустава с эвакуацией синовиальной жидкости). В 2000 г. — аппендэктомия с осложненным послеоперационным течением, вследствие которого произведено повторное оперативное вмешательство. В отдаленном послеоперационном периоде отмечались явления спаечной болезни. Герпетический анамнез — спокойный. Со слов, пациентка страдает пищевой аллергией.
Офтальмологический статус при поступлении. Острота зрения правого глаза — 0,4, коррекция сферической линзой +1,0 до 0,8; левого глаза — неправильная светопроекция. Внутриглазное давление: ОD — 19 и OS — 22 мм рт.ст. Критическая частота слияния мельканий: OD = 40 Гц, OS — не определяется.
OD: структуры переднего сегмента без видимой патологии.
Офтальмоскопия. OD: диск зрительного нерва (ДЗН) бледно-розовый, границы четкие, физиологическая экскавация. Артерии сужены, вены расширены (отношение диаметра артерии к диаметру вены — 1:3). Макулярная область без патологии. Видимая периферия — на 6 часах участок хориоретинальной атрофии с четкими границами, размерами ДЗН.
Эхография (26.03.2015 г.). В стекловидном теле интенсивный выпот слева.
Рентгенография придаточных пазух носа (26.03.2015 г.) — без патологических изменений.
Рентгенография органов грудной клетки (05.04.2015 г.). Легочные поля без видимых очаговых и инфильтративных изменений.
С помощью методов лабораторной диагностики у пациентки были исключены следующие инфекции: сифилис, СПИД, вирусные гепатиты, хламидиоз, уреаплазмоз, токсоплазмоз. В то же время — выявлены повышенные титры сывороточных иммуноглобулинов класса G к вирусу варицелла-зостер (>4000; N<150), цитомегаловирусу (101; N<6), вирусу Эпштейна-Барра (>750; N<20). Кроме того, обнаружено носительство аллеля 27 в локусе B генов HLA I класса.
Общий анализ крови, общий анализ мочи и коагулограмма — в пределах нормы. Отмечалось повышение глюкозы крови до 6,78 ммоль/л при поступлении с последующим снижением до 3,64 ммоль/л.
По совокупности выявленных глазных симптомов, жалоб, анамнеза заболевания, данных инструментальных и лабораторных методов исследования нами выставлен клинический диагноз: острый некроз сетчатки герпес-вирусной этиологии (ВВЗ+ВЭБ), сопровождающийся классической триадой симптомов (передний увеит с сальными преципитатами и задними синехиями, витреит и ретиноваскулит).
С первого дня поступления в стационар пациентке была назначена местная (дексазон) и системная кортикостероидная (парентеральная) терапия; антибиотикотерапия (аминогликозиды местно, препараты фторхинолонового ряда парентерально); противогрибковые препараты (нистатин); мидриатики (атропин 0,1% субконъюнктивальные инъекции, цикломед — инстилляции); витаминотерапия (аскорбиновая кислота); сосудистая терапия (реополиглюкин, этамзилат). После того как были получены результаты лабораторных маркеров реактивации герпес-вирусной инфекции, в схему лечения были включены противовирусные препараты (ацикловир per os, ганцикловир внутривенно).
На фоне проводимой интенсивной терапии динамика воспалительного процесса в первые дни привела к некоторой стабилизации воспалительного процесса, но повторное проведение эхографии 06.04.2015 г. выявило нарастающую клеточную инфильтрацию в стекловидном теле и угрозу отслоения сетчатки.
Учитывая интенсивность воспалительного процесса в левом глазу, эхо-признаки начинающейся отслойки сетчатки, данные лабораторных исследований, отрицательную динамику заболевания на фоне проводимой медикаментозной терапии было принято решение прибегнуть к хирургическому лечению (субтотальной витрэктомии) с целью сохранения остаточных зрительных функций. 06.04.2015 г. на левом глазу проведена закрытая субтотальная витрэктомия с введением перфторорганического соединения (ПФОС) в витреальную полость с целью мобилизации центральной зоны и тампонадой тяжелым силиконовым маслом. Результаты лабораторного исследования стекловидного тела и субретинальной жидкости пациентки показали наличие ДНК вируса варицелла-зостер и вируса Эпштейна-Барра (метод ПЦР), что позволило подтвердить герпес-вирусную природу воспалительного процесса и продолжить комплексную медикаментозную терапию с использованием аналогов нуклеозидов.
В послеоперационном периоде в OS сохранялись активные явления переднего увеита (рис. 2), в связи с чем пациентка была дообследована, обнаружена ДНК уреаплазмы (слеза и моча), назначена пероральная терапия доксициклином. На фоне комплексной терапии отмечалась положительная динамика в ходе инфекционного процесса: гиперемия конъюнктивы уменьшилась, преципитаты на эндотелии роговицы регрессировали, прозрачность влаги передней камеры восстановилась (рис. 3). Зрение левого глаза при выписке — движение руки у лица, ВГД — пальпаторно — норма.
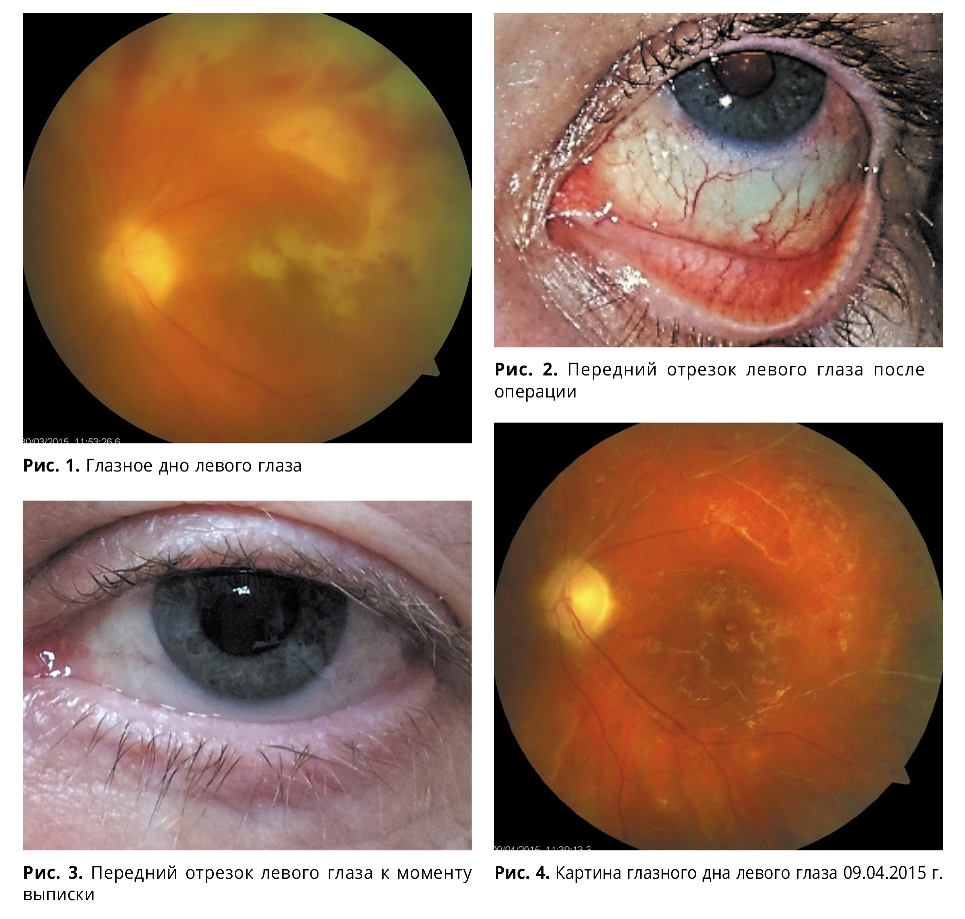
Картина глазного дна (09.04.2015 г.) левого глаза также свидетельст-вовала о купировании воспалительного процесса: ДЗН бледный, границы стушеваны. Отек ткани сетчатки уменьшился, сетчатка бледная, но прилежит на всем протяжении. Кровоток по носовым и верхне-височной артериям отсутствует, по нижне-височной — частично сохранен (рис. 4).
Заключение
В представленном клиническом случае диагноз острого некроза сетчатки был подтвержден обнаружением ДНК ВВЗ и ВЭБ в субретинальной жидкости и стекловидном теле методом ПЦР (одномоментно ДНК ВПГ 1 и 2 типов, ЦМВ, герпесвируса 6-го типа, уреаплазмы, хламидии и микоплазмы не выявлена). Кроме того, высокие титры сывороточных иммуноглобулинов G к данным представителям к ВВЗ и ВЭБ, выявленные в первые дни заболевания, безусловно, послужили подсказкой в диагностике заболевания, что позволило свое-временно начать адекватную противовирусную терапию. Проведение субтотальной витрэктомии с силиконовой тампонадой на фоне адекватной противовирусной и антибактериальной в пред- и после-операционном периодах позволило сохранить глаз как орган и остаточные зрительные функции.
Литература
Острый некроз сетчатки – редкий увеальный синдром вирусной этиологии, представляющий собой диффузный некротический ретинит, который при несвоевременной диагностике и неадекватном лечении может привести к необратимой слепоте. Поскольку это заболевание встречается довольно редко, в литературе имеется недостаточно данных об оптимальных алгоритмах его диагностики и лечения. Достижения молекулярной диагностики и современные возможности системной и интравитреальной терапии позволили улучшить прогноз заболевания. В настоящей статье представлен обзор последних достижений в лечении острого некроза сетчатки.
Диагноз острого некроза сетчатки традиционно ставится на основании данных клинического обследования согласно критериям, обозначенным Американским Обществом специалистов по увеитам в 1994 г.: минимум одна зона периферического некроза сетчатки с тенденцией к распространению по окружности, признаки воспаления в переднем отрезке глазного яблока и в витреальной полости, окклюзивная васкулопатия и быстрое прогрессирование заболевания при отсутствии терапии (Holland G.N., 1994). Лабораторные данные не входят в критерии диагностики острого некроза сетчатки, но в ряде клинических исследований сообщается о выявлении вирусной ДНК в образцах стекловидного тела или влаги передней камеры при помощи полимеразной цепной реакции (ПЦР) (Schoenberger S.D. et al., 2017). Наиболее часто выявляемыми возбудителями острого некроза сетчатки являются вирус varicella zoster (ВВЗ), вирус простого герпеса (ВПЧ) и цитомегаловирус (ЦМВ) (Shantha J.G. et al., 2015).
Исторически стандартом лечения острого некроза сетчатки было внутривенное введение противовирусных препаратов. Blumenkranz M.S. et al. в 1986 г. и Palay D.A. et al. в 1991 г. сообщали о значительном уменьшении симптомов заболевания на фоне внутривенной терапии ацикловиром (доза 1500 мг/м2/день, Blumenkranz M.S. et al.).
Однако с появлением новых пероральных противовирусных средств целесообразность внутривенной терапии стала обсуждаться. Tibbetts M.D. et al. в 2010 г. провели исследование, в котором сравнивали результаты лечения 36 глаз в эру внутривенного ацикловира (1981–1997) и результаты лечения в эру новых противовирусных препаратов (1998–2008); они не обнаружили значительных различий в конечных зрительных функциях при внутривенной или пероральной терапии. Baltinas J. et al. в 2018 г. провели прямое сравнение внутривенного введения ацикловира и перорального приема валацикловира у 68 пациентов с острым некрозом сетчатки и тоже не обнаружили статистически значимых различий в конечной остроте зрения или частоте развития отслойки сетчатки. Поэтому пероральный прием валацикловира может рассматриваться в качестве первой терапии острого некроза сетчатки так же, как и внутривенная терапия ацикловиром.
Интравитреальное введение противовирусных препаратов может улучшить результаты лечения. Baltinas J. et al. (2018) и Yeh S. et al. (2014) сравнивали результаты лечения 15 глаз только системным введением препаратов и 14 глаз системным и интравитреальным введением противовирусных препаратов (интравитреальные инъекции фоскарнета 2,4 мг/0.1 мл). На фоне комбинированной терапии у пациентов отмечалось более выраженное увеличение остроты зрения (на 2 строки и больше, P = 0,006) и уменьшение частоты развития отслойки сетчатки (P = 0,03). Wong R. et al. в 2010 г. также сообщил о меньшей частоте отслойки сетчатки в серии из 64 глаз на фоне комбинированной терапии, включавшей интравитреальные инъекции, по сравнению с только системной терапией 40 пациентов (36% vs 60%, P = 0,02). Согласно этим данным, сочетание системного и интравитреального введения противовирусных препаратов благоприятно влияет на анатомические и функциональные результаты лечения острого некроза сетчатки.
Профилактическая лазерная ретинопексия проводится с целью снижения частоты отслойки сетчатки у пациентов с острым некрозом сетчатки. Однако данные о ее эффективности довольно противоречивы. Lau C.H. et al. в 2006 г. сообщили о статистически значимо меньшей частоте развития отслойки сетчатки (P = 0,04) в глазах после проведения профилактической аргонлазерной ретинопексии (35,3%) и в глазах без проведения лазеркоагуляции (80%). В то же время профилактическая лазеркоагулция выполнялась только на глазах с относительно прозрачными оптическими средами. Это может свидетельствовать о некоторой предвзятости оценки результатов, поскольку более выраженное воспаление сопровождается более выраженным помутнением оптических сред.
Risseeuw S. et al. в 2019 г., напротив, не обнаружили влияния профилактической лазеркоагуляции на частоту развития отслойки при остром некрозе сетчатки. Tibbetts M.D. et al. (2010) также считают, что лазерная ретинопексия не влияет на частоту отслойки сетчатки. В их исследовании отслойка сетчатки возникла у 58% пациентов (11 из 19) после проведения лазеркоагуляции и у 46% пациентов (18 из 39), не получавших лазерную терапию (P = 0,40). В то же время решение о проведении лазерной ретинопексии принимали разные врачи на свое усмотрение, поэтому в данном исследовании также следует учитывать некоторую предвзятость.
Некоторые специалисты полагают, что ранее проведение витрэктомии при остром некрозе сетчатки помогает предотвратить развитие отслойки сетчатки и улучшить функциональные результаты. Hillenkamp J. et al. в 2009 г. отметили, что отслойка сетчатки возникла у 90% пациентов, получавших ацикловир внутривенно и преднизолон перорально, и только у 40% пациентов на фоне раннего проведения витрэктомии, промывания витральной полости раствором ацикловира и – при необходимости и по возможности – лазерное ограничение зоны некроза, эписклерального пломбирования и тампонады газом или силиконовым маслом (P = 0,007). При этом несмотря на лучшие анатомические результаты конечная острота зрения в обеих группах была идентична. Iwahashi-Shima C. et al. в 2013 г. и Risseeuw S. et al. в 2019 г. также не нашли достоверного влияния ранней витрэктомии на частоту развития отслойки сетчатки. На сегодняшний день данных об эффективности ранней витрэктомии при остром некрозе сетчатки недостаточно. Однако ввиду риска возникновения множественных очагов некроза и развития отслойки сетчатки требуется тщательное наблюдение пациентов.
При остром некрозе сетчатки возможно местное или пероральное применение кортикостероидов с целью уменьшения воспаления. Shantha J.G. et al. (2015) рекомендуют добавление кортикостероидов per os через 24–48 часов после начала противовирусной терапии. Периокулярные или интравитреальные инъекции кортикостероидов могут быть назначены при тяжелом, быстро прогрессирующем некрозе сетчатки. При этом необходимо помнить о том, что стероиды могут спровоцировать ухудшение состояния глаза (рис. 2). Weissman H.M. et al. в 2015 г. сообщили о пациенте с подозрением на неврит зрительного нерва, у которого после интравитреальной инъекции кортикостероида произошел билатеральный молниеносный некроз сетчатки и развился менингит. Локальное применение кортикостероидов может быть рекомендовано с целью профилактики кистозного макулярного отека, но при этом следует учитывать вероятность рецидива заболевания после отмены стероидов.
Choudhury H. et al. в 2014 г. описали 4 случая острого некроза сетчатки; пациенты принимали валацикловир и преднизолон после 24–48 часов per os. В связи со стойким витреитом через 1–2 недели пациентам были выполнены интравитреальные инъекции триамцинолона в дозе 4 мг / 0,1 мл. После этого симптомы витреита уменьшились, а острота зрения повысилась до 0,5 у 75% пациентов. В то же время ряд исследователей не отмечает улучшения анатомических и функциональных результатов на фоне применения кортикостероидов (Tibbetts M.D. et al., 2010; Lau C.H. et al., 2006).
Таким образом, согласно последним данным, оптимальное лечение острого некроза сетчатки включает пероральный прием высоких доз валацикловира и интравитреальное введение противовирусных препаратов. ПЦР является информативным методом, позволяющим подтвердить диагноз острого некроза сетчатки, однако ввиду высокого риска необратимой потери зрения лечение должно быть начато немедленно. Данных об эффективности ранней витрэктомии или профилактической лазерной ретинопексии в настоящее время недостаточно. Кортикостероиды могут улучшить состояние пациентов с острым некрозом сетчатки, однако их применение должно проводиться с осторожностью в связи с риском быстрого прогрессирования заболевания и потери зрения.
Li A.L., Shantha J. G., Yeh S. Update on the management of acute retinal necrosis. OSLI Retina. 2019; 12: 748–751.
Читайте также:

