Неонатальный герпес у новорожденных что это
Обновлено: 19.04.2024
Л.А.МАРЧЕНКО, доктор медицинских наук, ведущий научный сотрудник отделения гинекологической эндокринологии. Герпетическая инфекция нередко является причиной гибели зародыша. Ее последствия могут привести к возникновению у плода пороков развития.
Вагинальные инфекции относятся к разряду наиболее часто встречающихся заболеваний нижнего отдела полового тракта. Патологические выделения из влагалища являются симптомом более 20 заболеваний, поэтому первоначально правильно установленный этиологический диагноз во многом не только определяет успех лечения, но и является гарантом отсроченных осложнений.
В последние годы наряду с общеизвестными микроорганизмами, вызывающими специфические и неспецифические инфекционные заболевания половых путей, все чаще диагностируются поражения, обусловленные вирусной инвазией гениталий, среди которых, несомненно, важная роль принадлежит вирусу простого герпеса (ВПГ).
Различают два типа ВПГ. Большинство вирусов составляет 2-ю, антигенную группу - ВПГ-2, которые преимущественно вызывают генитальную патологию, ВПМ вызывают экстрагенитальные поражения.
Пути передачи. Эпидемиология
Генитальный герпес (ГГ) относится к заболеваниям, передающимся половым путем (ЗППП).
Заражение может происходить в случае, когда у партнера, являющегося источником инфекции, на половых органах имеются типичные герпетические высыпания (рецидив заболевания) или, что особенно важно, когда он выделяет вирус, не имея при этом клинических симптомов заболевания (атипичная форма, или бессимптомное вирусоносительство).
Инфицирование возможно также при орогенитальных контактах. Бытовой путь переноса инфекции встречается крайне редко и полностью исключается, если секрет, содержащий вирус, высыхает.
Генитальный герпес может вызываться вирусом и 1-го и 2-го типа.
Известно, что степень распространенности ВПГ-2 инфекции зависит от пола обследуемых, числа их сексуальных партнеров, возраста, низкого образовательного уровня и этнической принадлежности. Исследования в 10 развитых странах показали, что серопозитивными на ВПГ-2 являются 107 млн. человек, при этом частота инфицирования в США составляет от 22 до 33%, в Европе - от 7 до 24%, в странах Индокитая - до 6%. Ситуация с инфицированием ГГ в России остается во многом крайне неясной, так как, хотя ГГ и отнесен в группу ЗППП, учет заболеваемости ведется плохо. Согласно проведенным в 1994 г. эпидемиологическим исследованиям на примере закрытой популяции в Москве, частота инфицирования генитальным герпесом составляет 19,7%. Выявлено два ее возрастных пика - 16-24 года и 35-40 лет. Женщины в 1,7 раза чаще инфицируются ВПГ-2, чем мужчины, подобных половых различий в инфицировании экстрагенитальным герпесом не выявлено.
Многие исследователи считают, что истинная ситуация в мире в отношении роста заболеваемости ГГ в достаточной мере не контролируется в связи со значительным процентом его асимптомных форм. Частота последних составляет 40-74%.
Нередко психосоциальные последствия ГГ бывают более выраженными и значимыми, чем физические страдания, связанные с частыми обострениями заболевания. ГГ, безусловно, влияет на качество жизни пациентов, т.к. уже с момента обращения к врачу перед ними возникает ряд психологических и медицинских проблем, среди которых ведущая роль принадлежит следующим: страх обнаружения вируса, депрессия; влияние на сексуальную и интимную жизнь; снижение социальной активности и изменение образа жизни; отношение к ГГ, как к болезни, передающейся половым путем; страх заразиться или быть зараженным; страх быть отвергнутым обществом; боязнь быть неизлеченным и т.д.
Клиника. Диагностические критерии
По особенностям клинических проявлений инфекции ГГ разделяют на типичный и атипичный.
Инкубационный период в среднем составляет 3-9 дней, в течение которых экспрессия вируса минимальна.
Острый период заболевания при типичной форме инфекции характеризуется обширными эрозивно-язвенными высыпаниями на слизистой больших и малых половых губ, промежности, влагалища, шейки матки. Ему всегда предшествует продромальный период, сопровождающийся субъективными ощущениями в виде боли, зуда, жжения, парестезий в области гениталий, а также общей симптоматикой - недомогание, озноб, лихорадка и т.д. При этом в 13-35% случаев наблюдается асептический менингит с тошнотой, рвотой, онемением затылка, головной болью. Все эти симптомы самостоятельно проходят с появлением высыпаний, в 10-15% отмечается фарингостоматит.
Довольно часто при первичном эпизоде заболевания отмечается поражение мочевой системы, проявляющееся от незначительной дизурии до стойкой задержки мочеиспускания, обусловленной отеком и резкой болезненностью в области уретры в результате обширных герпетических язв или вовлечения в воспалительный процесс слизистой оболочки мочевого пузыря и уретры.
Для ГГ характерна фиксированность очагов высыпания. В зависимости от локализации последних выделяют следующие стадии поражения:
I - наружные гениталии;
II - влагалище и шейка матки;
III - матка и область придатков.
Однако подобная стадийность весьма условна. После первичного эпизода заболевания под влиянием провоцирующих факторов периодически возникают рецидивы инфекции.
Анализ провоцирующих факторов показал, что наиболее часто обострение возникает на фоне стресса (78%); переутомления (56%); менструации (50%), перенесенной простуды (24%), в то время как ультрафиолетовое облучение, физические нагрузки и употребление алкоголя встречаются, соответственно, в 12, 10 и 6% случаев.
При ГГ рецидивы возникают в 50-75% случаев, что значительно выше показателей обострения при экстрагенитальной инфекции. Это объясняется особенностями антигенной структуры вируса 2-го типа.
Частота рецидивов у многих пациентов с годами снижается. Однако довольно часто после длительной ремиссии возникает период учащения рецидивов.
В зависимости от частоты обострений выделяют три степени тяжести ГГ:
тяжелое течение - ремиссии от нескольких дней до 6 недель;
средней тяжести - ремиссии от 2 до 3 месяцев;
легкое - ремиссии не менее 4 месяцев.
Клиническая картина рецидивов хронической генитальной герпетической инфекции разнообразна. В 50-85% случаев ей сопутствует продромальный период в виде чувства жжения, зуда, болезненности в очаге поражения. В 25% случаев выявляется болевой синдром - боль иррадиирует в ногу, пах, ягодицу. В 10% случаев появляются лимфаденит, общее недомогание, озноб.
В 70% случаев во время рецидива визуализируются микроскопические везикулезно-язвенные очаги, при рецидиве не обнаруживаются какие-либо патологические изменения, и обострение бывает трудно диагностировать без дополнительных лабораторных методов исследования. Рецидив протекает, как правило, легко, продолжительность высыпаний не превышает 3-5 дней, после чего слизистые или кожные покровы полностью эпителизируются.
Диссеминация ГГ наблюдается крайне редко, только в случаях тяжелой сопутствующей инфекции либо у больных с выраженным наследственным или приобретенным иммунодефицитом.
Диагностическим критерием наличия ГГ во многом являются местные проявления заболевания. Однако при атипичных формах отсутствует манифестный признак инфекции - сгруппированные везикулы, наполненные серозной жидкостью, трансформирующиеся в эрозии и язвы, что в значительной степени затрудняет постановку диагноза. Отдует особо подчеркнуть, часто подобный тип течения ГГ характерен в значительном проценте случаев с самого начала заболевания, поэтому первичный эпизод инфекции ретроспективно выявить бывает крайне трудно.
В настоящее время в 40-75% случаев ГГ протекает атипично - без появления характерных герпетических высыпаний, включая первичный эпизод заболевания.
На основании многолетних наблюдений и соотношения жалоб с данными вирусологических исследований нами были разработаны клинические критерии, позволяющие в большинстве случаев подтвердить герпетическую природу заболевания при атипичных формах инфекции. Ведущими среди них являются стойкий зуд и жжение вульвы и влагалища; кольпиты, не поддающиеся традиционной антибактериальной терапии; рецидивирующие эрозии и лейкоплакии шейки матки; привычное невынашивание беременности; стойкий вегетативный тазовый ганглионеврит (см. рис.).
СЕМИОТИКА АТИПИЧНОЙ ФОРМЫ ГЕНИТАЛЬНОГО ГЕРПЕСА
Значение этих критериев чрезвычайно важно для выявления групп инфицированных. Необходимо информирование больных о часто встречающихся атипичных симптомах заболевания в связи с возможностью бессимптомной передачи инфекции. Согласно данным отдельных исследователей, только 20% инфицированных ВПГ имеют диагностированный симптоматический герпес, 60% - нераспознанный симптоматический ГГ (атипичную форму) и 20% - бессимптомный герпес.
К четвертому, относительно редко встречающемуся варианту течения инфекции относят бессимптомный герпес, или вирусоносительство, при котором нет никаких клинических проявлений инфекции, однако в образцах слизи из цервикального канала или в мазках-отпечатках с половых органов выявляется вирус герпеса.
Знание этих вариантов течения инфекции важно для разработки тактики ведения беременных, страдающих ГГ.
Существует три основных механизма инфицирования плода ВПГ-2:
- вирусы из влагалища и шейки матки могут проникать к плодному яйцу восходящим путем или эмбрион может быть инфицирован во время имплантации инфицированной спермой;
- трансплацентарный переход вирусов к плоду при наличии их в крови беременных;
- заражение плода при прохождении через инфицированные родовые пути.
Последствиями герпетической инфекции являются гибель зародыша, пороки развития (микроцефалия, хориоретинит, дисплазия сетчатки, микрофтальмия, помутнение хрусталика, пороки сердца, гепатоспленомегалия, поражение отдельных органов и систем).
При ведении пациенток с генитальным герпесом врачу необходимо ставить перед собой следующие цели:
- купирование симптомов;
- проведение профилактики последствии инфекции и ее передачи половому партнеру и новорожденному.
Риск внутриутробного заражения плода ВПГ определяется совокупностью факторов - вариантом клинического течения ГГ (первичный эпизод заболевания или рецидив), особенностями клинической картины (типичное, атипичное или бессимптомное течение инфекции), продолжительностью контакта плода с инфицированными родовыми путями матери и стадией герпетических высыпаний.
При совпадении первичного эпизода заболевания ГГ с I или III триместром беременности в 40-50% случаев наблюдается либо мертворождение, либо рождение ребенка с врожденным поражением мозга (микроцефалия и другие аномалии). Поэтому, согласно рекомендациям ВОЗ, при первичном эпизоде заболевания, особенно в случае первичной инфекции в I триместре, целесообразно беременность прервать.
При рецидивирующем герпесе риск инфицирования плода составляет всего О-8%, что объясняется пассивной передачей материнских антител, более низкими титрами вируса и более коротким периодом его воздействия. В этих случаях беременность следует сохранить.
Наибольшую значимость в плане возможного инфицирования плода имеют атипично протекающие формы хронической ге-нитальной герпетической инфекции. В 70% случаев дети с неонатальным герпесом рождаются именно от матерей с атипичными или бессимптомными формами ГГ, при том, что частота бессимптомного носительства ВПГ-2 составляет в различных популяциях 0,5-8%. Смертность новорожденных от неонатального герпеса в этой группе составляет 50-70%; из выживших новорожденных здоровыми остаются только 15%.
Таким образом, становятся понятны социальная значимость для нашей страны проблемы генитальной герпетической инфекции и ее неблагоприятный вклад в заболеваемость и перинатальные потери.
Для установления нормального контакта между врачом и пациентом необходимо:
- неосуждение со стороны врача;
- вовлечение пациента в управление своей болезнью;
- возможность больного получить лучшее из доступного на текущий момент лечение.
Принципы современной терапии
К базисному виду терапии относится прежде всего комплекс противовирусного лечения - длительная блокада репродукции вируса современными химиопрепаратами, на фоне которых следует проводить стимуляцию неспецифической и специфической резистентности организма. Необходимо подчеркнуть, что лечение всегда целесообразно подбирать индивидуально и в каждом конкретном случае выбор медикаментозного комплекса определяется клинической формой инфекции, фазой заболевания (рецидив или ремиссия), иммунологическим состоянием пациента, предшествующим лечением и его эффективностью, наличием сопутствующих заболеваний (особое внимание необходимо уделять аллергоанамнезу).
Идеальный противовирусный препарат должен обладать селективным и специфическим механизмом действия, не быть токсичным (мутагенным, тератогенным, канцерогенным), не иметь побочных эффектов, не вызывать резистентность. Препарат должен характеризоваться хорошей биодоступностью, не взаимодействовать с другими лекарствами и иметь удобный режим дозирования.
Наиболее безопасным вариантом химиотерапии оказалось создание синтетических аналогов какого-либо структурного компонента (нуклеозид) герпес-вирусной ДНК, который избирательно фосфорилируется не клеткой, а вирусспецифическим ферментом - тимидинкиназой.
К наиболее широко используемым в мировой клинической практике аномальным нуклеозидам относятся ацикловир (зовиракс, виролекс), валацикловир (валтрекс), фамцикловир (пенцикловир), ганцикловир и т.д. К аналогам пирофосфата относится триаптен. К препаратам с другим механизмом действия (специфические ингибиторы) - бонафтон, алпизарин, флакозид, хелипин, флореналь.
Чаще всего для лечения генитального герпеса используют ацикловир (АЦ), обладающий высокой степенью сродства и селективности в отношении герпес-вирусов.
Ацикловир проникает преимущественно в зараженные ВПГ клетки, однако в неизмененном виде инертен и малотоксичен, прежде чем стать активным, он должен фосфорилироваться.
Существует две методики лечения рецидивирующей герпетической инфекции АЦ: эпизодическое лечение каждого обострения и продолжительная супрессивная терапия с целью предотвращения рецидивов. Выбор режима терапии определяется клиническим вариантом инфекции (первичный эпизод или рецидив) и степенью ее тяжести, а также проблемой передачи инфекции в случае, если один из партнеров серонегативен, и при планировании беременности.
В последние годы в России в качестве химиопрепарата широко использовался алпизарин. Проведенное сравнительное исследование лечебного и профилактического эффекта алпизарина и зовиракса при тяжелом течении ГГ показало, что прием зовиракса в режиме супрессивной терапии по 800 мг в сутки способствовал стойкой ремиссии у 73% больных, в то время как прием алпизарина вызывал подобный эффект только в 19% случаев. Профилактический эффект зовиракса более чем в 5 раз превосходит эффект алпизарина по восстановлению качества жизни больных.
Однако биодоступность перорально вводимого ацикловира составляет всего 15-21 %, поэтому в течение последних 10 лет с целью повышения его эффективности разрабатывались различные аминокислотные эфиры ацикловира.
Всего было синтезировано более 18 аминокислотных эфиров. Валацикловир (L-валиловый эфир) показал биодоступность, равную 63%. В отличие от ацикловира валацикловир (валтреке) под влиянием фермента валацикловиргидролазы хорошо всасывается в кишечнике и быстро метаболизируется в печени, полностью превращаясь в ацикловир. Фармакокинетика и токсические свойства валацикловира идентичны таковым для ацикловира.
В клинической практике (особенно при лечении привычного невынашивания беременности) нередко возникает необходимость одновременно проводить профилактику как генитального герпеса, так и ЦМВ-инфекции. Использование в этих случаях валтрекса в значительной степени облегчает задачу врача, так как наиболее специфичный для ЦМВ-инфекции химиопрепарат ганцикловир оказывает выраженный гепатотоксический эффект и вызывает гипоплазию костного мозга.
Более высокие концентрации ацикловира в плазме как конечного продукта введения валацикловира позволяют также использовать его в случаях инфицирования больных резистентными штаммами герпес-вируса. Поддержание высоких уровней ацикловира в плазме при лечении валацикловиром позволяет уменьшить кратность приема препарата и способствует лучшему его усвоению.
В режиме эпизодической терапии валтрекс следует назначать по 500 мг 2 раза в день в течение 5 дней. Для профилактики рецидивов инфекции - по 100 мг один раз в сутки в течение 4-6 месяцев. За безопасностью применения ацикловира и его аналогов наблюдают с 1982 года. Подобная программа принята и для валацикловира. Наиболее частыми побочными эффектами являются головная боль, тошнота, диарея. Однако они не выражены.
Высокой биодоступностью (77%) обладает и фамцикловир (диацетил-6 - дезоксипроизводное пенцикловира). Пенцикловир имеет сходный, но не аналогичный ацикловиру спектр действия, включающий вирус ветряной оспы, ВПГ-1, ВПГ-2, а также вирус гепатита В. Фамцикловир превращается в пенцикловир при всасывании и пассаже через печень, последний активируется вирусной тимидинкиназой. Фамцикловир хорошо переносится, однако в дозе в 50 мг раз выше, чем терапевтическая повышает риск развития аденокарциномы груди у мышей.
Однако ни ацикловир, ни другие противовирусные агенты - фамцикловир, валацикловир - не предотвращают ни перехода вируса в латентное состояние, ни возникновения рецидивов после их отмены, ни передачи инфекции, а также, к сожалению, не влияют на естественное течение этой инфекции в плане полного излечения. Поэтому на протяжении последних 20 лет ученые изыскивают методы непосредственного воздействия на иммунную систему больных ГГ с целью стимуляции специфических и неспецифических ее факторов, тем самым способствуя блокаде репродукции вируса. Одним из перспективных подходов профилактики и лечения герпес-вирусных заболеваний являются применение препаратов иммуноглобулинов человека и вакцинотерапия.
Врожденный герпес – герпетическая инфекция, встречающаяся у новорожденных при антенатальном или интранатальном заражении от инфицированной матери. Характеризуется специфическими кожными проявлениями в виде везикулярной сыпи, которая может также располагаться на слизистых оболочках глаз, рта, внутренних органов. Часто развивается герпетический энцефалит с очаговой симптоматикой и судорогами. Патологические изменения отмечаются в печени, селезенке, легких, почках и других органах. Врожденный герпес диагностируется на основании результатов серологических, гистологических исследований, а также выявления частиц вируса. Лечение – противовирусные препараты, иммуномодуляторы, иммуноглобулины, витаминотерапия.
Общие сведения
Врожденный герпес является одним из множества вариантов герпетической инфекции, к которой также относятся цитомегалия, ветряная оспа, внезапная экзантема детей и другие нозологии. Частота встречаемости заболевания – 1 случай на 2,5-60 тыс. новорожденных. Предположительно, такой разброс статистических данных связан с низкой выявляемостью в развивающихся странах. Врожденный герпес имеет высокую значимость в педиатрии в связи с ростом заболеваемости, а также увеличением случаев рецидивирующего течения. Это обусловлено тем, что вирусом простого герпеса инфицировано практически все население планеты, а сам вирус постоянно претерпевает значительные мутации. Кроме того, низкая специфичность симптомов часто является причиной запоздалой диагностики, что, в свою очередь, представляет опасность для жизни ребенка.

Причины и классификация врожденного герпеса
Возбудитель заболевания – вирус простого герпеса человека. Известно множество типов данного вируса, однако врожденный герпес в 80% случаев вызывается вирусом 2 типа, который также известен как генитальный герпес. Оставшиеся 20% в структуре заболеваемости приходятся на долю вируса простого герпеса 1 типа. Заражение чаще всего происходит интранатально, при прохождении плода по инфицированным родовым путям. Реже врожденный герпес развивается еще в утробе, попадая в организм малыша через плаценту. В этом случае речь идет о наиболее тяжелом течении заболевания, результатом чего обычно является выкидыш или рождение ребенка с разной степенью недоношенности и тяжелыми пороками развития.
Заболевание может протекать в нескольких формах, которые отражают доминирующие клинические проявления. Выделяют 3 формы врожденного герпеса: локализованную, церебральную и генерализованную. Первая из них представлена характерными кожными высыпаниями, и именно этот симптом является ведущим. Церебральная форма, как правило, проявляется менингитом и энцефалитом герпетической природы. Генерализованный врожденный герпес у новорожденных достаточно часто развивается вследствие несовершенства иммунного ответа и сопровождается симптомами со стороны внутренних органов. Мозговые нарушения и кожные элементы также присутствуют.
Симптомы врожденного герпеса
Как уже было сказано выше, симптоматика различается в зависимости от формы заболевания. Чаще всего врожденный герпес дебютирует на 7-14 день жизни. Время появления первых клинических признаков зависит от многих факторов: сроки гестации, срока инфицирования, сопутствующей патологии и т. д. Примерно в половине случаев врожденный герпес проявляется специфической для данной нозологии везикулярной сыпью. Мелкие пузырьки с серозным содержимым могут локализоваться на любой части тела, при этом элементы располагаются группами, образуя скопления и иногда сливаясь. Везикулы окружены кольцом гиперемии и отека, за счет чего они слегка приподнимаются над кожей. Характерно поражение слизистой оболочки глаз в виде кератитов и конъюнктивитов.
Часто содержимое кожных элементов в короткие сроки становится геморрагическим или гнойным. После вскрытия на месте пузырьков остаются эрозии, заживающие путем образования корочки. Общее состояние малыша может ухудшаться незначительно, температура повышается до субфебрильных значений. Исключение составляют случаи так называемого первичного врожденного герпеса, представляющего собой локализованную форму заболевания и проявляющегося обильной сыпью, элементы которой часто сливаются, оставляя после вскрытия обширные эрозии. Температура высокая, высыпания присутствуют не только на коже, но и на слизистых. В отсутствие своевременной терапии генерализация происходит в 50% случаев.
Церебральная форма врожденного герпеса проявляется менингеальной симптоматикой при отсутствии поражения кожи. Иногда везикулярная сыпь возникает позже, спустя примерно неделю после дебюта мозговых нарушений, но элементов сыпи в этом случае всегда немного. На первый план выходят симптомы менингита и энцефалита: нарушения сознания, эпилептиформные, тонические и тонико-клонические судороги. Симптомы неспецифичны, поэтому герпетический энцефалит легко спутать с энцефалитом любой другой природы. Значительная интоксикация ухудшает состояние, однако у новорожденных лихорадка может быть не выражена. Также присутствуют признаки отека мозга, что проявляется стволовыми нарушениями: дисфагией, расстройствами дыхания и пр.
Генерализованная форма врожденного герпеса является самой опасной. Она включает в себя и элементы сыпи, и церебральную симптоматику, описанную выше. Помимо этого, заболевание проявляется поражением внутренних органов: гепатоспленомегалией, пневмонией, специфическими изменениями в почках и надпочечниках. Явления токсикоза выражены в значительной степени. Смертность при генерализованной форме врожденного герпеса составляет более 50%, а по некоторым данным достигает 80-90% случаев, при этом половина выживших детей остаются глубокими инвалидами. Медленный регресс общемозговых и очаговых расстройств и их частая необратимость являются особенностью герпетической инфекции.
Диагностика врожденного герпеса
Выявление заболевания сопряжено для педиатра со значительными трудностями. Во-первых, если отсутствуют кожные проявления, то врожденный герпес можно заподозрить с той же вероятностью, что и многие другие патологии неонатального периода, в частности, внутриутробные инфекции, гипоксическую травму и т. д. Кроме того, часто выявление возбудителя не является доказательством герпетической инфекции, поскольку основная масса населения в мире имела контакт с данным вирусом. Тем не менее, основой диагностики является обнаружение самого вируса или его антигенов в разных средах, например, в содержимом везикул, крови, мазках из носо- и ротоглотки, цереброспинальной жидкости и др.
Метод высокоспецифичен, но занимает много времени. По этой причине проводятся серологические исследования с целью определения специфических антител класса IgM, что является подтверждением острой фазы врожденного герпеса. Подтверждение диагноза возможно также на основании обнаружения антител класса IgG, при этом решающую роль играет не сам факт их наличия, а нарастание титра в динамике не менее чем в 4 раза (при отсутствии нарастания антитела являются материнскими). В диагностике герпетического энцефалита врачи опираются именно на данные серологического исследования. Врожденный герпес также подтверждается, исходя из анамнеза матери и результатов гистологического обследования последа.
Лечение и прогноз врожденного герпеса
Проводится этиотропная терапия заболевания, от сроков ее начала во многом зависит прогноз для жизни и здоровья ребенка. Применяются противовирусные препараты, высокотропные именно к вирусу простого герпеса. Используется парентеральный путь введения. Также назначаются средства наружного действия для лечения везикулярной сыпи. Кроме того, к терапии врожденного герпеса всегда подключаются иммуноглобулины и иммуномодуляторы, проводится курс витаминотерапии. По показаниям осуществляется кислородная поддержка и ИВЛ, вводятся противосудорожные препараты, проводится дегидратация.
Прогноз неблагоприятный. Врожденный герпес часто протекает в генерализованной форме, последствия герпетического энцефалита необратимы. Выжившие дети очень редко не отстают в развитии от сверстников. Большинство из них остаются инвалидами или погибают в период разгара клинических проявлений. Даже если терапия начата своевременно, заболевание может неоднократно рецидивировать с той же симптоматикой. Для профилактики рецидивов возможно использование герпетической вакцины. В настоящее время существует несколько ее видов, но вследствие частых мутаций вируса эффективность вакцинации остается под вопросом.

Неонатальная инфекция, вызванная ВПГ, обычно передается ребенку во время родов. Типичным признаком является везикулезная сыпь, которая может сопровождаться или прогрессировать до диссеминированной болезни. Диагноз устанавливают путем выделения вирусной культуры, тестирования методом полимеразной цепной реакции, иммунофлуоресценции, или электронной микроскопии. Лечение состоит в назначении парентерально высоких доз ацикловира и поддерживающей терапии.
При неонатальной инфекции, вызванной вирусом простого герпеса (ВПГ), отмечается высокая смертность и значительная заболеваемость. Заболеваемость составляет от 1/3000 до 1/20000 рождений. Частота случаев неонатальной инфекции, вызванной ВПГ 2-го типа, больше, чем вызванной ВПГ типа 1.
Заражение ВПГ происходит во время родов через инфицированные половые пути матери. В некоторых случаях возможна трансплацентарная передача вируса, а также внутрибольничная передача инфекции (контактный путь) от одного новорожденного ребенка другому с участием медицинского персонала, членов семьи. У матерей новорожденных детей, страдающих герпетической инфекцией, как правило, имеются вновь приобретенные половые инфекции, но многие из них не имели симптомов во время родов.
Клинические проявления
Симптомы обычно появляются между 1-й и 3-й неделями жизни, но редко могут не появиться и до конца 4-й недели. У новорожденных может быть местная или распространенная форма. Кожные везикулы одинаковы при любом типе инфекции и появляются примерно в 70% случаев. У новорожденных без кожных везикулярных высыпаний обычно развивается поражение центральной нервной системы (ЦНС). У новорожденных с изолированными высыпаниями в области кожи или слизистых оболочек, при отсутствии лечения, заболевание прогрессирует, и в течение 7–10 дней развиваются более тяжелые формы.

На данном снимке крупным планом рта новорожденного показана большая красная язва под верхней губой, вызванная ВПГ-1.
DR P. MARAZZI/SCIENCE PHOTO LIBRARY

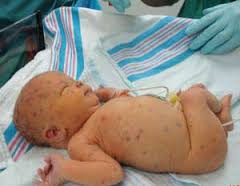
У данного новорожденного со СПИДом также выявлен диссеминированный ВПГ-2 с поражениями, покрывающими все тело.
DR M.A. ANSARY/SCIENCE PHOTO LIBRARY

Скопление везикул на эритематозной основе обладают характерными особенностями и могут присутствовать практически на любой части тела.
С разрешения издателя. Из Demmler G: Congenital and perinatal infections. В Atlas of Infectious Diseases: Pediatric Infectious Diseases . Edited by CM Wilfert. Philadelphia, Current Medicine, 1998.
Локализованная форма
Новорожденных детей с локализованным герпетическим поражением можно разделить на 2 группы. Для одной группы характерен энцефалит с выраженной неврологической симптоматикой, плеоцитозом спинномозговой жидкости и повышенным содержанием белка. Возможны сопутствующие поражения кожи, глаз и рта. Для другой группы характерно поражение только кожи, глаз, слизистой полости рта, без признаков вовлечения ЦНС или заболеваний внутренних органов.
Диссеминированная форма заболевания
Новорожденные дети с диссеминированной формой болезни и вовлечением внутренних органов имеют гепатит, пневмонию, ДВС-синдром или их комбинацию с или без энцефалита или поражений кожи.
Другие симптомы, которые могут возникать как изолированно, так и в комбинации, включают нестабильность температуры, вялость, гипотонию, дыхательную недостаточность, апноэ и судороги.
Диагностика
Исследование ВПГ с помощью культурального метода или методом полимеразной цепной реакции (ПЦР)
Иногда иммунофлуоресцентное тестирование поражений или электронная микроскопия
Экспресс-диагностика выделения культуры ВПГ или ПЦР имеет важное значение. Наиболее распространенным местом забора образцов являются кожные везикулы. Также необходимо исследовать носоглотку, глаза, прямую кишку, кровь и спинномозговую жидкость. У некоторых новорожденных с энцефалитом вирус присутствует только в ЦНС. Диагноз неонатальный ВПГ также можно поставить с помощью иммунофлуоресцентного окрашивания соскобов с пораженных участков, в частности с использованием моноклональных антител, и электронной микроскопии.
Если вирусологические средства диагностики недоступны, проводят пробу Тцанка пораженных участков, которая может выявить характерные многоядерные гигантские клетки и внутриядерные включения, но этот тест менее чувствителен, чем культуральный, и могут появиться ложноположительные результаты.
Прогноз
Смертность при нелеченой диссеминированной инфекции простого герпеса составляет 85%; среди новорожденных с нелеченым энцефалитом она составляет около 50%. Без лечения около 65% выживших после диссеминированной формы болезни или энцефалита имеют серьезные неврологические осложнения. Соответствующее лечение, в том числе назначение парентерального ацикловира, уменьшает смертность при заболеваниях ЦНС и диссеминированной форме на 50% и увеличивает часть детей, которые нормально развиваются примерно с 35% до 50–80%.
Летальный исход редко встречается у новорожденных детей с изолированным поражением кожи, слизистых глаз, полости рта. Тем не менее, без лечения, у многих из этих новорожденных заболевание будет прогрессировать до диссеминированной формы или поражения ЦНС, которые могут быть незамеченными.
Лечение
Парентеральное введение ацикловира
В подозрительных случаях, во время ожидания подтверждающих диагностических тестов следует немедленно превентивно начинать лечение ацикловиром. Младенцам с диссеминированной формой и/или болезнью ЦНС следует назначить в дозе 20 мг/кг внутривенно каждые 8 ч в течение 21 дней. После этого режима, младенцам с поражением ЦНС следует назначить ацикловир 300 мг/м 2 внутрь 3 раза в день в течение 6 мес.; этот долгосрочный режим улучшает исходы развития нервной системы в возрасте 1 года, но может вызвать нейтропению.
Необходима активная поддерживающая терапия, включающая внутривенное введение растворов, питание, поддержание дыхания, коррекцию нарушений свертывания крови и контроль судорог.
Профилактика

Усилия по предупреждению заражения герпетической инфекцией в родах были неэффективны. Универсальный скрининг не рекомендуется и не оказался эффективным, и большинство случаев материнской инфекции с риском передачи протекает бессимптомно. Тем не менее, женщины с генитальными очагами должны пройти в срок тестирование и серологию для диагностики ВПГ и определения риска передачи, также, как и для осуществления лечебного процесса по отношению к подвергшемуся воздействию, но без клинических проявлений новорожденному. Кесарево сечение рекомендовано для женщин с высоким риском передачи герпетической инфекции (например, имеющих активные генитальные высыпания на момент окончания срока вынашивания), даже когда мембраны герпетических везикул разорваны, так как при этом способе родоразрешения снижается риск заражения плода. Кроме того, эмбриональный монитор не должен использоваться во время родов, если у матери подозревают активное течение генитального герпеса. Новорожденные без клинических проявлений, родившихся у женщин с активными очагами на гениталиях на момент родов, должны пройти обследование и проверку на герпетическую инфекцию. Дополнительная информация доступна на портале Aмериканской академии педиатрии (1 Справочные материалы по профилактике Неонатальная инфекция, вызванная ВПГ, обычно передается ребенку во время родов. Типичным признаком является везикулезная сыпь, которая может сопровождаться или прогрессировать до диссеминированной. Прочитайте дополнительные сведения ).
Пероральный прием ацикловира или валацикловира в течение последних нескольких недель беременности женщинами с генитальным герпесом в анамнезе, может предотвратить рецидив во время родов и уменьшить необходимость в проведении кесарева сечения.
Справочные материалы по профилактике
1. Kimberlin DW, Baley J, Committee on infectious diseases, Committee on fetus and newborn: Guidance on management of asymptomatic neonates born to women with active genital herpes lesions. Pediatrics 131(2):e635-646, 2013. doi: 10.1542/peds.2012-3216
Основные положения
Неонатальный герпес может быть локализованным на коже, глазах или в полости рта, в центральной нервной системе или может быть распространенным.
Энцефалит и распространенная форма болезни имеют высокую смертность и неврологические последствия, которые распространены среди выживших.
В подозрительных случаях для улучшения исходов важны предположительная терапия и быстрая диагностика с помощью ПЦР ВПГ спинномозговой жидкости, крови или повреждениях.
Следует назначить ацикловир для парентерального введения как при локализованной, так и при распространенной болезни.
У кесарево сечение, если мать имеет активный генитальных поражений герпес, присутствующих на срок.
Более 20 лет назад — в 1993 году — в Российской Федерации была введена обязательная регистрация случаев генитального герпеса. Тем не менее гиподиагностика этого заболевания до сих пор остаётся актуальной практической проблемой, и таким же образом дело обстоит не только у нас, но и в странах ближнего зарубежья.
Просто сравним цифры: в США заболеваемость составляет 200 случаев на 100 тыс. жителей в год. В Западной Европе поменьше — в среднем 80 на 100 тыс. населения. И это в целом вполне можно принять на веру. Но можно ли поверить официальной статистике Украины — 15 случаев на 100 тыс. — или России — 21,7 случаев (данные 2005 года) 7,9,10 ? А недооценка этого заболевания опасна, особенно в акушерстве, поскольку неонатальный герпес способен уносить жизни до 80% инфицированных новорождённых, оставляя выживших инвалидами с нарушением работы центральной нервной системы 5 .
Если рассматривать заболеваемость герпесом на карте мира, то сразу видны два правдоподобных полюса. Место наивысшего накала — конечно, Африка: до 80% взрослых женщин и до 50% мужчин серопозитивны по ВПГ-2. Кстати, независимо от географии, наиболее высокие показатели инфицированности ВПГ-2 отмечены у ВИЧ-позитивных лиц, что отражает как проблемность социального поведения этой группы населения, так и взаимопотенцирующее действие обеих инфекций 7 . Не менее высока доля серопозитивных лиц среди пациентов клиник, специализирующихся на лечении и профилактике заболеваний, передаваемых половым путём, — до 86%8. Самый спокойный на карте уголок — Испания, в которой серопозитивны 4% женского и 3% мужского населения соответственно. Если взять эту страну за эталон, то наиболее близки к нему Италия и Великобритания со своими одинаковыми показателями — 7 и 5% женского и мужского населения. В среднем же в Западной Европе показатель серопозитивности держится на уровне 16,5%.
По данным ВОЗовской глобальной оценки распространённости (общее количество случаев) и заболеваемости (число новых случаев) ВПГ-2, в мире инфицированы более чем полмиллиарда людей, и каждый год к ним прибавляются ещё по 24 млн 5 . Существует мнение, что в развитых странах генитальным герпесом может страдать 10–20% взрослого населения 7 . В многочисленных популяционных исследованиях показано, что уровень заболеваемости генитальным герпесом повышается с возрастом: единичные случаи выявляют в возрасте до 14 лет, а самая высокая заболеваемость — у 20–29-летних. Второй пик приходится на 35–40 лет. Основными факторами риска генитального герпеса выступают большое количество половых партнёров на протяжении жизни, раннее начало половой жизни, мужской гомосексуализм, принадлежность к негроидной расе, женский пол (!) и наличие в анамнезе инфекций, передаваемых половым путём 2,7,8 .
Что же касается России, то эпидемиология генитального герпеса у нас изучена явно недостаточно. Известно, что доля серопозитивных людей в популяции увеличивается с возрастом: от 1% у подростков 14–17 лет до 19–38% в возрасте 55–64 года. Более точных достоверных цифр, которые можно было бы сравнить с зарубежными, за последние 10–15 лет найти не удаётся 32 . При этом регистрируемая заболеваемость (чуть менее 22 на 100 тыс.) сравнительно с развитыми странами подозрительно низка.
Вероятно, мы наблюдаем недорегистрацию, и причины этого явления довольно легко обозначить. Первая — низкая обращаемость вследствие недостатка информированности населения. Часть больных с такой симптоматикой, как зуд, жжение или выделения из половых путей не считают её достаточным поводом, чтобы обращаться к врачу, а значит, не получают лечения, не заботятся о предохранении и длительное время выступают резервуаром генитального герпеса в популяции. Вторая причина — частные клиники, не всегда добросовестно подающие сведения в органы регистрирующие инстанции.
Штрихи к портрету
ДНК-содержащие вирусы семейства Herpesviridae персисти-руют в организме хозяина пожизненно — генетический материал вируса встраивается в ДНК нервных клеток человека: ВПГ-1 обычно осваивает ганглии тройничного нерва, ВПГ-2 — тазовые ганглии (а также клетки слизистых оболочек половых путей, например цервикального эпителия). Это едва ли не самые распространённые в популяции патогенные микро-организмы 1–3 . Сегодня известны восемь типов герпесвирусов, однако орофациальные и генитальные поражения вызывают только два типа: ВПГ-1 (преимущественно лабиальный герпес) и более опасный последствиями ВПГ-2 4,7 . Передача ВПГ-2, как правило, происходит половым путём, но возможен и вертикальный путь передачи — от матери ребёнку во время родов.
У 70–80% больных генитальным герпесом заболевание вызвано ВПГ-2, а у остальных 20–30% — ВПГ-1. Однако в последние годы ВПГ-1 в мочеполовом тракте выявляют всё чаще 6 . Скорее всего, происходит это по двум причинам: во-первых, в социуме всё большее распространение получают орогенитальные контакты, а во-вторых (и эта причина гораздо прозаичнее), с внедрением высокоточных методов диагностики вирусные инфекции стали лучше выявлять.
Небезопасный спутник
Как и всякое заболевание, передаваемое половым путём, генитальный герпес нередко становится виновником психологических и психосексуальных расстройств. И этот аспект инфектологии изучен ещё далеко недостаточно. В частности, многие проведённые в этом направлении исследования, к сожалению, используют ограниченную выборку, слишком разнообразные для сравнивания анкеты и отчётности, отсутствуют контрольные группы, не ведётся учёт уже существующих до инфицирования психопатологических отклонений. Так, хотя было показано, что рецидивы генитального герпеса и стресс часто совпадают по времени, не удаётся установить, что же из них первично — данные ретроспективных и проспективных исследований расходятся.
Тем не менее есть причины утверждать, что у страдающих рецидивами генитального герпеса нередко возникают депрессии; у них снижена уверенность в себе, они испытывают подавленность, гнев и враждебные чувства по отношению к человеку, который, как они полагают, их заразил 11,12,17 .
В исследовании белорусских коллег были использованы анкеты-опросники DIQL (Дерматологический индекс качества жизни) и RGHQoL (Опросник качества жизни пациентов с рецидивирующим генитальным герпесом), и оказалось, что качество жизни пациентов с рецидивирующим генитальным герпесом средней степени тяжести значительно снижено и не превышает 30% нормы 36 .
В числе отрицательных следствий генитального герпеса значится также и влияние на половую потенцию — доказано, что ВПГ-инфицированные мужчины достоверно чаще обращаются к врачу по поводу эректильной дисфункции 18 .
При беременности и потом
В ряде европейских стран по ВПГ-2 серопозитивны от 10 до 40% беременных. В России этот показатель достигает 31%. У беременных ВПГ-2 опасен не только везикулярными высыпаниями и нарушением психологического равновесия — описаны случаи гораздо более серьёзных осложнений: острого гепатита с тромбоцитопенией и коагулопатией 21 , эндометрита, диссеминированной инфекции 23 . И хотя частота таких осложнений невелика, о потенциальной возможности подобных состояний врачу следует помнить. Любое необъяснимое осложнение во время беременности должно быть рассмотрено в том числе и с точки зрения вероятности герпетической атаки.
Однако наиболее серьёзную опасность ВПГ представляет для плода ввиду несформированности его иммунной системы. Риск передачи инфекции плоду максимален в III триместре; при этом в 80% случаев инфицирование происходит интранатально, в 15% — постнатально и в 5% — антенатально 31 . К счастью, частота неонатального герпеса относительно невелика. В США, где учёт проводят очень скрупулёзно, статистика приводит показатель заболеваемости неонатальным герпесом 3,3 на 100 тыс. новорождённых 28 , для контраста в Малави (Восточная Африка) заболеваемость в 22 раза выше — 72 на 100 тыс. 29 . А вот что касается России, то достоверных и свежих данных по количеству заболевших новорождённых найти не удалось; публикации на эту тему, представленные в интернете, не отличаются высокой достоверностью и весьма противоречивы. По крайней мере, в 1995 году этот показатель держался на уровне 14,1 на 100 тыс. 30 . Получается, мы где-то посередине, но где именно — установить не так-то просто. А между тем осложнения неонатального герпеса разнообразны и часто фатальны (летальность может достигать 80%). Перенесённый неонатальный герпес нередко выливается в инвалидность.
- Невезикулярные поражения гортани и гениталий плода 23 .
- Водянка плода и преждевременные роды 20 .
- Эпиглоттит новорождённого с тяжёлой интоксикацией 22 .
- Тяжёлые поражения кожи и центральной нервной системы, гиперлейкоцитоз 25 .
- Сепсис в первые 5 нед 24 .
- Энцефалит, при подостром течении приводящий к мультикистозной энцефалопатии с минерализацией и дефицитом цереброспинальной жидкости 19 .
- Респираторный дистресс-синдром, апноэ, гепатомегалия, гемофагоцитоз, менингит 26 .
- Острый некроз сетчатки глаза 27 .
С сибирской обстоятельностью
Для того факта, что в России сложно получить эпидемиологические данные, есть довольно простое объяснение. Дело в том, что для такого рода исследований необходимо финансирование, которое во всём мире происходит за счёт государственных средств и фондов научных исследовательских центров, что в России пока случается совсем нечасто. Тем ценнее редкие и качественные российские научные работы. Так, в течение многих лет, с 1994 по 2005 год проходило крупное исследование популяций народов Сибири, включая городские и сельское население — в Новосибирске, Республике Горный Алтай и Республике Тыва.
Эта работа была инициирована в рамках международных исследований: WHO MONICA (Мониторинг заболеваемости и смертности от сердечнососудистых заболеваний и уровней их факторов риска) и HAPIEE (Детерминанты сердечно-сосудистых заболеваний в Восточной Европе: мультицентровое когортное исследование). Вот его хронология.
В общей сложности были проанализированы образцы сыворотки крови 1014 жителей; 47,4% составили мужчины и 52,6% — женщины. Протокол исследования одобрен Этическим комитетом НИИ терапии Сибирского отделения РАМН. Все обследованные подписали информированное согласие для участия в исследовании.
Обсуждаем и сравниваем
Общая распространённость антител к ВПГ-1 у взрослых не различалась между обследованными популяциями и в целом составила 99,4%. Таким образом, инфицированы этим вирусом почти все взрослые жители обследованных регионов. Среди школьников 14–17 лет антитела выявляли гораздо реже — серопозитивными оказались 78,8% подростков (рРаспространённость антител к ВПГ-2 у взрослого населения Новосибирска в целом за 1994–2005 года составила 21,1%, будучи выше у женщин по сравнению с мужчинами (26,3 и 17% соответственно; p13. Не исключено, что достаточно низкая инфицированность сибирских подростков связана с тем, что в этом регионе очень распространён ВПГ-1, в результате чего возникает перекрёстный иммунитет заодно и к ВПГ-2 5 . Как и ожидали исследователи, общая частота выявления антител к ВПГ-2 возрастала пропорционально возрасту (см. инфографику).
Что касается Тывы и Горного Алтая, то распространённость антител к ВПГ-2 у коренного населения в целом составила 20,2%. Однако женщины были инфицированы достоверно чаще мужчин — 23,5 и 7,9% соответственно (p=0,03). В целом Западная и Восточная Сибирь не различались по частоте выявления антител к ВПГ-2, а значит, этот показатель не зависит от этнической принадлежности (европеоиды и монголоиды), а также уровня урбанизации (промышленный мегаполис или посёлок) — распространение инфекции в Сибири универсально. А вот в США данные контрастны: неевропеиоидное население инфицируется ВПГ-2 почти в 3 раза чаще (45,9%), чем европеоидное (17,6%) 14 .
Если сравнивать распространённость ВПГ-2 в Сибири с другими регионами мира, то получается, что показатели наиболее близки к США и Скандинавским странам, и до благополучной Испании нам ещё далеко. С другой стороны, не может не радовать, что лидируем по частоте серопозитивности всё-таки не мы, а Африка.
В разных популяциях Сибири женщины ожидаемо оказались в 1,5–3 раза чаще инфицированы ВПГ-2, чем мужчины. Сходные данные отмечают практически во всех исследованиях мира. Дело в том, что поверхность слизистой оболочки половых органов у женщин значительно обширнее по площади, что повышает вероятность инокуляции вируса. Кроме того, у мужчин чаще возникают рецидивы, при которых клинические проявления менее выражены. А значит, мужчины смело вступают в половые контакты и заражают партнёрш в наиболее контагиозный период. Не исключено также, что молодые женщины чаще имеют контакты с более взрослыми партнёрами, частота инфицирования которых выше, чем у молодых. И, наконец, вероятность передачи вируса от мужчины женщине шестикратно превышает риск заражения мужчины от женщины 7 . При этом женщины в возрасте от 18 до 39 лет составляют группу риска, у них заболеваемость генитальным герпесом достигает 136 на 100 тыс. населения данного пола и возраста 9,10 .
Она растёт
Эпидемиологические исследования — не только показатель интереса интеллектуального сообщества к тому или иному вопросу. Врачу на приёме, через кабинет которого ежедневно проходят примерно 30 женщин, следует чётко представлять, что почти все они, за казуистическим исключением, носительницы ВПГ-1, и каждая пятая рискует обострением ВПГ-2.
Такая настороженность — очевидный путь преодоления гиподиагностики генитального герпеса, а значит, и всех сопутствующих ему проблем.
Читайте также:

