Онкогенные вирусы что это такое
Обновлено: 23.04.2024
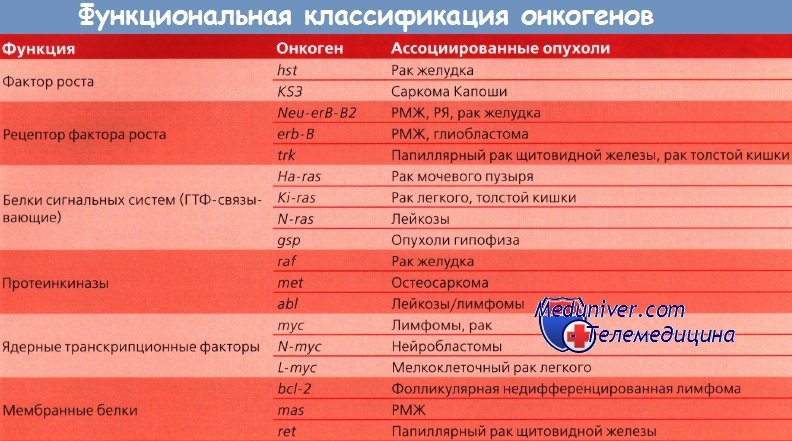
Онкогены и их функциональная классификация
За последние 25 лет произошел существенный прогресс в нашем понимании молекулярных механизмов развития злокачественных опухолей. Идентифицировано три типа генов, нарушения в которых приводят к раку: доминантные трансформирующие, или онкогены; рецессивные трансформирующие, или опухолевые супрессоры; гены, ответственные за репарацию ДНК. Многие онкогены были впервые выделены как формы протоонкогенов онкогенных РНК-содержащих вирусов.
На протяжении многих лет известно, что вирусы способны вызывать злокачественные опухоли у животных. Это наблюдение послужило стимулом к обширным исследованиям, направленным на выявление генов, которые вызывают рак и переносятся вирусами, и генов человека, повреждающихся при развитии злокачественных опухолей. В итоге обнаружили удивительный факт, что гены, вовлеченные в канцерогенез, часто представляют собой измененные формы вирусных генов.
Другие протоонкогены кодируют внутриклеточные белки, ответственные за усиление митогенного сигнала; третьи — кодируют белки, вовлеченные в контроль клеточного деления и находящиеся под контролем ядра. Такие онкогены могут быть активированы посредством нескольких механизмов: возможна амплификация гена и активация его копий; в редких случаях наблюдается траислокация гена на другую хромосому, где он попадает под контроль чужого промотора и стимулирует неконтролируемый рост. Три группы онкогенов находятся под разным контролем.
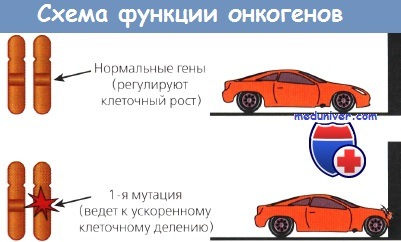
Первая группа включает пептидные факторы роста и их рецепторы, как, например, эпидермальный или тромбоцитарный.
Эти пептиды служат скорее костимуляторами опухолевого роста, чем факторами, непосредственно инициирующими опухолевую трансформацию. По мере расшифровки механизмов, стимулирующих опухолевую прогрессию, все более реальной становится молекулярно-нацеленная (таргетная) терапия, направленная непосредственно против продуктов этих генов или против белков, активируемых ростовыми факторами. Так разработаны препараты:
1) трастузумаб (Герцептин) — моноклональные антитела, блокирующие Her-2/neu;
2) иматиниба мезилат (Гливек) — препарат, частично блокирующий активность c-kit, BCR-ABL и некоторых других тирозинкиназ;
3) цетуксимаб (Эрбитукс) — моноклональные антитела, связывающиеся с рецептором эпидермального фактора роста;
4) гефитиниб (Пресса) — низкомолекулярный ингибитор некоторых изоформ рецептора эпидермалыюго фактора роста.

Другой класс онкогенов происходит из немембранных внеядерных факторов роста, передающих каскадные сигналы внутри клетки. К ним относятся G-белки и белки семейства ras. Наконец, некоторые онкогены кодируют ядерные регуляторные белки, например myc. Схематическое изображение функций онкогенов представлено на рисунке.
Открытие человеческих аналогов вирусных генов привело к формулировке многообещающей гипотезы, согласно которой злокачественные опухоли человека, включая большинство невирусной этиологии, могут возникать вследствие мутаций, превращающих полезные протоонкогены в опасные онкогены. В подтверждение этой гипотезы показано, что повреждение даже одного аллеля таких протоонкогенов достаточно для злокачественной трансформации некоторых клеток in vitro. Подобные доминантные мутации ведут к гиперэкспрессии нормального гена и, следовательно, гиперпродукции нормального белка или же к синтезу его аберрантной формы, обладающей повышенной активностью.
В любом случае результатом оказывается усиление стимулирующих сигналов внутри клетки, даже в отсутствие стимулирующих воздействий извне.
Парадоксально, но первым ключом к выявлению некоторых онкогенов стало исследование РНК-содержащих онкогенных вирусов животных, не вызывающих опухолей у человека. Эти ретровирусы, инфицирующие кур, грызунов, кошек и обезьян, оказались крайне высокоонкогенными: развитие опухоли часто наблюдали уже при первом контакте. У одного из вирусов этой группы, вируса саркомы кур Рауса, выявлен ген, ответственный за злокачественное перерождение инфицированных клеток. Этот тип трансформирующих онкогенов был назван вирусным онкогеном.
Единственный онкоген вируса саркомы Рауса, проникая в клетки кур, способен нарушать и перестраивать их метаболизм, направляя его по пути злокачественной трансформации.
В 1976 г. Varmus и Bishop показали, что онкоген вируса саркомы Рауса в действительности вовсе не есть вирусный ген, а происходит от предсуществовавшего клеточного гена, захваченного предком вируса саркомы Рауса. Однажды встроив его в свой геном, вирус далее использовал этот ген для трансформации клеток млекопитающих.
Более ранние предки вируса саркомы Рауса были способны реплицироваться в инфицированных клетках, но не могли трансформировать ее; туморогенный потенциал был приобретен после захвата нормального клеточного гена — протоонкогена. В связи с этим значение работы Varmus и Bishop гораздо больше, чем просто исследование вируса саркомы Рауса: показано существование гена в нормальном геноме клеток млекопитающих, обладающем трансформирующим потенциалом при соответствующей активации, в данном случае ретровирусом.
Информация, полученная при исследовании ретровирусов и онкогенов, существенно помогла в изучении причин злокачественных новообразований. Ретровирусы, так же как вирус саркомы Рауса, неинфекционны для человека и, соответственно, не могут активировать протоонкогены человека. Однако возможны альтернативные механизмы их активации. Эффекты, сходные с производимыми вирусом в последовательности ДНК, могут быть вызваны химическими или физическими воздействиями.
Это было подтверждено в начале 80-х годов прошлого столетия: в геноме опухолевых клеток были выявлены мутированные гены (протоонкогены). Во всех случаях причиной превращения протоонкогена в активный онкоген оказались изменения последовательности гена. Например, онкоген ras образуется из протоонкогена-предшественника в клетках рака мочевого пузыря человека вследствие замены одной пары нуклеотидных оснований; онкоген myc появляется во многих злокачественных новообразованиях в результате амплификации.
В последующем были изучены механизмы, посредством которых большинство, если не все онкогены вызывают трансформацию клеток. Это стало возможным благодаря определению путей, посредством которых клетки регулируют свой собственный рост. Рост иделение нормальной клетки вткани контролируется преимущественно ее окружением. В норме клетка редко или даже никогда не определяет скорости своего деления, а только реагирует на сигналы от окружающих клеток.
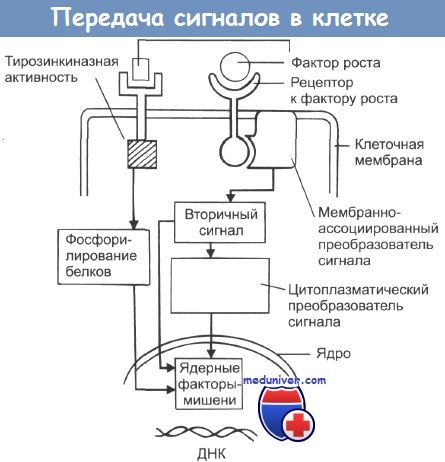
Эти сигналы, стимулирующие или подавляющие рост, передаются посредством ростовых факторов, выделяемых окружающими клетками. Ростовые факторы попадают в межклеточное пространство и связываются с рецепторами на поверхности клеток-мишеней. Клетки реагируют на сигналы ростовых факторов активацией механизмов синтеза клеточных структур, удвоением ДНК и делением. Нормальная клетка никогда не запускает программу роста, если она не получила внешнего сигнала. Каждая клетка обладает сложной системой, позволяющей ей получать ростовые сигналы, обрабатывать их и запускать программу деления. Эта система состоит из большого количества белков, ответственных за получение ростовых сигналов и передачу их в клетку. К этим белкам относятся:
1) рецепторы на клеточной поверхности, распознающие наличие во внеклеточном пространстве ростовых факторов и передающие сигнал во внутриклеточное пространство;
2) белки внутриклеточной сигнальной системы, которые активируются поверхностными рецепторами и затем передают сигнал дальше в клетку;
3) ядерные транскрипционные факторы, активирующиеся в ответ на сигнал, переданный белками внутриклеточной сигнальной системы, и, в свою очередь, активирующие широкий спектр клеточных генов.
Активирующиеся гены руководят программой роста клетки; именно эти гены определяют те события, которые вместе взятые приведут к делению клетки. Протоонкогены кодируют многие белки в этой сложной сигнальной системе, позволяющей нормальной клетке отвечать на экзогенные ростовые факторы. Белки онкогенов участвуют в сигнальной системе, отбирая ее неправильно функционирующие версии нормальных компонентов, и вызывают ее постоянную стимуляцию в отсутствие внешних ростовых сигналов. В результате клетка постоянно растет, даже если окружающая среда не содержит каких-либо факторов, в норме необходимых для клеточного роста.
Некоторые исследователи указывают, что в злокачественной клетке должны присутствовать как минимум две мутации в протоонкогенах, причем только строго определенные мутации могут вызывать злокачественную трансформацию. Это связано с тем, что отдельные онкогены, даже если они служат важными регуляторами клеточного метаболизма, сами по себе не способны индуцировать злокачественное новообразование. Данная точка зрения подтверждается выявлением в опухолевых клетках более 10 различных онкогенов. Однако при тщательном исследовании ожидаемые нарушения обнаруживают лишь примерно в 20 % опухолей.
Ни одна опухоль не несет ни одной пары сочетанных нарушений из выявляемых в культивируемых линиях злокачественных клеток. Предполагается также, что врожденные мутации, ответственные за предрасположенность людей к раку, не есть онкогены. Это объясняется существованием рецессивных антионкогенов, получивших название генов-супрессоров, тоже играющих крайне важную роль в развитии опухолей.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
РНК-вирусы как причина развития рака - вирусный канцерогенез
Открытие вирусов, вызывающих злокачественные опухоли у животных, произошло еще на рубеже XIX и XX веков. В 1910 г. Пейтон Рауш обнаружил, что бесклеточный фильтрат из тканей птичьей саркомы может вызывать развитие аналогичной саркомы у цыплят. Примерно в это же время была доказана вирусная природа птичьего миелобластоза. Позднее было обнаружено, что часто проходит весьма значительный латентный период между инфицированием вирусом и развитием рака.
Тем не менее вплоть до 1960-х годов не существовало четких доказательств того, что инкорпорация вирусной ДНК в геном клетки является необходимым условием развития злокачественной трансформации, как не было и случаев выделения вирусной ДНК из раковых клеток.
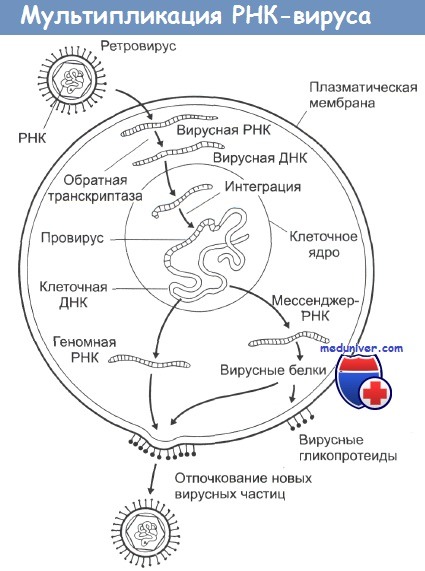
РНК-содержащие вирусы вызывают развитие целого ряда различных опухолей у животных, при этом наиболее распространена индукция этими вирусами лимфом, лейкемий и сарком. Типичная структура таких вирусов - это две идентичные цепочки молекул РНК в сочетании с ферментом обратная транскриптаза, одетых в гликопротеиновую оболочку. При инфицировании вирусом его обратная транскриптаза заставляет клетки синтезировать ДНК, комплементарную вирусной РНК.
Эта ДНК затем встраивается в клеточные хромосомы, и на ее основе клетка уже сама начинает синтез новых вирусных белков, вирусных обратных транскриптаз и элементов гликопротеиновой оболочки. Из-за механизма их действия этот тип вирусов получил название ретровирусы. Все они имеют весьма схожий внешний вид на электронных микрофотографиях и являются самыми маленькими из известных вирусов.
Некоторые из ретровирусов (например, вирусы птичьего лейкоза, кошачьей и мышиной лейкемии) содержат в себе только три гена и обладают очень длительным инкубационным периодом с момента заражения до возникновения опухоли. Другие вирусы (например, вирус саркомы Рауса (ВСР)) вызывают очень быструю злокачественную трансформацию и могут быть выделены из культуры опухолевых клеток.
Показано, что вирус ВСР содержит особый ген (v-src), способный вызывать трансформацию фибробластов in vitro. Этот ген кодирует наработку протеинкиназы, которая фосфорилирует тирозин. К сожалению, действие этой протеинкиназы запускает целый каскад различных метаболических процессов, и очень сложно оценить, какой именно из них ведет к злокачественной трансформации.
В настоящее время известно, что и нормальные, и злокачественные клетки содержат в своем генотипе участки ДНК, сходные или идентичные ряду последовательностей онкогенных РНК-содержащих вирусов. Такие участки получили название клеточных прото-онкогенов (чтобы отличать их от вирусных онкогенов). Постулируется, что активация этих участков, возникающая в результате канцерогенного воздействия, запускает целую цепочку событий, ведущую в итоге к злокачественной трансформации клетки. Считается также, что ретровирусы инкорпорировали эти клеточные участки в свой геном в процессе эволюции.
В настоящее время мы лучше понимаем механизмы действия продуктов вирусной активации. Примером такого продукта является протеинкиназа, активируемая геном sre, а также целый ряд других вирус-индуцированных канцерогенов. Это и рецепторы к эпидермальному фактору роста, продуцируемые геном v-erb, и тромбоцитарный фактор роста (ТФР), кодируемый фрагментами гена v-sis, и целый ряд связывающихся с ядром клетки белков, продукцию которых вызывает вирус птичьей лейкемии.
Как нормальные, так и раковые клетки содержат в себе участки последовательностей ДНК, гомологичные РНК онкогенных вирусов. Если происходит экспрессия или активация под действием канцерогенов этих клеточных онкогенов, это ведет к злокачественной трансформации клеток.
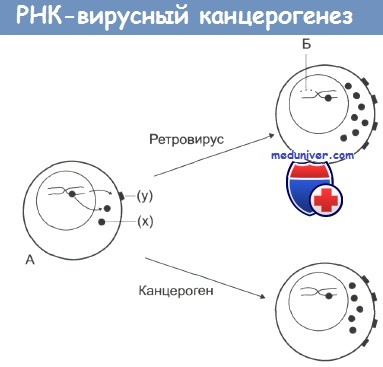
Онкогенная и злокачественная трансформация.
На стадии А нормальная клетка, которая характеризуется низкой протоонкогенной активностью, продуцирует фактор роста (х) или белки дифференцировки или рецепторы (у).
Канцерогены повышают активность протоонкогенов, что дает начало неопластической трансформации.
По другому механизму: при заражении ретровирусом происходит внедрение в ДНК клетки вирусных промоторов или онкогенов (Б), что также ведет к увеличению онкогенной активности и последующей злокачественной трансформации.
Первым ретровирусом, для которого была однозначно доказана связь со злокачественными новообразованиями, был вирус Т-клеточной лейкемии человека (ВТКЛ-1), выделенный из клеток хронической кожной Т-лимфомы. Этот вирус довольно широко распространен, может передаваться половым путем, через кровь, особенно в среде наркоманов, и от беременной женщины к плоду. Первоначально эндемический ареал циркуляции данного вируса был в основном представлен тропическими странами, однако в настоящее время в США серопозитивная реакция на вирус обнаруживается у каждого из 4000 человек населения. Кроме Т-клеточной лейкемии вирус вызывает тропический спастический паралич.
После 20 лет наблюдения за серопозитивными пациентами оценено, что риск развития последнего заболевания составляет около 5%. Один из вирусных генов, а именно tax-ген, вызывает увеличение продукции клеточного интерлейкина-2 (ИЛ-2) и его рецепторов, что является основным фактором, стимулирующим деление Т-клеток.
Ретровирусы могут вызывать опухолевые заболевания не напрямую, а опосредованно, как это было показано для вируса иммунодефицита человека (ВИЧ-1), вызывающего развитие СПИДа. Случаи развития рака у ВИЧ-инфицированных рассмотрены в одном из обзоров. Отмечается, что у ВИЧ-инфицированных наиболее часто развиваются три типа опухолей: мгновенная или высокозлокачественная В-клеточная лимфома; саркома Капоши (СК, которую вызывает другой вирус — герпесвирус ГСК, или герпесвирус 8); карцинома шейки матки.
До разработки эффективных методов терапии ВИЧ-инфицированных более 40% из них заболевали тем или иным видом рака. Тем не менее связь этого вируса с развитием онкологических заболеваний скорее всего косвенная и опосредована развитием общей хронической иммунодепрессии организма, которая и позволяет другим канцерогенным вирусам вызывать рак. В-клеточные лимфомы также характеризуются довольно сложным патогенезом. Хотя В-клетки не поражаются вирусом ВИЧ-1, они могут быть мишенью для других типов вирусов, например для вируса Эпштейна-Барра (ВЭБ). Рак шейки матки у женщин также развивается на основе вторичной вирусной инфекции — вируса папилломы человека (ВПЧ), на фоне общей иммунодепрессии, вызванной ВИЧ-1. По причине общего снижения иммунных реакций организма все эти опухоли развиваются особенно быстро и агрессивно.
Показано, что РНК-содержащий вирус гепатита С значительно увеличивает риск заболевания гепатоклеточной карциномой. У больных, инфицированных этим вирусом, риск развития раковой опухоли возрастает в 100 раз, но механизмы его канцерогенного действия в настоящее время почти не изучены. Если больной заражен еще и вирусом гепатита В, риск развития рака печени возрастает многократно. На земном шаре одним или обоими из этих вирусов заражено около миллиарда человек.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021

Большинство из нас знает, что введение вакцин, в разговорной речи называемое прививками, используется с целью стимуляции иммунной системы здорового человека для дальнейшей борьбы с инфекционными заболеваниями, такими как корь, краснуха, оспа и т. д. Иммунная система вырабатывает антитела к безвредным вирусным компонентам; в результате при повторном контакте с патогеном иммунитет с большей вероятностью сможет распознать и атаковать чужеродные вещества.
Вакцины от рака бывают двух типов:
- профилактические;
- лечебные (терапевтические).
Вакцины для профилактики рака
По своей сути профилактические вакцины ничем не отличаются от привычных нам вакцин. Данные препараты защищают организм от вирусов, способных вызывать рак. Основа патогенеза онковирусов заключается в связи между вирусной инфекцией и последующей трансформацией клетки в опухолевую. Следовательно, человек должен быть вакцинирован до заражения вирусом. К профилактическим вакцинам относятся, например:
- вакцина против ВПЧ (вирус папилломы человека), вызывающего почти все виды рака шейки матки и связанный с развитием некоторых видов новообразований, в т.ч. опухолей горла, прямой кишки, а также других видов рака;
- вакцина против гепатита В, которая предотвращает заражение вирусом гепатита В (HBV). Длительная инфекция HBV может вызвать рак печени.
Вакцины для лечения рака
Терапевтические вакцины предназначены для индукции лизиса раковых клеток посредством стимуляции иммунной системы. Этот тип вакцин наряду с другими видами терапии используется при обнаружении в организме человека опухоли. Терапевтические вакцины способствуют распознаванию белков, экспрессируемых определёнными раковыми клетками, что помогает иммунной системе обнаруживать и уничтожать опухолевые очаги.
Терапевтические вакцины способствуют:
- остановке дальнейшего роста опухоли;
- уничтожению раковых клеток, оставшихся после других видов терапии;
- предотвращению рецидивов.
Типы терапевтических вакцин [1]:
- Антигенные вакцины
Эти вакцины производятся на основе специальных белков (антигенов), присутствующих в раковых клетках. - Клеточные вакцины
При создании цельноклеточных вакцин используют всю раковую клетку, а не только определенный клеточный белок (антиген). Такие вакцины производятся на основе собственных раковых клеток, раковых клеток другого человека или раковых клеток, выращенных в лаборатории. - Вакцины с дендритными клетками
Дендритные клетки помогают иммунной системе распознавать и атаковать аномальные клетки — в частности, раковые. Для создания таких вакцин дендритные клетки выращивают в лаборатории вместе с раковыми и затем вводят больному. - ДНК-вакцины
Данные вакцины изготавливаются из кусочков ДНК опухолевых клеток.
Терапевтические противораковые вакцины, используемые в настоящее время, включают:
- Sipuleucel-T (Provenge), которая используется для лечения рака предстательной железы. Каждая доза содержит специфически модифицированные в лаборатории лейкоциты пациента [2].
- Вакцину Bacillus Calmette–Guérin (BCG, БЦЖ), которая первоначально была разработана против туберкулеза и затем одобрена для лечения рака мочевого пузыря. БЦЖ — это живые бактерии, вводимые в мочевой пузырь через катетер. Бактерия привлекает иммунные клетки, которые затем атакуют раковые [3].
Вирусы папилломы человека (ВПЧ/HPV) — разнородная группа вирусов семейства Papillomaviridae, которые могут выступать в роли онкогенных агентов. В 1976 году Харальд цур Хаузен впервые высказал предположение об онкогенном потенциале ВПЧ при раке шейки матки (по частоте онкологических заболеваний женщин занимает четвертое место [4]). Долгое время появление рака шейки матки пытались связать с инфекцией вирусом простого герпеса типа 2 (ВПГ-2). А уже в 1984 году Хаузен с соавторами публикует ряд статей, подтверждающих взаимосвязь рака шейки матки с ВПЧ: приблизительно 90 % биоптатов содержали последовательности ДНК папилломавирусов, из них 57,4 % — ВПЧ типа 16 или 18 [5, 6].
В 2008 году за эти открытия Харальд цур Хаузен был удостоен Нобелевской премии по физиологии и медицине. ВПЧ способны инфицировать только эпителиальные клетки, причем в дифференцированных клетках инфекция носит непродуктивный характер. Таким образом, ВПЧ способен поражать эпителий кожи, слизистую оболочку мочевыводящих и половых путей, ротовой полости, гортань, глаз и другие органы. Вирус блокирует экспрессию антионкогенов p53 и pRb и усиливает пролиферацию клеток. В связи с этим основное проявление ВПЧ-инфекции — это появление на пораженном участке новообразований, чаще доброкачественных, таких как обычные, плоские, аногенитальные бородавки и папилломы на подошвах ног.
Онкогенные типы ВПЧ обнаруживают при таких злокачественных новообразованиях, как колоректальный рак, рак влагалища, полового члена, слизистой оболочки ротоглотки. Но четкая взаимосвязь между вирусом и образованием злокачественной опухоли на данный момент была доказана только для рака шейки матки [7].
По современным данным, ВПЧ различных типов обнаруживают в 99,7 % биоптатов при верификации рака шейки матки, при этом типы 16 и 18 присутствуют в 70 %. Так как ВПЧ является одним из главных факторов риска развития данной разновидности рака, были предприняты успешные попытки разработки вакцин против ВПЧ, которые опосредованно служат вакцинами от рака шейки матки.
ВОЗ рекомендует проведение вакцинации на национальном уровне и девочкам, и мальчикам в возрасте 9–14 лет, то есть перед началом половой жизни. При этом вакцинироваться можно и позже, до 45 лет (ранее считалось, что только до 27 лет). В ряде стран вакцины против ВПЧ уже включены в национальный календарь прививок в различном объеме (не во всех странах вакцинируют мальчиков), в России — только в ряде регионов.
Еще одним онкогенным вирусом является вирус Эпштейна — Барр, которым заражены до 90 % населения Земли. Вирус является возбудителем инфекционного мононуклеоза, чаще всего проявляющегося клинически при заражении в юношеском возрасте.
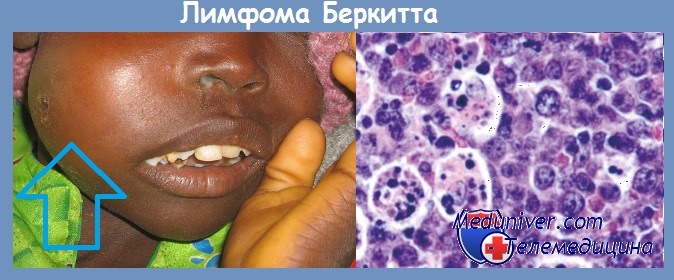
Этот вирус поражает клетки иммунной системы, а именно B-лимфоциты, ответственные за выработку антител. Носительство вируса Эпштейна — Барр связывают с возникновением таких форм онкологии, как лимфома Ходжкина, лимфома Беркитта, карцинома желудка и рак носоглотки. В настоящее время причина возникновения мутации доподлинно не известна, однако выявлена связь некоторых штаммов, распространенных в определенных областях, с развитием злокачественных новообразований. Так, у пациентов с лимфомой Беркитта в экваториальной Африке в 100 % случаях тест на вирус Эпштейна —Барр дает положительный результат [11].
В настоящее время вакцина от данного вируса все ещё находится в разработке. Процесс создания вакцины осложняется высокой вариабельностью штаммов вируса в зависимости от зоны распространения [12].
Развитие онкологических заболеваний можно также предупредить с помощью вакцин от вирусов гепатита. Гепатиты, вызываемые вирусами гепатита B и C, могут привести к развитию рака печени. Вирус гепатита B при персистировании в организме способен реактивироваться в условиях иммуносупрессии — например, при ВИЧ-инфекции или при прохождении химиотерапевтического лечения. В таком случае вакцина применяется не для профилактики рака, а для его лечения.
Вакцина против гепатита B, по данным некоторых исследователей, может работать в качестве противоракового адъюванта — вещества, усиливающего иммунный ответ [13]. Причем вакцина может использоваться не только при раке печени, но и при лечении злокачественных опухолей в других органах — например, глиобластомы [14]. Если говорить о формировании иммунитета против вируса после введения вакцины, то это возможно только в условиях нормального функционирования иммунной системы, то есть вакцинирование должно проводиться до развития иммунодефицита.
Итак, мы убедились, что привиться от рака возможно, но только в случае, если рак провоцируется онкогенными вирусами. Но помимо вирусов, инициаторами злокачественного роста могут служить и бактерии. Так, примером может служить широко известная Helicobacter pylori, с которой ассоциирован в том числе и рак желудка. При этом носители могут и не подозревать о таком риске, ведь часто присутствие H. pylori никак не проявляется [15].
К настоящему времени нам следует учитывать, что носителями H. pylori является более 50 % населения планеты и что, согласно данным Интернационального агентства по изучению рака, эта бактерия относится к первой группе канцерогенов [16].
В настоящее время все больше людей узнают о микробиоме и его пользе; при этом все реже мы задумываемся о вреде бактерий в желудочно-кишечном тракте, списывая все проблемы на иные микроорганизмы.
Но, во-первых, H. pylori приютилась не в кишечнике, а в желудке. Как известно, рН в желудке низкий (другими словами, кислотность высокая), а в таких условиях микроорганизмам крайне сложно выживать. Но, подобно тому, как это бывает в сценарии фильма, зло порой оказывается сильнее. Вот и в нашем случае в агрессивной среде желудка научилась выживать патогенная H. pylori.
Во время инфекции H. pylori воздействует, в частности, на клеточный белок кортактин, который необходим для правильной регуляции перестроек цитоскелета в здоровых клетках. Нарушение регуляции активности кортактина играет решающую роль в развитии различных форм рака, а также незлокачественных заболеваний, таких как воспалительные заболевания кишечника (гастриты) [17].
Из вышесказанного одно ясно точно — вакцины, которые препятствуют развитию рака, существуют, их активно используют в исследованиях, а некоторые даже применяют в клинике для лечения и профилактики онкозаболеваний — например, при терапии рака печени (вирус гепатита B) и предотвращения рака шейки матки (ВПЧ). Исследования в данном направлении интенсивно развиваются, и на сегодняшний день уже можно с уверенностью сказать, что они вносят весомый вклад в здравоохранение, а в дальнейшем такие разработки могут принести ещё больше пользы в борьбе против рака.
Очень велик, однако, вклад исследований онкогенных вирусов в понимание этиопатогенеза злокачественных заболеваний в целом. Ученые смогли удостовериться в том, что патогенез онкозаболеваний может быть связан с внешними биологическими возбудителями, и спектр воздействия на них в ходе терапии должен быть шире, методы — изящнее и продуманнее. Если брать во внимание подход, заключающийся в профилактике канцерогенных воздействий, можно с толикой уверенности предположить, что в будущем противоопухолевая терапия может стать крайне эффективной.
Вакцина против рака — это недостижимый идеал медицины, к которому стремятся ученые со всего мира, косвенно или напрямую. Хоть его приближение и связано в наибольшей степени с генной инженерией, в рамках которой уже сейчас используется виротерапия, мы были рады поделиться с вами этой безусловно полезной информацией о вакцинах против онковирусов, которые хоть и с натяжкой, но можно назвать вакцинами против рака.
ДНК-вирусы как причина развития рака - вирусный канцерогенез
В канцерогенезе также могут участвовать ДНК-содержащие вирусы. Наиболее крупные ДНК-содержащие вирусы принадлежат к группе герпесвирусов. Первым вирусом, выделенным из культуры опухолевых клеток, был вирус Эпштейна-Баррра (ЭБВ).
Вирус был получен из культуры опухолевых клеток больных лимфомой Беркита. В культуре in vitro ЭБВ вызывает бесконечную пролиферацию человеческих В-лимфоцитов. Вирусные гены, встраиваясь в геном этих клеток, инициируют пролиферацию путем активации клеточных генов-регуляторов роста (онкогенов).
В крови больных лимфомой Беркита обнаруживается более высокий, чем у здоровых людей, титр антител к антигенам вирусной оболочки и к мембранным антигенам. В то же время в африканских странах среди множества детей, инфицированных этим вирусом, лимфома развивается только в единичных случаях.
Механизм онкогенеза этого заболевания не может быть объяснен только вирусным заражением. К тому же, за пределами африканского континента регистрируются случаи заболевания лимфомой Беркита, абсолютно не связанные с инфицированием вирусом ЭБВ. По-видимому, ЭБВ также может принимать участие в патогенезе карциномы носоглотки, так как клетки этой опухоли экспрессируют вирусные антигены EBNA-1.
При исследованиях саркомы Капоши, развивающейся у больных СПИДом, в 1994 г. из ее клеток был выделен новый герпесвирус. Первоначально вирус получил название герпес-вируса саркомы Капоши (ГСК), впоследствии он был переименован в герпесвирус человека серотип 8 (ГВЧ 8). Вирус обнаруживается в веретеновидных клетках саркомы Капоши практически при всех случаях заболевания.
ГВЧ 8 был также найден в опухолевых клетках первичной эффузионной лимфомы и в клетках многоочаговой болезни Кастлемана. Данный вирус кодирует синтез циклина, который является промотором клеточного деления, чем и объясняется высокая пролиферативная активность инфицированных клеток.
Человеческие папилломавирусы (ПВЧ) вызывают кожные бородавки и ряд доброкачественных папиллом. Это весьма обширный класс вирусов, и некоторые его представители могут в той или иной степени участвовать в развитии злокачественных опухолей. Большинство вирусов вызывает лишь ограниченную пролиферацию клеток, но ряд серотипов может вызвать и развитие злокачественных новообразований.
Наибольшую опасность с точки зрения онкологии представляют серотипы 16, 18, 31 и 33. Более 90% опухолей карциномы шейки матки in situ обнаруживают в своих клетках генные последовательности вирусов ПВЧ. Эти вирусы также играют значительную роль в возникновении инвазивных и многоочаговых плоскоклеточных раков кожи, которые часто развиваются у больных после долгосрочных курсов иммуносупрессивной терапии.
Механизмы вирусного канцерогенеза в этом случае изучены недостаточно. В исследованиях доказано, что существует вероятность включения вирусной ДНК в клетки базального эпителия. Обычно в клеточную ДНК внедряются восемь ранних и два поздних гена. Ранние гены Е6 и Е7 вызывают пролиферацию клеток.
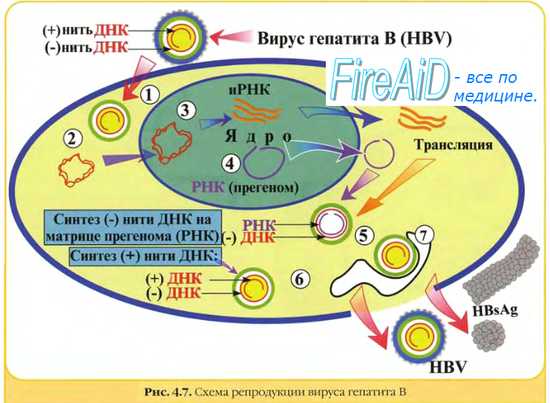
Вирус гепатита В четко связывают с развитием печеночно-клеточного рака. Риск развития этого заболевания у инфицированных вирусом в 200 раз превышает таковой у неинфицированных людей. Механизмы зарождения рака не до конца понятны: считается, что вирус вызывает бесконечную пролиферацию клеток, хотя зараженные вирусом клетки уничтожаются иммунной системой организма. Возможно, что пролиферирующие клетки становятся чувствительными к другим канцерогенам, например к афлатоксину.
Подытоживая вышесказанное, можно заключить, что основным механизмом канцерогенного воздействия является повреждение молекул ДНК и нарушения процессов ее репарации. Если не происходит исправления первичных повреждений ДНК, ошибки со временем начинают накапливаться, что ведет к дестабилизации структуры хромосом и к соматическим мутациям. Большинство таких мутаций летальны для клетки.
Однако, если часть клеток выживает, происходит постепенное накопление клеточной массы с опухолевым фенотипом, что в итоге приводит к клиническим проявлениям. Большой вклад в понимание этого процесса внесли современные исследования механизмов регулировки клеточного цикла и недавнее открытие регуляторных белков, которые запрещают клетке делиться, если ее геном сильно поврежден.
Для развития опухоли может быть недостаточно единичных мутаций в генах-регуляторах деления, но накопление массы ошибок в регуляторных генах может привести к фатальным последствиям. Особенно критичны мутации в генах, регулирующих клеточное деление, так называемых онкогенах. Очень опасны также мутационная инактивация генов, подавляющих клеточное деление — генов-подавителей опухоли, и мутации в генах, кодирующих белки, запрещающие деление при повреждении клеточного генотипа.
Накопление числа жизнеспособных мутаций по одному или нескольким из этих генов приводит к общей клеточной дезорганизации и к потере контроля над клеточным делением. В следующем разделе мы рассмотрим механизмы действия онкогенов и наиболее важные моменты контроля над клеточным циклом.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Читайте также:

