Опухоль мозга и грипп
Обновлено: 05.05.2024
Больные, находящиеся на лечении по поводу злокачественных новообразований, за счет измененного иммунного статуса подвержены простудным заболеваниям, которые в свою очередь еще больше истощают защитные силы организма и затрудняют терапию основного диагноза
ОРВИ при злокачественных новообразованиях: риски и сложности терапии
Острые респираторные вирусные инфекции (ОРВИ), в том числе и грипп, составляющие основную долю инфекционной патологии населения всех возрастов, представляют существенную угрозу пациентам из групп риска: пожилым, беременным, детям младшего возраста и пациентам с хроническими заболеваниями, в том числе онкологическими.
Больные, находящиеся на лечении по поводу злокачественных новообразований, за счет измененного иммунного статуса подвержены простудным заболеваниям, которые в свою очередь еще больше истощают защитные силы организма и затрудняют терапию основного диагноза.
При ОРВИ на фоне онкологического процесса лечащий врач сталкивается со следующими трудностями:
- Длительность ОРВИ у иммунокомпрометированных пациентов может достигать нескольких недель, в течение которых состояние больных значительно ухудшается, и не только по иммунным показателям.
- Инфекционный процесс заставляет откладывать очередной курс химиотерапии, что сильно сказывается на прогнозе.
- Назначение противовирусной терапии может вызвать осложнения, а в частности лекарственную гепатотоксичность, так как ее эффект накладывается на гепатотоксичное действие фармакотерапии злокачественного заболевания 1 .
Таким образом, можно сказать, что необходимость в профилактике и терапии ОРВИ у онкологических пациентов неоспорима, но последнее упомянутое обстоятельство резко ограничивает выбор конкретного средства.
Варианты противовирусной терапии
Вирус-специфические препараты римантадин, занамивир и осельтамивир доказали свою эффективность, которая распространяется однако только на вирус гриппа. Кроме того, эти средства имеют ряд противопоказаний, которые зачастую делают невозможным их применение у онкологических пациентов.
В случае назначения средств, действующих на определенные вирусные белки, следует учитывать также проблему резистентности, которую вырабатывают к ним вирусы 2 . Так, появились данные о повышении до 18% частоты устойчивости вирусов гриппа А (H3N2) к осельтамивиру среди детей, получавших данный препарат для лечения гриппа 3 .
В связи с вышесказанным сегодня как никогда высока потребность в противовирусных препаратах, действующих не на инфекционный агент, а на иммунные защитные механизмы.
Оптимальное противовирусное средство, которое может быть рекомендовано для онкологической практики, должно:
- не вызывать резистентности, вероятно вследствие отличного механизма действия;
- быть безопасным, в частности при длительном применении;
- иметь минимальный риск побочных эффектов при лекарственном взаимодействии.
Перспективы использования иммуномодуляторов
Указанным критериям в полной мере соответствуют иммуномодулирующие средства, благодаря чему интерес к ним клиницистов-онкологов в последние годы резко возрос.
Иммуномодуляторы – это лекарственные средства, которые обладают иммунотропной активностью и в терапевтических дозах восстанавливают эффективную иммунную защиту. Растущая опухоль вызывает существенные изменения в иммунном ответе, а проводимая химио- и лучевая терапия, а также любые оперативные вмешательства вызывают или усугубляют иммунную недостаточность 4 . Поэтому использование иммуномодуляторов, в частности для лечения сопутствующих инфекций, является оправданным.
Эргоферон: элегантное решение непростого вопроса
Главной особенностью релиз-активных препаратов является способность воздействовать на биологически активные молекулы мишени (эндогенные регуляторы), модифицируя их физико-химические свойства. Эффект проявляется не только на молекулярном, но и на клеточном, органном, системном и организменном уровнях.
Так, прием Эргоферона усиливает функциональную активность макрофагов, натуральных киллеров и ИФН при помощи релиз-активных антител к ИФН-γ и CD4+. На этапе цитотоксических клеточных реакций CD8+ и CD4+ Т-лимфоцитов Эргоферон поддерживает противовирусный иммунитет при участии компонента релиз-активных антител к CD4+. На более поздних этапах релиз-активные антитела к CD4+ через стимуляцию рецепторов CD4 Тх2 поддерживают гуморальный противовирусный иммунитет.
Третий компонент Эргоферона – релиз-активные антитела к гистамину – обеспечивает противовоспалительный и антигистаминный эффекты, которые проявляются уменьшением длительности и выраженности катаральных симптомов и аллергических реакций, сопутствующих инфекционному процессу 7 . Это является важным преимуществом Эргоферона перед другими противовирусными препаратами, так как позволяет снизить потребление других средств и нивелировать риск лекарственного взаимодействия при параллельно проводящейся противоопухолевой терапии.
Клинический опыт
Эргоферон применяется в клинической практике с 2011 года, и его эффективность была доказана в ходе рандомизированных клинических исследований. На данный момент завершено 3 клинических исследования и продолжаются еще 4.
Исследований по лечению ОРВИ именно у онкологических больных не проводилось. Однако в клинической практике накоплен опыт назначения Эргоферона госпитализированным больным с солидными опухолями (Шаповалова Ю.С). Учитывая актуальность проблемы отсрочек курсов химиотерапии и продления сроков госпитализации, в 2012 г. был разработан внутрибольничный протокол лечения ОРВИ у госпитализированных пациентов с солидными злокачественными новообразованиями. В него включены следующие противовирусные препараты: для лечения гриппа – ингибиторы нейраминидазы занамивир и осельтамивир, а также римантадин, умифеновир и Эргоферон; для лечения ОРВИ – умифеновир и Эргоферон. Эргоферон применялся в виде монотерапии (37 пациентов) или в комбинации с римантадином (14 пациентов) в течение первых 48 часов от начала проявления симптомов заболевания. Все пациенты выздоровели через 5-9 дней лечения; нежелательных реакций, связанных с изучаемой терапией, отмечено не было. Учитывая благоприятный профиль переносимости Эргоферона и отсутствие гепатотоксичности, его применение может быть востребовано для лечения ОРВИ у пациентов онкологического профиля, в том числе находящихся в процессе химиотерапии.
Следует также отметить, что согласно экспериментам использование релиз-активных антител к ИФН-γ не приводит к гиперпродукции ИФН-γ. Этот факт немаловажен в свете недавних исследований, показавших, что ИФН-γ в больших дозах может приводить к увеличению метастазирования в легкие и резистентности клеток меланомы к терапии 11 .
Учитывая безопасность Эргоферона, доказанную в исследованиях высокого методологического качества, можно сделать вывод, что препарат стоит рекомендовать для лечения ОРВИ у пациентов со злокачественными новообразованиями 12 .
Выводы
Как доказали результаты экспериментальных и клинических исследований Эргоферон является перспективным противовирусным препаратом с принципиально новым механизмом и мишенями воздействия, и он может помочь решить проблему лечения больных в условиях изменчивости антигенных свойств вирусов и исходно скомпрометированного иммунного статуса. Комплексный препарат, сочетающий противовирусное, иммуномодулирующее, противовоспалительное и антигистаминное действие, оказывает выраженный терапевтический эффект при ОРВИ у пациентов с онкологической патологией. Препарат имеет благоприятный профиль безопасности, и его назначение позволяет снизить лекарственную нагрузку и риск лекарственного взаимодействия с противоопухолевыми препаратами.
2 Heaton NS et al. Genome-wide mutagenesis of influenza virus reveals unique plasticity of the hemagglutinin and NS1 proteins. Proc Natl Acad Sci USA 2013; 25.
3 Антимикробная терапия по Джею Сэнфорду. Под ред. Д.Гилберта, Р.Меллеринга мл., Дж.Элиопулоса и др. М.: ГРАНАТ, 2013.
5 Сыроешкин А.В., Никифорова М.В., Колдина А.М., Горнак А.А., Тарабрина И.В. Лекарственные препараты на основе релиз-активных антител. Справочник поликлинического врача. 2018 (3):15-20
6 Эпштейн О.И. Сверхмалые дозы (история одного исследования). М.: Изд-во РАМН, 2008.
7 Жавберт Е.С., Дугина Ю.Л., Эпштейн О.И. Противовоспалительные и противоаллергические свойства антител к гистамину в релиз-активной форме: обзор экспериментальных и клинических исследований. Детские инфекции. 2014; 1: 40-3.
8 Архивъ внутренней медицины. 2013; 14 (6): 46.
9 Шиловский И.П., Корнилаева Г. В., Хаитов М.Р. Новые возможности в терапии респираторно-синцитиальной вирусной инфекции: данные доклинического исследования препарата Эргоферон. Иммунология. 2012; 33 (3): 144-8.
11 Taniguchi K, Petersson M, Höglund P et al. Interferon gamma induces lung colonization by intravenously inoculated B16 melanoma cells in parallel with enhanced expression of class I major histocompatibility complex antigens. Proc Natl Acad Sci USA 1987; 84 (10): 3405-9.
Прогноз рака головного мозга
Прогноз злокачественных глиом в значительной степени определяется степенью злокачественности опухоли и другими хорошо известными прогностическими факторами. Больных со злокачественными глиомами можно подразделить на две прогностические группы.
Больные с опухолями I и II степени характеризуются относительно неплохим прогнозом, и их 5- и 10-летняя выживаемость составляет 65% и 35% соответственно. У больных с опухолями III и IV степени 5-летняя выживаемость не превышает 10%, и еще более неутешительный прогноз существует для группы с опухолями IV степени.
Медиана выживаемости для больных с глиобластомой остается крайне низкой, около 11 месяцев. При неполном удалении опухолей прогноз по всем группам больных ухудшается.
В случаях медуллобластомы на прогноз влияют различные факторы. Одинаково важен возраст больных и полнота удаления опухоли; более благоприятный прогноз характерен для детей старше 15 лет. Если при первичном осмотре у ребенка обнаружены метастазы в спинной мозг, то шанса на излечение практически не остается. Важную роль играет как техника лучевой терапии, так и назначаемая доза радиации. Сейчас, при применении современной аппаратуры, срок 5-летной выживаемости больных превышает 40%.
При эпендимоме прогноз зависит от степени злокачественности опухоли. Медиана выживаемости больных после проведения им операции по поводу низкозлокачественной эпен-димомы составляет примерно 10 лет. Более злокачественные опухоли часто дают рецидивы, и медиана средней выживаемости больных со злокачественной эпендимомой не превышает 2-3 лет.
Хирургическое лечение опухолей гипофиза и менингиом совместно с лучевой терапией дает неплохой прогноз. Известны результаты, полученные на нескольких больших группах больных с опухолями гипофиза. Продолжительность жизни больных сильно варьирует. При хордоме прогноз крайне неблагоприятный, поскольку эту опухоль обычно трудно удалить полностью, и она содержит радиоустойчивые клетки.
Последние исследования, проведенные среди детей с высокозлокачественной глиомой, показали, что гиперэкспрессия белка р53 связана с неблагоприятным прогнозом, независимо от клинической картины болезни. Всего от опухолей мозга и ЦНС в Великобритании в 2001 г. умерло 3400 человек, что составляет 2% смертности от всех онкологических заболеваний. За последние двадцать лет в Великобритании несколько увеличились европейские стандартизованные коэффициенты смертности (с 5,5 до 6,3 на 100 000 мужчин и с 3,6 до 3,9 на 100 000 женщин).
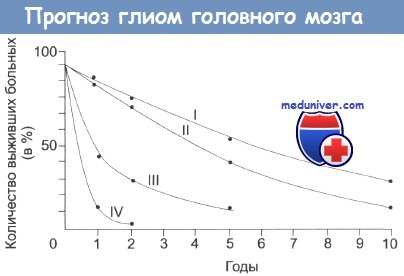
Продолжительность жизни больных со злокачественной глиомой различной степени.
Отметьте, что даже в случаях низкозлокачественной опухоли выживает немного больных.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Грипп с легочными осложнениями. Головной мозг при гриппе
Второй разновидностью тяжелой формы гриппа является грипп с легочными осложнениями, который развивается при присоединении бактериальной или второй вирусной инфекции.
Изменения периферических органов иммуногенеза при неосложненном гриппе характеризуются подавлением морфологических реакций, характеризующих иммуногенез, и преобладанием элементов повреждения тканей.
Причем отмечается особенно выраженное подавление иммуноморфологических реакций у детей в возрасте до 3 лет и у ослабленных детей [Гусман Б. С, 1975].
Изменения при гриппе в головном мозге и внутренних органах раньше трактовались как наступающие в результате циркуляторных расстройств и токсического действия вируса гриппа. В настоящее время при использовании метода иммунофлюоресцирующих антител выявлен антиген вируса гриппа в ганглиозных клетках головного мозга, тонком кишечнике, печени, эпителии канальцев почки, поджелудочной железе, выделен вирус гриппа из крови, мочи, спинномозговой жидкости [Ритова В. В., 1965], что указывает на возможность размножения вируса в различных органах, имеющих эпителий и эндотелий, в том числе и в мягких мозговых оболочках.
Поэтому генез изменений ЦНС и внутренних органов должен рассматриваться как результат прямого действия вируса и опосредованного — через циркуляторные расстройства, возникающие вследствие токсического действия вируса гриппа на сосудистую стенку.
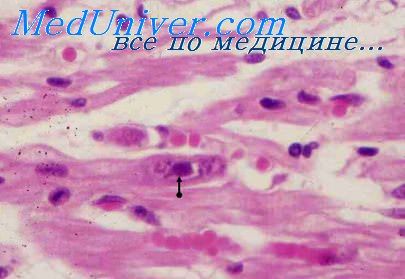
Микроскопически обнаруживаются полнокровие, стазы, гиалиновые тромбы, иногда кольцевидные кровоизлияния, дистрофия нервных клеток, иногда периваскулярные лимфомоноцитарные инфильтраты.
Все эти изменения наиболее выражены в диэнцефальной области и в вегетативных ганглиях [Ладодо К. С, 1972]. В редких случаях на почве циркуляторных расстройств в ткани головного мозга и оболочках бывают массивные кровоизлияния. В почках постоянно выявлялись цитоплазматические фуксинофильныс включения в нефротелии.
Наиболее выраженные изменения были обнаружены в нефротелии извитых, прямых канальцев и петлях нефрона и состояли в дистрофических изменениях цитоплазмы и лизисе ядер с превращением клеток в полиморфные безъядерные ацидофильные тельца с плотной цитоплазмой. В просвете канальцев скапливались десквамированные клетки, эритроциты, белковые преципитаты.
В клубочках выявлялись выраженные циркуляторные расстройства, в капсуле почечного клубочка — единичные эритроциты, белковые массы [Валькович Э. И., 1978]. Автор указывает на высокую частоту гломерулонефрита с минимальными изменениями у детей в возрасте до 1 года.
В сердце, кроме дистрофических изменений миокарда, иногда выявляются некротические изменения отдельных мышечных волокон и клеток интрамуральных ганглиев [Ильин Г. И. и др., 1977], что на основании экспериментальных данных объясняется нарушением иннервации сердца и сосудов [Сергеев Н. В. и др.. 1962] либо непосредственным действием па капилляры сердца токсических продуктов вируса [Соловьев В. Д. и др., 1973].Описаны единичные случаи миокардита [Новикова О. Я. и др., 1973].
Менингит — воспаление оболочек головного и спинного мозга — может встретиться в практике врача любой специальности. В настоящее время исход болезни определяется в основном своевременным началом адекватной терапии Этиология менингитов многообр
Менингит — воспаление оболочек головного и спинного мозга — может встретиться в практике врача любой специальности.
В настоящее время исход болезни определяется в основном своевременным началом адекватной терапии
 |
Этиология менингитов многообразна. Возбудителями менингита могут быть бактерии (менингококк, пневмококк, гемофильная и туберкулезная палочки, спирохеты и др.), вирусы (энтеровирусы группы Коксаки-ЕСНО, вирус эпидемического паротита и др. ), хламидии, микоплазмы, простейшие, грибы.
Менингиты могут быть первичными, т. е. развиваться без предшествующих признаков патологического процесса, вызванного соответствующим возбудителем, например менингококковым, или вторичными, когда поражению оболочек мозга предшествуют другие проявления инфекции. Например, эпидемический паротит — паротитный менингит, лептоспироз — менингит, отит — отогенный пневмококковый менингит и т. д. Менингиты, вызываемые одним и тем же возбудителем, могут протекать как первичные и вторичные (пневмококковый, туберкулезный и т. д.), поэтому вторичные менингиты правильнее рассматривать не как осложнение, а как проявление соответствующей инфекции.
Эпидемиология менингитов определяется свойствами возбудителя и механизмом его передачи. Первичные менингиты, как правило, являются воздушно-капельными инфекциями, энтеровирусные же имеют фекально-оральный механизм передачи. Для практического врача важно, во-первых, то обстоятельство, что менингит является лишь одной из клинических форм инфекции, вызываемых соответствующим микроорганизмом (например, менингококковая инфекция протекает чаще всего в форме назофарингита, энтеровирусная инфекция в форме респираторной или кишечной инфекции); во-вторых, вторичные менингиты могут вызываться условно-патогенной аутофлорой, поэтому случаи менингита в семейных очагах, как правило, единичные, спорадические, а групповые заболевания возможны только в коллективах (ясли, школа, общежитие, воинская часть и т. д.).
В оболочки мозга возбудители могут проникать гематогенно (при менингококковой инфекции, сепсисе, лептоспирозе и т. д.), лимфогенно и по контакту при наличии гнойно-воспалительных очагов на голове (отит) и в области позвоночника (остеомиелит, эпидуральный абсцесс).
Менингиты сопровождаются повышенной продукцией цереброспинальной жидкости и развитием внутричерепной гипертензии, повышением проницаемости гематоэнцефалического барьера, токсическим поражением вещества мозга, нарушением мозгового кровообращения, особенно микроциркуляции, нарушением ликвородинамики, гипоксией мозга, что в конечном итоге приводит к развитию отека-набухания мозга. Этому способствует распространение воспалительного процесса на желудочки и вещество мозга, что в особенности свойственно гнойным менингитам. При вирусных менингитах явления отека мозга менее выраженны, но вещество мозга также вовлекается в патологический процесс. При распространении воспалительного процесса на вещество мозга появляется очаговая неврологическая симптоматика.
Финалом отека-набухания мозга является его дислокация со сдавлением ствола мозга миндалинами мозжечка. Клинически при этом наблюдаются расстройства функций жизненно важных органов, прежде всего дыхания, что и является наиболее частой причиной смерти больных менингитами.
Хотя клинически менингиты различной этиологии существенно различаются, все же преобладают общие симптомы, объединяемые понятием “менингеальный” синдром. Менингиты чаще начинаются остро, нежели постепенно (туберкулезный, грибковые); обычно симптомам менингита предшествуют общие инфекционные симптомы — лихорадка, слабость, боли в мышцах и другие, свойственные данной болезни: при менингококковой инфекции — сыпь, при пневмококковой — ринит, пневмония, отит, при паротитной инфекции — поражение слюнных желез, при энтеровирусной — диспепсические расстройства и катаральные явления и т. д.
Наиболее ранним и ярким симптомом менингита является головная боль диффузного характера, которая быстро нарастает, приобретает распирающий характер и достигает такой интенсивности, что взрослые больные стонут, а дети кричат и плачут. Вскоре начинается тошнота и у части больных рвота, в некоторых случаях — многократная. Головная боль усиливается при перемене положения тела, от звуковых и зрительных раздражителей. Отмечается общая гиперестезия кожи. Больные обычно лежат на боку, согнув голову, иногда (особенно дети) поджав ноги к животу. При осмотре выявляется ригидность мышц затылка, верхний, средний и нижний симптомы Брудзинского, симптомы Кернига и Нери. Часто выявляется анизорефлексия, пирамидные знаки. В более поздние сроки возможны парезы черепных нервов, реже парезы конечностей, мозжечковые расстройства, нарушения сознания вплоть до развития мозговой комы, делириозный синдром.
Решающим для подтверждения диагноза менингита является исследование цереброспинальной жидкости. По показаниям проводят дополнительные исследования (рентгенографию черепа и придаточных пазух носа, осмотр глазного дна, электроэнцелографию, эхо-энцефалографию, компьютерную и ядерно-магнитнорезонансную томографию). При люмбальной пункции определяют давление цереброспинальной жидкости, проводят ликвородинамические пробы Стуккея и Квикенштедта, определяют визуальные характеристики жидкости (прозрачность, цвет). В осадке жидкости определяют количество и состав клеток, наличие микрофлоры. Проводят биохимические (количество белка, глюкозы, хлоридов, осадочные пробы и т. д.) и микробиологические исследования.
Менингококковый менингит начинается остро с высокой лихорадки, озноба. В первый-второй день у большинства больных появляется геморрагическая сыпь. Менингеальные симптомы появляются также на первые-вторые сутки болезни. Спинномозговая жидкость мутная, молочно-белого или желтоватого цвета, содержит в 1 мл несколько тысяч нейтрофилов, в цитоплазме которых часто видны характерные бобовидные диплококки; при посеве можно выделить культуру возбудителя. Количество белка значительно повышено, глюкозы — снижено. При помощи иммунологических методов в цереброспинальной жидкости можно обнаружить антиген возбудителя, а используя полимеразную цепную реакцию (ПЦР) — его ДНК. В крови резко выражены островоспалительные изменения. Если не проводить соответствующего лечения, летальность при менингите достигает 50%. При своевременной терапии летальность составляет менее 5%, главным образом за счет тяжелых форм менингококкцемии, осложненных инфекционно-токсическим шоком, при котором поражение оболочек мозга слабо выражено.
Пневмококковому менингиту, как правило, предшествует отит, синусит или пневмония, но у половины больных он протекает как первичный. Начало острое, менингеальный синдром выявляется несколько позже, чем при менингококковом менингите. Даже при условии ранней госпитализации болезнь быстро прогрессирует, рано появляются расстройства сознания, судороги, нередко парезы черепных нервов, гемипарез. Цереброспинальная жидкость гнойная, часто ксантохромная, обнаруживаются внеклеточно расположенные ланцетовидной формы диплококки. В связи с быстрым вовлечением в процесс вещества и желудочков мозга, быстрой консолидацией гнойного экссудата летальность достигает 15-25%, даже если терапия начала проводиться на ранних сроках.
Менингит, вызываемый гемофильной палочкой, чаще наблюдается у детей до 1 года; может начинаться как остро, так и постепенно с лихорадки, катаральных явлений. Менингеальные симптомы появляются на второй — пятый день болезни. При этом у детей до 1 года наиболее серьезными симптомами могут считаться срыгивание или рвота, немотивированный пронзительный крик, выбухание и прекращение пульсации родничка.
Большие трудности представляют для диагностики менингиты у больных, получавших лечение антибиотиками в недостаточных для выздоровления дозах. В этих случаях температура тела снижается до 37,5 — 38,5ОС, регрессируют менингеальные симптомы, головная боль становится менее интенсивной, но сохраняет упорный характер, часто остается тошнота, реже рвота. Через несколько дней в связи с распространением процесса на желудочки и вещество мозга наступает резкое ухудшение состояния больных. Появляется общемозговая и очаговая неврологическая симптоматика. В этой группе больных летальность и частота остаточных явлений резко возрастают.
Вирусные менингиты могут начинаться с симптомов, свойственных соответствующей инфекции, тогда как картина менингита развивается позже. В этих случаях наблюдается двухволновое течение болезни. Но менингит с первых дней может быть и ведущим проявлением болезни. В отличие от гнойных бактериальных менингитов, в этом случае лихорадка умеренная, менингеальные симптомы появляются на второй-третий или пятый-седьмой дни с момента начала заболевания, иногда позже. Несмотря на интенсивную головную боль и плохое самочувствие больных, менингеальные симптомы выражены умеренно, часто не в полном объеме, расстройства сознания (исключая вирусные менингоэнцефалиты) не характерны. Люмбальная пункция с эвакуацией 4-8 мл цереброспинальной жидкости приносит больному выраженное облегчение.
| Менингиты классифицируются по этиологии, по характеру воспалительного процесса (серозные, гнойные), причем гнойные менингиты в подавляющем большинстве носят бактериальный характер, а серозные — вирусный, однако последние могут быть и бактериальными (туберкулезный, лептоспирозный и др.). По патогенезу выделяют первичные и вторичные менингиты |
Цереброспинальная жидкость прозрачная, количество клеточных элементов измеряется десятками или сотнями, более 90% лейкоцитов составляют лимфоциты. (Иногда в первые два дня болезни могут преобладать нейтрофилы. В этих случаях через один-два дня следует во избежание диагностической ошибки повторить исследование.) Содержание глюкозы повышено или нормальное, количество белка может быть как понижено (разведенный ликвор), так и незначительно повышено, при посеве цереброспинальная жидкость стерильна (асептический менингит). В результате иммунологических исследований в цереброспинальной жидкости можно обнаружить антигены вирусов или антитела, методом ПЦР — наличие вирусной нуклеиновой кислоты. Картина крови в большинстве случаев мало характерна.
Туберкулезный менингит, который раньше обязательно заканчивался смертью больного, в настоящее время встречается чаще, причем у большинства больных он является первым клиническим проявлением туберкулезной инфекции. Нередко туберкулезный менингит протекает атипично, поэтому при наличии большого количества эффективных противотуберкулезных препаратов летальность составляет 15-25%. Обычно болезнь начинается с лихорадки. Через несколько дней появляется головная боль и рвота. Менингеальные симптомы появляются на третий — десятый дни болезни. Довольно часто обнаруживаются парезы черепных нервов. К концу второй недели, иногда позже, развиваются общемозговые симптомы. При отсутствии специфической терапии больные погибают к концу месяца, но даже неспецифическая терапия может продлить жизнь больного до 1,5—2 месяцев. Важно подчеркнуть, что нецеленаправленная терапия аминогликозидами, рифампицином, а также любыми другими антимикробными препаратами может вызвать временное улучшение, что в значительной степени затрудняет диагностику. Цереброспинальная жидкость при туберкулезном менингите опалесцирующая, вытекает под высоким давлением. Количество лейкоцитов (преимущественно лимфоциты) составляет от нескольких десятков до трех-четырех сотен в 1 мкл. Содержание белка, как правило, повышено; количество глюкозы — со второй-третьей недели болезни — снижено, осадочные пробы резко положительные. Микобактерии туберкулеза в цереброспинальной жидкости обнаруживается очень редко. Для подтверждения диагноза важно обнаружение антигенов возбудителя ИФА, выявление легочного процесса (чаще милиарный туберкулез).
Менингиты приходится дифференцировать с широким кругом болезней, протекающих с синдромом менингизма, то есть характеризующихся наличием менингеального синдрома, не связанного с воспалительным процессом в оболочках мозга.
Это прежде всего инфекционные болезни, протекающие с выраженным нейротоксикозом, например грипп, сальмонеллез, крупозная пневмония и др. В этих случаях наличие общих признаков инфекционной болезни, тяжесть состояния являются показанием для экстренной госпитализации в инфекционный стационар, менингеальный синдром служит показанием для спинномозговой пункции.
Второе место занимают субарахноидальные кровоизлияния, не связанные с черепно-мозговой травмой. Их причиной является разрыв аневризмы или патологически измененных сосудов оболочек головного мозга. Болезнь начинается с внезапной головной боли (удар в голову), которая сначала может быть локальной, но быстро приобретает диффузный характер. При осмотре выявляется менингеальный синдром, повышение артериального давления. Через два-три дня картина может измениться: головная боль нарастает, наблюдается рвота, температура тела повышается. Это связано с развитием асептического воспаления, не требующего специальной терапии. Такие пациенты должны госпитализироваться в неврологические отделения. Окончательный диагноз устанавливается после исследования цереброспинальной жидкости, которая в этих случаях равномерно окрашена кровью, после центрифугирования — красная, прозрачная (лаковая), позже — мутноватая, ксантохромная. В мазке — эритроциты, нейтрофилы и лимфоциты в различных соотношениях, количество белка повышено, иногда резко, глюкозы — в норме или повышено.
Синдром менингизма наблюдается при внутричерепных объемных процессах, интоксикациях (печеночная и уремическая кома, отравление суррогатами алкоголя), инсультах и многих других болезнях.
На догоспитальном этапе важно провести дифференциальный диагноз между первичными и некоторыми вторичными гнойными менингитами, при которых больные подлежат оперативному лечению (оториногенные менингиты; менингиты, осложняющие абсцесс мозга или эпидуральный абсцесс). Например, летальность при отогенных менингитах, лечение которых проводилось консервативными методами, достигает 25%, тогда как в результате своевременной операции летальность снижается до 5%.
Лечение больных той или иной формы менингита следует начинать на догоспитальном этапе. Перед транспортировкой целесообразно ввести седативные препараты и анальгетики, а также, если нет признаков обезвоживания, лазикс; при подозрении на бактериальный менингит — пенициллин в дозе 3-4 млн. ЕД в/м, так как большинство бактериальных менингитов вызывается чувствительной к нему флорой. При наличии судорог необходимы противосудорожные препараты. Если имеются признаки шока (цианоз, обильная геморрагическая сыпь, артериальная гипотензия, похолодание конечностей, анурия), а также отека мозга с дислокацией (кома, судороги, расстройства дыхания, нарушения гемодинамики), больные должны госпитализироваться реанимационной службой.
В стационаре лечение проводится по следующим направлениям:
- этиотропная терапия;
- лечение и профилактика развития отека мозга;
- дезинтоксикация;
- индивидуальная терапия.
При выборе этиотропных средств лечения менингитов следует помимо общих подходов, основанных на видовой или индивидуальной чувствительности возбудителя, учитывать биологическую доступность возбудителя, поскольку многие антибиотики (макролиды, аминогликозиды, пенициллины и цефалоспорины) плохо проникают через гематоэнцефалический барьер. В отношении пенициллинов и некоторых цефалоспоринов III поколения (цефотаксим, цефтриаксон), учитывая их низкую токсичность, терапевтической концентрации в субарахноидальном пространстве достигают за счет повышения дозы. Поскольку более 90% менингитов вызываются флорой, чувствительной к этим препаратам, они должны рассматриваться как препараты выбора до установления этиологии болезни. В зависимости от вида возбудителя могут быть использованы хлорамфеникол, тетрациклины, амикацин, рифампицин, ванкомицин, бисептол, фторхинолоны, азтреонам, меропенем, амфотерицин В и другие противогрибковые препараты. При туберкулезном менингите применяют комбинированную терапию (изониазид, этамбутол, рифампицин). Назначение антимикробных препаратов при вирусных менингитах бесполезно.
Для лечения и профилактики отека мозга проводят плановую дегидратацию с использованием таких препаратов, как лазикс, урегид, диакарб. В тяжелых случаях назначают дексазон в дозе до 0,25 мг/кг массы в сутки. Дегидратация должна сочетаться с введением жидкости перорально, через зонд и внутривенно в объемах, достаточных для поддержания нормоволемии. Важное значение имеет оксигенотерапия путем ингаляции кислородно-воздушной смеси, по показаниям — ИВЛ.
Целесообразно использование препаратов, улучшающих мозговой кровоток, антиоксидантов, антигипоксантов, ноотропов; если имеются показания, применяют противосудорожные средства.
Выписка из стационара производится после полного регресса менингеальной и общемозговой симптоматики, санации цереброспинальной жидкости, а при менингококковой инфекции — после получения отрицательных результатов бактериологического исследования носоглоточной слизи. В неосложненных случаях длительность госпитализации составляет около 20 дней.
После выписки больные должны находиться под наблюдением невропатолога. Вопросы восстановления трудоспособности, возможности обучения, посещения детских коллективов решаются индивидуально. Обычно необходимость в амбулаторном лечении и освобождении от работы сохраняется около 1 месяца. Реконвалесцентам необходимо избегать излишних физических и психоэмоциональных нагрузок, инсоляции, избыточного приема жидкости, ограничивать количество соли, исключить употребление алкоголя. С особенной осторожностью следует подходить к решению вопроса о восстановлении трудоспособности для лиц, работа которых связана с повышенной концентрацией внимания, быстротой реакции, возможностью нестандартных ситуаций.
Опухоль головного мозга может быть доброкачественной и злокачественной. Доброкачественные новообразования давят на участки мозга, расположенные поблизости опухоли, нарушают ликвородинамику и функцию отдельных структур мозга. Признаки рака головного мозга появляются при прогрессировании патологического процесса. Длительное время злокачественные новообразования мозга никак себя не проявляют. Головные боли при опухоли мозга могут быть единственным первым симптомом заболевания.
Для того чтобы определить их причину, локализацию и степень злокачественности патологического процесса, врачи Юсуповской больницы проводят обследование пациента с помощью современных методов нейровизуализации. Диагностические исследования выполняют на новейшей аппаратуре ведущих фирм США и европейских стран.
Основным методом лечения онкологии головного мозга является операция. Нейрохирурги Юсуповской больницы выполняют инновационные оперативные вмешательства, которые позволяют максимально убрать опухоль, не повреждая неповреждённую ткань мозга. Радиологи применяют инновационные методики лучевого лечения. Они облучают только очаг поражения головного мозга, минимально воздействуя на участки мозга, окружающие опухоль. Химиотерапию после операции проводят современными лекарственными средствами, обладающими минимальными побочными эффектами. Каждому пациенту индивидуально подбирают схему лечения и оптимальные дозы химиотерапевтических препаратов.
Как проявляется опухоль головного мозга
На ранних стадиях заболевания признаки опухоли головного мозга у взрослых изменчивы и нетипичные. Довольно часто врачи общей практики допускают различное их толкование, что весьма затрудняет раннюю диагностику. Важнейшим признаком опухоли головного мозга является прогрессирование симптомов заболевания.
Первым, но не обязательным признаком объёмного образования, расположенного внутри черепа, является головная боль. Она беспокоит пациентов при быстрорастущих формах опухоли мозга – глиобластоме, метастазах злокачественных новообразований.
При доброкачественной опухоли головного мозга симптомы заболевания на ранней стадии не определяются. Если злокачественное новообразование растёт медленно, оно также длительное время не проявляется никакими симптомами. Большинство таких опухолей мозга неврологи выявляют при развитии симптомов выпадения или явлений раздражения головного мозга с эпилептиформными припадками. Если новообразование располагается в немых зонах полушарий головного мозга, первыми признаками болезни быть изменением психики пациента.
При офтальмологическом обследовании врачи определяют застойный сосок глазного дна. Ранним признаком опухоли мозга на ранней стадии может быть нарушение остроты зрения. Симптомы рака головного мозга на ранней стадии заболевания у мужчин такие же, как и у женщин.
Первыми признаки рака головного мозга, которые не указывают на локализацию опухоли у взрослых, являются следующие симптомы: односторонние или двусторонние частичные параличи отводящего нерва, синдром ущемления в области задней и средней черепных ямок. При сдавлении глазодвигательного нерва определяется расширенный зрачок и паралич наружных мышц глаза. К первым симптомам опухоли головного мозга у взрослых относятся признаки нарушения сознания и возрастающие двигательные парезы.
Признаки прогрессирующей опухоли головного мозга
Как проявляется рак головного мозга? При прогрессировании опухоли повышается внутричерепное давление. Пациентов беспокоит гипертензионная головная боль. Она нарастает в горизонтальном положении.
Признаками опухоли головного мозга у взрослых являются очаговые симптомы:
- При новообразованиях проекционной двигательной коры – парезы и Джексоновские припадки (судороги, которые возникли однажды в определённой части тела и продолжают периодически возникать в этой части тела);
- В случае поражения области шпорной борозды – фотопсии (появление в поле зрения движущихся точек, пятен, фигур, молний) и гомонимная гемианопсия (состоянием, при котором человек может видеть только одну сторону, правую или левую);
- При локализации опухоли в области мозжечка – нарушение стояния и ходьбы.
Они возникают в связи с раздражением и выпадением функций поражённого отдела головного мозга. Какие симптомы при раке головного мозга в случае прогрессирования заболевания? По мере роста опухоли очаговые симптомы углубляются. Признаки раздражения сменяются симптомами выпадения: вместо джексоновских припадков возникают параличи, фотопсии сменяются гемианопсиями (двухсторонней слепотой в одной половине поля зрения).
Причиной очаговых нарушений может быть поражение Очаговые признаки опухолей больших полушарий головного мозга могут быть связаны с нарушением функции отёка, сосудистых расстройств и других факторов. Постепенно нарастают явления ликворной гипертензии.
Очаговые симптомы рака головного мозга у мужчин и женщин связаны с расположением опухоли в определённой доле мозга.
Опухоль лобной доли головного мозга проявляется следующими симптомами:
- Эпилептическими припадками;
- Моторной афазией (развивается при поражении доминантного полушария);
- Нарушением обоняния;
- Грубым нарушением психики, изменением поведения, личности (с плоскими шутками) и настроения;
- Гиперкинезами (непроизвольными движениями);
- Расстройством координации движений в виде лобной атаксии (нарушений стояния и ходьбы).
Температура при опухоли головного мозга на начальной стадии развития злокачественного новообразования может повышаться до 37-38 градусов. Постепенное разрастание опухоли воздействует на гипоталамус, ухудшает работу гипофиза, значительно снижает скорость реакции и провоцируя скачкообразное непредсказуемое изменение температуры тела. При раке оболочек мозга повышенная температура может сохраняться на протяжении длительного времени за счёт воздействия атипичных клеток на иммунную систему, которая отвечает повышением температуры тела. Резкие перепады и низкая температура при раке головного мозга (менее 35 градусов) наблюдается в случае активного разрастания новообразования.
Симптомы опухоли мозжечка зависят от гистологического типа новообразования. Астроцитома разрастается относительно медленно и редко распространяется в другие участки. У пациентов возникает утреннее недомогание и головная боль, которые могут наблюдаться на протяжении нескольких недель или месяцев. Порой отмечаются атаксия (нарушение согласованности движений различных мышц при условии отсутствия мышечной слабости) и дисдиадохокинезия (неловкое выполнение быстрых чередующихся движений).
Опухоль мозжечка проявляется следующими симптомами:
- Ночной и утренней головной болью;
- Тошнотой и рвотой;
- Сильной апатией;
- Спутанностью мышления и потерей ориентации.
Иногда у пациентов возникают следующие признаки объёмного образования мозжечка:
- Онемение или слабость в конечностях;
- Расстройство речи;
- Ухудшение зрения, размытость или двоение в глазах;
- Потеря памяти;
- Нарушение сознания.
Диспластическая ганглиоцитома мозжечка является доброкачественной опухолью головного мозга, которая развивается вследствие аномального развития коры мозжечка. Пациенты страдают мигренью, головокружением, тошнотой, рвотой. Иногда наблюдаются следующие симптомы:
- Судороги;
- Ортостатическая гипотензия (снижение артериального давления при переходе из горизонтального в вертикального положение);
- Признаки субарахноидального кровоизлияния.
Диагностика новообразований головного мозга
Симптомы нарушения функции того или иного отдела головного мозга являются показанием для обращения к неврологу. В Юсуповской больнице врачи проводят комплексное обследование пациента:
- Оценку общего статуса;
- Выявление неврологической симптоматики и признаков внутричерепной гипертензии по офтальмоскопической картине глазного дна;
- Электроэнцефалографию;
- И применяют современные
- Компьютерную и магнитно-резонансную томографию.
Для решения вопроса о возможности и целесообразности выполнения оперативного вмешательства онкологи Юсуповской больницы проводят магнитно-резонансную томографию согласно стандарту, в трёх проекциях и в трёх режимах (Т1, Т2 и FLAIR). При необходимости используют дополнительные возможности МРТ:
- МРТ-перфузию;
- Функциональную магнитно-резонансную томографию;
- МРТ-диффузию;
- Магнитно-резонансную спектроскопию.
Если исследование не может быть выполнено, проводят контрастную томографию без контрастирования и с контрастным усилением. В рамках дополнительного протокола выполняют позитронную эмиссионную томографию с метионином. Если по данным магнитно-резонансной предполагается обильное кровоснабжение опухоли, нейрохирурги с целью оптимизации тактики оперативного вмешательства выполняют прямую или компьютерную ангиографию.
Биопсия головного мозга является инвазивной диагностической процедурой, при проведении которой хирург извлекает небольшой образец ткани мозга для дальнейшего исследования под микроскопом. В Юсуповской больнице врачи выполняют все биопсии, рекомендованные международной ассоциацией онкологов-нейрохирургов:
- Пункционную биопсию головного мозга, при которой осуществляется просверливание в черепной коробке небольшого отверстия (через отверстие или с помощью тонкой полой проводится забор небольшого образца новообразования или ткани мозга);
- Стереотаксическую биопсию головного мозга – забор небольшого участка ткани мозга или опухоли минимально инвазивным методом (процедуру осуществляют под контролем магнитно-резонансной или компьютерной томографии, высокую безопасность за счёт очень точного перемещения иглы;
- Открытую биопсию головного мозга – забор образца головного мозга во время оперативного вмешательства.
Для диагностики рака головного мозга проводят исследование уровня онкомаркеров:
- α-фетопротеина;
- ПСА;
- СА-15,3;
- CYFRA-21,1.
Первым диагностическим критерием наличия злокачественной опухоли новообразования в организме является повышение уровня α-протеина. Онкомаркер ПСА относится к опухолевым антигенам, которые вырабатывают клетки предстательной железы. У мужчин до сорока лет его концентрация не должна превышать 2,7 нг/мл четырёх нанограмм в миллилитре, а улиц старшего возраста – 4,0 нг/мл. Уровень ПСА повышается при метастазах в головной мозг атипичных клеток из простаты.
Уровень онкомаркера СА 15-3 определяют при подозрении на метастазы рака грудной железы в головной мозг. У женщин в норме концентрация онкомаркера СА 15-3 не превышает двадцати единиц в миллилитре. Если показатель исследования этого опухолевого антигена превышает пятьдесят единиц, можно думать о наличии метастазов рака других органов в головной мозг.
Маркер злокачественной опухоли CYFRA 21-1 исследуют при подозрении на наличие метастазов рака лёгкого в головной мозг. Интерферентные значения онкомаркера Н CYFRA 21-1 не превышают 3,5 нг/мл.
Все случаи рака головного мозга профессора и врачи высшей категории обсуждают на заседании Экспертного Совета Юсуповской больницы. На консультацию приглашают ведущих нейрохирургов из клиник-партнёров. Клиника онкологии оснащена современным оборудованием, укомплектована специально подготовленным персоналом. Это позволяет осуществлять все инновационные операции на высоком профессиональном уровне и обеспечить качественный уход в послеоперационном периоде.
Инновационные методики лечения рака мозга
Нейрохирурги Юсуповской больницы проводят комплексное лечение опухолей головного мозга. Благодаря оснащённости операционных клиники онкологии новейшим оборудованием, врачи выполняют все новейшие операции. Кандидаты и доктора медицинских наук, врачи высшей категории совместно принимают решение о выборе схемы терапии опухоли головного мозга. Химиотерапевты используют новейшие лекарственные препараты, которые обладают высокой эффективностью и минимальным побочным действием. На базе клиники онкологии проводятся клинические исследования, в рамках которых пациентам предлагают дополнительное лечение: фотодинамическую терапию, иммунотерапию.
Целью хирургической операции при опухоли головного мозга является максимально возможное удаление новообразования, компенсация состояния пациента, точный гистологический диагноз. Операция обеспечивает улучшение качества жизни для большинства больных и увеличивает продолжительность жизни для отдельных пациентов. Удаление раковой опухоли мозга уменьшает количество неопластических клеток, что изменяет клеточную кинетику и обеспечивает большую чувствительность клеток опухоли к химиотерапии.
В Юсуповской больнице врачи проводят хирургическое лечение опухоли головного мозга, которое соответствует европейским стандартам нейрохирургии. Удаление опухоли выполняют с использованием микрохирургического инструментария, интраоперационной оптики и нейронавигации при работе в области функциональных зон. Использование навигационной системы позволяет нейрохирургам точнее планировать ход операции и определять границы новообразования при его диффузном росте. Применение нейронавигации позволяет уменьшить размеры краниотомии увеличить степень удаления опухоли.
Для удаления внутримозговых опухолей, сохранение целостности сосудов и мозговой ткани применяют ультразвуковой деструктор. Он уменьшает до минимума травматичность операции. После операции больных активизируют на 2-3 сутки, не зависимо от объёма оперативного вмешательства. Клиническая симптоматика в послеоперационном периоде остаётся минимальной.
Несмотря на быстрое технологическое развитие, стандартная фотонная лучевая терапия до сих пор оставляет за собой ряд вопросов. Целью новых методов в радиотерапии головного мозга является доставка дозы излучения протонного пучка в ткань опухоли как можно более точно. В Юсуповской больнице для лечения пациентов, страдающих опухолями головного мозга, применяют протонную терапию.
Для применения высокоточного метода протонного пучка опухоль рассматривают и определяют с помощью комбинации компьютерной, магнитно-резонансной и позитронно-электронной томографии. Метод применяют для лечения детей со злокачественными заболеваниями или опухолями головного мозга и молодых больных. Вторая группа – раковые заболевания головного мозга, неизлечимые фотонный лучевой терапией из-за их расположения или низкой чувствительностью к радиации.
После операции пациентам, страдающим раком головного мозга, назначают химиотерапевтические препараты. Новые способы введения химиотерапевтических средств местного действия позволяют миновать гематоэнцефалический барьер головного мозга и повысить эффективность химиотерапии. В настоящее время химиотерапевты используют следующие пути введения лекарственных препаратов при раке головного мозга:
- Интратекально – препарат вводят в спинномозговую жидкость;
- Внутрь тканей опухоли – лекарственное средство вводится в полость, которая образовалась после удаления злокачественной опухоли в виде капсул;
- Конвекционно – непосредственно в опухоль или близлежащие к нему ткани вводят катетер, через него химиотерапевтический препарат очень медленно поступает в головной мозг очень в течение нескольких дней, после чего катетер убирают;
- Внутриартериально – препарат вводится напрямую в артерии головного мозга.
Иногда в саму опухоль мозга вводят специальные пластинки, которые содержат химиотерапевтическое средство. Чтобы пройти курс лечения опухоли головного мозга, звоните по телефону Юсуповской больницы.
Читайте также:

