Осложнения противовирусной терапии гепатита с
Обновлено: 24.04.2024
Вирусом гепатита С инфицировано 3% населения Земли. Заболевание в 50-80% случаев принимает хронический характер с разной степенью поражения печени, включая цирроз и гепатоцеллюлярную карциному. Могут развиваться и внепеченочные осложнения. Для их возникновения важное значение имеет длительное течение заболевания, стимуляция В-лимфоцитов антигенами вируса, а также его репликация в отдельных тканях (эпителий слизистой оболочки рта, слюнных желез и т.д.). Ассоциированные осложнения при HCV-инфекции разделены на 3 группы: заболевания, при которых доказана этиологическая роль HCV (смешанная криоглобулинемия); oсложнения, в развитии которых HCV принимает участие в качестве одного из этиологических факторов относятся (узелковый полиартериит, В-клеточная неходжкинская лимфома, иммунная тромбоцитопения, синдром Шегрена, поздняя кожная порфирия, красный плоский лишай и т.д.). и группа состояний, в развитии которых участие вируса предполагается, но требует дополнительных доказательств (гигантоклеточный височный артериит, фиброзирующий альвеолит, полимиозит, миокардит, дерматомиозит и др.). Появление внепеченочных осложнений затрудняет процесс лечения. Поэтому особенно важным является раннее начало лечения гепатита, еще до развития внепеченочных осложнений.

HCV-инфекция относится к индикаторам социального и медицинского благополучия общества [7]. Вирусом гепатита С инфицировано около 3% (180 000 000 человек) населения Земли [39], что по масштабу в 5 раз превосходит расспространенность ВИЧ [40].
Концепция системных поражений при хроническом вирусном гепатите С впервые была сформулирована Апросиной З.Г. [1]. Дальнейшие исследования [12, 25] показали, что при прогрессировании заболевания нередко развиваются внепеченочные осложнения, которые могут протекать как клинически латентно, так и в виде ярких клинических синдромов или самостоятельных заболеваний. Частота их, по результатам исследований больших групп больных, составляет в странах Европы 40-74% [12] и в Северной Америке - 38% [25], что превышает частоту внепеченочных осложнений при вирусном гепатите B (10-20%) [19, 24, 32].
Развитие внепеченочных осложнений происходит не у всех пациентов и определяется комплексом из трех факторов:
1. Длительная персистенция вируса (6-20 лет), что, как полагают, может быть связана с его высокой изменчивостью. Одной из ее возможных причин является высокая изменчивость последнего, так как генетический материал HCV представлен молекулой РНК, для которой в клетке не существует систем репарации [4, 22].
2. Стимуляция CD5 + В-лимфоцитов. Вирус связывается с В-лимфоцитами с помощью гликопротеина Е2 (входит в состав липидной оболочки HCV), который взаимодействует с СD81-рецепторами на поверхности В-лимфоцитов [26, 41]. CD81 экспрессируется практически на всех ядерных клетках и образует различные комплексы со многими поверхностными молекулами, такими как CD19, CD21, HLA-DR на В-лимфоцитах и с CD4, CD8 и СD82 на Т-лимфоцитах. На B-лимфоцитах CD81, как и другие члены этого суперсемейства рецепторов, является необходимым компонентом специфической сети, учавствующей в межклеточной сигнализации, антигенной презентации и клеточной адгезии [33]. Связывание HCV с CD81 на B-лимфоцитах в составе комплекса CD81/CD19/CD21, что понижает активационный порог, что вызывает клональную пролиферацию и продукцию различных аутоантител [37]. Направленная стимуляция В-клеток к клональной пролиферации и продукции аутоантител описана для вируса Epstein Barr [30], который активирует В-клетки, связываясь с CD21. Не исключено, что и HCV проводит активационный сигнал через тот же комплекс [9].
У части больных длительная пролиферация В-лимфоцитов с накоплением генетических мутаций при определенных средовых факторах может привести к развитию злокачественной В-клеточной пролиферации [9, 16, 42].
3. Прямое цитопатическое действие на другие органы и ткани. Доказана возможность репликации HCV в некоторых тканях нелимфоидного происхождения (эпителий слизистой оболочки рта и слюнных желез) [14, 20, 38].
Сообразно доказанности этиологической роли HCV в развитии многообразных ассоциированных осложнений [2, 10, 12, 25, 31, 36] они разделены на 3 группы [4]:
1. Заболевания, при которых доказана роль HCV как основного этиологического фактора (смешанная криоглобулинемия).
2. Заболевания, при которых НСV является одним из этиологических факторов (узелковый полиартериит, В-клеточная неходжкинская лимфома, иммунная тромбоцитопения, синдром Шегрена, поздняя кожная порфирия, красный плоский лишай и др.).
3. Заболевания, при которых роль НСV как одного из этиологических факторов вероятна, но требует дополнительных доказательств (гигантоклеточный височный артериит, фиброзирующий альвеолит, полимиозит, миокардит, дерматомиозит
и др.).
Смешанная криоглобулинемия характеризуется наличием специфических иммуноглобулинов, которые обратимо осаждаются (преципитируют) в сосудах при температуре ниже 37°С, образуя криопреципитаты [23]. Криоглобулинемия классифицируется по компонентам криопреципитата (рис. 1): I тип - в состав криопреципитата входят моноклональные иммуноглобулины только одного класса (наиболее часто - моноклональные IgM, редко - IgG и еще реже - IgA); II и III типы - криоглобулины состоят из иммуноглобулинов разных классов (II - поликлонального IgG и моноклонального IgM, III - поликлонального IgG и моноклонального IgM). При этом поликлональный IgG в обоих типах является антигеном, а IgM - антителом против Fc-фрагмента IgG [6].
Криоглобулинемию II и III типа обозначают как смешанную криоглобулинемию. Основную роль в ее развитии играет вирус гепатита С [5]. У большинства больных смешанной криоглобулинемией выявляется маркер репликации вируса гепатита - HCV РНК в сыворотке крови (70-86%) и в криопреципитатах (93-99%), причем концентрация HCV РНК в криопреципитатах в десятки тысяч раз превосходит таковую в сыворотке [8]. При других заболеваниях смешанная криоглобулинемия встречается значительно реже, например при ревматических болезнях - 6,4% [5].
Рис. 1. Классификация криоглобулинов по J.Brouet [11] и состав криопреципитата
Факторами, способствующими образованию криопреципитатов являются: охлаждение, повышенное гидростатическое давление, а также стаз крови [35]. Криопреципитаты формируются in situ через фиксацию HCV на эндотелии с присоединением циркулирующих иммуноглобулинов. Развитие иммунного воспаления происходит в результате активации комплемента и привлечения лейкоцитов [6]. Клинически это проявляется различными формами поражения микрососудов (геморрагическая пурпура, синдром Рейно, периферическая полиневропатия, гломерулонефрит, легочный васкулит и т.д.).
Геморрагическая пурпура (67- 99%) - воспалительные пятна, до 5 мм в диаметре, (описать как в коже), локализующаяся преимущественно на коже нижних конечностях и нижней половины живота, с тенденцией к изъязвлению. Такие же кожные элементы могут появляться на других легко охлаждаемых участках тела: нос, уши. Отмечаются и другие кожные изменения - ретикулярное ливедо, уртикарная сыпь [6].
Летучие артралгии (40-56%) - мигрирующие суставные боли, провоцируемые переохлаждением, при отсутствии рентгенологических изменений в структуре сустава даже после повторных атак [6]. Наблюдается преимущественное поражение суставов кистей и стоп.
Синдром Рейно (25-50%) - проявляется приступообразными спазмами в периферийных частях тела - чаще всего кистей рук [6].
Периферинеская полиневропатия (20-56%) - симметричное, сенсорной, сенсорно-моторной. Проявляется парестезиями, онемением и двигательными нарушениями нижних конечностях и/или множественных мононевритов [6]. Механизм невропатии при смешанной криоглобулинемии связывают с развитием эпиневрального васкулита (поражение vasa nervorum) и нарушением микроциркуляции из-за интраваскулярного отложения криоглобуинов, что ведет к ишемии, дегенерации аксонов и демиелинизации. Отмечается корреляция между клиническими проявлениями и степенью поражения vasa nervorum. Некротизирующий васкулит ассоциируется с наиболее тяжелыми формами полинейропатии. При смешанной криоглобулинемии могут встречаться и другие поражения нервной системы в виде энцефалопатию или зрительную невропатию, однако среди неврологических симптомов криоглобулинемия ведущее место занимает периферическая невропатия.
Криоглобулинемический гломерулонефрит (20-30%) - характеризует поздние стадии заболевания, морфологически - мезангиокапиллярный гломерулонефрит. В 50% случаев проявляется умеренно выраженная протеинурия, 25% - тяжелый острый нефритический синдром и 25% - нефротический синдром. Для всех вариантов характерна тяжелая артериальная гипертензия [15]. Исход: ХПН в 30 % случаев [6].
Также могут наблюдаться легочные васкулиты (0,7-12%). Считается, что нет органа или системы, которые не могли бы быть вовлечены в патологический процесс при смешанной криоглобулинемии.
Осложнения с участием HCV в качестве одного из этиологических факторов - насчитывается около десятка заболеваний в развитии которых принимает участие HCV.
Узелковый полиартериит (12%) - показано, что HCV-инфекция выявляется у 5-12% больных узелковым полиартериитом и является одним из этиологических факторов этого васкулита, основную роль в этиологии которого, как известно, играет HBV [13, 34]. Узелковый полиартериит - второй по частоте системный васкулит, встречающийся при HCV-инфекции. Нередко наблюдается сочетание узелкового полиартериита и криоглобулинемическим васкулитом [4].
В-клеточная неходжкинская лимфома (13%) - обобщение большого числа эпидемиологических исследований показало, что частота HCV-инфекции среди больных В-клеточной неходжкинской лимфомой (в среднем около 13%) превышает среднюю частоту HCV-инфекции в популяции (около 1,5%) и среди больных другими формами лимфопролиферативных заболеваний (около 3%) [4, 17, 18, 38]. Считают, что риск развития В-клеточной лимфомы у больных смешанной криоглобулинемией составляет до 10% [25].
Иммунная тромбоцитопения - наиболее частое поражение системы крови, наблюдающееся при HCV-инфекции. В отсутствие гиперспленизма и сниженной продукции тромбопоэтина основными ее механизмами являются аутоиммунный (связанный с продукцией антитромбоцитарных аутоантител) и непосредственный ингибирующий эффект вируса, реплицирующегося в клетках-предшественниках гемопоэза, на продукцию тромбоцитов в костном мозге [4, 28, 29]. В пользу наличия аутоиммунного механизма тромбоцитопении свидетельствуют также развитие тяжелой тромбоцитопении вследствие терапии ИФН-α и положительный эффект терапии кортикостероидами [4].
Синдром Шегрена - высокая частота заболевания при HCV инфекции связана с доказанным тропизмом вируса к слюнным железам [4, 25, 36, 38].
Развитие внепеченочных осложнений влияет на тактику лечения и эффективность противовирусной терапии HCV-инфекции. Оно преследует две цели: 1) элиминацию вируса, что достигается с помощью этиотропного лечения; 2) подавление продукции аутоантител, образования и отложения в сосудах иммунных комплексов, а также уменьшение воспалительной реакции с помощью иммуносупрессивной терапии, плазмафереза. Современная противовирусная терапия интерфероном-γ, обладающая иммуностимулирующими эффектами, способна вызвать усугубление внепеченочных осложнений. С другой стороны, патогенетическая терапия, эффективная при активных формах васкулитов и аутоиммунных синдромах, способствует репликации вируса. С учетом разнонаправленности действия обоих видов терапии в отношении вирусной инфекции одновременное их назначение оказывается малоэффективным [21, 31]. Трудности лечения обосновывают тактику возможно более раннего лечения гепатита, еще до развития внепеченочных осложнений. Бессимптомную криоглобулинемию у больных хроническим гепатитом С следует рассматривать как предвестник тяжелых внепеченочных поражений [3].
Доступность и широкое использование в клинической практике антиретровирусной терапии (АРВТ) для борьбы с вирусом иммунодефицита человека (ВИЧ) снизили частоту развития синдрома приобретенного иммунодефицита (СПИДа) и оппортунистических инфекций [1, 2, 3, 4]. Сдерживание этих заболеваний продлило жизнь ВИЧ-инфицированных, и они стали доживать до срока развития печеночной недостаточности в исходе хронического гепатита С (ХГС) [5, 6]. Есть сведения, что после внедрения АРВТ, смертность от болезней печени у ВИЧ-инфицированных увеличилась с 5-12% до 35-50% [7].
В Росийской Федерации по данным Федерального научно-методического центра по профилактике и борьбе со СПИДом в структуре летальных исходов среди больных ВИЧ-инфекцией терминальная стадия поражений печени в исходе хронических вирусных гепатитов до 2009 г. уже составляла существенную долю - 13,5-14,5%. В 2009 г. этот показатель вырос до 15,7%, хотя общая смертность среди ВИЧ-инфицированных снизилась с 3,4% (2008 г.) до 3% (2009 г.) [8].
Неблагоприятное течение гепатита С при наличии ВИЧ-инфекции, увеличение смертности от заболеваний печени, повышение риска гепатотоксического действия лекарственных препаратов - аргументы, указывающие на необходимость лечения гепатита С у больных ВИЧ-инфекцией [10, 11, 12].
Целью настоящего исследования явилось изучение эффективности противовирусной терапии (ПВТ) ХГС при моно- и коинфекции с ВИЧ.
Курс противовирусной терапии соответствовал рекомендуемым стандартам: при коинфекции ВИЧ/ХГС – 48 недель, независимо от генотипа вируса гепатита С (ВГС), при моноинфекции ХГС – 24-48 недель в зависимости от генотипа. У 5 (4,6%) больных коинфекцией ВИЧ/ХГС, в связи с поздней элиминацией РНК ВГС из сыворотки крови (к 24 неделе лечения), продолжительность терапии составила 72 недели. В исследование не были включены пациенты: ранее получавшие ПВТ, с микст-гепатитами, c серьезными хроническими сопутствующими заболеваниями, с компенсированным и декомпенсированным циррозом печени, принимающие алкоголь и наркотики, с уровнем СД4+ лимфоцитов менее 350 клеток/мкл.
Вирусологический мониторинг РНК ВГС методом полимеразной цепной реакции (ПЦР) проводился согласно рекомендациям Федерального научно-методического центра по профилактике и борьбе со СПИДом (2007 г.) на сроках 4 недели и в последующем каждые 12 недель. После завершения ПВТ больные обследовались в течение 2–х лет (1 раз в 6 месяцев). У всех больных коинфекцией определяли уровень CD4+лимфоцитов каждые 12/24 недели на протяжении курса наблюдения.
Высокую вирусную нагрузку РНК ВГС (более 2 млн. копий/мкл) имели 69 больных (63,3%) с коинфекцией ВИЧ/ХГС и 9 больных (36,0%) с моноинфекцией ХГС. Генотип 1 ВГС был обнаружен у 55 пациентов (50,5%) с коинфекцией и у 17 (68,0%) с моноинфекцией ХГС.
В соответствии с клинической классификацией ВИЧ-инфекции В.И. Покровского (2002г.) 48 больных (44,0%) коинфекцией ВИЧ/ХГС находились на субклинической стадии (3 стадия) ВИЧ-инфекции, 60 (55,0%) – на стадии 4А и 1 больной на стадии 4Б в фазах ремиссии. На момент начала противовирусной терапии 32 (29,4%) пациента получали антиретровирусную терапию.
Схемы АРВТ у 31 (96,9%) пациента включали бустированные ритонавиром ингибиторы протеазы (ИП): у 19 – лопинавир, у 6 – дарунавир, у 4-х – реатаз, по одному пациенту получали – телзир и саквинавир. Схему с ненуклеозидным ингибитором обратной транскриптазы (ННИОТ) – эфавирензом принимал один пациент (3,1%). Из нуклеозидных/нуклеотидных аналогов (НИОТ) пациенты получали ламивудин в сочетании с абакавиром - 90,6% (29 пациентов), либо с фосфазидом – 9,4% (3 пациента).
Статистическая обработка полученных результатов проводилась с помощью программного обеспечения Microsoft Excel и STATISTICA. При этом использовались параметрические методы оценки результатов – вычисление средней арифметической, среднеквадратического отклонения, средней ошибки средней арифметической. Оценка различий между сопоставляемыми группами по избранным критериям осуществлялась по критерию Стьюдента. Достоверность изменений признавалась при вероятности ошибки ρ меньшей или равной 0,05.
В группе больных моноинфекцией ХГС БВО наблюдался у 11 (44 %) больных: с 1-м генотипом у 5-ти (29,4%), с генотипом 2 и 3 – у 6-ти пациентов (75%). РВО был отмечен у 21 (84%) больного: с 1-м генотипом - у 13 (76,5%), с генотипом 2 и 3 – у 8 (100%) больных.
Из 109 коинфицированных ВИЧ/ХГС пациентов 63 (57,8%) человека прошли полный курс терапии. У 16 (14,7%) пациентов отсутствовал вирусологический ответа на фоне ПВТ, поэтому 11 человек из их завершили лечение в 24 недели, остальные 5 пациентов, в ввиду высокой приверженности, прошли 48–ми недельный курс. ПВТ была прекращена у 4 (3,7%) пациентов из-за вирусологического прорыва на сроках 24-36 недель и у 6 (5,5%) - из-за осложнений на сроках 22-47 недель. Отказались от продолжения лечения на сроках 33-38 недель 20 (19,2%) пациентов (все имели отрицательные результаты ПЦР-детекции РНК-ВГС на момент завершения ПВТ). Из них 17 пациентов сохранили устойчивый вирусологический ответ (УВО), у 3-х - через 6 месяцев после лечения наблюдался рецидив заболевания.
В группе больных ХГС моноинфекцией полный курс прошел 21(84,0%) пациент. Из 4-х пациентов (16,0%), у которых не снижалась вирусная нагрузка до 24 недель ПВТ, 2 - завершили лечение в 24 недели; 2 - продолжили курс до 48 недель.
Таким образом, завершили лечение с получением непосредственного вирусологического ответа 89 пациентов (81,7%) с коинфекцией ВИЧ/ХГС и 21 пациент (84,0%) с моноинфекцией ХГС. Не получен вирусологический ответ у 20 пациентов (18,3%) с ВИЧ/ХГС и у 4 (16,0%) - с моноинфекцией ХГС. Все пациенты, не ответившие на терапию, были инфицированы генотипом 1 ВГС.
В ходе исследования выявлено, что частота УВО у больных ВИЧ/ХГС коинфекцией составила 67,0%/73: с генотипом 1 – у 43,6%/24, с генотипом 2 и 3 – у 90,7%/49. Среди больных с моноинфекцией ХГС частота УВО составила 76,0%/19: с генотипом 1 – у 64,7%/11, с генотипом 2 и 3 в 100% случаев (n=8).
Рецидив заболевания (через 6 месяцев после окончания терапии) возник у 16 (14,7%) пациентов с ВИЧ/ХГС (с генотипом 1 – 11 человек и генотипом 2,3 – 5 человек) и у 2 (8,0%) с моноинфекцией (с 1 генотипом).
Таким образом, БВО у больных инфицированных ВГС генотипом 2, 3 прогнозировал более высокий процент УВО как при ко-, так и при моноинфекции. При генотипе 1 ВГС в обеих группах была низкая частота БВО – 23,6% и 29,4% соответственно, и частота УВО в этих группах была ниже. Лучший результат в достижении УВО при генотипе 1 наблюдался у больных моноинфекцией - 64,7% относительно 43,6% больных при коинфекции.
Как известно, при составлении прогноза эффективности лечения ХГС, традиционно, учитываются следующие факторы: возраст, стаж инфицирования ВГС и наличие фиброза, генотип ВГС и уровень вирусной нагрузки, а так же наличие быстрого клиренса РНК ВГС в ответ на ПВТ (БВО) [13, 14, 15]. Мы проанализировали данные критерии при сравнении групп больных в зависимости от достижения УВО. У больных коинфекцией дополнительно рассматривались показатели по ВИЧ-инфекции: уровень СД4+ лимфоцитов и прием антиретровирусных препаратов (табл. 1).
На рис. 1 представлены результаты по достижению УВО в зависимости от генотипа ВГС и проведения АРВТ.
Таблица 1. Сравнительная характеристика больных ВИЧ/ХГС в зависимости от достижения УВО (%).


Рис. 1. Устойчивый вирусологический ответ в зависимости от генотипа у пациентов, получавших и не получавших АРВТ: *р

Рис. 2. Динамика активности АлАТ у больных коинфекцией ВИЧ/ХГС в зависимости от результата УВО (ЕД/л)
Как известно, ПЕГ-ИФН и рибавирину свойственны разнообразные нежелательные явления. Нами проводился сравнительный анализ частоты выявления нежелательных явлений у пациентов с ВИЧ/ХГС коинфекцией и ХГС моноинфекцией. Выявлено, что нежелательные явления в обеих группах были однотипными и не отличались от ранее описанных в литературе [21, 23-25]. Кроме того, нами было замечено, что характер и выраженность нежелательных явлений зависят от сроков проведения ПВТ. Гриппоподобный синдром (подъем температуры до фебрильных цифр, озноб, головная боль, миалгия, артралгия) наблюдался на 1-2–й неделе лечения у 75,2% больных с ВИЧ/ХГС коинфекцией и был более выражен у больных ХГС моноинфекцией - 92% (р<0,02). В последующем температурная реакция снижалась, но начинали нарастать астенический синдром (слабость, недомогание, повышенная утомляемость, снижение работоспособности), чаще наблюдавшийся у больных коинфекцией - 89% против 60% больных с моноинфекцией, и диспепсический синдром (тошнота, сухость во рту, снижение аппетита).
На 4-12 неделе ПВТ в обеих группах регистрировались кожный зуд, сухость, гиперемия в местах инъекций. На 12-24-й неделе лечения отмечались усиление выпадения волос у 52 (47,7%) больных ВИЧ/ХГС и 11 (44,0%) - в группе ХГС и нейропсихические расстройства (раздражительность, снижение памяти и внимания, плаксивость, беспокойство, бессонница, апатия, плохое настроение) - у 47,7% больных ВИЧ/ХГС коинфекцией и 40% - ХГС. Коррекция депрессивных состояний осуществлялась при активном участии психиатра и психолога, в редких случаях назначались антидепрессанты. По литературным данным около 20% больных не доводят лечение до конца из-за непереносимости побочных реакций [26]. В нашем исследовании 18,3% больных ВИЧ/ХГС коинфекцией досрочно прекратили терапию на сроке 33-38 недель. Однако, несмотря на укорочение курса лечения, большинство из них - 85% имели УВО.
Как известно, терапия α-интерфероном и рибавирином часто вызывает гематологические нарушения. Среди наблюдаемых нами пациентов – 51,5 % имели снижение гематологических показателей (анемия, тромбоцитопения, нейтропения). Отмены противовирусной терапии не было ни в одном случае, что позволило закончить терапию с УВО у 37,6% больных с ВИЧ/ХГС коинфекцией и у 32% больных ХГС.
Нами проанализирован уровень СД4+ лимфоцитов у больных ВИЧ/ХГС коинфекцией во время проведения ПВТ в зависимости от наличия УВО (рис. 3).
Как видно из рис. 3, ни на одном этапе наблюдения нами не выявлено достоверных различий между исследуемыми группами.
В обеих группах в ходе терапии происходило снижение абсолютного количества СД4+ лимфоцитов: число больных с уровнем ниже 350 клеток/мкл составило 40,4%/44. Из них больше половины - 68,2%/30 достигли УВО. Среди 65 пациентов, у которых на фоне лечения уровень СД4+ сохранялся выше 350 клеток/мкл частота УВО составила 63,1%/41 (р>0,65).

Рис. 3. Динамика уровня СД4 лимфоцитов в зависимости от результата УВО на разных этапах ПВТ (кл/мкл)
Несмотря на то, что снижение СД4-лимфоцитов у большинства не сопровождалось развитием клинической симптоматики вторичных заболеваний, у 6 (5,5%) пациентов терапия была прекращена в связи с развитием осложнений (табл. 2). У всех был получен УВО: 4 пациента с 1 генотипом, 3 – с 3 генотипом.
Таким образом, укорочение курса ПВТ даже при наличии осложнений, явившихся причиной ее отмены, не повлияло на эффективность ПВТ.
Таблица 2. Осложнения на фоне ПВТ у больных ВИЧ/ХГС коинфекцией (n=6)

В группе больных моноинфекцией осложнений не наблюдалось.
Заключение
1. Противовирусная терапия ВГС-инфекции показывает высокую эффективность в плане достижения УВО у больных коинфекцией ВИЧ/ХГС преимущественно при генотипах 2,3 вируса.
2. Частота нежелательных явлений при проведении ПВТ у больных коинфекцией ВИЧ/ХГС не является критерием отмены лечения.
3. Сочетание антиретровирусной и противовирусной терапии ХГС снижает частоту УВО у больных коинфекцией преимущественно с 1 генотипом ВГС.
4. Снижение уровня СД4+ лимфоцитов на фоне проведения ПВТ не влияет на частоту УВО.
Список использованных источников:
1. Блохина Н.П. Клинические аспекты гепатита С у ВИЧ-инфицированных// Вирусные гепатиты: достижения и перспективы. Информ.- 2001.- № 2 (12). – С. 3-7.
2. Покровский В.В. и др. ВИЧ-инфекция и СПИД. - М.: ГЭОТАР-Медиа, 2010. - 192 с.
3. Murphy E., Collier A., Kalish L. et al. Highly active antiretroviral therapy decreases mortality and morbidity in patients with advanced HIV disease// Ann Intern Med. – 2001.- Vol. 135. – Р. 17–26.
4. Kakinami L., Block R.C., Adams M.J. et al. Risk of cardiovascular disease in HIV, hepatitis C, or HIV/hepatitis C patients compared to the general population// Int J Clin Pract. – 2013. - Vol. 67(1). – Р. 6-13.
5. Хоффман К., Рокштро Ю.К. Лечение ВИЧ-инфекции 2009.- М.: Р.Валент. - 2010.- С. 476-486.
6. George S., Gebhardt J., Klinzman D. et al. Hepatitis C viremia in HIV-infected individuals with negative ВГС antibody tests//J. Acquir Immun Defic Syndr. – 2002. - Vol. 31. – Р. 154–162.
7. Scott J., Kitahata M., van Rompaey S. et al. Hepatitis C virus co-infection is associated with higher risk of death due to HIV and liver-related diasease among an HIV-infected cohort// Program and abstracts of the 13th Conference on retroviruses and opportunistic infections; Febr. 5-8, 2006; Denver, Colorado.- Denver. - 2006. - Abstract 865.
8. Голиусов А.Т., Дементьева Л.А. Эпидемическая ситуация по ВИЧ-инфекции в Российской Федерации в 2009 г.// Журн. микробиол.- 2010. - №6. - С.31-34.
9. Бобкова М.Р., Самохвалов Е.И., Кравченко А.В. и др. Генетические варианты вируса гепатита С у ВИЧ-инфицированных наркоманов// Вопр. вирусол. - 2002. - Т. 47, №3.- С. 15-20.
10. Soriano V., Barreiro P. and Nunez M. Management of chronic hepatitis B and C in HIV-coinfected patients// Journal of Antimicrobial Chemotherapy.- 2006.- Vol. 57. – Р. 815–818.
11. Bambha K., Pierce C., Cox C. et al. Assessing mortality in women with hepatitis C virus and HIV using indirect markers of fibrosis// AIDS. – 2012. - Vol. 26(5). – Р. 599-607.
12. Bani-Sadr F., Krastinova E., Fromentin D. et al. Severe transaminitis after interferon-ribavirin therapy in HIV/ВГС-coinfected patients: influence of a sustained ВГС response// J Viral Hepat. – 2012. - Vol. 19(6). – Р. 431-435.
13. Лопаткина Т.Н. Возможности противовирусной терапии хронического гепатита С у больных, злоупотребляющих алкоголем// Гепатологический форум. - 2005. - №4. - С. 28.
14. Еналеева Д.Ш., Фазылов В.Х., Созинов А.С. Хронические вирусные гепатиты В и С. Что нужно знать о болезни? – М.: МЕДпресс-Информ, 2003. - 144 с.
15. Kenneth E Sherman et al. Sustained long-term antiviral maintenance therapy in ВГС/HIV сoinfected рatients (SLAM-C)// J. Acquir Immune Defic Syndr. – 2010. - Vol. 55(5). – Р. 597–605.
16. Solmone M., Girardi E., Lalle E. et al.. Evolution of HVR-1 quasispecies after 1-year treatment in HIV/ВГС-coinfected patients according to the pattern of response to highly active antiretroviral therapy// Antivir Ther. – 2006. - Vol. 11(1). – Р. 87-94.
17. Abbate I., Lo Iacono O., Di Stefano R. et al. J. HVR-1 quasispecies modifications occur early and are correlated to initial but not sustained response in ВГС-infected patients treated with pegylated- or standard-interferon and ribavirin// Hepatol. – 2004. - Vol. 40(5). – Р. 831-836.
18. Poizot-Martin I., Marimoutou C., Benhaim S. et al. Efficacy and tolerance of ВГС treatment in HIV-ВГС coinfected patients: the potential interaction of PI treatment// HIV Clin. Trials. – 2003. – Vol. 4(4). – Р. 262-268.
19. Кравченко А.В., Канестри В.Г., Ганкина Н.Ю. и др. Усиленные ритонавиром нгибиторы протеазы ВИЧ в составе схем первой линии АРВТ// Эпидемиология и инфекционные болезни, 2010.- №3.- С.22-27.
20. Poordad F.F., Flamm S.L. Virological relapse in chronic hepatitis C// Antivir Ther. - 2009. - Vol.14(3). – Р. 303-313.
21. Soriano V., Vispo E., Labarga P. et al. Uptate on HIV and ВГС coinfection// Hot Topics Viral Hep. – 2010. - Vol. 6(17). – Р. 17-22.
22. Канестри В.Г., Кравченко А.В. Особенности вирусного гепатита у больных ВИЧ-инфекцией.// Медицинская помощь. - 2001. - № 2. - С. 21-24.
23. Максимов С.Л. Клиническое течение, исходы и лечение вирусных гепатитов у больных ВИЧ-инфекцией: Автореф. дис. … д-ра мед. наук. – М., 2010. - 46 с.
24. Ивашкин В.Т. Диагностика, лечение и ведение пациентов с гепатитом С// Клин. микробиол. антимикроб. химиотер.- 2006, т. 8, №2. – С. 102-129.
25. Soriano V., Barreiro P. and Nunez M. Management of chronic hepatitis B and C in HIV-coinfected patients// Journal of Antimicrobial Chemotherapy.- 2006.- Vol. 57. – Р. 815–818.
26. Апросина З.Г., Игнатова Т.М., Козловская Л.В. Хронический вирусный гепатит/ Под ред. В.В. Серова, З.Г. Апросиной. - М.: Медицина, 2004.- 384 с.
Подписано в печать: 02.07.2013
Что такое гепатит Б? Причины возникновения, диагностику и методы лечения разберем в статье доктора Александрова Павла Андреевича, инфекциониста со стажем в 14 лет.
Над статьей доктора Александрова Павла Андреевича работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Вирусный гепатит В (Б) — острое и хроническое инфекционное заболевание, вызываемое вирусом гепатита В, с гемоконтактным механизмом передачи (через кровь), протекающее в различных клинико-морфологических вариантах, и возможным развитием цирроза печени и гепатоцеллюлярной карциномы. Всего в мире, по самым скромных оценкам, инфицировано более 250 млн человек.
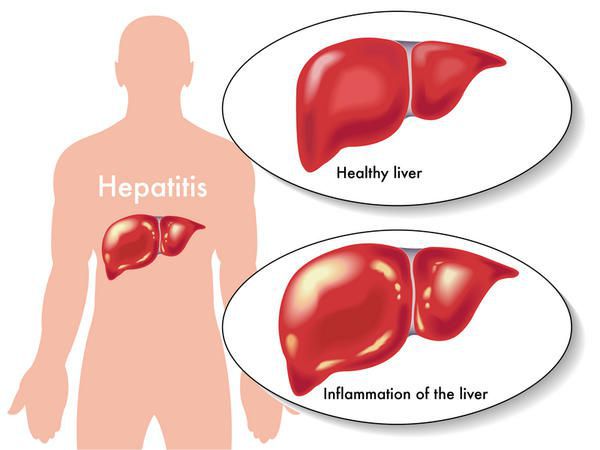
Этиология
вид — вирус гепатита В (частица Дейна)
Развитие вируса гепатита Б происходит в гепатоцитах (железистых клетках печени). Он способен к интеграции в ДНК человека. Имеются 9 генотипов вируса с различными подтипами — генетическая изменчивость позволяет вирусу образовывать мутантные формы и ускользать от действия лекарств.
Имеет ряд собственных антигенов:
- поверхностный HbsAg (австралийский). Появляется за 15-30 дней до развития болезни, свидетельствует об инфицировании (не всегда). Антитела к HbsAg выявляются через 2-5 месяцев от начала заболевания, а сам HbsAg исчезает из крови (при благоприятном течении процесса);
- сердцевинный HbcorAg (ядерный, коровский). Появляется в инкубационном периоде и совместно с ним появляются антитела (HbcorAb). Длительное присутствие HbcorAg в крови свидетельствует о вероятной хронизации процесса (неадекватный иммунный ответ);
- антиген инфекциозности и активного размножения вируса (HbeAg). Появляется совместно с HbsAg и отражает степень инфицированности. Его продолжительная циркуляция в крови является свидетельством развития хронизации процесса, а антитела к нему являются благоприятным прогностическим признаком (не всегда, но по меньшей мере указывают на возможность более благоприятного процесса, срок их циркуляции после выздоровления окончательно не определён, но не более пяти лет после благоприятного разрешения процесса);
- HbxAg — регулятор транскрипции, способствует развитию гепатокарциномы.
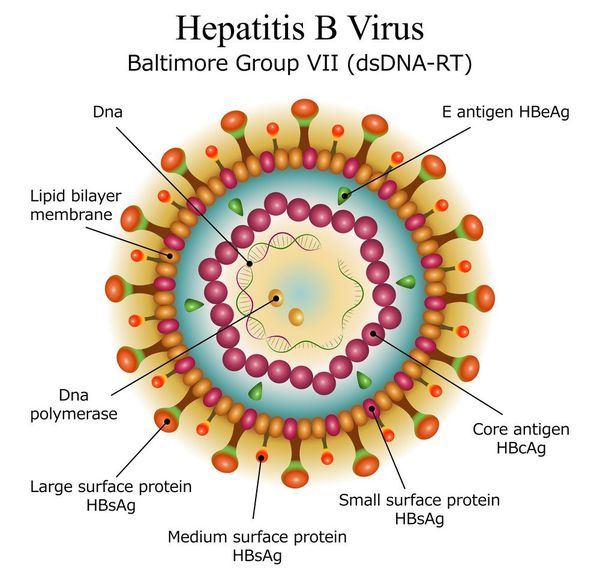
Вирус гепатита В чрезвычайно устойчив к действию всевозможных естественных факторов окружающей среды, инактивируется при 60 °C за 10 часов, при 100 °C за 10 минут, при оптимальной температуре сохраняется до 6 месяцев, при автоклавировании погибает за 5 минут, в сухожаровом шкафу — через 2 часа, 2% раствор хлорамина убивает вирус за 2 часа. [1] [3]
Эпидемиология
Источник инфекции — только человек, больной острой или хронической формой инфекции.
Механизм передачи: гемоконтактный и вертикальный (от матери к ребёнку), не исключается трансмиссивный механизм передачи (например, при укусах комаров в результате раздавливания и втирания инфицированного тела комара в поврежденную ткань человека).
Пути передачи: половой, контактно-бытовой, гемотрансфузионный (например, при переливании крови или медицинских манипуляциях). Восприимчивость всеобщая. Заболеваемость — 30-100 человек на 100 тысяч населения (зависит от страны). Летальность от острых форм — до 2%. После перенесённого острого заболевания при условии выздоровления иммунитет стойкий, пожизненный.
Для заражения характерна малая заражающая доза (невидимые следы крови). [1] [2]
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы гепатита Б
Инкубационный период гепатита В длится от 42 до 180 дней (следует иметь в виду, что наличие клинической симптоматики характеризует лишь незначительную долю всех случаев заболевания).
Начало постепенное. Характерные синдромы:
- общей инфекционной интоксикации (проявляется как астеноневротический синдром);
- холестатический (нарушение секреции желчи);
- артрита;
- нарушения пигментного обмена (появление желтухи при уровне общего билирубина свыше 40 ммоль/л);
- геморрагический (кровоточивость кровеносных сосудов);
- экзантемы;
- отёчно-асцитический (скопление жидкости в брюшной полости);
- гепатолиенальный (увеличение печени и селезёнки).
При первых признаках гепатита B нужно обратиться к доктору.
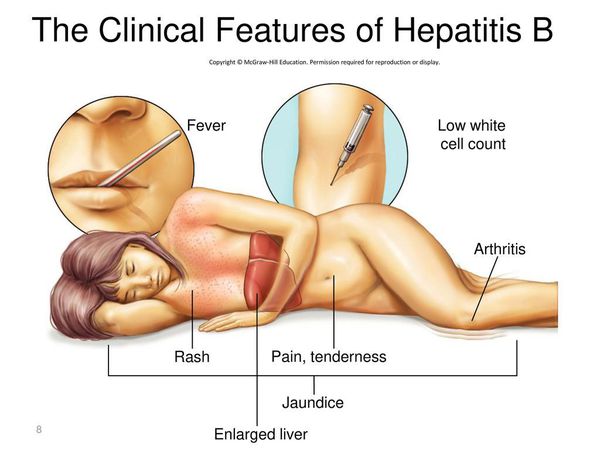
Первые признаки гепатита B
Начальный (преджелтушный) период продолжается 7-14 дней. Чаще протекает по многообразному типу с болевыми ощущениями в различных суставах по ночам и утром, уртикарными высыпаниями, астеновегетативными проявлениями (снижение аппетита, апатия, нервозность, слабость, разбитость, повышенная утомляемость). Изредка развивается синдром Джанотти-Крости — симметричная, яркая пятнисто-папулёзная сыпь. Не исключены умеренные диспептические явления (расстройства пищеварения). К концу периода происходит потемнение мочи, обесцвечивание кала.
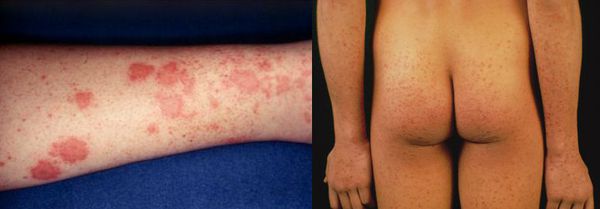
Желтушный период
Этот период продолжительностью около одного месяца характеризуется возникновением желтушного окрашивания кожи (различных оттенков) на фоне продолжающегося или ухудшающегося общего состояния. Характерна длительность и стойкость симптоматики. Появляется тяжесть и болезненность в правом подреберье, горечь во рту, тошнота, выражённый зуд кожи (практически не снимаемый никакими средствами). На фоне усиления астеноневротического компонента появляются геморрагические проявления, урежение пульса, гипотензия, отёки (отражает степень интоксикации и нарушения функций печени).
Выздоровление
Следующим этапом в развитии болезни является нормализации общего состояния, спадение желтухи и реконвалесценция, которая в зависимости от конкретной ситуации и состояния иммунной системы может закончиться как выздоровлением, так и движением развития заболевания в хроническое течение, характеризующееся маловыраженой неусточивой симптоматикой, преимущественно в виде слабости, периодического дискомфорта в правом подреберье, бурно сигнализирующим лишь на стадии цирроза и полиорганных осложнений.
- гепатиты другой этиологии;
- желтухи другой этиологии (например, гемолитическая болезнь, токсическое поражение, опухоли);
- малярия; ;
- лептоспироз;
- ревматоидный артрит.
Гепатит В у беременных
Острый гепатит характеризуется более тяжёлым течением у беременной, возникновении повышенного риска преждевременных родов, аномалий развития плода на ранних сроках и кровотечений. Вероятность передачи при острой форме зависит от сроков беременности: в первом триместре риск 10% (но более тяжёлые проявления), в третьем триместре — до 75% (чаще бессимптомное течение после родов). У большинства детей при заражении во внутриутробном и постнатальном периодах происходит хронизация инфекции. [1] [3] [6]
Патогенез гепатита Б
С движением кровяной массы вирус попадает в печеночную ткань, где локализуется в гепатоцитах и теряет свою протеиновую сферу в лизосомах. Происходит выход вирусной ДНК с последующим ресинтезом аномальных протеинов LSP, а параллельно образование новых частиц Дейна.
В процессе эволюции вирусчеловеческого взаимодействия возможно развитие двух вариантов:
При репликативном пути происходит следующее: белки LSP совместно с HbcorAg вызывают увеличение продукции гамма-интерферона, что приводит к активации главного комплекса гисотсовместимости (HLA), проистекает преобразование молекул гистосовместимости 1 и 2 классов, в результате чего клетка становиться для организма враждебной в антигенном формате.
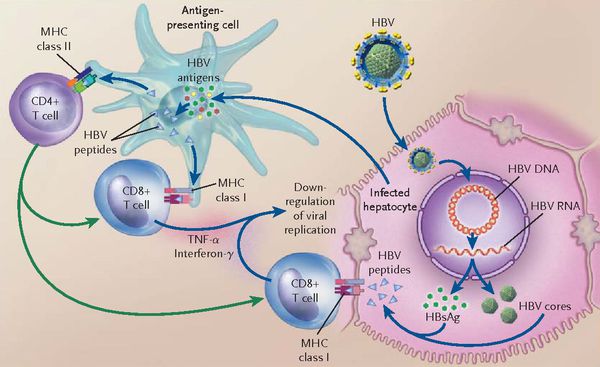
Антигенпрезентирующие макрофаги содействуют изменению В-лимфоцитов в плазматические клетки и экспрессии ими агрессивных белков-антител к посторонним антигенам. В итоге на поверхности печёночных клеток формируются вирусспецифические иммунные комплексы (антиген + антитело + фракция комплемента С3в).
В динамике может реализоваться два сценария:
- в первом варианте запуск каскада комплимента ведёт к появлению в составе иммунных комплексов агрессивной фракции С9 (мембранатакующий комплекс) — наблюдается значительный некроз гепатоцитов без участия лимфоцитов (молниеносная форма гепатита В);
- при альтернативной варианте (наблюдающимся в большинстве случаев) каскад комплемента в силу иммуноиндивидуалистических свойств не активируется — тогда идёт умеренное разрушение Т-киллерами меченых антителами заражённых вирусом гепатоцитов. Образуются ступенчатые некрозы с образованием на месте гибели гепатоцитов соединительной ткани — рубцов (то есть острый гепатит В при плохом иммунном ответе постепенно переходит в хронический).
Непременным атрибутом патогенеза является формирование иммунопатологического процесса. Гибель гепатоцитов, инфицированных вирусом гепатита В, следует за счёт иммунокомпетентных частиц, Т-киллеров и макрофагальных элементов.
Серьёзным значением является нарушение свойств мембраны клеток печени, что сопровождается экскрецией (выделением) лизосомальных ферментов, разрушающих гепатоциты. Сообразно этому, гибель гепатоцитов происходит за счёт иммунокомпетентных клеток, лизосомальных ферментов и противопечёночных гуморальных аутоантител, то есть острая болезнь наступает (и благоприятно заканчивается) только при хорошем иммунитете, а при плохом идёт хронизация.
При тяжёлом цитолитическом синдроме (массивные некрозы гепатоцитов) возникает гипокалиемический алкалоз, острая печёночная недостаточность, печёночная энцефалопатия (ПЭП), церебротоксическое действие, нарушение функции обмена нервной ткани. [2] [3] [6]
Классификация и стадии развития гепатита Б
По цикличности течения:
- острый;
- острый затяжной;
- хронический.
По клиническим проявлениям:
- субклинический (инаппарантный);
- клинически выраженный (желтушный, безжелтушный, холестатический, фульминантный).
По фазам хронического процесса:
Группы риска хронического гепатита B
Хроническим гепатитом чаще страдают дети младше шести лет. При заражении в первый год жизни он развивается в 80–90 % случаев, от года до шести лет — в 30–50 %, у взрослых без сопутствующих заболеваний — менее чем в 5 %. [7]
Осложнения гепатита Б
Чем опасен гепатит Б
Заболевание может привести к острой печёночной недостаточности (синдрому острой печеночной энцефалопатии).
Выделяют четыре стадии болезни:
Диагностика гепатита Б
Многообразие форм, тесная взаимосвязь с иммунной системой человека и зачастую достаточно высокая стоимость исследований часто затрудняют принятие конкретного решения и диагноза в стационарный отрезок времени, поэтому во избежание роковых (для больного) ошибок следует подходить к диагностике с учётом всех получаемых данных в динамическом наблюдении:
- общеклинический анализ крови с лейкоцитарной формулой (лейкопения, лимфо- и моноцитоз, уменьшение СОЭ, тромбоцитопения);
- общий анализ мочи (появление уробилина);
- биохимический анализ крови (гипербилирубинемия в основном за счёт связанной фракции, повышение уровня АЛТ и АСТ, ГГТП, холестерина, щелочной фосфатазы, снижение протромбинового индекса, фибриногена, положительная тимоловая проба);
- маркеры гепатита В: HbsAg, HbeAg, HbcorAg, HbcorAb IgM и суммарные, HbeAb, anti-Hbs, ПЦР в качественном и количественном измерении);
- УЗИ органов брюшной полости, КТ и МРТ диагностика;
- фиброскан (применяется для оценки степени фиброза). [3][4]
Скрининг при хроническом гепатите
Пациентам с хроническим гепатитом В рекомендуется не реже чем раз в полгода проходить обследование: УЗИ органов брюшной полости, клинический анализ крови, АЛТ, АСТ, тест на альфа-фетопротеин. Скрининг позволяет вовремя заметить обострение болезни и начать специфическую терапию.
Лечение гепатита Б
Лечение острых форм гепатита В должно осуществляться в стационаре (учитывая возможность быстрых и тяжёлых форм болезни), хронических — с учётом проявлений.
Диета и режим при гепатите В
В острый период показан постельный режим, печёночная диета (№ 5 по Певзнеру): достаточное количество жидкости, исключение алкоголя, жирной, жареной, острой пищи, всё в мягком и жидком виде.
Медикаментозная терапия
При лёгкой и средней тяжести острого гепатита этиотропная противовирусная терапия (ПВТ) не показана. При тяжёлой степени и риске развития осложнений назначается специфическая противовирусная терапия на весь период лечения и возможно более длительное время.
В лечении хронических форм гепатита показаниями к назначению ПВТ является наличие уровня DNA HBV более 2000 МЕ/мл (при циррозе печении независимо от уровня), умеренное и высокое повышение АЛТ/АСТ и степени фиброза печёночной ткани не менее F2 по шкале METAVIR, высокая вирусная нагрузка у беременных женщин. В каждом конкретном случае показания определяются индивидуально, в зависимости от выраженности процесса, временной тенденции, пола, планирования беременности и другого.
Существует два пути противовирусного лечения:
- терапия пегилированными интерферонами (имеет ряд существенных противопоказаний и серьёзных побочных эффектов — не менее 12 месяцев);
- нуклеозидно-аналоговой терапии NA (используются препараты с высоким порогом резистентности вируса, длительно — не менее пяти лет, удобство применения, хорошая переносимость).
В отдельных случаях может рассматриваться применение комбинированной терапии.
Из средств патогенетической терапии в острый период используются внутривенно вводимые растворы 5% глюкозы, дезинтоксикантов, антиоксидантов и витамины. Показан приём энтеросорбентов, ферментных препаратов, при выраженном холестазе применяются препараты Урсодезоксихолевой кислоты, при тяжёлом течении — глюкокортикостероиды, методы аппаратного плазмофереза.
В хронической стадии заболевания при наличии соответствующей активности процесса и невозможности назначения ПВТ может быть показан приём групп гепатопротекторов и антиоксидантов. [1] [3]
Прогноз. Профилактика
Основное направление профилактики на сегодняшний день — это проведение профилактической вакцинации против гепатита В в младенческом возрасте (в том числе усиленная вакцинация детей, рождённых от матерей с гепатитом В) и далее периодические ревакцинации раз в 10 лет (или индивидуально по результатам обследования). Достоверно показано, что в странах, где была введена вакцинация, резко сократилось количество вновь выявленных случаев острого гепатита В.
Вторая составляющая стратегии профилактики включает обеспечение безопасности крови и её компонентов, использование одноразового или стерилизованного инструментария, ограничение числа половых партнёров и использование барьерной контрацепции. [1] [2]
Хронический гепатит С – заболевание печени, вызванное вирусом гепатита С, длительностью 6 и более месяцев. В 10 – 40% случаев хронический гепатит С прогрессирует до цирроза печени, а в 5% случаев до гепатоцеллюлярной карциномы (чаще у пациентов с циррозом или выраженным фиброзом).
Пользователи протокола: гастроэнтерологи, инфекционисты, терапевты, врачи общей практики, а также врачи смежных специальностей, осуществляющие ведение и лечение пациентов с гепатитом С на разных стадиях заболевания.
Методология: Протокол разработан на основе Клинических руководств ведущих международных сообществ (EASL, AASLD, CASL, SASL, FASL, EACS, РОПИП) и адаптирован с учетом используемых на территории Казахстана методов диагностики и лечения. Классификация рекомендаций, использованная в данном протоколе, представлена в Таблице 1.
Таблица 1. Классификация рекомендаций
Классификация
Клиническая классификация
Общепринятой классификации ХГС не существует. При постановке диагноза необходимо указывать вирусологический статус (генотип и вирусную нагрузку), активность (биохимическую и/или гистологическую), а также стадию заболевания (по данным непрямой эластографии или морфологического исследования).
Диагностика
II. МЕТОДЫ, ПОДХОДЫ И ПРОЦЕДУРЫ ДИАГНОСТИКИ И ЛЕЧЕНИЯ
Перечень основных и дополнительных диагностических мероприятий
(+) исследования необходимые для пациентов с ЦП
Хронический гепатит С протекает бессимптомно или малосимптомно и может сопровождаться такими неспецифичными симптомами как:
• Депрессия (оценивается у всех пациентов с использованием шкалы Бека)
• сахарный диабет 2 типа
При сборе анамнеза следует учитывать указания на гемотрансфузии, трансплантацию органов и тканей, небезопасные инвазивные (немедицинские) манипуляции, принадлежность в группам риска (потребители наркотиков, лица с беспорядочными половыми связями, пациенты, находящиеся на хроническом гемодиализе, пациенты с онкогематологическими заболеваниями, лица, живущие с ВИЧ и другими парентеральными инфекциями, сексуальные партнеры лиц с ВГС, медицинские работники, дети, рожденные от HCV-инфицированных матерей, лица с измененными функциональными пробами печени). Лицам с указанными факторами риска необходим профилактический скрининг на наличие ВГС (anti-HCV).
При физикальном обследовании на начальной стадии ХГС патологии не выявляется, за исключением незначительной гепатомегалии. По мере прогрессирования заболевания может отмечаться увеличение и уплотнение печени. Спленомегалия и другие стигмы хронического заболевания печени могут проявляться на более поздних стадиях.
Вирусный гепатит С преимущественно протекает бессимптомно. При переходе хронического гепатита С в цирроз в 6,4% случаев отмечаются симптомы, обусловленные дисфункцией печени и портальной гипертензией:
В ряде случаев ВГС выявляется у пациентов с ГЦК, которая, как правило, протекает бессимптомно, кроме случаев запущенной стадии, когда опухоль достигает значительных размеров, вызывая ухудшение функции печени (желтуха, асцит, печеночная энцефалопатия), боли в верхнем правом квадранте, астенизацию и потерю веса.
ОАК с подсчетом тромбоцитов. Могут быть выявлены анемия (в результате гиперспленизма, кровотечений из ВРВ), лейкопения, тромбоцитопения (в результате гиперспленизма и прямого миелодепрессивного влияния ВГС), ускорение СОЭ (при инфекционных осложнениях).
Биохимический профиль включает определение показателей АЛТ, АСТ, ГГТП, альбумина, билирубина, щелочной фосфатазы, МНО или ПВ, а также рутинных (глюкозы, креатинина, холестерина) и некоторых специфических показателей, таких как, гамма-глобулины, IgG (скрининг аутоиммунного гепатита), сывороточное железо и ферритин (скрининг гемохроматоза и вторичной перегрузки железом), церулоплазмин (скрининг болезни Вильсона-Коновалова), АФП (скрининг ГЦК). Активность АЛТ и АСТ может быть минимальной ( < ВГН), слабовыраженной (< 5 ВГН), умеренной (5-10 ВГН), выраженной (>10 ВГН) и не всегда коррелирует с гистологической активностью. Уровень билирубина при ХГС, как правило, нормальный. Его увеличение может наблюдаться при остром гепатите или свидетельствовать об ухудшении деятельности печени на поздней стадии заболевания, что также сопровождается снижением уровня альбумина и увеличением МНО или ПВ. Показатели щелочной фосфатазы и ГГТП могут увеличиваться при остром гепатите и оставаться на уровне нормы при хроническом гепатите.
В план клинического лабораторного обследования включаются также ОАМ, копрограмма.
- anti-HCV, маркеры других парентеральных инфекций таких как ВГВ (HBsAg, HBeAg, anti-HBs, anti-HBe, anti-HBc total/IgM), ВГD (anti-HDV у носителей HBsAg), ВИЧ (anti-HIV), а также (при подозрении на острый гепатит) ВГА (anti-HAV) и ВГЕ (anti-HEV)
Качественное определение HCV RNA с помощью высокочувствительной ПЦР в режиме реального времени с нижним лимитом определения 15 МЕ/мл на автоматических анализаторах закрытого типа.
• В случае подозрения на острый ВГС или у иммуносупрессивных пациентов необходимо определение HCV RNA (рекомендация А1)
• Если тест на anti-HCV положительный, необходимо определить HCV RNA, чувствительным молекулярным методом (рекомендация А1)
• Пациенты с положительным тестом anti-HCV и отрицательным молекулярным тестом на HCV RNA должны быть протестированы на HCV RNA через 3 месяца для подтверждения элиминации вируса (рекомендация А1).
− ИФА (+) в 50% в момент острых проявлений, поэтому ПЦР при подозрении на ОГС проводится во всех, в том числе, ИФА (–) случаях
Количественное определение HCV RNA с помощью высокочувствительной ПЦР в режиме реального времени с нижним лимитом определения 15 МЕ/мл на автоматических анализаторах закрытого типа, а также определение генотипа ВГС.
В настоящий момент известно 6 различных типов вируса, которые обозначаются цифрами от 1 до 6. Также существует подтипы, обозначаемые буквами (например, подтип 1а и 1b). На территории РК преимущественно распространенны генотипы 1b, 2 и 3.
Функциональные пробы щитовидной железы (ТТГ)
Тест на беременность
Определение полиморфизма гена интерлейкина – 28В. Результат анализа полиморфизма в гене ИЛ28В полезен в прогнозе эффективности лечения и принятии решения о выборе режима терапии у пациентов с ВГС 1 генотипа. 1
Инструментальные исследования
Радиологическое исследование
Радиологическое исследование печени (в первую очередь УЗИ) позволяет идентифицировать признаки стеатоза, выраженного фиброза и перехода в цирроз печени (закругление контуров печени, неравномерность поверхности и крупнозернистость паренхимы печени), признаки портальной гипертензии и тромбоза (увеличение диаметра, кавернозная трансформация, наличие тромбов воротной и селезеночной вен, асцит, спленомегалия), а также наличие объемных образований (ГЦК). Могут использоваться и другие визуализирующие технологии (КТ, МРТ).
Эндоскопическое исследование
При прогрессировании хронического гепатита С в цирроз диагностика портальной гипертензии может, помимо прочих методов, осуществляться путем эндоскопического обследования, позволяющего выявить варикозное расширение вен (пищевода и желудка) и портальную гастропатию.
Оценка тяжести заболевания печени должна проводиться до ПВТ. Выявление пациентов с циррозом печени имеет особое значение, так как эффективность ПВТ обратно пропорциональна стадии фиброза. Отсутствие выраженного фиброза имеет значение при принятии решения о времени начала ПВТ. Пациенты с явными клиническими признаками цирроза не нуждаются в биопсии печени для оценки стадии фиброза. Пациенты с признаками цирроза печени должны быть обследованы на ГЦК. Выраженный фиброз может быть у пациентов с нормальной активностью АЛТ, поэтому оценка степени тяжести заболевания должна проводиться независимо от показателей АЛТ. Пункционная биопсия остается эталонным методом оценки стадии фиброза печени. Риск тяжелых осложнений при биопсии очень низок (от 1/4000 до 1/10000). У пациентов с нарушением свертываемости крови можно использовать трансюгулярную биопсию печени с одновременной оценкой давления в портальной вене. При ХГС альтернативные, неинвазивные методы (непрямая эластография и биомаркеры) могут быть использованы вместо биопсии. Непрямая эластография может быть использована для оценки стадии фиброза печени у пациентов с ХГС, но необходимо учитывать факторы, которые могут повлиять на достоверность результатов, например выраженная активность заболевания, ожирение. Оба метода (непрямая эластография и биомаркеры) точны при оценке цирроза и нулевого фиброза, но менее точны при промежуточных стадиях фиброза. Комбинирование биомаркеров и непрямой эластографии повышает точность оценки стадии фиброза и уменьшает необходимость в проведении ункционной биопсии. В случае противоречивых результатов биомаркеров и непрямой эластографии, можно использовать пункционную биопсию печени. Гистологическая оценка также необходима при смешанной этиологии (например, ВГС с ВГВ, метаболическим синдромом, алкоголизмом или аутоиммунными заболеваниями).
Пункционная биопсия печени (ПБП) – относительно безопасный метод оценки морфологических изменений печени у пациентов с ХГС. ПБП позволяет оценить выраженность фибротического процесса и некровоспалительных изменений. Результаты ПБП легко интерпретируются и поддаются полуколичественной оценке. ПБП проводится в динамике с целью оценки прогрессирования поражения печени при ХГС. ПБП – единственный доступный метод, позволяющий оценить вклад сопутствующих заболеваний (стеатогепатит, гемохроматоз, аутоиммунный гепатит и т.д.) в патологическом процессе и их влияние на течение и эффективность лечения ХГС. Необходимо помнить, что ПБП имеет ряд ограничений. В частности, имеет значение опыт врача, проводящего пункцию, и морфолога, оценивающего морфологические изменения; малый объем образцов ткани печени; инвазивность и дискомфорт для пациентов; риск развития осложнений. ПБП требует строгого выполнения правил ее выполнения в условиях специализированных отделений и наличия квалифицированных морфологов.
2. Всем пациентам перед выполнением биопсии печени должно быть выполнено УЗИ ОБП. Данное исследование позволяет выявить анатомический вариант строения печени и наличие очаговых образований в ее паренхиме, что может потребовать проведения прицельной биопсии под визуальным контролем.
3. В течение недели перед проведением пункции необходимо определить количество тромбоцитов и протромбиновое время (ПВ), либо протромбиновый индекс (ПИ)
• Если количество тромбоцитов ≥90 000 /мм3, то манипуляцию можно выполнять рутинным способом (чрескожная биопсия печени)
• Если ПВ удлинено менее чем на 3 сек. в сравнении с контрольным значением (предоставляется лабораторией, в которой выполняется исследование образца крови), ПИ не менее 70%, тромбиновое время (ТВ) и активированное частичное тромбопластиновое время (АЧТВ) не превышают 1,5 нормы, биопсию можно проводить чрескожным доступом
• Во всех других случаях решение о выполнении биопсии печени принимается на индивидуальной основе путем оценки пользы и риска от планируемой манипуляции. В случае строгой необходимости в проведении биопсии печени у пациентов с гипокоагуляцией или низким количеством тромбоцитов в некоторых случаях может быть оправдана заместительная терапия
4. Перед биопсией необходимо подписать у пациента информированное согласие, в котором доступно описана методика манипуляции и возможные осложнения.
5. Во время выполнения биопсии врач и пациент должны быть в постоянном контакте. Больной четко и своевременно должен выполнять команды врача. При повышенной возбудимости пациента и отсутствии признаков печеночной недостаточности возможно назначение седативных препаратов.
6. Выбор иглы для биопсии целесообразно осуществлять с учетом личного опыта оператора. В повседневной практике удобны в применении иглы Менгини и иглы типа Tru-cut.
7. Врачи, личный опыт которых не превышает 20 манипуляций, выполняют биопсию в присутствии и под контролем более опытного доктора в условиях специализированного гепатологического центра.
9. Активное наблюдение пациентов в течение 8 часов и первой ночи после манипуляции должно проводиться в условиях медицинской организации. Оценка результатов ПБП проводится с применением полуколичественных шкал описания степени некро-воспалительных изменений и стадии фиброза ткани печени (см. Таблицы 3 и 4).
Таблица 3. Морфологическая диагностика степени некровоспалительной активности гепатита
*Для определения стадии заболевания печени чаще применяется шкала METAVIR
К преимуществам метода относятся:
• Неинвазивность
• Воспроизводимость
• Больший чем при биопсии оцениваемый объем ткани печени (в 100-200 раз больше)
• Быстрота и удобство применения (обследование занимает в среднем 5 мин)
• Немедленный результат
• Оценка эффективности терапии
• Возможность обследования детей
• Высокой биохимической активности (АЛТ/АСТ выше верхнего лимита нормы в 3 и более раз)
• Не менее 60% успешных измерений.
Таблица 5. Интерпретация результатов непрямой эластографии
Читайте также:

