Основными звеньями патогенеза чумы являются
Обновлено: 24.04.2024
Чума - острая, особо опасная зоонозная трансмиссивная инфекция с тяжёлой интоксикацией и серозно-геморрагическим воспалением в лимфатических узлах, лёгких и других органах, а также возможным развитием сепсиса.
Что провоцирует / Причины Чумы:
Возбудитель - грамотрицательная неподвижная факультативно-анаэробная бактерия Y. pestis рода Yersinia семейства Enterobacteriaceae. По многим морфологическим и биохимическим признакам чумная палочка сходна с возбудителями псевдотуберкулёза, иерсиниоза, туляремии и пастереллёза, вызывающих тяжёлые заболевания как у грызунов, так и у людей. Отличается выраженным полиморфизмом, наиболее типичны овоидные палочки, окрашивающиеся биполярно, Выделяют несколько подвидов возбудителя, различных по вирулентности. Растёт на обычных питательных средах с добавлением гемолизированной крови или сульфита натрия для стимуляции роста. Содержит более 30 антигенов, экзо- и эндотоксины. Капсулы защищают бактерии от поглощения полиморфноядерными лейкоцитами, а V- и W-антигены предохраняют их от лизиса в цитоплазме фагоцитов, что обеспечивает их внутриклеточное размножение. Возбудитель чумы хорошо сохраняется в экскретах больных и объектах внешней среды (в гное бубона сохраняется 20-30 дней, в трупах людей, верблюдов, грызунов - до 60 дней), но высокочувствителен к солнечным лучам, атмосферному кислороду, повышенной температуре, реакции среды (особенно кислой), химическим веществам (в том числе дезинфектантам). Под действием сулемы в разведении 1:1000 гибнет через 1-2 мин. Хорошо переносит низкие температуры, замораживание.
Больной человек может в определённых условиях стать источником инфекции: при развитии лёгочной чумы, непосредственном контакте с гнойным содержимым чумного бубона, а также в результате заражения блох на больном с чумной септицемией. Трупы умерших от чумы людей часто являются непосредственной причиной инфицирования окружающих. Особую опасность представляют больные лёгочной формой чумы.
Возможны контактный (через повреждённую кожу и слизистые оболочки) при разделке туш и обработке шкур убитых заражённых животных (зайцы, лисы, сайгаки, верблюды и др.) и алиментарный (при употреблении в пищу их мяса) пути заражения чумой.
Естественная восприимчивость людей очень высокая, абсолютная во всех возрастных группах и при любом пути заражения. После перенесённого заболевания развивается относительный иммунитет, не предохраняющий от повторного заражения. Повторные случаи заболевания не являются редкостью и протекают не менее тяжело, чем первичные.
Патогенез (что происходит?) во время Чумы:
Адаптационные механизмы человека практически не приспособлены сопротивляться внедрению и развитию чумной палочки в организме. Это объясняется тем, что чумная палочка очень быстро размножается; бактерии в большом количестве вырабатывают факторы проницаемости (нейраминидаза, фибринолизин, пестицин), антифагины, подавляющие фагоцитоз (F1, HMWPs, V/W-Ar, РН6-Аг), что способствует быстрому и массивному лимфогенному и гематогенному диссеминированию прежде всего в органы мононуклеарно-фагоцитарной системы с её последующей активизацией. Массивная антигенемия, выброс медиаторов воспаления, в том числе и шокогенных цитокинов, ведёт к развитию микроциркуляторных нарушений, ДВС-синдрома с последующим исходом в инфекционно-токсический шок.
Клиническая картина заболевания во многом определяется местом внедрения возбудителя, проникающего через кожные покровы, лёгкие или ЖКТ.
Схема патогенеза чумы включает три стадии. Сначала возбудитель от места внедрения лимфогенно диссеминирует в лимфатические узлы, где кратковременно задерживается. При этом образуется чумной бубон с развитием воспалительных, геморрагических и некротических изменений в лимфатических узлах. Затем довольно быстро бактерии проникают в кровь. В стадии бактериемии развивается сильнейший токсикоз с изменениями реологических свойств крови, нарушениями микроциркуляции и геморрагическими проявлениями в различных органах. И, наконец, после преодоления возбудителем ретикулогистиоцитарного барьера происходит его диссеминирование по различным органам и системам с развитием сепсиса.
Микроциркуляторные нарушения вызывают изменения в сердечной мышце и сосудах, а также в надпочечниках, что обусловливает острую сердечно-сосудистую недостаточность.
При аэрогенном пути заражения поражаются альвеолы, в них развивается воспалительный процесс с элементами некроза. Последующая бактериемия сопровождается интенсивным токсикозом и развитием септико-геморрагических проявлений в различных органах и тканях.
Антительный ответ при чуме слабый и формируется в поздние сроки заболевания.
Симптомы Чумы:
Инкубационный период составляет 3-6 сут (при эпидемиях или септических формах сокращается до 1-2 дней); максимальный срок инкубации - 9 дней.
Данная симптоматика проявляется, особенно в начальный период, при всех формах чумы.
Согласно клинической классификации чумы, предложенной Г.П. Рудневым (1970), выделяют локальные формы заболевания (кожную, бубонную, кожно-бубонную), генерализованные формы (первично-септическую и вторично-септическую), внешнедиссеминированные формы (первично-лёгочную, вторично-лёгочную и кишечную).
Кожная форма. Характерно образование карбункула в месте внедрения возбудителя. Первоначально на коже возникает резко болезненная пустула с тёмнокрасным содержимым; она локализуется на отёчной подкожной клетчатке и окружена зоной инфильтрации и гиперемии. После вскрытия пустулы образуется язва с желтоватым дном, склонная к увеличению в размерах. В дальнейшем дно язвы покрывает чёрный струп, после отторжения которого образуются рубцы.
Бубонная форма. Наиболее частая форма чумы. Характерно поражение лимфатических узлов, регионарных по отношению к месту внедрения возбудителя - паховых, реже подмышечных и очень редко шейных. Обычно бубоны бывают одиночными, реже множественными. На фоне выраженной интоксикации возникают боли в области будущей локализации бубона. Через 1-2 дня можно пропальпировать резко болезненные лимфатические узлы, сначала твёрдой консистенции, а затем размягчающиеся и становящиеся тестообразными. Узлы сливаются в единый конгломерат, малоподвижный из-за наличия периаденита, флюктуирующий при пальпации. Длительность разгара заболевания около недели, после чего наступает периодреконвалесценции. Лимфатические узлы могут самостоятельно рассасываться или изъязвляться и склерозироваться вследствие серозно-геморрагического воспаления и некроза.
Кожно-бубонная форма. Представляет сочетание кожных поражений и изменений со стороны лимфатических узлов.
Эти локальные формы заболевания могут переходить во вторичный чумной сепсис и вторичную пневмонию. Их клиническая характеристика не отличается от первично-септической и первично-лёгочной форм чумы соответственно.
Первично-септическая форма. Возникает после короткого инкубационного периода в 1-2 дня и характеризуется молниеносным развитием интоксикации, геморрагическими проявлениями (кровоизлияния в кожу и слизистые оболочки, желудочно-кишечные и почечные кровотечения), быстрым формированием клинической картины инфекционно-токсического шока. Без лечения в 100% случаев заканчивается летально.
Первично-лёгочная форма. Развивается при аэрогенном заражении. Инкубационный период короткий, от нескольких часов до 2 сут. Заболевание начинается остро с проявлений интоксикационного синдрома, характерного для чумы. На 2-3-й день болезни появляется сильный кашель, возникают резкие боли в грудной клетке, одышка. Кашель сопровождается выделением сначала стекловидной, а затем жидкой пенистой кровянистой мокроты. Физикальные данные со стороны лёгких скудные, на рентгенограмме обнаруживают признаки очаговой или долевой пневмонии. Нарастает сердечно-сосудистая недостаточность, выражающаяся в тахикардии и прогрессивном падении артериального давления, развитии цианоза. В терминальную стадию у больных развивается сначала сопорозное состояние, сопровождающееся усилением одышки и геморрагическими проявлениями в виде петехий или обширных кровоизлияний, а затем кома.
Кишечная форма. На фоне синдрома интоксикации у больных возникают резкие боли в животе, многократная рвота и диарея с тенезмами и обильным слизисто-кровянистым стулом. Поскольку кишечные проявления можно наблюдать и при других формах заболевания, до последнего времени остаётся спорным вопрос о существовании кишечной чумы как самостоятельной формы, по-видимому, связанной с энтеральным заражением.
Дифференциальная диагностика
Кожную, бубонную и кожно-бубонную формы чумы следует отличать от туляремии, карбункулов, различных лимфаденопатий, лёгочные и септические формы - от воспалительных заболеваний лёгких и сепсиса, в том числе менингококковой этиологии.
Для кожной, бубонной и кожно-бубонной форм чумы характерна резкая болезненность в месте поражения, стадийность в развитии карбункула (пустула - язва - чёрный струп - рубец), выраженные явления периаденита при формировании чумного бубона.
Лёгочные и септические формы отличают молниеносное развитие тяжёлой интоксикации, выраженных проявлений геморрагического синдрома, инфекционно-токсического шока. При поражении лёгких отмечают резкие боли в груди и сильный кашель, отделение стекловидной, а затем жидкой пенистой кровянистой мокроты. Скудные физикальные данные не соответствуют общему крайне тяжёлому состоянию.
Диагностика Чумы:
Лабораторная диагностика
Основана на использовании микробиологических, иммуносерологических, биологических и генетических методов. В гемограмме отмечают лейкоцитоз, нейтрофилию со сдвигом влево, увеличение СОЭ. Выделение возбудителя проводят в специализированных режимных лабораториях для работы с возбудителями особо опасных инфекций. Исследования проводят для подтверждения клинически выраженных случаев заболевания, а также для обследования лиц с повышенной температурой тела, находящихся в очаге инфекции. Бактериологическому исследованию подвергают материал от больных и умерших: пунктаты из бубонов и карбункулов, отделяемое язв, мокроту и слизь из ротоглотки, кровь. Проводят пассаж на лабораторных животных (морские свинки, белые мыши), погибающих на 5-7-е сутки после заражения.
Из серологических методов применяют РНГА, РНАТ, РНАГ и РТПГА, ИФА.
Положительные результаты ПЦР через 5-6 ч после её постановки свидетельствуют о наличии специфической ДНК чумного микроба и подтверждают предварительный диагноз. Окончательным подтверждением чумной этиологии болезни являются выделение чистой культуры возбудителя и её идентификация.
Лечение Чумы:
Больных чумой лечат только в стационарных условиях. Выбор препаратов для этиотропной терапии, их доз и схем применения определяет форма заболевания. Курс этиотропной терапии при всех формах болезни составляет 7-10 дней. При этом применяют:
• при кожной форме - котримоксазол по 4 таблетки в сутки;
• при бубонной форме - левомицетин в дозе 80 мг/кг/сут и одновременно стрептомицин в дозе 50 мг/кг/сут; препараты вводят внутривенно; эффективен также тетрациклин;
• при лёгочных и септических формах заболевания комбинацию левомицети-на со стрептомицином дополняют назначением доксициклина в дозе 0,3 г/сут или тетрациклина по 4-6 г/сут внутрь.
Одновременно проводят массивную дезинтоксикационную терапию (свежезамороженная плазма, альбумин, реополиглюкин, гемодез, кристаллоидные растворы внутривенно, методы экстракорпоральной детоксикации), назначают препараты для улучшения микроциркуляции и репарации (трентал в сочетании с солкосерилом, пикамилон), форсирования диуреза, а также сердечные гликозиды, сосудистые и дыхательные аналептики, жаропонижающие и симптоматические средства.
Успех лечения зависит от своевременности проведения терапии. Этиотропные препараты назначают при первом подозрении на чуму, основываясь на клинико-эпидемиологических данных.
Профилактика Чумы:
Эпидемиологический надзор
Объём, характер и направленность профилактических мероприятий определяет прогноз эпизоотической и эпидемической обстановки по чуме в конкретных природных очагах с учётом данных слежения за движением заболеваемости во всех странах мира. Все страны обязаны сообщать ВОЗ о появлении заболеваний чумой, движении заболеваемости, эпизоотиях среди грызунов и мерах борьбы с инфекцией. В стране разработана и функционирует система паспортизации природных очагов чумы, позволившая провести эпидемиологическое районирование территории.
Профилактические мероприятия
В комплексе мер профилактики и борьбы с чумой решающая роль принадлежит мероприятиям, исключающим завоз инфекции из других стран и предупреждающим возникновение заболеваний в энзоотических очагах. Для профилактики завоза чумы из других стран большое значение имеет строгое соблюдение всеми странами международных санитарных правил. В энзоотических очагах противочумные мероприятия включают наблюдение за видовым составом и численностью грызунов, исследование грызунов и их эктопаразитов на инфицированность чумной палочкой. При выявлении эпизоотии проводят дератизацию и дезинсекционные мероприятия в том или ином объёме. Синантропных грызунов истребляют без выявления среди них больных чумой, если их численность превышает 15% попадаемости в ловушки. Грызунов и эктопаразитов в поле и вокруг населённых пунктов уничтожают противочумные учреждения, а в населённых пунктах - дератизационно-дезинсекционные отделы Центров санитарно-эпидемиологического надзора.
Показаниями к проведению профилактической иммунизации населения являются эпизоотия чумы среди грызунов, выявление больных чумой домашних животных и возможность завоза инфекции больным человеком. В зависимости от эпидемической обстановки вакцинация проводится на строго определённой территории всему населению (поголовно) и выборочно особо угрожаемым контингентам - лицам, имеющим постоянную или временную связь с территориями, где наблюдается эпизоотия (животноводы, агрономы, охотники, заготовители, геологи, археологи и т.д.). Все лечебно-профилактические учреждения должны иметь на случай выявления больного чумой определённый запас медикаментов и средств личной защиты и профилактики, а также схему оповещения персонала и передачи информации по вертикали. Меры по предупреждению заражения людей чумой в энзоотичных районах, лиц, работающих с возбудителями особо опасных инфекций, а также предупреждение выноса инфекции за пределы очагов в другие районы страны осуществляют противочумные и другие учреждения здравоохранения.
Мероприятия в эпидемическом очаге
При появлении больного чумой или подозрительного на эту инфекцию принимают срочные меры для локализации и ликвидации очага. Границы территории, на которой вводят те или иные ограничительные мероприятия (карантин), определяют исходя из конкретной эпидемиологической и эпизоотологической обстановки, возможных действующих факторов передачи инфекции, санитарно-гигиенических условий, интенсивности миграции населения и транспортных связей с другими территориями. Общее руководство всеми мероприятиями в очаге чумы осуществляет Чрезвычайная противоэпидемическая комиссия. При этом строго соблюдают противоэпидемический режим с использованием противочумных костюмов. Карантин вводят решением Чрезвычайной противоэпидемической комиссии, охватывая им всю территорию очага.
Больных чумой и пациентов с подозрением на это заболевание госпитализируют в специально организованные госпитали. Транспортировка больного чумой должна осуществляться в соответствии с действующими санитарными правилами по биологической безопасности. Больных с бубонной чумой размещают по несколько человек в палате, больных лёгочной формой - только в отдельные палаты. Выписывают больных при бубонной форме чумы не ранее 4 нед, при лёгочной - не ранее 6 нед со дня клинического выздоровления и отрицательных результатов бактериологического исследования. После выписки переболевшего из стационара за ним устанавливают медицинское наблюдение в течение 3 мес.
В очаге проводят текущую и заключительную дезинфекцию. Лица, соприкасавшиеся с больными чумой, трупами, заражёнными вещами, участвовавшие в вынужденном забое больного животного и т.д., подлежат изоляции и медицинскому наблюдению (6 дней). При лёгочной чуме проводят индивидуальную изоляцию (в течение 6 дней) и профилактику антибиотиками (стрептомицин, рифампицин и др.) всем лицам, которые могли инфицироваться.
К каким докторам следует обращаться если у Вас Чума:
Вас что-то беспокоит? Вы хотите узнать более детальную информацию о Чумы, ее причинах, симптомах, методах лечения и профилактики, ходе течения болезни и соблюдении диеты после нее? Или же Вам необходим осмотр? Вы можете записаться на прием к доктору .
Клиника и признаки чумы. Варианты и формы течения чумы
Инкубационный период 3-6 дней, может быть короче. Болезнь начинается остро, иногда внезапно, с сильного озноба, сменяющегося жаром, быстрым подъемом температуры до 40°С. Больные жалуются на сильную головную боль, головокружение, резкую слабость, тошноту, иногда появляется рвота, боль в мышцах. Состояние многих возбужденное, больные говорливы, излишне подвижны, суетливы, возможны бред и галлюцинации. Иногда, напротив, апатичны. Кожные покровы лица гиперемированы, оно одутловатое, глаза инъецированы, походка шатающаяся, речь невнятная, что бывало причиной диагностических ошибок, когда больных чумой в начальной стадии принимали за опьяневшего.
Клиническое течение чумы отличается разнообразием форм. Помимо общетоксического синдрома, вскоре на первый план выходят те или иные ее проявления. Общепринятой классификацией чумы является предложенная Г.П. Рудневым, большим знатоком этой инфекции. Он рассматривает клинику чумы с патогенетических и эпидемиологических позиций, что важно для практики ведения больных чумой и проведения противоэпидемических мероприятий.

Чумной бубон
Различают локальные формы-кожную, кожно-бубонную, бубонную и генерализованные: внутренне диссеминированные (первично-септическая) и внешне диссеминированные (первично-легочная, вторично-легочная, кишечная).
При кожной форме чумы местные изменения проходят стадии пятна, папулы, везикулы, пустулы, язвы. Язва отличается болезненностью, медленным заживлением с образованием рубца.
Характерным признаком бубонной формы является резко болезненный, увеличенный лимфоузел. Наиболее часто при чуме увеличиваются паховые, подмышечные и шейные лимфоузлы; они болезненны, локальная боль появляется в месте будущего бубона гораздо раньше, чем сам бубон. Над бубоном появляется отечность, увеличенные лимфоузлы сливаются в единый конгломерат, резко болезненный. Изменения окраски кожи, приобретающей красный лоснящийся цвет, появляются позднее самого бубона. Бубоны раньше, как правило, самостоятельно вскрывались с образованием втянутого рубца или склерозировались.
При современном лечении они могут рассасываться. В прошлом летальность даже при бубонной форме чумы достигала 40-90%. В настоящее время при антибиотикотерапии все больные выздоравливают.
Первично-септическая форма чумы встречается редко (1-3% случаев). Изменений на коже при этой форме болезни не наблюдается. Болезнь сразу приобретает картину остроразвивающегося сепсиса с быстрым нарастанием токсикоза, возможным появлением менингоэн-цефалита, развитием ТГС и скоротечным течением (1-3 дня). Заканчивается летальным исходом при явлениях ИТШ и комы.
Вторично-септическая форма чумы - следствие бубонной формы, которая быстро переходит в сепсис с прогрессирующей бактериемией и интоксикацией. Для нее характерны вторичные очаги инфекции с выраженными проявлениями геморрагической септицемии. Эта форма отличается большой тяжестью течения и частыми летальными исходами.
Клиника вторичной легочной чумы напоминает описанную картину поражения легких при первичной легочной чуме с той разницей, что ей предшествует развитие прогрессирующей бубонной формы, когда возникает гематогенная генерализация инфекции.
Группа геморрагических лихорадок включает острые лихорадочные заболевания вирусной этиологии, в патогенезе и клинических проявлениях которых ведущую роль играет поражение сосудов, приводящее к развитию тромбогеморрагического синдрома.
Впервые в качестве самостоятельной нозологической формы геморрагическую лихорадку (геморрагический нефрозонефрит) описал в 1941 г. А. В. Чурилов (профессор кафедры инфекционных болезней Военно-медицинской академии). В последующие годы был описан целый ряд геморрагических лихорадок в различных странах мира. В группу геморрагических лихорадок были включены некоторые болезни, которые были описаны раньше (денге, желтая лихорадка).
Что провоцирует / Причины Геморрагических лихорадок:
Возбудители геморрагических лихорадок относятся к 4 семействам вирусов: тогавирусы, буньявирусы, аренавирусы и филовирусы, общим свойством которых является высокий тропизм к эндотелию сосудов.
Геморрагические лихорадки - природноочаговые инфекции, при которых основным резервуаром и источниками болезни являются различные виды животных, а переносчиками при значительной части из них - членистоногие (клещи, комары). В остальных случаях передача инфекции реализуется другими путями - воздушно-пылевым, алиментарным, водным, при зоонозном контакте, парентерально. В соответствии с особенностями передачи возбудителя болезни выделяют: клещевые (Крымская-Конго, Омская и Кьясанурского леса), комариные (желтая лихорадка, Денге лихорадка, лихорадка Чикунгунья и лихорадка долины Рифт) и контагиозные геморрагические лихорадки (геморрагическая лихорадка с почечным синдромом, лихорадки Лаоса, Аргентинская, Боливийская, Венесуэльская, Бразильская, Марбурга и Эбола). Хотя восприимчивость к этим инфекциям довольно высока, наиболее часто заболевания регистрируют среди лиц, имеющих профессиональный контакт с животным и или объектами дикой природы. В городах геморрагической лихорадкой с почечным синдромом в основном заболевают работники бытового хозяйства и лица без определенного места жительства, имеющие контакт с синантропными грызунами или их выделениями.
Патогенез (что происходит?) во время Геморрагических лихорадок:
Патогенез геморрагических состояний при геморрагических лихорадках. Тромбогеморрагический синдром (синдром Мачабели) является важным звеном патогенеза многих инфекционных болезней. Тромбогеморрагический синдром - это симптомокомплекс, обусловленный универсальным и неспецифическим свойством крови, лимфы, тканевой жидкости, клеточных и межклеточных структур обратимо и необратимо сгущаться вследствие активации их способности к коагуляции и в результате ретракции расслаиваться на компоненты различного агрегатного состояния. Тромбогеморрагический синдром в своем развитии проходит 4 стадии.
Стадия гиперкоагуляции начинается в клетках тканей поврежденного органа, что приводит к высвобождению коагуляционно-активных веществ, реакция активации коагуляции распространяется на кровь. Эта стадия обычно кратковременная.
Стадия нарастающей коагулопатии потребления, непостоянной фибриполитической активности. Она характеризуется падением числа тромбоцитов и уровня фибриногена, а также расходом других плазменных факторов коагуляционнолитической системы организма. Это - стадия начинающегося и нарастающего ДВС (неполный синдром ДВС).
Стадия дефибриногенации и тотального, но не постоянного фибринолиза (дефибриногенационно-фибринолитическая). Синоним этой стадии - полный синдром ДВС.
Восстановительная стадия или стадия остаточных тромбозов и окклюзии. При благоприятном течении синдрома отмечается возвращение к физиологическим нормам всех факторов коагуляционнолитической системы организма.
По клиническим проявлениям различают различные формы тромбогеморрагического синдрома (молниеносный, острый, хронический, латентный, геморрагический, гиперергический и др.). Тромбогеморрагический синдром наблюдается при травмах, хирургических заболеваниях, в онкологии, при акушерской патологии, при сепсисе и многих инфекционных болезнях. В настоящей главе мы рассматриваем только особенности патогенеза геморрагического синдрома при геморрагических лихорадках.
При геморрагических лихорадках первичная патология страдания развивается на клеточно-молекулярном уровне с обязательным вовлечением в инфекционный процесс эндотелиальных клеток кровеносной системы и стволовых полипотентных клеток костного мозга. Скорость развития процесса обусловлена агрессивностью патогена и его тропностью и к другим чувствительным клеткам, например, макрофагам-моноцитам, а также степенью зрелости иммунной системы пораженного конкретным возбудителем индивидуума. В итоге нормальный физиологический уровень функционирования эндотелия и кроветворных органов динамически меняется. В разгар инфекции происходит тотальное изменение анатомо-морфологической целостности и, соответственно, функций системы микроциркуляции крови. Оно сопровождается ухудшением трофики всех органов и тканей, развивается гипоксия и их функциональная недостаточность. Процесс сопровождается нарушением деятельности терморегулирующего и координирующего центров ЦНС, сердечно-сосудистой и выделительной систем, развивается легочная или иная органная патология и нередко больные погибают в коматозном состоянии. Угрожающая жизни объемная потеря крови редка, хотя повышенная кровоточивость, как признак изменения сосудистой проницаемости, выступает в качестве одного из ведущих симптомов геморрагических вирусных лихорадок.
Среди причин геморрагического синдрома, развивающегося достаточно быстро и часто заканчивающегося смертью больных, известны вирусы пяти семейств: Arena-, Bunya-, Filo-, Flavi- и Togaviridae. Они включают вирусы Ласса, Хунин, Мачупо, Гуанарито, Сэбия (семейство аренавиру-сов) - возбудители, соответственно, лихорадок Ласса, Аргентинской, Боливийской, Венесуэльской и Бразильской; лихорадки долины рифт и Крым Конго (семейство буньявирусов); желтой лихорадки (семейство флавивирусов); лихорадок Марбург и Эбола (семейство филовирусов), лихорадки денге, къясанурской лесной болезни и геморрагической лихорадки с почечным синдромом (семейства тогавирусов). Возбудители клещевых риккетсиозов, эрлихиозов и группы сыпного тифа, напротив, причастны к геморрагическому синдрому с более медленным и большей частью доброкачественным течением. Следовательно, по привязанности к возбудителю инфекционной болезни геморрагический синдром полиэтиологичен.
Широкий спектр возбудителей, вызывающих единый по клинике комплекс симптомов, обусловлен однотипным механизмом его формирования. Из данных морфологического и иммуногистологического изучения вышеуказанных заболеваний известно, что основная патология развертывается в эндотелиальных клетках микродиркуляторной системы, клетках костного мозга и для некоторых инфекций (лихорадки Марбург, денге) в процесс вовлекаются мононуклеарные фагоциты, как циркулирующие в русле крови, так и тканевые. Это находит отражение в клеточном, белковом и пептидном (кинины, лейкотриены) составе крови и балансе ее биологически активных компонентов. Затрагивается деятельность систем комплемента, кининовой, коагуляции и антикоагуляции. Последние регулируют тонус сосудов, их проницаемость, секреторную деятельность эндотелия, реологические свойства крови и ответственны за субъективные ощущения боли, усталости и другую симптоматику болезней.
Несмотря на этиологическое разнообразие патогенов, ассоциируемых с развитием геморрагического синдрома, их объединяет идентичный или весьма близкий механизм доставки возбудителя к клеткам-мишеням на начальной стадии инфекционного процесса. Возбудители лихорадок, передающиеся с участием кровососущих переносчиков, контактно через расчесы кожи или аэрогенно через альвеолярно-капиллярные мембраны легких, по существу механически переносятся к чувствительным к патогену клеткам эндотелия и тканевым оседлым макрофагам в местах микротравм, вызванных колюще-сосущим аппаратом переносчиков или повреждением эпителия. Именно в этих точках или же в альвеолярно-капиллярных мембранах, на которых произошла задержка частиц инфекционного аэрозоля, формируется первичный локальный процесс. Защитная реакция у места входных ворот сопровождается и одновременной генерализацией инфекционного процесса вследствие диссеминации возбудителя с крово-лимфооттоком с дальнейшим последовательно нарастающим поражением клеток-мишеней в органах и тканях, удаленных от места входных ворот инфекции. При этом часть частичек возбудителя поглощается макрофагами и другими клетками крови, например, эритроцитами при риккетсиозах и бартонеллезах, но не инактивируется вследствие недостаточной концентрации цитокинов, таких как интерферонгамма (ИНФ-у), фактора некроза опухоли-альфа (ФНО-а), других монокинов и отсутствия специфических нейтрализующих антител в плазме крови на момент заражения и в начальный период болезни.
Локальное повреждение физиологически высокоактивных, регулирующих гемостаз клеток в области входных ворот патогена и одновременная генерализация инфекции с трансмиссивным механизмом передачи предопределены особенностями кровососания клещей и комаров, переносчиков возбудителей большинства геморрагических лихорадок, и особенностями анатомического строения тканевых и альвеолярных капилляров. Синхронность формирования локального и генерализованного процессов объясняется тем, что кровососание у переносчиков длится долго и прерывисто, особенно у клещей (до нескольких суток). Периодический отсос крови сопровождается периодическим же вспрыскиванием в капилляр слюны, а в некоторых случаях и коксальной жидкости, содержащих патоген, антикоагулянты и ферменты кровососа.
Инфекционный процесс на уровне клетка-возбудитель начинается по обычной для внутриклеточных паразитов схеме: прикрепление к поверхностной мембране и ее разрыхление, проникновение в цитоплазму, размножение или гибель (в случае абортивной инфекции), выход в окружающее межклеточное пространство или русло крови, с инфицированием прилегающих и отдаленных интактных клеток. Последняя стадия взаимодействия клетка-патоген сопровождается либо разрушением и некролизом первой, либо усилением внутриклеточных физиологических процессов с повышенной продукцией цитокинов и других метаболитов их нормального функционирования.
Дальнейшая прогрессирующая структурно-функциональная дезорганизация эндотелия, герминтативных точек стволовых клеток костного мозга и других (при желтой лихорадке и лихорадке Марбург - гепатоцитов и мононуклеарных фагоцитов) приводит к нарастанию капилляропатии и, соответственно, токсикоза, вплоть до развития инфекционно-токсической энцефалопатии (ИТЭ) с полной утратой сознания и восприятия окружающей среды, т.е. развивается состояние комы (синоним, ИТЭ III-й степени. Динамически колеблется уровень цитокинов и медиаторов, причастных к пирогенезу (ПГЕз, ИЛ-1, лейкотриены), коагуляции - антикоагуляции, начинает снижаться синтез колониестимулирующих факторов (КСФ). Уменьшение КСФ сопровождается подавлением процесса самообновления полипотентных стволовых клеток; направление дифференциации клеток крови, в частности нейтрофилов, и их созревание меняются.
Необычное против физиологической нормы содержание продуктов распада клеток, затронутых патогеном, и усиление синтеза и секреции эйкозаноидов на начальной стадии инфекционного процесса сопровождается возрастающей недостаточностью выделительной функции почек и обезвреживающей деятельности печени из-за ишемии, а при некоторых геморрагических инфекциях и вследствие ее прямого поражения возбудителем, синхронно протекающего с затронутостью эндотелия и других клеток. Для ГЛПС с более медленным по сравнению с лихорадками Марбург и Эбола течением васкулярные тромбы и некроз клеток эндотелия нехарактерны, а клиника обусловлена генерализованным расширением капилляров, отеками, инфильтрацией крупных органов и лимфатических узлов гранулоцитами. Для данной нозоформы наиболее заметна возросшая проницаемость капилляров, в том числе и нефронов, отражающая дисфункцию эндотелия в сочетании с дисбалансом медиаторов и других регуляторных компонентов гемостаза.
На завершающей стадии вирусных геморрагических лихорадок с неблагоприятным исходом сохраняются тромбоцитопения вследствие убыли тромбоцитов в агрегаты и микротромбы, дефицит фактора Хагемана, тромбооксана А2, других медиаторов, фаза гипокоагуляции плавно переходит в состояние глубокой гипокоагуляции с развитием соответствующей симптоматики - многократно увеличивается время свертываемости крови, уровень тромбоцитов и лейкоцитов максимально низок, кровоточивость достигает максимума, тогда как температура тела снижается.
Таким образом, патогенез геморрагических состояний при геморрагических лихорадках отражает комплекс динамически протекающих сопряженных процессов, наслаивающихся друг на друга, основу которых составляет:
- разрегулирование нормального физиологического соотношения компонентов систем, обеспечивающих гемостаз (см. выше), в связи с изменением секреторной деятельности клеток, причастных к гемостазу;
- анатомо-морфологическое обнажение стенок кровеносных сосудов в наиболее активной (в аспекте ее функциональной деятельности) части, а именно - в участках микроциркуляции (артериола-капилляр-венула);
- повышение проницаемости сосудов из-за нарушения их целостности и меняющегося содержания в крови вазоактивных компонентов (тромбоцитов, эйкозаноидов, кининов, адреналина и других фармакологически активных соединений);
- отставанием иммунологически важных защитных реакций макроорганизма, в том числе и в виде формирования специфических антител, от нарастания деструктивных изменений при генерализации инфекционного процесса;
- суммарным формированием ДВС-симптоматики различной степени выраженности.
При этом изменения в крови последовательно развиваются через фазу гиперкоагуляции в стадию гипокоагуляции с обязательной тромбо- и лейкопенией потребления и сдвигом формулы нейтрофилов влево. Скорость развития симптоматики и исход болезни определяются степенью патогенности возбудителя, конституциональными особенностями и иммунным статусом заболевшего.
Симптомы Геморрагических лихорадок:
Диагностика Геморрагических лихорадок:
Диагностика геморрагических лихорадок базируется на клинико-эпидемиологических и лабораторных данных. В специфической диагностике используются серологические (РСК, РНИФ и др.), иммунохимические (ИФА), молекулярно-биологические (ПЦР, гибридизация), иногда вирусологический методы.
Дифференциальная диагностика проводится с гриппом, лептоспирозом, риккетсиозами, целым рядом арбовирусных инфекций, не относящихся к геморрагическим лихорадкам, менингококковой инфекцией, сепсисом, тромбогеморрагической пурпурой (болезнь Верльгофа), геморрагическим васкулитом (болезнь Шенлейна-Геноха) и др.
Лечение Геморрагических лихорадок:
Все больные должны быть госпитализированы и за ними необходим тщательный уход. Назначают полужидкую, легкоусвояемую и калорийную пищу с максимальным обогащением диеты витаминами, особенно С и В (свежие овощи и фрукты, натуральные фруктовые и ягодные соки, настой шиповника, дрожжи). Рекомендуется давать больному до 600-800 мг аскорбиновой кислоты внутрь ежедневно, витамин Р; ввиду наличия геморрагических явлений назначать витамин К (викасол) по 0,015 г 4 раза в день на протяжении 4 дней.
Следует иметь в виду, что геморрагические проявления могут достигнуть наибольшего развития не в лихорадочном периоде болезни, а после его окончания.
Применяют также внутривенные вливания глюкозы (40% раствор по 40-50 мл ежедневно). В лихорадочном периоде болезни рекомендуются переливания крови по 125-150 мл через день, внутримышечные инъекции камполона или антианемина (по 2 мл ежедневно на протяжении 5-7 дней), прёпараты железа внутрь. В качестве вспомогательного терапевтического средства дают внутрь десенсибилизирующий (антигистаминный) препарат димедрол по 0,08 г 4 раза в день в течение 4-6 дней. Выздоравливающий нуждается в постельном режиме до полного исчезновения клинических симптомов; после выписки необходимо медицинское наблюдение. Прогноз. Тяжесть клинического течения геморрагических лихорадок колеблется в очень широких пределах. Дальневосточный нефрозонефрит протекает значительно тяжелее, чем другие описанные здесь геморрагические лихорадки, и в отдельных случаях заканчивается летально.
Профилактика Геморрагических лихорадок:
Успех борьбы с распространением геморрагических лихорадок определяется в первую очередь результатами мероприятий по уничтожению переносчиков инфекции и по защите от их укусов здоровых людей. В местностях, где встречаются заболевания, необходима тщательная расчистка земельного участка под жилые и производственные помещения: скашивание травы, уничтожение кустарника, сжигание опавших листьев.
Лица, работающие или проживающие в местностях, где встречаются геморрагические лихорадки, должны носить сапоги, перчатки, а также специальные комбинезоны; обязательна пропитка производственной одежды препаратами, отпугивающими клещей. Необходимость проведения этих мероприятий зависит от конкретной эпидемиологической обстановки. Перечисленные средства обеспечивают защиту человека от укусов зараженных клещей, являющихся переносчиками геморрагических лихорадок.
С целью специфической профилактики омской геморрагической лихорадки в природных очагах этой болезни применяют профилактическую вакцинацию населения при помощи эмульсии вируса, убитого формалином (прививки производят по специальной инструкции).
Основная роль в профилактике геморрагических лихорадок принадлежит все же не вакцинации, а систематическому осуществлению указанных выше мероприятий.
К каким докторам следует обращаться если у Вас Геморрагические лихорадки:
Вас что-то беспокоит? Вы хотите узнать более детальную информацию о Геморрагических лихорадок, ее причинах, симптомах, методах лечения и профилактики, ходе течения болезни и соблюдении диеты после нее? Или же Вам необходим осмотр? Вы можете записаться на прием к доктору .
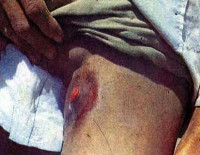
Бубонная чума – это карантинная природно-очаговая инфекция. Основным клиническим симптомом является наличие чумного бубона. Для нозологии характерна высокая лихорадка, выраженная интоксикация, при иммуносупрессии возможно висцеральное поражение, генерализация инфекции. Диагностика построена на обнаружении возбудителя в биологических материалах (микроскопия, посев, ПЦР), серологические методы малоинформативны, практически не применяются. Лечение проводится в условиях обязательного карантина, включает в себя антимикробную этиотропную терапию, массивную дезинтоксикацию, симптоматические методы. Реже прибегают к хирургическим вмешательствам.
МКБ-10
Общие сведения

Причины
Возбудитель болезни – бактерия Yersinia pestis. Источником и резервуаром инфекции служат больные люди, грызуны, зайцы, лисы, верблюды, домашние кошки и другие животные. Переносчики – блохи, в пищеварительном тракте которых размножаются чумные палочки. Заразными насекомые становятся уже через 3-5 суток после попадания в них возбудителя и остаются таковыми в течение года. При укусе блоха срыгивает внутрь ранки содержимое желудка с большим количеством бактерий. Также описаны воздушно-капельный, фекально-оральный и контактно-бытовые пути инфицирования.
Основными факторами риска заражения бубонной чумой считаются проживание и несение воинской службы на эндемичных территориях, профессии, связанные с истреблением грызунов, работой в зернохранилищах, ветеринарной службе. Опасности подвергаются археологические экспедиции, вскрывающие места старинных захоронений, а также животноводы, медицинский персонал, пастухи, туристы, работники международных аэропортов, зоопарков. Бубонной чуме наиболее подвержены дети, лица, не достигшие 20-ти лет, и взрослые мужчины.
Патогенез
После проникновения в организм чумные бактерии размножаются в месте внедрения, образуя воспалительный уплотненный участок либо папулу, пустулу с геморрагическим содержимым. Распространение возбудителя происходит лимфогенно до регионарных лимфатических узлов, внутри которых бактерии размножаются. Особенностью Y. рestis является способность к подавлению фагоцитарной активности макрофагов, внутриклеточному размножению в них. При этом выделяется большое количество токсинов, продуктов распада тканей, возбудителей, что обусловливает интоксикационные симптомы.
Плотная фиброзная нодулярная оболочка препятствует попаданию в очаг воспаления полиморфно-ядерных лейкоцитов и специфических антител. Активная репликация возбудителя способствует расплавлению и увеличению лимфатической ткани регионарных узлов, вследствие чего возникают конгломераты. Длительная персистенция, массивный воспалительный процесс приводит к геморрагическому некрозу нодулярной ткани и выходу чумной палочки в системный кровоток с последующей генерализацией инфекции; в 10-20% случаев развиваются симптомы вторично-легочной чумы.
Симптомы бубонной чумы
Инкубационный период составляет 2-6 суток, реже 1-12 суток, ведущими симптомами являются нарастающие локальные боли (обычно в паху), лихорадка до 39-40° C и более. Пациенты вынуждены сохранять крайне неудобные позы для уменьшения болевых ощущений. Характерны сильные ознобы, выраженная слабость, головные боли, расстройства сна, беспокойство, дискоординация движений, иногда бред, галлюцинации. Около половины заболевших бубонной чумой отмечают симптомы расстройств ЖКТ: абдоминальные боли, тошноту, рвоту, эпизоды диареи.
Спустя 1-3 дня без лечения преимущественно в паховой области, реже в зоне подмышек или шеи обнаруживается очень плотное, резко болезненное образование с гиперемированной, горячей, иногда лоснящейся над ним кожей. Конгломерат неподвижен, поскольку спаян с окружающей клетчаткой. Движения в конечности (чаще – нижней) ограничиваются. Через несколько дней образование размягчается, в нем появляются пульсирующие боли, может образовываться свищевое отверстие с изливающимся гнойным содержимым. После вскрытия бубона больные отмечают некоторое улучшение самочувствия, уменьшение выраженности симптомов.
Осложнения
К наиболее частым негативным последствиям бубонной чумы относят симптомы со стороны свертывающей системы крови (до 86% больных), что в 5-10% случаев приводит к возникновению сухой гангрены кожи, верхних и нижних конечностей. 5-50% пациентов имеют осложнения в виде единичных, множественных, либо массивных кровоизлияний. У больных бубонной чумой с нарушениями иммунитета, тяжелыми сопутствующими болезнями системного характера на 2-3 сутки заболевания возникает переход в генерализованную форму.
Диагностика
Стандарты диагностики бубонной чумы предусматривают консультацию инфекциониста, другие врачи привлекаются для осмотра и лечения по показаниям. Важным элементом диагностического поиска является сбор эпидемиологического анамнеза, строгое соблюдение правил осмотра, взятия, транспортировки и исследований биологических субстанций; работа с ними разрешена только в условиях лабораторий карантинных инфекций. Наиболее информативными инструментальными и лабораторными исследованиями при бубонной чуме считаются:
- Физикальные данные. Объективно определяются симптомы интоксикационного вовлечения ЦНС: больные возбуждены, беспокойны, речь невнятная. Пальпаторно бубон представляет собой резко болезненный малоподвижный конгломерат лимфоузлов с нечеткими контурами, гиперемированной горячей кожей над ним, флюктуацией либо свищами; около образования возникают чумные фликтены. Отмечается вынужденная поза пациента. Патологические изменения со стороны внутренних органов обычно отсутствуют.
- Лабораторные исследования. Общеклинический анализ крови характеризуется выраженным лейкоцитозом, сдвигом лейкоцитарной формулы влево, нейтрофилезом, нарастающей тромбоцитопенией, вторичной анемией, ускорением СОЭ. Изменения биохимических параметров транзиторны, чаще отмечается увеличение активности АЛТ, АСТ, общего билирубина, мочевины, креатинина, гипопротеинемия. В общем анализе мочи обнаруживается эритроцитурия.
- Выявление инфекционных агентов. Через 1-2 часа лаборатория должна предоставить результаты микроскопии свищевого отделяемого или пунктата бубона; разрешается применение ПЦР. Обязательным является посев биологических материалов на питательные среды. Серологические методики (ИФА, РПГА) можно оценить только со 2-ой недели инфекции, исследуя парные сыворотки с интервалом 14 дней для фиксации роста титра антител не менее чем четырехкратно.
- Инструментальные методики. Обязательно проведение рентгенографии грудной клетки для исключения рентгенологических симптомов чумной пневмонии; реже показаны КТ, МРТ. С целью дифференциального диагноза со злокачественными новообразованиями рекомендуется ультразвуковое исследование молочных желез, малого таза, органов брюшной полости, мягких тканей, забрюшинного пространства, лимфатических узлов; под контролем УЗИ возможна пункция бубона.
Дифференциальная диагностика осуществляется с туляремией (малоболезненный, не спаянный с кожей бубон). При туберкулезе рост лимфоузла постепенный, есть указания на иммунодефицит, симптомы туберкулеза в анамнезе. Укус крысы, пятнисто-уртикарная сыпь или оцарапывание кошкой, лимфангоит свидетельствуют в пользу содоку и болезни кошачьих царапин соответственно. Лимфогранулематоз манифестирует симптомами поражения легких, костей, ЖКТ. Хламидиозная инфекция иногда протекает с паховым односторонним лимфаденитом, спаиванием с окружающими тканями, формированием свищей.
Лечение бубонной чумы
Все пациенты с подозрением на заболевание либо с патогномоничными симптомами обязательно госпитализируются в боксированную палату инфекционного отделения для немедленного начала лечения. Постельный режим назначается до 4-5 дней нормализации температуры тела, передвижение ограничивается боксом. Диетические рекомендации неспецифичны, обусловлены необходимостью введения антибиотиков с широким спектром нежелательных токсических явлений, поэтому из рациона больного исключается тяжелая пища и алкоголь. Питьевой режим увеличивается с целью дезинтоксикации.
Консервативная терапия
Лечение больных с бубонной чумой направлено на снижение выраженности симптомов, профилактику заражения других людей. Пациентам обязательно назначаются антибактериальные средства, эффективные в отношении возбудителя и вводимые парентерально. К таковым относятся стрептомицин, тетрациклины, фторхинолоны, аминогликозиды, цефалоспорины, рифампицин. Требуется массивная внутривенная дезинтоксикация глюкозо-солевыми, сукцинат-содержащими растворами, назначение обезболивающих, противовоспалительных, жаропонижающих средств. Объем симптоматического лечения зависит от клинической необходимости.
Хирургическое лечение
Местное лечение бубонов вне их размягчения не проводится. С лечебно-диагностической целью может осуществляться тонкоигольная пункционная биопсия лимфатических узлов с одновременным опорожнением бубона. При наличии кожной язвы проводят её иссечение с целью гистологического исследования. Хирургическое вскрытие и дренирование бубонов рекомендовано при появлении симптома флюктуации конгломератов, одновременно внутрибубонно вводят антибиотики, активные в отношении Y. Pestis, стрептококков и стафилококков.
Экспериментальное лечение
В ходе современных исследований установлено, что макрофаги несут на себе рецептор к кортикостероидам, что способствует потенцированию действия собственной иммунной системы при симптомах бубонной чумы. В экспериментах с лечением мышей было доказано повышение макрофагальной способности инфильтрировать инфицированные ткани и поглощать апоптозные нейтрофилы под действием указанных гормональных препаратов. Также было отмечено усиление бактериального поглощения и улучшение выживаемости зараженных животных.
Прогноз и профилактика
Прогноз при отсутствии лечения серьезный, смертность достигает 7-26%. Наиболее неблагоприятными локализациями считаются подмышечные (15-20%) и шейные (5%) зоны из-за риска развития симптомов легочной формы болезни и отека воздухопроводящих путей. Общая продолжительность стационарного лечения для больных, страдающих бубонной чумой, должна составлять не менее 4-х недель, медицинское наблюдение после выписки – не менее 3-х месяцев. Срок изоляции контактных лиц – 7 дней.
Специфическая профилактика показана лицам, проживающим в эндемичных регионах, туристам, военным. Вакцинация осуществляется сухой живой вакциной. К неспецифическим мерам относится строгий санитарный контроль над системами водоснабжения и водоотведения, плановая дератизация в канализационных коллекторах, надзор за мигрантами, туристами, ввозимыми продуктами, животными. Важными мерами борьбы с распространением чумы являются ранняя изоляция и лечение больных, карантинизация контактных лиц, дезинфекция в очаге, улучшение санитарно-гигиенических условий жизни.
3. Adjunctive Corticosteroid Treatment Against Yersinia pestis Improves Bacterial Clearance, Immunopathology, and Survival in the Mouse Model of Bubonic Plague/ Yinon Levy, Yaron Vagima, Avital Tidhar// The Journal of Infectious Diseases – 2016 - V.214, №6.
Читайте также:

