Острые респираторные вирусные инфекции калюжин о в
Обновлено: 06.05.2024
Острые респираторные вирусные инфекции (ОРВИ) являются самой распространенной формой острых заболеваний. Основным симптомокомплексом при ОРВИ является катаральное воспаление дыхательных путей, развивающееся через 2–7 дней после инфицирования. Цели лабораторного обследования при ОРВИ — обнаружение бактериальных очагов, не определяемых клиническими методами, а также мониторинг коморбидной патологии. Для лечения гриппа доступны ингибиторы нейраминидазы, производные адамантана, умифеновир, при этом химиопрофилактика и химиотерапия не являются альтернативой вакцинации и не влияют на ее эффективность. Однако многообразие возбудителей и отсутствие для большинства из них средств этиотропной терапии вызывают необходимость поиска и изучения лекарственных средств с неспецифическим механизмом действия, в т. ч. патогенетических. Фармакотерапевтический комплекс при ОРВИ должен быть минимизирован и формироваться на основе средств с доказанной эффективностью. В отношении остальных групп препаратов целесообразно проведение качественных исследований, в ходе которых будет определено возможное место (или его отсутствие) в существующей программе помощи больным ОРВИ. Показано, что гомеопатический препарат Афлубин ® ускоряет регрессию симптомов ОРВИ (назальные симптомы, головная боль, головокружение, миалгии, температурная реакция).
Ключевые слова: острые респираторные вирусные инфекции, вирусно-бактериальные ассоциации, бактериальные очаги, полипрагмазия, эффективность.
Для цитирования: Белан Э.Б., Садчикова Т.Л. Острые респираторные вирусные инфекции: актуальный взгляд на проблему и современный подход к лечению. РМЖ. Медицинское обозрение. 2018;2(11):60-64.
E.B. Belan, T.L. Sadchikova
Volgograd State Medical University
Acute respiratory viral infections (ARVI) are the most common form of acute diseases. The main symptom complex in ARVI is catarrhal inflammation of the respiratory tract, which develops 2–7 days after infection. The purpose of laboratory examination in ARVI is a detection of bacterial foci that are not determined by clinical methods, as well as monitoring of comorbid pathology. Neuraminidase inhibitors, adamantane derivatives, umifenovir are available for treatment of influenza, while chemoprophylaxis and chemotherapy are not an alternative to vaccination and do not affect its effectiveness. However, the diversity of pathogens and the lack of etiotropic therapy for most of them necessitate the search and study of medications with a nonspecific mechanism of action, including pathogenetic ones. Pharmacotherapeutic complex in ARVI should be minimized and formed on the basis of agents with proven effectiveness. With respect to the remaining groups of medications, it is advisable to conduct a qualitative study, during which a possible place (or its absence) in the existing program of care for ARVI patients is determined. It is shown that the homeopathic drug Aflubin ® accelerates the regression of symptoms of ARVI (nasal symptoms, headache, dizziness, myalgia, temperature reaction).
Key words: acute respiratory viral infections, viral-bacterial associations, bacterial foci, polypragmasia, efficacy.
For citation: Belan E.B., Sadchikova T.L. Acute respiratory viral infections: сurrent view on the problem and the modern approach to treatment // RMJ. Medical Review. 2018. № 11. P.60 –64.
Статья посвящена современным аспектам терапии острых респираторных вирусных инфекций.
Введение
Острые респираторные вирусные инфекции (ОРВИ) являются самой распространенной формой острых заболеваний, составляющих в РФ 80–90% от всех регистрируемых инфекций. Не менее 1 раза в год болеет практически каждый житель страны [1]. Причинами этого являются высокая контагиозность возбудителей, разнообразие их видового состава (рис. 1) (известно более 200 вирусов — возбудителей ОРВИ, образующих различные группы (вирусы парагриппа, гриппа, аденовирусы, риновирусы, энтеровирусы и т. д.) при генетической лабильности многих возбудителей, приводящей к постоянному образованию новых штаммов [1]. Способствовать хронизации процесса, затяжному и/или осложненному течению заболевания могут также представители семейства Herpesviridae [2]. Одновременное коинфицирование несколькими возбудителями приводит к более тяжелому течению заболевания (рис. 2).
Классификация
Для различных форм ОРВИ предусмотрены следующие коды в МКБ-10:
J00 Острый назофарингит
J02 Острый фарингит
J04 Острый ларингит и трахеит
J04.0 Острый ларингит
J04.1 Острый трахеит
J04.2 Острый ларинготрахеит
J06 Острые инфекции дыхательных путей множественной и неуточненной локализации
J06.0 Острый ларинготрахеит
J06.9 Острая инфекция верхних дыхательных путей неуточненная
Особые проблемы — отсутствие средств этиотропной терапии для большинства возбудителей или резистентность к имеющимся средствам, высокая частота вирусно-бактериальных ассоциаций, сопровождающихся более тяжелыми формами заболевания. По данным О. Kurskaya et al. [3], частота вирусных ассоциаций у госпитализированных больных составляла до 30%.
Несмотря на то, что заболевание в большинстве случаев носит саморазрешающийся характер, непосредственной причиной смерти обычно является развитие на фоне респираторной вирусной инфекции тяжелых осложнений (пневмонии, бронхита, синусита, острого среднего отита, энцефалопатии, бронхиальной астмы, многочисленных сердечно-сосудистых и обменных нарушений) [4, 5].
Особенности течения
Инкубационный период большинства ОРВИ составляет 2–7 дней. Максимальное выделение вируса происходит на 3-й день после заражения (этот же период характеризуется и наиболее выраженными симптомами), резко снижается к 5-му дню заболевания (появляется вирусспецифический IgM), хотя у некоторых больных вирус может выделяться до 2 нед. (до достижения титра вирусспецифических IgG, достаточного для элиминации возбудителя) [7].

Основным симптомокомплексом при ОРВИ является катаральное воспаление дыхательных путей. Вместе с тем развитие симптомов является не столько следствием повреждающего действия возбудителя в отношении эпителиальных клеток, сколько результатом их десквамации и реакции иммунной системы, прежде всего факторов врожденного иммунитета. Синтез провоспалительных цитокинов (IL-1, IL-6, IL-8 и др.) способствует развитию пирогенной реакции при инфекционных болезнях, индуцирует системную и локальную воспалительные реакции. Повышение проницаемости сосудов слизистой дыхательных путей при ОРВИ связано с гиперсекрецией слизи, исчезновение прозрачности назального секрета и возможное появление желтоватого или зеленоватого оттенка — с миграцией активированных лейкоцитов в очаг реакции. Подобные симптомы необязательно свидетельствуют о присоединении бактериальной инфекции и необходимости назначения антибиотиков [7]. Несмотря на участие иммунных механизмов в развитии клинических симптомов ОРВИ, их следует рассматривать в качестве патогенетического, но не патогенного фактора, необходимо обеспечить нормальное функционирование иммунной системы при заболевании.
Диагностика ОРВИ базируется на клинико-эпидемиологических данных, результатах инструментального и лабораторного обследования [5, 7].
Несмотря на сходство клинических проявлений ОРВИ различной этиологии, существуют особенности клинических проявлений гриппа, респираторно-синцитиальной вирусной инфекции (РСВ) и т. д. (табл. 1) [8].
Методы исследования
Целью лабораторного обследования при ОРВИ является обнаружение бактериальных очагов, не определяемых клиническими методами, у детей, а у взрослых — приведшей к ухудшению течения коморбидной патологии.
Клинический анализ крови у взрослых относится к обязательным методам исследования (типичны нормоцитоз и ускорение СОЭ), у детей целесообразен только при выраженных общих симптомах с лихорадкой [5, 7].
Клинический анализ мочи у взрослых является обязательным методом исследования (при неосложненном течении ОРВИ не должно быть изменений), у детей — рекомендуется проводить при наличии лихорадки без катаральных явлений [5, 7].
Определение уровня С-реактивного белка (СРБ) рекомендовано для исключения тяжелой бактериальной инфекции у детей с фебрильной лихорадкой (повышение температуры выше 38 °С), особенно при отсутствии видимого очага инфекции (вероятность 85% при уровне СРБ >30–40 мг/л) [7].
Плановые вирусологическое и бактериологическое исследования в настоящее время не рекомендуются, поскольку они требуют дополнительных визитов в лечебно-профилактическое учреждение, сопряжены с дополнительными затратами, часто не дают немедленного ответа, а результаты не влияют на выбор тактики лечения больных. Исключение составляют экспресс-тесты на грипп у пациентов с высокой лихорадкой и на стрептококк при подозрении на острый стрептококковый тонзиллит.
Инструментальные исследования (рентгенография органов грудной клетки при подозрении на пневмонию; рентгенография придаточных пазух носа при подозрении на развитие синусита; ЭКГ при наличии кардиальных симптомов) при неосложненном течении не проводят. Детям с симптомами острого ринофарингита не рекомендуется проводить рентгенографию пазух носа в первые 12 дней болезни. У взрослых консультация врача-оториноларинголога показана при подозрении на развитие синусита или отита, детям отоскопия рекомендована во всех случаях ОРВИ. При тяжелом/среднетяжелом течении или отказе от госпитализации рекомендована консультация врача-инфекциониста.
Лечение
В статье представлены результаты анализа опубликованных в течение 25 лет работ, посвященных эффективности и безопасности применения человеческого рекомбинантного интерферона альфа-2b. Суммированы и оценены результаты проведенных исследований по эффективно
Treatment of acute viral respiratory infections and influenza in children: metaanalysis results T. A. Ruzhentsova, D. S. Levitskaya
The article presents analysis results for the works published during 25 years, dedicated to efficiency and safety of application of human recombinant interferon alpha-2b. The results of the studies on efficiency and safety of application of human recombinant interferon alpha-2b for treatment of influenza and acute viral respiratory infections in children were summarized and assessed.
Острые респираторные вирусные инфекции (ОРВИ) и грипп остаются наиболее часто встречающимися заболеваниями у детей любого возраста, сохраняют лидирующую позицию в структуре заболеваемости во всем мире. Основой лечения, по большинству имеющихся рекомендаций, является симптоматическая терапия: жаропонижающие препараты и назальные деконгестанты. Но оно не способствует элиминации вируса, что особенно важно при гриппе, когда репликация наиболее активна и высок риск развития осложнений, связанный с этим.
Впервые решение этой задачи стало возможным с открытием в 1957 г. А. Айзексом и Д. Линденманном интерферонов (ИФН), которые реализуют врожденную неспецифическую локальную и системную реакции организма в ответ на внедрение и репликацию вирусов [1, 2]. В настоящее время интерфероны применяют при различных заболеваниях вирусной этиологии [1–4].
В терапии используют человеческие рекомбинантные ИФН, синтезируемые бактериями, в генетический аппарат которых встроен ген человеческого ИФН-α, β или γ. Эти ИФН индуцируют синтез специфических ферментов, подавляющих синтез вирусных РНК и белков в клетке, стимулируют экспрессию HLA-молекул, презентацию антигенов иммунным клеткам и активность киллеров. Интерферон альфа-2b вызывает экспрессию генов, нарушающих проникновение вируса в клетку и трансляцию вирусных белков, а также запускает механизм апоптоза инфицированных клеток.
Отечественный препарат Виферон, содержащий человеческий рекомбинантный интерферон альфа-2b, альфа-токоферола ацетат и аскорбиновую кислоту, был создан в 1980-е гг. Альфа-токоферола ацетат и аскорбиновая кислота усиливают противовирусное действие ИФН, сохраняют его биологическую активность в лекарственной форме и способствуют стимуляции неспецифического иммунитета [5]. Однако по результатам отдельных проведенных исследований не всегда видно достоверное влияние на ту или другую симптоматику. Суммирование данных позволяет повысить объективность и достоверность выводов.
Целью данной работы было суммировать и оценить результаты проведенных исследований по эффективности и безопасности применения препарата Виферон для лечения гриппа и ОРВИ у детей.
Материал и методы исследования
Проведен метаанализ доступных публикаций, посвященных эффективности и безопасности применения препарата Виферон для лечения гриппа и ОРВИ у детей. Результат представлен в соответствии со стандартами, установленными в Положении о качестве представления метаанализа (Quality of Reporting of Meta-analyses, QUOROM, 1999) [6]. Проведен поиск в электронных базах данных для выявления материалов, отвечающих критериям включения в систематический обзор.
Критерии включения работ в метаанализ
Стратегия поиска
Экспертная оценка включения и невключения исследований
Просмотр результатов поиска (названий и рефератов статей) осуществляли два независимых эксперта. После отбора всех потенциально подходящих статей был проведен анализ их полного содержания для установления соответствия с принятыми критериями включения.
Оценка качества исследований
Статистические методы
Для обработки данных использовали встроенные программы статистического анализа в программе Excel, в частности функцию TTEST для поиска различий результатов между сравниваемыми группами в исследованиях, включенных в метаанализ. Для определения достоверности различий исходов по взвешенным средним (x) в сравниваемых группах использовали программу Statistica 6.1 (StatSoft Inc., США) с предварительным определением среднего квадратичного отклонения взвешенной (σ) по формуле σ =, где m — ошибка средней арифметической, n — число детей в группе. Различия между рассчитанными показателями в группах оценивали по двустороннему Z-критерию, статистически значимыми считали при вероятности > 95% (p < 0,05).
Результаты
В ходе поиска было установлено, что рекомбинантный препарат интерферон альфа-2b был впервые применен для лечения вирусных инфекций в 1986 г. Первое исследование было проведено в Австралии [7], затем, позднее, — в 2005 г. и в 2010 г. — в Китае [8, 9], последующие — в Москве, Санкт-Петербурге, а также в Казахстане [10]. Помимо этого компанией-производителем были предоставлены отчеты о 2 клинических испытаниях, проведенных в московских клиниках.
В ходе поиска был обнаружен 21 источник [7–27]. Семнадцать РКИ [10, 11, 12–26] соответствовали критериям включения в данный систематический обзор (табл. 1), другие 4 исследования [7–9, 27] были исключены из-за несоответствия по возрасту для данного метаанализа или недостаточно полного представления результатов. Другие публикации, содержащие сведения о проведенных и опубликованных ранее исследованиях, обзоры литературных данных и клинические наблюдения, также были исключены.
Основные сведения об исследованиях, включенных в метаанализ, представлены в табл. 1:
- В 17 исследованиях участвовали 2246 пациентов (1398 пациентов в основной группе и 787 в группе сравнения).
- 5 исследований [11, 14, 17, 25, 26] были двойными слепыми рандомизированными плацебо-контролируемыми исследованиями.
- 12 исследований были открытыми [10, 12, 13, 15, 16, 18–24], в которых проводилось сравнение эффективности и безопасности Виферона в разных формах (мазь, или гель, или свечи) с плацебо [10, 12, 13, 16, 19, 20, 22, 23] или препаратами сравнения — другими противовирусными или иммуномодулирующими препаратами — Генфероном [15], Анафероном и Арбидолом [18], умифеновиром и осельтамивиром [21].
- Возраст участников был сопоставимым во всех исследованиях.
- Суточная доза Виферона была схожей во всех исследованиях, хотя имели место различия в длительности применения (5, 7–10 дней, до 2,5 месяцев в 1 исследовании).
- В 17 отобранных исследованиях препарат Виферон применяли в разных формах выпуска. Чаще всего (табл. 1 и 2), в 9 исследованиях [15, 18–24, 26], использовали препарат в форме суппозиториев в возрастной дозировке по инструкции. В 4 исследованиях [14, 16, 17, 25] детям назначали Виферон в форме геля интраназально и в одном исследовании интраназально и на миндалины [13], в 3 исследованиях использовали 2 формы препарата — в виде мази или геля в течение 5 суток и суппозиториях 1–2 раза в сутки [10–12].
- В 16 из 17 проанализированных исследований применялся плацебо-контроль, в двух были сформированы дополнительные группы, в которых назначали другие противовирусные препараты (Генферон, умифеновир, Анаферон), в одной — группа сравнения получала осельтамивир или умифеновир.
- Отмечена клиническая гомогенность в условиях проведения исследований — во всех исследованиях лечение проводилось в стационарных условиях, за исключением 1 исследования с наблюдением до 2,5 месяцев.
- Методологическое качество исследований варьировало: скрытие распределения было неопределенным. Выбор пациентов чаще всего проводился методом случайной выборки, только 5 испытаний были двойными слепыми [11, 14, 17, 25, 26], однако часто не указывалось, кого касалось маскирование. Остальные исследования были открытыми.
- Полнота наблюдений была адекватной во всех исследованиях.
- Анализ полученных результатов в зависимости от назначенного лечения был выполнен во всех исследованиях.
Основной целью всех исследований, включенных и не включенных в метаанализ, являлась оценка эффективности лечения препаратом Виферон при ОРВИ и гриппе у детей раннего и более взрослого возраста. Результаты представлены в табл. 2.
Как видно из табл. 2, несмотря на то, что далеко не все исследования подтверждают клиническую эффективность Виферона, при его применении у детей с ОРВИ и гриппом отмечается достоверное сокращение средней продолжительности катаральных явлений (на 1,75 суток), ринореи (на 1,71 суток), интоксикации (на 1,18 суток) и в меньшей степени — лихорадочного синдрома (рис.). В выводах, сформулированных по данным проведенных исследований, отмечено, что, даже при сохранении субфебрилитета, катаральных явлений и интоксикации у детей, получавших Виферон, существенно увеличивалась двигательная активность и аппетит. В исследовании, проведенном А. Н. Сейпеновой и соавт., общая длительность заболевания при терапии Вифероном была на 4,8 суток меньше — 5,1 ± 1,1, тогда как в группе сравнения — 9,9 ± 2,1 [10].
Таким образом, результаты всех 17 исследований, включенных в данный метаанализ, подтверждают положительное действие препарата Виферон в любой форме — гель, мазь или суппозитории — для лечения ОРВИ. У детей, получавших его, снижалась средняя продолжительность клинических проявлений, в первую очередь катаральных. Полученные результаты позволяют расценить класс и уровень доказательности IA по каждому из критериев на основании оценки ряда больших двойных слепых плацебо-контролируемых исследований, а также данных, полученных при метаанализе нескольких рандомизированных контролируемых исследований.
В рассмотренных публикациях не было указаний на какие-либо нежелательные явления, связанные с применением различных форм Виферона. При назначении Виферона следует учитывать патогенетические механизмы действия интерферона альфа-2b и относительно небольшое влияние на средние показатели лихорадочного синдрома.
Выводы
Литература
Т. А. Руженцова¹, доктор медицинских наук, профессор
Д. С. Левицкая, кандидат медицинских наук
ФБУН ЦНИИЭ Роспотребнадзора, Москва
Лечение острых респираторных вирусных инфекций и гриппа у детей: результаты метаанализа/ Т. А. Руженцова, Д. С. Левицкая
Для цитирования: Лечащий врач № 3/2020; Номера страниц в выпуске: 52-57
Теги: респираторные вирусные инфекции, неспецифический иммунитет, стимуляция
Что такое острые респираторные заболевания (ОРЗ)? Причины возникновения, диагностику и методы лечения разберем в статье доктора Александрова Павла Андреевича, инфекциониста со стажем в 14 лет.
Над статьей доктора Александрова Павла Андреевича работали литературный редактор Елена Бережная , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Острые респираторные заболевания (ОРЗ) — группа острых инфекционных заболеваний, при которых возбудители проникают в организм человека через дыхательные пути и вызывают синдром поражения респираторного тракта и общей инфекционной интоксикации. Употребление термина ОРВИ (острое респираторное вирусное заболевание) при отсутствии лабораторно подтверждённой этиологической расшифровки является некорректным.
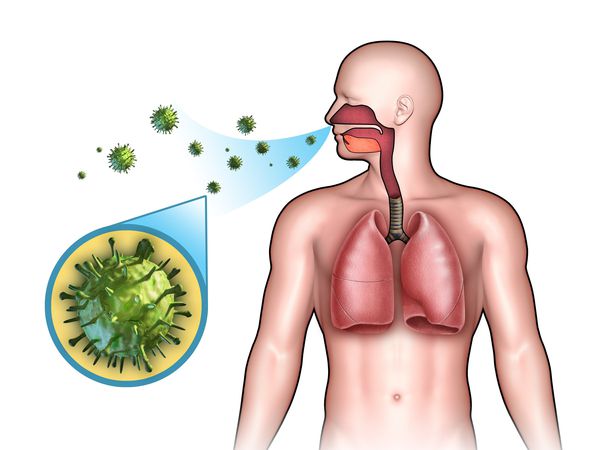
Этиология
ОРЗ — полиэтиологический комплекс заболеваний, т. е. они могут быть вызваны различными видами возбудителей:
- бактерии (стафилококки, стрептококки, пневмококки, гемофильная палочка, моракселла катаралис и др.);
- вирусы (риновирусы, аденовирусы, респираторно-синцитиальный вирус, реовирусы, коронавирусы, энтеровирусы, герпесвирусы, вирусы парагриппа и гриппа);
- хламидии (х ламидия пневмония , хламидия пситаки, хламидия трахоматис );
- микоплазмы (м икоплазма пневмония ).
Чаще всего возбудителем ОРЗ являются вирусы, поэтому термин ОРВИ используют небезосновательно. В последнее время иногда встречается употребление термина ОРИ (острая респираторная инфекция) [2] [4] .
Эпидемиология
ОРЗ — это преимущественно антропонозы, т. е. болезни, способные поражать только человека . Являются самой многочисленной и частой группой заболеваний у человека (до 80 % всех болезней у детей). Поэтому они представляют серьёзную проблему для здравоохранения различных стран вследствие наносимого ими экономического ущерба.
Источник инфекции — больной человек с выраженными или стёртыми формами заболевания. Восприимчивость всеобщая, иммунитет к некоторым возбудителям (аденовирусы, риновирусы) стойкий, но строго типоспецифичный. Это значит, что заболеть ОРЗ, вызванным одним видом возбудителя, но разными серотипами (их могут быть сотни), можно многократно. Заболеваемость повышается в осенне-зимний период, может принимать вид эпидемических вспышек, довлеет к странам с прохладным климатом. Чаще болеют дети и лица из организованных коллективов (особенно в период адаптации).
Основной механизм передачи — воздушно-капельный (аэрозольный, в меньшей степени воздушно-пылевой путь), но может также играть роль контактно-бытовой механизм (контактный — при поцелуях, бытовой — через загрязнённые руки, предметы или воду) [2] [7] .
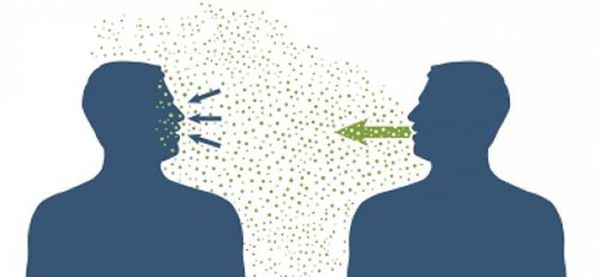
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы острых респираторных заболеваний (ОРЗ)
Инкубационный период различен и зависит от вида возбудителя, может варьироваться от нескольких часов до 14 дней (аденовирус).
Для каждого возбудителя ОРЗ имеются свои специфические особенности протекания заболевания, однако все их объединяет наличие синдромов общей инфекционной интоксикации (СОИИ) и поражения дыхательных путей в той или иной степени. СОИИ проявляется общей слабостью, адинамией, быстрой утомляемостью, повышенной температурой тела, потливостью и др.
Синдром поражения респираторного тракта (СПРТ) — основной синдром для данных заболеваний, он включает:
- Ринит — воспаление слизистой оболочки носа. Характеризуется заложенностью носа, снижением обоняния, чиханием, выделениями из носа — сначала прозрачными слизистыми, затем слизисто-гнойными (более плотные выделения жёлто-зелёного цвета появляются в результате присоединения вторичной бактериальной флоры). — воспаление слизистой оболочки глотки. Основные симптомы: першение и боли в горле различной интенсивности, сухой кашель — "горловой".
- Ларингит — воспаление слизистых оболочек гортани. Проявляется осиплостью голоса, иногда афонией (отсутствием голоса), кашлем и болью в горле.
- Трахеит — воспаление трахеи. Сопровождается мучительным, преимущественно сухим кашлем, саднением и болями за грудиной.
- Бронхит — воспаление слизистой оболочки бронхов. При этом возникает кашель с наличием мокроты и без, сухие хрипы, редко крупнопузырчатые хрипы при аускультации (выслушивании).
- Бронхиолит — воспаление бронхиол (мелких бронхов). Характеризуется наличием кашля различной интенсивности и хрипов разных калибров.
Дополнительными синдромами могут быть:
- синдром экзантемы (высыпания на кожных покровах);
- тонзиллита (воспаления миндалин);
- лимфаденопатии (ЛАП) — увеличения лимфатических узлов ; ( воспаления слизистой оболочки глаза) ;
- гепатолиенальный синдром (увеличение печени и селезёнки);
- геморрагический синдром ( повышенная кровоточивость) ;
- синдром энтерита (воспаления слизистой оболочки тонкого кишечника) .
Алгоритм по распознаванию ОРЗ различной этиологии:
Наиболее распространенным заболеванием, имеющим тяжёлое течение и высокий риск развития осложнений является грипп. Инкубационный период гриппа длится от нескольких часов до 2-3 дней. В отличие от других острых респираторных заболеваний, при гриппе сначала появляется синдром общей инфекционной интоксикации (высокая температура, озноб, сильная головная боль, слезотечение, боль при движении глазных яблок, ломота в мышцах и суставах). На 2-3-день присоединяются симптомы поражения респираторного тракта: першение в горле, насморк, сухой надсадный кашель.
Типичное ОРЗ начинается с чувства дискомфорта, першения в носу и горле, чихания. В течение непродолжительного периода симптоматика нарастает, першение усиливается, появляется чувство интоксикации, повышается температура тела (обычно не выше 38,5 ℃), появляется насморк, неярко-выраженный сухой кашель. В зависимости от вида возбудителя и свойств микроорганизма могут последовательно появляться все перечисленные синдромы ОРЗ в различных сочетаниях и степени выраженности. Возможно появление осложнений и неотложных состояний [6] [7] .
Патогенез острых респираторных заболеваний (ОРЗ)
- у аденовирусов — гликопротеином (фибриллы);
- у парамиксо- или ортомиксовирусов шипами гемагглютинина;
- у коронавирусов — S-белком соединения и гликолипидами.
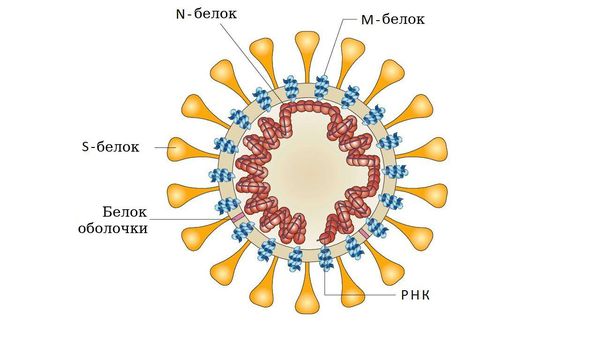
Взаимодействие болезнетворного агента с клеточными рецепторами необходимо не только для прикрепления его к клетке, но и для запуска клеточных процессов, подготавливающих клетку к дальнейшей инвазии. Т. е. наличие соответствующих рецепторов на поверхности клеток — это один из важнейших факторов, определяющих возможность или невозможность возникновения инфекционного процесса. Внедрение возбудителя в клетку хозяина вызывает поток сигналов, активирующих целый ряд процессов, с помощью которых организм пытается от него освободиться, например, ранний защитный воспалительный ответ, а также клеточный и гуморальный иммунный ответ. Повышение метаболизма клеток представляет собой защитный процесс, но с другой стороны в результате накопления свободных радикалов и факторов воспаления запускается патологический процесс:
- нарушается липидный слой клеточных мембран эпителия верхних отделов респираторного тракта и лёгких;
- нарушаются матричные и барьерные свойства внутриклеточных мембран, увеличивается их проницаемость;
- развивается дезорганизация жизнедеятельности клетки вплоть до её гибели.
Второй этап инфицирования характеризуется вирусемией — попаданием вируса в кровь и распространением по всему организму. В совокупности с повышением деятельности защитных механизмов и появлением в крови продуктов распада клеток этот процесс вызывает интоксикационный синдром.
Третий этап характеризуется усилением выраженности реакций иммунной защиты, элиминацию (выведение) микроорганизма и восстановление строения и функции поражённой ткани хозяина [5] [7] .
Классификация и стадии развития острых респираторных заболеваний (ОРЗ)
По вовлечению отдельных частей дыхательной системы:
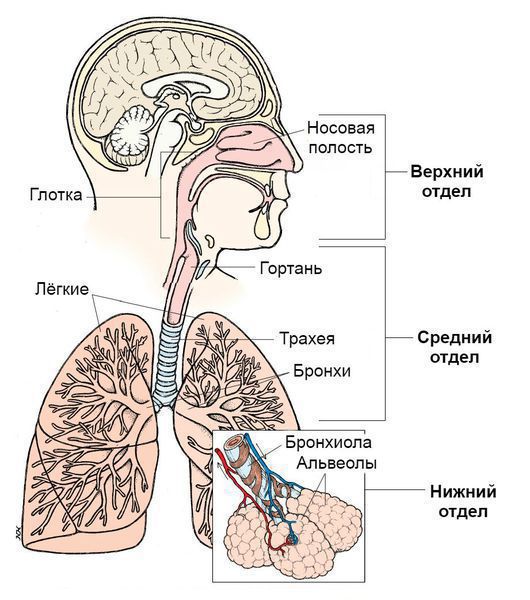
- Инфекции верхних дыхательных путей. Верхние дыхательные пути начинаются с носа и включают голосовые связки в гортани, придаточные пазухи носа и среднее ухо.
- Инфекции нижних дыхательных путей. Нижние дыхательные пути начинаются с трахеи и бронхов и заканчиваются бронхиолами и альвеолами.
По клинической форме:
- Типичная.
- Атипичная:
- акатаральная (отсутствие признаков поражения дыхательных путей при наличии симптомов общей инфекционной интоксикации);
- стёртая (маловыраженная клиника);
- бессимптомная (полное отсутствие клинической симптоматики).
По течению:
По степени тяжести:
По длительности течения:
- острое (5-10 дней);
- подострое (11-30 дней);
- затяжное (более 30 дней) [8] .
Осложнения острых респираторных заболеваний (ОРЗ)
Если острое респираторное заболевание не пролечить вовремя, могут появиться различные более серьёзные заболевания:
- Связанные с ЛОР-органами: отит, синуситы, бактериальный ринит, ложный круп.
- Связанные с лёгочной тканью: вирусные пневмонии, вирусно-бактериальные и бактериальные пневмонии, абсцесс лёгкого ( ограниченный очаг гнойного воспаления в лёгочной ткани) , эмпиема плевры ( скопление гноя в плевральной полости) . Пневмония проявляется значимым ухудшением общего состояния, выраженным кашлем, усиливающимся на вдохе, при аускультации звуком крепитации ( потрескиванием или похрустыванием) , влажными мелкопузырчатыми хрипами, иногда одышкой и болями в грудной клетке.

- Связанные с поражением нервной системы: судорожный синдром, неврит ( воспаление нерва) , менингит ( воспаление оболочек головного и спинного мозга) , менингоэнцефалит (воспаление оболочек и вещества головного мозга), синдром Гийена—Барре и др. [10]
- Связанные с поражением сердца: миокардит (воспаление сердечной мышцы).
- Связанные с обострением хронических заболеваний: обострение ревматизма, тонзиллита, туберкулёза, пиелонефрита (воспаление почки) и др. [7]
Диагностика острых респираторных заболеваний (ОРЗ)
В широкой рутинной практике лабораторная диагностика ОРЗ (особенно при типичном неосложнённом течении) обычно не проводится. В отдельных случаях могут использоваться:
- Развёрнутый клинический анализ крови. При этом может обнаружиться лейкопения ( снижение количества лейкоцитов) и нормоцитоз ( нормальный размер эритроцитов) , лимфо- и моноцитоз ( увеличение числа лимфоцитов и моноцитов) , при наслоении бактериальных осложнений — нейрофильный лейкоцитоз со сдвигом влево (увеличение количество нейтрофилов и появление их незрелых форм );
- Общеклинический анализ мочи (изменения малоинформативны, указывают на степень интоксикации).
- Биохимические анализы крови. Может выявляться С-реактивный белок (указывает на наличие инфекции). При некоторых системных возбудителях, например аденовирусной инфекции, характерно повышение АЛТ.
- Серологические реакции. Возможна ретроспективная диагностика методами РСК, РА, ИФА, однако она редко используется в практической деятельности. В настоящее время широко применяется ПЦР-диагностика мазков-отпечатков, но её применение ограничено в основном стационарами и научно-исследовательскими группами.
При подозрении на развитие осложнений проводят соответствующие лабораторные и инструментальные исследования (рентген придаточных пазух носа, органов грудной клетки, КТ и др.) [3] [5] .
Лечение острых респираторных заболеваний (ОРЗ)
ОРЗ встречается очень часто и в большинстве случаев протекает в лёгкой и средней степени тяжести, поэтому обычно больные проходят лечение дома. При тяжёлых формах (с риском развития или развившимися осложнениями) пациенты должны проходить терапию в условиях инфекционного стационара до нормализации процесса и появления тенденций к выздоровлению. В домашних условиях лечением ОРЗ занимается терапевт или педиатр (в некоторых случаях инфекционист).
Пища должна быть разнообразной, механически и химически щадящей, богатой витаминами, рекомендуются мясные нежирные бульоны (идеально подходит негустой куриный бульон и т. п.), обильное питьё до — 3 л/сут. (тёплая кипячёная вода, чай, морсы). Хороший эффект оказывает тёплое молоко с мёдом, чай с малиной, отвар брусничных листьев.
Медикаментозная терапия ОРЗ включает в себя этиотропную (т. е. воздействующую на возбудителя заболевания), патогенетическую (дезинтоксикация) и симптоматическую (уменьшение беспокоящих симптомов) терапию.
Этиотропная терапия имеет смысл лишь при назначении в раннем периоде и лишь при ограниченном спектре возбудителей (в основном при гриппе). Использование средств отечественной фарминдустрии ("Арбидол", "Кагоцел", "Изопринозин", "Амиксин", "Полиоксидоний" и т. п.) не обладают никакой доказанной эффективностью и могут иметь эффекта, лишь в качестве плацебо.
В качестве симптоматической терапии могут быть использованы препараты следующих групп:
- жаропонижающие при температуре у взрослых свыше 39,5, у детей — свыше 38,5 ℃ (парацетамол, ибупрофен);
- противовирусные и антибактериальные глазные капли при конъюнктивите;
- сосудосуживающие капли в нос при заложенности носа и насморке (не более 5 дней);
- солесодержащие капли в нос при рините для разжижения слизи;
- противоаллергические препараты при аллергическом компоненте ОРЗ;
- средства противовоспалительного и противомикробного действия местного действия (таблетки, пастилки и др.);
- средства для улучшения образования, разжижения и выделения мокроты (муколитики);
- антибиотики широкого спектра действия (при отсутствии улучшения в течении 4-5 дней, присоединении вторичной бактериальной флоры и развитии осложнений) [2][6] .
Прогноз. Профилактика
Прогноз при ОРЗ — положительный. Больные обычно выздоравливают в течение 5-10 дней без неблагоприятных последствий. Осложнения респираторных заболеваний могут возникнуть при гриппе, другие возбудители менее агрессивны. Также неблагоприятные последствия возможны у пациентов с ослабленным иммунитетом. После выздоровления организмом вырабатывается иммунитет к той инфекции, которой человек переболел .
Ведущую роль в профилактике распространения ОРЗ (исключая грипп) является:
консультативное отделение ГНИЦ профилактической медицины Минздрава России, Москва, Россия
клинический отдел инфекционной патологии ЦНИИ эпидемиологии Роспотребнадзора России, Москва, Россия
Влияние респираторных вирусов на течение хронической обструктивной болезни легких: на пути к оптимизации лечения
Журнал: Терапевтический архив. 2015;87(3): 98‑104
Проанализированы современные данные о влиянии респираторных вирусов (РВ) на обострения и клинический фенотип хронической обструктивной болезни легких (ХОБЛ), а также о молекулярных механизмах этого влияния. Подчеркнута роль острых респираторных вирусных инфекций (ОРВИ), в первую очередь риновирусной инфекции (РВИ), как важнейших пусковых факторов обострений ХОБЛ и причины их более тяжелого и длительного течения. Особое внимание уделено индуцированным ОРВИ вторичным бактериальным инфекциям, отягощающим обострения ХОБЛ. Описаны механизмы потенцирования РВ хронического воспаления и ремоделирование дыхательных путей, вызванные табачным дымом. Приведены аргументы о гораздо большей, чем это удается выявить с помощью молекулярных методов верификации РВ, связи острых эпизодов утяжеления респираторных симптомов ХОБЛ с ОРВИ. Генетически обусловленный и/или приобретенный избыточный ответ организма на вирусную инвазию не отражает эффективности противовирусной защиты и является эндогенным повреждающим фактором в рассматриваемой ситуации. Роль РВ в формировании клинических фенотипов ХОБЛ с частыми обострениями остается предметом дискуссии. Выкристаллизовывается необходимость поиска и более активного внедрения в практику средств для предотвращения индуцированных вирусами обострений ХОБЛ. В этом плане выделяются химические и механические поливалентные бактериальные лизаты для перорального и сублингвального применения. Эти препараты, помимо неспецифической стимуляции противовирусной защиты, индуцируют антигенспецифические мукозальные и системные реакции в отношении входящих в их состав бактериальных патогенов. Роль возбудителей ОРВИ в обострениях ХОБЛ заслуживает большего практического внимания на пути к оптимизации лечения этого социально-значимого заболевания.
консультативное отделение ГНИЦ профилактической медицины Минздрава России, Москва, Россия
клинический отдел инфекционной патологии ЦНИИ эпидемиологии Роспотребнадзора России, Москва, Россия
БА — бронхиальная астма
ВИ — вирусные инфекции
ПЦР — полимеразная цепная реакция
РВ — респираторные вирусы
РВИ — риновирусная инфекция
РИ — респираторная инфекция
Тh2 — Т-хелперы 2-го типа
ХОБЛ — хроническая обструктивная болезнь легких
hRV — риновирус человека
RSV — респираторно-синцитиальный вирус
TSLP — тимический стромальный лимфопоэтин
Клиническая картина ХОБЛ характеризуется хроническими проявлениями симптомов с периодами обострений. Последние признаны важными событиями в ходе заболевания и имеют огромное значение для пациентов и для медицинских работников. Они ускоряют прогрессирование ХОБЛ, ухудшают качество жизни, обусловливают значительную морбидность больных и являются основной причиной их смерти. Кроме того, они являются основными драйверами избыточных расходов, связанных с лечением, незапланированными визитам и госпитализациями. Поэтому предотвращение обострений является одной из основных и, к сожалению, пока далеких до полного решения задач ведения пациентов со стабильным течением ХОБЛ.
В настоящем обзоре проанализированы современные данные о влиянии возбудителей ОРВИ на обострения и клинический фенотип ХОБЛ, а также о механизмах этого влияния, чтобы сделать еще один шаг к дальнейшей оптимизации лечения этого заболевания, в частности к более широкому использованию эффективных и безопасных средств профилактики РИ и связанных с ними обострений ХОБЛ. Кроме того, приведены данные о некоторых механизмах индуцированных вирусами обострений бронхиальной астмы (БА) в силу их общности с таковыми при ХОБЛ и достаточно высокой частоты перекрестных фенотипов заболевания (ХОБЛ + астма).
Влияние вирусов на течение ХОБЛ. Исторически патогенные бактерии рассматривались как основная инфекционная причина обострений ХОБЛ. Однако высокая степень ассоциации острых эпизодов утяжеления течения этой болезни с зимними пиками заболеваемости ОРВИ, а также частое предварение обострений ХОБЛ симптомами острых инфекций верхних дыхательных путей позволили предположить большее этиологическое значение респираторных вирусов (РВ). В работах, проведенных в 70—80-е годы прошлого века, в которых для верификации возбудителей ОРВИ использовали серологические и клеточные культуральные тесты, РВ выявлялись в 10—20% случаев обострений ХОБЛ. В исследованиях, выполненных в последние 10—15 лет с применением молекулярных методов определения патогенов, установлено, что вирусы присутствуют в респираторном тракте у 47—56% больных с обострением ХОБЛ [15].
В недавнем систематическом обзоре проанализированы данные 8 оригинальных работ по верификации РВ при обострениях ХОБЛ с помощью полимеразной цепной реакции (ПЦР) и/или ПЦР с обратной транскрипцией. Средневзвешенная частота выявления этих патогенов составляла 34,1%. Наиболее часто (17,3%) обнаруживали пикорнавирусы (преимущественно hRV), затем вирус гриппа — 7,4%, респираторно-синцитиальный вирус (RSV) — 5,3%, коронавирусы — 3,1%, вирусы парагриппа — 2,6%, аденовирус — 1,1%, метапневмовирус человека — 0,7%. Максимальная доля ассоциированных с вирусами обострений ХОБЛ регистрировалась в исследованиях, проведенных в Европе, за которым следовали в порядке убывания этого показателя работы из США, Австралии и Азии. Пикорнавирусы (главным образом hRV) оказались наиболее распространенными находками в западных странах, тогда как возбудители гриппа доминировали в Азии. Представленные результаты свидетельствуют, что географическая эпидемиология вирусов должна учитываться при выработке оптимальной региональной стратегии ведения больных ХОБЛ, направленной на предотвращение обострений [16].
По данным последнего из доступных метаанализов на эту тему, в который включены результаты опубликованных в 1990—2012 гг. 17 независимых оригинальных исследований, отвечающих 7 заданным критериям, средневзвешенная частота выявления РВ при обострениях ХОБЛ составляла 39,3%, тогда как при стабильном течении заболевания — 13,6% [17]. Метаанализ подтверждает роль возбудителей ОРВИ, в первую очередь hRV, как индукторов острых эпизодов усугубления симптомов ХОБЛ, обусловливающих необходимость изменения терапии.
Вероятно, реальная частота ассоциированных с вирусами обострений ХОБЛ значительно выше, так как верификация возбудителей проводится при обращении за медицинской помощью, что часто бывает существенно позже начала этого обострения, т. е. когда вирус уже может не определяться.
Связь вирусных инфекций (ВИ) и характера течения ХОБЛ привлекает внимание из-за отсутствия полной ясности в вопросе о причинах существовании различных по частоте обострений клинических фенотипов этого заболевания. Несмотря на то что в целом существует корреляция частоты обострений и тяжести заболевания, описаны и легкие формы ХОБЛ с частыми эпизодами ухудшения респираторных симптомов [18]. В этой связи выдвинута и является предметом проверки гипотеза о существовании фенотипа с частыми обострениями, не зависящими от тяжести заболевания. Эта гипотеза подразумевает существование базовых механизмов (генетических, биологических или поведенческих), которые определяют восприимчивость к повторным обострениям [19, 20]. Высокая восприимчивость к ВИ дыхательных путей рассматривается как один из таких механизмов [21]. Потенциальная высокая чувствительность к ОРВИ может быть объяснена увеличением экспрессии молекулы межклеточной адгезии ICAM-1, которая является основным рецептором для некоторых вирусов [22]. Как правило, индуцированные вирусом обострения ХОБЛ являются более тяжелыми и длительными. T. Seemungal и соавт. [23] выявили увеличение частоты обострений у больных, у которых при стабильном течении ХОБЛ в биологических образцах из верхних дыхательных путей обнаруживали РВ, главным образом RSV. Следует отметить, что в этом исследовании частота выявления RSV, но не других возбудителей ОРВИ, во время обострений была меньше (14,2%), чем при стабильном течении заболевания (23,5%). Присутствие RSV в респираторном тракте больных вне обострения коррелировало с повышением уровня фибриногена в плазме и интерлейкина-6 (ИЛ-6) в сыворотке крови. Это свидетельствует, что хроническая ВИ может поддерживать воспаление в дыхательных путях и увеличивать тяжесть ХОБЛ стабильного течения. В поддержку этого тезиса можно привести данные о роли латентной аденовирусной инфекции, которая у лиц с генетической предрасположенностью способствует развитию и прогрессированию ХОБЛ у курящих людей [24].
Вместе с тем в недавней работе швейцарские ученые на вполне репрезентативной выборке больных продемонстрировали, что связь текущего обострения с выявлением РВ не увеличивает частоты последующих обострений и смертности в течение года наблюдения. Авторы этого исследования подтвердили известный тезис о том, что надежным предиктором высокой частоты острых эпизодов усугубления респираторных симптомов ХОБЛ, при которых требуется коррекция лечения, является анамнез частых предыдущих обострений [21]. Таким образом, роль вирусов в формировании фенотипов ХОБЛ с частыми обострениями нуждается в дальнейшем уточнении.
В контексте вирусно-бактериальных причинно-следственных связей приведем данные более раннего исследования, в котором установлено, что у больных ХОБЛ в начале обострения в 21% случаев в биологических образцах из носа и глотки выявляли только РВ, в 30% — только патогенные бактерии, а в 12% — вирусно-бактериальные ассоциации. Когда через 5—7 дней пациентов с обнаруженными вирусами подергали повторному обследованию для выявления респираторных патогенов, у 36% из них отмечали развитие вторичной бактериальной инфекции. В то же время симптомы ВИ верхних дыхательных путей предваряли возникновение обострения ХОБЛ у 71% всех больных с верифицированными патогенными бактериями и у 78% пациентов c наиболее часто выявляемым в этой работе патобионтом — H. influenzae [27]. Таким образом, истинная доля индуцированных с вирусами вторичных бактериальных инфекций, в значительной степени определяющих тяжесть и длительность обострения ХОБЛ, может быть существенно выше.
Механизмы индуцированных вирусами обострений ХОБЛ. Как отмечалось, важной, но при этом не единственной причиной того, что РВ провоцируют и увеличивают тяжесть обострений ХОБЛ, является индукция вторичной бактериальной инфекции. Помимо упомянутой деградации антимикробных пептидов, обусловленной активацией продукции эластазы нейтрофилами, существуют и другие индуцированные вирусами механизмы реактивации патобионтов, колонизирующих респираторные пути, и приобретения новых патогенных бактерий из окружающей среды.
Взаимодействие вирусов и бактерий в патогенезе РИ широко освещено в литературе [8]. Наиболее изучен синергизм между вирусами гриппа и S. pneumoniae. Установлено, что не только существует однонаправленная вирусная провокация пневмококковой инфекции, но и, наоборот, бессимптомное носительство S. pneumoniae облегчает инвазию возбудителя гриппа и влияет на исход вирусного заболевания [28]. Нейраминидаза (NA) пневмококков может играть ведущую роль в распространении вирусов гриппа, участвуя в высвобождении почкующихся дочерних вирионов, когда их собственная NA подавлена действием занамивира или осельтамивира [29].
Выявлены ассоциации и между другими РВ и бактериями. Ключевые события, за счет которых вирусы потенцируют развитие вторичных бактериальных инфекций, раскрыты и включают нарушение эпителиального барьера, усиление адгезии бактерий за счет стимуляции экспрессии молекул адгезии на эпителиальных клетках и некоторых других механизмов (например, за счет того, что NA вирусов гриппа и парагриппа отщепляет остатки сиаловых кислот на поверхности респираторного тракта, открывая рецепторы для патобионтов), а также дисфункцию различных компонентов иммунной системы [30].
Механизмы иммуносупрессивного действия РВ, провоцирующие бактериальные суперинфекции, разнообразны: подавление функции нейтрофилов, усиление их апоптоза, угнетение функции естественных киллеров (NK-клеток) и моноцитов, а также истощение альвеолярных макрофагов [31].
В последнее время уточняется роль интерферонов (ИФН) 1-го и 3-го типа — центрального звена врожденной противовирусной защиты — в предотвращении/развитии РИ и обострении хронических заболеваний легких. В ряде исследований установлено угнетение продукции ИФН 1, 2 и 3-го типов у больных БА, муковисцидозом и ХОБЛ. Недостаточность выработки этих цитокинов, с одной стороны, ведет к преобладанию зависимых от Т-хелперов 2-го типа (Тh2) иммунных реакций, а с другой стороны — к дефициту врожденной противовирусной защиты и клеточных иммунных реакций, направленных на инфицированную вирусом клетку [15, 32].
Другое объяснение причины увеличения чувствительности к пневмококковой инфекции заключается в том, что индуцированные вирусами ИФН 1-го типа подавляют функцию легочных γδT-клеток, в частности продукцию ими ИЛ-17 — важнейшего для эффективной защиты от S. pneumoniae цитокина [35].
В совокупности представленные данные свидетельствуют о том, что вызванное ИФН 1-го типа подавление выработки СХС-хемокинов и негативная регуляция γδT-клеток являются важными, если не ключевыми, механизмами, посредством которых ответ организма на вирусную инвазию повышает восприимчивость к вторичной бактериальной инфекции [8].
В экспериментах in vivo и in vitro установлена активация продукции эктрацеллюлярных визикул клетками различных типов дыхательных путей в ответ как на вирусные, так и на бактериальные стимулы [36]. На фоне повышенного уровня внеклеточного АТФ, который наблюдается в респираторном тракте больных ХОБЛ [37], индуцированное патогеном увеличение уровня этих везикул ведет к зависимому от АТФ высвобождению из них ИЛ-1β и ИЛ-18 — цитокинов, концентрация которых коррелирует с уровнем нейтрофилии и тяжестью обострений ХОБЛ [36].
Выявлены дефекты гуморального звена противовирусной защиты, предрасполагающие к более тяжелым ассоциированным с hRV обострениям ХОБЛ. Пациенты, госпитализированные по поводу острого утяжеления респираторных симптомов этого заболевания, имели более низкие уровни специфических антител в сыворотке к hRV, чем пациенты с обострениями, тяжесть которых не требовала стационарного лечения [38].
Как один из возможных медиаторов индуцированных вирусами обострений ХОБЛ и БА привлекает внимание тимический стромальный лимфопоэтин (TSLP) — ИЛ-7-подобный проаллергический цитокин, продуцируемый главным образом эпителиоцитами и способный прямо или через дендритные клетки направлять дифференцировку незрелых посттимических Т-клеток-предшественников в направлении Тh2 [39]. Продемонстрирована гиперпродукция TSLP клетками респираторного эпителия больных ХОБЛ, но не здоровых доноров, в ответ на различные вирусные стимулы: инфицирование hRV, внесение в культуру клеток двуспиральной ДНК (агониста эндосомального рецептора ТLR3) или двуспиральной РНК (агониста цитозольных подобных RIG-I хеликаз) [40]. Способность индуцировать зависимую от RIG-I выработку TLSP описана и для RSV [41]. В культурах бронхиальных эпителиальных клеток двуспиральная РНК индуцировала большую экспрессию мРНК TSLP и продукцию соответствующего белкового продукта у больных ХОБЛ в сравнении с аналогичными культурами, изолированными у клинически здоровых курящих лиц. Установлено, что статины, в частности симвастатин, подавляют индуцированную вирусами продукцию TSLP респираторными эпителиоцитами [42]. Это и ретроспективные данные о способности статинов снижать летальность и частоту госпитализаций у больных ХОБЛ [43] подтверждают гипотезу об участии TSLP в патогенезе ассоциированных с ОРВИ обострений и определяют перспективное направление поиска средств предотвращения и снижения тяжести индуцированных вирусами эпизодов усугубления респираторных симптомов ХОБЛ. Вероятно, гиперпродукция TSLP у больных ХОБЛ связана с полиморфизмом гена этого цитокина, что продемонстрировано у пациентов с БА [44].
В целом бронхиальные эпителиальные клетки больных ХОБЛ характеризуются избыточным воспалительным ответом на инвазию hRV и некоторых других респираторных патогенов, выраженность которого не отражает эффективность противовирусной защиты. Чрезмерная продукция ИФН-β и ИФН-λ 1 , вызванная hRV в культуре бронхиальных эпителиоцитов больных ХОБЛ, усиливала апоптоз этих клеток, но не потенцировала подавление репликации вирусов по сравнению с таковыми у здоровых доноров. Установлен целый ряд генов, в том числе сигнальных белков pellino-1 и IRAK2 (киназы-2, ассоциированной с рецептором ИЛ-1), полиморфизм которых обусловливает гиперреактивность респираторного эпителия при ВИ [45].
Вероятнее всего, у больных с хроническими бронхолегочными заболеваниями базовый уровень выработки ИФН 1-го и 3-го типов действительно снижен, что является причиной высокой восприимчивости к ОРВИ, но при возникновении последних не дефицит, а, наоборот, избыточная продукция этих цитокинов провоцирует обострения БА и ХОБЛ. При возникновении РВИ у пациентов с БА именно уровень ИФН-α и ИФН-λ1, но не вирусная нагрузка, коррелировал с обострением этого заболевания. Следует отметить, что ИФН-λ 2/3 не имели такого патогенетического значения [46].
Еще одним механизмом индуцированных вирусами обострений ХОБЛ и БА может быть десенситизация β 2 -адренорецепторов гладких мышечных клеток дыхательных путей. Обнаружено, что заражение этих клеток hRV in vitro, а также внесение в культуральную среду РНК этого вируса или комбинации синтетических агонистов TLR3 и TLR7/8 (вирусных миметиков) приводили к зависимой от циклооксигеназы-2 индукции простагландинов и десенситизации β 2 -адренорецепторов [47]. Предположительно сходное влияние на чувствительность указанных рецепторов оказывают и некоторые другие Р.В. Благодаря этому возбудители ОРВИ могут не только непосредственно усугублять выраженность обструкции дыхательных путей у больных БА и ХОБЛ, но и снижать эффективность бронхолитических препаратов.
Весомый вклад в прогрессирование ХОБЛ и БА может вносить выявленная в моделях in vitro и in vivo способность hRV индуцировать ремоделирование дыхательных путей за счет усиления продукции экстрацеллюлярных матриксных протеинов бронхиальными эпителиоцитами и фибробластами паренхимы легких [48].
В экспериментах in vivo установлено, что повторные RSV-инфекции подверженных табачному дыму животных увеличивают миграцию в дыхательные пути макрофагов, нейтрофилов и лимфоцитов, потенцируют выработку цитокинов (ИФН-γ, ИЛ-1α, 17, 13, колониестимулирующего фактора гранулоцитов и макрофагов), хемокинов (KC, CXXL9, RANTES, MIF) и протеаз (матриксных металлопротеиназ MMP-2, 8, 12, 13, 16 и катепсинов E, S, W, Z). Кроме того, RSV и табачный дым синергично активировали апоптоз респираторного эпителия и подавляли экспрессию фосфатаз, оказывающих противовоспалительное и антипротеазное действие. В результате сочетание этих двух патогенных факторов приводило к выраженному фиброзу и ремоделированию дыхательных путей [49].
Заключение
Очевидно, что мишенями иммуномодулирующей терапии у больных ХОБЛ с индуцированными вирусами обострениями могут быть не только сами вирусы, ни и вторичные медиаторы индуцируемых ими патогенетических событий. Так или иначе, роль возбудителей ОРВИ в обострениях ХОБЛ заслуживает большего внимания.
Читайте также:

