Острые респираторные вирусные инфекции в амбулаторной практике врача-педиатра
Обновлено: 17.04.2024
Острые респираторные инфекции (ОРИ) — это группа острых инфекционно-воспалительных заболеваний органов дыхания, развивающихся в результате аэрогенного инфицирования различными возбудителями (респираторными вирусами, бактериями, атипичными микроорганизмам
Вакцинопрофилактика ОРИ
В настоящее время не вызывает сомнений тот факт, что наиболее эффективным методом профилактики инфекционных заболеваний является активная специфическая иммунизация [8, 12]. Однако возможности вакцинопрофилактики респираторных инфекций существенно ограничены. Это обусловлено широким этиологическим спектром ОРИ (более 150 возбудителей), в то время как эффективные и безопасные вакцины разработаны лишь против нескольких респираторных патогенов, таких как вирус гриппа, гемофильная палочка (тип В) и пневмококк. Но, несмотря на столь ограниченный арсенал средств активной иммунизации против ОРИ, профилактический потенциал имеющихся вакцин должен быть использован максимально. Так противогриппозная вакцинация, широко проводимая в последние годы, позволила существенно уменьшить заболеваемость данной инфекцией среди привитых. При этом вводимая с 2006 г. обязательная противогриппозная иммунизация дошкольников и учеников 1–4 классов не только позволит снизить частоту гриппа среди вакцинированных, но и значительно ограничит распространение данной инфекции в организованных детских коллективах в целом [6].
Современные гриппозные вакцины являются тривакцинами, так как содержат штаммы (или их антигены) трех актуальных вирусов гриппа — А(Н1N1), A(H3N2) и В [8, 11, 12]. В России для иммунизации против гриппа у детей разрешены как живые, так и инактивированные вакцины (табл. 1). При этом живые вакцины используются только после достижения детьми 3-летнего возраста. Данный тип вакцин вводится интраназально — по 0,25 мл в каждый носовой ход, двукратно с интервалом 3–4 нед.
Среди инактивированных гриппозных вакцин различают цельновирионные, расщепленные и субъединичные. Цельновирионные вакцины содержат весь набор антигенов актуальных штаммов вируса гриппа. Иммуногенность цельновирионных вакцин высока, но из-за липидов вирусной оболочки, содержащихся в их составе, данные препараты более реактогенны. Цельновирионные гриппозные вакцины имеют существенные возрастные ограничения — их использование разрешено у детей старше 7 лет. Вакцины данного типа у детей вводятся только интраназально. При этом следует строго соблюдать рекомендованный режим дозирования — двукратное с интервалом 3–4 недели по 0,25 мл в каждый носовой ход. Следует отметить, что в последние годы цельновирионные гриппозные вакцины у детей используются редко.
Расщепленные гриппозные вакцины (сплит-вакцины) содержат поверхностные (гемагглютинин, нейраминидаза) и внутренние антигены, благодаря чему препараты характеризуются высокой иммуногенностью. При этом высокая степень очистки от реактогенных липидов определяет их хорошую переносимость. К расщепленным вакцинам относятся ваксигрип, бегривак, флюарикс. Большинство сплит-вакцин разрешены для использования у детей, начиная с 6-месячного возраста. Субъединичные гриппозные вакцины содержат только поверхностные антигены (гемагглютинин, нейраминидаза), что определяет хорошую иммуногенность и переносимость. К субъединичным вакцинам относятся гриппол, инфлювак, агриппал. Данные препараты, так же как и сплит-вакцины, разрешены для использования у детей с 6-месячного возраста. Следует отметить, что вакцинацию против гриппа необходимо проводить, строго придерживаясь международных рекомендаций по режиму дозирования. Так, иммунизация у детей первых 9 лет жизни, ранее не привитых и не болевших гриппом, должна проводиться двукратно с интервалом в 4 нед. При этом детям в возрасте от 6 мес до 3 лет 11 мес рекомендовано вводить по 0,25 мл вакцины, а начиная с 4-летнего возраста — по 0,5 мл.
Неспецифическая иммунопрофилактика и иммунотерапия ОРИ
Максимальное снижение заболеваемости ОРИ может быть достигнуто при сочетанном использовании вакцинации и средств неспецифической иммунопрофилактики (иммуномодуляторы). Для лечения и профилактики ОРИ в последние годы наиболее часто применяются такие иммуномодуляторы, как интерфероны, индукторы эндогенного интерферона и иммуномодуляторы бактериального происхождения. Кроме того, в комплексную систему неспецифической профилактики ОРИ входят фитоадаптогены с легким иммуномодулирующим эффектом (производные эхинации пурпурной, заманихи, корня солодки и т. д.) и поливитаминно-микроэлементные комплексы. Все реже в настоящее время используются препараты тимуса, а от введения с профилактической целью иммуноглобулинов (гамма-иммуноглобулинов) в последние годы отказались вообще.
Интерфероны. В течение нескольких десятилетий для лечения и профилактики респираторных инфекций у детей с успехом используются препараты интерферона, обладающие универсальным противовирусным эффектом. В результате воздействия интерферонов в клетках организма синтезируются ферменты, которые тормозят образование вирусных белков и разрушают вирусные рибонуклеиновые кислоты. Интерфероны также стимулируют экспрессию антигенов I и II классов главного комплекса гистосовместимости, что изменяет топографию клеточной мембраны, препятствует прикреплению вирусов к клеточной оболочке и нарушает их проникновение внутрь клеток. Кроме того, активизируя цитотоксическую активность Т-лимфоцитов, интерфероны стимулируют лизис клеток, инфицированных вирусами. Таким образом, интерфероны препятствуют вирусному инфицированию, а также подавляют репродукцию вирусов на стадии синтеза специфических белков [2, 7, 9]. Среди препаратов интерферона выделяют интерфероны природные (интерферон человеческий лейкоцитарный) и рекомбинатные (виферон, гриппферон и др.). При этом в последние годы для лечения и профилактики ОРИ все реже стали применять интерферон человеческий лейкоцитарный сухой и лейкинферон. В настоящее время предпочтение отдается рекомбинатным интерферонам (виферон, гриппферон). При этом наибольший опыт в педиатрической практике накоплен при использовании виферона — рекомбинатного интерферона α-2, обладающего также антиоксидантным эффектом за счет входящих в его состав витаминов С и Е. Наибольший терапевтический эффект от использования препаратов интерферона при лечении ОРИ достигается в тех случаях, когда этиология имеет вирусную или вирусно-бактериальную природу, а лечение начинается с первых часов заболевания [2, 7]. При этом включение данных препаратов в комплексную терапию ОРИ позволяет не только существенно уменьшить выраженность воспалительных процессов и продолжительность заболевания, но и снижает в целом риск развития осложнений.
Индукторы эндогенного интерферона. К химиотерапевтическим индукторам эндогенного интерферона относятся производные тилорона (амиксин), арбидол и циклоферон. Кроме того, эффектом усиления образования интерферона обладает анаферон — иммуномодулятор, содержащий сверхмалые дозы аффинно очищенных антител к гамма-интерферону человека. Имеются убедительные данные о профилактической и терапевтической эффективности данных лекарственных средств [2, 7, 9]. Следует отметить, что практически все представленные препараты не только индуцируют синтез эндогенного интерферона, но и обладают иммуномодулирующим эффектом (стимулируют фагоцитоз и клеточный иммунитет). При этом арбидол и амиксин оказывают также прямое ингибирующее действие на респираторные вирусы. При выборе конкретного препарата необходимо обращать внимание не только на его фармакологическую активность, но и на возрастные ограничения. Так анаферон разрешен к применению, начиная с 6-месячного возраста, арбидол может быть использован у детей старше 2 лет, в то время как амиксин и циклоферон имеют более жесткие возрастные ограничения [1, 10]. Циклоферон при этом разрешен у детей старше 4 лет, а амиксин (тилорон) — только у детей старше 7 лет. Особо следует подчеркнуть, что максимальная терапевтическая эффективность препаратов данного класса достигается в тех случаях, когда лечение начинается с первых часов заболевания.
Иммуномодуляторы бактериального происхождения в последние годы все шире используются для профилактики ОРИ, особенно у часто и длительно болеющих детей [3, 5, 7]. Терапевтическая эффективность и безопасность применяющихся у детей иммуномодуляторов бактериального происхождения подтверждена рядом контролируемых исследований. При этом различают следующие препараты: высокоочищенные бактериолизаты, мембранные фракции и рибосомально-протеогликановые комплексы. В свою очередь, среди высокоочищенных бактериолизатов выделяют препараты системного (бронхо-мунал, бронхо-ваксом) и топического действия (ирс 19, имудон). К препаратам, содержащим мембранные фракции бактериальной стенки, относится биостим, а также ликопид, в состав которого входит мурамилдипептид — синтетический аналог иммуноактивной части клеточной мембраны бактерий. Рибосомально-протеогликановые комплексы (рибомунил) содержат рибосомы определенных респираторных патогенов и мембранные факторы. В целом механизм действия всех иммуномодуляторов бактериального происхождения связан с их стимулирующим действием на фагоциты, повышением продукции интерферона и активацией естественных киллеров. Кроме того, ряд препаратов (бактериолизаты и рибосомально-протеогликановые комплексы) обладают легким вакцинирующим эффектом против тех возбудителей, антигены которых входят в их состав. При этом очень важно подчеркнуть, что благодаря этому поддерживается протекторная активность местного иммунитета (препараты потенцируют специфический иммунитет на слизистых). Учитывая тот факт, что в состав данных иммуномодуляторов входят антигены наиболее распространенных бактериальных возбудителей респираторных инфекций (пиогенный стрептококк, пневмококк, гемофильная палочка и т. д.), становится понятной их высокая профилактическая эффективность. Помимо этого, иммуномодуляторы бактериального происхождения обладают и терапевтическим эффектом, что позволяет назначать их короткими курсами во время ОРИ или при обострении хронических заболеваний ЛОР-органов. При этом отмечено, что данные препараты при одновременном использовании с антибиотиками потенцируют их антибактериальную активность. Установлено также, что иммуномодуляторы бактериального происхождения повышают иммуногенность вакцин, поэтому в последние годы, особенно у часто болеющих детей, плановую иммунизацию рекомендуют проводить на фоне приема данных препаратов [3, 7, 9].
В комплекс профилактических и терапевтических мероприятий при ОРИ может входить и назначение иммуномодуляторов растительного происхождения. Наиболее широко в последние годы в педиатрической практике стали использовать производные эхинацеи пурпурной (иммунал и др.). Эффективность препаратов эхинацеи пурпурной связывают с активацией неспецифического иммунитета. Иммунал назначают как для лечения неосложненных ОРИ (в течение 1 нед), так и для их профилактики (не более 8 нед). Иммунал (капли) назначают детям от 1 года до 4 лет — по 1 мл 3 раза в день, детям от 6 лет до 12 лет — по 1,5 мл 3 раза в день. При использовании иммунала в таблетках следует соблюдать следующий режим дозирования — детям от 4 до 6 лет — по 1 таблетке 1–2 раза в сутки, детям 6–1 2 лет — по 1 таблетке 1–3 раза в день [1, 10].
В последние годы иммуномодуляторы тимического происхождения, как природные (тималин, тактивин, тимоптин, тимактид, тимостимулин, вилозен), так и синтетические (тимоген) для профилактики и лечения ОРИ используются все реже. Это связано с тем, что корректное использование данных лекарственных средств требует предварительного иммунологического обследования и выявления убедительных данных о нарушении клеточного иммунитета. Иммуноглобулины, ранее широко используемые для профилактики и лечения ОРИ у детей, в настоящее время также применяются только по специальным показаниям. Назначение при данных состояниях иммуноглобулинов может быть оправдано лишь в тех случаях, когда заболевание приобретает тяжелое и осложненное течение, либо развивается на фоне выраженного иммунодефицитного состояния (агаммаглобулинемия, комбинированные иммунодефициты, общая вариабельная иммунная недостаточность, приобретенные гипогаммаглобулинемии на фоне нефротического синдрома, энтеропатий, хронического лимфолейкоза и др.). Предпочтение при этом должно отдаваться препаратам иммуноглобулина, которые предназначены для внутривенного введения (интраглобин, пентаглобин и др.).
Таким образом, в настоящее время в арсенале врачей-педиатров имеются высокоэффективные средства специфической и неспецифической иммунопрофилактики, рациональное использование которых позволяет не только существенно снизить заболеваемость ОРИ у детей, но и сократить риск развития тяжелых и осложненных форм заболевания.
Литература
А. Л. Заплатников, доктор медицинских наук, профессор
РМАПО, Москва
Для цитирования: Заплатников, Коровина Н.А. Острые респираторные инфекции у детей: современные возможности этиотропной терапии. РМЖ. 2002;3:103.
Российская медицинская академия последипломного образования МЗ РФ, Москва
О стрые респираторные инфекции занимают ведущее место в структуре общей заболеваемости населения России [1]. При этом наибольшую актуальность проблема острых респираторных заболеваний (ОРЗ) приобретает в педиатрической практике [2]. Это обусловлено значительной распространенностью ОРЗ в детской популяции, а также высоким риском развития серьезных осложнений и значительным удельным весом этих инфекций в структуре смертности среди детей первых трех лет жизни [2, 3].
Этиотропная терапия ОРЗ вирусной этиологии
В последние годы в России арсенал врачей–педиатров пополнился новыми противовирусными препаратами, что существенно расширило возможности этиотропной терапии ОРВИ у детей [9, 10]. Среди лекарственных средств, обладающих противовирусным эффектом, различают препараты, воздействующие непосредственно на респираторные вирусы и/или на их ферменты (и др.), а также интерфероны и их индукторы. К противовирусным химиотерапевтическим лекарственным средствам, разрешенным для лечения ОРВИ у детей, относятся производные римантадина, рибавирина, тилорона, озельтамивир, арбидол (табл. 2). Некоторые из них (арбидол, амиксин), помимо прямого противовирусного действия, оказывают также иммуномодулирующий эффект – индукцируют синтез эндогенного интерферона, стимулируют фагоцитоз и Т–клеточное звено иммунитета. Характеризуя данную группу противовирусных лекарственных средств, следует отметить, что их применение имеет определенные возрастные ограничения, связанные как с недостаточно изученной безопасностью их применения у детей раннего возраста (арбидол, озельтамивир), так и с выраженными побочными эффектами при системном применении (рибавирин).
Производные римантадина (альгирем, ремантадин) ингибируют раннюю стадию специфической репродукции вируса гриппа, нарушают процессы передачи вирусного генетического материала в цитоплазму клетки, а также угнетают выход вирусных частиц из клетки. Применение римантандина ограничено теми формами гриппозной инфекции, которые вызваны вирусом гриппа типа А. При этом наибольший терапевтический эффект римантандина отмечается при лечении респираторных инфекций, обусловленных вирусом гриппа А2. Особо следует отметить, что римантадин снижает эффективность противоэпилептических препаратов и при этом может спровоцировать развитие эпилептического припадка. Снижение эффективности римантадина отмечается при одновременном приеме с адсорбентами, вяжущими и обволакивающими лекарственными средствами (за счет уменьшения всасывания римантадина), а также с аскорбиновой кислотой и другими препаратами, изменяющими рН мочи в кислую сторону (вследствие усиления его выведения почками).
Озельтамивир (тамифлю) является специфическим противогриппозным препаратом, который избирательно ингибирует нейраминидазу вируса гриппа типа А и В и, препятствуя выходу вирионов из инфицированной клетки, предотвращает дальнейшее распространение инфекции в организме. Частота резистентности к озельтамивиру среди клинических изолятов вируса гриппа не превышает 2% и не является клинической проблемой [9, 11]. Для достижения терапевтического эффекта при лечении гриппа озельтамивиром терапию препаратом необходимо начинать не позднее 48 часов от момента развития симптомов заболевания.
Арбидол – синтетический противовирусный препарат, способный также стимулировать синтез эндогенного интерферона, активизировать фагоцитоз и влиять на состояние Т–клеточного звена иммунитета [9]. Установлено, что арбидол специфически ингибирует вирусы гриппа А и В и повышает резистентность организма к другим респираторным вирусам. Арбидол относится к малотоксичным препаратам. При пероральном применении в рекомендуемых дозах не оказывает какого–либо отрицательного воздействия на детский организм. Отмечено, что арбидол не обладает мутагенным, канцерогенным, тератогенным и эмбриотоксическим действием [9]. Совместим с другими лекарственными препаратами.
К синтетическим противовирусным препаратам относится тилорон (амиксин), обладающий также иммуномодулирующей активностью. Отмечено, что под действием тилорона в организме повышается образование альфа–, бета– и гамма–интерферонов, стимулируется Т–клеточный иммунитет, а также повышается активность фагоцитов и естественных киллеров [9]. В контролируемом исследовании установлено, что применение амиксина при неосложненных формах гриппа и ОРВИ у детей сопровождалось достоверным сокращением продолжительности периода интоксикации и катаральных проявлений. У детей с осложненным течением ОРВИ включение амиксина в комплексную терапию позволило сократить сроки выздоровления в 2 раза по сравнению с контрольной группой (р<0,001) [12]. Авторы особо подчеркивают хорошую переносимость и безопасность препарата. Следует также отметить, что тилорон (амиксин) может применяться одновременно с антибиотиками и симптоматическими лекарственными средствами, традиционно используемыми для лечения вирусных и бактериальных заболеваний органов дыхания.
В основе противовирусного действия рибавирина лежит конкурентное ингибирование его метаболитами вирусной дегидрогеназы инозинмонофосфата, что тормозит синтез вирусных ДНК и РНК. Показана активность препарата против вирусов гриппа А и В, РС–вирусов, а также герпес–вирусов. Однако в педиатрической практике из–за высокой токсичности препарат используется только в виде ингаляций через небулайзер при тяжелых поражениях органов дыхания (бронхиолит, пневмония), вызванных РС–вирусом. При этом в связи с высоким риском развития серьезных побочных эффектов (бронхоспазм, брадикардия, остановка сердца и дыхания) рибавирин может применяться только в условиях реанимационного отделения.
В педиатрической практике для лечения и профилактики респираторных инфекций часто и с высокой эффективностью используются препараты интерферона, обладающие универсальным неспецифическим антивирусным эффектом [13]. При этом противовирусная активность интерферона не связана с непосредственным воздействием на вирион, а является следствием изменения обменных процессов на клеточном уровне. Интерфероны вызывают значительные физико–химические и структурные изменения в клеточной мембране, повышая экспрессию антигенов I и II классов главного комплекса гистосовместимости, что изменяет топографию мембраны, приводит к нарушению прикрепления вирусов к клеточной оболочке и препятствует их пенетрации. Активизируя цитотоксическую активность Т–лимфоцитов, интерфероны стимулируют лизис клеток, инфицированых вирусом. Кроме этого, под воздействием интерферонов в клетке синтезируются ферменты, тормозящие синтез вирусных белков и расщепляющие вирусные РНК. Таким образом, интерфероны препятствуют инфицированию вирусами незараженных клеток, а также подавляют их репродукцию на стадии синтеза вирусоспецифических белков [13]. Среди препаратов интерферона выделяют интерфероны природные (интерферон человеческий лейкоцитарный, лейкинферон) и рекомбинатные (виферон, гриппферон и др.) (табл. 3). В последние годы все чаще предпочтение отдается рекомбинатным интерферонам. При этом наибольший опыт в педиатрической практике накоплен при использовании виферона – рекомбинатного a –2b–интерферона, обладающего также антиоксидантным эффектом за счет входящих в его состав витаминов С и Е. Отмечено, что включение виферона в комплексную терапию гриппа и ОРВИ сопровождалось сокращением периода лихорадки, уменьшением выраженности и длительности интоксикации и катаральных изменений, а также снижением частоты суперинфекции и развития осложнений (p<0,05) [14].
К системным индукторам эндогенного интерферона относят циклоферон и криданимод (неовир). Следует отметить, что в настоящее время нет убедительных данных о безопасности этих препаратов для детей, что ограничивает их широкое применение в педиатрической практике. Кроме указанных лекарственных средств, эффектом стимуляции синтеза эндогенного интерферона и активизации натуральных киллеров обладает также мукозональная вакцина бактериального происхождения рибомунил, что позволяет активно использовать его при лечении гриппа и других ОРВИ [2].
Учитывая, что большинство химиотерапевтических противовирусных препаратов обладают существенными побочными эффектами, их использование у детей оправдано лишь при тяжелом, осложненном течении ОРВИ, либо в тех случаях, когда респираторную инфекцию переносят дети с иммунодефицитами, хроническими соматическими и/ил неврологическими заболеваниями и др. При этом своевременное уточнение этиологии заболевания позволяет целенаправленно назначить этиотропный противовирусный препарат, например, римантадин – при гриппе А2, рибавирин – при РС–инфекции. В тех случаях, когда у детей не удается верифицировать этиологию тяжело протекающего ОРВИ, предпочтительнее использовать те лекарственные средства, которые обладают комбинированным – противовирусным и иммуномодулирующим эффектами (арбидол, тилорон, рибомунил, виферон).
На этиотропной терапии бактериальных и вирусно–бактериальных ОРЗ мы остановимся во второй части статьи в одном из следующих номеров Русского медицинского журнала.
1. Шаханина И.Л. Грипп и острые респираторные заболевания – приоритетная социально–экономическая проблема здравоохранения / Вакцинопрофилактика гриппа. – М., 1998. – С. 10–16.
2. Острые респираторные заболевания у детей: лечение и профилактика / Научно–практическая программа Союза педиатров России. – М.: Международный Фонд охраны здоровья матери и ребенка, 2002. – 69 с.
3. Маринич И.Г., Тимошенко О.Ф., Игнатьева Г.С., Морозов И.В. Летальность от гриппа, других острых респираторных заболеваний и острой пневмонии в Санкт–Петербурге. Вакцинация. – 1999, 5: 4–5.
4. Антибактериальная терапия стрептококкового тонзиллита и фарингита (Под ред. Н.А.Насонова, Б.С.Белов, Л.С.Страчунский и др.) / Рекомендовано комиссией по антибиотической политике при МЗ РФ и РАМН, Межрегиональной ассоциацией по клинической микробиологии и антимикробной химиотерапии, Институтом ревматологии РАМН. – Клиническая микробиология и антимикробная терапия. – 1999. – №1. – С. 78–82.
5. Антибактериальная терапия пневмонии у детей (Под ред. В.К.Таточенко, Е.В.Середа, А.М.Федоров и др.) / Рекомендовано комиссией по антибиотической политике при МЗ РФ и РАМН. – Клиническая микробиология и антимикробная терапия. – 2000. – №1. – С. 77–84.
6. Рачинский С.В., Таточенко В.К. (ред). Болезни органов дыхания у детей: Руководство для врачей – М.: Медицина, 1987.
7. Red Book: 1994. Report of the Committee on Infection Diseases. 23rd: American Academy of Pediatrics, 1994, 687 p.
8. Учайкин В.Ф. Руководство по инфекционным заболеваниям у детей. – М.: Гэотар Медицина, 1998. – 700 с.
10. Федеральное руководство для врачей по использованию лекарственных средств (формулярная система): М., МЗ РФ: Выпуск 1, 2000.
11. Winquist A.G., Fukuda K., Bringes C.B. et al. Neuraminidase inhibitors for treatment of Influenza A and B infections. – MMWR, 1999, 48 (14): 1–9.
12. Учайкин В.Ф., Чешик С.Г., Балаболкин И.И. Терапевтическая эффективность и безопасность амиксина при гриппе и других респираторных вирусных инфекциях у детей. – РМЖ. – 2001. – Том 9, № 19. – С. 5–7.
13. Ершов Ф.И. Система интерферона в норме и патологии. – М.: Медицина, 1996.
14. Чеботарева Т.А., Тимина В.П., Малиновская В.В., Павлова Л.А. Применение Виферона при гриппе и других острых респираторных вирусных инфекциях у детей// Детский доктор. – 2000. – №5. – С. 16 – 18.
15. Коровина Н.А., Заплатников А.Л., Захарова И.Н. Антибактериальная терапия респираторных заболеваний в амбулаторной практике врача–педиатра. – М.: Медпрактика, 2000. – 57 с.
Для цитирования: Усенко Д.В., Горелова Е.А., Каннер Е.В. Рациональный подход к терапии ОРВИ и гриппа в клинической практике врача-педиатра. РМЖ. 2015;3:174.
ОРВИ по заболеваемости и распространенности занимают лидирующие позиции среди всех инфекций у взрослых и детей, являются самым частым поводом для обращения к врачу и в аптечные учреждения, самолечения.
Согласно официальной статистике, в России ежегодно регистрируют до 30–60 млн и более случаев ОРВИ, более половины из них — у детей. Заболеваемость ОРВИ не имеет тенденции к снижению, растет во всех возрастных группах, несмотря на значительные успехи фармакологии и фармакотерапии [1, 2]. Ситуация осложняется еще и тем, что в последнее время врачам все чаще приходится иметь дело с ее осложненными вариантами — . Таким образом, вопросы эффективной терапии и профилактики ОРВИ не теряют своей актуальности.
Ежегодно, по данным ВОЗ, дети в среднем переносят от 5 до 8 острых заболеваний верхних дыхательных путей, большей частью легкого течения [3]. Столь частые заболевания респираторного тракта объясняются многообразием этиологических факторов и высокой контагиозностью респираторных вирусов [4].
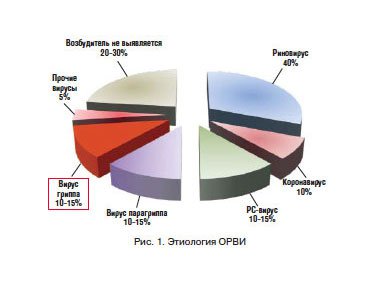
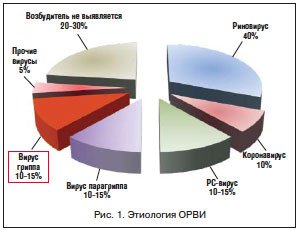
ОРЗ включают в себя инфекции, вызываемые как вирусами, в основном респираторными, так и пневмотропными бактериями, нередко вегетирующими в дыхательных путях [5]. Общее число вирусов и их серотипов, вызывающих ОРЗ, достигает 200, и на их долю приходится 95% всех случаев поражений дыхательных путей у детей. Вирусами гриппа вызываются только 10–15% заболеваний (рис. 1).
Вирусные инфекции нередко осложняются бактериальной инфекцией, обостряют течение хронических заболеваний, представляют серьезную угрозу здоровью ребенка [6, 7]. У 70–80% детей, особенно младшего возраста, в воспалительный процесс вовлекаются : околоносовые пазухи, среднее ухо, трахея, бронхи, следствием чего могут быть поражения глазной орбиты и мозговых оболочек. Поэтому начинать рациональное лечение необходимо уже в первые часы заболевания [8–10].
Ежегодная высокая заболеваемость острыми респираторными инфекциями и гриппом, риск осложнений, постоянно меняющаяся мозаика возбудителей, а также наносимый этими инфекциями экономический и социальный ущерб делают разработку и внедрение в практику эффективных способов профилактики гриппа и острых респираторных инфекций приоритетными задачами современной медицины [2, 11, 12].
Несомненно, наиболее эффективной является специфическая профилактика, применяемая в отношении вирусов гриппа. Доказано, что своевременно проведенная вакцинация способна защитить от гриппа до 80% взрослых и детей [11, 13–15]. Разработка специфических вакцин против всего спектра возбудителей ОРВИ нецелесообразна огромного многообразия серотипов респираторных вирусов и их ежегодно изменяющегося соотношения в структуре заболеваемости на разных континентах, в различных странах и городах. Осложняет ситуацию наблюдающаяся в последние годы резистентность ряда респираторных вирусов к химиопрепаратам, одной из причин которой является нерациональная фармакотерапия [16].
Помимо того, практическим врачам известно, что в ряде случаев существуют объективные причины, не позволяющие достичь оптимального соотношения вакцинированных людей в популяции, что снижает индекс защищенности от вируса гриппа [8, 15, 17]:
- абсолютные и относительные противопоказания к назначению вакцин (коморбидные заболевания, аллергия к белковым компонентам вакцин, обострение хронических воспалительных процессов, неоплазии и др.);
- запаздывание производства необходимого количества вакцинных препаратов к началу эпидсезона;
- появление новых типов и серотипов вирусов;
- немотивированный отказ взрослых людей и родителей детей от проведения вакцинации.
- Поэтому вполне понятен и обоснован интерес медиков различных стран к неспецифическим средствам профилактики гриппа и ОРВИ.
Экспертами ВОЗ подчеркивается важность выполнения простых и доступных общегигиенических рекомендаций: проветривание помещений, полноценное питание, прием комплексов, закаливание, мытье рук, использование масок при общении с больными, ограничение посещения мест большого скопления людей в периоды эпидемии и др. [11–13, 18].
Таким образом, поиск и внедрение лекарственных средств для профилактики и лечения ОРВИ продолжаются и относятся к числу приоритетных задач клинической педиатрии. Выбор рациональной фармакотерапии различных ОРВИ, в первую очередь гриппа, а также оптимальной схемы и длительности лечения — актуальная проблема медицины на протяжении многих десятилетий и постоянная тема для дискуссий в медицинском сообществе.
Спектр лекарственных средств, применяемых пациентами для лечения и профилактики гриппа и ОРВИ как по рекомендации врача, так и самостоятельно, весьма разнообразен. Но какие из этих лекарств действительно приносят пользу?
На сегодняшний день не вызывает сомнения целесообразность раннего применения при гриппе этиотропной противовирусной терапии, особенно при наличии риска развития осложнений. Это единственная группа препаратов, рекомендации по применению которых при гриппе основаны на результатах международных рандомизированных контролируемых клинических исследований. К ним относятся рекомендуемые ВОЗ препараты осельтамивир и занамивир. Эти препараты продемонстрировали высокую эффективность при начале лечения в первые 48 ч заболевания. Однако в реальной практике пациент обращается к врачу только на 3–4 сут, когда характер и тяжесть симптомов не оставляют сомнений в том, что он болен гриппом. Для профилактики гриппа в связи с высокой частотой развития резистентности ВОЗ не рекомендует применять осельтамивир. Поэтому ключевым показанием к назначению осельтамивира является грипп, верифицированный в первые 2 сут от начала заболевания, особенно у пациентов из группы риска.
Грипп и другие ОРВИ часто являются поводом для полипрагмазии и нерационального использования лекарственных средств. Для облегчения симптомов заболевания родители по рекомендации врача или самостоятельно прибегают к применению симптоматических препаратов, например, жаропонижающих, обезболивающих, муколитических, противоотечных, сосудосуживающих назальных капель Результаты клинических испытаний показали, что их использование в ряде случаев может облегчить течение заболевания, но не оказывает существенного влияния на его исходы [20–23]. Клиническая эффективность адаптогенов, общеукрепляющих средств, традиционно популярных среди населения, не доказана, и применение их при ОРВИ нецелесообразно.
Данные Кокрейновских систематических обзоров и клинических руководств говорят о том, что антибиотики, также часто применяемые при ОРВИ, не только не улучшают исходы заболевания, но и могут привести к таким неблагоприятным последствиям, как удлинение сроков выздоровления, повышение частоты нежелательных лекарственных реакций и рост антибиотикорезистентности [20, 24, 25].
Данные клинических и фармакоэпидемиологических исследований убедительно показали нецелесообразность применения антигистаминных препаратов, которые также не только не улучшают исходы ОРВИ, но и достаточно часто приводят к нежелательным лекарственным реакциям [21].
Число лекарств, предлагаемых для лечения и профилактики ОРВИ и гриппа, с каждым годом увеличивается. Проблемами противовирусной терапии являются снижение эффективности лечения при позднем начале приема препарата, возрастные ограничения, узкая специфичность и снижение эффективности ряда лекарственных средств за счет роста резистентности, отсутствие устойчивой доказательной базы по целому ряду препаратов, токсичность большинства препаратов, низкая комплаентность. Кроме того, при назначении индукторов интерферона необходимо учитывать, что концентрация интерферонов в сыворотке крови у больных ОРВИ в разгар заболевания существенно повышается, сам вирус является мощным интерфероногеном, а дополнительная искусственная стимуляция выработки интерферонов чревата срывом компенсаторных возможностей иммунной системы организма.
В этом аспекте определенный интерес вызывают гомеопатические этиотропные лекарственные средства для лечения респираторных вирусных инфекций, которые практически не имеют противопоказаний и возрастных ограничений, лишены побочных эффектов и могут использоваться в комплексе с другими препаратами [26]. Несомненным достоинством гомеопатических средств является возможность их длительного приема на фоне терапии сопутствующей патологии.
Развитие данного метода лечения обусловило отход от традиции отказа от использования параллельно аллопатических препаратов и создание комплексных гомеопатических лекарств. Эти препараты являются безрецептурными, их могут применять врачи любых специальностей, не владеющие основами гомеопатии. Различные формы таких препаратов — таблетки, гранулы, сиропы, мази — не вызывают сложностей в определении дозировки и сроков лечения и широко используются во всех возрастных группах без ограничения, и в период эпидемических подъемов ОРВИ, особенно гриппа [27, 28].
Эффективность Оциллококцинума в лечении гриппа и ОРВИ известна на протяжении более полувека. Препарат продается в более чем 50 странах, особенно он популярен во Франции, где производится около 70 лет и является самым продаваемым в стране безрецептурным средством против гриппа. В США объемы продажи лекарства достигают 15 млн долларов в год. В России Оциллококцинум рекомендован в качестве лекарственного средства для профилактики и лечения гриппа и вирусных респираторных заболеваний [30–34]. Показания к применению определены как грипп и простудные заболевания, противопоказанием является только повышенная индивидуальная чувствительность к отдельным компонентам препарата.
Оциллококцинум рекомендовано принимать за 15 мин до приема пищи или через 1 ч после него, средство необходимо держать во рту до полного растворения. В начальной стадии заболевания следует как можно раньше принять 1 дозу препарата, затем при необходимости повторить 2–3 раза с интервалом 6 ч. В более поздние сроки рекомендован прием по 1 дозе утром и вечером в течение 1–3 дней. Желательно начинать лечение как можно раньше, при появлении первых проявлений простуды, в этом случае использование препарата наиболее эффективно. При нарастании симптомов в течение суток на фоне использования Оциллококцинума и при значительно выраженной интоксикации следует обратиться к врачу. Препарат может быть использован пациентами любого возраста, беременными и кормящими женщинами. Дозировка Оциллококцинума определяется только стадией заболевания и целью назначения. Оциллококцинум может применяться для профилактики в период распространения ОРВИ и гриппа, в этом случае рекомендуется принимать 1 дозу в неделю.
Явные преимущества препарата подтверждены данными, полученными при проведении многочисленных клинических наблюдений во многих странах мира.
В многоцентровом рандомизированном исследовании, выполненном во Франции, эффективность Оциллококцинума оценивалась при лечении 300 больных гриппом. Пациенты основной группы при появлении первых симптомов заболевания (озноб, ломота, высокая температура тела) принимали Оциллококцинум в течение 3–4 дней до исчезновения симптомов. Пациентам контрольной группы назначали плацебо. Температура тела, примерно одинаковая в обеих группах больных до начала лечения, быстрее снижалась у пациентов, получавших Оциллококцинум, и нормализовалась к 4 дню. Озноб, исходно имевший место в обеих группах, исчез к 4 дню у 55% больных, принимавших активный препарат, и только у 26,5% пациентов, получавших плацебо [28].
В другом исследовании, проведенном в Германии в период эпидемического подъема ОРВИ с осени 1990 до весны 1991 г., также оценивалась эффективность применения Оциллококцинума для лечения гриппа. При этом 188 пациентов (93 женщины и 95 мужчин, средний возраст — 35,1±12,7 года) получали Оциллококцинум, а 184 (88 женщин и 96 мужчин, средний возраст — 34,9±12,1 года) — плацебо. Оценка состояния больных проводилась в начале лечения, через 2 сут и в период с по день. Дважды в день измерялась температура тела, регистрировались изменения 9 симптомов (кашель, насморк, мышечные боли, боли в горле и др.). Кроме того, регистрировалось возможное использование других лекарственных средств [35]. Препарат признавался эффективным, если число пациентов из принимавшей его группы, у которых все гриппоподобные симптомы исчезали в течение первых 2 сут, превышало число выздоровевших пациентов из группы плацебо, и/или если период полного выздоровления был менее продолжительным при использовании Оциллококцинума, чем при приеме плацебо. У всех пациентов регистрировались точность, с которой они следовали всем необходимым предписаниям, полнота и регулярность заполнения анкет и развитие побочных явлений. В результате нарушения условий протокола 21 пациент из основной группы и 17 из контрольной были выведены из исследования. Таким образом, в каждой из групп оценивалось состояние 167 пациентов.
Результаты исследования подтвердили эффективность Оциллококцинума в лечении гриппа и показали, что в течение первых 2 сут у 19,2% лиц, принимавших препарат, симптомы гриппа исчезли полностью, и они смогли полноценно трудиться. На 5 сут некоторые симптомы гриппа оставались у 26,4% лиц основной группы и 32,3% контрольной. Через 7–10 дней после начала лечения у 133 (80,1%) пациентов, принимавших Оциллококцинум, симптомов гриппа не наблюдалось. В группе, получавшей плацебо, к этому сроку выздоровели 128 (76,6%) человек.
Авторы особо подчеркивают положительное действие препарата на тяжесть течения заболевания. Через 2 сут после начала лечения значительное улучшение состояния отмечали 43,7% больных, принимавших Оциллококцинум, и 33,5% из группы плацебо. В контрольной группе к этому моменту у 5,4% пациентов отмечено ухудшение состояния, связанное, , с присоединением вторичной инфекции, которое потребовало дополнительных лечебных мероприятий.
Пациенты, принимавшие плацебо, в 1,5 раза чаще по сравнению с основной группой прибегали к применению сопутствующих лекарственных средств (анальгетиков, отхаркивающих, противокашлевых препаратов и др.). Исследователи отметили, что процент работоспособных пациентов в группе активного лечения был несколько выше, чем в группе плацебо: соответственно 16,3 и 9,2% — через 2 дня после начала лечения и 48,9 и 46,7% — через 4 дня. У 5 пациентов, участвовавших в этом исследовании, наблюдались нежелательные явления. Согласно заключению авторов, у 4 из них они не были связаны с действием исследуемого препарата. У 1 пациента отмечалась головная боль, связанная, возможно, с его приемом.
Таким образом, применение Оциллококцинума способствует более быстрому купированию клинических симптомов гриппа и сокращает продолжительность заболевания.
В России и соавт. подтвердили высокую эффективность препарата в нескольких исследованиях, проведенных у медицинского персонала (2006) и у молодых людей в возрасте от 16 до 22 лет (2007) [17].
Высокая эффективность и безопасность Оциллококцинума в лечении и профилактике респираторных вирусных инфекций подтверждены в многочисленных отечественных и зарубежных исследованиях. Несмотря на множество вопросов о противовирусном механизме действия гомеопатических препаратов, эффективность Оциллококцинума показана в клинических исследованиях, с использованием плацебо.
Воздействуя на организм на и электромагнитном уровне, индивидуальном для данного вещества, гомеопатический препарат Оциллококцинум не имеет побочных эффектов, работает тонко, избирательно, не перегружая организм. Результаты приведенных наблюдений позволяют сделать вывод об эффективности гомеопатического препарата Оциллококцинум в лечении ОРВИ и гриппа.
Оциллококцинум хорошо переносится, может быть использован как средство монотерапии при ОРВИ и гриппе. Отсутствие побочных эффектов и ограничений в сроках начала лечения и по возрасту позволяет рекомендовать данное средство к широкому использованию для лечения ОРВИ в амбулаторной практике. Применение Оциллококцинума в качестве профилактического средства позволяет снизить уровень заболеваемости и риск формирования патологии у детей.
Резюме. В статье представлена эпидемиология острых респираторных вирусных инфекций (ОРВИ) у детей, описаны вопросы их дифференциальной диагностики. Освещены общие принципы терапии респираторных инфекций, показания для госпитализации пациентов. Представлен механизм действия раннего индуктора интерферона 1-го и 2-го типов -Циклоферона, описаны его интерферониндуцирующее, иммунотропное, противовирусное действия. Охарактеризовано влияние Циклоферона на продукцию цитокинов. Описаны фармакокинетика препарата, его переносимость, безопасность, режимы дозирования, возможность применения совместно с другими препаратами. Описаны роль Циклоферона в повышении неспецифической резистентности организма, а также возможность его применения для экстренной профилактики острых респираторных вирусных инфекций.
Ключевые слова: респираторные вирусные инфекции, цитокины, иммунный ответ, интерфероны, индукторы интерферонов, лечение ОРВИ, дети, Циклоферон ®
Summary. The article presents the epidemiology of respiratory viral infections (ARVI) in children, describes the issues of their differential diagnosis. General principles of treatment of respiratory infections, indications for hospitalization of patients are highlighted. The mechanism of action of an early inducer of interferon types 1 and 2 - Cycloferon ® is presented. Its interferon-inducing, immunotropic, and antiviral effects are described. The effect of Cycloferon ® on cytokine production is characterized. The pharmacokinetics of the drug, its tolerability, safety, dosage regimens, and the possibility of using it in conjunction with other drugs are described. The role of Cycloferon ® in increasing non-specific resistance of the body is described, as well as the possibility of its use for emergency prevention of acute respiratory viral infections.
Key words: respiratory viral infections, cytokines, immune response, interferons, interferon inducers, ARVI treatment, children, Cycloferon ®
Острые респираторные вирусные инфекции (ОРВИ) - это группа инфекционных заболеваний, которые вызываются респираторными вирусами, передающимися воздушно-капельным путем, и протекают с поражением дыхательной системы.
Распространение ОРВИ определяется социально-экономической и миграционной ситуацией, экологической обстановкой. Особо активному распространению вирусных инфекций у детей способствуют пребывание в тесных организованных коллективах (детские сады, школы), отсутствие навыков личной гигиены, затруднение в интерпретации ребенком собственного состояния, а также чрезвычайная сложность распознавания инфекционного процесса в инкубационном и продромальном периодах.
Острые респираторные инфекции неизменно занимают ведущее место в структуре инфекционной патологии среди детей. В Российской Федерации ежегодно регистрируется примерно 70-80 тыс. заболеваний на 100 тыс. населения данного возраста (примерно в 3,3 раза выше, чем у взрослых) без тенденции к снижению, при этом встречаемость гриппа во время сезонного подъема заболеваемости наблюдается не всегда чаще, а иногда и реже, чем ОРВИ другой этиологии в сумме, что объяснимо повышением охвата детского населения вакцинопрофилактикой гриппа [1, 2].
ОРВИ протекают с разной степенью тяжести и обусловлены более 150 вирусами, принадлежащими как минимум к 7 семействам: ортомиксовирусы (род инфлюенцавирусов - грипп типа А, В, С), парамиксовирусы (корь, эпидемический паротит, парагрипп, респираторно-синцитиальный вирус человека, респировирусы, рубулавирусы - парагрипп), пикорнавирусы (энтеровирусы, риновирусы), коронавирусы (альфа- и бета-коронавирусы), реовирусы (ротавирусы А-Е, ортореовирусы), парвовирусы, аденовирусы [1, 2].
Таблица. Дифференциальная диагностика ОРВИ различной этиологии
| Признаки | Группы вирусов | |||||
| Грипп | Парагрипп | РСВ | Аденовирус | Корона-вирус | Реовирус | |
| Преимущественный сезон | Зима | Осень-зима | Зима-весна | Осень-зима-весна | Осень-зима-весна | Круглый год |
| Наиболее восприимчивый возраст | Школьный | 2-3 года | Новорожденные, дети до 2 лет | Любой | Любой | 6 мес.-3 года |
| Выраженность и длительность интоксикации, дни | ++++/+++ | ++/+ 2-5 | + 2-5 | +++/++ 5-12 | +++/++ 2-5 | + 2-5 |
| Температура тела,°C | > 39,0 | 37,0-38,0 | >38,0 | >38,0 | ||
| Катаральные проявления | Кашель, умеренный ринит, фарингит, трахеит | Выраженный ринит, ларинготрахеит | Умеренный фарингит, >50% - бронхит, бронхиолит, пневмония | Выраженный ринит, тонзиллит, ларингит, трахеит, конъюнктивит | Ринит, фарингит, бронхит, в 30% -пневмония | Ринит, фарингит |
| Желудочно-кишечные нарушения | +/- | - | - | +/- | +/- | + |
| Острота течения | Острое | Острое | Острое и затяжное | Затяжное, волнообразное | Острое | Острое |
Несмотря на общие входные ворота при ОРВИ любой этиологии (слизистая оболочка носовых ходов и носоглотки) с обязательным развитием локального воспаления (ринит, фарингит), эти инфекции отличаются значительным полиморфизмом клинической симптоматики и отсутствием, кроме вирусов гриппа, чувствительности к противогриппозным препаратам (ингибиторам нейраминидазы) (таблица). Доказано, что выраженность и быстрота развития клинических проявлений, а также тяжесть течения ОРВИ и частота развития осложнений обусловлены как патогенностью возбудителя, так и активностью факторов защиты пациента.
Дети с легкими и среднетяжелыми формами ОРВИ лечатся в основном амбулаторно. Госпитализации подлежат больные с тяжелыми и осложненными формами заболевания, новорожденные и дети первых лет жизни со среднетяжелыми формами болезни, но с осложненным течением, обострением сопутствующих заболеваний, а также пациенты из закрытых учебных заведений или проживающие в неблагоприятных бытовых условиях. При подозрении на тяжелый острый респираторный синдром (ТОРС), если пациент прибыл из стран Восточной, Юго-Восточной Азии, Ближнего Востока, независимо от тяжести процесса он должен быть госпитализирован в бокс [3, 7].
Диета ребенка, больного ОРВИ, должна быть полноценной, богатой витаминами, содержать достаточное количество жидкости (вода, чай с лимоном, соки, отвары плодов и ягод: шиповника, малины, черной смородины, земляники, клюквы, брусники). Желательно, чтобы пища была легкоусвояемой.
Лечение легких форм респираторных инфекций у детей, как правило, симптоматическое: обильное теплое питье, промывание слизистых оболочек носа и ротоглотки. Однако при выраженной клинической симптоматике, наличии осложнений и сопутствующей коморбидной патологии могут быть использованы различные группы лекарственных средств.
Препаратов, обладающих специфической противовирусной активностью по отношению к возбудителям ОРВИ, немного. Это блокаторы ионных каналов: римантадин, его полимерное производное римантадин + альгинат натрия; ингибиторы нейраминидазы - осельтамивир и занамивир, ингибитор слияния - умифеновир, аналоги нуклеозидов широкого спектра действия (рибавирин и инозин пранобекс). Их применение в детском возрасте ограничено несколькими факторами: в настоящее время регистрируется резистентность вирусов к римантадину, прием осельтамивира при гриппе эффективен только при условии применения в первые 48 ч заболевания, неэффективен в случае ОРВИ другой этиологии, а также имеет высокую стоимость. Занамивир применяется в виде ингаляций, эффективен только при гриппе, а также противопоказан детям до 5 лет, лицам с бронхиальной астмой и при наличии бронхообструкции, так как у лиц с осложненным преморбидным фоном может сам провоцировать ее развитие [2, 5, 9-10].
Один из важных направлений формирования полноценного иммунного ответа - регуляция синтеза IFN-g Т-хелперами. Циклоферон ® является ранним индуктором смешанного Th1 и Th-2 типа иммунного ответа. Индукторы IFN часто применяются как корректоры сдвигов иммунного ответа. Введение Циклоферона ® приводит к существенным изменениям в составе субпопуляций лимфоцитов (повышается относительное и абсолютное число исходно сниженных общих Т-лимфоцитов (CD3+), Т-хелперов (CD4+), иммунорегуляторного индекса и естественных киллеров (CD16+); снижается количество CD8+ и СD72+-лимфоцитов). Повышается уровень иммуноглобулина А (IgA) при одновременном снижении концентрации иммуноглобулина Е (IgE). Циклоферон ® увеличивает провоспалительный потенциал нейтрофилов периферической крови, а также функциональную активность фагоцитирующих клеток за счет генерации активных форм кислорода, обеспечивая бактерицидность клеток.
Циклоферон ® занимает достойное место при лечении заболеваний дыхательных путей у детей (ОРВИ, грипп, бронхит), уменьшая интоксикацию, катаральные симптомы, нормализуя температуру тела без применения антибактериальных препаратов, оказывая местный цитопротекторный эффект 11.
Препарат быстро проникает в кровь, а также через гематоэнцефалический барьер. С альбуминами плазмы крови молекулы Циклоферона ® почти не связываются, печенью не метаболизируются, и в течение 24 ч 99% введенной дозы препарата выводится почками в неизмененном виде. При этом индукция эндогенного IFN организмом начинается уже через 2-3 ч после введения. Через 4 ч после однократного введения наблюдается пик концентрации эндогенного IFN в крови, а его терапевтические концентрации могут сохраняться до 72 ч. Циклоферон ® отличается широким спектром профилактического и терапевтического действия при ОРВИ, поскольку проявляет интерферониндуцирующее, противовоспалительное и иммуномодулирующее свойства. Кроме того, он действует не только на возбудителей гриппа и ОРВИ, но и на цитомегаловирус, а также на вирус простого герпеса, тем самым препятствуя обострению хронических латентных инфекций. При этом препарат не отличается аллергенностью, не дает мутагенный, тератогенный, канцерогенный, эмбриотоксический эффекты. Циклоферон ® является препаратом с высокой безопасностью, его можно применять у детей и комбинировать с абсолютным большинством традиционных лекарственных препаратов 11.
В последние годы в Российской Федерации наблюдается рост числа осложненных форм гриппа и ОРВИ, по всей видимости, обусловленный недостаточно широким охватом вакцинацией от гриппа, пневмококковой, гемофильной инфекции, вирулентными свойствами возбудителей, а также сопутствующей инфицированностью вирусами герпетической группы. В случае осложненного течения респираторных инфекций назначаются антибактериальные препараты, а также индукторы IFN. Циклоферон ® можно применять одновременно с антибиотиками, витаминами, что снижает риск развития устойчивости микроорганизмов к препаратам. Комплексное лечение основного заболевания поможет быстрее выздороветь, избежать развития неприятных осложнений.
В исследованиях доказано, что прием Циклоферона ® в 94,8% случаев не сопровождался появлением каких-либо нежелательных реакций. В 4,4% случаев симптомы имели транзиторный характер и исчезали самопроизвольно, без отмены препарата. И лишь в 0,8% случаев выявленные реакции на препарат можно расценивать как непредвиденные [11].
Читайте также:

