От перитонита гепатит с
Обновлено: 22.04.2024
Острый вирусный гепатит С (ОВГС) представляет собой аитропонозную, широко распространенную вирусную инфекцию, близкую по эпидемиологическим характеристикам к ОВГВ.
Распространенность. В некоторых регионах мира вирусом гепатита С инфицировано до 5-10 % взрослого населения. Наблюдаемая в последние годы эпидемия гепатита С в России обусловлена резким ростом числа лиц, практикующих внутривенное введение наркотических препаратов. Распространение гепатита С естественными путями (от матери к плоду, половой путь) происходит гораздо менее интенсивно, чем HBV, так как концентрация вируса в крови, сперме и ДР) гих биологических субстратах существенно ниже.
Патогенез (что происходит?) во время Острого вирусного гепатита С:
Вирус гепатита С (HCV) имеет сферическую форму размером 50 нм.
Ген вируса представлен одноцепочечной линейной нитевой РНК протяженностью около 10 000 нуклеотидов. Отличительной особенностью его является генетическая неоднородность, обусловленная быстрой замещаемостью нуклеотидов.
Существует 6 генотипов и более 90 субтипов HCV и множественных вариантов вируса, обозначаемых как квазивиды. В Европе чаще встречаются 2-й и 3-й генотипы HCV, а в Северной Америке - 1-й. В России чаще всего выявляют генотипы lb и За. Генотипы 1 и 4 проявляют более высокую резистентность к терапии по сравнению с генотипами 2 и 3. В результате изменчивости HCV внутри одного генотипа образуется большое количество мутантных, генетически отличающихся друг от друга вариантов вируса, квазивидов HCV, циркулирующих в организме хозяина. С их наличием связывают ускользание вируса от иммунного ответа, длительную персистенцию HCV в организме, формирование хронического процесса, устойчивость к интерферонотерапии и возможность повторного заражения. Квазивиды - генетически близкородственные варианты одного и того же изолята HCV, возникающие в результате мутации в ходе репликации вируса в организме хозяина. Квазивиды могут быть причиной неспособности организма хозяина самостоятельно элиминировать возбудитель на ранней стадии.
В настоящее время вариабельность HCV рассматривается на трех уровнях: 1-й уровень составляют генотипы (гомология около 70 %); 2-й уровень - субтипы (гомология от 77 до 80 %); 3-й уровень - изоляты (гомология от 91 до 99 %), среди которых различают квазивиды.
Основным путем передачи ОВГС является парентеральный. Переливание зараженной крови и ее компонентов - наиболее частый классический путь передачи HCV, который в прошлом называли "пост-трансфузионным" гепатитом. Высокий риск заражения HCV имеют наркоманы, у которых часто выявляются микст-гепатиты (HCV + HBV + HDV). Возможно заражение больных, находящихся на диализе, и при трансплантации органов.
Непарентеральный путь инфицирования встречается значительно реже в силу низкой виремии. Контактно-бытовой и половой пути заражения не превышают 10 %. Вертикальный путь регистрируется значительно реже, чем при ОВГВ. Заражение через молоко кормящей матери с HCV-инфекцией представляет большую редкость. Наблюдение за беременными женщинами с ХВГС без перехода в далеко зашедший цирроз печени свидетельствует о том, что беременность у них протекает относительно спокойно и не ухудшает течение гепатита Имеются сведения о частой заболеваемости ОВГС людей, злоупотребляющих алкоголем. По данным К. П. Майера, HCV-инфекция регистрировалась у алкоголиков в 16 % случаев, что, по мнению автора, возможно связано со значительным снижением иммунных свойств организма. Довольно часто выявить источник заражения ОВГС не удается.
HCV относится к гепатотропным вирусам, и для развития заболевания необходимо проникновение возбудителя в печень. В настоящее емя доказано, что его репликация возможна вне печени, в частности клетках крови (мононуклеарах) и других органах, о чем свидетельствуют внепеченочные поражения. HCV может реплицироваться в лимфоидной ткани, причем различные квазивиды проявляют и различный тропизм по отношению к этим тканям - как invivo, так и invitro. В настоящее время не установлена зависимость тканевой тропности от структурных особенностей оболочечных белков вируса. Выявлена четкая связь между лимфотропизмом HCV и рядом лимфо-пролиферативных и аутоиммунных заболеваний. Именно поэтому хроническая HCV-инфекция должна рассматриваться не как заболевание печени, а как системный патологический процесс, в котором тканевый тропизм возбудителя является важнейшим фактором.
Отличительной особенностью патогенеза ОВГС от ОВГВ является отсутствие интеграции вируса HCV в геном инфицированных гепатоцитов и более слабое формирование гуморального иммунитета (антителообразование в низких титрах). В отличие от ВГВ антитела появляются поздно, уже после повышения активности АлАТ, а именно через 6-8 нед после инфицирования, и почти не обладают вируснейтрализу-ющим свойством. При ОВГВ HBcorAb IgM появляются рано, в инкубационном периоде, и обнаруживаются в высоких титрах еще до появления повышения активности АлАТ, оказывая выраженный вирус -нейтрализующий эффект.
Симптомы Острого вирусного гепатита С:
Особенности клинических проявлений. Инкубационный период составляет в среднем 6-8 нед (2-26 нед). Чаще встречаются безжелтушные формы заболевания (более 80 %), протекающие, как правило, бессимптомно. Основные клинические симптомы ОВГС принципиально не отличаются от таковых при других парентеральных гепатитах. Заболевание в целом протекает значительно легче по сравнению с другими острыми вирусными гепатитами, однако и диагностируется из-за латентного течения достаточно редко, даже случайно, вызывая со временем тяжелые осложнения, что достаточно точно отражено в его популярном названии "ласковый убийца". Действительно, заболевание начинается постепенно. Ведущими симптомами преджелтушного периода (до 10 дней) являются слабость, утомляемость, снижение аппетита, метеоризм, дискомфорт в эпигастральной области и правом подреберье. Реже появляются такие симптомы, как кожный зуд, головная боль, головокружение, диарея, лихорадка. При появлении желтухи в жалобах превалируют слабость, снижение петита и дискомфорт в животе Практически у всех пациентов определяется увеличение размеров печени, которая имеет мягкую консистенцию, а у 20% - спленомегалия. Заболевание чаще протекает в среднетяжелой форме Острая инфекция может протекать тяжело, но фульминантные формы встречаются крайне редко. Выздоровление регистрируется не более чем у 15-20 % больных. Летальный исход встречается редко.
Острый гепатит С часто протекает бессимптомно, но дает высокий процент (50-80 %) исхода в хронический гепатит или хроническое вирусоносительство. Симптомы заболевания не являются специфичными и могут исчезать через несколько недель после снижения уровня АЛТ.
"Хроническое носительство HCV", или инаппарантный вариант хронического гепатита С латентного течения, характеризуется наличием виремии (HCV RNA+), нормальными показателями сывороточных трансаминаз и отсутствием клинических симптомов заболевания, однако у большинства вирусоносителей в пунктатах печени выявляются признаки хронического ее поражения.
Длительное наблюдение за "носителями" с положительной HCV RNA не выявило прогрессирования заболевания у некоторых больных, и в течение ряда лет отсутствовали биохимические и гистологические признаки поражения печени. Однако наличие виремии у них требует повторного исследования активности АлАТ хотя бы 1 раз в месяц в течение 6-9 мес и далее - ежеквартально.
У некоторых лиц в период наблюдения возникает активация процесса (появление клинической симптоматики, повышение активности АлАТ и др.), и при гистологическом исследовании через 9-10 лет у них обнаруживаются признаки цирроза печени.
Диагностика Острого вирусного гепатита С:
Особенности диагностики. HCV РНК может быть обнаружена в крови через 1-3 нед после инфицирования. Анти-HCV выявляются с помощью иммуноферментного анализа (ИФА) лишь у 50-70 % больных при появлении симптомов и достигают 90 % спустя 3 мес. Через 2-8 нед о поражении печени свидетельствует повышение уровня аланинами-нотрансферазы (АлАТ). При биохимическом исследовании выявляется гипербилирубинемия и повышение активности АлАТ иногда в 10-30 раз выше нормы. Гиперферментемия может сохраняться и после исчезновения HCV RNA. Специфическими маркерами в диагностике ОВГС являются HCVAb, обнаруживаемые в ИФА современными тест-системами начиная со 2-3-й недели болезни. Для выявления ложнопози-тивных образцов целесообразно использование иммуноблота в качестве подтверждающего теста. Большое значение имеет определена HCV RNA с помощью ПЦР в различных биологических субстратах сыворотка крови, лимфоциты, ткань печени и др.) для определения активности репликативного процесса и оценки результатов интерферонотерапии. После перенесенного острого вирусного гепатита С HCVAb сыворотке крови сохраняются длительно, иногда в течение 10-15 лет, однако они не обладают защитными свойствами.
Таким образом, для верификации HCV-инфекции используют несколько типов диагностических тестов:
- Иммуноферментный анализ (ИФА) - для скрининга и постановки предварительного диагноза HCV-инфекции в группах высокого риска.
- Анализ методом рекомбинантного иммуноблоттинга (РИБА) - для выявления ложноположительных результатов исследования методом ИФА у бессимптомных больных, доноров крови и у лиц с низким риском развития инфекций.
- Методы выявления HCV RNA (молекулярные методы анализа):
- для подтверждения инфекции:
- у больных с положительным результатом ИФА и неясным результатом РИБА;
- у больных с отрицательным результатом ИФА и подозрением на острый гепатит;
- у больных с гепатитом неустановленной этиологии;
- у больных с большой вероятностью ложноотрицательных результатов анализов на антитела;
- в целях подтверждения виремии у больных ХВГС;
- для определения генотипа и продолжительности лечения.
Лечение Острого вирусного гепатита С:
Особенности лечения ОВГС. Так как самоизлечение острого вирусного гепатита С происходит всего лишь в 10-15 % случаев, а течение болезни у большинства больных легкое, то терапия должна быть направлена на профилактику хронизации процесса.
Заболевание имеет неблагоприятный прогноз, так как исходом болезни у 80 % переболевших является развитие хронического гепатита С. Серьезность прогноза связана с возможностью развития первичной гепатоцеллюлярной карциномы.
К каким докторам следует обращаться если у Вас Острый вирусный гепатит С:
Вас что-то беспокоит? Вы хотите узнать более детальную информацию о Острого вирусного гепатита С, ее причинах, симптомах, методах лечения и профилактики, ходе течения болезни и соблюдении диеты после нее? Или же Вам необходим осмотр? Вы можете записаться на прием к доктору .
Что такое цирроз печени? Причины возникновения, диагностику и методы лечения разберем в статье доктора Васильева Романа Владимировича, гастроэнтеролога со стажем в 15 лет.
Над статьей доктора Васильева Романа Владимировича работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов
![Васильев Роман Владимирович, гастроэнтеролог, гепатолог, врач общей практики - Санкт-Петербург]()
Определение болезни. Причины заболевания
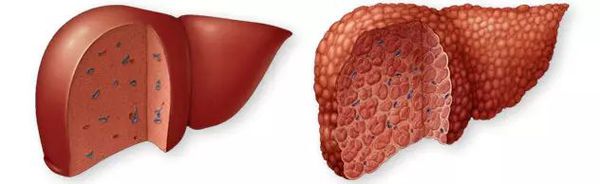
Цирроз печени (ЦП) — это хроническое дегенеративное заболевание печени, связанное с диффузным патологическим процессом, при котором нормальные клетки печени повреждаются, а затем замещаются рубцовой тканью, образуя избыточный фиброз и структурно-анатомические регенераторные узлы.
![Замещение клеток печени рубцовой тканью]()
Этиология
По этиологическим характеристикам можно выделить:
- распространённые формы ЦП;
- редкие формы ЦП.
К распространённым относят вирусные (В, С, D), алкогольные и метаболические формы цирроза печени.
Редкими формами ЦП являются:
- аутоиммунные, лекарственные, токсические, первичные и вторичные билиарные циррозы;
- генетически обусловленные патологии — гемохроматоз (нарушение обмена железа), болезнь Вильсона — Коновалова, дефицит белка альфа-1-антитрипсина, гликогеноз IV типа (недостаток ферментов), галактоземия, наследственная тирозинемия и непереносимость фруктозы;
- нарушение венозного оттока из печени — венокклюзионные формы ЦП (болезнь Бадда — Киари);
- тяжёлая правожелудочковая сердечная недостаточность;
- флебопортальные циррозы (типа Банти).
Пути заражения
Заразиться циррозом печени нельзя. Однако, если он вызван вирусным гепатитом, то возбудитель может передаться через кровь, при половых контактах и от матери к ребёнку.
Основную роль в возникновении и развитии вирусного ЦП играют симптомные, малосимптомные и бессимптомные формы острого вирусного гепатита В, С, а также одновременное заболевание гепатитами В и D с последующим переходом в активный хронический вирусный гепатит. У большинства больных интервал между острым гепатитом С и клинически выраженными проявлениями ЦП превышает 30 лет. Только у мужчин, употребляющих более 50 г спирта в день, выраженные формы ЦП возникают через 13-15 лет.
Наиболее частыми причинами смерти больных ЦП является:
- большая печёночная недостаточность;
- кровотечение из варикозно расширенных вен пищевода;
- первичный рак печени;
- иммунопротективная недостаточность, влекущая за собой активизацию инфекционных (микробных) процессов, в первую очередь спонтанного бактериального перитонита и пневмонии, а также возникновение оксидативного стресса.
У больных в терминальной (заключительной) фазе заболеваний печени в основном наблюдаются декомпенсированные формы цирроза печени: асцит, варикозное расширение вен пищевода и желудка, энцефалопатия и желтуха.
Особенности цирроза печени у детей
Заболевание у детей встречается крайне редко и обычно связано:
- с аутоиммунным поражением печени;
- кардиогенными заболеваниями — лёгочной гипертензией и хронической сердечной недостаточностью;
- болезнью Бадда — Киари;
- врождёнными болезнями накопления — наследственным гемохроматозом, лизосомальными болезнями накопления, болезнью Вильсона — Коновалова;
- флебопортальным циррозом (типа Банти).
Прогноз у таких детей неблагоприятный, чаще всего они погибают, так как не успевают попасть к гепатологу и выяснить диагноз. Также они обычно страдают от множества сопутствующих болезней, в том числе от основного заболевания, ставшего причиной цирроза.
Проявления заболевания у детей и взрослых схожи. Единственный эффективный метод лечения цирроза у детей — это пересадка печени. Поэтому крайне важно вовремя диагностировать заболевание и встать в очередь на пересадку печени.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы цирроза печени
Цирроз печени в течение длительного времени может протекать латентно, т. е. бессимптомно.
Клиническая картина ЦП зависит от его формы и течения, активности основного заболевания, а также наличия или отсутствия печёночно-клеточной недостаточности, синдрома портальной гипертензии, холестаза и внепечёночных проявлений.
Основные общие симптомы, которые чаще всего встречаются при ЦП:
- повышенная утомляемость;
- похудение;
- нарушения сознания и поведения;
- ухудшение аппетита и чувство дискомфорта в животе;
- пожелтение кожи, белковых оболочек глаз и слизистой;
- осветление или обесцвечивание кала;
- потемнение мочи;
- болевые ощущения в животе;
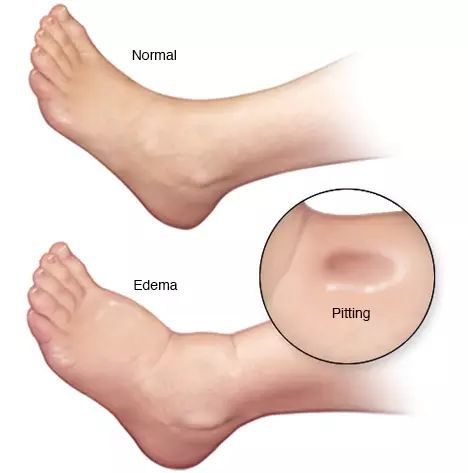
- отёки;
![Отёк ноги при циррозе печени]()
- асцит (скопление жидкости в брюшной полости);
- кровотечения из носа, желудочно-кишечного тракта, дёсен или геморроидальных узлов, а также подкожные кровоизлияния;
- часто возникающие бактериальные инфекции (например, органов дыхания);
- снижение полового влечения;
- кожный зуд.
Симптомы распространённых форм ЦП
При высокоактивном ЦП, кроме общей утомляемости, осветления стула и потемнения мочи, может возникать тупая боль в правом подреберье и вздутие живота.
Во время осмотра часто выявляют:
- субиктеричность (желтушность) склер;
- расширение вен брюшной стенки, напоминающее голову медузы;
- венозный шум при выслушивании в эпигастральной области живота (шум Крювелье — Баумгартена);
- серо-коричневатый цвет шеи;
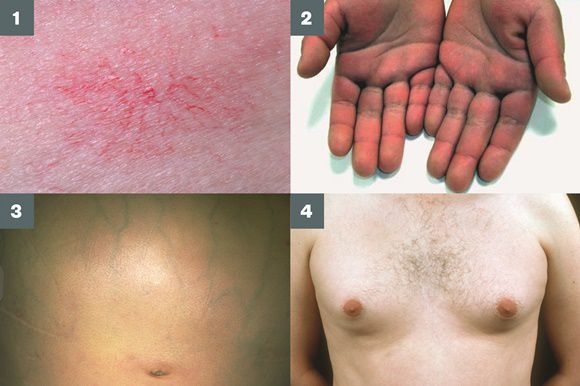
- гинекомастию (увеличение грудных желёз);
- гипогонадизм (у мужчин);
- контрактуру Дюпюитрена (укорочение сухожилий ладоней).
![Симптомы цирроза печени]()
Три последних признака цирроза печени зачастую наблюдаются при алкогольных ЦП.
В области грудной клетки в 50-80% случаев наблюдаются телеангиэктазии кожи (расширения мелких сосудов), чаще при алкогольных ЦП. Пальпаторно печень отчётлива уплотнена, имеет неровный нижний край. Размеры печени различны — от значительного увеличения до уменьшения.
Часто при пальпации выявляется умеренно увеличенная селезёнка, причём её край может выступать из-под рёберной дуги на 1-3 см.
При развитии ЦП появляются симптомы белково-энергетической недостаточности, асцит, отёки, а также печёночный запах при тяжёлой печёночной недостаточности.
Симптомы при малоактивных и начальных стадиях ЦП
Данные формы ЦП зачастую протекают бессимптомно и выявляются в ходе периодических медицинских осмотров, диспансеризации, а также как случайная находка при обследовании пациента со смежной патологией или внепечёночными проявлениями.
При малоактивном ЦП, как правило, не возникают жалобы, связанные с печенью. Во время активного расспроса можно выявить весеннее снижение работоспособности, частые болезни, после которых возможны кровоточивость дёсен и потемнение мочи. Такие пациенты хуже, чем раньше, переносят длительные физические и нервно-психические нагрузки.
Желтухи и выраженного увеличения билирубина, за исключением периода интеркурентного острого гепатита, нет. Неяркая телеангиоэктазия кожи (сосудистые звёздочки) в области грудной клетки наблюдаются у 40-60% людей с ЦП.
Телеангиоэктазии кожи, плотная печень с фестончатым краем и умеренно увеличенная селезёнка — ценная клинико-диагностическая триада, которая с вероятностью 80-90% свидетельствует о ЦП или далеко зашедшем активном хроническом гепатите.
Патогенез цирроза печени
В основе патофизиологии цирроза лежит повреждение и некроз паренхимы (основной ткани) печени с деструкцией и гибелью гепатоцитов (клеток печени), а также системное поражение интерстициальной ткани.
При всех формах ЦП нарушается иммунологическое равновесие организма, преобладающими становятся аутоиммунные процессы: иммунная система человека принимает собственные клетки печени за чужеродные и повреждает их. В конечном итоге, это приводит к разрушению гепатоцитов и структуры печени в целом. Однако при этом каждая форма ЦП имеет свои патогенетические особенности:
- при вирусных гепатитах повреждающим агентом является сама вирусная частица, которая, размножаясь в клетке, разрушает её, вызывая цитолиз;
- при алкогольном ЦП прямое токсическое воздействие на мембраны гепатоцитов оказывает ацетальдегид с развитием алкогольной жировой болезни печени и алкогольного стеатогепатита;
- при метаболическом ЦП ведущую роль в патогенезе играет ожирение и сахарный диабет через стадию неалкогольного стеатогепатита с инсулинорезистентностью и последующей запрограммированной гибелью клеток печени.
В основе патогенеза более редких причин цирроза печени лежат ещё более частные механизмы развития повреждения и разрушения гепатоцитов и структуры печени:
- нарушение обмена и накопления железа при гемохроматозе;
- накопление меди при болезни Вильсона — Коновалова;
- окклюзия в системе воротной вены при гепатопортальном склерозе.
Цирроз формируется на протяжении многих лет. С течением времени происходят изменения генетического аппарата клеток печени, в результате чего появляются новые патологические клетки. Этот процесс в печени является иммуновоспалительным, он поддерживается чужеродными агентами, в роли которых могут выступать разные субстраты:
- вирус гепатита В;
- алкогольный гиалин;
- денатурированные белки;
- некоторые лекарственные средства;
- медьбелковые и железобелковые комплексы (ферритин).
В итоге повреждения паренхимы печени развивается гепатоцеллюлярная (печёночно-клеточная) недостаточность за счёт диффузного фиброза и трансформации ткани печени в анормальные узлы-регенераты. [3] [4] [5]
Классификация и стадии развития цирроза печени
В 1974 году на съезде гепатологов в Акапулько (Мексика) была принята единая морфологическая классификация, которую позже уточнили и несколько доработали эксперты ВОЗ. В настоящее время она является общепринятой.
Что провоцирует / Причины Спонтанного бактериального перитонита:
Наиболее вероятно развитие СБП у больных алкогольным циррозом печени, а также у больных с фульминантиым течением острого гепатита и у лиц, страдающих первичным билиарным циррозом. К основным факторам риска развития спонтанного бактериального перитонита относятся:
- Цирроз печени.
- Гастроинтсстинальное кровотечение.
- Эпизоды СБП в анализе.
- Содержание белка в асцитической жидкости меньше 1 г%.
- Уровень сывороточного альбумина больше 2,5 мг/дл.
- Уровень сывороточного креатинина больше 2 мг/дл.
Развитие СБП, как правило, обусловлено микробной контаминацией асцитической жидкости, которая чаще инфицируется без видимой причины или после парацентеза. Инфицирование происходит гематогенным и транслокационным путями и в 90 % случаев обусловлено одним возбудителем, чаще кишечной группы. Основным источником обсеменения брюшной полости является микрофлора толстой кишки, проникающая в асцитическую жидкость вследствие повышенной проницаемости стенки кишки. Важное место отводится гепатогенному распространению инфекции на фоне нарастающей бактериемии, при осложненном парацентезе, перфорации или дилатации толстой кишки или очаге инфекции в брюшной полости. Возбудителями спонтанного бактериального перитонита чаще являются Escherihia coll (70 % случаев). Реже причиной перитонита служат Streptococcus pneumoniae , Strepto coccus faecalis , анаэробы. В 10 % высевают смешанную флору.
Проникновению патологических возбудителей в кровь способствует нарушение проницаемости стенки кишечника. При циррозе печени в брыжеечных лимфатических узлах часто обнаруживаются бактерии. Предрасположенность к развитию спонтанного бактериального перитонита у данной категории пациентов обусловлена снижением неспецифической резистентности организма и антибактериальной активности асцитической жидкости.
Патогенез (что происходит?) во время Спонтанного бактериального перитонита:
В развитии СБП важная роль отводится характеру и количеству асцитической жидкости. При большом ее объеме уменьшается возможность контакта нейтрофилов с бактериальными клетками. Жидкость становится благоприятной средой для роста бактерий, нормальный фагоцитоз жидкости нарушен вследствие дефицита опсонинов, в результате чего нарушаются процессы фагоцитоза. "Опсоническая" активность асцитической жидкости прямо пропорциональна количеству белка, поэтому спонтанный бактериальный перитонит чаще возникает при концентрации белка в ней менее 1%. К факторам биохимического риска развития СБП, помимо содержания белка, относятся высокие уровни сывороточного билирубина, креатинина. Кроме того, в асцитической жидкости уменьшается содержание иммуноглобулинов (IgA, IgG), компонентов системы комплемента (СЗ), фибриногена, фибронектина.
Известно, что ведущую роль в обезвреживании эндотоксина грамотрицательных бактерий, образовавшегося в кишечнике, играют резидентные печеночные макрофаги - клетки Купфера, эндотелиоциты, находящиеся в тесном взаимодействии с гистиоцитами. При циррозе печени существенно угнетается их функциональная активность, нарушается кооперативное взаимоотношение между клетками, что способствует поступлению в системную циркуляцию большого количества токсинов и их метаболитов. Нарушение процессов детоксикации усугубляется нарушением гемодинамики в печеночной ткани, вследствие чего значительное количество эндотоксинов попадает в общий кровоток в обход синусоидов по внутри- и внепеченочным портосистем-ным шунтам. Высокая энтотоксемия способствует существенному нарушению процессов фагоцитоза микроорганизмов: хемотаксиса, адгезии, дегрануляции, захвата и инактивации. Наличие воспалительно-деструктивных процессов и избыточное содержание токсинов приводит к усиленному образованию иммунных комплексов.
В печени происходит обезвреживание эндотоксина грамотрицательных бактерий, образующегося в кишечнике и поступающего в портальный кровоток. Основную роль по элиминации эндотоксина в печени выполняют клетки Купфера, эндотелиоциты, гепатоциты. Нами установлено, что при цирротическом процессе нарушается кооперативное взаимодействие клеточных популяций, участвующих в процессах детоксикации, что приводит к избыточному поступлению эндотоксина в системную циркуляцию, активизации каскада провоспалительных цитокинов, угнетающих защитные механизмы. Следствием указанных процессов является нарушение всех этапов фагоцитоза, функции комплемента.
Симптомы Спонтанного бактериального перитонита:
Клинические проявления.Основными симптомами спонтанного бактериального перитонита являются высокая лихорадка (30-76 %), боли в животе, болезненность при пальпации брюшной стенки (63-72 %), рвота, диарея, парез кишечника, проявления печеночной энцефалопатии (46-71%).
В ряде случаев появляются признаки септического шока: тахикардия (более 100 уд/мин), снижение АД ниже 90 мм рт. ст., олигурия.
В то же время у 14 % больных СБП почечная симптоматика отсутствует или является стертой. У 30 % пациентов СБП не проявляется никакими клиническими симптомами и распознается только с помощью парацентеза. Заболевание при этом выявляется случайно или при исследовании асцитической жидкости Наиболее тяжелым осложнением, определяющим прогноз спонтанного бактериального перитонита, является почечная недостаточность.
Диагностика Спонтанного бактериального перитонита:
Диагностика СБП в классических случаях, как правило, несложна. Спонтанный бактериальный перитонит можно заподозрить в случаях резкого ухудшения состояния и развития печеночной энцефалопатии у больных циррозом печени. Решающее значение в диагностике имеет исследование асцитической жидкости - парацентез, который проводится с целью выявления СБП.
Процедура парацентеза показана больным циррозом печени с наличием асцита даже при отсутствии клинических признаков инфекции При этом выделяют собственно спонтанный бактериальный перитонит и культуронегативный нейтрофильный асцит. Показаниями к парацентезу являются:
- местные признаки перитонеальной инфекции - болевой синдром в брюшной полости, нарушение перистальтики кишечника;
- системные проявления инфекции - лихорадка, лейкоцитоз, септические состояния;
- нарастание признаков печеночной энцефалопатии без видимых причин;
- обследование больных с асцитом, осложненным кровотечением из желудочно-кишечного тракта, для выбора антибактериальной терапии.
У большинства больных СБП выявляются монобактериальные инфекции. Диагноз собственно спонтанного бактериального перитонита подтверждают при положительном результате посева асцитической жидкости, где количество нейтрофилов превышает 250/мм3 (либо больше 500 в 1 мм3 независимо от результата посева). В посеве обнаруживается рост бактерий, отсутствуют интраабдоминальные источники инфицирования. При геморрагическом асците количество эритроцитов, как правило, больше 10 000/мм3, количество же лейкоцитов необходимо оценивать из расчета 1 лейкоцит на 250 эритроцитов.
Для культуронегативного нейтрофильного асцита характерно наличие нейтрофилов более 250/мм 3 при отрицательном результате посева и отсутствии антибиотикотерапии в течение 30 предшествующих дней. У большинства больных СБП инфекционный агент, выделенный из крови, является этиологическим фактором, минимальное количество асцитической жидкости для посева составляет 10 мл. Повышенное количество палочкоядерных лейкоцитов в асцитической жидкости при ложноотрицательных результатах исследования асцитической жидкости и крови на стерильность необходимо расценивать как признак СБП. Термин "бактериальный асцит" используется для обозначения колонизации асцитической жидкости бактериями при отсутствии в ней воспалительной реакции. Диагноз бактериального асцита используется в случаях выделения бактериальной культуры при количестве палочкоядерных лейкоцитов ниже 250/мм 3 .
Лечение Спонтанного бактериального перитонита:
Лечение СБП целесообразно начинать очень быстро, что способствует увеличению выживаемости больных еще до получения культуры бактерий, высеянной из асцитической жидкости. Если не удается высеять микроорганизмы и, следовательно, приходится проводить учение "вслепую", целесообразно одновременно использовать нор-Флоксацин и лактулозу для предотвращения проникновения бактерий из кишечника.
Низкая эффективность антибиотикотерапии определяется следующими признаками:
- Отсутствие клинического эффекта через 3 дня после начала лечения.
- Отсутствие снижения количества нейтрофилов в асцитической жидкости.
- Наличие резистентной к данному антибиотику флоры по результатам посева.
Наличие одного или нескольких из этих признаков является показанием для замены антибиотика. Инфицирование анаэробами является показанием к назначению метронидазола.
Профилактический курс антибиотикотерапии показан больным циррозом печени при наличии кровотечений из органов желудочно-кишечного тракта для предупреждения бактериальных осложнений. Профилактику можно осуществлять несколькими антибиотиками. Препаратом выбора является норфлоксацин в дозе 400 мг 2 раза в день в течение 7 дней Однако при этом появляется резистентные колонии бактерий. Эффективен триметоприл (сульфометоксазол).
При развитии почечной недостаточности у больных циррозом печени показаны инфузии альбумина, противошоковых жидкостей (поли-глюкин) в комбинации с фуросемидом внутривенно 80-160 мг в сутки. Кроме того, назначение диуретиков способствует повышению общего содержания белка и стимулирует "опсонирующую" активность асцитической жидкости. Рецидивирующий спонтанный бактериальный перитонит является показанием к трансплантации печени.
После первого эпизода СБП общая смертность в течение года достигает 61-78%.
К каким докторам следует обращаться если у Вас Спонтанный бактериальный перитонит:
Вас что-то беспокоит? Вы хотите узнать более детальную информацию о Спонтанного бактериального перитонита, ее причинах, симптомах, методах лечения и профилактики, ходе течения болезни и соблюдении диеты после нее? Или же Вам необходим осмотр? Вы можете записаться на прием к доктору .
ПВТ — противовирусная терапия
СН — сердечная недостаточность
ХГС — хронический гепатит С
HCV — вирус гепатита С
NT-pro-BNP — N-концевой предшественник мозгового натрийуретического пептида
Хронический гепатит С (ХГС) — актуальная междисциплинарная проблема. Хорошо изучены различные внепеченочные проявления ХГС, такие как смешанная криоглобулинемия, гломерулонефрит, поздняя кожная порфирия, красный плоский лишай, синдром Шегрена и др. Однако существует целый ряд системных проявлений, которые нуждаются в более тщательном изучении, в частности поражение сердца. При ХГС описаны миокардит, гипертрофическая (ГКМП) и дилатационная (ДКМП) кардиомиопатии, коронарит вследствие криоглобулинемического васкулита мелких сосудов сердца, аритмогенная дисплазия правого желудочка, аневризма левого желудочка, раннее развитие атеросклероза и ишемической болезни сердца [1—6]. Возможно развитие цирротической кардиомиопатии (КМП), которая наблюдается при циррозах печени различной этиологии, в том числе вирусной. Развивается диастолическая дисфункция миокарда и синдром удлиненного интервала Q—T, выраженность которого увеличивается по мере нарастания декомпенсации функции печени [7—11]. Наконец, широко используемая противовирусная терапия (ПВТ) ХГС может сопровождаться кардиотоксичностью интерферона (ИФН), имеющей клинические особенности и нередко проявляющейся развитием декомпенсации деятельности сердца.
Миокардит является одним из мало изученных внепеченочных проявлений ХГС [3, 4]. В клинике им. Е.М. Тареева описана серия наблюдений из 22 больных хроническим гепатитом вирусной этиологии с миокардитом, у 13 из которых диагностирован цирроз печени. Поражение сердца у 4 больных стало причиной летального исхода. В 3 наблюдениях на аутопсии выявлена картина хронического активного миокардита: обширные очаги лизиса кардиомиоцитов (КМЦ) с очаговой лимфогистиоцитарной инфильтрацией; многочисленные продуктивные и продуктивно-деструктивные эндофлебиты; диффузный фиброз стромы; лимфогистиоцитарная инфильтрация стромы. В одном случае диагностированы диффузный кардиосклероз, миокардиофиброз, диффузный склероз эндокарда. Особенностью двух других наблюдений явились выраженные изменения в проводящей системе сердца: волокна проводящей системы замурованы в грубоволокнистую фиброзную ткань, отмечены резко выраженная дистрофия и некробиоз КМЦ. У этих больных наблюдались различные нарушения проводимости [4].
Первичные КМП представляют собой гетерогенную группу заболеваний миокарда различной этиологии. Наибольший интерес к проблеме миокардитов и КМП, ассоциированных с HCV-инфекцией, отмечен у исследователей из Японии. Выявлена высокая распространенность HCV-инфекции у больных ГКМП, ДКМП и миокардитом [17—20]. При многоцентровом исследовании по программе Комитета по изучению идиопатических КМП в Японии, антитела HCV в сыворотке выявлены у 74 (10,6%) из 697 больных ГКМП и у 42 (6,3%) из 633 больных ДКМП, значительно превышая частоту обнаружения антител HCV у сопоставимых по возрасту доноров крови (2,4%) [20].
По данным A. Matsumori [1], у 113 больных ГКМП, HCV-инфекция диагностирована у 16 (14,1%), причем ни у одного из них не было семейного анамнеза по ГКМП. В 4 наблюдениях имелись указания на гемотрансфузии в анамнезе, у 10 больных определялся повышенный уровень трансаминаз в сыворотке, у 7 выявлен гепатоцеллюлярный рак. При морфологическом исследовании отмечены умеренная или выраженная гипертрофия правого и левого желудочков, фиброз различной степени и умеренная клеточная инфильтрация миокарда. РНК HCV генотипа 1b выявлена в сыворотке у 7 больных, РНК HCV в ткани миокарда — у 6, минус-цепи РНК HCV обнаружены в биоптатах сердца у 2 больных. Другая группа исследователей выявила антитела HCV у 18 (22,5%) из 80 больных ГКМП [21].
Многоцентровое исследование, проводимое научным комитетом по изучению КМП Всемирной федерации заболеваний сердца, ставило задачу выявления вирусных геномов энтеровирусов, аденовируса, цитомегаловируса и HCV в формалиновых срезах ткани сердца. Геном HCV выявлен в 2 (18%) из 11 биоптатов больных ДКМП и миокардитом в Италии и у 4 (36%) из 11 больных в США, у 2 из них выявлен миокардит и у 2 — аритмогенная дисплазия правого желудочка. Несмотря на то что метод выявления генома HCV в парафиновых (фиксированных в формалине) срезах менее чувствительный, чем в замороженных образцах, предполагается, что HCV-инфекция может быть более частой причиной ряда заболеваний миокарда, в первую очередь миокардита [22]. Показано также, что частота развития КМП, обусловленных HCV, варьирует в различных регионах мира и различных популяциях. Среди больных КМП в Канаде (Ванкувер) РНК HCV не обнаружена ни в одном из 24 образцов ткани сердца. Ряд европейских исследователей также высказываются против связи HCV-инфекции и заболеваний сердца [23].
В последние годы также изучается вопрос о взаимосвязи ХГС и уровня натрийуретических пептидов. Так, в крупном ретроспективном исследовании антитела к HCV выявлены у 59 (4,4%) из 1355 больных с СН неясной этиологии, что значительно превышало частоту НCV-инфекции в общей популяции (1,8%). Уровень N-концевого предшественника мозгового натрийуретического пептида (NT-pro-BNP) в сыворотке у больных с СН и ХГС достоверно выше, чем у больных с СН без маркеров HCV (р<0,0001) [24]. Интересным представляется исследование А. Antonelli и соавт. [25], которые выявили повышенный уровень NT-pro-BNP у 34% больных ХГС, в то время как в группе неинфицированных, сопоставимых по полу и возрасту, повышение данного лабораторного показателя отмечалось лишь в 6% наблюдений. Это может свидетельствовать в пользу субклинического поражения сердца у некоторых больных ХГС.
Генетические факторы и патогенетические звенья поражения сердца при HCV. Несмотря на то что в последнее время в литературе описываются клинические наблюдения ДКМП и ГКМП, ассоциированных c HCV [1, 6, 18, 21]; механизм, посредством которого HCV приводит к их развитию, полностью не изучен. У ряда пациентов с ассоциированной с HCV КМП идентифицированы HLA- и не-HLA-гаплотипы, которые дают основание полагать, что фактором развития данного вида поражения сердца является генетическая предрасположенность. Так, в развитии ДКМП участвует α-фактор некроза опухоли (α-ФНО) — один из ключевых цитокинов, усиление синтеза которого наблюдается при HCV-инфекции [26].
Причиной миокардита, приводящего к ДКМП и СН, могут быть некоторые вирусы, обладающие тропизмом к миокарду [27, 28]. Считается, что в основе развития вирусного миокардита и прогрессирования его в КМП лежат механизмы смерти клетки в результате апоптоза, а также индуцированные вирусами иммунные реакции [29]. Предполагаемым иммунным механизмом является постоянное обновление иммунокомпетентных клеток и продуцируемых ими цитокинов [30, 31]. Среди всех цитокинов, участвующих в развитии и прогрессировании миокардита, наиболее важную роль играет α-ФНО [32—34]. Отдельные исследования показали, что имеется связь как между сниженной функцией миокарда и повышенной экспрессией α-ФНО, так и между концентрацией α-ФНО в плазме и миокарде у больных миокардитом [35] и ДКМП [36]. С помощью иммуногистохимического анализа установлено, что α-ФНО продуцируется КМЦ при вирусных миокардитах, ассоциированных с аденовирусом, цитомегаловирусом, вирусом Эпштейна—Барр, вирусами гриппа, А и B, а также HCV [35, 37]. Отрицательный инотропный эффект α-ФНО обусловлен связыванием α-ФНО со специфическими рецепторами TNFR1 и TNFR2, которые экспрессируются на мембране КМЦ [38]. Также вероятно, что α-ФНО ингибирует кальциевые каналы L-типа, что приводит к снижению систолической функции миокарда [39]. Другим механизмом, посредством которого α-ФНО влияет на миокард, является стимулирование продукции оксида азота (NO), который оказывает отрицательное инотропное действие на миокард, действуя как эндогенный ингибитор и фактически уменьшая положительный инотропный ответ на β-адренергическую стимуляцию [40].
Некоторые гены, например гены системы HLA, причастны к клиренсу и персистенции HCV-инфекции [41]. В нескольких исследованиях сообщалось, что ДКМП и ГКМП ассоциируются с некоторыми аллелями системы HLA. Так, у инфицированных HCV пациентов, у которых развивается ДКМП, более часто выявляются гаплотипы HLA-DPB1*0901 и HLA-DRB1*1201, а у инфицированных HCV пациентов с ГКМП — гаплотипы HLA DRB1*0901 и DQB1*0303 [1, 42]. По данным других авторов, развитие ДКМП, ассоциированной с HCV, наиболее отчетливо коррелирует с аллелями не-HLA-генов, чем с генами системы HLA [43]. Таким образом, пилотные исследования демонстрируют, что имеется генетическая предрасположенность к развитию поражения миокарда у пациентов с ХГС (рис. 1).
![]()
Рис. 1. Генетическая предрасположенность к поражению миокарда при HCV-инфекции.
По данным N. O’Garra и соавт. [44], в печени развивается выраженный CD4+ Th1 клеточный ответ, наиболее вероятно индуцируемый интерлейкином (ИЛ) 12, ИФН-α и ИФН-β, которые продуцируются моноцитами, нейтрофилами и макрофагами после стимуляции Toll-like-рецепторов HCV производными продуктами. Если определенные гаплотипы кодируют молекулы главного комплекса гистосовместимости (ГКГ) II класса с более высоким сродством к производным пептидам HCV, то их функция как молекул, презентирующих антигены клеткам Th1 CD4+, повышается. После активации клетки Th1 CD4+ продуцируют ИФН-γ, который активирует макрофаги к продукции провоспалительных цитокинов [44]. Главными цитокинами, продуцируемыми макрофагами, являются ИЛ-1 и α-ФНО [45], которые могут приводить к обновлению иммунных клеток и высокой концентрации α-ФНО в миокарде.
Другим механизмом, посредством которого гаплотипы HLA могут влиять на развитие ДКМП, ассоциированной с HCV, в контексте α-ФНО является так называемая неклассическая функция клеток ГКГ II класса, т. е. их роль в качестве сигнальных трансдукционных молекул, активируемых суперантигенами в клетках некоторых типов [46, 47]. Суперантигены являются протеинами бактериального или вирусного происхождения, которые активируют до 20% Т-клеточной популяции путем одновременного связывания Т-клеточных рецепторов и молекул ГКГ II класса, что приводит к массивному высвобождению цитокинов, которые секретируются как Т-клетками, так и антигенпрезентирующими клетками [48—50]. В контексте полиморфизма HLA предполагалось, что они принимают непосредственное участие в исходе, к которому приводит продукция цитокинов, стимулируемая суперантигенами [51, 52]. Можно предположить, что определенные гаплотипы HLA кодируют эпитопы молекул ГКГ II класса с высоким сродством к производным HCV суперантигенам или антителам, а это ведет к чрезмерной продукции цитокинов, в частности α-ФНО. Более активное обновление иммунных клеток может привести у генетически предрасположенных инфицированных HCV пациентов к развитию миокардита и впоследствии к ДКМП. Следует отметить, что часто при ассоциированном с HCV хроническом активном миокардите у пациентов отмечался нормальный уровень активности печеночных трансаминаз в сыворотке крови вплоть до формирования терминальной стадии СН [53].
Развитие и прогрессирование вирусного миокардита, в том числе у больных ХГС, осуществляется через различные патогенетические звенья (рис. 2): 1) прямое действие вируса на миокард; 2) непрямое (иммунологическое) действие; 3) смерть клеток в результате апоптоза.
![]()
Рис. 2. Механизмы поражения миокарда при HCV-инфекции. АФК — активные формы кислорода.
Воздействие HCV на миокард. Ряд исследователей указывают на возможность прямого воздействия HCV на миокард. Показано, что HCV реплицируется в миокарде, о чем свидетельствует выявление там негативных цепей РНК [53—55]. Механизм, посредством которого протеин HCVcorе вызывает повреждение миокарда, остается неясным; однако он может быть сходным с механизмом поражения печени. Показано, что изменения в структуре рецепторов TNFR1, вызываемых протеином HCVcorе, повышают чувствительность клеток к цитолизу, опосредованному α-ФНО [56]. Кроме того, протеин HCVcorе вызывает дисфункцию митохондрий, что приводит к развитию окислительного стресса клеток печени [57, 58]. Фактически, протеин HCVcore ограничивает свое действие в митохондриях, в частности он взаимодействует с наружной мембраной митохондрий, повышает поглощение кальция митохондриями и вызывает окисление глутатиона, что приводит к дальнейшему повышению продукции АФК [59, 60]. Повышение образования АФК инициирует продукцию α-ФНО [61], который, как отмечено ранее, оказывает отрицательное инотропное действие на миокард. В некоторых ранее проводимых исследованиях продемонстрировано, что у пациентов с острой и хронической СН, развившихся в исходе КМП, в миокарде определяется повышение выработки АФК [62, 63].
К тому же ряд исследований на животных подтверждают роль протеина HCVcore в развитии КМП. В частности, развитие КМП наблюдалось у трансгенных мышей, носителей гена HCVcore, в возрасте 12 мес. Гистологический анализ миокарда этих мышей выявил гипертрофию КМЦ, кардиальный фиброз, дезорганизацию, дефицит и лизис миофибрилл, вакуолизацию и деформацию ядер, повышенное количество митохондрий неправильной формы [55], что убедительно подтверждает определяющие действие протеина HCVcore на развитие КМП, ассоциированной с HCV.
Непрямой иммунологический механизм поражения миокарда включает вовлечение в патологический процесс В-клеток, Т-клеток и макрофагов. Участие В-клеток в КМП, ассоциированной с HCV, предположено в результате обследования 3 пациентов с ассоциированным с HCV миокардитом, ответивших на иммуносупрессивную терапию. В сыворотке крови этих больных выявлены антитела к миокарду, что дало основание предполагать иммунологический механизм повреждения клеток. В дальнейшем подтверждение иммуноопосредованного механизма КМП, ассоциированной с HCV, было основано на эффективности иммуносупрессивных препаратов (преднизолон и азатиоприн), терапия которыми привела к нормализации размеров камер сердца и регрессу признаков СН, несмотря на продолжающуюся персистенцию HCV [54].
Прямой и непрямой механизмы развития ДКМП, ассоциированной с HCV, связаны со смертью клеток через апоптоз. Благодаря способности повышать продукцию АФК, протеин HCVcore может инициировать митохондриальный путь апоптоза. АФК могут вызывать диссоциацию цитохрома С на внутренней мембране митохондрий, что приводит к активации каспаз, результатом чего является фрагментация геномной ДНК и смерть клетки [64]. В результате связывания лигандов с внеклеточными рецепторами суперсемейства рецепторов α-ФНО происходит активация рецепторзависимого сигнального пути апоптоза [65]. Наиболее важными лигандами этих рецепторов являются α-ФНО и Fas-лиганд (FasL). Высокий уровень α-ФНО в миокарде у пациентов с ассоциированным с HCV миокардитом может активировать данный механизм смерти клеток путем взаимодействия с рецепторами ФНО [66].
Заключение
Имеются убедительные доказательства того, что поражение сердца служит одним из внепеченочных проявлений HCV-инфекции. Механизм, посредством которого HCV может приводить к поражению миокарда у генетически предрасположенных пациентов, является многофакторным и включает прямое повреждающее действие вируса, аутоиммунный механизм и апоптоз.
Поражение миокарда при ХГС может прогрессировать в хронический персистирующий миокардит через прямой (вирусный) и непрямой (иммунный) механизмы повреждения, которые приводят к активации зависимой от рецепторов смерти КМЦ, результатом чего является развитие фиброза миокарда с возможной трансформацией в ДКМП. Кроме того, описаны случаи взаимосвязи HCV и ГКМП.
До настоящего момента HCV-инфицированным больным с вовлечением сердца ПВТ, как правило, не проводилась из-за побочных эффектов ИФН. Однако за последние несколько лет в ПВТ вирусного гепатита С произошли кардинальные изменения. Длительное изучение механизмов репликации HCV привело к созданию ингибиторов протеаз HCV (NS¾A, NS5A, NS5B), которые позволяют достичь элиминации вируса у 90—99% пациентов за существенно более короткий срок (как правило, 12 нед) без применения препаратов ИФН (так называемая безинтерфероновая терапия). Это делает данную терапию гораздо более безопасной и хорошо переносимой, в том числе в отношении миокарда [67—69].
Нуждается в отдельном изучении вопрос эффективности и безопасности ПВТ у пациентов с ХГС и ассоциированного с ним поражения сердца, включая сравнение только ПВТ и сочетания ПВТ с сердечно-сосудистыми препаратами и/или иммуносупрессорами. Выявление антител к миокарду и определение уровня α-ФНО в сыворотке крови во время терапии может быть использовано для оценки влияния терапии на данные маркеры.
Вирусный гепатит С (Ц) очень серьёзное заболевание, вызываемое вирусом, проникающим в организм человека с кровью больного человека – парентерально. Заболевание отличается скрытностью течения, когда человек не подозревает, что он когда-то заразился и уже сам стал разносчиком инфекции. Нередко у пациента выявляется цирроз печени, и только тогда он узнает, что много лет в его крови циркулирует вирус.
![Нагибина Маргарита Васильевна]()
![Нагибина Маргарита Васильевна]()
Высокопрофессиональные инфекционисты и современное диагностическое оборудование международной клиники Медика24 позволяют выявить все предрасполагающие факторы для развития заболевания, провести дифференциальную диагностику и исключить все возможные ложноотрицательные и неоднозначные трактовки.
Часто ли встречается гепатит C?
В в международной клинике Медика24 используются самые эффективные отечественные и зарубежные методики терапии, что позволяет существенно улучшить качество жизни наших пациентов и сохранить их активность.
Все вирусные гепатиты очень похожи друг на друга, и отличить их можно по анализам. Но в клинической картине есть и различия в интенсивности симптомов, так при вирусном гепатите С все признаки начала болезни смазаны. Нечасто можно установить, сколько длится период от заражения вирусом до появления первых симптомов, но во всех случаях стараются отследить инфекционный контакт, чтобы в будущем предотвратить невольное заражение других людей.
В в международной клинике Медика24 в кратчайший срок проведут обследование и поставят правильный диагноз, что повысит эффективность лечения и сократит период реабилитации. Даже самый сложный диагностический случай не останется неразгаданной загадкой для наших врачей-инфекционистов.
Какие симптомы возникают при остром гепатите С?
В большинстве клиническая картина острой инфекции проявляется:
Если с подобным нездоровьем прийти в поликлинику, где в обход всяких медицинских традиций предложат сдать биохимический анализ крови, то по изменениям печёночных ферментов и проб печени будет заподозрено заболевание печени. Но такими настороженными, как правило, врачи бывают только с членами семьи больного хроническим гепатитом С. В обыденной практике при симптомах ОРВИ и ОРЗ анализ крови на биохимию не предлагается.
Острый гепатит С проходит под маской небольшого недомогания, провести лечение гепатита С и не дать шанса для развития хронического заболевания, позволит только своевременная диагностика.
Какие симптомы возникают при хроническом гепатите С?
Когда болезнь существует более полугода, то это уже хроническая форма. При ней клиническую картину определяет состояние печени, если изменения минимальны, то один сценарий, если обширны – другой.
- В картине превалирует астеновегетативный синдром – сильная слабость и быстрая утомляемость.
- Возможна неприятная реакция на жирную пищу и плохая переносимость алкоголя, всё это проявляется подташниванием и неприятным привкусом во рту.
- Могут быть тянущие болезненные ощущения в правом подреберье.
- А может ничего, кроме слабости, и не быть.
Способствуют неприятностям при хронической форме злоупотребление алкоголем, ожирение и нарушения обмена, в этих случаях прогрессирование фиброза с исходом в цирроз печени проходят быстрее и интенсивнее.
Какие симптомы гепатита с характерны для женщин?
Признаки гепатита С у женщин такие же, как у мужчин, но выраженность симптомов меньше, сказывается защитное действие половых гормонов эстрогенов. Поэтому молодые женщины переносят болезнь лучше пожилых дам. Женщины внимательнее относятся к своему здоровью, по статистике чаще обращаются за медицинской помощью и охотно сдают анализы.
В хронической стадии нарушение функций печени может сказаться на свертываемости крови, что может изменить длительность менструаций и неблагоприятно сказаться на течении варикозной болезни вен нижних конечностей.
В клинике инфекционных заболеваний Международная клиника Медика24 есть всё необходимое для результативного лечения и эффективного восстановления, все программы индивидуализированы и основаны на мировых стандартах диагностики и лечения.
Отличительные признаки гепатита С у мужчин
Симптомы гепатита С у мужчин более выражены, прогноз в отношении развития осложнений хуже. Молодые переносят заболевание легче пожилых, но хуже женщин. Мужчины редко обращаются за медицинской помощью при наличии только слабости и утомляемости, а это ведущие и часто единственные симптомы болезни, анализы сдают под принуждением.
При существенном нарушении функций печени развиваются гинекомастия и эректильная дисфункция. Весомую роль в развитии цирроза печени играет увлечение алкогольными напитками и нездоровое питание. Небрежное отношение к собственному телу приближает тягостные последствия. Раньше появляются признаки цирроза печени: варикозное расширение вен пищевода, выпоты в полостях.
Причина гепатита С – заражение вирусом, который относят к одному из самых агрессивных возбудителей инфекций, он самый злой из поражающих печень. Особенность гепатита С - в высокой частоте перехода остр ой формы в хроническую, почти 80%. Хроническая форма очень часто становится причиной цирроза печени и гепатоцеллюлярного рака.
Позаботьтесь о себе, запишитесь на консультацию сейчас
Какие бывают разновидности вируса гепатита C?
Вирусная частица - всего одна скрученная нитка молекулы РНК, состоящая из 9600 белковых кусочков, в жировой капсуле с включениями белков.
Возбудитель гепатита С имеет шесть разновидностей - генотипов, что характерно, переболев одним, от остальных перекрестного иммунитета не возникает. Но количество дополнительных вариантов – субтипов уже достигло сотни, поэтому идея сделать вакцину оставлена за неосуществимостью.
- В России распространены по частоте встречаемости генотипы 1, 3, 2.
- В европейских странах обитает преимущественно 2 и 3 типы.
- Причина американского гепатита - генотип 1, а японского – генотип 2.
- Ближневосточный и заодно африканский 4 генотип для россиян непривычен.
А ещё есть и квазивиды, формируемые из-за постоянной изменчивости вирусной частицы, которая внутри себя придумывает мутации, во время деления специально путает местами гены, вместо одной копии гена создает несколько. Причина мимикрических безобразий инфекционного агента – самозащита от иммунитета хозяина.
Раннее выявление инфекции позволяет предотвратить передачу вируса и начать эффективное лечение гепатита С. Регулярный прием лекарств под контролем количества циркулирующих в крови вирусный копий на десятилетия отодвигает причину развития смертельных осложнений. Отличное лабораторное оборудование и весь спектр обследования доступен в международной клинике Медика24, врачи проанализирую результаты обследования по канонам лучших мировых центров.
Сколько нужно вирусов, чтобы заразиться?
Можно ли заразиться одной вирусной частицей? Вероятно, можно, а возможно, что и невозможно. Причина такой глобальной неясности в том, что для экспериментирования вирусная частица непригодна из-за чрезвычайно плохой живучести вне живого организма. Не такой жизнестойкий инфекционный агент, как вирус гепатита В, для заражения требуется больше частиц, но посильнее ВИЧ. Половой путь передачи парентерального гепатита С во время случайного секса отнюдь не ведущий, его многократно опережает заражение во время медицинских манипуляций в полуподпольных косметических салонах и стоматологиях.
Современное оборудование в руках специалиста международной клиники инфекции Медика24 с большим опытом клинической работы позволяет практически во всех ситуациях выявить точную причину, вызывающую страдание, и проследить весь путь инфекции от заражения до заболевания.
Как можно заразиться?
Но это типичные группы риска, а в принципе, любой добропорядочный человек может заразиться везде, где пользуются многоразовым режущим инструментарием, например, при маникюре. В группы риска также входят и люди, которые профессионально связаны с чужой кровью – медицинские работники.
В педагогических, детских и коллективах пожилых людей, находящихся в интернатах и длительно проживающих в психиатрических учреждениях, облегчается контакт для передачи любого инфекционного агента. Пациенты с пересаженными органами или на гемодиализе, получившие чужую кровь, тоже имею причину для инфицирования. Прекрасно выживают вирусные частицы во флаконе с кровью.
Причиной выхода заболевания из-под контроля может стать обманчивая надежда, что хорошее самочувствие пациента невозможно при высокой вирусной нагрузке. Самочувствие никак не коррелирует с жизнедеятельностью инфекционного агента.
Гепатит С не передается через грязную воду или чихание, им невозможно заразиться при поцелуе и рукопожатии, и незащищенные половые контакты дают небольшую вероятность инфицирования. Вирус крайне трепетно относится к окружающей среде и быстро погибает в неудобных для его существования условиях. Зато в крови инфекционный агент прекрасно себя чувствует, поэтому передача его возможна в капле крови и необходима ранка кожи или слизистой оболочки, а лучшее средство передачи инфекции от больного здорового - шприц с остатками зараженной крови, игла и венозный сосуд. И после инкубационного периода не более 180 дней можно готовиться к лечению гепатита С.
Высокопрофессиональные специалисты и современное диагностическое оборудование международной клиники инфекционных заболеваний Медика24 позволяют выявить все предрасполагающие факторы для развития заболевания, все имеющиеся заболевания и предотвратить тяжелые осложнения.
По каким критериям оценивают эффективность терапии?
Терапия инфекции долгая, сегодня не придерживаются канонического подхода со строго определенной длительностью от 12 до 48 недель, а ориентируется по индивидуальным характеристикам вируса и пациента, и реакцию на противовирусные препараты оценивают по определенным критериям.
- Во всех случаях желаем устойчивый вирусологический ответ (УВО), когда в крови пропадает и более уже не определяется вирусная РНК.
- Быстрый ответ – в течение первых 4 недель, очень хороший результат.
- Если РНК исчезает к 12 недели терапии, это тоже считается ранним ответом.
- Когда анализ показывает снижение количества вирусный копий в 100 раз с 12 недельного срока терапии, а после 24 недель кровь чиста от инфекционного агента, то это медленный ответ.
- Признается частичный ответ при снижении численности вирусов в 100 раз, но после 24 недель агент также остается в крови.
- Отсутствует реакция на лечение, когда после 12 недели вирус снижается менее 100 раз.
- Во время лечения может случиться вирусологический прорыв – появление вируса после его отсутствия.
- Про рецидив говорят, когда терапия завершена с успехом, но через некоторое время вновь в крови появился инфекционный агент.
При обнаружении вируса гепатита С необходимо регулярное наблюдение врача, чтобы контролировать процесс жизнедеятельности вируса, вовремя выявлять его устойчивость к лекарствам.
При хронической форме гепатита С хороший эффект обещают:
- Вирус не 1 генотипа, а если 1 генотип, то с полиморфизмом гена интерлейкина 28;
- Вирусная нагрузка не выше 400 тысяч в миллилитре крови;
- Молодой возраст, желательно до 40 лет;
- Женский пол и европеоидная раса;
- Отсутствие избыточного веса, а лучше менее 75 кг;
- Минимальный фиброз печени и высокий уровень печеночных трансфераз в биохимическом анализе крови.
Можно ли вылечить острый гепатит С?
Но главное: бережливое к себе отношение с ограничением нагрузок, строгий диетический режим и обильное питьё, отказ от лекарств, приём которых не обязателен – печени и без них очень трудно.
В любом клиническом случае в международной клинике Медика24 каждый пациент получит всё возможное и необходимое лечение вируса для возвращения к жизни нормального качества.
Читайте также: