Паралич от герпеса инфекции
Обновлено: 22.04.2024
Для цитирования: Камчатнов П.Р., Евзельман М.А., Чугунов А.В. Постгерпетическая тригеминальная невралгия – возможности предупреждения и лечения. РМЖ. 2014;6:454.
В основе заболевания лежит реактивация вируса Varicella zoster, способного на протяжении длительного периода времени персистировать в ганглиях заднего рога. Соответственно, в отношении тройничного нерва областью их нахождения является гассеров узел. В случае возникновения определенных условий, благоприятных для активации вируса, развивается заболевание. Считается, что факторами риска для его реактивации являются пожилой возраст или, наоборот, инфицирование в детском возрасте (до 18 мес.), состояние иммуносупрессии различного происхождения (приобретенный иммунодефицит, онкологические заболевания, иммуносупрессивная терапия), внутриутробный контакт с вирусом ветряной оспы. Заболевание реализуется в условиях снижения клеточного иммунитета, обусловленного различными причинами.
Вирус герпеса может передаваться от человека к человеку, в частности, в тех случаях, когда индивидуум не переносил ветряной оспы или не был своевременно вакцинирован по поводу данной инфекции. Заболевание не склонно к рецидивированию. Считается, что рецидивы наблюдаются примерно у 6% пациентов, причем период от первого эпизода до рецидива может составлять несколько десятилетий [5]. Клинический опыт свидетельствует о том, что рецидив может быть обусловлен возникшим у пациента заболеванием, наличие которого негативным образом сказывается на состоянии и характере иммунного ответа.
Клинические проявления
Развитию заболевания предшествует продромальный период, который характеризуется лихорадкой, тошнотой, диффузной головной болью, которые, нарастая, могут наблюдаться на протяжении нескольких суток. Характерным является нарастание локальных болей, которые имеют характер нейропатических, а также неприятный жгучий, колющий оттенок зуда, способных сопровождаться аллодинией, гиперестезией и гиперпатией. Как правило, такого рода боли локализованы в области последующих высыпаний и ограничиваются зоной одного или нескольких соответствующих дерматомов. В подавляющем большинстве случаев указанные проявления носят односторонний характер, хотя у отдельных пациентов они могут распространяться и на противоположную половину туловища [8]. Боль может носить исключительно интенсивный характер, что нередко симулирует ряд соматических заболеваний, в частности плеврит, острый инфаркт миокарда, почечную колику. Поражение гассерова узла может вызвать трудности при проведении дифференциальной диагностики со стоматологическими заболеваниями, поражением придаточных пазух носа.
На фоне указанных симптомов появляются гиперемия и множественные макулопапулярные высыпания, которые впоследствии приобретают характер везикулярных. Пузырьки заполнены прозрачным бесцветным серозным содержимым. В случаях благоприятного течения заболевания высыпания могут быль локализованы только в отдельной части дерматома. Появление новых высыпаний возможно на протяжении 5–7 дней. Через несколько суток от момента появления первых высыпаний содержимое их становится мутным (так называемая стадия пустуляции). В последующем, при отсутствии осложнений, на месте имевшихся высыпаний образуются сухие корочки, которые отпадают через 2–3 нед. В этих зонах могут оставаться рубцовые изменения или зоны измененной пигментации. Заболевание, как правило, имеет благоприятный прогноз, характеризуется монофазным течением и в незначительной степени обладает тенденцией к рецидивированию.
Диагностика может быть затруднена до появления характерных высыпаний. После их возникновения правильная постановка диагноза обычно не вызывает трудностей. Подтверждение диагноза возможно при проведении полимеразной цепной реакции, позволяющей выявить ДКН вируса Varicella zoster в содержимом имеющихся высыпаний.
Осложнения
Среди возможных осложнений следует отметить локальные инфекционные поражения, обусловленные инфицированием поврежденных кожных покровов стрептококком или стафилококком, вплоть до развития целлюлита. При вовлечении в патологический процесс офтальмической ветви тройничного нерва возможно развитие кератита, способного привести к тяжелым последствиям в виде поражения роговицы, вплоть до монокулярной слепоты. Редко встречаются поражения герпетической инфекцией ткани головного мозга (с развитием энцефалита) или его оболочек с возникновением серозного менингита.
Одним из наиболее частых и достаточно тяжелых осложнений ганглионита гассерова узла, обусловленного герпетической инфекцией, является постгерпетическая невралгия. Патогенез указанного состояния достаточно сложен и включает в себя по меньшей мере два основных механизма [5]. Во-первых, в его развитии принимает участие повышение возбудимости первичных афферентов вследствие поражения периферических нейронов. В результате этого возникают избыточная возбудимость ноцицепторов и, как следствие, формирование центральной сенситизации. Клинически такая совокупность патофизиологических процессов проявляется возникновением боли и развитием аллодинии. Во-вторых, вследствие дегенерации ноцицептивных нейронов возникает деафферентация вышерасположенных сенсорных систем, обусловливающая их гиперактивность. В результате этого наблюдается формирование боли, которая, однако, не сопровождается аллодинией. По мнению авторов, у одного пациента возможно сочетание обоих механизмов, с чем связано своеобразие болевого синдрома и различий в эффективности проводимой терапии.
Данное патологическое состояние характеризуется всеми типичными для нейропатического болевого синдрома клиническими характеристиками. Установление диагноза возможно в том случае, если боль сохраняется на протяжении не менее 30 сут после наступления полного заживления имеющихся высыпаний.
Факторами риска развития постгерпетической тригеминальной невралгии являются возраст старше 60 лет, женский пол, наличие продромального периода, множественность высыпаний, а также высокая интенсивность болевого синдрома в дебюте заболевания [6]. По мнению авторов исследования, болевой синдром умеренной интенсивности, не сопровождающийся развитием в последующем постгерпетической невралгии, наблюдается у более молодых пациентов и, вероятно, связан с обширным локальным повреждением тканей и воспалительным процессом при наличии множественных высыпаний. Следует подчеркнуть значимость возрастного фактора как важного предиктора развития болевого синдрома – у пациентов, перенесших опоясывающий герпес в возрасте старше 90 лет, постгерпетическая невралгия возникает примерно в половине случаев [5]. Неблагоприятным прогностическим фактором развития болевого синдрома является выявление вируса Varicella zoster в крови.
Как и в отношении подавляющего большинства хронических нейропатических болевых синдромов, исключительно важную роль в развитии постгерпетической невралгии играет совокупность психосоциальных факторов. Наличие предшествующих депрессивных и тревожных расстройств, недостаточная социальная адаптированность пациента, нарушение социальных связей, проживание вне семьи и др. могут повышать вероятность развития болевого синдрома.
Течение постгерпетической невралгии может быть различным. У части пациентов наблюдается значительный регресс или полное исчезновение имеющегося болевого синдрома за период времени около полугода. К сожалению, возможно менее доброкачественное течение, когда болевой синдром приобретает хронический характер и приводит к инвалидизации пациента и резкому снижению качества его жизни [10]. Риск возникновения тяжелого болевого синдрома нарастает с возрастом, так, более чем у 5% пожилых больных интенсивный болевой синдром сохраняется более 12 мес. [5]. Особенности течения заболевания могут быть связаны с различиями патогенеза болевого синдрома, направленностью и интенсивностью компенсаторных реакций организма, а также с эффективностью и адекватностью проводимой терапии, в частности, ее своевременным началом.
Достаточно часто наряду с развитием постгерпетической невралгии у пациентов наблюдаются двигательные нарушения в виде периферических парезов черепных нервов (наиболее часто – лицевого нерва) [1]. Данная форма герпетической инфекции известна в качестве синдрома Рамсея Ханта. Не получено убедительных данных о прогностической значимости моторных нарушений в отношении частоты и длительности болевого синдрома.
Лечение
Вероятно, несоблюдение указанного правила привело к тому, что результаты систематизированного обзора, посвященного изучению результатов противовирусной терапии, не смогли подтвердить ее эффективность в отношении предупреждения развития невралгии через 4 и 6 мес. после появления высыпаний [7]. Эти данные свидетельствуют о необходимости правильного выбора пациентов для достижения желаемого эффекта и своевременного начала лечения.
Для достижения терапевтического эффекта в виде уменьшения риска развития постгерпетической невралгии необходимо применение валацикловира (Вирдел) в суточной дозе 1000 мг 3 раза на протяжении 7 сут. Возможно использование и местных лекарственных форм противовирусных препаратов, но достижение терапевтического эффекта возможно только при их системном введении в адекватных суточных дозировках и достаточном сроке лечения. Препарат Вирдел хорошо переносится, возможно его одновременное применение с другими лекарственными средствами.
В качестве средства, потенцирующего лечебные эффекты валацикловира, предлагается одновременное назначение глюкокортикоидов. Имеются данные о том, что комбинированная терапия способна снизить интенсивность болевого синдрома в острой стадии заболевания [12]. Менее убедительны сведения о способности глюкокортикоидов уменьшить риск формирования постгерпетической невралгии. Авторы проведенных в этом направлении исследований указывают на то, что использование глюкокортикоидов ассоциировано с повышенным риском развития нежелательных побочных эффектов, в частности, обострения язвенной болезни желудка, гипергликемии, присоединения локального инфекционного процесса, причем частота такого рода осложнений повышается с возрастом. Несомненно, что проведение комбинированной терапии требует всестороннего учета возможного положительного ее эффекта и связанного с лечением риска побочных реакций, обусловленного состоянием конкретного пациента.
В том случае, если у больного имеется стойкая постгерпетическая невралгия, наблюдающаяся в отдаленном периоде после заживления высыпаний, лечение больного требует других подходов. В данной ситуации могут быть использованы представители трициклических антидепрессантов (амитриптилин, нортриптилин), которые обладают достаточно высокой эффективностью. Вместе с тем, несмотря на хороший противоболевой эффект, широкое применение этих препаратов ограничивается частым возникновением нежелательных побочных реакций, в особенности при их назначении в высоких дозировках. Достижение противоболевого эффекта при снижении риска побочных эффектов возможно за счет назначения антидепрессантов, обладающих способностью ингибировать обратный захват как серотонина, так и норадреналина. Следует отметить, что противоболевой эффект антидепрессантов при постгерпетической невралгии, как и при других нейропатических болевых синдромах, не связан только с их антидепрессивным эффектом.
Для лечения пациентов с постгерпетической невралгией традиционной широко применяются противоэпилептические препараты, в частности карбамазепин. В настоящее время распространение получили новые лекарственные средства, фармакологические эффекты которых реализуются вследствие взаимодействия с рецепторами гамма-аминомасляной кислоты – основного тормозного медиатора в центральной нервной системе (габапентин, прегабалин). Отмечается их лучшая переносимость по сравнению с противоэпилептическими препаратами предыдущих поколений. В ряде стран при постгерпетической невралгии используются слабые или даже сильные опиоиды.
Интерес представляет возможность применения локальных форм лекарственных препаратов. Так, показано, что местное использование препаратов лидокаина может быть целесообразным при наличии болевого синдрома, сопровождающегося аллодинией. Имеются также сведения о возможной эффективности капсаицина у пациентов с постгерпетической невралгией. Следует отметить, что его широкое применение ограничивается не всегда удовлетворительной переносимостью терапии.
Таким образом, имеющиеся сведения об эффективности использования валацикловира (Вирдел) у пациентов с опоясывающим герпесом позволяют рекомендовать его широкое применение у данного контингента больных. Своевременное начало лечения, правильный отбор больных для назначения препарата способны повысить эффективность проводимой терапии, профилактировать развитие постгерпетической невралгии.
Герпетический энцефалит. Поражение нервной системы вирусом герпеса
К вирусам герпеса относятся:
• вирус простого герпеса I и II типов,
• вирус Варицелла-Зостер,
• цитомегаловирус,
• вирус Эпштейна-Барр.
Энцефалит, вызываемый вирусом простого герпеса, — самая частая спорадическая форма острого очагового энцефалита, возбудителем которой в подавляющем большинстве случаев служит вирус простого герпеса I типа.
Вопрос о том, возникает ли заболевание в результате первичното инфицирования вирусом через обонятельную систему или реактивации латентной вирусной инфекции, персистируюшей в организме, остается открытым.
Клиническая картина характеризуется лихорадкой, головной болью, спутанностью сознания, необычным поведением, сонливостью, менингеальным синдромом, эпилептическими припадками (генерализованными, сложными парциальными), афазией, очаговыми двигательными и чувствительными нарушениями, а также верхнекватрантной гемианопсисй.
На основании клинической картины герпетический энцефалит трудноотличим от других вирусных энцефалитов или заболеваний, с которыми проводится их дифференциальная диагностика.
Изменения в ЦСЖ также соответствуют общим изменениям при вирусных энцефалитах. Диагностически важными являются КТ и особенно МРТ.
На КТ выявляются гиподенсивные очаги, а на МРТ — очаги с измененной интенсивностью сигнала в медиальной области височных долей с распространением на латеральные отделы базальных ганглиев и инсулярную кору.
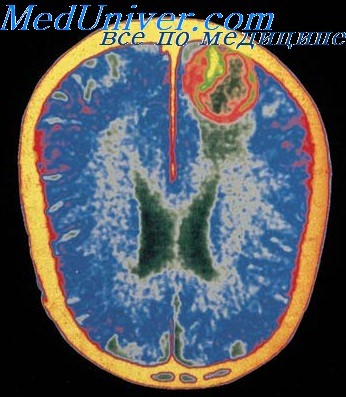
Одновременно наблюдается отек мозга, способный вызвать масс-эффект и привести к транстенториальпому вклинению. Возможны кровоизлияния в зоне воспаления. Поражение мозга в большинстве случаев резко асимметрично, поэтому дифференциальная диагностика с инсультом бывает затруднена.
Однако при инсультах практически не наблюла ется одновременного поражения зоны кровоснабжения средней (инсулярная кора, базальные ганглии) и задней (медиальные отделы височных долей) мозговых артерий. На ЭЭГ наблюдаются одно- или двусторонние периодические острые волны, регистрирующиеся каждые 2-3 секунды нал височными областями.
Серологическое исследование, выявляющее рост титра антител, не имеет значения для выбора лечения. Более раннее подтверждение диагноза можно получить с помощью ПЦР или биопсии мозга. Однако биопсия мозга редко бывает необходима лля диагностики.
Средством выбора является ацикловир (10 мг/кг в/в каждые 8 часов в течение 10 дней). С появлением ацикловира летальноегь снизилась с 60-70 до 30%. Эффективен также фоскарнет.
Вирус простого герпеса II типа вызывает генитальный герпес, но может также служить возбудителем асептического менингита, зостероподобной невропатии, вызывать задержку мочи, а у лип с иммунодефицитом — диффузный энцефалит. вирус оНоясывающего герпеса (варипелла-зостер) у детей вызывает ветряную оспу.
У взрослых может происходить реактивация вируса, приводящая к опоясывающему герпесу, что особенно часто наблюдается у пациентов с иммунодефицитом. Осложнением опоясывающего герпеса могут быть энцефалит или гранулематозный ангиит, поражающий крупные мозговые артерии. Может наблюдаться и ангиит более мелких сосудов.
Лечение состоит в применении ацикловира, валациклонира и фамцикловира, которые одинаково эффективны при заболеваниях, вызываемых вирусом варицелла-зостер.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Паралич лицевого нерва - паралич Белла. Токсичные для ушей лекарства
Паралич Белла — это острый односторонний паралич без установленной причины. Один из возможных этиологических факторов — вирус простого герпеса 1-го типа. Опоясывающий ушной герпес (ОУГ) вызывает острый лицевой паралич, сопровождающийся болью и патологическими изменениями, сходными с оспой, которые затрагивают ушную раковину, точнее, центральный участок вогнутой поверхности внешнего уха. Очевидно, это происходит из-за оспенно-герпесной вирусной инфекции коленчатого ганглия. Зачастую поражается черепно-мозговой нерв, что приводит к тяжелой нейросенсорной тугоухости наряду с утратой вестибулярной функции. Отек блокирует лицевой нерв в том месте, где он проходит через узкую фаллопиеву трубу, что ведет к ишемии и дисфункции нервной системы.
Применение глюкокортикостероидов для лечения острого паралича лицевого нерва остается предметом дискуссий. Эти препараты не показаны при неполном параличе лицевого нерва, поскольку обычно он полностью проходит без лечения. При полном параличе Белла или ОУГ глюкокортикостероиды следует назначать в течение 10 сут с момента проявления симптомов, а затем постепенно снижать дозу.
Ацикловир (ациклогуанозин) является аналогом нуклеозидов, который подавляет воспроизводство ДНК вирусов и уменьшает функциональный дефицит у пациентов с ОУГ на фоне сниженного иммунитета. Польза ацикловира в лечении паралича Белла не доказана. В идеале лечение необходимо начать как можно раньше, после проявления первых симптомов — в пределах 72 час после начала заболевания.
Токсичные для ушей лекарства
Поражение внутреннего уха может быть вызвано четырьмя классами клинически важных лекарств. Возможно нарушение как слуха, так и равновесия. Шум в ушах — дополнительный симптом, сопровождающий вызванную лекарствами ототоксичность.
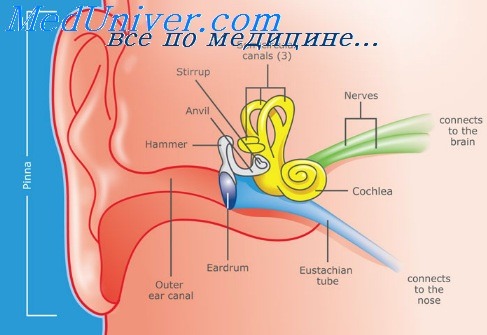
Противомикробные препараты. У аминогликозидных антибиотиков наблюдается побочное действие на почки и на внутреннее ухо. Стрептомицин и гентамицин оказывают наибольшее токсическое воздействие на вестибулярный аппарат, а канамицин, тобрамицин и амикацин — на волосковые сенсорные клетки улиткового лабиринта. Гентамицин вызывает поражение внутреннего уха приблизительно у 5% пациентов. По некоторым данным, потеря слуха при лечении нетилми-цином происходит у 1 пациента из 250, а вестибулярная дисфункция — у 1 из 150.
Аминогликозиды связывают наружную поверхность волосковой мембраны и блокируют проходящие через нее каналы Са2+. Препараты этой группы также соединяются с бифосфатом фосфатидилинозитола внутренней поверхности клеточной мембраны. Подавление внутриклеточного Са2+ и процессов, регулируемых полиаминами, наносит дополнительный ущерб мембране и постепенно ведет к гибели клеток. Возникающая ототоксичность может быть как обратимой, так и тяжелой или необратимой, при которой часто встречаются не поддающиеся лечению ограничения слуха. Поскольку состояние некоторых пациентов, нуждающихся в аминогликозидах, характеризуется слабостью, их жалобы на головокружение и шум в ушах могут быть проигнорированы, особенно если пациент прикован к постели.
Слишком часто длительную вестибулярную токсичность у амбулаторных пациентов распознают на поздних стадиях, когда развиваются:
• непереносимость движения;
• осциллопсия (трудности при стабилизации взгляда во время движений головы);
• атаксия.
Необходимо выявлять пациентов с повышенным риском аминогликозидной ототоксичности, контролировать концентрацию сыворотки крови и как можно скорее переводить таких пациентов на антибактериальные препараты без ототоксичного побочного действия. Измерение слуховой функции, например, с помощью последовательной аудиометрии — хороший способ раннего определения ототоксичности. Слух может быть ослабленным даже при таких концентрациях сыворотки крови, которые сопоставимы с нормой. Концентрация аминогликозидов в перелимфе улиткового лабиринта зависит от времени и от плазмы. Как следствие такой ототоксичности, аминогликозиды следует назначать самыми малыми эффективными дозами в течение возможно более короткого времени.
Гликопептидные антибиотики, например ванкомицин, все больше употребляют в связи с растущей проблемой антибактериальной устойчивости. Механизм ототоксичности, вызванной гликопептидными антибиотиками, неясен, но схема утраты внешних волосковых сенсорных клеток, предшествующая утрате внутренних, такая же, как и у аминогликозидов.
Пример лечения паралича лицевого нерва после герпеса (Herpes zoster oticus)
32-летний мужчина отмечает паралич правого лицевого нерва в течение двух недель. Глазная щель не смыкалась, подвижность правой половины лица отсутствовала (Н-В VI/VI). Появлению паралича предшествовал разрыв пузырьков вокруг правого уха и в нижней части лица в области иннервации ЧН V. Пациент обратился за помощью спустя восемь дней после появления паралича.
Отоскопическая картина была нормальной. Рядом с правой ушной раковиной у пациента обнаружилось несколько заживающих пузырьков, в ротоглотке или носоглотке высыпаний не было. При обследовании камертоном 512 Гц каких-либо отклонений обнаружено не было, слух в норме. По результатам ЭНГ дегенерации подверглось 64% волокон седьмого черепного нерва справа.
До этого пациенту уже были назначены кортикостероиды в очень низкой дозе. Режим дозирования был изменен на 60 мг преднизона в день с последующим снижением дозы. В течение семи дней он уже получал фамцикловир в дозе 2 г в день, в продолжении противовирусной терапии смысла не было.
Днем пациент применял искусственную слезу, на ночь наносил лубриканты, тем не менее, в течение дня его все равно беспокоила сильная сухость глаза. Примерно через неделю после обращения в верхнее веко был установлен золотой грузик. При повторных ЭНГ уровень дегенерации не опускался ниже 62%. На второй неделе после обращения появилась небольшая подвижность в правой лобной области.
Постепенно подвижность правой половины лица восстановилась, синкинезии не появлялись. Пациент находился под наблюдением в течение трех лет, на протяжении которых функция лицевого нерва была нормальной (H-BI).
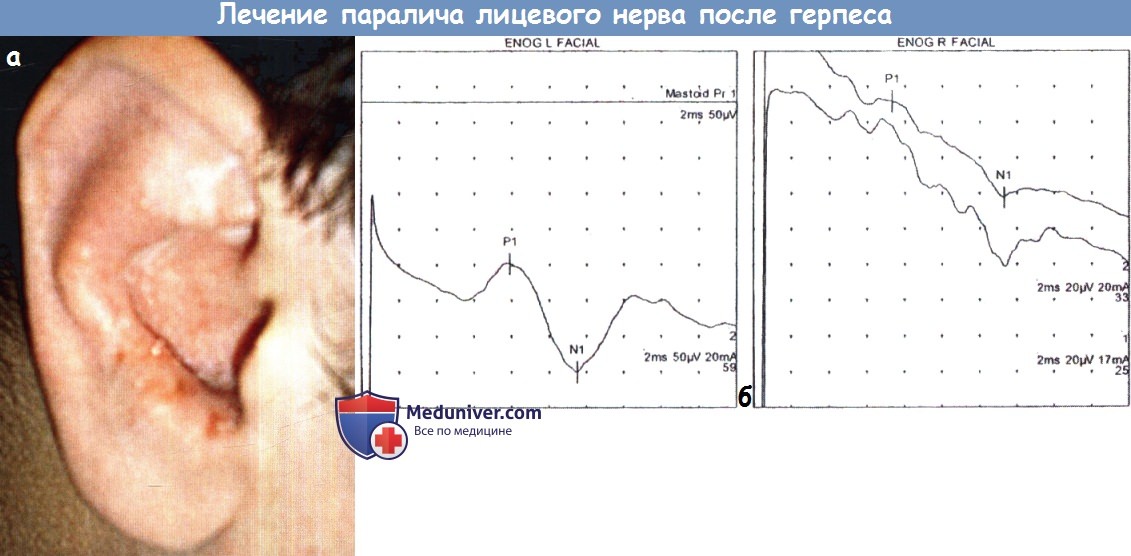
а - Везикулярные высыпания на нижних отделах правой ушной раковины.
б - ЭНГ через три дня после появления паралича правого лицевого нерва, определяется его частичная дегенерация.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Герпетический энцефалит — это диффузное или очаговое поражение мозгового вещества, вызванное герпесвирусами ВПГ-1, ВПГ-2, Varicella Zoster. Основные симптомы болезни: фебрильная лихорадка, прогрессирующее угнетение сознания, судорожные приступы. По завершении острого периода инфекции в течение длительного времени сохраняются резидуальные неврологические нарушения. Для установления диагноза необходимо проведение ПЦР-диагностики ликвора, томографии головного мозга, электроэнцефалограммы. Лечение патологии включает противовирусные препараты, противоотечную, нейрометаболическую и противосудорожную терапию.
МКБ-10
Общие сведения
Энцефалит герпетического происхождения составляет до 15-20% всех вирусных воспалительных процессов в мозговой ткани. Симптомы встречаются с частотой 4-5 случаев на 1 млн. населения, причем до трети больных составляют дети, а еще около 20% приходится на возрастную категорию старше 60 лет. Заболевание не теряет своей актуальности в современной неврологии, поскольку для успешного исхода патологии необходимо вовремя поставить диагноз и начать лечение, а промедление в оказании медицинской помощи чревато смертью пациента.

Причины
Болезнь в 95% случаев вызывается вирусом простого герпеса 1 типа, что объясняется высокой распространенностью возбудителя. По данным ВОЗ, около 2/3 населения мира в возрасте до 50 лет инфицированы ВПГ-1. На втором месте по частоте находится Varicella Zoster Virus (VZV) — возбудитель ветряной оспы, опоясывающего герпеса. Энцефалит, вызванный ВПГ-2, встречается редко, преимущественно у иммунокомпрометированных пациентов.
Ведущим среди факторов риска служит сниженный иммунный статус. Герпетическая инфекция протекает латентно, активизируется на фоне нарушения общей резистентности организма (при переохлаждении, стрессе, менструации у женщин). В группе риска находятся люди с врожденными и приобретенными иммунодефицитами, больные, получающие лечение иммуносупрессивными препаратами. К триггерам относят реинфицирование другими штаммами герпесвирусов, сопровождающееся аутоиммунными реакциями.
Патогенез
Первичное заражение ВПГ-1, как правило, происходит в детстве при попадании вирусных частиц на слизистые оболочки, после чего возбудитель начинает размножаться, мигрирует в нервные ганглии, где длительное время находится в состоянии латентной инфекции. Заражение ВПГ-2 наблюдается после начала сексуальной жизни через слизистые половых путей, а дальнейший путь развития патогена сходен с ВПГ-1.
Симптомы болезни в большинстве случаев возникают при реактивации инфекции под действием провоцирующих факторов. Герпесвирусы проникают в головной мозг гематогенным путем либо по нервным стволам (через тройничный или обонятельный нерв). Из гассерова узла они распространяются на таламус, подкорковые ядра, кору больших полушарий. При распространении по ольфакторному тракту первой страдает лимбическая система (гиппокамп, височная кора).
Симптомы герпетического энцефалита
В типичном течении острого мозгового воспаления выделяется несколько последовательных стадий: ранняя, период разгара болезни, регресс признаков, стадия остаточных явлений. В 70% патология манифестирует с внезапно возникшей высокой лихорадки (более 39°С), сопровождающейся интенсивными головными болями в лобно-височной зоне, сильной сонливостью, рвотой, не связанной с приемом пищи.
На вторые-третьи сутки симптомы дополняются нарушениями сознания: больные начинают путаться во времени и пространстве, не узнают родственников, испытывают разнообразные галлюцинации. По мере усугубления тяжести состояния появляются фокальные или генерализованные судорожные припадки. Изредка наблюдается оперкулярный автоматизм — повторяющиеся причмокивающие или сосательные движения.
В среднем через 3 дня заболевание переходит в стадию разгара. Основное проявление — глубокое угнетение сознания вплоть до комы. Пациенты не отвечают на звуковые и тактильные раздражители, однако двигательные реакции на болевые стимулы остаются в пределах нормы. Также могут возникать симптомы декортикации или децеребрации, аритмичное дыхание, двусторонние моторные нарушения.
Если пациенту было предоставлено комплексное лечение, с 3-4 недели начинается обратное развитие симптомов герпетического энцефалита. Этот этап длится от нескольких месяцев до 1 года, характеризуется постепенным восстановлением временно утраченных неврологических функций. По окончании третьей стадии около 80% больных имеют стойкие резидуальные (остаточные) явления, которые могут сохраняться пожизненно.
Осложнения
В остром периоде прогностическим неблагоприятным является прогрессирование отека мозга, что чревато его вклинением. При височно-тенториальной форме вклинения возникает триада признаков: потеря сознания, гемипарез, анизокория. Симптомами транстенториальной формы являются отсутствие реакции зрачков на свет, фиксация глазных яблок по срединной линии, двусторонний гипертонус мышц. Зачастую нарушается работа дыхательного центра.
Патология имеет тяжелое течение, при отсутствии своевременной медицинской помощи летальность достигает 70%. Даже если проводится этиотропное лечение, смертельный исход регистрируется у 15-20% пациентов, чаще у младенцев, пожилых людей, больных из группы риска. У выздоровевших полный регресс неврологической симптоматики наблюдается только в 20% случаев, а остальные сталкиваются с резидуальными симптомами.
Наиболее опасным хроническим осложнением заболевания считается прогрессирующее вегетативное состояние (акинетический мутизм), характеризующийся необратимым разрушением высших психических функций. У больных сохранено сознание, витальные функции (дыхание, кровообращение), однако полностью отсутствует познавательная деятельность. Такие пациенты не говорят, не реагируют на внешние раздражители, требуют постоянного ухода.
К типичным последствиям герпетической формы энцефалита относится синдром Клювера-Бьюси, при котором развиваются тяжелые длительные расстройства психической и когнитивной сферы. Симптомы расстройства включают ажитированное состояние, агрессивность, патологическую гиперсексуальность. Также наблюдаются интеллектуальные нарушения, проблемы с концентрацией внимания, ослабление памяти.
Диагностика
Обследованием пациента занимаются инфекционисты, неврологи, врачи экстренной помощи и реанимационного отделения. Заподозрить энцефалит удается по острому началу, наличию фебрильной лихорадки, сочетанию общемозговых и очаговых симптомов. Для подтверждения заболевания, уточнению этиологии воспалительного процесса назначаются следующие методы исследования:
Лечение герпетического энцефалита
Консервативная терапия
Герпетический энцефалит характеризуется быстрым нарастанием неврологического дефицита, прогрессированием общемозговых симптомов, поэтому комплексное лечение должно начинаться в максимально ранние сроки. Наилучшие шансы на полное выздоровление у пациентов, которые начали получать этиотропные препараты в первые сутки манифестации болезни. Лечение заболевания включает следующие группы медикаментов:
Реабилитация
Благотворное влияние на состояние ЦНС после перенесенного герпетического энцефалита оказывают витаминные комплексы (витамины группы В, аскорбиновая кислота) в сочетании с антиоксидантами. Восстановительное лечение также включает ноотропы и нейрометаболические препараты для улучшения когнитивных мозговых функций. Коррекция иммунологического статуса проводится адаптогенами, актопротекторами, неспецифическими иммуномодуляторами.
Для восполнения энергозатрат организма, стимуляции репаративных процессов показано адекватное по калорийности и витаминному составу энтеральное питание. Большое внимание уделяется физиотерапевтическим процедурам, массажу и лечебной физкультуре, направленным на улучшение двигательной функции. При наличии показаний рекомендуются занятия с логопедами, дефектологами.
Прогноз и профилактика
Несмотря на проводимое этиотропное лечение, прогноз при герпетическом энцефалите остается неблагоприятным, показатель летальности составляет 15-20%. У большинства выздоровевших сохраняется неврологический дефицит. Для предупреждения заболевания необходима рациональное лечение герпеса кожи и слизистых оболочек, своевременное консультирование больных с диссеминированной герпетической инфекцией.
2. Менингиты и энцефалиты: уч. пос. для врачей/ Д. А. Валишин, Р. Т. Мурзабаева, А. П. Мамон, М. А. Мамон, Л. В. Мурзагалеева. — 2012.
3. Герпетическое поражение нервной системы/ М.Н. Лебедюк, М.Э. Запольский, Ю.И. Горанский// Украинский журнал дерматологии, венерологии, косметологии. — 2011. — №2.
4. Герпетический энцефалит/ Т.В. Матвеева, Н.В. Токарева, Г.А. Шакирзянова// Неврология. — 2006. — №16.
Читайте также:

