Переходно клеточная папиллома лоханки
Обновлено: 18.04.2024
Второй характеристикой опухоли почки, как впрочем и большинства других опухолей, является потеря спецификации клетки – так как клетка быстро делится, она просто не успевает специализироваться. Таким образом, опухоль почки в первом приближении можно характеризовать, как массу клеток, бесконтрольно делящихся и потерявших способность к специализации. Чем меньше специализирована клетка опухоли для выполнения своей функции, чем быстрее она делится и чем больше его способность к распространению по кровеносным и лимфатическим сосудам, тем опухоль злокачественнее.
Почти 90 % опухолей почки злокачественны. Оставшиеся 10 процентов приходятся на ангиомиолипомы и другие, гораздо более редкие доброкачественные опухоли почки. Между тем, даже доброкачественные опухоли почки вполне могут быть опасны для здоровья. Например, ангиомиолипома может повредить сосуды почки, вызывая кровотечение. Что же касается злокачественных опухолей или рака почки, то тут мы сталкиваемся с повреждением функционирующей почечной ткани, ее сосудов и кровотечением, с метастазированием в кости, легкие, головной мозг и, соответственно, нестерпимыми болями.
Метастазы рака почки
Метастазирование — это распространение опухоли по кровеносным или лимфатическим сосудам. Опухоли, как и всему живому в организме, требуется питание, обеспечиваемое сосудами. Вот в эти сосуды и попадают 1-2 клетки из основной опухоли, которые распространяются на различные органы. Для рака почки характерно метастазирование в кости и легкие, а также в печень, надпочечники и головной мозг.
Как часто и у кого встречается
Причины рака почки
Основными факторами, увеличивающими риски развития рака почки являются:
- Курение — повышает вероятность развития почечно-клеточного рака по сравнению с некурящими людьми.
- Артериальная гипертензия.
- Ожирение. Также повышает вероятность развития почечно-клеточного рака по сравнению с теми, у кого нет избыточной массы тела.
- Сахарный диабет.
- Длительный прием мочегонных препаратов.
Симптомы рака почки: когда нужно посетить врача?
В некоторых случаях рак почки удается выявить на ранних стадиях, когда опухолевые клетки не распространяются за пределы органа. Но зачастую заболевание диагностируют на более поздних стадиях. Во-первых, это связано с тем, что рак почки может очень долго протекать бессимптомно. Во-вторых, для этого типа рака на данный момент не существует рекомендованных скрининговых исследований.
Все симптомы можно разделить на ренальные (связанные с поражением почек) и экстраренальные.
Среди ренальных проявлений рака почки наиболее характерны три:
- Гематурия (примесь крови в моче) – самый распространенный и зачастую первый симптом. Он возникает более, чем у половины пациентов с раком почки. Моча приобретает красный цвет, при этом боль не беспокоит либо носит острый характер и возникает после гематурии. Этим злокачественная опухоль отличается от неопухолевых заболеваний почки, например, мочекаменной болезни, при которой обычно сначала возникает боль, а потом появляется примесь крови в моче. Гематурия периодически исчезает, но через некоторое время снова появляется, причем промежутки между кровотечениями сокращаются. Количество крови в моче не зависит от размеров опухоли.
- Боли беспокоят около половины пациентов. Острая боль после гематурии возникает из-за того, что сгустки крови перекрывают просвет мочеточника. Тупые сильные боли зачастую говорят о плохом прогнозе.
- Пальпируемая опухоль – симптом, который выявляет врач во время осмотра примерно у трети пациентов.
Все три симптома одновременно встречаются у одного из десяти пациентов с раком почки. Обычно при этом выявляют запущенные опухоли.
Среди экстраренальных симптомов в первую очередь стоит отметить повышение температуры тела. У 5% больных лихорадка – единственное проявление заболевания. У некоторых пациентов повышается артериальное давление, отмечается покраснение лица из-за увеличения количества эритроцитов в крови, у мужчин – расширение вен мошонки (варикоцеле). На поздних стадиях снижается аппетит, пациент теряет вес без видимой причины, постоянно ощущает утомление, недомогание.
Диагностика
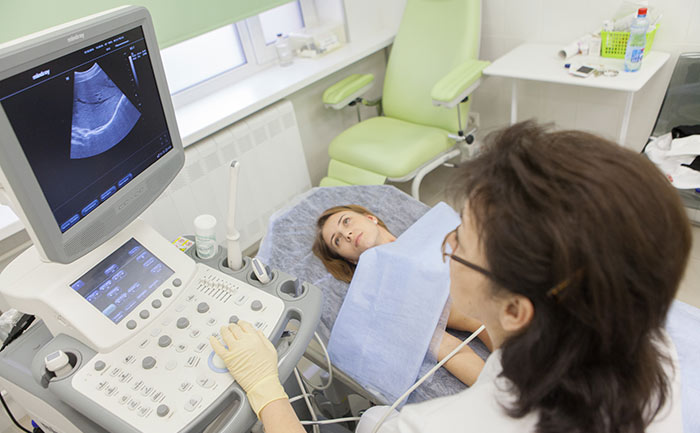
При подозрении на рак почки пациенту назначают общий анализ мочи, общий и биохимический анализы крови.
Один из наиболее информативных методов диагностики рака почки – компьютерная томография. Она помогает оценить размер, форму и локализацию злокачественного новообразования, обнаружить очаги в лимфатических узлах и других анатомических структурах за пределами почек. Исследование нередко дополняют внутривенным контрастированием. Введение контраста противопоказано при нарушении функции почек.
Магнитно-резонансную томографию применяют реже, чем КТ. Она показана, когда пациенту нельзя проводить компьютерную томографию с контрастом, если имеется подозрение на прорастание опухоли в нижнюю полую вену или другие крупные сосуды, для обнаружения метастатических очагов в головном и спинном мозге.

Ангиография – рентгенография с контрастирование сосудов, почки. Она помогает в диагностике заболевания и планировании хирургического лечения.
Позитронно-эмиссионная томография помогает обнаружить вторичные очаги рака в различных частях тела. Суть метода в том, что в организм пациента вводят вещество, которое обладает слабой радиоактивностью и накапливается в опухолевых клетках. Затем выполняют снимки с помощью специального аппарата, и на них опухолевые очаги хорошо видны.
В отличие от других онкологических заболеваний, биопсия при раке почки проводится редко. Обычно результатов других исследований хватает для того, чтобы принять решение о необходимости хирургического вмешательства. Уже после операции удаленную опухоль направляют в лабораторию, чтобы подтвердить диагноз. Биопсию проводят, если другие исследования не позволяют разобраться, показана ли операция. В случаях, когда хирургическое вмешательство противопоказано, исследование опухолевой ткани помогает определиться с тактикой лечения.
Всегда ли нужна операция при раке почки?

Сколько живут после операции по поводу рака почки?
Это зависит главным образом от стадии, на которой была диагностирована опухоль, и начато лечение. Пятилетняя выживаемость (процент пациентов, оставшихся в живых спустя 5 лет) наиболее высока для I стадии и составляет 81%. На II и III стадиях она, соответственно, составляет 74 и 53%. При IV стадии — 8%.
Как врач определяет стадию рака почки и на чем основывается, предлагая тот или иной метод лечения?
Стадия рака почки зависит от размеров и расположения опухоли. Так, рак почки первой стадии — это опухоль меньше 7 см, не выходящая за пределы почки. Рак почки второй стадии — это опухоль меньше 10 см, также не выходящая за пределы почки. А вот рак почки третьей стадии — это уже опухоль любых размеров, ограниченная почкой, либо повреждающая надпочечник, почечную вену, но имеющую метастаз в ближайших лимфатических узлах. Рак почки четвертой стадии может быть любых размеров, однако при этой стадии опухоль либо выходит за пределы почечной фасции, либо имеются больше одного метастаза в ближайших лимфатических узлах, либо имеются метастазы в легкие, кости, печень или головной мозг.
Стадию рака почки определяют в соответствии с международной классификацией TNM. Рядом с каждой из трех букв аббревиатуры указывают индекс, описывающий характеристики первичной опухоли (T), поражение регионарных лимфатических узлов (N), наличие отдаленных метастазов (M):
T1 — опухоль, находящаяся в пределах границ почки и имеющая наибольший диаметр не более 4 см (T1a) или 4–7 см (T1b).
T2 — опухоль, находящаяся в пределах границ почки и имеющая наибольший диаметр 7–10 см (T2a) или более 10 см (T1b).
T3 — злокачественное новообразование распространяется на почечную вену и ее ветви, на надпочечник на одноименной стороне, паранефральную клетчатку, не прорастая фасцию Героты (T3a), на нижнюю полую вену ниже (T3b) или выше (T3c) диафрагмы или врастает в стенку вены.
T4 — опухоль распространяется за пределы фасции Героты.
N0 — опухолевые очаги в регионарных лимфоузлах отсутствуют.
N1 — обнаруживается опухолевый очаг в одном лимфоузле.
N2 — обнаруживаются опухолевые очаги в двух и более регионарных лимфоузлах.
M0 — отдаленных метастазов нет.
M1 — отдаленные метастазы присутствуют.
В зависимости от значений T, N и M, выделяют четыре стадии рака почки:
- Стадия I: опухоль в почке не более 7 см (T1), лимфоузлы не поражены, отдаленных метастазов нет.
- Стадия II: первичная опухоль более 7 см (T2), отсутствуют очаги поражения в лимфатических узлах и отдаленные метастазы.
- Стадия III: злокачественная опухоль распространяется на соседние структуры (T3) и/или поражен один регионарный лимфатический узел (N1).
Стадия IV: опухоль распространяется на соседние структуры (T4), либо поражено 2 и более регионарных лимфоузла (N2), либо обнаружены отдаленные метастазы (M1).
Почему в одном случае при опухоли почки размером в 2 см предлагается удаление почки, а в другом случае опухоль достигает 5 см, но врач говорит о возможности удаления только опухоли с сохранением почки?
Опухоль почки размером 2 см может быть расположена вблизи почечных сосудов и ее удаление технически может быть невозможным. Однако данные литературы указывают, что если нет метастазов в лимфатические узлы и отдаленные органы, то опухоль почки до 7 см можно удалять с сохранением почки, что, безусловно, лучше полного удаления почки и инвалидизации пациента.
Как лечат злокачественные опухоли почки?
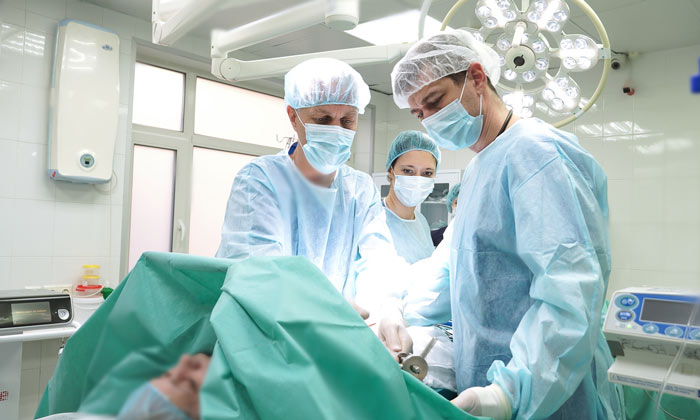
Лечение на разных стадиях
Выбор тактики лечения при раке почки в первую очередь определяется стадией опухоли и состоянием здоровья пациента.
При стадиях I и II возможно хирургическое лечение. Стандартным вариантом считается нефрэктомия. К органосохраняющим операциям прибегают реже, в частности, при опухолях в единственной почке. Кроме того, на выбор объема операции влияет размер опухоли. Также удаляют близлежащие лимфатические сосуды, особенно если они увеличены, окружающую жировую клетчатку.
При III стадии рака почки основным методом лечения также является нефрэктомия, при этом должны быть удалены все регионарные метастазы. Если опухоль прорастает в почечную или нижнюю полую вену или мигрирует в их просвете в виде опухолевого тромба, пораженные ткани также нужно удалить, при этом может потребоваться подключение пациента к аппарату искусственного кровообращения.
При высоком риске рецидива после операции применяют адъювантную терапию таргетным препаратом сунитинибом. Пациенты получают его в течение года.
Если хирургическое вмешательство противопоказано, прибегают к радиочастотной аблации, эмболизации.
На IV стадии подходы к лечению могут быть разными, в зависимости от степени распространения рака в организме. В некоторых случаях возможно хирургическое лечение, в том числе циторедуктивные операции, во время которых хирурги не могут убрать опухоль полностью, но стараются удалить как можно больший ее объем. В редких случаев возможно удаление основной опухоли в почке и единичных вторичных очагов в других органах. После операции назначают курс таргетной терапии, иммунотерапии.
При неоперабельном раке почки основными методами лечения становятся иммунотерапия и таргетная терапия.

Симптомы рака почки: когда нужно посетить врача?
В некоторых случаях рак почки удается выявить на ранних стадиях, когда опухолевые клетки не распространяются за пределы органа. Но зачастую заболевание диагностируют на более поздних стадиях. Во-первых, это связано с тем, что рак почки может очень долго протекать бессимптомно. Во-вторых, для этого типа рака на данный момент не существует рекомендованных скрининговых исследований.
Все симптомы можно разделить на ренальные (связанные с поражением почек) и экстраренальные.
Среди ренальных проявлений рака почки наиболее характерны три:
- Гематурия (примесь крови в моче) – самый распространенный и зачастую первый симптом. Он возникает более чем у половины пациентов с раком почки. Моча приобретает красный цвет, при этом боль не беспокоит либо носит острый характер и возникает после гематурии. Этим злокачественная опухоль отличается от неопухолевых заболеваний почки, например, мочекаменной болезни, при которой обычно сначала возникает боль, а потом появляется примесь крови в моче. Гематурия периодически исчезает, но через некоторое время снова появляется, причем, промежутки между кровотечениями сокращаются. Количество крови в моче не зависит от размеров опухоли.
- Боли беспокоят около половины пациентов. Острая боль после гематурии возникает из-за того, что сгустки крови перекрывают просвет мочеточника. Тупые сильные боли зачастую говорят о плохом прогнозе.
- Пальпируемая опухоль – симптом, который выявляет врач во время осмотра примерно у трети пациентов.
Все три симптома одновременно встречаются у одного из десяти пациентов с раком почкеи. Обычно при этом выявляют запущенные опухоли.
Среди экстраренальных симптомов в первую очередь стоит отметить повышение температуры тела. У 5% больных лихорадка – единственное проявление заболевания. У некоторых пациентов повышается артериальное давление, отмечается покраснение лица из-за увеличения количества эритроцитов в крови, у мужчин – расширение вен мошонки (варикоцеле). На поздних стадиях снижается аппетит, пациент теряет вес без видимой причины, постоянно ощущает утомление, недомогание.
Доброкачественные новообразования (папилломы) мочевого пузыря занимают около 1% от всех заболеваний данной локализации. Длительное время они могут никак не проявлять себя клинически. В редких случаях приводят к нарушению мочеиспускания и изменению нормального состава мочи. Несмотря на невысокую распространенность и отсутствие симптоматики со стороны мочевыводящих путей, папилломатозные выросты могут представлять серьёзную опасность из-за имеющегося риска трансформации в злокачественную опухоль.
Онкогенный потенциал папиллом различен и зависит от множества внешних и внутренних факторов. Правильная тактика заключается в обязательном удалении обнаруженных во время обследования доброкачественных новообразований мочевого пузыря и последующем проведении профилактических осмотров пациента.
Общая информация
Папиллома по своему строению представляет собой вырост на слизистой оболочке мочевого пузыря, исходящий из клеток эпителиального слоя. Она может иметь различную форму, но чаще всего представлена одиночным узловым образованием, расположенным на широком основании или тонкой ножке, идущей к поверхности слизистой. Сверху доброкачественное новообразование покрыто нормальным уротелием.
Все папилломатозные выросты относят к доброкачественным новообразованиям, имеющим онкогенный потенциал различной степени. Риск трансформации в злокачественную опухоль зависит от множества факторов: длительное воздействие неблагоприятных факторов (канцерогены химического происхождения, ионизирующее излучение), нарушение уродинамики, хронические воспалительные процессы в стенке пузыря и некоторые другие. При этом в эпителиальном слое происходят изменения, приводящие к нарушению нормального клеточного и тканевого состава — атипия и дисплазия. Выраженность этих процессов напрямую влияет на риск злокачественной трансформации.
Причины
Точные причины появления папиллом мочевого пузыря остаются неизвестными, однако существуют факторы риска, которые увеличивают вероятность развития заболевания. К ним относятся:
- престарелый и старческий возраст;
- снижение местного иммунитета слизистой оболочки;
- хронические воспалительные заболевания мочеполовой системы;
- нарушение пассажа мочи;
- врожденные и приобретенные иммунодефицитные состояния.
В последнее время активно изучается влияние цитопатогенных вирусов на слизистую оболочку мочевого пузыря: папилломавирусная инфекция, вирусы простого герпеса, цитомегаловирусная инфекция, вирус Эпштейна-Барр. Присутствие данных возбудителей в организме длительное время остается незамеченным, они выявляют себя при стойком снижении иммунной сопротивляемости организма, одним из проявлений которых может являться усиление тканевой пролиферации и рост новообразований.
В подавляющем большинстве случаев доброкачественные эпителиальные выросты представлены двумя типами: переходно-клеточным и плоскоклеточным. Переходно-клеточная (уротелиальная) папиллома составляет до 4% от всех новообразований мочевого пузыря. Она представляет собой сосочковое разрастание с рыхлой соединительной тканью, внутри которой имеются мельчайшие кровеносные сосуды. Покрыто новообразование уротелием, выстилающим поверхность всего органа изнутри. Встречается уротелиальная папиллома у пациентов старше 50 лет. Она имеет крайне низкий риск рецидива и озлокачествления. Новообразование чаще всего представлено изолированными эпителиальными выростами на тонкой ножке или широком плоском основании, но может иметь и диффузный (рассыпной) характер расположения.
Один из ее морфологических вариантов — папиллома погружного типа. Она обладает теми же гистологическими характеристиками, но располагается иначе. Рост новообразования происходит преимущественно в толщу слизистой оболочки. Таким образом, основная часть папилломы глубоко прорастает в стенку мочевого пузыря, а в просвете органа расположен лишь небольшой экзофитный компонент. Встречается папиллома погружного типа менее, чем в 1% случаев и обычно наблюдается у пациентов старше 65-70 лет. Она характеризуется медленным ростом и доброкачественным клиническим течением, редко подвергается злокачественной трансформации. Большинство таких новообразований одиночные, локализуются в области шейки или треугольника Льето мочевого пузыря.
Плоскоклеточная папиллома — новообразование, в отношении которого до сих пор имеется множество разногласий со стороны клиницистов и исследователей. В ряде случаев доброкачественный эпителиальный вырост имеет высокий онкогенный потенциал. Истинная доброкачественная плоскоклеточная папиллома встречается в 2-3% случаев. Она имеет вид одиночной нежной ворсины, выступающей в просвет пузыря. Покрыт вырост неизмененным уротелием, который содержит не более 6 слоев клеток. О высоком риске злокачественной трансформации говорят в том случае, когда увеличивается количество слоев в эпителиальном пласте и появляется клеточная атипия.
Возможные симптомы
Единичные и небольшие полипы могут никак не проявлять себя клинически и длительное время растут в просвет мочевого пузыря. В некоторых случаях возможно появление дизурического синдрома — комплекса симптомов, связанного с нарушением мочеиспускания. К ним относятся:
- субъективный дискомфорт во время и после мочеиспускания;
- ощущение неполного опорожнения мочевого пузыря;
- рези при мочеиспускании.
Большие папилломы погружного типа могут стать причиной гематурии — появления крови в моче. Как правило, наблюдается микрогематурия (выявляется только лабораторно по наличию эритроцитов в моче), но иногда встречается и макрогематурия — примесь крови, определяемая визуально. Моча при этом имеет багрово-алый оттенок.
Диагностика и лечение
Как правило, в клинической практике диагностическая цистоскопия сразу же переходит в лечебную — обнаруженное новообразование удаляется, а в месте повреждения слизистой оболочки проводится эндоскопический гемостаз (профилактика кровотечения). Полученный папилломатозный вырост сразу отправляется на гистологическое исследование.
Вспомогательную роль в диагностике играют контрастные рентгенологические исследования и УЗИ мочевыводящих путей, методы компьютерной и магнитно-резонансной томографии. В обязательный минимум обследования входят анализы крови и мочи, при необходимости лечащий врач может назначить мазки из уретры и влагалища, а также расширенные исследования мочи (по Каковскому-Аддису, Нечипоренко, посев на микрофлору и другие).
Дальнейшая тактика
Цистоскопия — амбулаторная манипуляция, поэтому пациент может в тот же день вернуться к привычному образу жизни. В течение 1-3 дней после эндоскопического исследования возможно учащение мочеиспускания и появление неприятных ощущений в виде резей. Это связано с непосредственной травматизацией чувствительной слизистой оболочки уретры и мочевого пузыря во время процедуры. Слизистые покровы обладают высокой регенераторной способностью и быстро заживают самостоятельно. В течение первых суток после удаления полипов возможно появление незначительной примеси крови в моче или слизисто-кровянистого отделяемого из уретры.
После полипэктомии пациенту рекомендуется планово проходить медицинское обследование. Его кратность определяется лечащим врачом. Как правило, после цистоскопии врач назначает пациенту контрольное исследование крови и мочи. Через 6-12 месяцев следует пройти повторное эндоскопическое исследование, чтобы исключить рецидивы и оценить состояние слизистой мочевого пузыря.
Папиллярная аденокарцинома почки – это гистологическая разновидность рака, поражающего чашечно-лоханочную систему почки. Проявляется гематурией, болью в пояснице, характер и интенсивность которой может достигать степени почечной колики; слабостью, похуданием. Диагностика требует проведения УЗИ почек, урографии, почечной ангиографии, КТ, радиоизотопной сцинтиграфии, МРТ. Радикальным оперативным объемом при папиллярной аденокарциноме почки является нефруретерэктомия; при диссеминации опухоли проводится химиотерапия.
Общие сведения
Папиллярная аденокарционома почки в клинической онкоурологии диагностируется в 7-16% от всех случаев рака почки. Опухоль развивается из клеток переходного эпителия, выстилающего чашечно-лоханочный комплекс. Макроскопически имеет вид мягкого узлового образования, на разрезе приобретающего характерную пеструю окраску. При микроскопическом рассмотрении имеет (сосочковую) папиллярную или тубулярную структуру. Как и рак паренхимы почки, папиллярная аденокарцинома чаще развивается у мужчин, достигая возрастного пика заболеваемости в 50-70 лет.

Причины
Заболевание является полиэтиологическим. Определяющую роль в развитии папиллярной аденокарциномы могут играть генетические дефекты и наследственные заболевания. Риск развития рака лоханки почки увеличивается при длительном приеме анальгетиков, НПВП, мочегонных средств; воздействии ионизирующего излучения, никотина и алкоголя. Трансформацию переходного эпителия почечных лоханок могут вызывать состояния иммунодефицита, длительное проведение гемодиализа, артериальная гипертензия, сахарный диабет, ожирение. У пациентов в анамнезе нередко отмечается цистэктомия по поводу карциномы мочевого пузыря.
Классификакция
TNM-классификация выделяет следующие стадии папиллярной аденокарциномы почки:
По распространенности первичной опухоли (T):
- Т0 – первичный очаг не выявляется
- Tis – преинвазивная аденокарцинома in situ
- Т1 – аденокарцинома прорастает субэпителиальный слой лоханки
- Т2 - аденокарцинома прорастает мышечный слой лоханки
- Т3 – аденокарцинома распространяется в окололоханочную клетчатку или почечную паренхиму
- Т4 - аденокарцинома прорастает в стенки соседних органов или паранефральную клетчатку.
По наличию метастазов в регионарных лимфоузлах (паракавальных, парааортальных, в воротах печени) (N):
- N0 - в регионарных лимфоузлах метастазы отсутствуют
- N1 - единичные метастазы в лимфоузлах до 2-х см в диаметре
- N2 – единичные метастазы в лимфоузлах до 5 см в диаметре
- N3 - метастазы в лимфоузлах более 5 см в диаметре
По наличию отдаленных метастазов (M) в легких, костях, печени, головном мозге, плевре, брюшине:
- М0 – отсутствие данных за отдаленные метастазы
- М1 – наличие данных за отдаленные метастазы
Симптомы аденокарциномы
Опухоль почки протекает бессимптомно у 10-25 % пациентов. Обычно манифестирует с тотальной гематурии (70-90% случаев), которая у трети больных сочетается с болевым синдромом в области поясницы. При обтурации мочеточника кровяным сгустком болевой приступ может протекать по типу почечной колики. В 10% наблюдений имеет место классическая триада симптомов рака почки: гематурия, боль, пальпируемая опухоль.
Обычно наличие типичной триады указывает на распространенность опухолевой инвазии и неблагоприятный прогноз. О далеко зашедшей стадии заболевания также свидетельствует похудание, слабость, субфебрилитет, артериальная гипертензия, анемия, нарушение аппетита. Метастазирование происходит гематогенным или лимфогенным способом. На момент выявления рака почечной лоханки метастазы в лимфоузлах и отдаленных органах имеются уже у четверти пациентов. Чаще всего аденокарцинома почки метастазирует в легкие, плевру, кости, печень, мозг.
Диагностика
Распознавание папиллярной аденокарциномы почки производится врачом-онкоурологом, нередко связано с существенными затруднениями. Проведение трехкратного цитологического исследования осадка мочи позволяет обнаружить атипичные клетки лишь в 30% случаев. Иногда для получения биоматериала прибегают к катетеризации мочеточника или забору промывных вод в процессе уретеропиелоскопии.
При экскреторной урографии папиллярная аденокарцинома определяется по дефекту заполнения почечной лоханки контрастным веществом, а при нарушении пассажа мочи – по признакам гидронефроза. Данные экскреторной урографии уточняются с помощью ретроградной уретеропиелографии, КТ почек с контрастным усилением, МСКТ, МРТ, сцинтиграфии. Почечная ангиография информативна при прорастании аденокарциномы в паренхиму почки и позволяет точно определить локализацию первичного очага (в лоханке или паренхиме).
Ценность УЗИ почек заключается в возможности выявления гидронефрротической трансформации, а также дифференциации рентгенонегативных камней почки и опухолей лоханки. Более информативные данные получают в ходе эндолюминальной эхографии: неоплазия выявляется в виде эхопозитивного образования; также метод позволяет выяснить глубину инвазии опухоли в слои почечной лоханки.
Для исключения имплантационных метастазов в мочеточник и мочевой пузырь проводится эндоскопическое обследование мочевых путей – уретероскопия, цистоскопия, при необходимости – биопсия. Папиллярную аденокарциному дифференцируют с туберкулезом почки, пиелитом, нефролитиазом. При подозрении на отдаленные метастазы выполняется рентгенография легких, головного мозга, костей, УЗИ печени.
Лечение папиллярной аденокарциномы почки
При операбельном процессе показано выполнение нефруретерэктомии и резекции мочевого пузыря, что позволяет предупредить имплантационное распространение новообразования по мочевым путям. Меньший объем вмешательства (пиелотомия с удалением опухоли, резекция почки или тотальная нефрэктомия) могут привести к рецидиву аденокарциномы и генерализации процесса. Органосохраняющая тактика может быть оправдана при поражении единственной почки либо выраженной недостаточности функции почек.
Целесообразность выполнения лимфаденэктомии при неизмененных лимфоузлах остается предметом дискуссий, однако удаление лимфоузлов имеет значение для стадирования опухолевого процесса. При распространенном раке лоханки операция дополняется химиотерапией или лучевой терапией.
Прогноз и профилактика
Исход определяется стадией процесса и степенью дифференцировки опухоли. Прогноз пятилетней выживаемости после радикальной нефруретерэктомии и резекции мочевого пузыря при неинвазивном росте переходноклеточной аденокарциномы составляет 75-90%. При метастазировании или нерадикальной операции прогноз крайне неблагоприятный – выживаемость не превышает 2-3-х лет. Профилактика предусматривает исключение предрасполагающих факторов.
Опухоли мочеточника – это первичные и метастатические новообразования выводного протока, соединяющего почечную лоханку с мочевым пузырем. Неоплазия проявляется гематурией, болью в пояснице на стороне поражения. При диагностике учитывают данные УЗИ, уретероскопии, экскреторной урографии, ретроградной уретеропиелографии и трансуретеральной биопсии. С учетом морфологического строения и распространенности опухоли может выполняться ее трансуретеральная резекция, нефроуретерэктомия или уретерэктомия с пластикой мочеточника.
Общие сведения
В клинической онкоурологии первичные опухоли мочеточника встречаются нечасто и составляют около 1% от всех неопластических поражений верхних мочевых путей. Чаще новообразования мочеточника имеют вторичный характер и являются имплантационными метастазами рака почечной лоханки. До 80% объемных образований обнаруживается у пациентов в возрасте 40-70 лет. Наличие неоплазии мочеточника на 30-50% повышает риск развития рака мочевого пузыря.
Причины
Уротелий мочеточников очень чувствителен к различного рода химическим канцерогенам, содержащимся в моче. На сегодняшний день совершенно точно определены специфические факторы, способствующие развитию уротелиальных опухолей мочеточника. Среди них ведущая роль отводится табакокурению, повышающему риск возникновения переходно-клеточной карциномы мочевых путей в 3 раза. По статистике, 70% мужчин и около 40% женщин, страдающих раком почек и мочеточника – курильщики.
Существенно повышает вероятность развития уротелиального рака длительное применение анальгетиков, которые индуцируют капилляросклероз и нефропатию, ассоциированную с высокой частотой опухолей мочеточников. Неблагоприятное воздействие на уротелий мочеточников оказывают цитостатические препараты, в частности, циклофосфамид и его метаболит акролеин. Частота возникновения опухолей мочеточника в 2 раза увеличена у пациентов с артериальной гипертензией, особенно тех, кто получает лечение диуретиками.
Отмечено, что риск развития злокачественных новообразований мочеточника, повышен у работников нефтеперерабатывающих производств, а также лиц, занятых на производстве пластика и пластмассы. Определенную роль играет хроническая инфекция мочевых путей (пиелонефрит), травмы и камни мочеточника. Существуют данные о наследственной природе неоплазий мочеточника, связи карциномы мочевых путей с синдромом Линча II, характеризующегося развитием рака толстого кишечника, а также рака матки, яичников и поджелудочной железы.
Классификация
Среди первичных новообразований выделяют опухоли мочеточника соединительнотканного и эпителиального происхождения. Соединительнотканные неоплазии встречаются редко и могут быть представлены фибромами, лейомиомами, нейрофибромами, ангиофибромами, липомами, рабдомиомасаркомами. Большая часть опухолей происходит из уротелиального эпителия и гистологически чаще соответствует папилломе, плоскоклеточной или переходно-клеточной (папиллярной) аденокарциноме. При наличии дивертикулов мочеточника вероятность развития в них опухолей значительно повышается.
Новообразования могут иметь неинвазивный или инвазивный характер роста, одно- либо двустороннюю локализацию. Первичные опухоли преимущественно образуются в нижней (68%) или средней (20,3%) части мочеточника; в 9,4% случаев поражается верхняя треть, а в 2,3% наблюдений - весь мочеточник. На прилоханочную область и верхние отделы мочеточника, как правило, распространяются первичные опухоли лоханки.
Симптомы опухоли мочеточника
Типичными симптомами неоплазии служат гематурия, боль в пояснице и дизурия. Гематурия присутствует в 70-95% наблюдений, причем макрогематурия выявляется у 65-70% пациентов и обычно становится основной причиной обращения к врачу-урологу. Болевой синдром развивается в 25-50% случаев и вызывается обтурацией лоханочно-мочеточникового сегмента или мочеточника опухолью.
Позднее присоединяются дизурические расстройства (у 5-10% пациентов) и общие симптомы (5-10%) – субфебрилитет, понижение аппетита, похудание. В запущенных стадиях в результате повышения гидростатического давления в почке развивается гидронефроз, опухоль может пальпироваться в животе в виде объемного образования. Доброкачественные новообразования мочеточника длительное время могут развиваться без значимой клинической симптоматики.
Диагностика
В комплекс исследований при подозрении на опухоль мочеточника включают физикальное обследование, цитологический анализ мочи, УЗИ почек, экскреторную урографию, ретроградную уретеропиелографию, почечную артериографию, цистоскопию, уретероскопию, КТ почек.
В случае резкого снижения функций почки, невозможности катетеризации мочеточника предпринимается выполнение пункционной антеградной пиелоуретерографии. Эндоскопические урологические исследования (цистоскопия, уретероскопия) позволяют визуально рассмотреть расположение опухоли, выполнить биопсию тканей для проведения морфологического исследования. В ходе цистоскопии определяется пролабирующая из устья мочеточника опухоль, выделение крови из мочеточника.
УЗИ почек производится для выявления инфильтрации неоплазии в почечную паренхиму, дифференциации новообразований с рентгенонегативными камнями почек и мочеточников. КТ почек и мочевых путей позволяет оценить распространенность опухоли за пределы почки (глубину инвазии), вовлеченность лимфоузлов и соседних органов. При необходимости выявления отдаленных метастазов может потребоваться выполнение рентгенографии грудной клетки, сцинтиграфии и УЗИ печени, лимфографии, сцинтиграфии костей.
Лечение опухоли мочеточника
Лечение, в основном, оперативное. При раке мочеточника в дополнение к хирургическому вмешательству проводится радио- и химиотерапия, однако опухолевые клетки к ним малочувствительны. При выборе лечебной тактики руководствуются типом и локализацией новообразования, состоянием противоположной почки и пр. Доброкачественные неоплазии удаляются путем эндоскопической трансуретеральной резекции (электрорезекции, электрокоагуляции, лазерной коагуляции). При поверхностных, неинвазивно растущих опухолях дистальной трети мочеточника возможно проведение сегментарной резекции органа с формированием уретероцистоанастомоза.
Стандартно при локализованной форме переходно-клеточного рака мочеточника и лоханки выполняется нефроуретерэктомия с частичной резекцией мочевого пузыря, что диктуется высокой опасностью дальнейшего распространения опухоли по мочеточнику. При этом резекция мочевого пузыря может производиться трансуретрально, а нефроуретерэктомия – из лапароскопического доступа. Постоперационное лечение может дополняться адъювантной терапией: системной химиотерапией, радиотерапией, топической (внутримочеточниковой) иммунохимиотерапией и химиотерапией.
Прогноз и профилактика
Доброкачественные опухоли мочеточника обязательно должны быть удалены, поскольку могут подвергаться малигнизации. После их удаления прогноз для жизни благоприятный. Неинвазивная переходно-клеточная карцинома мочеточника излечима в 80% случаев; инвазивно растущие опухоли – лишь в 10-15%. Злокачественные новообразования после удаления рецидивируют у 12-18% пациентов. При метастатическом или рецидивном течении прогноз неудовлетворительный.
После удаления опухоли необходимо наблюдение уролога (онкоуролога), периодический эндоскопический, рентгенологический и цитологический контроль. Избежать возникновения новообразований можно, исключив курение, употребление нефротоксичных препаратов, ограничив взаимодействие с вредными химическими факторами, проводя своевременное лечение заболеваний мочевыводящих путей.
Читайте также:

