Пигментный обмен при вирусных гепатитах
Обновлено: 25.04.2024
Печень - непарный орган массой 1300-1800 г. Она расположена под диафрагмой в правом верхнем квадранте живота. На нижней, висцеральной ее поверхности определяется короткая поперечная глубокая бороздка - ворота печени. В области ворот находятся печеночная артерия, воротная вена, желчный и лимфатический протоки.
Наиболее распространено деление органа на правую и левую доли, которые в свою очередь состоят из сегментов. Всего насчитывается 8 сегментов. К каждому из них подходят ветви воротной вены, печеночной артерии, а выходят желчный проток и печеночная вена.
На нижней поверхности печени, примыкающей к воротам, расположена небольшая хвостатая доля (спигелиева). Она соответствует первому сегменту.
Более 60% печени составляют гепатоциты. Около 15-20% клеточного состава - эндотелиальные клетки. Остальное падает на протоковые, соединительнотканные и иные клетки.
В эксперименте удаление части печени ведет к быстрой регенерации этого участка. Так, например, удаление 2/3 печени крысы ведет к восстановлению ее прежних размеров всего за несколько дней. Однако полное восстановление печени ad integrum, по-видимому, возможно при удалении не более 10% массы органа (Bucher N. et al„ 1979).
Установлено, что если хвостатая доля остается неповрежденной, то регенерация печени протекает быстрее (Foucou В. et al., 1983; Soyeux Н. et al., 1984, и др.).
Основу структуры печени составляет долька, которая формируется из клеток, в первую очередь гепатоцитов. Центр печеночной дольки - печеночная вена; радиально от нее располагаются атоциты, образуя балки. На периферии дольки, примыкая к ней, находится портальное поле с разветвлениями воротной вены, печеночной артерии и мельчайшим желчным протоком.
Распределение ферментов в различных отделах печени неодинаково. Так, по данным Е. Schmidt и F. Schmidt (1982), при преимущественном поражении центральных отделов дольки (острый алкогольный гепатит и особенно острый венозный застой) в сыворотке крови нарастает активность глутаматдегидрогеназы, при преимущественном поражении портальных трактов и прилегающих отделов печеночной дольки (острый вирусный гепатит и хронический активный гепатит) в первую очередь повышается активность аминотрансфераз.
2. Гепатоцит
В гепатоците различают васкулярный полюс, в котором при помощи микроворсин осуществляется эндоцитоз (захват веществ извне и введение их в клетку) и экзоцитоз, и билиарный полюс, где при помощи микроворсин происходит выделение веществ из клетки.
Клетка состоит из оболочки, цитоплазмы и внутриклеточных структур - органоидов. Обычно в центральной части клетки расположено ядро

Цитоплазматическая мембрана гепатоцита
Отдел мембраны, прилегающий к синусу, занимает 40-50% поверхности всей оболочки. Мембрана высокоактивна в отношении избирательного переноса веществ из крови в гепатоцит, а также из гепатоцита в кровь. Контакт между двумя соседними гепатоцитами осуществляется при помощи латеральной мембраны, занимающей 30-40% поверхности клетки. Большое количество щелей в этой мембране способствует обмену веществ между двумя соседними гепатоцитами.
В сторону желчных ходов обращена канальцевая мембрана, занимающая около 10% поверхности клетки. Мембрана образует большое количество выростов, особенно богатых щелочной фосфатазой, γ-глутамилтрансферазой и 5-нуклеотидазой, получившими вследствие этого название мембранозависимых ферментов. Ферменты обнаруживаются в различных органоидах и отделах клеток. Большинство ферментов локализуется преимущественно в определенных отделах гепатоцита.
Цитоплазма (цитозоль, гиалоплазма) составляет большую часть клетки и содержит различные органоиды, в частности пластинчатый комплекс (тельца Гольджи).
В цитоплазме обнаруживаются следующие ферменты: аланинаминотрансфераза (АлАТ); часть фермента аспартатаминотрансфераза (АсАТ); лактатдегидрогеназа (ЛДГ); сорбит-дегидрогеназа (СДГ); или L-идитолдегидрогеназа; орнитин-карбамоилтрансфераза (ОКТ); часть фермента аргиназа (Apr); часть фермента алкогольдегидрогеназа (АлДГ); γ-глутамилтрансфераза или γ-глутамилтранспептидаза (ГГТФ или ГГТП); фруктозобисфосфат-альдолаза (АЛД), глутатионтрансфераза.
Митохондрии размещены в основном около ядра и в зоне гранулярного эндоплазматического ретикулума у васкулярного полюса гепатоцита. Они производят основную энергию, необходимую для жизнедеятельности клетки. Гепатоцит особенно богат митохондриями; количество их в одной клетке достигает тысячи. В них осуществляются в значительной мере цикл Кребса, окислительное фосфорилирование и окисление жирных кислот. Клинические наблюдения над колебаниями активности глутаматдегидрогеназы дают основание предполагать прямую связь части митохондрий с пребилиарными образованиями клетки.
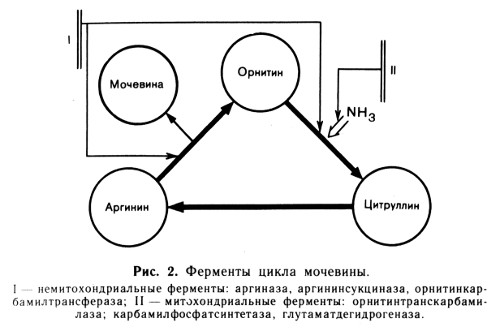
Ферменты, сосредоточенные в основном в митохондриях: часть фермента аспартатаминотрансфераза (АсАТ), глутаматдегидрогеназа (ГлДГ), часть фермента алкогольдегидрогеназа (АлДГ), карбамоилфосфатсинтетаза (КФС), орнитин-транскарбамилаза (ОТК).
До последнего времени информация по расположению ферментов внутри клетки находила применение обычно лишь в чисто диагностическом плане. Сейчас эти данные начали использовать для объяснения патогенеза отдельных синдромов. Такой подход оказался очень плодотворным при расшифровке синдрома Рея, который возникает преимущественно у детей до 10 лет под влиянием вирусных инфекций (ветряная оспа, грипп и др.) и интоксикаций (в первую очередь афлотоксином, возможно, ацетилсалициловой кислотой) и представляет собой своеобразный вариант острого жирового гепатоза с развитием тяжелых форм портально-печеночной недостаточности. Обнаружено избирательное поражение митохондрий гепатоцитов с нарушением митохондриального отрезка преобразования мочевины. Блокада двух ферментов цикла мочевины - орнитиновой транскарбамилазы и карбамоилфосфатсинтетазы - ведет к исчезновению цитруллина в печени. Таким образом, возникает перерыв последовательных преобразований в цепи аммиак - мочевина. Крайне резко возрастает концентрация аммиака сыворотки крови. Обычно при этом заболевании наблюдается тяжелая энцефалопатия, нередко регистрируется гипогликемия и рвота.
В противоположность синдрому Рея при печеночноклеточной коме в основном подавляется активность внемитохондриальных ферментов, участвующих в цикле преобразования мочевины: аргининсукцинатсинтетазы, аргининсукциназы и аргиназы
Специального обсуждения заслуживает термин "микросомы" или "микросомная фракция" . По современным представлениям, к микросомам относят фрагменты мембран эндоплазматической сети, как гладкой, так и гранулярной. С момента четкого выделения двух видов эндоплазматической сети (см. ниже) несколько аморфные представления о микросомах, казалось, должны были бы в значительной мере потерять свое значение. Однако по традиции этот термин продолжают достаточно широко использовать в клинической практике. Так, выделяют премикросомальную, микросомальную и постмикросомальную желтуху, подразумевая под ними нарушения пигментного обмена до или после преобразований билирубина в гладком эндоплазматическом ретикулуме, т. е. желтуху, протекающую преимущественно с повышением в сыворотке крови концентрации билирубина, еще не подвергавшегося конъюгации, с повышением концентрации конъюгированного (прямого) билирубина и гипербилирубинемии, а также желтухи, прямо связанные с нарушением конъюгации билирубина.
Гранулярный эндоплазматический ретикулум расположен в основном вокруг ядра и митохондрий. Основу зернистой цитоплазматической сети составляют цистерны, наружная поверхность которых усеяна рибосомами. В них образуются плазмопротеины, за исключением иммуноглобулинов. Синтезируемые белки, в первую очередь альбумины и фибриноген, и большая часть глобулинов через пластинчатый аппарат Гольджи выводятся из гепатоцитов в кровь. Здесь же синтезируются и основные факторы свертывания крови.
Ферменты, сосредоточенные преимущественно в гранулярном эндоплазматическом ретикулуме: холинэстераза (ХЭ), холестерол-лецитин - ацилтрансфераза.
Гладкий эндоплазматический ретикулум, или гладкая цитоплазматическая сеть, расположен вокруг ядра и митохондрий и около билиарного полюса гепатоцита. В нем осуществляются биотрансформация и конъюгация как веществ эндогенного происхождения, так и чужеродных для организма соединений (ксенобиотиков). С деятельностью этого органоида в значительной мере связано образование и накопление гликогена. Предполагается, что преимущественно здесь же осуществляется детоксикационная функция печени. В частности, в этих органоидах происходит конъюгация (соединение) токсических веществ с глюкуроновой кислотой, таким путем вещества из жирорастворимых переходят в водорастворимые. Здесь, в частности, осуществляется конъюгация билирубина. Предполагается, что цитохром Р-450, играющий важную роль в преобразовании лекарств и иных ксенобиотиков, в основном сосредоточен в этой фракции. Индикатором Р-450 служит антипириновая проба. Белковая часть глико- и липопротеидов образуется в гранулярном эндоплазматическом ретикулуме и поступает в гладкий эндоплазматический ретикулум, где используется для синтеза этих сложных белков. В этом процессе участвует также пластинчатый комплекс.
В гладком эндоплазматическом ретикулуме обнаруживают глюкозо-6-фосфатазу, билирубингликозилтрансферазу (УДФ-глюкуронилтрансферазу).
Пластинчатый комплекс (аппарат Гольджи) частично с помощью лизосом осуществляет транспорт из клетки ряда веществ, образующихся в эндоплазматическом ретикулуме. Часть этих веществ претерпевает во время транспортировки существенные преобразования. В частности, под влиянием гликозилтрансфераз к молекулам белка присоединяются углеводные комплексы. Таким путем синтезируется часть гликопротеидов или гликозаминогликанов.
Ферменты, сосредоточенные в пластинчатом комплексе, пока в сыворотке крови обычными методами не обнаружены.
Лизосомы - мембранные пузырьки, богаты кислыми гидролазами, осуществляющими расщепление крупных молекул как внутри-, так и внеклеточного происхождения. Такая судьба, в частности, ожидает нередко и бактерии, внедрившиеся в гепатоцит. Лизосомы тесно связаны с пластинчатым комплексом, часто расположены вблизи билиарного полюса, участвуют в секреции желчи. При обычно врожденном нарушении ферментных систем лизосом искажаются нормальные превращения (катаболизм) ряда липидов и гликогена. В случае подобных нарушений эти вещества начинают накапливаться в клетках, вызывая ряд заболеваний, в частности болезнь Гоше, связанную с врожденной недостаточностью лизосомного фермента глюкозилцерамид-β-глюкозидазы (Р - glc). Велика заинтересованность лизосом в патологических процессах при болезни Вильсона - Коновалова.
Резкие изменения pH среды и повреждения лизосом могут приводить к активации гидролаз и разрушению клетки. Таковы, в частности, элементы патогенеза субмассивных и массивных некрозов печени.
Ферменты, сосредоточенные в основном в лизосомах: кислая фосфатаза, катепсин D, β-глюкуронидаза, β-гексозаминидаза, α-глюкозидаза, рибонуклеаза, дезоксирибонуклеаза.
Микроворсинки билиарного полюса гепатоцита формируют истоки желчных канальцев, играют важную роль в выведении продуктов жизнедеятельности гепатоцитов.
Ферменты, сосредоточенные в основном в микроворсинках: щелочная фосфатаза (ЩФ), 5-нуклеотидаза (5-НТ), аланинаминопептидаза (ААП), γ-глутамилтрансфераза или γ-глутамилтранспептидаза (часть ее сосредоточена в цитоплазме).
Взаимоотношения желчных капилляров (канальцев) и микроворсинок играют важную роль в нормальной секреции желчи. Стенки желчного капилляра образованы канальцевыми отделами мембран гепатоцитов. От места появления эпителия желчного хода и формирования таким путем самостоятельной стенки желчного канала этот отрезок желчевыводящих путей называется мельчайшим желчным протоком.
3. Кле́тки Купфера
Кле́тки Купфера (синонимы: клетки Бровича — Купфера, клетки береговые, клетки синусоидные, клетки эндотелиальные звездчатые) — специализированные макрофаги печени, являющиеся частью ретикулоэндотелиальной системы. Основной функцией клеток Купфера является захват и переработка старых нефункциональных клеток крови. При этом разрушаются молекулы гемоглобина, их глобиновые цепи повторно утилизируются, а гем расщепляется на железо и билирубин.
Названы в честь Карла Вильгельма Купфера, впервые описавшего их в 1876 году
4. Клетки Ито
Клетки Ито (синонимы: звёздчатая клетка печени, жирозапасающая клетка, липоцит, англ. Hepatic Stellate Cell, HSC, Cell of Ito, Ito cell ) — перициты, содержащиеся в перисинусоидальном пространстве печёночной дольки, способные функционировать в двух различных состояниях — спокойном и активированном. Активированные клетки Ито играют главную роль в фиброгенезе — формировании рубцовой ткани при повреждениях печени.
В неповрежденной печени, звёздчатые клетки находятся в спокойном состоянии. В таком состоянии клетки имеют несколько выростов, охватывающих синусоидный капилляр. Другой отличительной чертой клеток является присутствие в их цитоплазме запасов витамина А (ретиноида) в форме жировых капель. Спокойные клетки Ито составляют 5-8 % численности всех клеток печени. [1]
Выросты клеток Ито подразделяются на два типа: перисинусоидальные (субэндотелиальные) и интергепатоцеллюлярные. Первые выходят из тела клетки и простираются вдоль поверхности синусоидного капилляра, охватывая его тонкими пальцеобразными ответвлениями. Перисинусоидальные выросты покрыты короткими ворсинками и имеют характерные длинные микровыбросы, простирающиеся ещё дальше по поверхности эндотелиальной трубки капилляра. Интергепатоцеллюлярные выросты, преодолев пластинку гепатоцитов и достигнув соседнего синусоида, делятся на несколько перисинусоидальных выростов. Таким образом, клетка Ито в среднем охватывает чуть больше двух соседних синусоидов. [2]
При повреждении печени клетки Ито переходят в активированное состояние. Активированный фенотипхарактеризуется пролиферацией, хемотаксисом, сокращаемостью, потерей запасов ретиноида [3] и образованием клеток, напоминающих миофибробластные. Активированные звёздчатые клетки печени также демонстрируют повышенное содержание новых генов, таких как α-SMA, ICAM-1, хемокины и цитокины. Активация свидетельствует о начале ранней стадии фиброгенеза и предшествует повышенному продуцированию ЕСМ-белков. Финальная стадия заживления печени характеризуется усиленным апоптозом активированных клеток Ито, вследствие чего их количество резко сокращается. [4]
Для визуализации клеток Ито при микроскопии применяется окрашивание хлоридом золота. Установлено также, что надёжным маркером для дифференциации этих клеток от других миофибробластов является экспрессия ими белка рилин. [5]
История

Вверху — схематическое изображение клетки Ито (HSC) по соседству с ближайшими гепатоцитами (PC), ниже синусоидальных эпителиальных клеток печени (EC). S — синусоид печени; KC — клетка Купфера. Внизу слева — клетки Ито в культуре под световым микроскопом. Внизу справа — электронная микроскопия позволяет разглядеть многочисленные жировые вакуоли (L) клеток Ито (HSC), в которых хранятся ретиноиды.
5. Образование желчи
Конъюгированный билирубин секретируется гепатоцитом в желчный капилляр (каналец). Секреция осуществляется в зоне микроворсинок, к мембранам которых очень близко прилегают лизосомы и аппарат Гольджи. По современным воззрениям, желчные канальцы, микроворсинки, прилегающие к ним лизосомы и пластинчатый комплекс составляют желчьсекретирующий аппарат. Этот аппарат секретирует билирубин, холестерин, желчные кислоты, электролиты, воду и другие компоненты желчи. Характерной особенностью желчного канальца является его полная изоляция от кровеносных капилляров.
Тонкий механизм секреции желчи предусматривает выделение холестерина, желчных кислот и пигментов, а также фосфолипидов (в основном лецитина) в виде специфического макромолекулярного комплекса, или желчной мицеллы. Соотношение этих четырех основных компонентов, составляющих мицеллу, в нормальных условиях достаточно постоянно и обеспечивает растворимость компонентов. Ведь холестерин почти нерастворим в воде, плохо растворим в растворе желчных солей, но сочетание желчных кислот и лецитина резко повышает растворимость холестерина. Желчные кислоты, а также хлорид натрия в значительной мере определяют осмотическое давление желчи, а следовательно, и экскрецию воды из гепатоцита.
За сутки выделяется около 600 мл желчи. Строгие соотношения, необходимые для растворимости компонентов желчной мицеллы, объясняют уязвимость процессов желчной секреции и последующей желчединамики. Секреция желчи, а значит, и формирование мицеллы часто нарушаются: в результате патологических сдвигов в гормональной регуляции холестерино- и фосфолипидогенеза: при беременности (особенно в III триместре), реже - в менопаузе, а также при приеме гормональных препаратов (тестостерон, пероральные противозачаточные средства и др.). Воспалительно-дистрофические изменения гепатоцитов, в частности гладкого эндоплазматического ретикулума, лизосом и канальцевых мембран, при многих острых, а нередко и при хронических заболеваниях печени приводят к грубым нарушениям секреции желчи, что усугубляется поражением мельчайших желчных ходов. Как и при упомянутых выше гормональных нарушениях, может развиться желтуха (см. ниже).
Знание ультраструктуры гепатоцита и, в том числе, размещения в нем ферментов становится необходимым в клинической практике, в частности в диагностике синдромов и заболеваний печени, в объяснении патогенеза ряда болезней печени (синдром Рея, болезнь Гоше и др.) и в оценке эффективности лечения.
Что такое гепатит А (болезнь Боткина)? Причины возникновения, диагностику и методы лечения разберем в статье доктора Александрова Павла Андреевича, инфекциониста со стажем в 14 лет.
Над статьей доктора Александрова Павла Андреевича работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Вирусный гепатит А (Hepatitis A viruses, HAV) — острое инфекционное заболевание, вызываемое вирусом гепатита А, клинически характеризующееся синдромом общей инфекционной интоксикации, синдромом нарушения пигментного обмена, синдромами энтерита, холестаза, увеличением печени и в некоторых случая селезёнки, сопровождающееся нарушением функции печени, преимущественно доброкачественного течения.
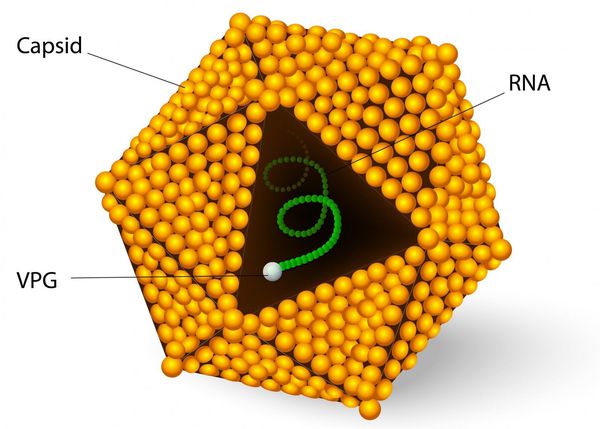
Этиология
семейство — пикорнавирусы (Picornaviridae)
вид — вирус гепатита А (HAV)
Во внешней среде очень устойчив: при температуре окружающей среды около 4°C сохраняется несколько месяцев, при 2°C — несколько лет, при замораживании очень длительно, при комнатной температуре — несколько недель. В растворе хлорсодержащих средств (0,5-1 мг/л) гибнет в течение часа, при 2,0-2,5 мг/л — в течение 15 минут, ультрафиолетовое облучение приводит к гибели в течение минуты, при кипячении сохраняется до 5 минут. В кислой среде желудка не погибает.
Наиболее значимым маркером вирусного гепатита А являются антитела класса М (анти-HAV IgM), которые образуются в начальный период заболевания и выявляются до 5 месяцев. Появление анти-HAV IgG (маркера перенесённой ранее инфекции) начинается с 3-4 недели заболевания. Антиген вируса выявляется в каловых массах за 7-10 дней до начала манифестных (явно выраженных) проявлений болезни. [1] [2] [4]
Эпидемиология
Заражение гепатитом А происходит при контакте с источником инфекции — живым человеком (больной различными формами заболевания и вирусоноситель). Больные с типичными формами являются главным источником распространения вируса (от конца скрытого и всего желтушного периодов).
Ежегодно в мире регистрируется примерно 1,5 млн случаев заболевания (количество субклинических и бессимптомных форм сложно даже представить). Смертность по миру в 2016 г., по данным ВОЗ, составила 7134 человек [10] .
Условно существует территориальное распределение по уровням инфицирования населения: высокий, средний и низкий.
Районы с высоким уровнем инфицирования это преимущественно Юго-Восточная Азия, Средняя Азия, Африка, Центральная Америка (плохие санитарные условия и низкий доход) — большинство населения к периоду взросления уже переболели и имеют иммунитет, вспышки болезни встречаются редко.
Районы со средним уровнем инфицирования — страны с переходной экономикой, развивающиеся, имеющие различия в санитарно-гигиенических условиях на территории одного региона, например Россия (большая часть населения к периоду взросления не болела и не имеет иммунитета к вирусу, возможны большие вспышки болезни).
Районы с низким уровнем инфицирования — развитые страны с высоким уровнем дохода и хорошими санитарно-гигиеническими условиями, например США, Канада, Европа, Австралия. Большинство людей не имеет иммунитета и не болела, вспышки случаются редко и чаще среди групп риска [7] .
В окружающую среду вирус выделяется преимущественно с фекалиями.
Механизм передачи: фекально-оральный (пути — водный, контактно-бытовой, пищевой), парентеральный (редко при переливании крови), половой (орально-анальный контакт).
Восприимчивость населения высокая.
Факторы риска заражения:
- высокая скученность населения;
- несоблюдение правил личной гигиены и правил хранения, обработки и приготовления продуктов питания;
- неудовлетворительное состояние объектов водоснабжения;
- бытовой очаг заболевания.
Кто находится в группе риска
- путешественники (особенно в страны жаркого климата и с плохими социальными условиями);
- гомосексуалисты;
- люди, употребляющие наркотики (любые), алкоголики;
- медработники (непривитые и не болевшие);
- бездомные;
- люди, имеющие постоянные контакты (в силу профессии или иных причин) с мигрантами из неблагополучных по гепатиту А регионов.
Характерна осенне-весенняя сезонность, повышенная привязанность к жарким южным регионам.
Иммунитет после перенесённого заболевания стойкий, пожизненный, то есть повторно заболеть нельзя [1] [3] [4] [7] [10] .
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы гепатита А
Заболевание начинается постепенно. Инкубационный период гепатита А протекает 7-50 дней.
Синдромы вирусного гепатита А:
- общей инфекционной интоксикации;
- нарушения пигментного обмена (желтуха);
- энтерита (воспаление слизистой тонкой кишки);
- холестаза (уменьшение количества желчи, поступающей в двенадцатиперстную кишку);
- гепатолиенальный (увеличение печени и селезёнки);
- отёчный;
- нарушения функции печени.
Типичное течение болезни — это желтушная форма болезни средней степени тяжести (устаревшее название — желтуха или болезнь Боткина).
Начальный период болезни (преджелтушный) имеет продолжительность от 2 до 15 дней и может протекать по нескольким вариантам:
При осмотре обнаруживается увеличение печени и, в меньшей степени, селезёнки, чувствительность края печени, повышение ЧСС (пульса), носовые кровотечения. В конце периода моча темнее, а кал становится светлее.
Следующий период (желтушный) длительностью около 7-15 дней характеризуется снижением выраженности симптомов предшествующего периода (то есть с появлением желтухи самочувствие улучшается). Усиливается желтушное окрашивание склер, кожных покровов и слизистой оболочки ротоглотки. Моча приобретает цвет тёмного пива, кал белеет. Присутствует общая слабость, недомогание, плохой аппетит, чувство тяжести и переполненности в правом подреберье, больной расчёсывает себя из-за зуда кожи (лихенификация), появляются петехии (мелкие кровоизлияния) на коже.
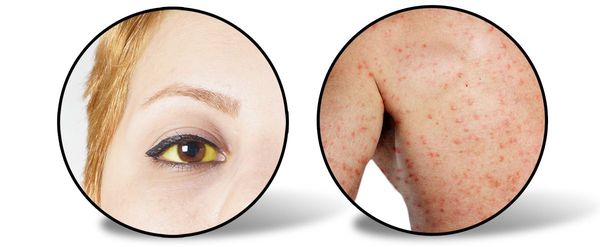
При врачебном исследовании выявляется увеличение печени и селезёнки, явственно положителен симптом Ортнера (болезненность при поколачивании ребром ладони по правой рёберной дуге), гипотония (может быть и нормотония), токсическая брадикардия (снижение ЧСС), появляются периферические отёки, возможны боли в суставах (артралгии).
Далее при благоприятном течении заболевания (которое наблюдается в большинстве случаев) происходит регресс клинической симптоматики, осветление мочи и потемнение кала, более медленное спадение желтушности кожи, склер и слизистых оболочек.
Под нетипичным течением болезни подразумеваются лёгкие безжелтушные формы гепатита А (отсутствие симптомов или лёгкая слабость без желтухи, тяжесть в правом подреберье), фульминантные формы.
Факторы, увеличивающие риск тяжёлого течения гепатита А:
Последствия для беременных
У беременных гепатит А протекает в целом несколько тяжелее, чем у небеременных. Примерно в 36 % случаев возможно развитие слабости родовой деятельности, преждевременные роды (31-37 неделя) и послеродовые кровотечения. Вирус не проникает через плаценту, то есть какого-то специфического действия на плод не оказывает. В грудном молоке вирус не содержится [1] [2] [4] [7] .
Патогенез гепатита А
Воротами для проникновения вируса является слизистая оболочка органов желудочно-кишечного тракта, где происходит его первичное размножение в эндотелиальной выстилке тонкого кишечника и мезентериальных лимфоузлах.
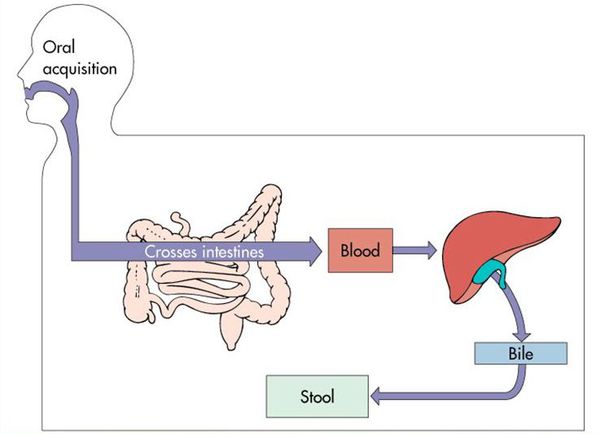
Далее происходит гематогенное распространение вирусных частиц и проникновение их в печень, где они локализуются в ретикулогистиоцитарных клетках Купфера и гепатоцитах. В результате этого происходит повреждение клеток:
- проникновение вируса в клетку;
- захват лизосомой;
- разрушение белковой оболочки вируса;
- сборка белков по программе вирусной РНК;
- встраивание этих белков в цитолемму клетки;
- образование патологических пор в оболочке клетки;
- поступление внутрь клетки ионов натрия и воды;
- баллонная дистрофия (разрушение ультраструктур клетки и образование крупных вакуолей) с последующим некрозом (его объём, как правило, ограничен);
- гибель клетки и лимфоцитарная иммунная реакция, приводящая к основному объёму поражения.
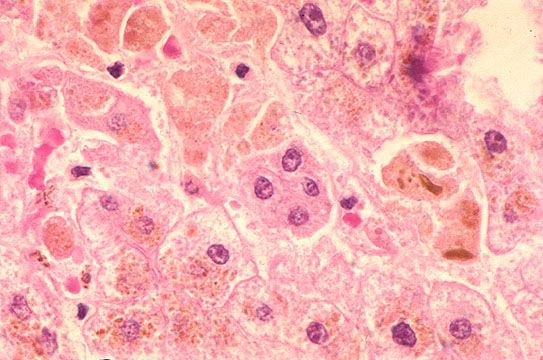
В дальнейшем вирус попадает в желчь, с ней он проникает в кишечник и выводится в окружающую среду с фекалиями. Вследствие компетентных реакций иммунной защиты размножение вируса заканчивается, и он покидает организм больного. [2] [3] [4]
Классификация и стадии развития гепатита А
По степени разнообразия проявлений выделяют две формы гепатита А:
- клинически выраженная (желтушная, безжелтушная, стёртая);
- субклиническая (инаппарантная).
По длительности течения также выделяют две формы гепатита А:
- острая циклическая (до трёх месяцев);
- острая затяжная (более трёх месяцев).
Степени тяжести гепатита А:
- лёгкая;
- среднетяжёлая;
- тяжёлая;
- фульминатная (молниеносная).
Согласно МКБ-10 (Международной классификации болезней десятого пересмотра), заболевание подразделяют на три вида:
- В15. Острый гепатит А;
- В15.0. Гепатит А с печёночной комой;
- В15.9. Гепатит А без печёночной комы. [2][4]
Осложнения гепатита А
Заболевание может привести к следующим осложнениям:
- печёночная кома (дисфункция центральной нервной системы, связанная с тяжёлым поражением печени — встречается крайне редко);
- холецистохолангит (выраженные боли в правом подреберье, нарастание желтухи и зуда кожи);
- гемолитико-уремический синдром, преимущественно у детей (гемолитическая анемия, тромбоцитопения, острая почечная недостаточность);
- развитие аутоиммунного гепатита I типа.
Гепатит А не приводит к формированию хронических форм, однако из-за выраженного воспалительного процесса возможно появление длительных резидуальных (остаточных) явлений:
- дискинезия (нарушение моторики) желчевыводящих путей;
- постгепатитная гепатомегалия (увеличение размеров печени из-за разрастания соединительной ткани);
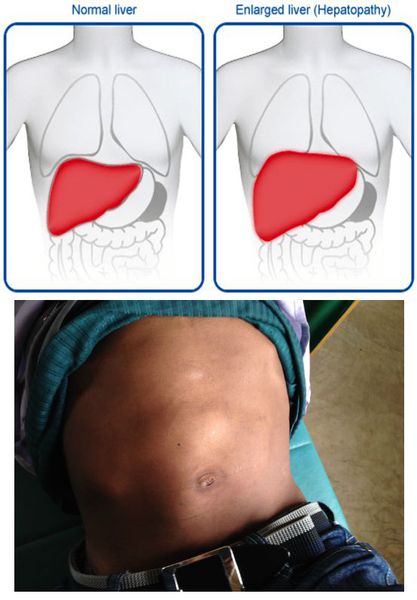
- постгепатитный синдром (повышенная утомляемость, аснено-невротические проявления, тошнота, дискомфорт в правом подреберье). [1][5]
Диагностика гепатита А
Методы лабораторной диагностики:
- Клинический анализ крови — нормоцитоз или лейкопения, лимфо- и моноцитоз, нейтропения, СОЭ в норме или снижена.
- Биохимический анализ крови — повышение общего билирубина и в большей степени его связанной фракции (реакция Эрлиха), повышение аланинаминотрансферазы и аспартатаминотрансферазы, снижение протромбинового индекса, повышение тимоловой пробы (снижение альбуминов и повышение гамма-глобулинов), повышение гамма-глутамилтранспептидазы, щелочной фосфатазы и другие показатели.
- Биохимический анализ мочи — появление уробилина и желчных пигментов за счёт прямого билирубина. Ранее, особенно в вооруженных силах, для выявления больных на начальной стадии практиковалось использование пробы Разина: утром производится опускание индикаторной полоски в мочу (при наличии уробилина она меняет цвет), и военнослужащий с подозрением на заболевание госпитализировался для углублённого обследования. Тест на уробилин становится положительным в самом начале заболевания — в конце инкубационного периода из-за болезни печёночной клетки.
- Серологические тесты — выявления анти-HAV IgM и анти-HAV IgG методом ИФА (иммуноферментного анализа) в различные периоды заболевания и HAV RNA с помощью ПЦР-диагностики (полимеразной цепной реакции) в острый период.
- Ультразвуковое исследование органов брюшной полости — увеличение печени и иногда селезёнки, реактивные изменения структуры печёночной ткани, лимфаденопатия ворот печени.
Обследование лиц, бывших в контакте с больным
Лица, контактирующие с больным вирусным гепатитом А, подлежат осмотру врачом-инфекционистом с последующим наблюдением до 35 дней со дня разобщения с больным. Наблюдение включает термометрию, осмотр кожных покровов, определение размеров печени и селезёнки, а также лабораторное обследование (АЛТ, общий билирубин, антитела классов М и G к вирусу гепатита А вначале и через три недели от первичного обследования).
Дифференциальная диагностика проводится со следующими основными заболеваниями:
- в начальный период: ;
- гастрит, гастроэнтероколит;
- полиартрит;
- энтеровирусная инфекция;
- в желтушный период: ;
- псевдотуберкулёз; ;
- желтухи другой этиологии (гемолитическая болезнь, токсические поражения, опухоли ЖКТ и другие заболевания);
- гепатиты другой этиологии (вирусные гепатиты В, С, Д, Е и другие, аутоиммунные гепатиты, болезнь Вильсона — Коновалова и т.п.) [1][2][3][4][9] .
Лечение гепатита А
Этиотропная терапия (направленная на устранение причины заболевания) не разработана.
Медикаменты
В зависимости от степени тяжести и конкретных проявлений назначается инфузионная терапия с глюкозо-солевыми растворами, обогащёнными витаминами. Показано назначение сорбентов, препаратов повышения энергетических ресурсов, при необходимости назначаются гепатопротекторы, в тяжёлых случаях — гормональные препараты, препараты крови, гипербарическая оксигенация и плазмаферез.
Нужна ли госпитализация
В случае лёгких форм гепатита А лечение может проводиться на дому (при наличии условий). Госпитализация потребуется, начиная со среднетяжёлых форм, лицам групп риска по тяжёлому течению, пациентам с осложнёнными формами, беременным и детям. Каких-либо особенностей при дальнейшем лечении вирусного гепатита А у детей нет.
Режим постельный или полупостельный. При гепатите А нарушаются процессы образования энергии в митохондриях, поэтому предпочтителен длительный отдых.
Лечение в стационаре и выписка
Лечение гепатита А проходит в инфекционном отделении больницы. Выписка пациентов происходит после появления стойкой и выраженной тенденции к клиническому улучшению, а также улучшения лабораторных показателей.
Критерии выписки больных:
- стойкая и выраженная тенденция к клиническому улучшению (отсутствие интоксикации, уменьшение размеров печени, регресс желтухи);
- стабильное улучшение лабораторных показателей (нормализация уровня билирубина, значительное снижение уровня АЛТ и АСТ).
При неосложнённых формах реконвалесценты (выздоравливающие больные) подлежат наблюдению в течении трёх месяцев с осмотром и обследованием не реже одного раза в месяц. [2] [3] [6]
Физиотерапия
В фазе реконвалесценции, особенно при затяжных формах болезни, возможно применение физиотерапевтических методов лечения:
- грязевых аппликаций на область правого подреберья;
- акупунктуры;
- массажа проекции области печени, желчного пузыря, желчевыводящих протоков.
Диета
Показана диета № 5 по Певзнеру — механически и химически щадящая, употребление повышенного количества жидкости и витаминов, запрет алкоголя. Исключается острое, жареное, копчёное, ограничивается кислое и соль. Все блюда готовятся на пару, тушатся, отвариваются и подаются только в тёплом виде.
Прогноз. Профилактика
Прогноз заболевания, как правило, благоприятный. Пациенты выздоравливают спустя 1-3 месяца после выписки из стационара. В редких случаях заболевание приобретает затяжной характер.
Критерии излеченности:
- отсутствие интоксикации;
- полная нормализация уровня билирубина, АЛТ и АСТ;
- нормализация размеров печени и селезёнки;
- появление в крови антител к вирусу гепатита А класса G (Anti-HAV-IgG).
Неспецифические мероприятия, позволяющие снизить количество случаев инфицирования:
- обеспечение условий и факторов потребления безопасной питьевой воды (водоснабжение);
- обеспечение и контроль за соблюдением утилизации сточных вод (канализационное хозяйство);
- контроль за качеством обследования персонала, связанного с пищевой промышленностью;
- контроль и соблюдение технологии хранения, приготовления и транспортировки пищевых продуктов и воды.
К личным профилактическим мерам относится тщательное мытьё рук после посещения туалета, смены подгузников, а также перед приготовлением или приёмом пищи.
Вакцинация
Специфическим профилактическим мероприятием является проведение иммунизации против гепатита А: практически у 100% привитых двукратно людей вырабатывается стойкий иммунитет, предотвращающий развитие заболевания. Вакцинация — это самый лучший способ предотвратить заражение.
УДК 616.36-002.1-4
ББК 54.135
Лихота О.С., Цикуниб А.Д.
Адыгейский государственный университет, кафедра химии
Особенности метаболизма и маркеры биохимических нарушений в печени при гепатитах
Аннотация. В статье представлен аналитический обзор современной научной литературы, раскрывающий особенности метаболизма печени при гепатитах и обсуждены маркеры биохимических нарушений при различных по происхождению и интенсивности заболеваниях печени.
Ключевые слова: метаболизм печени, маркеры биохимических нарушений печени, гепатиты.
Likhota O. S., Tsikunib, A. D.
Adyghe state University, department of chemistry
Characteristics of metabolism and markers of biochemical disorders in the liver with hepatitis
Abstract. The article presents an analytical overview of modern scientific literature, revealing the peculiarities of the metabolism of the liver in hepatitis and discussed markers of biochemical disorders in various origins and intensity of liver diseases.
Keywords: liver metabolism, markers of biochemical disorders of the liver, hepatitis.
Печень является важнейшим органом, в котором протекают биохимические процессы, чрезвычайно значимые для организма в целом [11]. В ней синтезируются белки (альбумины, протромбин, фибриноген, другие факторы свертывания крови), липиды (холестерин), липопротеиды, образуются желчные кислоты, билирубин, желчь [2, 15]. В печени утилизируются токсические вещества, возникающие в организме и поступающие в организм (антитоксическая функция) [4, 12]. Печень синтезирует гликоген и участвует тем самым вместе с поджелудочной железой в регуляции углеводных запасов в организме [14]. Ее активная роль в пищеварении заключается в том, что желчь эмульгирует жиры и улучшает расщепление их липазой поджелудочной железы [13]. Продукты расщепления пищи (жиры, жирные кислоты, глицерин, аминокислоты, углеводы, минеральные вещества, вода, витамины) поступают через сосуды воротной вены в печень, в ней они частично депонируются, частично перерабатываются, используются и частично подготавливаются для использования другими тканями [10].
При заболеваниях печени возникают нарушения той или другой ее функции, что используется в диагностических целях. Наиболее широко выполняются в клинических лабораториях исследования нарушений пигментной, углеводной, белок образовательной функций. При острых воспалительных и токсических поражениях печени из ее ткани освобождается значительное количество внутриклеточных ферментов. Диагностическое значение приобрели исследования альдолаз, аланиновой и аспарагиновой трансаминаз(аминофераз), лактатдегидрогеназы и ее фракций, холинэстераз, аргиназы [1, 5, 9]. Печень участвует во всех этапах обмена жиров. Для нормального всасывания жира в кишечнике нужна желчь. Она выполняет функцию детергентаи эмульгатора жира, облегчает работу панкреатической липазы, улучшает всасывание жира в кишечнике. В печени синтезируются фосфолипиды в присутствии липотропных веществ, выступающих в качестве донаторов липидных групп (метионин, холин) либо фактора, способствующего синтезу фосфолипидов (витамин B12) [5]. При недостатке липотропных веществ в печени накапливаются нейтральные жиры, а количество гликогена уменьшается. При заболевании печени в ней уменьшается содержание аденозинтрифосфата, дающего энергию для синтетических процессов [10, 12].
Уровень холестерина в крови является важнейшим показателем синтеза липидов в печени. У здоровых людей в сыворотке крови содержится 3,0—6,5 ммоль/л (116—150 мг %) холестерина. При гепатитах и циррозах печени наблюдается нарушение содержания холестерина в крови: гиперхолестеринемия, по-видимому, связанная с нарушением выделительной функции печени, реже — гипохолестеринемия, связанная со снижением синтеза его в печени [3].
В печени осуществляется также синтез липопротеидов очень низкой плотности и утилизация липопротеидов высокой плотности. Хиломикроны и небольшая часть липопротеидов очень низкой плотности образуются в эпителиальных клетках тонкой кишки. Синтез и распад липопротеидов протекает при участии липопротеидлипазы, которая связывается с гепарином. Отмечено, что при циррозе печени содержание гепарина в крови снижается. Таким образом, печень участвует как в образовании липопротеидов, так и в их разрушении. При заболеваниях печени (гепатиты, начальные формы циррозов печени) имеет место дислипопротеинемия, в основном повышенное образование липопротеидов, преимущественно бета-липопротеидов [8].
Печень осуществляет переаминирование аминокислот, окисление их до пировиноградной кислоты в цикле трикарбоновых кислот, синтез белка. Все альбумины, 75—90 % альфа-глобулинов, 50 % бета-глобулинов синтезируются в печени. Здоровая печень может ежесуточно вырабатывать 13—18 г альбумина. Синтез белка происходит при участии энергии. Одной из причин снижения синтетической функции печени является уменьшение содержания в ней макроэргических соединений. При тяжелых заболеваниях печени общее количество сывороточного белка может понизиться до 40 г/л вместо 80 г/л. Значительно уменьшается содержание альбуминов (до 20 г/л вместо 40 г/л). В условиях патологии печень синтезирует глобулины с необычными свойствами (парапротеины) [6].
При острых воспалительных процессах (гепатит) повышается уровень альфа-глобулинов в 1,5—2 раза. Гамма-глобулины продуцируются лимфоцитами и клетками ретикулоэндотелиальной системы. При хронических гепатитах, протекающих с выраженными аутоиммунными процессами, содержание гамма-глобулинов в крови существенно увеличивается (до 30 %) [4].
При тяжелых нарушениях функции печени процесс дезаминирования аминокислот нарушается, что приводит к увеличению их содержания в крови и моче. Если у здоровых людей содержание аминного азота в сыворотке крови составляет 50—80 мг/л, то при тяжелых дистрофических процессах в печени оно может увеличиться до 300 мг/л (коэффициент перечисления аминного азота, выраженного в мг % или в ммоль/л составляет 0,7139). Отмечено, что при остром вирусном гепатите увеличивается содержание в сыворотке крови глютатиона, глютаминовой кислоты, метионина, фенилаланина, серина, треонина. При хронических гепатитах обнаруживаются те же изменения в содержании аминокислот в крови, но выраженные в меньшей степени [9].
Печень играет важную роль в обмене железосодержащих белков - гемоглобина, миоглобина, цитохромов и др. [7]. Образующийся при катаболизме данных белков токсичный, нерастворимый, свободный билирубин, не дающий прямой реакции с диазореактивом Эрлиха (непрямой) обезвреживается в печени под действием фермента билирубиндиглюкуронилтрансферазы путем конъюгации с глюкуроновыми кислотами с образованием билирубиндиглюкуронида (рисунок 1).

Рис. 1- Схема обезвреживания билирубина в печени.
Данная форма билирубина является уже нетоксичной, растворимой и прямой (дающей прямую реакцию с диазореактивом). Далее в норме обезвреженный билирубин активно переводится печенью в желчные капилляры, поступает в кишечник и превращается в мезобилиноген, часть которого обратно всасывается в кровь, поступает в печень и подвергается более глубокому катаболизму, а остальная часть в кишечнике превращается в основные пигменты кала и мочи и выводится из организма.
Чаще всего биохимические нарушения в печени происходят именно в пигментном обмене. Наиболее важное диагностическое и прогностическое значение имеет определение содержания общего билирубина и его различных фракций в сыворотке крови, исследование уробилина, стеркобилина, желчных пигментов в моче. Эти показатели прямо или косвенно отражают процесс превращения билирубина в печени. Так, при печеночно-клеточной или паренхиматозной желтухе, развивающейся при остром вирусном гепатите, обострении хронического гепатита, циррозе печени, алкогольном поражении печени, при воздействии ряда токсических веществ (хлорированные углеводороды, бензол и его производные, фосфор, свинец, ртуть, мышьяк, ядовитые грибы), а также некоторых лекарственных препаратов нарушаются захват, конъюгация и экскреции билирубина из клеток печени, а также, его регургитация. В результате указанных нарушений функций гепатоцита, отмечается умеренное или резкое повышение уровня общего билирубина крови (при норме не более 20,1 мкМоль/л, от 30 до 60-85 мкМоль/л при легкой форме, при 85-160 мкМоль/л появляются признаки средней тяжести, выше 170 мкМоль/л - тяжелая форма) с преобладанием прямой фракции (при норме не более 0 - 3,4 мкМоль/л), повышение уровня мезобилиногена (уробилина) в моче, снижение уровня холестерина и повышение активности аминотрансфераз, а также диспротеинемия с гипергаммаглобулинемией и снижение уровня протромбина[9].
Гепатоциты печены характеризуются высоким разнообразием ферментного состава. Ферменты печени, как и других органов, делятся на органоспецифические и неспецифические. Для печени органоспецифическими ферментами являются орнитинкарбамилтрансфераза, глютаматдегидрогеназа, фосфофруктоальдолаза, гистидаза, сорбитдегидрогеназа. Кроме того, специфическим считается пятый изофермент лактатдегидрогеназы ЛДГ5 [3].
Повреждение гепатоцитов приводит к освобождению значительного количества внутриклеточных ферментов и накоплению их в крови. В этой связи диагностическое значение приобрели трансаминазы, альдолазы и ряд других ферментов [5].
Альдолазы - групповое название ферментов, участвующих в механизмах аэробного расщепления углеводов. Сывороточная альдолаза катализирует обратное расщепление фруктозо-1,6-дифосфата на две фосфотриозы — фосфоглицериновый альдегид и монофосфатдиоксиацетона (рисунок 2).

Рис. 2- Химизм альдолазной реакции (по Северину Е.С. [11]).
Активность альдолазы в сыворотке крови повышена при остром эпидемическом гепатите и в меньшей мере- при остром токсическом гепатите. При остром вирусном гепатите 5—20-кратное возрастание активности фруктозодифосфатальдолазы наблюдается у 90 % больных. Ее увеличение происходит за 3—15 дней до появления других клинических признаков болезни. Спустя 5 дней от начала желтушного периода активность альдолазы уменьшается. Повышение активности альдолазы отмечается также при безжелтушных формах острого гепатита. У больных с хроническими воспалительными процессами в печени активность альдолазы возрастает незначительно, причем у небольшого их количества[10].
Аминотрансферазы (трансаминазы) часто используются с целью диагностики воспалительных заболеваний печени. Аминотрансферазы в организме человека осуществляют процессы переаминирования: обратного переноса аминогрупп аминокислот на кетокислоты (рисунок 3).

Рис. 3- Схема переаминированияальфа-аминокислот с альфа- кетокислотами, катализируемая трансаминазами(по Северину Е.С. [11]).
Наибольшее диагностическое значение имеет исследование активности аспартатаминотрансферазы (АсТ) и аланинаминотрансферазы (АлТ). Эти ферменты широко распространены в разных органах и тканях — печени, миокарде, скелетных мышцах, почках и др. [8]. При эпидемическом гепатите активность аминотрансфераз повышается с большим постоянством и в ранние сроки, еще до появления желтухи (рисунок 4).

Рис. 4- Динамика изменения активности аминотрансфераз при остром гепатите (по Коротяеву А.И. [8]).
При токсическом гепатите и обострении хронического активность аминотрансфераз возрастает в 3—5 раз(при норме не более 45 ЕД/л). Не столь закономерны изменения при циррозе печени[16].
Лактатдегидрогеназа (ЛДГ) — гликолитический фермент, обратимо катализирующий окисление 1-лактата в пировиноградную кислоту. Для ЛДГ в качестве промежуточного акцептора водорода требуется никотинамиддинуклеотид (рисунок 5).

Рис. 5- Химизм лактатдегидрогеназной реакции (по Григорьеву П.Я. [3]).
В сыворотке крови выявлено пять изоферментов ЛДГ. В печени содержится ЛДГ5 Фермент ингибируется мочевиной, и это свойство фермента облегчает его определение.
При вирусном гепатите активность ЛДГ4 и ЛДГ5 повышена в первые 10 дней у всех больных, степень ее повышения зависит от тяжести заболевания. Уровень активности общей ЛДГ в норме 240—480 МЕ/л. При остром вирусном гепатите активность ЛДГ в сыворотке крови увеличена в первые дни желтушного периода, и при легкой и среднетяжелой формах заболевания довольно бы¬стро возвращается к нормальному уровню. Тяжелые формы вирусного гепатита, и особенно развитие печеночной недостаточности, сопровождаются выраженным и более длительным повышением ЛДГ.При механической желтухе на первых стадиях закупорки желчных протоков активность ЛДГ в норме, на более поздних стадиях наблюдается подъем активности вследствие вторич¬ных повреждений печени.При карциномах печени или метастазах рака в печень может иметь место подъем актив¬ности ЛДГ.В стадии ремиссии при хроническом гепатите и циррозе печени активность ЛДГ в крови остается в пределах нормы или слегка повышена. При обострении процесса отмечается по¬вышение активности фермента[6].
Таким образом, анализ отечественной и зарубежной научной литературы показывает разнообразие и высокую диагностическую значимость маркеров заболеваний печени, основанных на особенностях метаболизма в гепатоцитах и специфике биохимических нарушений при гепатитах.
Примечания:
1. Апросина 3.Г. Хронический активный гепатит как системное заболевание. М.: Медицина, 1981. 248 с.
2. Гирин В.А. Гепатит: Современное лечение и профилактика. М.: Медицина, 2003. 435 с.
3. Григорьев П.Я. Клиника и диагностика хронического вирусного гепатита // Клиническая медицина. 1984. Т. 62, № 2. С. 56-61.
4. Иммунноферментный анализ в клинико-диагностических лабораториях / В.В. Долгов, Н.Г. Ракова, В.Е. Колупаев, Н.С. Рытикова. Тверь: Триада, 2011. 320 с.
5. Дмитириев Г.А., Глазко И.И. Диагностика инфекций, передаваемых половым путем. М.: БИНОМ, 2007. 320 с.
6. Казанцев А.П., Матковский В.С. Справочник по инфекционным болезням. 3-е изд., перераб. и доп. М.: Медицина, 2009. 320 с.
7. Комаров Ф.И., Коровкин Б.Ф., Меньшов В.В. Биохимические исследования в клинике. 2-е изд. Л.: Медицина, 1997. 407 с.
8. Коротяев А.И., Бабичев С.А. Медицинская микробиология, иммунология и вирусология: учеб. для мед. вузов. 4-е изд. М., 2008. 305 с.
9. Ивлев А.С., Хазанов А.И., Румянцев О.Н. Длительные холестазы у больных с дефицитом иммуноглобулина А сыворотки крови // Клиническая медицина. 2007. Т. 65, № 10. С. 131-133.
10. Мусил Я. Основы биохимии патологических процессов. М.: Медицина, 1995. 430 с.
11. Биохимия: учеб. для вузов / под ред. Е.С. Северина. М.: Гоэтар-Медиа, 2003. 779 с.
12. Guthik G. Current heratology. Chichester: John Wiley, 2004. 25 р.
13. Prognostic value of serum fibronectin concentration in alconolikcirrotic patients / S. Neveau, Th. Poynard, A. Abella, J. Rignon // Hematology. 2005. 45 р.
14. Schiff L.E.R. Diseases ot the liver. 5 th ed. Philadelphia: Lirinuott, 2012. 125 р.
15. Tietz N.W. Clinical guide to laboratory tests. Philadelphia: W. B. Saunder Company, 2003. 305 р.
16. Wallhofer H., Schmidt E., Schmidt F.W. Synopsis der Leberkrankheiter. Stuttgart: G. Thime, 2007. 75 р.
_____________________________________________________________________________________
Лихота Ольга Сергеевна, магистрант, тел. 89898090399, e-mail: Этот адрес электронной почты защищен от спам-ботов. У вас должен быть включен JavaScript для просмотра.
Likhota Olga Sergeevna, undergraduate, tel 89898090399, e-mail: Этот адрес электронной почты защищен от спам-ботов. У вас должен быть включен JavaScript для просмотра. .
Цикуниб Аминет Джахфаровна, доктор биологических наук, профессор, директор НИИ комплексных проблем АГУ, зав. лабораторией нутрициологии и экологии, 385000, г. Майкоп, ул. Гагарина, 13, 8928461725, Этот адрес электронной почты защищен от спам-ботов. У вас должен быть включен JavaScript для просмотра. .
Tsikunib Aminet Dzhakhfarovna, Head of Nutrition and Environment Laboratory, Director of Scientific Research Institute of complex Problems of Adyghe State University
Что такое гепатит Б? Причины возникновения, диагностику и методы лечения разберем в статье доктора Александрова Павла Андреевича, инфекциониста со стажем в 14 лет.
Над статьей доктора Александрова Павла Андреевича работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Вирусный гепатит В (Б) — острое и хроническое инфекционное заболевание, вызываемое вирусом гепатита В, с гемоконтактным механизмом передачи (через кровь), протекающее в различных клинико-морфологических вариантах, и возможным развитием цирроза печени и гепатоцеллюлярной карциномы. Всего в мире, по самым скромных оценкам, инфицировано более 250 млн человек.
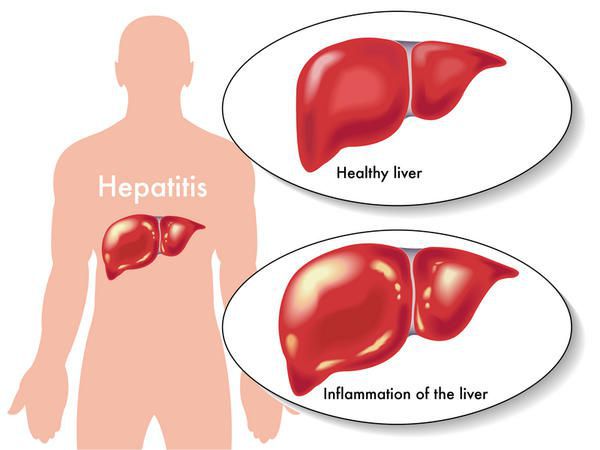
Этиология
вид — вирус гепатита В (частица Дейна)
Развитие вируса гепатита Б происходит в гепатоцитах (железистых клетках печени). Он способен к интеграции в ДНК человека. Имеются 9 генотипов вируса с различными подтипами — генетическая изменчивость позволяет вирусу образовывать мутантные формы и ускользать от действия лекарств.
Имеет ряд собственных антигенов:
- поверхностный HbsAg (австралийский). Появляется за 15-30 дней до развития болезни, свидетельствует об инфицировании (не всегда). Антитела к HbsAg выявляются через 2-5 месяцев от начала заболевания, а сам HbsAg исчезает из крови (при благоприятном течении процесса);
- сердцевинный HbcorAg (ядерный, коровский). Появляется в инкубационном периоде и совместно с ним появляются антитела (HbcorAb). Длительное присутствие HbcorAg в крови свидетельствует о вероятной хронизации процесса (неадекватный иммунный ответ);
- антиген инфекциозности и активного размножения вируса (HbeAg). Появляется совместно с HbsAg и отражает степень инфицированности. Его продолжительная циркуляция в крови является свидетельством развития хронизации процесса, а антитела к нему являются благоприятным прогностическим признаком (не всегда, но по меньшей мере указывают на возможность более благоприятного процесса, срок их циркуляции после выздоровления окончательно не определён, но не более пяти лет после благоприятного разрешения процесса);
- HbxAg — регулятор транскрипции, способствует развитию гепатокарциномы.
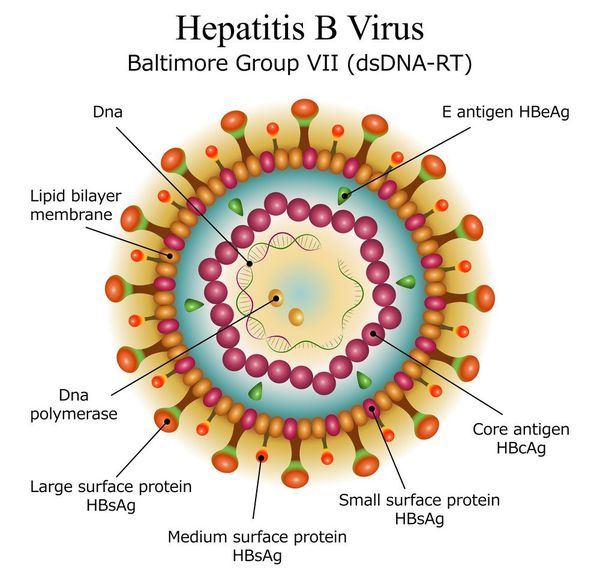
Вирус гепатита В чрезвычайно устойчив к действию всевозможных естественных факторов окружающей среды, инактивируется при 60 °C за 10 часов, при 100 °C за 10 минут, при оптимальной температуре сохраняется до 6 месяцев, при автоклавировании погибает за 5 минут, в сухожаровом шкафу — через 2 часа, 2% раствор хлорамина убивает вирус за 2 часа. [1] [3]
Эпидемиология
Источник инфекции — только человек, больной острой или хронической формой инфекции.
Механизм передачи: гемоконтактный и вертикальный (от матери к ребёнку), не исключается трансмиссивный механизм передачи (например, при укусах комаров в результате раздавливания и втирания инфицированного тела комара в поврежденную ткань человека).
Пути передачи: половой, контактно-бытовой, гемотрансфузионный (например, при переливании крови или медицинских манипуляциях). Восприимчивость всеобщая. Заболеваемость — 30-100 человек на 100 тысяч населения (зависит от страны). Летальность от острых форм — до 2%. После перенесённого острого заболевания при условии выздоровления иммунитет стойкий, пожизненный.
Для заражения характерна малая заражающая доза (невидимые следы крови). [1] [2]
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы гепатита Б
Инкубационный период гепатита В длится от 42 до 180 дней (следует иметь в виду, что наличие клинической симптоматики характеризует лишь незначительную долю всех случаев заболевания).
Начало постепенное. Характерные синдромы:
- общей инфекционной интоксикации (проявляется как астеноневротический синдром);
- холестатический (нарушение секреции желчи);
- артрита;
- нарушения пигментного обмена (появление желтухи при уровне общего билирубина свыше 40 ммоль/л);
- геморрагический (кровоточивость кровеносных сосудов);
- экзантемы;
- отёчно-асцитический (скопление жидкости в брюшной полости);
- гепатолиенальный (увеличение печени и селезёнки).
При первых признаках гепатита B нужно обратиться к доктору.
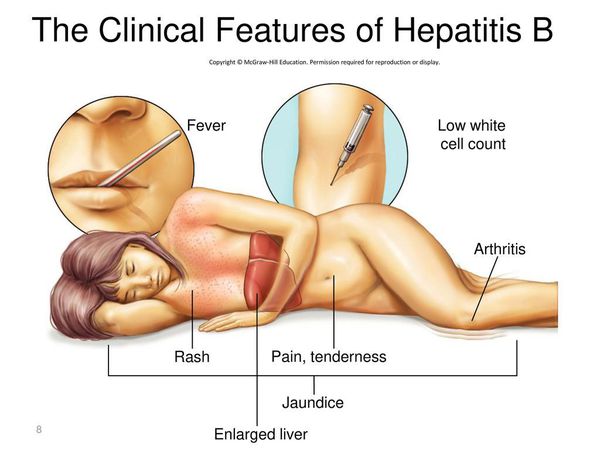
Первые признаки гепатита B
Начальный (преджелтушный) период продолжается 7-14 дней. Чаще протекает по многообразному типу с болевыми ощущениями в различных суставах по ночам и утром, уртикарными высыпаниями, астеновегетативными проявлениями (снижение аппетита, апатия, нервозность, слабость, разбитость, повышенная утомляемость). Изредка развивается синдром Джанотти-Крости — симметричная, яркая пятнисто-папулёзная сыпь. Не исключены умеренные диспептические явления (расстройства пищеварения). К концу периода происходит потемнение мочи, обесцвечивание кала.
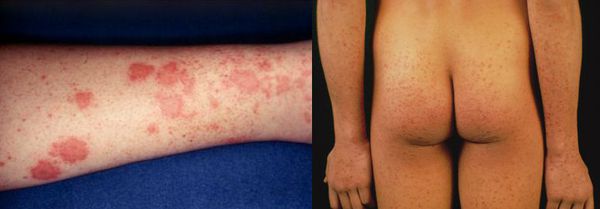
Желтушный период
Этот период продолжительностью около одного месяца характеризуется возникновением желтушного окрашивания кожи (различных оттенков) на фоне продолжающегося или ухудшающегося общего состояния. Характерна длительность и стойкость симптоматики. Появляется тяжесть и болезненность в правом подреберье, горечь во рту, тошнота, выражённый зуд кожи (практически не снимаемый никакими средствами). На фоне усиления астеноневротического компонента появляются геморрагические проявления, урежение пульса, гипотензия, отёки (отражает степень интоксикации и нарушения функций печени).
Выздоровление
Следующим этапом в развитии болезни является нормализации общего состояния, спадение желтухи и реконвалесценция, которая в зависимости от конкретной ситуации и состояния иммунной системы может закончиться как выздоровлением, так и движением развития заболевания в хроническое течение, характеризующееся маловыраженой неусточивой симптоматикой, преимущественно в виде слабости, периодического дискомфорта в правом подреберье, бурно сигнализирующим лишь на стадии цирроза и полиорганных осложнений.
- гепатиты другой этиологии;
- желтухи другой этиологии (например, гемолитическая болезнь, токсическое поражение, опухоли);
- малярия; ;
- лептоспироз;
- ревматоидный артрит.
Гепатит В у беременных
Острый гепатит характеризуется более тяжёлым течением у беременной, возникновении повышенного риска преждевременных родов, аномалий развития плода на ранних сроках и кровотечений. Вероятность передачи при острой форме зависит от сроков беременности: в первом триместре риск 10% (но более тяжёлые проявления), в третьем триместре — до 75% (чаще бессимптомное течение после родов). У большинства детей при заражении во внутриутробном и постнатальном периодах происходит хронизация инфекции. [1] [3] [6]
Патогенез гепатита Б
С движением кровяной массы вирус попадает в печеночную ткань, где локализуется в гепатоцитах и теряет свою протеиновую сферу в лизосомах. Происходит выход вирусной ДНК с последующим ресинтезом аномальных протеинов LSP, а параллельно образование новых частиц Дейна.
В процессе эволюции вирусчеловеческого взаимодействия возможно развитие двух вариантов:
При репликативном пути происходит следующее: белки LSP совместно с HbcorAg вызывают увеличение продукции гамма-интерферона, что приводит к активации главного комплекса гисотсовместимости (HLA), проистекает преобразование молекул гистосовместимости 1 и 2 классов, в результате чего клетка становиться для организма враждебной в антигенном формате.
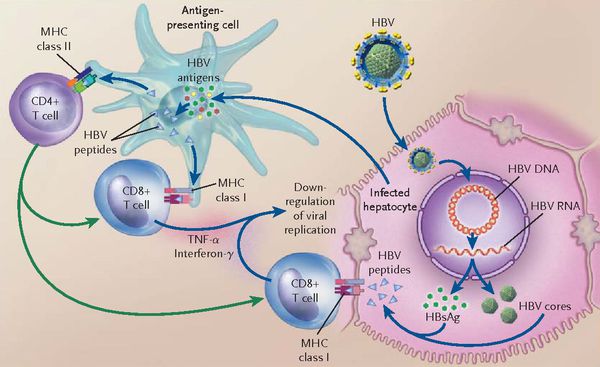
Антигенпрезентирующие макрофаги содействуют изменению В-лимфоцитов в плазматические клетки и экспрессии ими агрессивных белков-антител к посторонним антигенам. В итоге на поверхности печёночных клеток формируются вирусспецифические иммунные комплексы (антиген + антитело + фракция комплемента С3в).
В динамике может реализоваться два сценария:
- в первом варианте запуск каскада комплимента ведёт к появлению в составе иммунных комплексов агрессивной фракции С9 (мембранатакующий комплекс) — наблюдается значительный некроз гепатоцитов без участия лимфоцитов (молниеносная форма гепатита В);
- при альтернативной варианте (наблюдающимся в большинстве случаев) каскад комплемента в силу иммуноиндивидуалистических свойств не активируется — тогда идёт умеренное разрушение Т-киллерами меченых антителами заражённых вирусом гепатоцитов. Образуются ступенчатые некрозы с образованием на месте гибели гепатоцитов соединительной ткани — рубцов (то есть острый гепатит В при плохом иммунном ответе постепенно переходит в хронический).
Непременным атрибутом патогенеза является формирование иммунопатологического процесса. Гибель гепатоцитов, инфицированных вирусом гепатита В, следует за счёт иммунокомпетентных частиц, Т-киллеров и макрофагальных элементов.
Серьёзным значением является нарушение свойств мембраны клеток печени, что сопровождается экскрецией (выделением) лизосомальных ферментов, разрушающих гепатоциты. Сообразно этому, гибель гепатоцитов происходит за счёт иммунокомпетентных клеток, лизосомальных ферментов и противопечёночных гуморальных аутоантител, то есть острая болезнь наступает (и благоприятно заканчивается) только при хорошем иммунитете, а при плохом идёт хронизация.
При тяжёлом цитолитическом синдроме (массивные некрозы гепатоцитов) возникает гипокалиемический алкалоз, острая печёночная недостаточность, печёночная энцефалопатия (ПЭП), церебротоксическое действие, нарушение функции обмена нервной ткани. [2] [3] [6]
Классификация и стадии развития гепатита Б
По цикличности течения:
- острый;
- острый затяжной;
- хронический.
По клиническим проявлениям:
- субклинический (инаппарантный);
- клинически выраженный (желтушный, безжелтушный, холестатический, фульминантный).
По фазам хронического процесса:
Группы риска хронического гепатита B
Хроническим гепатитом чаще страдают дети младше шести лет. При заражении в первый год жизни он развивается в 80–90 % случаев, от года до шести лет — в 30–50 %, у взрослых без сопутствующих заболеваний — менее чем в 5 %. [7]
Осложнения гепатита Б
Чем опасен гепатит Б
Заболевание может привести к острой печёночной недостаточности (синдрому острой печеночной энцефалопатии).
Выделяют четыре стадии болезни:
Диагностика гепатита Б
Многообразие форм, тесная взаимосвязь с иммунной системой человека и зачастую достаточно высокая стоимость исследований часто затрудняют принятие конкретного решения и диагноза в стационарный отрезок времени, поэтому во избежание роковых (для больного) ошибок следует подходить к диагностике с учётом всех получаемых данных в динамическом наблюдении:
- общеклинический анализ крови с лейкоцитарной формулой (лейкопения, лимфо- и моноцитоз, уменьшение СОЭ, тромбоцитопения);
- общий анализ мочи (появление уробилина);
- биохимический анализ крови (гипербилирубинемия в основном за счёт связанной фракции, повышение уровня АЛТ и АСТ, ГГТП, холестерина, щелочной фосфатазы, снижение протромбинового индекса, фибриногена, положительная тимоловая проба);
- маркеры гепатита В: HbsAg, HbeAg, HbcorAg, HbcorAb IgM и суммарные, HbeAb, anti-Hbs, ПЦР в качественном и количественном измерении);
- УЗИ органов брюшной полости, КТ и МРТ диагностика;
- фиброскан (применяется для оценки степени фиброза). [3][4]
Скрининг при хроническом гепатите
Пациентам с хроническим гепатитом В рекомендуется не реже чем раз в полгода проходить обследование: УЗИ органов брюшной полости, клинический анализ крови, АЛТ, АСТ, тест на альфа-фетопротеин. Скрининг позволяет вовремя заметить обострение болезни и начать специфическую терапию.
Лечение гепатита Б
Лечение острых форм гепатита В должно осуществляться в стационаре (учитывая возможность быстрых и тяжёлых форм болезни), хронических — с учётом проявлений.
Диета и режим при гепатите В
В острый период показан постельный режим, печёночная диета (№ 5 по Певзнеру): достаточное количество жидкости, исключение алкоголя, жирной, жареной, острой пищи, всё в мягком и жидком виде.
Медикаментозная терапия
При лёгкой и средней тяжести острого гепатита этиотропная противовирусная терапия (ПВТ) не показана. При тяжёлой степени и риске развития осложнений назначается специфическая противовирусная терапия на весь период лечения и возможно более длительное время.
В лечении хронических форм гепатита показаниями к назначению ПВТ является наличие уровня DNA HBV более 2000 МЕ/мл (при циррозе печении независимо от уровня), умеренное и высокое повышение АЛТ/АСТ и степени фиброза печёночной ткани не менее F2 по шкале METAVIR, высокая вирусная нагрузка у беременных женщин. В каждом конкретном случае показания определяются индивидуально, в зависимости от выраженности процесса, временной тенденции, пола, планирования беременности и другого.
Существует два пути противовирусного лечения:
- терапия пегилированными интерферонами (имеет ряд существенных противопоказаний и серьёзных побочных эффектов — не менее 12 месяцев);
- нуклеозидно-аналоговой терапии NA (используются препараты с высоким порогом резистентности вируса, длительно — не менее пяти лет, удобство применения, хорошая переносимость).
В отдельных случаях может рассматриваться применение комбинированной терапии.
Из средств патогенетической терапии в острый период используются внутривенно вводимые растворы 5% глюкозы, дезинтоксикантов, антиоксидантов и витамины. Показан приём энтеросорбентов, ферментных препаратов, при выраженном холестазе применяются препараты Урсодезоксихолевой кислоты, при тяжёлом течении — глюкокортикостероиды, методы аппаратного плазмофереза.
В хронической стадии заболевания при наличии соответствующей активности процесса и невозможности назначения ПВТ может быть показан приём групп гепатопротекторов и антиоксидантов. [1] [3]
Прогноз. Профилактика
Основное направление профилактики на сегодняшний день — это проведение профилактической вакцинации против гепатита В в младенческом возрасте (в том числе усиленная вакцинация детей, рождённых от матерей с гепатитом В) и далее периодические ревакцинации раз в 10 лет (или индивидуально по результатам обследования). Достоверно показано, что в странах, где была введена вакцинация, резко сократилось количество вновь выявленных случаев острого гепатита В.
Вторая составляющая стратегии профилактики включает обеспечение безопасности крови и её компонентов, использование одноразового или стерилизованного инструментария, ограничение числа половых партнёров и использование барьерной контрацепции. [1] [2]
Читайте также:

