Плоскоклеточная папиллома гортани с дисплазией
Обновлено: 19.04.2024
Статья посвящена папилломавирусной инфекции (ПВИ) - одной из самых распространенных вирусных инфекций, передаваемых половым путем. Представлены сведения о биологии вируса, путях заражения, патогенезе, клинических проявлениях инфекции. Рассматриваются различные клинические формы заболевания: манифестные - остроконечные кондиломы (аногенитальные бородавки), субклинические (интраэпителиальная неоплазия) и латентные. Обсуждаются подходы к лечению лечения ПВИ, включающие деструктивные (физические, химические), хирургические, иммунологические и комбинированные методы. Приводятся доказательства эффективности применения препарата Изопринозина - иммуномодулятора с противовирусной активностью при различных формах ПВИ, изученного в многочисленных зарубежных и отечественных исследованиях.
Ключевые слова: папилломавирусная инфекция, остроконечные кондиломы, деструктивные методы лечения, иммунокорригирующая терапия, Изопринозин
Папилломавирусная инфекция (ПВИ) относится к наиболее распространенным инфекциям, передаваемым половым путем. В США ежегодно выявляют около 5 млн новых случаев этого заболевания. По данным зарубежных исследований, практически каждый человек, живущий половой жизнью, инфицирован вирусом папилломы человека (ВПЧ). Заражение ВПЧ может произойти даже при однократном половом контакте вследствие высокой контагиозности вируса. Более половины женщин и мужчин приобретают эту инфекцию в течение первых двух лет сексуально активной жизни. Риск заражения значительно возрастает при наличии многочисленных половых партнеров и раннем начале половой жизни. По данным отечественных исследований, разные формы ПВИ гениталий встречаются у 44,3 % пациенток, обращающихся в гинекологические учреждения по различным причинам. По данным биопсий шейки матки, субклинические формы инфекции выявляются у 8,1 % женщин.
Этиопатогенез папилломавирусной инфекции
ВПЧ относится к безоболочечным вирусам, содержит двухцепочечную ДНК, имеет икосаэдрическую форму. Он является строго эпителиотропным, т. к. вначале поражает базальный слой эпителия кожи и слизистых оболочек гениталий и других органов (гортани, ротовой полости, глаз и др.), а его жизненный цикл связан с дифференциацией эпителиальных клеток. Репликация ДНК ВПЧ происходит только в клетках базального слоя, а в клетках других слоев эпидермиса вирусные частицы лишь персистируют. При заражении ВПЧ в клетках эпидермиса нарушается нормальный процесс дифференцировки. Происходит клональная экспансия инфицированных ВПЧ-клеток базального слоя с их трансформацией и последующей малигнизацией. Этот процесс контролируют гены ВПЧ, кодирующие ранние белки Е6 и Е7. Морфологически при этом наблюдаются деформация слоев эпидермиса, общее утолщение кожи и слизистых оболочек. В стадии развитой инфекции клетки шиповатого слоя при переходе в зернистый оказываются наиболее активными в синтезе вирусной ДНК. Эта фаза жизненного цикла ВПЧ характеризует второй этап экспансии вирусной инфекции внутри эпидермиса. Экспрессия поздних генов L1 и L2 наступает на конечной стадии дифференцировки в роговом слое, где наблюдаются активная сборка зрелых вирусных частиц и их выделение из клеток на поверхности кожи. Участки кожи и слизистых оболочек, на поверхности которых происходит активное выделение и почкование вируса, представляют наибольшую опасность для контактного заражения [1, 15].
Типы ВПЧ "высокого риска", особенно 16-й, 18, 31 и 45-й, ассоциируются с дисплазией шейки матки, а также с раком шейки матки, заднего прохода, вульвы и полового члена. Типы ВПЧ "низкого риска", прежде всего 6-й и 11-й, вызывают развитие остроконечных кондилом. Пациенты с остроконечными кондиломами могут быть одновременно инфицированы вирусами нескольких типов. Определение типа ВПЧ помогает оценить риск малигнизации [2].
Сексуальные контакты — основной путь заражения ВПЧ. Аутоинокуляция, контактнобытовой путь передачи инфекции допускаются, но изучены мало. Заражению способствуют микротравмы кожи и слизистых оболочек. Возможен вертикальный способ заражения, т. е. вирус может передаться новорожденному во время прохождения по родовым путям и послужить причиной развития рецидивирующего респираторного папилломатоза.
Клинические проявления ПВИ
В большинстве случаев инфекция ВПЧ протекает бессимптомно. Наиболее известными практическим врачам проявлениями этой инфекции являются остроконечные кондиломы, которые возникают в среднем через 1—3 месяца после заражения. С момента инфицирования и до развития предраковых заболеваний или рака in situ обычно проходит от 5 до 30 лет и очень редко - менее года. У 40 % больных отмечены субклинические, малосимптомные проявления заболевания в виде мелких плоских бородавок.
Манифестация инфекции ВПЧ наиболее часто сопровождается появлением остроконечных кондилом (аногенитальных бородавок). Они возникают, как правило, на коже и слизистых оболочках половых органов или в анальной области в местах трения и травматизации при половом акте. У лиц, практикующих орально-генитальные контакты, кондиломы могут возникнуть на губах, языке, небе. Чаще высыпания представлены узелковыми образованиями, сгруппированными по 5-15 элементов, иногда сливающимися в бляшки; реже высыпания бывают единичными. Слияние в крупные бляшки происходит при иммуносупрессии, соматических заболеваниях, метаболических нарушениях, интоксикациях. У некоторых больных с выраженными нарушениями клеточного иммунитета (ВИЧ-инфекцией, на фоне иммуносупрессивной терапии), при беременности развиваются очень крупные генитальные бородавки - гигантские кондиломы Бушке-Левенштейна. Эта предраковая инвазивная и деструктирующая опухоль ассоциируется с ВПЧ-6 и ВПЧ-11. Кондиломы могут быть плоской, конической или напоминающей цветную капусту форм. Цвет образований варьируется от беловато-телесного до розовато-синюшного, реже - красновато-коричневого.
Клинически выделяют четыре типа остроконечных кондилом:
Остроконечные кондиломы обычно бессимптомны и часто случайно выявляются самим больным или врачом при осмотре. Однако крупные или травмированные, изъязвленные или подвергшиеся вторичной инфекции бородавки сопровождаются зудом, болью, неприятным запахом и гнойным отделяемым. При локализации кондилом в уретре могут развиться признаки вялотекущего уретрита, кондиломы могут вызвать раздвоение струи мочи или даже обструкцию уретрального отверстия [3].
Диагностика и принципы лечения
Для диагностики ВПЧ-инфекции помимо клинического осмотра проводят лабораторные методы исследования: цитологические, гистологические, а также молекулярно-генетические, получившие в последнее время широкое распространение. ПЦР является более чувствительным методом диагностики, чем цитологическое исследование, и способна выявить субклинические и латентные формы заболевания. Метод имеет не только важную диагностическую ценность, но и прогностическое значение, т. к. позволяет идентифицировать отдельные типы ВПЧ [2].
Лечение ВПЧ-инфекции направлено на устранение ее клинических проявлений - остроконечных кондилом.
Для этого применяют различные методы наружной терапии:
Эффективность этих методов лечения составляет от 30 до 70 %. Активность ВПЧ зависит прежде всего от иммунного статуса и реакции организма на инфекцию. Для повышения эффективности терапии в лечебный комплекс необходимо включать противовирусные препараты и иммуномодуляторы для стимуляции иммунного ответа пациента [4, 16].
Показано, что иммунный ответ хозяина имеет большое значение в предотвращении клинической манифестации ВПЧ-инфекции. Клеточный иммунитет играет основную роль как в персистенции, так и в спонтанном регрессе кондилом, который может наступить через 6-8 месяцев. Это подтверждается данными о более высокой частоте ВПЧ-ассоциированных заболеваний у реципиентов трансплантата внутренних органов и ВИЧ-инфицированных. Нарушение Т-клеточного иммунитета у больных кондиломами проявляется снижением количества клеток Лангерганса в очагах поражения и большом числе CD4+- и CD8+-T-лимфоцитов в инфильтрате регрессирующих генитальных бородавок [1].
Изопринозин в лечении ПВИ
Иммуномодулирующее действие Изопринозина заключается в усилении пролиферации и стимулировании функций Т-лимфоцитов: Т-хелперов, естественных клеток-киллеров; увеличении продукции интерлейкинов и нормализации продукции интерферона. Препарат стимулирует биохимические процессы в макрофагах, повышает хемотаксическую и фагоцитарную активность моноцитов, макрофагов и полиморфноядерных клеток. Иммуномодулирующие потенции Изопринозина более активно проявляются в стимулировании клеточного, чем гуморального, иммунитета. Опытным путем было показано, что его действие в большей степени проявляется при иммуносупрессии по сравнению со здоровым организмом. Изопринозин восстанавливает и усиливает деятельность клеток иммунной системы, тем самым повышает способность организма эффективно противостоять инфекциям.
Препарат отличается от других иммуномодуляторов тем, что обладает не только иммуномодулирующим, но и противовирусным (подтвержденным in vivo и in vitro) действием. Противовирусное действие Изопринозина заключается в подавлении репликации ДНК и РНК вирусов посредством связывания с рибосомой клетки и изменения ее стереохимического строения. Фармакокинетика препарата хорошо изучена. Максимальная концентрация Изопринозина достигается через час после приема 1,5 г препарата. Первый период полувыведения (50 минут) связан в выведением инозина и проходит с образованием мочевой кислоты. Второй период полувыведения диметиламино-2-пропанол β-ацетамидо-бензоата равен 3—5 часам, при этом метаболиты выводятся почками. Во время приема Изопринозина не рекомендуется применять иммунодепрессанты, а также лекарственные препараты, обладающие нефротоксичным действием [5, 6].
Благодаря своему комплексному действию Изопринозин более 35 лет успешно применяется при лечении различных, в т. ч. трудно поддающихся терапии, инфекционных заболеваниях кожи и слизистых оболочек. Основными показаниями к применению препарата в дерматовенерологии служат вирусные дерматозы: ПВИ, простой герпес, опоясывающий лишай. Многочисленные исследования подтвердили высокую клиническую эффективность Изопринозина в лечении персистирующих герпес-вирусных инфекций. Антивирусная активность препарата проявляется не только в области клинических проявлений (везикулы, эрозии), но и в нервных ганглиях. Поэтому он оказывает свое лечебное действие как в фазе обострения герпетической инфекции, так и в межрецидивный период. Препарат можно назначать в поддерживающей дозе на период до 6 месяцев [7, 14, 18].
Проведенные исследования показали, что применение инозиплекса в комплексе с деструктивными методами у пациентов с остроконечными кондиломами способствует более активному их разрешению и уменьшает частоту рецидивов, что объясняется активным иммунокорригирующим и противовирусным действиями препарата во всех зонах инвазии ВПЧ в коже [10, 17]. Препарат применяли по 1000 мг три раза в сутки в течение 28 дней.
В настоящее время несомненной представляется ведущая роль ВПЧ в генезе рака шейки матки. ВПЧ также может инициировать и поддерживать хронические воспалительные процессы в нижних отделах гениталий, поскольку при ВПЧ-индуцированном изменении структуры эпителия создаются предпосылки к заражению различными вирусными, бактериальными, протозойными, грибковыми и другими инфекциями. Показано, что одновременное инфицирование ВПЧ и вирусом простого герпеса II типа в два раза повышает риск развития плоскоклеточного рака шейки матки [19]. Имеются данные об успешном применении Изопринозина в лечении ПВИ шейки матки, цервикальной интраэпителиальной неоплазии и даже преинвазивного рака шейки матки.
В поликлиническом отделении Центра охраны здоровья матери и ребенка была изучена эффективность комбинированного лечения (этиотропный препарат, Изопринозин и абляция) 64 больных с гистологически подтвержденными субклиническими формами ПВИ на фоне хронического цервицита. Все пациентки были разделены на основную группу, в которой применяли комбинированное лечение с Изопринозином и этиотропным средством, и контрольную группу, где после курса этиологического лечения проводили только локальную монодеструкцию очагов плоскоклеточного интраэпителиального поражения. Изопринозин назначали по 2 таблетки (1000 мг) 3 раза в сутки на протяжении 5 дней за 7-10 дней до деструкции очагов. Анализ результатов проведенного лечения и последующее наблюдение за пациентками показали, что эффективность комбинированного лечения с применением Изопринозина была выше и составила 87,5 %, а при монодеструкции - 65,6 %. Рецидивирование ПВИ к 6-му месяцу наблюдения было выявлено лишь у 9,4 % женщин, принимавших Изопринозин, а в контрольной группе - у 28,1 % пациенток. Симптоматика воспалительного процесса на шейке матки наблюдалась только при рецидиве ВПЧ-инфекции. Кроме того, на фоне комплексного лечения через 6 месяцев чаще наблюдалась элиминация ВПЧ (65,6 и 46,9 % соответственно) и более качественная эпителизация. На основании полученных данных авторы пришли к выводу, что адекватная иммунотерапия способствует более полной элиминации ПВЧ, т. к. позволяет воздействовать не только на участок эпителия, где произошла клиническая манифестация, но и на резервуары ВПЧ в эпителии, находящиеся в латентном состоянии. Поэтому включение антивирусного иммуномодулирующего препарата Изопринозин в курс лечения больных хроническим цервицитом и ПВИ является обоснованным и перспективным [5].
Заключение
ПВИ вследствие ее широкой распространенности и отсутствия надежных методов лечения на сегодняшний день является актуальной проблемой в клинической практике. Терапевтическая стратегия при этом заболевании должна быть направлена не только на удаление локальных очагов инфекции — остроконечных кондилом, но и на воздействие на субклинические и латентные формы ВПЧ-инфекции. При этом большое значение в предотвращении рецидива и процесса канцерогенеза имеет элиминация ВПЧ. Поэтому в терапевтический комплекс необходимо включать препараты с противовирусным и иммуномодулирующим действиями для активации иммунной системы организма и подавления вирусной активности. Изопринозин является одним из наиболее изученных и эффективных иммунных препаратов с противовирусным действием. Более 35 лет его с успехом применяют в широкой клинической практике для лечения ПВИ и других вирус-ассоциированных заболеваний кожи и слизистых оболочек. Хорошая переносимость препарата, минимум побочных эффектов, возможность применять его в индивидуальной дозировке и в комбинации с другими методами лечения позволяют использовать его в лечении ВПЧ как у детей, так и у взрослых.
Папиллома трахеи. Аденома трахеи и бронхов.
Папиллома встречается редко. Различают солитарные и множественные папилломы (папилломатоз). Солитарная папиллома наблюдается преимущественно у лиц в возрасте 50—70 лет, однако может быть и у лиц молодого возраста. Опухоль располагается в трахее или крупных бронхах в виде бородавчатого образования на широком основании.
Плоскоклеточная папиллома при микроскопическом исследовании состоит из соединительной ткани, покрытой метаплазированным (многослойным плоским) эпителием, иногда с примесью слизьобразующих клеток. Переходно-клеточная папиллома развивается из респираторного эпителия. Сосочки покрыты кубическим, призматическим и даже мерцательным эпителием.
В то же время встречаются фокусы плоскоклеточной метаплазии, могут встречаться участки дисплазии.
Ряд авторов указывают на необходимость тщательного исследования папиллом для исключения папилломатозного плоскоклеточного рака.
Папилломатоз (множественные папилломы нижних дыхательных путей) наблюдается редко, преимущественно в возрасте до 30 лет. Может сочетаться с папилломами гортани, что позволяет думать о вирусном его происхождении. После удаления папилломы могут рецидивировать. Длительно существующие папилломы могут озлокачествляться.
Аденома. В подслизистом слое трахеи и бронхов имеются серозные и слизистые железы, идентичные с большими слюнными железами. Из этих желез возникают опухоли, которые по морфологическим признакам и, по большей части биологическим свойствам, аналогичны опухолям слюнных желез.
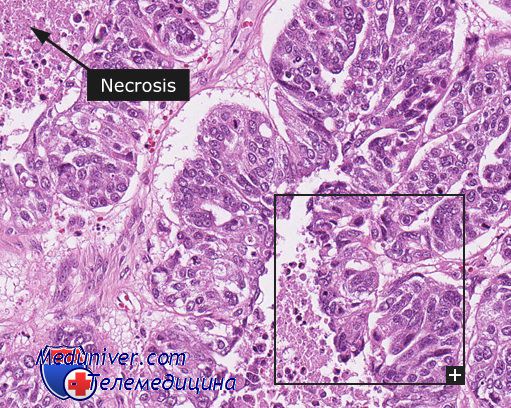
Мономорфная аденома — редкая доброкачественная опухоль. Встречается одинаково часто у мужчин и женщин в любом возрасте. Обычно возннкает в крупных бронхах, вызывая их обтурацню, несколько чаще — в правом легком. Макроскопически (при бронхоскопическом исследовании) имеет вид выбухающего образования с четкими контурами. При микроскопическом исследовании состоит из хорошо дифференцированных железистых образований (бронхиальных желез) с выраженным слизеобразованием. Преобладают кистозно расширенные железистые структуры (цистаденомы), но могут встречаться и солидные.
К другим типам относятся мукоэпидермоидные опухоли, состоящие из ацинарных и плоскоэпителиальных структур без признаков злокачественности.
Представления о дисплазии эпителия бронхов возникли в 50—60-х годах, когда стали широко применяться цитологические исследования мокроты у больных с различными заболеваниями легких. Сопоставление цитологических изменений с результатами, полученными при гистологическом исследовании в легких, удаленных по поводу рака и других заболеваний, и привело к современным представлениям о тех процессах, которые предшествуют развитию рака бронхов. Было показано, что в эпителии бронхов, преимущественно крупных (главных, долевых, сегментарных), имелись очаги метаплазии респираторного эпителия в переходно-клеточный и многослойный плоский, часто с изменениями, характерными для разной степени дисплазии. Морфологическими признаками дисплазии является клеточная и структурная атипия при сохранении целостности базальной мембраны. Дисплазия может проявляться пролиферацией базальных клеток (базально-клеточиая гиперплазия), увеличением их размеров, утратой базальной ориентации. В участках плоскоклеточной метаплазии эпителия степень выраженности дисплазии может быть различной от легкой, при которой изменения ограничены нижней третью, до тяжелой, при которой изменения наблюдаются в нижней половине или на протяжении двух третей толщи эпителиального пласта. При этом нарушается полярность расположения клеток, меняются ядерно-цитоплазматические соотношения в сторону увеличения ядра, отмечается клеточный и ядерный полиморфизм, встречаются фигуры митозов. Обычно несколько поверхностных слоев сохраняют нормальное строение. При карциноме in situ изменения захватывают всю толщу эпителиального пласта. Но материалам О. Auerbach и соавт (1957), в 89% случаев в легких, удаленных по поводу рака, были обнаружены фокусы рака in situ, рассеянные почти по всему бронхиальному дереву. В ряде случаев отмечается врастание диспластического эпителия и карциномы in situ в выводные протоки слизистых желез бронха с последующим развитием инвазивного рака. В литературе дисплазии эпителия бронхов, так же как и шейки матки, рассматривается как обратимый процесс. Устранение причин, вызвавших дисплазию (в частности. курение) ведет к ее регрессии. В литературе не приводятся цифровые мате риалы о частоте перехода дисплазии в рак и ее регрессии. Если причины выбывающие дисплазию и рак in situ, не устраняются, эти состояния могут прогрессировать иногда в течение длительного времени до развития инвазивного рака.
Большинство исследователей, изучающих рак легкого, придают большое значение определенным изменениям эпителия бронхов, в частности базально-клеточной гиперплазии и внутриэпителиальному раку, рассматривая их как возможные стадии развития плоскоклеточного и, вероятно, недифференцированного рака. На материале Всесоюзного онкологического научного центра АМН СССР (ВОНЦ) дисплазия эпителия и внутриэпителиальный рак наблюдались при плоскоклеточном раке легкого и редко — при мелкоклеточном.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Проблема папилломатоза гортани (ПГ) имеет многовековую историю. Поражая гортань, растущая опухоль приводит к нарушению голосообразовательной, а в последующем, при сужении ее просвета, и дыхательной функции органа, что имеет жизненно важное значение.
ПГ отличается частым рецидивированием, в связи с чем внимание исследователей к этой проблеме не иссякает.
Микроларингоскопия и эндоларингеальная микрохирургия значительно расширили диагностические и лечебные возможности при ПГ. Тем не менее проблема противорецидивного лечения ПГ — одна из самых актуальных в современной оториноларингологии и до настоящего времени остается во многом неразрешенной.
В послеоперационном периоде широко используются противоопухолевые препараты проспидин, блеомицин, подофиллин, однако эти препараты имеют выраженный токсический эффект. Антивирусные препараты, такие как ацикловир, рибаверин, 13-цисретиноевая кислота, и фотодинамическая лазерная терапия дают некоторый эффект, но широкое внедрение этих препаратов требует дальнейшего их изучения.
Известен противорецидивный способ лечения ПГ препаратами интерферона (ИФН): человеческим лейкоцитарным интерфероном, эги-фероном, реафероном, реальдироном, вифероном, рофероном-А, интроном-А и др. Применение препаратов экзогенного ИФН имеет определенные особенности. Необходим длительный непрерывный курс лечения — до 24-36 месяцев, используются преимущественно парентеральные методы введения. Вводимый больному экзогенный ИФН в ряде случаев распознается как чужеродный антиген и вызывает образование нейтрализующих антител. Известны также токсические, субъективные и объективные побочные реакции на введение ИФН. Кроме того, лечение препаратами ИФН — достаточно дорогой метод.
Индукторы ИФН вызывают образование собственного ИФН в организме хозяина. Процесс этот более физиологичен, чем постоянное введение больших доз ИФН. Кроме того, продукция ИФН в ответ на действие индукторов контролируется самим организмом.
Разработанный нами способ лечения ПГ включает в себя щадящее эндоларингеальное удаление папилломатозных разрастаний инструментальным методом под микроскопическим контролем с последующим включением в схему лечения препарата, стимулирующего систему ИФН, — циклоферона.
Материалы и методы
Циклоферон назначали по 2,0 мл 12,5% раствора в 1, 2, 4, 6, 8,11, 14, 17, 20, 23-и сутки и далее по 1 инъекции 1 раз в 10 дней в течение 6 месяцев.
Применение циклоферона сочетали с антиоксидантной терапией витаминами С, Е, назначали эссенциале, при необходимости антибиотики.
Теоретической предпосылкой для обоснования предложенного способа лечения явился выявленный при исследовании интерферонового статуса дефицит системы ИФН. Исследования проводили в лаборатории НИИ эпидемиологии и микробиологии им. Н. Ф. Гамалеи РАМН. У всех больных изучали систему клеточного иммунитета, чувствительность к циклоферону, ставили реакции ИФН-статуса I ступени (по С. С. Григорян), позволяющие определить количественные параметры ИФН-ответа in vitro и in vivo до оперативного вмешательства и через 1,5-2 месяца после прекращения лечения. Критерием эффективности лечения служило уменьшение количества рецидивов заболевания.
Под нашим наблюдением находились 48 больных ПГ в возрасте от 16 до 88 лет. Срок наблюдения — 2,5 года.
Для проведения эндоларингеального микрохирургического вмешательства использовали операционный микроскоп с фокусным расстоянием 400 мм, что дает возможность свободно манипулировать гортанным зеркалом и инструментами. Вмешательство проводили под местной аппликационной анестезией слизистой оболочки гортани 2-6 мл 10% раствора лидокаине и 0,5 мл 0,1% раствора адреналина.
На вторые сутки после операции назначали циклоферон и рекомбинантный ИФН. 20 больных получали циклоферон, остальные 28 — рекомбинантный препарат ИФН реаферон — они составили контрольную группу.
Результаты и их обсуждение
В целом оценка результатов лечения представляет большие трудности, обусловленные прежде всего своеобразием клинического течения папилломатоза. В частности, известно, что в течении этого заболевания могут спонтанно наступать как длительные ремиссии, так и периоды бурного роста папиллом.
Исследование интерферонового статуса перед началом лечения обнаружило у большинства больных снижение продукции а-ИФН от 40 до 320 ед/мл и у-ИФН от 4 до 32 ед/мл с преобладанием дефицита продукции у-ИФН, указывающего, в свою очередь, на дефицит Т-клеточного звена иммунитета. Таким образом, наблюдалось снижение ИФН-продуцирующей способности лейкоцитов II и III степени. Спонтанная продукция ИФН и выявляемые нередко повышенные титры сывороточного ИФН явились дополнительным свидетельством наличия персистирующей вирусной инфекции. Кроме того, было замечено нарастание титров сывороточного ИФН и степени выраженности дефицита продукции а- и у-ИФН в зависимости от тяжести клинического проявления заболевания.
При исследовании клеточного иммунитета у большинства больных наблюдали дефицит Т-клеток (CD4, CD8).
Контроль ИФН-статуса, проведенный через 1,5-2 мес после завершения основного курса лечения, выявил разной степени улучшение ИФН-статуса — снижение показателей сывороточного ИФН до 2-8 ед/мл и повышение уровней а- и у-ИФН в среднем в 2-3 раза от исходного.
Клиническая эффективность лечения ПГ оценивалась по уменьшению количества рецидивов заболевания в группе за 29 месяцев наблюдения. В течение 14 месяцев рецидив наблюдали только у 1 пациента из 20 больных, получавших циклоферон. За 29 месяцев наблюдения рецидив ПГ отмечен у 4 (20%) больных, получавших циклоферон. Эффективность лечения циклофероном составила 80%.
В группе больных, получавших реаферон, также отмечалась тенденция к нормализации значений ИФН-статуса, однако рецидивы отмечали чаще — у 17 (60,7%) больных в сроки от 6 до 29 мес. Эффективность лечения составила 39,3%.
Таким образом, применение щадящего микрохирургического вмешательства в сочетании с индукторами ИНФ можно считать методом выбора в лечении ПГ.
Статья посвящена папилломавирусной инфекции (ПВИ) - одной из самых распространенных вирусных инфекций, передаваемых половым путем. Представлены сведения о биологии вируса, путях заражения, патогенезе, клинических проявлениях инфекции. Рассматриваются различные клинические формы заболевания: манифестные - остроконечные кондиломы (аногенитальные бородавки), субклинические (интраэпителиальная неоплазия) и латентные. Обсуждаются подходы к лечению лечения ПВИ, включающие деструктивные (физические, химические), хирургические, иммунологические и комбинированные методы. Приводятся доказательства эффективности применения препарата Изопринозина - иммуномодулятора с противовирусной активностью при различных формах ПВИ, изученного в многочисленных зарубежных и отечественных исследованиях.
Ключевые слова: папилломавирусная инфекция, остроконечные кондиломы, деструктивные методы лечения, иммунокорригирующая терапия, Изопринозин
Папилломавирусная инфекция (ПВИ) относится к наиболее распространенным инфекциям, передаваемым половым путем. В США ежегодно выявляют около 5 млн новых случаев этого заболевания. По данным зарубежных исследований, практически каждый человек, живущий половой жизнью, инфицирован вирусом папилломы человека (ВПЧ). Заражение ВПЧ может произойти даже при однократном половом контакте вследствие высокой контагиозности вируса. Более половины женщин и мужчин приобретают эту инфекцию в течение первых двух лет сексуально активной жизни. Риск заражения значительно возрастает при наличии многочисленных половых партнеров и раннем начале половой жизни. По данным отечественных исследований, разные формы ПВИ гениталий встречаются у 44,3 % пациенток, обращающихся в гинекологические учреждения по различным причинам. По данным биопсий шейки матки, субклинические формы инфекции выявляются у 8,1 % женщин.
Этиопатогенез папилломавирусной инфекции
ВПЧ относится к безоболочечным вирусам, содержит двухцепочечную ДНК, имеет икосаэдрическую форму. Он является строго эпителиотропным, т. к. вначале поражает базальный слой эпителия кожи и слизистых оболочек гениталий и других органов (гортани, ротовой полости, глаз и др.), а его жизненный цикл связан с дифференциацией эпителиальных клеток. Репликация ДНК ВПЧ происходит только в клетках базального слоя, а в клетках других слоев эпидермиса вирусные частицы лишь персистируют. При заражении ВПЧ в клетках эпидермиса нарушается нормальный процесс дифференцировки. Происходит клональная экспансия инфицированных ВПЧ-клеток базального слоя с их трансформацией и последующей малигнизацией. Этот процесс контролируют гены ВПЧ, кодирующие ранние белки Е6 и Е7. Морфологически при этом наблюдаются деформация слоев эпидермиса, общее утолщение кожи и слизистых оболочек. В стадии развитой инфекции клетки шиповатого слоя при переходе в зернистый оказываются наиболее активными в синтезе вирусной ДНК. Эта фаза жизненного цикла ВПЧ характеризует второй этап экспансии вирусной инфекции внутри эпидермиса. Экспрессия поздних генов L1 и L2 наступает на конечной стадии дифференцировки в роговом слое, где наблюдаются активная сборка зрелых вирусных частиц и их выделение из клеток на поверхности кожи. Участки кожи и слизистых оболочек, на поверхности которых происходит активное выделение и почкование вируса, представляют наибольшую опасность для контактного заражения [1, 15].
Типы ВПЧ "высокого риска", особенно 16-й, 18, 31 и 45-й, ассоциируются с дисплазией шейки матки, а также с раком шейки матки, заднего прохода, вульвы и полового члена. Типы ВПЧ "низкого риска", прежде всего 6-й и 11-й, вызывают развитие остроконечных кондилом. Пациенты с остроконечными кондиломами могут быть одновременно инфицированы вирусами нескольких типов. Определение типа ВПЧ помогает оценить риск малигнизации [2].
Сексуальные контакты — основной путь заражения ВПЧ. Аутоинокуляция, контактнобытовой путь передачи инфекции допускаются, но изучены мало. Заражению способствуют микротравмы кожи и слизистых оболочек. Возможен вертикальный способ заражения, т. е. вирус может передаться новорожденному во время прохождения по родовым путям и послужить причиной развития рецидивирующего респираторного папилломатоза.
Клинические проявления ПВИ
В большинстве случаев инфекция ВПЧ протекает бессимптомно. Наиболее известными практическим врачам проявлениями этой инфекции являются остроконечные кондиломы, которые возникают в среднем через 1—3 месяца после заражения. С момента инфицирования и до развития предраковых заболеваний или рака in situ обычно проходит от 5 до 30 лет и очень редко - менее года. У 40 % больных отмечены субклинические, малосимптомные проявления заболевания в виде мелких плоских бородавок.
Манифестация инфекции ВПЧ наиболее часто сопровождается появлением остроконечных кондилом (аногенитальных бородавок). Они возникают, как правило, на коже и слизистых оболочках половых органов или в анальной области в местах трения и травматизации при половом акте. У лиц, практикующих орально-генитальные контакты, кондиломы могут возникнуть на губах, языке, небе. Чаще высыпания представлены узелковыми образованиями, сгруппированными по 5-15 элементов, иногда сливающимися в бляшки; реже высыпания бывают единичными. Слияние в крупные бляшки происходит при иммуносупрессии, соматических заболеваниях, метаболических нарушениях, интоксикациях. У некоторых больных с выраженными нарушениями клеточного иммунитета (ВИЧ-инфекцией, на фоне иммуносупрессивной терапии), при беременности развиваются очень крупные генитальные бородавки - гигантские кондиломы Бушке-Левенштейна. Эта предраковая инвазивная и деструктирующая опухоль ассоциируется с ВПЧ-6 и ВПЧ-11. Кондиломы могут быть плоской, конической или напоминающей цветную капусту форм. Цвет образований варьируется от беловато-телесного до розовато-синюшного, реже - красновато-коричневого.
Клинически выделяют четыре типа остроконечных кондилом:
Остроконечные кондиломы обычно бессимптомны и часто случайно выявляются самим больным или врачом при осмотре. Однако крупные или травмированные, изъязвленные или подвергшиеся вторичной инфекции бородавки сопровождаются зудом, болью, неприятным запахом и гнойным отделяемым. При локализации кондилом в уретре могут развиться признаки вялотекущего уретрита, кондиломы могут вызвать раздвоение струи мочи или даже обструкцию уретрального отверстия [3].
Диагностика и принципы лечения
Для диагностики ВПЧ-инфекции помимо клинического осмотра проводят лабораторные методы исследования: цитологические, гистологические, а также молекулярно-генетические, получившие в последнее время широкое распространение. ПЦР является более чувствительным методом диагностики, чем цитологическое исследование, и способна выявить субклинические и латентные формы заболевания. Метод имеет не только важную диагностическую ценность, но и прогностическое значение, т. к. позволяет идентифицировать отдельные типы ВПЧ [2].
Лечение ВПЧ-инфекции направлено на устранение ее клинических проявлений - остроконечных кондилом.
Для этого применяют различные методы наружной терапии:
Эффективность этих методов лечения составляет от 30 до 70 %. Активность ВПЧ зависит прежде всего от иммунного статуса и реакции организма на инфекцию. Для повышения эффективности терапии в лечебный комплекс необходимо включать противовирусные препараты и иммуномодуляторы для стимуляции иммунного ответа пациента [4, 16].
Показано, что иммунный ответ хозяина имеет большое значение в предотвращении клинической манифестации ВПЧ-инфекции. Клеточный иммунитет играет основную роль как в персистенции, так и в спонтанном регрессе кондилом, который может наступить через 6-8 месяцев. Это подтверждается данными о более высокой частоте ВПЧ-ассоциированных заболеваний у реципиентов трансплантата внутренних органов и ВИЧ-инфицированных. Нарушение Т-клеточного иммунитета у больных кондиломами проявляется снижением количества клеток Лангерганса в очагах поражения и большом числе CD4+- и CD8+-T-лимфоцитов в инфильтрате регрессирующих генитальных бородавок [1].
Изопринозин в лечении ПВИ
Иммуномодулирующее действие Изопринозина заключается в усилении пролиферации и стимулировании функций Т-лимфоцитов: Т-хелперов, естественных клеток-киллеров; увеличении продукции интерлейкинов и нормализации продукции интерферона. Препарат стимулирует биохимические процессы в макрофагах, повышает хемотаксическую и фагоцитарную активность моноцитов, макрофагов и полиморфноядерных клеток. Иммуномодулирующие потенции Изопринозина более активно проявляются в стимулировании клеточного, чем гуморального, иммунитета. Опытным путем было показано, что его действие в большей степени проявляется при иммуносупрессии по сравнению со здоровым организмом. Изопринозин восстанавливает и усиливает деятельность клеток иммунной системы, тем самым повышает способность организма эффективно противостоять инфекциям.
Препарат отличается от других иммуномодуляторов тем, что обладает не только иммуномодулирующим, но и противовирусным (подтвержденным in vivo и in vitro) действием. Противовирусное действие Изопринозина заключается в подавлении репликации ДНК и РНК вирусов посредством связывания с рибосомой клетки и изменения ее стереохимического строения. Фармакокинетика препарата хорошо изучена. Максимальная концентрация Изопринозина достигается через час после приема 1,5 г препарата. Первый период полувыведения (50 минут) связан в выведением инозина и проходит с образованием мочевой кислоты. Второй период полувыведения диметиламино-2-пропанол β-ацетамидо-бензоата равен 3—5 часам, при этом метаболиты выводятся почками. Во время приема Изопринозина не рекомендуется применять иммунодепрессанты, а также лекарственные препараты, обладающие нефротоксичным действием [5, 6].
Благодаря своему комплексному действию Изопринозин более 35 лет успешно применяется при лечении различных, в т. ч. трудно поддающихся терапии, инфекционных заболеваниях кожи и слизистых оболочек. Основными показаниями к применению препарата в дерматовенерологии служат вирусные дерматозы: ПВИ, простой герпес, опоясывающий лишай. Многочисленные исследования подтвердили высокую клиническую эффективность Изопринозина в лечении персистирующих герпес-вирусных инфекций. Антивирусная активность препарата проявляется не только в области клинических проявлений (везикулы, эрозии), но и в нервных ганглиях. Поэтому он оказывает свое лечебное действие как в фазе обострения герпетической инфекции, так и в межрецидивный период. Препарат можно назначать в поддерживающей дозе на период до 6 месяцев [7, 14, 18].
Проведенные исследования показали, что применение инозиплекса в комплексе с деструктивными методами у пациентов с остроконечными кондиломами способствует более активному их разрешению и уменьшает частоту рецидивов, что объясняется активным иммунокорригирующим и противовирусным действиями препарата во всех зонах инвазии ВПЧ в коже [10, 17]. Препарат применяли по 1000 мг три раза в сутки в течение 28 дней.
В настоящее время несомненной представляется ведущая роль ВПЧ в генезе рака шейки матки. ВПЧ также может инициировать и поддерживать хронические воспалительные процессы в нижних отделах гениталий, поскольку при ВПЧ-индуцированном изменении структуры эпителия создаются предпосылки к заражению различными вирусными, бактериальными, протозойными, грибковыми и другими инфекциями. Показано, что одновременное инфицирование ВПЧ и вирусом простого герпеса II типа в два раза повышает риск развития плоскоклеточного рака шейки матки [19]. Имеются данные об успешном применении Изопринозина в лечении ПВИ шейки матки, цервикальной интраэпителиальной неоплазии и даже преинвазивного рака шейки матки.
В поликлиническом отделении Центра охраны здоровья матери и ребенка была изучена эффективность комбинированного лечения (этиотропный препарат, Изопринозин и абляция) 64 больных с гистологически подтвержденными субклиническими формами ПВИ на фоне хронического цервицита. Все пациентки были разделены на основную группу, в которой применяли комбинированное лечение с Изопринозином и этиотропным средством, и контрольную группу, где после курса этиологического лечения проводили только локальную монодеструкцию очагов плоскоклеточного интраэпителиального поражения. Изопринозин назначали по 2 таблетки (1000 мг) 3 раза в сутки на протяжении 5 дней за 7-10 дней до деструкции очагов. Анализ результатов проведенного лечения и последующее наблюдение за пациентками показали, что эффективность комбинированного лечения с применением Изопринозина была выше и составила 87,5 %, а при монодеструкции - 65,6 %. Рецидивирование ПВИ к 6-му месяцу наблюдения было выявлено лишь у 9,4 % женщин, принимавших Изопринозин, а в контрольной группе - у 28,1 % пациенток. Симптоматика воспалительного процесса на шейке матки наблюдалась только при рецидиве ВПЧ-инфекции. Кроме того, на фоне комплексного лечения через 6 месяцев чаще наблюдалась элиминация ВПЧ (65,6 и 46,9 % соответственно) и более качественная эпителизация. На основании полученных данных авторы пришли к выводу, что адекватная иммунотерапия способствует более полной элиминации ПВЧ, т. к. позволяет воздействовать не только на участок эпителия, где произошла клиническая манифестация, но и на резервуары ВПЧ в эпителии, находящиеся в латентном состоянии. Поэтому включение антивирусного иммуномодулирующего препарата Изопринозин в курс лечения больных хроническим цервицитом и ПВИ является обоснованным и перспективным [5].
Заключение
ПВИ вследствие ее широкой распространенности и отсутствия надежных методов лечения на сегодняшний день является актуальной проблемой в клинической практике. Терапевтическая стратегия при этом заболевании должна быть направлена не только на удаление локальных очагов инфекции — остроконечных кондилом, но и на воздействие на субклинические и латентные формы ВПЧ-инфекции. При этом большое значение в предотвращении рецидива и процесса канцерогенеза имеет элиминация ВПЧ. Поэтому в терапевтический комплекс необходимо включать препараты с противовирусным и иммуномодулирующим действиями для активации иммунной системы организма и подавления вирусной активности. Изопринозин является одним из наиболее изученных и эффективных иммунных препаратов с противовирусным действием. Более 35 лет его с успехом применяют в широкой клинической практике для лечения ПВИ и других вирус-ассоциированных заболеваний кожи и слизистых оболочек. Хорошая переносимость препарата, минимум побочных эффектов, возможность применять его в индивидуальной дозировке и в комбинации с другими методами лечения позволяют использовать его в лечении ВПЧ как у детей, так и у взрослых.
Папиллома трахеи. Аденома трахеи и бронхов.
Папиллома встречается редко. Различают солитарные и множественные папилломы (папилломатоз). Солитарная папиллома наблюдается преимущественно у лиц в возрасте 50—70 лет, однако может быть и у лиц молодого возраста. Опухоль располагается в трахее или крупных бронхах в виде бородавчатого образования на широком основании.
Плоскоклеточная папиллома при микроскопическом исследовании состоит из соединительной ткани, покрытой метаплазированным (многослойным плоским) эпителием, иногда с примесью слизьобразующих клеток. Переходно-клеточная папиллома развивается из респираторного эпителия. Сосочки покрыты кубическим, призматическим и даже мерцательным эпителием.
В то же время встречаются фокусы плоскоклеточной метаплазии, могут встречаться участки дисплазии.
Ряд авторов указывают на необходимость тщательного исследования папиллом для исключения папилломатозного плоскоклеточного рака.
Папилломатоз (множественные папилломы нижних дыхательных путей) наблюдается редко, преимущественно в возрасте до 30 лет. Может сочетаться с папилломами гортани, что позволяет думать о вирусном его происхождении. После удаления папилломы могут рецидивировать. Длительно существующие папилломы могут озлокачествляться.
Аденома. В подслизистом слое трахеи и бронхов имеются серозные и слизистые железы, идентичные с большими слюнными железами. Из этих желез возникают опухоли, которые по морфологическим признакам и, по большей части биологическим свойствам, аналогичны опухолям слюнных желез.

Мономорфная аденома — редкая доброкачественная опухоль. Встречается одинаково часто у мужчин и женщин в любом возрасте. Обычно возннкает в крупных бронхах, вызывая их обтурацню, несколько чаще — в правом легком. Макроскопически (при бронхоскопическом исследовании) имеет вид выбухающего образования с четкими контурами. При микроскопическом исследовании состоит из хорошо дифференцированных железистых образований (бронхиальных желез) с выраженным слизеобразованием. Преобладают кистозно расширенные железистые структуры (цистаденомы), но могут встречаться и солидные.
К другим типам относятся мукоэпидермоидные опухоли, состоящие из ацинарных и плоскоэпителиальных структур без признаков злокачественности.
Представления о дисплазии эпителия бронхов возникли в 50—60-х годах, когда стали широко применяться цитологические исследования мокроты у больных с различными заболеваниями легких. Сопоставление цитологических изменений с результатами, полученными при гистологическом исследовании в легких, удаленных по поводу рака и других заболеваний, и привело к современным представлениям о тех процессах, которые предшествуют развитию рака бронхов. Было показано, что в эпителии бронхов, преимущественно крупных (главных, долевых, сегментарных), имелись очаги метаплазии респираторного эпителия в переходно-клеточный и многослойный плоский, часто с изменениями, характерными для разной степени дисплазии. Морфологическими признаками дисплазии является клеточная и структурная атипия при сохранении целостности базальной мембраны. Дисплазия может проявляться пролиферацией базальных клеток (базально-клеточиая гиперплазия), увеличением их размеров, утратой базальной ориентации. В участках плоскоклеточной метаплазии эпителия степень выраженности дисплазии может быть различной от легкой, при которой изменения ограничены нижней третью, до тяжелой, при которой изменения наблюдаются в нижней половине или на протяжении двух третей толщи эпителиального пласта. При этом нарушается полярность расположения клеток, меняются ядерно-цитоплазматические соотношения в сторону увеличения ядра, отмечается клеточный и ядерный полиморфизм, встречаются фигуры митозов. Обычно несколько поверхностных слоев сохраняют нормальное строение. При карциноме in situ изменения захватывают всю толщу эпителиального пласта. Но материалам О. Auerbach и соавт (1957), в 89% случаев в легких, удаленных по поводу рака, были обнаружены фокусы рака in situ, рассеянные почти по всему бронхиальному дереву. В ряде случаев отмечается врастание диспластического эпителия и карциномы in situ в выводные протоки слизистых желез бронха с последующим развитием инвазивного рака. В литературе дисплазии эпителия бронхов, так же как и шейки матки, рассматривается как обратимый процесс. Устранение причин, вызвавших дисплазию (в частности. курение) ведет к ее регрессии. В литературе не приводятся цифровые мате риалы о частоте перехода дисплазии в рак и ее регрессии. Если причины выбывающие дисплазию и рак in situ, не устраняются, эти состояния могут прогрессировать иногда в течение длительного времени до развития инвазивного рака.
Большинство исследователей, изучающих рак легкого, придают большое значение определенным изменениям эпителия бронхов, в частности базально-клеточной гиперплазии и внутриэпителиальному раку, рассматривая их как возможные стадии развития плоскоклеточного и, вероятно, недифференцированного рака. На материале Всесоюзного онкологического научного центра АМН СССР (ВОНЦ) дисплазия эпителия и внутриэпителиальный рак наблюдались при плоскоклеточном раке легкого и редко — при мелкоклеточном.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Читайте также:

