Плоскоклеточная папиллома пищевода чем опасна взяли биопсию
Обновлено: 23.04.2024
Опухоли пищевода. Доброкачественные и злокачественные опухоли пищевода.
В дистальном отделе пищевода изредка наблюдают аденому, имеющую такое же строение, что и аденомы желудка. Она может развиваться из слизистой оболочки при так называемом пищеводе Баррета, когда в результате хронического рефлюкс-эзофагита и гегеротопяи (что менее вероятно) многослойный плоский эпителий нижней части пищевода замещается цилиндрическим эпителием с формированием структур, соответствующих слизистой оболочке фундального или кардиального отделов желудка, нередко с явлениями кишечной метаплазии.
Рак — наиболее часто встречающаяся злокачественная опухоль пищевода. Чаще наблюдают у мужчин? возраст большинства которых 50—70 лет. К предрасполагающим факторам относятся особенности питания — употребление очень горячей и грубой пищи; недостаток витаминов, особенно В2, А; железа, меди, цинка; вредные привычки (курение, алкоголь и др.); некоторые географические особенности местности; аномалии и посттравматические рубцовые изменения пищевода, грыжа пищеводного отверстия диафрагмы, тилоз (гиперкератоз ладоней и подошв), синдром Пламмера—Винсона (железодефицитная анемия, гипохлоргидрия, дисфагия), наблюдающийся преимущественно у жительниц стран Скандинавского полуострова в возрасте 40 -45 лет и др.
Заболеваемость раком пищевода колеблется в очень широких пределах, достигая наиболее высоких показателей в некоторых районах Ирана, Китая, Туркменской, Казахской, Узбекской ССР и др. Эпидемиологические исследования показали, что в этих районах среди населения чрезвычайно широко распространен хронический эзофагит (60—80% населения и более), который, очевидно, имеет значение в развитии рака пищевода. При гистологическом исследовании на фоне хронического эзофагита обнаруживают очаговые и диффузные атрофические и гиперпластические изменения многослойного плоского эпителия, пролиферацию базальных клеток, очаги дисплазии, внутриэпителиальный и ранний инвазивный рак.
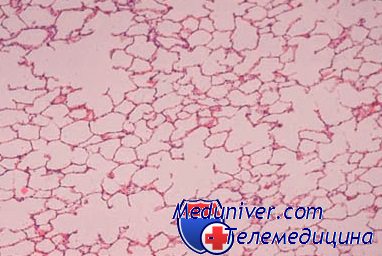
Такие же изменения часто можно обнаружить при раке пищевода, исследуя слизистую оболочку на различном расстоянии от опухоли. Эти изменения, по-видимому, являются основными этапами морфогенеза рака пищевода, что подтверждается динамическими наблюдениями, проведенными в районах Китая с повышенной заболеваемостью раком пищевода.
В тех случаях, когда базальная мембрана не прослеживается, имеется тенденция к погружному росту и отшнуровка эпителиальных комплексов, изменения должны расцениваться как начало инвазивного рака.
При гистологическом исследовании, особенно по материалу эндоскопической биопсии, бывает трудно дифференцировать диспластические (предраковые) изменения и реактивную гиперплазию базальных клеток, которая может наблюдаться, например, при рефлюкс-эзофагите.
Трудности возникают также при дифференциальной диагностике тяжелой дисплазии, карциномы in situ и инвазивного рака. Для уточнения характера процесса необходимы динамическое наблюдение за такими больными и повторные биопсии.
Основная масса форм плоскоклеточного рака пищевода, видимо, развивается из покровного эпителия. Другим источником развития рака пищевода могут быть слизистые железы, в которых при хроническом гастрите также наблюдают атрофические и гиперпластические изменения, образование кист, пролиферацию резервных клеток, плоскоклеточную метаплазию и дисплазию эпителия. Из них могут возникать плоскоклеточный рак, аденокарцинома, железисто-плоскоклеточный рак, а также мукоэлидермоидная опухоль и аденокистозный рак (цилиндрома), аналогичные соответствующим опухолям слюнных желез. Аденокарциномы в пищеводе могут развиваться также от остатков цилиндрического эпителия, выстилающего пищевод на ранних стадиях эмбриогенеза, участков гетеротопии слизистой оболочки желудка.
Аденокарциномы дистальной части пищевода могут развиваться также на фоне так называемого пищевода Баррета. Во многих случаях труден или невозможен дифференциальный диагноз такой аденокарциномы и рака кардиального отдела желудка, прорастающего в пищевод.
Рак пищевода наиболее часто локализуется в средней его трети, затем следует нижняя треть пищевода; верхняя его треть поражается редко. Исключение составляет рак пищевода при синдроме Пламмера—Винсона, который наблюдается преимущественно у женщин 40—45 лет и поражает самый верхний отрезок пищевода.
Макроскопически большинство форм рака пищевода представляет собой изъязвленные блюдцеобразные или эндофитные опухоли, часто циркулярно охватывающие стенку, нередко на значительном протяжении. Экзофитные опухоли встречаются редко. Рак пищевода может распространяться по подслизистому слою далеко за пределы видимого очага опухоли, а также прорастать в прилежащие к пищеводу ткани и органы. Для суждения о степени распространенности процесса и радикальности оперативного вмешательства при исследовании удаленного отрезка пищевода необходимо изучение линий операционных разрезов и глубины прорастания стенки пищевода.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Симптомы опухоли пищевода и ее лечение
а) Доброкачественные опухоли пищевода. Доброкачественные опухоли пищевода встречаются редко. Они могут расти в толще стенки, в просвет пищевода или периэзофагально. Наиболее часто встречаются лейомиомы, рабдомиомы, фибромы, гемангиомы, липомы, невромы и папилломы. Они часто не проявляются клинически, пока не достигнут значительных размеров. В таких случаях они вызывают дисфагию, стеноз, боль, ощущение распирания за грудиной и кровотечение.
Диагностика. Диагноз ставят на основании результатов контрастной рентгенографии, эзофагоскопии и биопсии.
Лечение. Опухоль удаляют эндоскопически или путем открытого вмешательства шейным, грудным или абдоминальным доступом в зависимости от типа опухоли и ее локализации.
Все техники операций представлены в статьях сайта раздела "Хирургия пищевода".
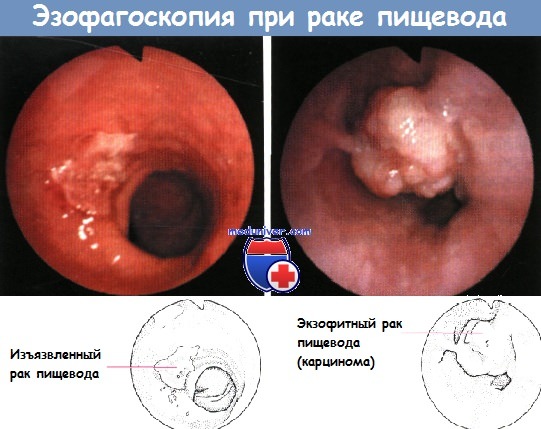
б) Злокачественные опухоли пищевода. Наиболее частой злокачественной опухолью пищевода является плоскоклеточный рак, который у многих больных отличается низкой степени дифференцировки. На долю плоскоклеточного рака приходится 40% всех опухолей ЖКТ.
Эта опухоль наблюдается почти исключительно у мужчин старше 50 лет. Рак пищевода может развиться без какой-либо предшествующей патологии, но он возможен и при таких фоновых заболеваниях, как коррозионный эзофагит, дивертикул пищевода, короткий пищевод типа синдрома Баррета, рефлюкс-эзофагит, грыжа пищеводного отверстия диафрагмы, ахалазия кардии, синдром Пламмера-Винсона (Патерсона-Келли).
В редких случаях рак может перейти с соседних органов, например щитовидной железы, гортани, трахеи, бронхов или желудка. Возможно также прорастание опухоли из пораженных метастазами лимфатических узлов. Более редкими гистологическими формами рака пищевода являются аденокарцинома, обычно поражающая нижний сегмент пищевода, и саркома.
Клиническая картина. Клинические проявления злокачественных опухолей пищевода включают прогрессирующую дисфагию, которая сначала появляется только при приеме твердой пищи, ощущение жжения и полноты за грудиной, боль (поздний симптом), имеющая непостоянный характер и локализующаяся за грудиной или в спине, похудание, икота, рвота, кашель и охриплость голоса вследствие паралича возвратного нерва. В среднем симптомы появляются через 4-5 мес. Позднее отмечаются похудание, невозможность принимать пищу, рвота, выраженная жажда и интенсивная боль.
Диагностика. Диагноз часто оказывается слишком запоздалым. При рентгенографии выявляют расширение тени средостения и латеральное смещение трахеи. При контрастной рентгенографии отмечается дефект наполнения, задержка контрастирования, неправильность контуров стенки пищевода, стеноз пищевода. Иногда первым клиническим проявлением опухоли бывают симптомы поражения возвратного гортанного нерва.
Наиболее часто для установления диагноза выполняют ригидную эзофагоскопию с биопсией.
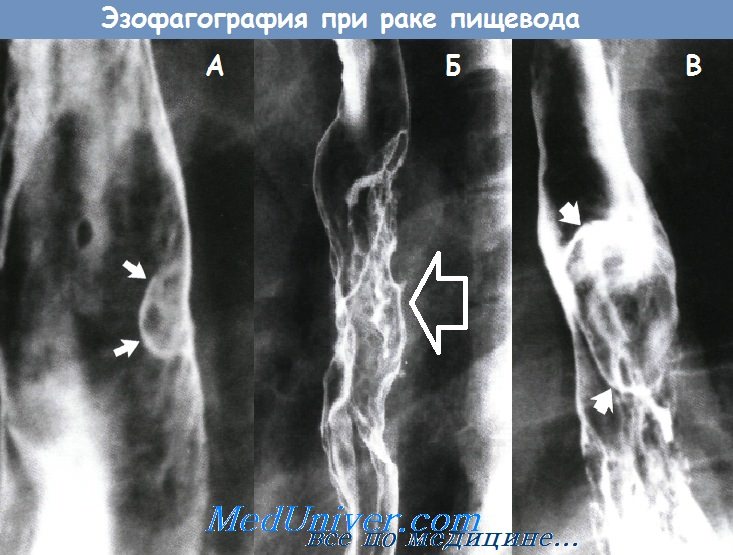
А - рак пищевода в виде полипа на широком основании
Б - инфильтрирующий рак пищевода
В - полипозный рак пищевода
Дифференциальный диагноз. Перечень дифференцируемых заболеваний включает ахалазию кардии, стеноз пищевода, дивертикул пищевода, синдром Пламмера-Винсона, доброкачественные опухоли пищевода, рак бронха, прорастающий в пищевод, и инородное тело пищевода.
Лечение. Хирургическое лечение показано лишь в трети случаев, обычно когда опухоль локализуется в средней и нижней трети пищевода. Альтернативой ему являются химио- и лучевая терапия, которые, однако, малоэффективны.
Дополнительной паллиативной мерой является интубация пищевода трубчатым протезом для временного восстановления проходимости и чрескожная эндоскопическая гастростомия.
Все техники операций представлены в статьях сайта раздела "Хирургия пищевода".

Чрескожная эндоскопическая гастростомия:
а Для трансиллюминации стенки желудка используется освещение гибкого эндоскопа. Для перфорации стенки желудка в освещенном месте используют острую иглу (1).
б Вводят проволочный проводник (2), оттягивают его с помощью эзофагоскопа (3) и выводят через рот.
в Гастростомическую трубку соединяют с проволочным проводником и последний выводят через стенку желудка вместе с трубкой (4).
г Герметизация стенки желудка обеспечивается упорной шайбой и пуговчатым концом трубки.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Мезенхимальные новообразования желудочно-кишечного тракта представлены большой группой опухолей, исходящих из различных типов тканей. Эти опухоли обладают различным злокачественным и метастатическим потенциалом, разнятся подходами к лечению и последующему наблюдению. Гастроинтестинальная шваннома — медленнорастущее доброкачественное образование, которое может быть локализовано в любом отделе ЖКТ. При этом шванномы исходят из межмышечного нервного сплетения и требуют открытого хирургического лечения в объеме резекции. В данном обзоре литературы рассмотрены вопросы диагностики гастроинтестинальных шванном различной локализации и подходы к их лечению.
Enter the password to open this PDF file:
Полный текст статьи:
Шванномы ЖКТ — крайне редкие опухоли нейрогенного происхождения, развивающиеся из шванновских клеток, входящих в состав оболочки периферических нервов. В большинстве случаев шванномы желудочно-кишечного тракта развиваются из межмышечного сплетения (Ауэрбаха) [2]. На долю шванном приходится всего 2–6% всех мезенхимальных опухолей, представляющих собой гетерогенную группу новообразований, которые могут исходить из различных типов тканей [2, 4, 14]. В порядке убывания частоты встречаемости мезенхимальные опухоли ЖКТ также представлены гастроинтестинальными стромальными опухолями (ГИСО), лейомиомами, лейомиосаркомами, нейрофибромами, ганглионейромами, параганглиомами, липомами, зернистоклеточными и гломусными опухолями [2].
Точные показатели заболеваемости гастроинтестинальными шванномами не определены [12]. Но известно, что самая частая локализация шванномы в ЖКТ — желудок (83%), за ней следует тонкая кишка (12%) и наконец ободочная и прямая кишки [2].
Окончательная диагностика шванном желудочно-кишечного тракта основана на гистологическом и иммуногистохимическом исследовании резецированных опухолей (рис. 1, 2, 6 — С). Все гастроинтестинальные шванномы — твердые однородные опухоли, как правило, покрытые оболочкой. Микроскопически шванномы представлены веретенообразными клетками, переплетающимися пучками или тяжами с нечеткими границами слабобазофильной цитоплазмы и овальными либо вытянутыми ядрами. Клеточно-волокнистые пучки располагаются беспорядочно или формируют своеобразные ритмичные структуры в виде завихрений, параллельных рядов или палисадных структур. Все гастроинтестинальные шванномы иммунореактивны к белку S100, что позволяет дифференцировать их от других мезенхимальных опухолей ЖКТ. Они характеризуются низкой частотой митозов, отсутствием атипичных митотических фигур и ядерной гиперпигментацией. Степень агрессивности зависит от индекса Ki-67 и митотического индекса. В качестве показателя злокачественности рекомендуется использовать индекс Ki-67. Значение более 5% коррелирует с большей агрессивностью опухоли, а более 10% является показателем злокачественности [2, 7].
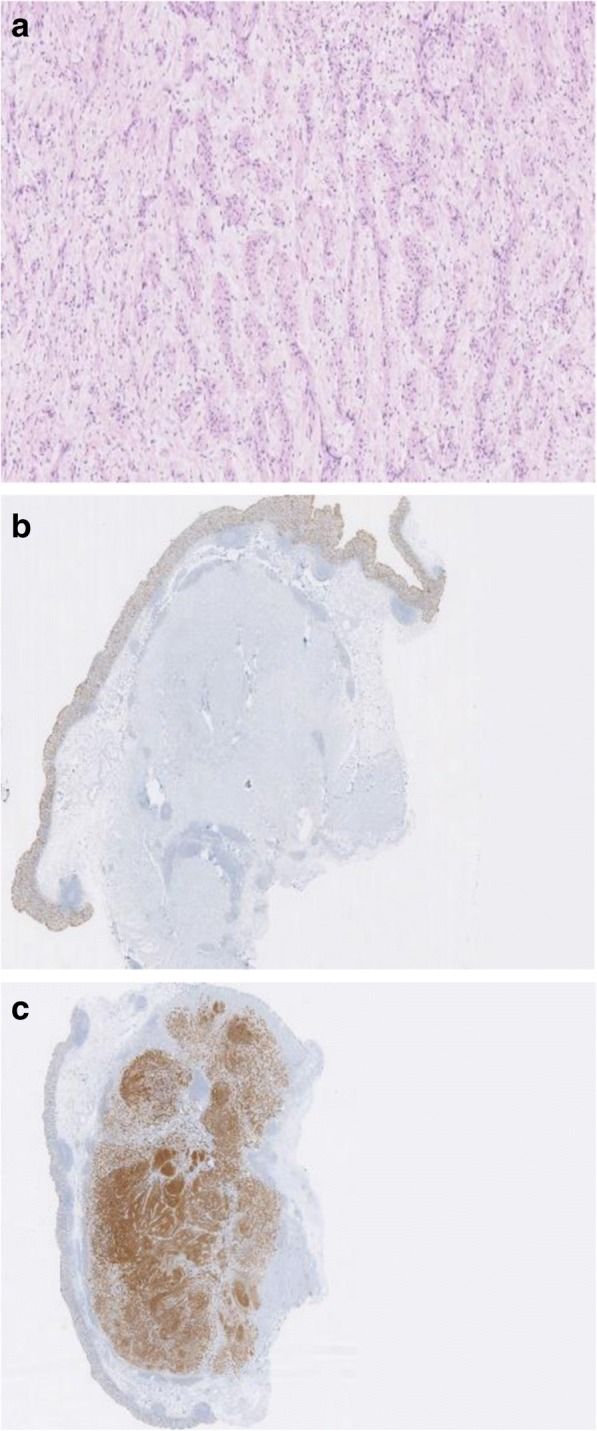
Рисунок 1. Гистологическое и иммуногистохимическое исследование шванномы слепой кишки [2].
A. Гистологическое исследование, окраска гематоксилином и эозином. Опухоль имеет веретеноклеточное строение.
B. Иммуногистохимическое исследование. Опухоль иммунонегативна к CD117.
C. Иммуногистохимическое исследование. Опухоль иммунореактивна к белку S100.
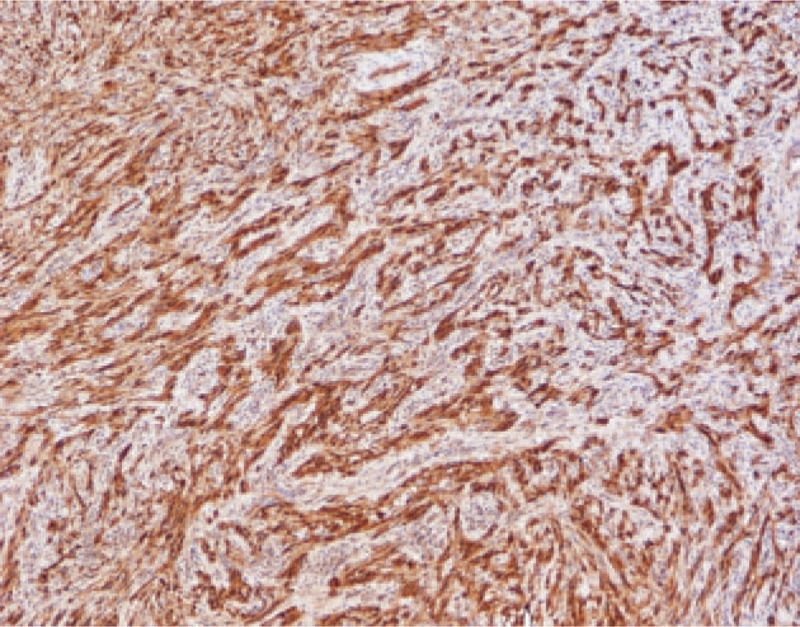
Рисунок 2. Иммуногистохимическое исследование шванномы прямой кишки, сильная иммунореактивность к белку S100 [15].
Шванномы пищевода (рис. 3). Доброкачественные первичные опухоли пищевода редки и составляют примерно 2% всех новообразований данной локализации. Более 80% доброкачественных опухолей пищевода представлено лейомиомами, но в редких случаях могут встречаться и шванномы. Шваннома пищевода чаще развивается у женщин, чем у мужчин, и эти опухоли обычно расположены в верхней и средней трети пищевода. Предоперационная диагностика заболевания сложна, и окончательный диагноз часто устанавливается только после резекции. Лечение шванном пищевода хирургическое. Торакоскопическая энуклеация используется для небольших опухолей диаметром ≤2 см. При опухолях больших размеров, ≥8 см, выполняется резекция пищевода с эзофагогастростомией. Химиотерапия и лучевая терапия неэффективны [5, 8].
Шванномы желудка. Шванномы желудка — редкое заболевание, на их долю приходится лишь 0,2% всех опухолей данной локализации [9, 10]. Voltaggio с соавторами подсчитали, что соотношение ГИСО к шванномам в желудке составляет примерно 45:1 [7]. Хотя эти опухоли очень схожи внешне, подходы к лечению и прогноз у них совершенно разные. Поэтому необходима тщательная дифференциальная диагностика данных заболеваний [9, 14].
Шванномы желудка у женщин встречаются несколько чаще, чем у мужчин, в соотношении 1,4:1. Средний возраст заболевших — 58 лет. Шванномы желудка могут протекать бессимптомно или проявляться слабой диспепсией. В случаях изъязвления возможно развитие кровотечения [10].
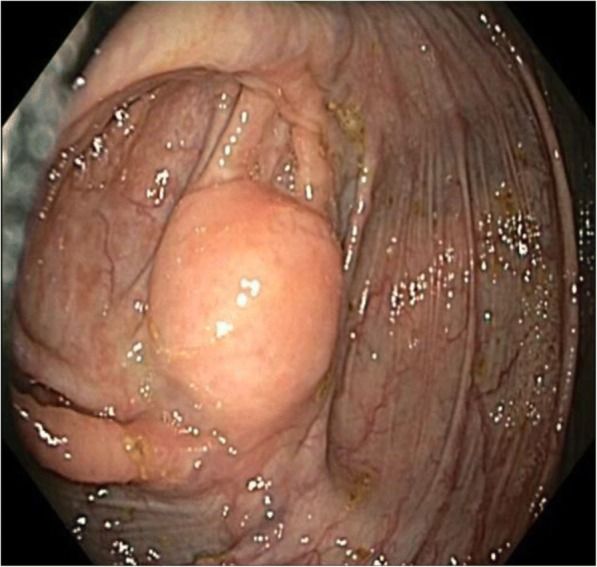
В большинстве случаев шванномы желудка — случайная находка при скрининговой гастроскопии. Эндоскопически это типичные субэпителиальные образования, покрытые визуально неизмененной слизистой (рис. 4, 6 — А) [10]. Компьютерная томография, магнитно-резонансная томография и позитронно-эмиссионная томография предоставляют ограниченную информацию для дифференциации шванномы от других мезенхимальных опухолей в желудке [11]. Эндосонография с тонкоигольной биопсией является ценным диагностическим методом. Эхоскопически шванномы желудка — гетерогенные гипоэхогенные поражения с четкими краями и краевым усилением, которые расположены в собственном мышечном слое. Эхогенность этих поражений ниже, чем у окружающего нормального мышечного слоя (рис. 5, 6 — В). Кистозные изменения и кальцификации встречаются редко. Эти особенности могут быть полезны для дифференциальной диагностики шванномы желудка от других мезенхимальных опухолей, особенно ГИСО [14]. Шваннома может быть диагностирована с помощью эндосонографии с тонкоигольной биопсией (ЭУС-ТИП), если получен достаточно большой образец. Однако ЭУС-ТИП не является идеальным методом для диагностики шванномы. Его чувствительность, по данным Takasumi и соавторов, составляет 66,5% [11].
В некоторых случаях возможно проведение эндоскопической резекции шванномы желудка. Но учитывая тот факт, что данные опухоли чаще исходят из межмышечного нервного сплетения, методом выбора является хирургическая резекция. Рецидивы этих опухолей также встречаются редко и в основном связаны с неполной резекцией [10].
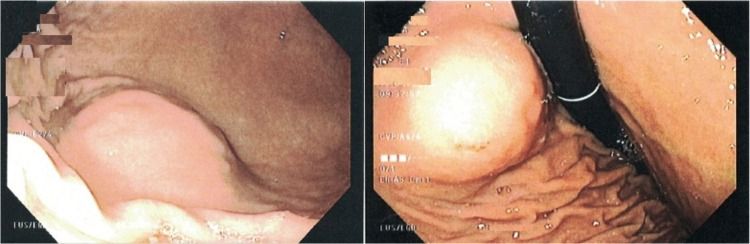
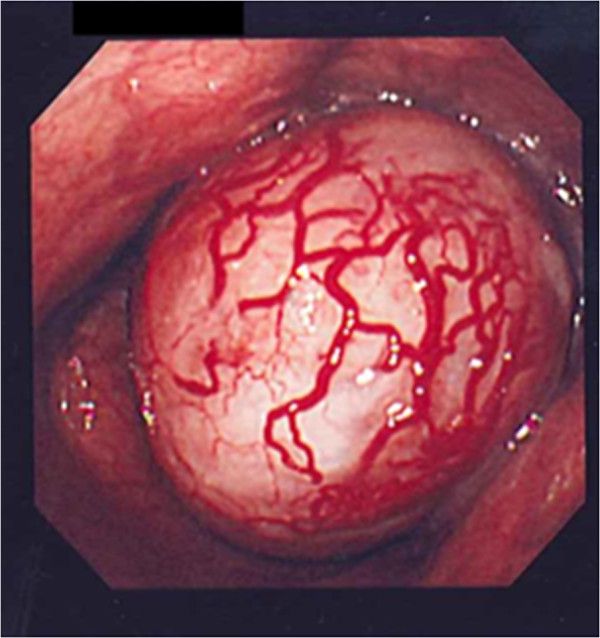
Рисунок 4. Шваннома желудка [10].
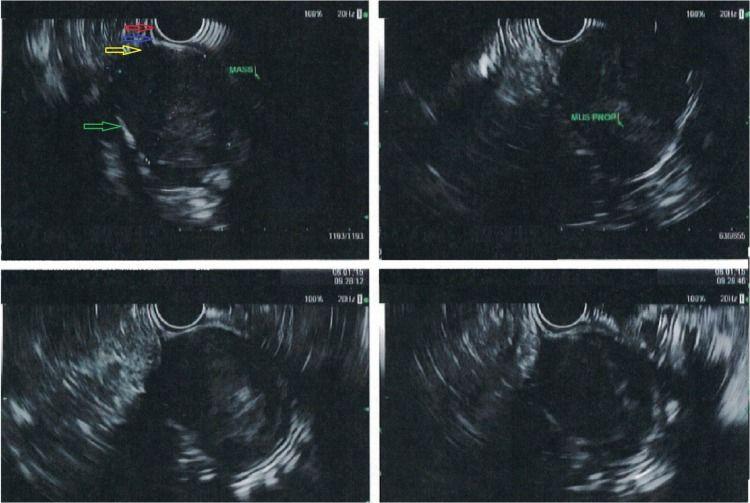
Рисунок 5. Эндосонография шванномы желудка [10]. В теле желудка лоцируется образование 3,5×3 см, исходящее из мышечного слоя (желтая стрелка). Дифференцируются другие эхослои стенки желудка: мышечная пластинка слизистой (красная стрелка), подслизистая (синяя стрелка) и серозная (зеленая стрелка) оболочки.
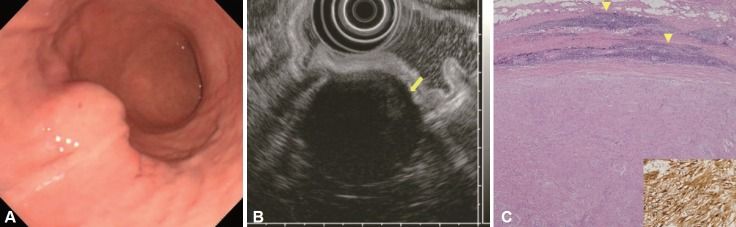
A. На гастроскопии выявлено субэпителиальное образование в средней трети тела желудка.
B. При ЭУС опухоль имеет гетерогенную гипоэхогенную по отношению к окружающему мышечному слою структуру с краевым усилением эхосигнала (указано стрелкой). Размеры образования 30×35 мм.
С. При микроскопическом исследовании (окраска гематоксилином и эозином, увеличение 40x) выявлена ограниченная опухоль, состоящая из веретенообразных клеток разного типа организации с лимфоидной инфильтрацией (указаны стрелками). При иммуногистохимическом исследовании клетки опухоли положительны к S100 (увеличение 400 x).
Шванномы двенадцатиперстной кишки. Шванномы данной локализации в основном расположены во второй или третьей части ДПК. Гендерных различий в заболеваемости шванномами двенадцатиперстной кишки не существует. Выявляются на пятом или шестом десятилетии жизни. Дуоденальные шванномы обычно протекают бессимптомно и выявляются случайно. Наиболее распространенные симптомы — кишечное кровотечение и дискомфорт в животе. Эндоскопически имеют вид типичного субэпителиального образования. Эндосонографические признаки точно не определены из-за редкости данного заболевания [4], однако, по всей видимости, являются общими для всех гастроинтестинальных шванном (рис. 7).
Дуоденальные шванномы обычно доброкачественные, а злокачественная трансформация происходит крайне редко. Гистологические критерии определения степени злокачественности шванномы на светооптическом уровне отсутствуют, а метастатический потенциал пока не известен. Поэтому иногда требуется тщательное наблюдение после операции [4].
Метод лечения — полная хирургическая резекция, объем которой зависит от размера опухоли, ее локализации и гистологических особенностей. Оптимальное лечение злокачественной шванномы полностью еще не определено. Роль химиотерапии и лучевой терапии остается неясной. Неполная резекция может быть связана с местным рецидивом. Таким образом, наиболее важный прогностический фактор — границы резекции [4].

Рисунок 7. Шваннома луковицы двенадцатиперстной кишки [4].
A. Дуоденоскопия: в луковице ДПК визуализируется субэпителиальное образование, покрытое неизмененной слизистой.
B. Эндосонография: опухоль имеет гетерогенную гипоэхогенную структуру с ровными четкими контурами, исходящую из мышечного слоя. Размеры образования 15×7 мм.
Колоректальные шванномы. Распространенность колоректальных шванном несколько больше среди женщин (59%), средний возраст заболевших — 60–65 лет, но могут возникнуть в любом возрасте [7]. Наиболее часто шваннома встречается в слепой (рис. 8) и восходящей ободочной кишках (30,5%), за которыми следуют сигмовидная (28,1%), прямая кишка (21,1%) (рис. 10), нисходящая ободочная кишка (8,3%), поперечная ободочная кишка (5,3%) и аппендикс (1,1%) (рис. 9). Шванномы в большинстве случаев протекают бессимптомно и являются случайными находками при проведении скрининговой колоноскопии. Таким образом, для данной группы пациентов используются стандартные рекомендации по подготовке к колоноскопии. Применение малообъемного препарата полиэтиленгликоля с аскорбатным комплексом (МОВИПРЕП ® ) так же эффективно, как и стандартного полиэтиленгликоля в объеме 4 л при условии, что они используются в одинаковом режиме. Отмечено, что препарат полиэтиленгликоля с аскорбатным комплексом (МОВИПРЕП ® ) лучше переносится, вызывая меньше нежелательных явлений в виде тошноты и рвоты, и особенно удобен для подготовки амбулаторных пациентов. В настоящее время рекомендуется использование двухэтапной подготовки или одноэтапной — в день исследования, так как на качество подготовки влияет время, прошедшее с момента приготовления до осмотра. Оптимальным интервалом является 4 часа, максимальным — 8 часов [3, 6, 13].
Эндоскопически колоректальные шванномы имеют типичный вид подслизистой опухоли с гладкой поверхностью, покрытой визуально неизмененной слизистой, и только в редких случаях (6,8%) имеют изъязвление [2, 7]. Как и при других субэпителиальных опухолях, щипцовая биопсия чаще всего неинформативна [2, 15].
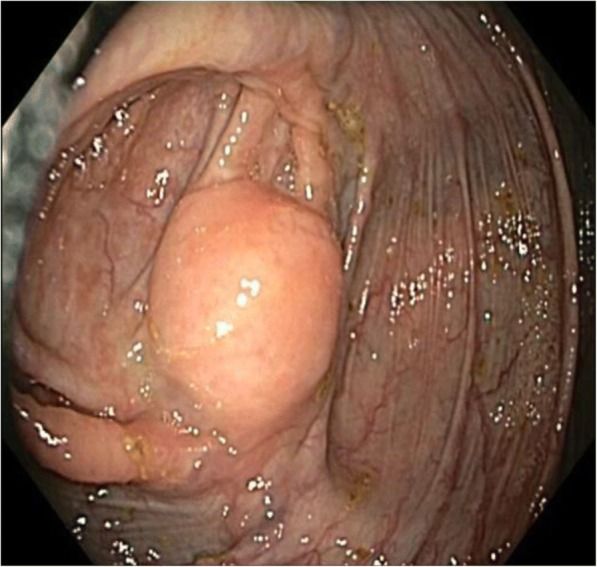
Рисунок 8. Шваннома слепой кишки [2].
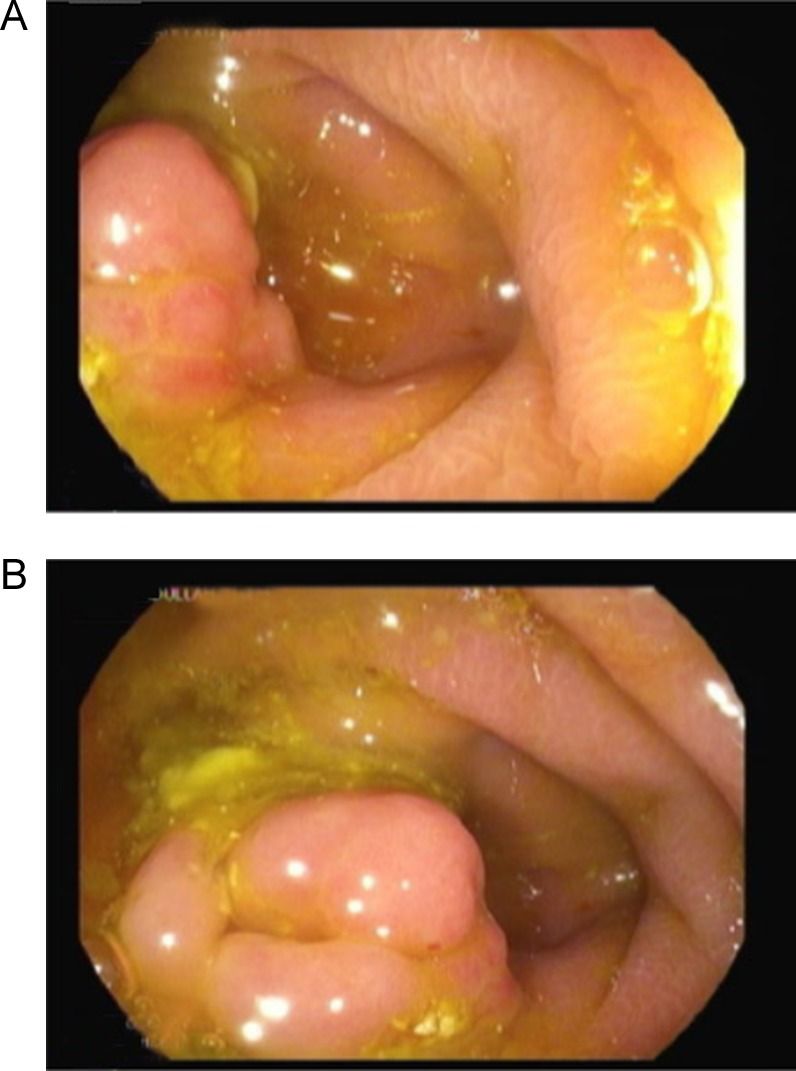
Рисунок 9. Шваннома аппендикса [1].
В устье аппендикса выявлено субэпителиальное образование.
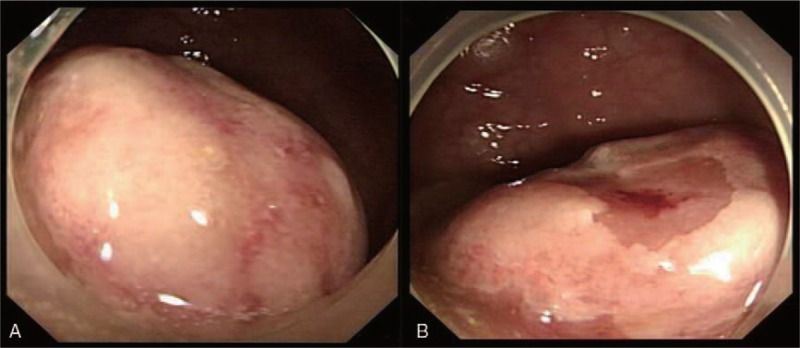
Рисунок 10. Шваннома прямой кишки [15].
Колоректальные шванномы являются доброкачественными в ≥98% случаев. Но так как опухоли исходят из межмышечного нервного сплетения, лучший метод лечения — полная хирургическая резекция [2, 10].
Шванномы желудочно-кишечного тракта — это крайне редкие субэпителиальные образования. В большинстве случаев протекают бессимптомно и являются случайной находкой при проведении эндоскопического исследования. На основании эндоскопической картины или щипцовой биопсии дифференциальная диагностика шванномы от других мезенхимальных опухолей желудочно-кишечного тракта невозможна. Окончательная диагностика гастроинтестинальных шванном основана на иммуногистохимическом исследовании удаленных опухолей. Шванномы данной локализации отличаются медленным ростом и доброкачественным течением. На сегодняшний день метод лечения шванном — хирургическая резекция. Развитие местных рецидивов связано с неполным удалением первичной опухоли.
Список литературы:
1. Alshamrani A.M., Sairafi R.A., Alzahrani A.M., Abdel-Raheem M. Appendicular schwannoma presenting as vague abdominal pain. J Surg Case Rep. 2018. Jul 3; 2018 (7): rjy149. eCollection 2018 Jul. PMID: 29992004. PMCID: PMC6031008. DOI: 10.1093/jscr/rjy149.
4. Kahng D.H., Kim G.H., Park S.G., Lee S.J., Park D.Y. A Rare Duodenal Subepithelial Tumor: Duodenal Schwannoma. Clin Endosc. 2018. May 15. PMID: 29764009. DOI: 10.5946/ce.2018.050.
6. Kojecky V., Dastych M., Zadorova Z., Varga M., Hajer J., Kment M., Kroupa R., Kunovska M., Matous J., Misurec M., Hep A., Kianicka B., Latta J. [Effective bowel preparation before coloscopy — low-volume PEG in the divided dose regimen]. Vnitr Lek. 2016. Apr; 62 (4): 249–254. PMID: 27250601.
8. Mishra B., Madhusudhan K.S., Kilambi R., Das P., Pal S., Srivastava D.N. Malignant Schwannoma of the Esophagus: A Rare Case Report. Korean J Thorac Cardiovasc Surg. 2016. Feb; 49 (1): 63–66. Epub 2016 Feb 5. PMID: 26889451. PMCID: PMC4757402. DOI: 10.5090/kjtcs.2016.49.1.63.
9. Sanei B., Kefayat A., Samadi M., Goli P., Sanei M.H., Khodadustan M. Gastric Schwannoma: A Case Report and Review of the Literature for Gastric Submucosal Masses Distinction. Case Rep Med.2018. Apr 10; 2018: 1230285. eCollection 2018. PMID: 29849652. PMCID: PMC5914132. DOI: 10.1155/2018/1230285.
10. Sunkara T., Then E.O., Reddy M., Gaduputi V. Gastric schwannoma-a rare benign mimic of gastrointestinal stromal tumor. Oxf Med Case Reports. 2018. Mar 12; 2018 (3): omy002. eCollection 2018 Mar. PMID: 29564143. PMCID: PMC5846295. DOI: 10.1093/omcr/omy002.
11. Takasumi M., Hikichi T., Takagi T., Suzuki R., Watanabe K., Nakamura J., Sugimoto M., Kikuchi H., Konno N., Waragai Y., Asama H., Obara K., Ohira H. Efficacy of endoscopic ultrasound-guided fine-needle aspiration for schwannoma: six cases of a retrospective study. Fukushima J Med Sci. 2017. Aug 9; 63 (2): 75–80. Epub 2017 Jul 5. PMID: 28680005. PMCID: PMC5597526. DOI: 10.5387/fms.2015-21.
12. Wang W.B., Chen W.B., Lin J.J., Xu J.H., Wang J.H., Sheng Q.S. Schwannoma of the colon: A case report and review of the literature. Oncol Lett. 2016 Apr; 11 (4): 2580–2582. Epub 2016 Feb 24. PMID: 27073520. PMCID: PMC4812459. DOI: 10.3892/ol.2016.4271.
13. Xie Q., Chen L., Zhao F., Zhou X., Huang P., et al. (2014) A Meta-Analysis of Randomized Controlled Trials of Low-Volume Polyethylene Glycol plus Ascorbic Acid versus Standard-Volume Polyethylene Glycol Solution as Bowel Preparations for Colonoscopy. PLoS One.9 (6): e99092. DOI:10.1371/journal.pone.0099092.
14. Yoon J.M., Kim G.H., Park D.Y., Shin N.R., Ahn S., Park C.H., Lee J.S., Lee K.J., Lee B.E., Song G.A. Endosonographic Features of Gastric Schwannoma: A Single Center Experience. Clin Endosc.2016. Nov; 49 (6): 548–554. Epub 2016 Mar 15. PMID: 26975861. PMCID: PMC5152784. DOI: 10.5946/ce.2015.115.
15. Zhang K., Qu S., Li J., Cheng Y., Shi J., Liu T. A case report of rectal schwannoma treated with laparoscopic proctectomy. Medicine (Baltimore). 2018. Feb; 97 (7):e9866. PMID: 29443751. PMCID: PMC5839841. DOI: 10.1097/MD.0000000000009866.

Что такое доброкачественные новообразования пищевода?
Доброкачественные новообразования пищевода – это опухоли, которые растут в верхней части желудочно-кишечного тракта (ЖКТ). Их главным отличием от рака пищевода является невозможность распространяться в виде метастазов и более благоприятный прогноз для пациента. Однако не стоит думать, что болезнь не несет угрозы здоровью человека. При отсутствии правильного лечения происходит постепенное разрушение пищевода с нарушением нормальной функции пищеварения. Поэтому при появлении любых подозрительных симптомов нужно обращаться за специализированной медицинской помощью.
Виды доброкачественных новообразований пищевода
Доброкачественные опухоли пищевода встречаются в 5-7% случаев всех онкологических заболеваний пищеварительного тракта. Эти патологии одинаково часто поражают мужчин и женщин. Страдают в основном пациенты в возрасте старше 35 лет, отдающие предпочтение острой и горячей пище.
В зависимости от характера роста опухоли пищевода бывают:
- экзофитные – растут внутрь полости органа (полипообразные новообразования);
- эндофитные (интрамуральные) – растут внутрь стенки органа.
В зависимости от гистологической структуры новообразования могут быть очень разными. Наиболее распространенными являются аденомы, папилломы, полипы пищевода. Реже встречаются миксомы, рабдомиомы, лейомиомы, гемангиомы.
Симптомы доброкачественных новообразований пищевода
Доброкачественные опухоли пищевода отличаются медленным темпом роста. Это обуславливает отсутствие клинической симптоматики на ранних стадиях заболевания. Пациент может годами даже не подозревать о наличии новообразования и вести обычный образ жизни.
Признаки заболевания возникают уже при больших размерах опухолей, когда они напрямую начинают мешать пищеварению или сдавливать соседние органы. Наиболее распространенными симптомами патологии являются:
- Затрудненное глотание (дисфагия). Опухоль механически мешает пище пройти по пищеводу. Пациент должен запивать еду водой, ему трудно употреблять мясо, хлеб и твердые продукты.
- Легкая или умеренная боль в груди в проекции пищевода. Дискомфорт вызван сдавливанием нервных окончаний опухолью.
- Отрыжка, тошнота, рвота. Эти признаки являются следствием нарушения пищеварения.
- Похудение, общая слабость. Обусловлены нарушением метаболизма на фоне длительного существования опухоли.
При больших размерах новообразований, когда они сдавливают бронхи, легкие или сердце, может возникать одышка, тахикардия, кашель, аритмии.
Причины доброкачественных новообразований пищевода
Точных причин развития онкологического процесса в пищеводе пока не установлено. Известно, что болезнь возникает из-за неправильного роста и размножения клеток в слизистой или мышечной оболочке органа. В результате хаотического и неконтролируемого разрастания тканей образуются патологические элементы.
Факторами, которые увеличивают риск возникновения доброкачественных опухолей пищевода, являются:
- генетическая предрасположенность;
- химические и физические повреждения пищевода;
- влияние радиации;
- контакт с химическими канцерогенами (лакокрасочные изделия, смолы, фенолы).
Получить консультацию
Если у Вас наблюдаются подобные симптомы, советуем записаться на прием к врачу. Своевременная консультация предупредит негативные последствия для вашего здоровья.
Узнать подробности о заболевании, цены на лечение и записаться на консультацию к специалисту Вы можете по телефону:

Диагностика доброкачественных новообразований пищевода
Пациенты чаще всего обращаются за помощью к гастроэнтерологу, когда возникает нарушение глотания. При оценке жалоб пациента и сборе анамнеза заболевания врач может заподозрить наличие патологического новообразования в пищеводе.
Для подтверждения диагноза гастроэнтеролог может назначить:
- рентгенологическое исследование пищевода с применением бария;
- эзофагогастродуоденоскопию (ЭГДС) с биопсией для дальнейшего гистологического анализа тканей опухоли;
- компьютерную (КТ) или магнитно-резонансную томографию (МРТ).
Все указанные методики позволяют визуализировать полость пищевода и зафиксировать наличие новообразования. При выявлении опухоли пациент направляется к онкологу для выбора дальнейшей тактики лечения.
Мнение эксперта
Как онколог, хочу сказать, что доброкачественные опухоли пищевода несут прямую угрозу для здоровья пациента. Несмотря на свою условную безопасность, они могут переродиться в злокачественные опухоли с уже совсем другими последствиями для пациента. Поэтому нельзя игнорировать симптомы заболевания. Нужно обращаться за специализированной помощью и лечить новообразования. При своевременном начале терапии шанс выздороветь близится к 100%.
Мингболатов Фейзула Шахболатович, врач уролог-андролог, врач-онколог, к.м.н., врач высшей категории, доцент кафедры урологии РУДН

Методы лечения доброкачественных новообразований пищевода
Лечение доброкачественных образований пищевода проводится хирургическим путем.
Эффективных консервативных методов лечения доброкачественных опухолей пищевода не существует. Медикаменты применяются временно и только для уменьшения выраженности симптомов, доставляющих дискомфорт.
Хирургическое лечение
Оптимальным вариантом решения проблемы остается радикальная операция, направленная на полное удаление опухоли. Доступ к патологическому участку может быть осуществлен 2 путями:
- Эндоскопические операции. Через естественные отверстия в полость органа вводится оптическая система и небольшие инструменты, которыми и осуществляется иссечение опухоли. На коже разрез отсутствует.
- Традиционные операции. С помощью скальпеля делается достаточно большой разрез в области шеи, грудной клетки или верхнего этажа брюшной полости (в зависимости от того, в каком отделе пищевода находится опухоль). На коже остается рубец.
С учетом размеров новообразования и степени поражения близлежащих тканей могут использоваться следующие хирургические методы лечения:
- Полипэктомия. Применяется для удаления полипов, которые не прорастают вглубь стенки органа.
- Энуклеация. Операция используется для удаления кистообразных опухолей и предусматривает их вылущивание с капсулой. В ходе процедуры пищевод сохраняется полностью.
- Резекция части пищевода. При глубоком прорастании опухоли используется частичное удаление органа в пределах здоровых тканей.
Выбор метода лечения проводится индивидуально в зависимости от особенностей конкретного клинического случая.

Профилактика доброкачественных новообразований пищевода
Специфической профилактики опухолей пищевода не существует. Рекомендуется вести здоровый образ жизни, избегать контактов с известными канцерогенами и умеренно употреблять острую и горячую пищу.
Реабилитация после операции
После проведения эндоскопической операции пациент полностью восстанавливается в течение 1 месяца. Первые несколько дней рекомендуется употреблять пюреобразную пищу в небольших количествах. Постепенно рацион расширяется. Также в это время стоит ограничить физическое перенапряжение, воздействие стрессовых факторов.
При открытых операциях с удалением части пищевода реабилитация предусматривает пребывание в стационаре еще 5-7 дней после вмешательства. Ежедневно врач проводит перевязки, оценивает состояние пациента. Швы снимаются на 7-10-й день. Рекомендуется строгая диета, которая создает функциональный покой для пищевода. Полное восстановление может затянуться до 4-6 месяцев.
Вопросы и ответы
Какой врач лечит доброкачественные новообразования пищевода?
Лечением доброкачественных новообразований пищевода занимается онколог. Первичную диагностику зачастую проводит гастроэнтеролог.
Можно ли лечить доброкачественные новообразования пищевода консервативно?
Когда нужно заподозрить доброкачественные новообразования пищевода?
Чаще всего проблема впервые проявляет себя нарушением глотания. Если человек без видимой на то причины начинает постоянно запивать еду водой для того, чтобы проглотить, это весомый повод, чтобы записаться на прием к гастроэнтерологу.


Все материалы данного сайта являются объектами авторского права (в том числе дизайн). Запрещается копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного письменного согласия правообладателя. Указание ссылки на источник информации является обязательным.
Лицензия № ЛО-77-01-018779 от 19 сентября 2019 г.
Опухоли пищевода – доброкачественные и злокачественные новообразования, возникающие из различных слоев пищеводной стенки. Клинически проявляются нарушением глотания, рвотой и отрыжкой, болями и тяжестью за грудиной, ощущением комка в горле, кашлем, исхуданием, анемией. В диагностике используются рентгенография пищевода с контрастированием, эзофагоскопия, эндоскопическая биопсия, обзорная рентгенография органов грудной клетки, МРТ и КТ органов грудной клетки. Лечение доброкачественных опухолей пищевода только хирургическое, злокачественных – комплексное (оперативное, лучевая и полихимиотерапия).
Общие сведения
Классификация опухолей пищевода
Все опухоли пищевода разделяют на две большие группы: доброкачественные (менее 1%) и злокачественные (более 99%). Доброкачественные опухоли классифицируют по гистологическому строению и характеру роста. Гистологически выделяют следующие виды доброкачественных опухолей пищевода: эпителиальные (полипы, аденомы, папилломы), неэпителиальные (липомы, фибромы, ангиомы, миомы, нейрофибромы, хондромы, миксомы и др.). Неэпителиальные опухоли встречаются гораздо чаще. По характеру роста опухоль пищевода может быть внутрипросветной и интрамуральной (внутристеночной).
Злокачественные опухоли пищевода классифицируют по гистологическому строению, расположению, распространенности процесса и т. д. В морфологическом плане выделяют эпителиальные злокачественные новообразования - плоскоклеточный ороговевающий и неороговевающий рак (более 95%), базальноклеточный, переходноклеточный, мукоэпидермоидный и анапластический рак, аденокарцинома (менее 5%); неэпителиальные – саркома, лимфома, меланома.
Классификация TNM систематизирует рак пищевода по следующим критериям:
1. Анатомическая область – шейный отдел пищевода, внутригрудной отдел (верхний, средний, нижний). Если опухоль поражает одновременно пищевод и желудок, то ее локализация определяется исходя из преимущественного поражения органа (более 50% образования находится в пищеводе или желудке). В случаях, когда новообразование равномерно распространяется в обе стороны, опухолью пищевода считают плоскоклеточный и мелкоклеточный рак, недифференцированные опухоли; опухолью желудка – аденокарциному и перстневидноклеточный рак.
2. Вовлечение в патологический процесс регионарных и отдаленных лимфоколлекторов.
3. Первичная опухоль – какие слои пищевода поражены, есть ли инвазия опухоли в соседние органы и ткани.
4. Степень дифференцировки – высокая, средняя, низкая, недифференцированная опухоль пищевода.
Доброкачественные опухоли пищевода
Симптомы доброкачественных опухолей пищевода
Доброкачественные опухоли пищевода встречаются достаточно редко и насчитывают не более 1% всех новообразований этого органа пищеварения. Львиная доля доброкачественных новообразований - это неэпителиальные опухоли, 70% из которых занимает лейомиома пищевода. Интрапросветные опухоли обычно представлены полипами эпителиального (железистые полипы, папилломы, аденомы) либо мезенхимального (фибромы, липомы, смешанные полипы) происхождения. В отдельную группу выделяют такие редко встречающиеся опухоли, как миксома, хондрома, гамартома, гемангиома.
Доброкачественные новообразования обнаруживаются во всех отделах пищевода. Обычно это одиночные опухоли на широкой ножке, имеющие гладкую или бугристую структуру. Учитывая достаточно медленный рост таких новообразований, клиническое течение часто бывает бессимптомным, а по достижению опухолью больших размеров появляются признаки непроходимости пищевода и сдавления органов средостения. Однако чаще всего доброкачественные опухоли пищевода являются случайной находкой во время обзорной рентгенографии органов брюшной полости.
Различные виды доброкачественных опухолей имеют определенные особенности клинической и рентгенологической картины. Так, полип пищевода может быть одиночным либо множественным, располагаться в любом отделе органа. Он явно выступает в просвет пищевода, имеет выраженную подвижность за счет широкого основания и ножки. Проявляется дисфагией, периодически возникающей в течение многих лет. Характерным признаком при рентгенологическом исследовании является смещаемый дефект наполнения барием с четкими и ровными контурами, сохраненная рельефность и перистальтика на уровне дефекта.
Папиллома обычно имеет большие размеры, чем полип, дольчатую или бородавчатую поверхность. Склонна к малигнизации. Лейомиомы являются наиболее распространенными опухолями пищевода. Располагаются в нижних и средних его отделах, интрамурально на широком основании. Течение обычно бессимптомное, первыми признаками являются изъязвление опухоли и кровотечение. Липомы встречаются очень редко, не имеют четких клинических отличий от других опухолей.
Диагностика и лечение доброкачественных опухолей пищевода
При проведении рентгенографии пищевода с контрастированием выявляются дефекты наполнения, деформация просвета пищеводной трубки, изменения рельефа слизистой. По рентгенологической картине можно выделить опухоли, полностью находящиеся в просвете органа; растущие как в просвет, так и интрамурально; распространяющиеся из внутренних слоев пищевода кнаружи и сдавливающие его извне. Отличием доброкачественных неэпителиальных опухолей от рака является сохраненный рельеф слизистой и эластичность стенок пищевода на уровне расположения новообразования. Диагноз подтверждается гистологически.
Дифференциальная диагностика проводится с такими заболеваниями, как инородное тело, варикозное расширение вен, злокачественные новообразования пищевода. Для установления правильного диагноза в условиях стационара проводится эзофагоскопия и хромоскопия пищевода, эндоскопическая биопсия тканей опухоли с последующим гистологическим исследованием, обзорная рентгенография грудной полости и рентгенография пищевода с контрастированием. При трудностях диагностики показано проведение магнитно-резонансной или компьютерной томографии органов грудной клетки.
Следует обращать внимание на такие неблагоприятные прогностические признаки, как быстрый рост опухоли, изъязвление, нетипичная форма опухолевого узла, изменение рельефа слизистой и эластичности стенок пищевода в месте локализации новообразования. Данные симптомы могут говорить о малигнизации доброкачественной опухоли и требуют от гастроэнтеролога обязательного назначения эзофагоскопии с биопсией.
Лечение только хирургическое, удаление доброкачественных опухолей пищевода может проводиться эндоскопическим либо полостным способом. В послеоперационном периоде назначается специальная диета, ингибиторы протонного насоса длительным курсом (в случае, если опухоль сопровождалась явлениями эзофагита, недостаточности кардии).
Злокачественные опухоли пищевода
Симптомы злокачественных опухолей пищевода
Злокачественные опухоли пищевода в подавляющем своем большинстве представлены раком. Это новообразование коварно тем, что выявляется обычно уже на поздних стадиях, в связи с чем доля операбельных опухолей составляет не более 30%, а летальность превышает 15%. Достаточно часто встречаются множественные злокачественные опухоли пищевода. По гистологической структуре чаще выявляется плоскоклеточный неороговевающий рак, реже базальноклеточный и ороговевающий, крайне редко – аденокарцинома и другие злокачественные новообразования. Чаще всего злокачественные новообразования локализуются в средней части пищевода, а расположение опухоли в дистальных отделах обычно связано с ее распространением из желудка. Растущая опухоль может поражать трахею, крупные артерии и вены, корень легкого, лимфатический проток, печень и диафрагму. Метастазы при раке пищевода выявляются в 60% случаев.
Злокачественные опухоли пищевода имеют характерную клинику: медленно прогрессирующая дисфагия, боль при глотании, отрыжка, слюнотечение. Часто отмечается отвращение к мясу. На поздних стадиях развиваются симптомы опухолевой интоксикации, гнойный медиастинит. Бессимптомное течение злокачественных новообразований возможно только на начальных этапах развития опухоли.
Саркома пищевода может происходить из соединительной, мышечной, сосудистой, нервной, пигментной тканей; также встречаются смешанные и дисэмбриопластические опухоли. Чаще всего диагностируются лейомиосаркомы. По характеру роста выделяют инфильтрирующие опухоли и полиповидные. Рентгенологические признаки сарком неспецифичны, напоминают доброкачественные опухоли. Отличительной чертой может служить множественность опухолевых узлов.
Злокачественные лимфомы пищевода обычно развиваются при генерализованных онкологических заболеваниях лимфатической ткани. Выделяют опухолевую, инфильтративную и комбинированную формы лимфом. Рентгенологически данные новообразования весьма схожи с эзофагеальным раком, отличает их менее выраженный стеноз пищевода, высокая частота изъязвлений с разрывом пищевода, формированием свищей. Также для лимфом характерно сохранение перистальтики пищеводной стенки над опухолью.
Диагностика и лечение злокачественных опухолей пищевода
Диагностирование злокачественных опухолей пищевода обычно включает в себя эзофагоскопию с биопсией, контрастную рентгенографию пищевода, МРТ и компьютерную томографию. Признаки, которые говорят в пользу злокачественного новообразования: нетипичное изменение рельефности слизистой; неравномерность контуров пищеводной стенки или дефект наполнения, сопровождающийся отсутствием перистальтики на этом уровне; неравномерность просвета пищевода, стеноз пищевода с расширением просвета над опухолевым узлом, подрытые контуры стенки пищевода на границе здоровой ткани и опухоли. Компьютерная томография позволяет с большой вероятностью определить возможности оперативного лечения, составить прогноз для выздоровления и жизни пациента.
Лечение злокачественных опухолей пищевода является весьма сложной задачей. Учитывая тип опухоли, стадию и распространенность процесса, может использоваться оперативное лечение (резекция, экстирпация пищевода с последующей эзофагопластикой), лучевая и полихимиотерапия в различных комбинациях. На поздних этапах заболевания терапия паллиативная (гастростомия).
Прогноз опухолей пищевода
При доброкачественных опухолях пищевода прогноз благоприятный, однако пациенты требуют пожизненного диспансерного наблюдения из-за высокой частоты рецидивов. При злокачественных новообразованиях прогноз зависит от сроков выявления и начала лечения опухоли. При наличии метастазов прогноз для выздоровления и жизни неблагоприятный. Специфической профилактики опухолей пищевода не существует.
Читайте также:

