Пневмоцистная пневмония у вич инфицированных лечение бисептолом
Обновлено: 22.04.2024
Форма выпуска, упаковка и состав препарата Бисептол 480
Концентрат для приготовления раствора для инфузий в виде прозрачной, бесцветной или светло-желтой жидкости с запахом спирта.
| 1 мл | 1 амп. | |
| сульфаметоксазол | 80 мг | 400 мг |
| триметоприм | 16 мг | 80 мг |
Вспомогательные вещества: пропиленгликоль, натрия гидроксид, этанол, бензиловый спирт, натрия метабисульфит, вода д/и.
5 мл - ампулы (10) - пачки.
5 мл - ампулы (5) - упаковки контурные пластиковые (2) - пачки картонные.
Фармакологическое действие
Комбинированный антибактериальный препарата, содержащий сульфаметоксазол, обладающий средней длительностью действия, тормозящий синтез фолневой кислоты путем конкурентного антагонизма с парааминобензойной кислотой, а также триметолрим-ингибитор бактериальной редуктазы дигидрофолиевой кислоты. Сочетание обоих препаратов дает еннергический эффект антибактериального действия в связи с чем бактериальная устойчивость проявляется реже, по сравнению с другими препаратами.
Бисептол обладает широким спектром антибактериального действия. Он активен в отношении : Streptococcus (Streptococcus pneumoniae), Neisseria meningitidis, Neisseria gonorrhoeae (включая энтеротоксогенные штаммы), Staphylococcus, Escherichia coli, Klebsiella, Enterobacter, Proteus mirabilis, Proteus spр., Haemophilus influenzae, Salmonella spp. (включая Salmonella typhi и Salmonella paratyphi), Vibrio cholerae, Bacillus anthracis, Listeria spp., Nocardia asteroides, Bordclella pertussis, Enterococcus faecalis, Pasteurella spp., Brucella spp., Mycobacterium spp. (в т.ч. Mycobacterium leprae), Citrobacter, Enterobacter spp., Legionella pneumonia, Providencia, некоторые виды Pseudomonas (кроме P.aerugenosa), Serratia marcescens, Yersinia spp., Morganella spp., Chlamydia spp. (в т.ч. Chlamydia trachomatis, Chlamydia psittaci), Shigella, Plasmodium spp., Toxoplasma gondii, Pneumocystis carini, Actinomyces israelii, Coccidioides immitis, Histoplasma capsulatum, Leishmania spp.
Устойчивы к препарату: Corynebacterium spp., Pseudomonas aerugenosa, Mycobacterium tuberculosis, Troponema spp., Leptospira spp., вирусы.
Угнетает жизнедеятельность кишечной палочки, приводит к уменьшению синтеза тиамина, рибофлавина, никотиновой кислоты и дрругих витаминов группы В в кишечнике. Продолжительность терапевтического эффекта составляет 7 ч.
Фармакокинетика
Препарат быстро проникает в ткани и биологические жидкости организма.
Хорошо распределяется. Проникает через ГЭБ, плацентарный барьер и в грудное молоко. В легких и моче создает концентрации превышающие содержание в плазме. В меньшей степени накапливаются в бронхиальном секрете, влагалищных выделениях, секрете и тканях предстательной железы, жидкости среднего уха, спиномозговой жидкости, желчи, костях, слюне, водянистой влаге глаза, грудном молоке, интерстициальной жидкости. Распределение обоих препаратов разное: сульфаметоксазол распределяется исключительно во внеклеточном пространстве, а триметоприм - как внутри клеток, так и во внеклеточном пространстве. Связывание с белками плазмы - 66% у сульфаметоксазола, у триметоприма - 45%. Оба препарата метаболизируются в печени.
В большей степени метаболизируется сульфаметоксазол (с образованием ацетилированных производных), метаболиты не обладают противомикробной активностью.
Выводятся почками, как путем фильтрации, так и путем активной секреции канальцами, в виде метаболитов (80% в течение 72 ч) и в неизмененном виде (20% сульфаметоксазола, 50% триметоприма ), концентрация действующих веществ в моче значительно выше, чем в крови. Незначительное количество препарата выводится через кишечник. T 1/2 сульфаметоксазола - 9-11 ч, триметоприма - 10-12ч, у детей - существенно меньше и зависит от возраста: до первого года - 7-8ч, 1-10 лет - 5-6 ч. У пожилых и пациентов с нарушением функции почек T 1/2 увеличивается.
Показания препарата Бисептол 480
- острые и хронические инфекции мочеполовых органов: уретрит, пиелонефрит, цистит, пиелит, простатит, эпидидимит, гонорея, мягкий шанкр, венерическая лимфогранулема, паховая гранулема;
- инфекции дыхательный путей: бронхит (острый и хронический) бронхоэктатическая болезнь, крупозная пневмония, бронхопневмония, пневмоцистная пневмония, эмпиема плевры, абсцесс легкого;
- инфекции ЛОР-органов: средний отит, синусит, ларингит, ангина, скарлатина;
- инфекции ЖКТ: брюшной тиф, паратиф, сальмонеллоносительство, холера, дизентерия, холецистит, холангит, гастроэнтериты, вызванные энтеротоксичными штаммами E.coli;
- инфекции кожи и мягких тканей: акне, фурункулез, пиодермия, абсцесс и раневые инфекции, инфекции после хирургических вмешательств;
- сепсис, острый бруцеллез, токсоплазмоз, остеомиелит, остеоартикулярные инфекции, южноамериканский бластомикоз, малярия (Plasmodium falciparum), коклюш (в составе комплексной терапии).
| Код МКБ-10 | Показание |
| A00 | Холера |
| A01 | Тиф и паратиф |
| A02 | Другие сальмонеллезные инфекции |
| A03 | Шигеллез |
| A04.0 | Энтеропатогенная инфекция, вызванная Escherichia coli |
| A23 | Бруцеллез |
| A37 | Коклюш |
| A38 | Скарлатина |
| A40 | Стрептококковый сепсис |
| A41 | Другой сепсис |
| A54 | Гонококковая инфекция |
| A55 | Хламидийная лимфогранулема (венерическая) |
| A57 | Шанкроид |
| B40 | Бластомикоз |
| B50 | Малярия, вызванная Plasmodium falciparum |
| B59 | Пневмоцистоз (B17.3*) |
| H66 | Гнойный и неуточненный средний отит |
| J01 | Острый синусит |
| J03 | Острый тонзиллит |
| J04 | Острый ларингит и трахеит |
| J15 | Бактериальная пневмония, не классифицированная в других рубриках |
| J20 | Острый бронхит |
| J32 | Хронический синусит |
| J35.0 | Хронический тонзиллит |
| J37 | Хронический ларингит и ларинготрахеит |
| J47 | Бронхоэктатическая болезнь |
| J85 | Абсцесс легкого и средостения |
| J86 | Пиоторакс (эмпиема плевры) |
| J90 | Плевральный выпот |
| K29 | Гастрит и дуоденит |
| K81.0 | Острый холецистит |
| K81.1 | Хронический холецистит |
| K83.0 | Холангит |
| L01 | Импетиго |
| L02 | Абсцесс кожи, фурункул и карбункул |
| L03 | Флегмона |
| L08.0 | Пиодермия |
| M00 | Пиогенный артрит |
| M86 | Остеомиелит |
| N10 | Острый тубулоинстерстициальный нефрит (острый пиелонефрит) |
| N11 | Хронический тубулоинтерстициальный нефрит (хронический пиелонефрит) |
| N30 | Цистит |
| N34 | Уретрит и уретральный синдром |
| N41 | Воспалительные болезни предстательной железы |
| N45 | Орхит и эпидидимит |
| T79.3 | Посттравматическая раневая инфекция, не классифицированная в других рубриках |
Режим дозирования
Препарат следует вводить в/в капельно, после разбавления (например, 5% раствором декстрозы, 0.9% раствором натрия хлорида, раствором Рингера или 0.45% раствором натрия хлорида с 2.5% раствором декстрозы). Раствор для инфузии необходимо приготовить сразу же перед введением, тщательно перемешав. После разведения, полученный раствор следует применять в течение 6 ч.
Не следует применять препарат в виде быстрой в/в инъекции.
Взрослым и детям старше 12 лет назначают по 960 мг (2 ампулы по 5 мл, разведенные в 250 мл раствора) через каждые 12 ч. В особо тяжелых случаях следует назначать по 1440 мг (3 ампулы) 2-3 раза/сут.
Детям в возрасте до 12 лет суточную дозу назначают из расчета 36 мг/кг массы тела в двух равных дозах.
Больным с почечной недостаточностью (при клиренсе креатинита 15-30 мл/мин) назначают 50% средней терапевтической дозы.
Побочное действие
Бисептол обычно хорошо переносится больными. Однако могут отмечаться в следующие эффекты:
Со стороны ЖКТ: анорексия, гастрит, абдоминальные боли, глоссит, стоматит, холестаз, повышение активности печеночных трансаминаз, гепатит, псевдомембранозный энтероколит, тошнота, рвота, диарея, некроз печени.
Со стороны ЦНС: головные боли и головокружения. В отдельный случаях - асептический менингит, депрессия, апатия, тремор, периферические невриты.
Со стороны дыхательной системы: бронхоспазм, легочные инфильтраты.
Со стороны органов кроветворения: редко - нейтропения, агранулоцитоз, мегалобластная анемия, лейкопения, тромбоцитопения, гипопротромбинемия.
Со стороны мочевыделительной системы: полиурия, интерстициальный нефрит, нарушение функции почек, кристаллурия, гематурия, повышение содержания мочевины, гипокреатининемия, токсическая нефропатия с олигурией и анурией.
Со стороны костно-мышечной системы: артралгия, миалгия.
Аллергические реакции: кожные высыпания и зуд, фотосенсибилизация, сыпь, полиморфная эритема, эксфолиативный дерматит, аллергический миокардит, повышение температуры тела, отек Квинке, покраснение склер.
Местные реакции: тромбофлебит (в месте венопункции), болезненность в месте введения.
Противопоказания к применению
- мегалобластная анемия на фоне дефицита фолиевой кислоты, апластическая анемия, В 12 -дефицитная анемия, агранулоцитоз, лейкопения;
- дефицит глюкозо-6-фосфатдегидрогеназы;
- гипербилирубинемия у детей;
- печеночная и/или почечная недостаточности клиренс креатинина менее 15 мл/мин);
- возраст до 6 лет (только для в/м введения);
- беременность;
- период лактации;
- повышенная индивидуальная чувствительность к сульфаниламидам или триметоприму.
Не следует применять препарат у недоношенных, новорожденных и грудных детей до 2 месяца жизни.
С осторожностью применяется при дефиците фолиевой кислоты, бронхиальной астме, заболеваниях щитовидной железы, нарушение функции печени и почек.
Применение при беременности и кормлении грудью
Не следует назначать препарат во время беременности и в период грудного вскармливания.
В статье представлены основные данные по эпидемиологии, распространению и патогенезу пневмоцистоза, а также рассматриваются его клинические проявления, методы современной диагностики и подходы к лечению и профилактике этого заболевания при ВИЧ-инфекции. Приводятся схемы лечения и профилактики пневмоцистной пневмонии основными (Бисептол, пентамидин) и резервными препаратами, а также необходимые компоненты патогенетической терапии.
Пневмоцистоз привлек в последние годы внимание многих исследователей в связи с пандемией ВИЧ-инфекции, хотя его изучением занимались и раньше – сначала как проблемой детской патологии, а затем и как проблемой внутрибольничных инфекций. Среди оппортунистических инфекций при СПИДе он занимает одно из лидирующих мест.
Со времени открытия возбудителя пневмоцистной пневмонии (ПП) в 1909 г. и вплоть до 1981 г. во всем мире было описано лишь несколько десятков случаев заболевания, в основном, у младенцев с недостаточностью питания и взрослых больных с гематологическими и онкологическими заболеваниями, получавших иммунодепрессанты [1]. Частота случаев ПП резко увеличилась, начиная с 1981 г. Это заболевание стало основным клиническим проявлением СПИДа, на основании которого были распознаны его первые случаи в США: ПП выявлялась при первом осмотре у 64% больных, а на более поздних стадиях регистрировалась еще у 20% пациентов.
Возбудителем заболевания является Рneumocystis carinii – микроорганизм, который большинство исследователей относят к простейшим (подтип Sporozoa, класс Haplospora). Это – внеклеточный паразит с преимущественным тропизмом к легочной ткани, поражающий пневмоциты 1 и 2 порядков.
До сих пор ведутся споры о таксономическом положении пневмоцист. Ряд специалистов относит их к грибам, так как имеются данные о сходстве между нуклеотидными последовательностями рибосомальной РНК P. carinii и аналогичными структурами у Saccharomyces cervisae и Neurospora crassae [2].
Пневмоцисты широко распространены во всех регионах мира и практически у всех животных – диких, синантропных и сельскохозяйственных. В многочисленных исследованиях показано широкое носительство пневмоцист среди людей в различных географических зонах как в общей популяции, так и у отдельных контингентов населения [1,3-7]. Нами было выявлено широкое носительство Р. carinii в отделении ВИЧ-инфекции у госпитализированных больных (92,9%) и у персонала (80%) [5].
Манифестные формы заболевания развиваются у ослабленных младенцев (преимущественно первых 4-6 месяцев жизни), а в старших возрастных группах они встречаются только при выраженном иммунодефиците, причем имеется четкая связь с характером последнего. Так, средняя частота ПП при ВИЧ-инфекции составляет в настоящее время более 50%, а при других иммунодефицитных состояниях – не превышает 1%.
Патогенез ПП связан с механическим повреждением стенок интерстиция легких. Весь жизненный цикл пневмоцист проходит в альвеоле, к стенке которой они очень плотно прикрепляются. Для развития пневмоцистам необходимо повышенное содержание кислорода. Постепенно размножаясь, они заполняют все альвеолярное пространство, захватывая все большие участки легочной ткани. При тесном контакте трофозоитов со стенками альвеол повреждаются фосфолипиды, постепенно нарушается растяжение легких, увеличивается толщина альвеолярных стенок (в 5-20 раз). Вследствие этого развивается альвеолярно-капиллярный блок, ведущий к тяжелой гипоксии. Отягощающим моментом является образование участков ателектаза, что усугубляет нарушение вентиляции и газообмена. Тяжелому течению болезни способствуют сопутствующие заболевания легких при ВИЧ-инфекции, чаще всего, цитомегаловирусная пневмония.
Наиболее характерными симптомами ПП у больных СПИДом являются: одышка (90-100%), лихорадка (60%), кашель (50%), в то время как у неинфицированных ВИЧ больных эти показатели несколько иные (например, кашель регистрируется гораздо чаще, в 80–95% случаев).
Одышка – наиболее ранний симптом ПП, наблюдающийся практически у всех больных. Вначале она бывает выражена при умеренной физической нагрузке, что особенно заметно при подъеме по лестнице. Если в этот период провести функциональные пробы (велоэргометрия), то после 5-минутной нагрузки дыхание становится более частым и поверхностным (а у здоровых людей – более глубоким), что свидетельствует о неэффективности внешнего дыхания. Этот период может быть растянут во времени и иногда достигает нескольких недель и даже месяцев. Мы наблюдали больного, у которого время от начала одышки при физической нагрузке до развернутой клинической картины с одышкой в покое до 50 в минуту, лихорадкой и кашлем составило 4 месяца. Постепенно одышка нарастает и начинает беспокоить больных уже в покое. Повышение температуры тела может сопровождаться ознобом, повышенной потливостью. В начале заболевания обычно наблюдается субфебрильная температура; в последующем она либо повышается (до 38–39°С), либо остается субфебрильной. Более высокие цифры регистрируются, как правило, у детей раннего возраста. Температурная кривая отличается постепенным нарастанием, постоянным, ремитирующим или неправильным характером. Кашель сухой, обычно, без отделяемого, хотя появление мокроты возможно у больных с сопутствующим бронхитом другой этиологии или у курильщиков. В начале болезни характерно навязчивое покашливание из-за постоянного ощущения раздражения за грудиной или в гортани. В дальнейшем кашель почти постоянный и приобретает коклюшеподобный характер, особенно он беспокоит в ночное время. Свойственных коклюшу приступов и реприз не бывает.
У взрослых ПП, как правило, проявляется более тяжело, отмечается затяжное и рецидивирующее (до 3-6 и более манифестаций) течение с высокой летальностью.
При клиническом обследовании в легких очень часто не удается выявить каких-либо характерных изменений. Перкуторно может определяться короткий оттенок легочного звука, аускультативно – жесткое дыхание, усиленное в передневерхних отделах, иногда рассеянные сухие хрипы. При исследовании других органов обычно наблюдается увеличение размеров печени, нередко отмечается и увеличение селезенки. В связи с возможной диссеминацией пневмоцист по органам (которая происходит все чаще) и вероятностью развития внелегочного пневмоцистоза обследование больного должно быть очень тщательным. Пневмоцисты могут поражать практически любой орган, за исключением суставных сумок и предстательной железы. Описаны поражения лимфатических узлов, селезенки, печени, костного мозга, слизистой оболочки желудочно-кишечного тракта, глаз, щитовидной железы, сердца, головного и спинного мозга, тимуса, брюшины и т.д.
При исследовании периферической крови специфических изменений при ПП не наблюдается. Часто регистрируются изменения, характерные для поздних стадий ВИЧ-инфекции: анемия, лейкоцитопения, тромбоцитопения и др. СОЭ всегда повышена и может достигать 40-60 мм/ч. Самым характерным биохимическим неспецифическим показателем является значительное повышение суммарной активности лактатдегидрогеназы (ЛДГ) как отражение дыхательной недостаточности. По наблюдениям зарубежных исследователей, неблагоприятными прогностическими признаками при ПП являются высокая активность ЛДГ (более 500 МЕ/л); продолжительное течение с развитием рецидивов; дыхательная недостаточность и/или сопутствующая цитомегаловирусная пневмония, а также низкий уровень гемоглобина (ниже 100 г/л), альбумина и Y-глобулина [8].
У больных ВИЧ-инфекцией развитие пневмоцистоза обычно наблюдается при уменьшении числа СD4-лимфоцитов ниже 0,2x10 9 /л.
Если больной не получает лечения, нарастают одышка (до 70 в минуту и более) и признаки легочно-сердечной недостаточности, могут развиться пневмоторакс и даже пневмомедиастинит, а в дальнейшем – отек легких. Нелеченое заболевание часто приводит к гибели больного.
Серологические методы диагностики ненадежны. Для выделения возбудителя из мокроты используют методы индуцированного ее получения (стимуляция кашлевых толчков 2-3% солевым раствором); в дальнейшем применяют прямую микроскопию окрашенных мазков. Используют также исследование бронхоальвеолярного смыва, что увеличивает возможность получения положительного результата с 60% до 90%. В последнее время для более точной диагностики разработаны и применяются методы ПЦР, иммунофлюоресцентные методы с моно- и поликлональными антителами [7].
Несмотря на то, что в настоящее время разработана эффективная терапия, летальность от ПП при ВИЧ-инфекции у больных, получающих лечение, превышает 10%, а при его отсутствии колеблется в пределах от 25% до 80%.
Лечение ПП обязательно должно сочетаться с терапией ВИЧ-инфекции (назначение комбинированной противоретровирусной терапии, если больной не получал ее ранее), а также с патогенетической и симптоматической терапией.
Бисептол, содержащий 480 мг действующих ингредиентов (80 мг триметоприма и 400 мг сульфометоксазола), назначают из расчета 20 мг/кг триметоприма в сутки. Эта доза делится на 4 части для приема каждые 6 часов. Обычно применяется таблетированная форма, но при тяжелом течении заболевания и при нарушении всасывания в желудочно-кишечном тракте препарат вводят внутривенно капельно. Для этого разовую дозу (1 ампула содержит 20 мг триметоприма) растворяют в 250 мл 5% раствора глюкозы. Курс лечения продолжается 21 день. В первые 3-4 дня приема возможно не только отсутствие эффекта, но и временное ухудшение – усиление одышки, повышение температуры тела. По завершении курса лечения проводится поддерживающая терапия – взрослые принимают Бисептол по 1 таблетке (480 мг) 1 раз в сутки.
В среднем, после перенесенной ПП выживают 75% больных, а в некоторых медицинских центрах этот показатель достигает 90%. При рецидивах выживают около 60% пациентов. Одним из критериев эффективности лечения является частота рецидивов, вероятность которых в первые 6 месяцев после первого эпизода ПП составляет около 35%, а в последующие 6 месяцев достигает 60%.
Побочные реакции, обычно, наблюдаются с 6 по 14 день приема ко-тримоксазола. Они могут проявляться повышением температуры тела, сыпью и зудом, тошнотой, увеличением печени, диареей, лейкоцитопенией, тромбоцитопенией, агранулоцитозом, повышением активности сывороточных трансаминаз, уровня креатинина и др. Кожные высыпания, поражения печени, нейтропения и тромбоцитопения чаще наблюдаются у больных со значительными нарушениями функции печени и почек (особенно, если клиренс креатинина ниже 15 мл/мин), поэтому этим категориям пациентов ко-тримоксазол назначать нельзя. Некоторые реакции могут исчезать на фоне продолжающегося лечения. После 2-недельного приема препарата необходимо провести контрольное исследование периферической крови. В случае обнаружения тяжелых нарушений показано назначение препаратов фолиевой кислоты.
За рубежом при непереносимости или недостаточной эффективности ко-тримоксазола больным назначают пентамидин парентерально (препарат не всасывается в желудочно-кишечном тракте). Его вводят внутривенно медленно в дозе 4 мг/кг/сут, разведенной в 250 мл 5% раствора глюкозы, или в форме аэрозоля (водный раствор в суточной дозе 4 мг/кг). При ингаляции пентамидина токсические реакции регистрируются реже и выражены в меньшей степени, чем при внутривенном введении (к наиболее тяжелым токсическим эффектам относятся гепато- и нефротоксичность, гипогликемия). Однако ингаляционный путь введения пентамидина при развившейся болезни имеет ряд ограничений: возможность бронхоспазма, раздражение слизистой оболочки глотки, неодинаковая вентиляция разных отделов легких и др. Чаще ингаляции пентамидина используют с профилактической целью, хотя этот метод профилактики также имеет ряд недостатков, основным из которых является вероятность развития внелегочного пневмоцистоза и пневмоторакса. Продолжительность внутривенного курса лечения составляет 21 день.
Третьим, наиболее часто применяемым при ПП препаратом, является дапсон (препарат резерва), обычно используемый для терапии лепры. Дапсон (100 мг 1 раз в сутки) рекомендуется сочетать с триметопримом (15-20 мг/кг/сут к 100 мг 1 раз в сутки каждые 8 часов). Продолжительность лечения – 21 день. Данная комбинация хорошо переносится. Ее основной побочный эффект – гемолиз у больных с дефицитом глюкозо-6-фосфатдегидрогеназы. Также возможно развитие метгемоглобинурии.
Другой резервной схемой лечения ПП умеренной степени тяжести является комбинация клиндамицина (1,2 г/день внутривенно или перорально) и примахина (0,03 г/день перорально), которую применяют в течение 21 дня. Эту схему также нельзя назначать больным с дефицитом глюкозо-6-фосфатдегидрогеназы, а на 2-3 неделе лечения необходим контроль уровня метгемоглобина.
При отсутствии угрожающих жизни осложнений, но при наличии дыхательной недостаточности применение кортикостероидов способствует более быстрому уменьшению гипоксии. С этой целью назначают преднизолон по 60 мг в сутки в 2-3 приема в первой половине дня в течение 7 дней с последующей постепенной отменой.
Короткий курс кортикостероидной терапии позволяет избежать диссеминации пневмоцист из легких в другие органы. Применение кортикостероидов нецелесообразно при легком течении заболевания и отсутствии отрицательной динамики. При наличии у больных других оппортунистических заболеваний кортикостероиды следует назначать с осторожностью, так как на фоне их применения возможно прогрессирование этих болезней и даже генерализация процесса (герпетическая инфекция, цитомегаловирусная инфекция).
Искусственную вентиляцию легких назначают по показаниям при наличии условий для ее проведения; 20–30% больных, которым она производится, выздоравливают и продолжают жить еще 6-12 месяцев.
При отсутствии первичного профилактического лечения ПП развивается на поздних стадиях ВИЧ-инфекции у 80% больных, а вероятность рецидива при отсутствии вторичной профилактики составляет 70% (в течение 1 года). У больных, получающих ко-тримоксазол, частота ПП составляет 3,5% в год. Кроме того, ко-тримоксазол действует на другие микроорганизмы, благодаря чему оказывает профилактический эффект в отношении ряда инфекций (токсоплазмоз, пневмококковая пневмония и др.).
В России профилактическое лечение ПП проводится у больных с уровнем CD4-лимфоцитов менее 0,2x10 9 /л (первичная профилактика) и пациентов, ранее перенесших ПП (вторичная профилактика). При неизвестном уровне CD4-клеток профилактика пневмоцистоза проводится больным со стадией IIIБ в период клинической активности при наличии легочной патологии, а также всем больным со стадией IIIВ (по клинической классификации ВИЧ-инфекции, 1989). За рубежом показаниями к проведению химиопрофилактики пневмоцистоза являются эпизоды ПП в анамнезе, уровень CD4-лимфоцитов менее 0,2x10 9 /л, а также лихорадка неясного генеза в течение 2 недель [10].
Для профилактики применяется ко-тримоксазол (3 дня в неделю взрослым по 2 таблетки по 480 мг, детям – в соответствии с массой тела). Альтернативный режим – аэрозоль пентамидина по 300 мг/мес или в/в по 4 мг/кг в течение 2-4 недель, или дапсон по 200 мг в сочетании с пириметамином по 75 мг и фолиновой кислотой по 25 мг в неделю.
Для вторичной профилактики в течение 4 недель после окончания курса лечения острого процесса рекомендуется принимать ежедневно по 1 таблетке (480 мг) ко-тримоксазола (поддерживающая терапия), а затем, в случае отсутствия отрицательной клинической и рентгенологической динамики, перевести больного на схему первичной профилактики. При появлении признаков активации болезни переходят на ежедневный прием препарата в соответствии со схемой лечения.
Форма выпуска, упаковка и состав препарата Бисептол
Суспензия для приема внутрь белого или светло-кремового цвета, с земляничным запахом.
| 5 мл | |
| сульфаметоксазол | 200 мг |
| триметоприм | 40 мг |
Вспомогательные вещества: макрогола глицерилгидроксистеарат, магния алюмосиликат, кармеллоза натрия, лимонной кислоты моногидрат, метилгидроксибензоат, пропилгидроксибензоат, натрия сахаринат, натрия гидрофосфата додекагидрат, мальтитол, ароматизатор земляничный, пропиленгликоль, вода очищенная.
80 мл - флаконы темного стекла (1) - пачки картонные.
Фармакологическое действие
Ко-тримоксазол - комбинированный противомикробный препарат, состоящий из сульфаметоксазола и триметоприма в соотношении 5:1.
Сульфаметоксазол, сходный по строению с пара-аминобензойной кислотой (ПАБК), нарушает синтез дигидрофолиевой кислоты в бактериальных клетках, препятствуя включению ПАБК в ее молекулу. Триметоприм усиливает действие сульфаметоксазола, нарушая восстановление дигидрофолиевой кислоты в тетрагидрофолиевую - активную форму фолиевой кислоты, ответственную за белковый обмен и деление микробной клетки.
Оба компонента, таким образом, нарушают процесс образования фолиевой кислоты, необходимой для синтеза микроорганизмами пуриновых соединений, а затем и нуклеиновых кислот (РНК и ДНК). Это нарушает образование белков и приводит к гибели бактерий. In vitro является бактерицидным препаратом широкого спектра действия, однако чувствительность может зависеть от географического местоположения.
Обычно чувствительные возбудители (минимальная подавляющая концентрация (МПК) менее 80 мг/л по сульфаметоксазолу): Moraxella (Branhamella) catarrhalis, Haemophilus influenzae (бета-лактамазообразующие и бета-лактамазонеобразующие штаммы), Haemophilus parainfluenzae, Escherichia coli (включая энтеротоксогенные штаммы), Citrobacter spp. (в т.ч. Citrobacter freundii), Klebsiella spp. (в т.ч. Klebsiella pneumoniae, Klebsiella oxytoca), Enterobacter cloaceae, Enterobacter aerogenes, Hafnia alvei, Serratia spp. (в т.ч. Serratia marcescens, Serratia liquefaciens), Proteus mirabilis, Proteus vulgaris, Morganella morganii. Shigella spp. (в т.ч. Shigella flexneri. Shigella sonnet). Yersinia spp. (в т.ч. Yersinia enterocolitica), Vibrio cholerae, Edwardsiella tarda, Alcaligenes faecalis, Burkholderia (Pseudomonas) cepacia, Burkholderia (Pseudomonas) pseudomallei.
Так же, чувствительными могут быть Brucella spp.. Listeria monocytogenes, Nocardia asteroides, Pneumocystis carinii, Cyclospora cayetanensis.
Частично чувствительные возбудители (МПК 80-160 мг/л по сульфаметоксазолу): коагулазоотрицательные штаммы Staphylococcus spp. (в т.ч. метициллиночувствительные и метициллиноустойчивые штаммы Staphylococcus aureus). Streptococcus pneumoniae (пенициллиночувствительные и пенициллиноустойчивые штаммы), Haemophilus ducreyi, Providencia spp. (в т.ч. Providencia rettgeri), Salmonella typhi. Salmonella enteritidis, Slenotrdphomonas maltophilia (ранее называвшаяся Xanthomonas maltophilia), Acinetobacter Iwoffii, Acinetobacter baumanii, Aeromonas hydrophila.
Устойчивые возбудители (МПК более 160 мг/л по сульфаметоксазолу): Mycoplasma spp., Mycobacterium tuberculosis, Treponema pallidum, Pseudomonas aeruginosa.
Если препарат назначается эмпирически, необходимо учитывать местные особенности устойчивости к препарату возможных возбудителей конкретного инфекционного заболевания. При инфекциях, которые могут быть вызваны частично чувствительными микроорганизмами, рекомендуется провести пробу на чувствительность, чтобы исключить резистентность возбудителя.
Фармакокинетика
При пероральном приеме абсорбция быстрая и почти полная - 90%. После однократного приема 160 мг триметоприма + 800 мг сульфаметоксазола C max триметоприма - 1.5-3 мкг/мл, а сульфаметоксазола - 40-80 мкг/мл. С max в плазме крови достигается через 1-4 ч; терапевтический уровень концентрации сохраняется в течение 7 ч после однократного приема. При многократном приеме с интервалом в 12 ч минимальные равновесные концентрации стабилизируются в пределах 1.3-2.8 мкг/мл для триметоприма и 32-63 мкг/мл для сульфаметоксазол. C ss препарата достигается в течение 2-3 дней.
Хорошо распределяется в организме. V d триметоприма составляет около 130 л, сульфаметоксазола - около 20 л. Проникает через гематоэнцефалический барьер, плацентарный барьер и в грудное молоко. В легких и моче создает концентрации, превышающие содержание в плазме. Триметоприм несколько лучше, чем сульфаметоксазол проникает в невоспаленную ткань предстательной железы, семенную жидкость, секрет влагалища, - слюну, здоровую и - воспаленную ткань легких, желчь, в то время как в спинномозговую жидкость и водянистую влагу глаза оба компонента препарата проникают одинаково. Большие количества триметоприма и несколько меньшие количества сульфаметоксазола поступают из кровотока в интерстициальную и другие экстравазальные жидкости организма, при этом концентрации триметоприма и сульфаметоксазола превышают МПК для большинства патогенных микроорганизмов. Связывание с белками плазмы - 66% у сульфаметоксазола, у триметоприма - 45%. Метаболизируется в печени. Некоторые метаболиты обладают противомикробной активностью. Сульфаметоксазол метаболизируется преимущественно путем N4-ацетилирования и, в меньшей степени, конъюгацией с глюкуроновой кислотой. Выводится почками в виде метаболитов (80% в течение 72 ч) и в неизмененном виде (20% сульфаметоксазола, 50% триметоприма); незначительное количество - через кишечник. Оба вещества, а также их метаболиты, выводятся почками, как путем клубочковой фильтрации, так и канальцевой секреции, вследствие чего концентрации обоих активных веществ в моче значительно выше, чем в крови.
T 1/2 сульфаметоксазола - 9-11 ч, триметоприма - 10-12 ч, у детей -существенно меньше и зависит от возраста: до 1 года - 7-8 ч, 1-10 лет - 5-6 ч.
У пожилых пациентов и/или пациентов с нарушением функции почек (клиренс креатинина (КК) 15-20мл/мин) T 1/2 увеличивается, что требует коррекции дозы.
Показания препарата Бисептол
Инфекционно-воспалительные заболевания, вызванные чувствительными к препарату микроорганизмами:
Лечение пневмоцистной инфекции. Профилактика
Препаратом выбора в лечении пневмоцистной инфекции является триметоприм/сульфаметоксазол (бисептол). При назначении препарата дозу расчитывают по триметоприму — 20 мг/кг в сутки, доза сульфаметоксазола составляет 100 мг/кг в сутки. Суточную дозу делят на 3—4 приема, вводят внутривенно или перорально.
Концентрация триметоприма/сульфаметоксазола в сыворотке крови является эквивалентной при использовании его внутривенно или перорально (в случае нормальной функции желудочно-кишечного тракта). Длительность лечения составляет 14—21 день.
Концентрация сульфаметоксазола в крови более чем 200 мкг/мл ассоциируется с учащением токсических эффектов, прежде всего миелосупрессией. Терапия триметопримом/сульфаметоксазолом может быть продолжена даже при появлении некоторых побочных эффектов: сыпь, умеренное повышение активности печеночных трансаминаз, незначительная депрессия кроветворения. В этих случаях суточную дозу препарата уменьшают, или реже вводят, или изменяют форму применения.
К наиболее частым побочным эффектам, возникающим при лечении триметопримом/сульфаметоксазолом, относят сыпь, лейкопению, тромбоцитопению, тошноту, рвоту, нефротоксичность. Симптомы аллергии могут быть от сыпи до возникновения тяжелых проявлений, таких, как синдром Стивенса— Джонсона, гепатотоксичность с эозинофилией и некрозом клеток печени, экссудативной мультиформной эритемой. Миелосупрессия является обратимой при снижении дозы препарата.
Быстрой положительной динамики при лечении пневмоцистной инфекции получить не удается. Стабилизацию состояния и улучшение состава газов артериальной крови отмечают на 3—4-е сутки терапии. Если после 4 дней лечения регистрируется отрицательная динамика в виде повышения лихорадки и сохранения артериальной гипоксемии, появления дополнительных инфильтратов в легких, то это является показанием к проведению дополнительных исследований, направленных на поиск иных причин инфекции, или, при отсутствии сопутствующей инфекции, модификации антипневмоцистной терапии.
Неудачи при лечении триметопримом/сульфаметоксазолом пневмоцистной пневмонии обусловлены прежде всего неадекватной концентрацией препарата в сыворотке крови или в ткани легких, выраженным повреждением легких пневмоцистами, сопутствующим иным инфекционным процессом. При секвенировании штаммов, выделенных от пациентов при неэффективной профилактике или лечения пневмоцистной пневмонии, обнаружены однотипные мутации определенного гена dihydropteroate synthase gene, свидетельствующие о возможном развитии приобретенной резистентности к сульфаниламидам и ко-тримоксазолу.
Коррелируемой связи между обнаружением мутаций указанного гена и неуспешной терапией клинических случаев пока не получено. В большинстве случаев при сохраняющейся клинической симптоматике пневмоцистной инфекции на фоне терапии триметопримом/сульфаметоксазолом определяется иной процесс в легких (инфекция, опухоль, аллергия), осложняющий пневмоцистную пневмонию, чем резистентность к триметоприму/сульфаметоксазолу.
Препаратами второго ряда являются атоваквон, пентамидин (пентамидина изотионат) или сочетание дапсона с триметопримом.
Пентамидин назначают в дозе 4 мг/кг в сутки (максимальная суточная доза 300 мг), вводят однократно внутривенно в 5 % растворе глюкозы, длительность инфузии составляет 1—2 ч. Терапевтическая эффективность проявляется более медленно — через 5—7 дней применения препарата.
Препарат обладает высокой токсичностью, поэтому не рассматривается как средство первой линии. Токсическое действие пентамидина существенно увеличивается при назначении его больным с нарушенной функцией почек. Побочные эффекты при терапии пентамидином отмечаются у 50 % больных и включают гипогликемию, гипергликемию, азотемию, нейтропению, тромбоцитопению, панкреатиты, тошноту, рвоту, гипокальциемию, гипотензию, нарушения ритма сердца. Панкреатиты чаще всего наблюдаются в случаях, если суммарная доза пентамидина превышает 3 г. Повреждение органов может возникнуть и после прекращения терапии пентамидином ввиду длительного периода полувыведения препарата, составляющего около 2 мес.
Заменять при лечении внутривенную форму пентамидина на ингаляционную не рекомендуется, поскольку ингаляционное введение препарата используется только с профилактической целью.
Назначать другие препараты для терапии пневмоцистной пневмонии рекомендуется при аллергии к триметоприму/сульфаметоксазолу или пентамидину либо из-за их токсичности. Дапсон (100 мг/сут, перорально) применяют в сочетании с триметопримом (15 мг/кг/сут, перорально, в 3 приема); атоваквон (суспензия) — по 750 мг 2 раза в сутки перорально; триметрексат — 45 мг/м2 внутривенно с фолиевой кислотой (80 мг/м2); клиндамицин — по 450—600 мг внутривенно или перорально каждые 6 ч с примаквином (15 мг однократно перорально). Длительность лечения 21 день.
У части пациентов наблюдается ухудшение состояния в первые дни специфической терапии пневмоцистной пневмонии в виде нарастания одышки, снижения показателей оксигенации вследствие внутриальвеолярной гибели микроорганизмов, приводящей к развитию местного воспалительного процесса и снижению насыщения кислородом.
Как правило, эти пациенты нуждаются в терапии кислородом, нередко в проведении искусственной вентиляции легких (ИВЛ), которая в большинстве случаев осложняется присоединением бактериальной или грибковой суперинфекции. Назначение кортикостероидов предотвращает необходимость в ИВЛ у 50 % больных, уменьшает потребность в оксигенотерапии, снижает частоту побочных эффектов, обусловленных применением антибиотиков. Преднизолон рекомендуется назначать при гипоксемии (РаО2 < 70 мм рт. ст.) до интубации по 40 мг 2 раза (перед введением триметоприма/сульфаметоксазола), через 5— 7 дней дозу преднизолона снижают, длительность применения 7—14 дней.
Профилактика пневмоцистной инфекции
Профилактика пневмоцистной инфекции показана при терапии глюкокортикоидами (преднизолон по 20 мг/кг в сутки в течение 2— 3 нед), лечении препаратами, приводящими к снижению числа CD4-лимфоцитов, реципиентам аллогенных стволовых гемопоэтических клеток (до 180-го дня после трансплантации); пациентам, имевшим в анамнезе пневмоцистную пневмонию. Назначают один из следующих препаратов:
- триметоприм/сульфаметоксазол (бисептол): дозу рассчитывают по триметоприму (5 мг/кг в сутки), принимают в 2 приема перорально или вводят внутривенно ежедневно либо 3 дня в неделю;
- дапсон — по 100 мг ежедневно перорально;
- пентамидин — 300 мг (в виде аэрозоля через респираторный ингалятор) или внутривенно один раз каждые 3—4 нед.
Препараты назначают в период цитостатической терапии и далее в течение всего периода нейтропении.
При использовании триметоприма/сульфаметоксазола одновременно проводят профилактику в отношении Toxoplasma gondii, Listeria monocytogenes, Nocardia asteroides.
Пациенты, инфицированные пневмоцистами, не должны находиться в палате с другими иммунокомпрометированными больными.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
а) Терминология:
1. Аббревиатура:
• Пневмоцистная пневмония (ПЦП)
2. Синоним:
• Пневмония, вызванная Pneumocystis jirovecii
3. Определение:
• Жизнеугрожающая респираторная инфекция, развивающаяся у людей с иммунодефицитом:
о Например, у ВИЧ-инфицированных; у людей, получающих иммуносупрессивную терапию
• Этиология: Pneumocystis jirovecii, старое название - Pneumocystis carinii
б) Визуализация:
2. Рентгенография легких при пневмоцистной пневмонии:
• Норма (10-30%)
• Двухсторонние прикорневые или диффузные симметричные плохо отграниченные затемнения, или ретикулярные изменения
• Участки консолидации, занимающие несколько долей:
о В результате прогрессирования заболевания или развития острого респираторного дистресс-синдрома (ОРДС)
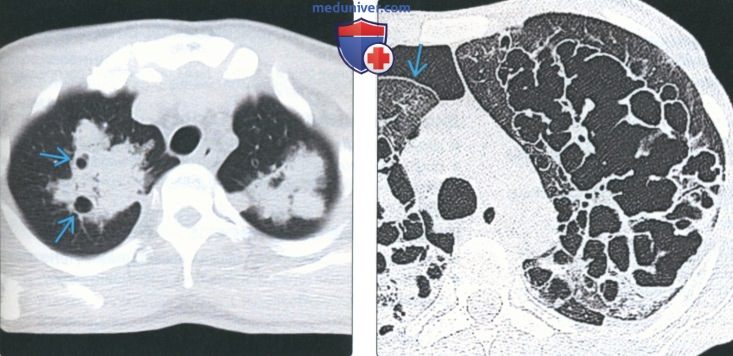
(Слева) На аксиальной КТ без КУ у пациента с пневмоцистной пневмонией в верхушечных отделах обоих легких визуализируются участки снижения пневматизации с кистозными включениями. Кисты (участки некроза и кавитации) возникают в 30% случаев пневмоцистной пневмонии.
(Справа) На аксиальной КТВР у мужчины 31 года с пневмоцистной пневмонией и СПИД определяются сливные участки пневматоцеле в верхних долях обоих легких в сочетании с правосторонним пневмотораксом, вероятным осложнением пневматоцеле.
3. КТ легких при пневмоцистной пневмонии:
• Хроническая ПЦП:
о Неправильные линейные затемнения
о Тракционные бронхоэктазы
о Нарушение архитектоники легкого
о Крупный очаг(и)
4. Рекомендации по визуализации:
• Лучший метод диагностики:
о КТВР
в) Дифференциальная диагностика пневмоцистной пневмонии:
г) Патология:
1. Общая характеристика:
• Pneumocystis jirovecii: широко распространенный эукариотический микроорганизм
• Рибосомная РНК аналогична таковой у грибков, что позволяет классифицировать Pneumocystis jirovecii как грибковый организм
• Серологические исследования демонстрируют практически общую серопозитивную реакцию на пневмоцисты к двухлетнему возрасту
• Патофизиология неизвестна; возможна реактивация латентной детской инфекции, передача возбудителя между восприимчивыми хозяевами, или заражение из внешней среды
• У пациентов с ВИЧ/СПИД и ПЦП намного выше нагрузка пневмоцистами, ниже уровень нейтрофилов по сравнению с инфицированными, но ВИЧ(-) пациентами
2. Микроскопия:
• Менее типичные проявления:
о Интерстициальный фиброз
о Гранулемы
о Формирование гиалиновых мембран
д) Клинические особенности:
1. Проявления:
• Типичные признаки/симптомы:
о Прогрессирующее диспноэ
о Непродуктивный кашель
о Субфебрильная лихорадка
• Другие признаки/симптомы:
о Острая боль в грудной клетке:
- Может быть связана с пневмотораксом
о Тахипноэ
о Тахикардия
о Кровохарканье (3%)
о Отсутствие симптомов (3%)
о Отсутствие нарушений при аускультации
• Клинический профиль:
о СПИД-главный фактор риска ПЦП
о Другие факторы риска: химиотерапия при злокачественных опухолях, иммуносупрессивная терапия, врожденные нарушения иммунитета
о ВИЧ-инфицированные пациенты:
- Младшая возрастная группа
- Подострое клиническое течение
- Средний интервал между появлением симптомов и диагнозом: 28 дней
- CD4(+) клетки: о ВИЧ(-)пациенты:
- Старшая возрастная группа
- Внезапное развитие дыхательной недостаточности
- Средний интервал между появлением симптомов и диагнозом: 5 дней
о Диагностика:
- Индукция мокроты в гипертоническом солевом растворе: диагностическая ценность 50-90%
- Бронхоальвеолярный лаваж: идентификация возбудителя при помощи различных вариантов окраски:
Трофические формы: модифицированная окраска по Папаниколау, по Райту-Гимзе, по Граму-Вейгерту
Цисты: окраска по Гомори, толуидиновым синим
- Моноклональные антитела: выше чувствительность и специфичность по сравнению с традиционным окрашиванием образцов индуцированной мокроты
- ПЦР: выше чувствительность и специфичность по сравнению с бронхоальвеолярным лаважом и исследованием индуцированной мокроты
2. Демография:
• Мужчины и женщины заболевают одинаково часто
• Снижается заболеваемость у лиц, страдающих СПИД, в связи с появлением высокоактивной антиретровирусной терапии и всеобщей профилактики ПЦП
3. Течение и прогноз:
• ВИЧ(+) пациенты:
о Летальность в начальном стадии 10-20% о ↑ смертность у пациентов, которым требуется ИВЛ
о Меньшее количество воспалительных клеток соотносится с большей оксигенацией и лучшей выживаемостью
• ВИЧ(-) пациенты:
о Летальность 30-60%
о У пациентов, страдающих злокачественными опухолями, выше риск гибели
4. Лечение пневмоцистной пневмонии:
• Метод выбора: триметоприм-сульфаметоксазол и адъюнктивная терапия кортикостероидами (для подавления воспалительного процесса в легких у пациентов с тяжелыми инфекциями)
• Первичную профилактику ПЦП у ВИЧ-инфицированных взрослых людей необходимо начинать при уровне CD4 • Пожизненная профилактика у пациентов, ранее переносивших ПЦП
ж) Список использованной литературы:
1. Bienvenu AL et al: Pneumocystis pneumonia suspected cases in 604 non-HIV and HIV patients. Int J Infect Dis. 46:11-7, 2016
2. Lu PX et al: Correlation between imaging features of Pneumocystis Jiroveci pneumonitis (PCP), CD(4) (+) T lymphocyte count, and plasma HIV viral load: A study in 50 consecutive AIDS patients. Quant Imaging Med Surg. 2(2): 124-9, 2012
Читайте также:

