Полудан при генитальном герпесе
Обновлено: 19.04.2024
Самарский государственный медицинский университет , Самара, Россия , 443099
Самарский государственный медицинский университет
Государственное учреждение здравоохранения Самарской Области Тольяттинский Кожно-венерологический диспансер, Тольятти, Россия, 445004
Государственное учреждение здравоохранения Самарской Области Тольяттинский Кожно-венерологический диспансер, Тольятти, Россия, 445004
Генитальный герпес: эффективность противовирусной терапии
Журнал: Клиническая дерматология и венерология. 2015;14(3): 40‑45
Плохо контролируемый и постоянно увеличивающийся рост герпетической инфекции, развитие рецидивов генитального герпеса у пациентов, перенесших первичную инфекцию, требуют оценки эффективности лечения. Цель исследования — оценить эффективность ациклических нуклеозидов ацикловир и валацикловир (Валвир) в лечении рецидивирующей герпетической инфекции, а также комплаентность лечению. Материал и методы. 67 пациентов с рецидивирующим генитальным герпесом во время рецидива получали валацикловир (Валвир) по 500 мг 2 раза в сутки (n=34) и ацикловир по 200 мг 5 раз в сутки в течение 5 дней (n=33). Результаты. Отмечено некоторое ускорение разрешения клинических проявлений в группе принимавших валацикловир. Заключение. Ацикловир и валацикловир (Валвир) эффективны в лечении рецидивирующего генитального герпеса. Меньшая частота применения валацикловира (Валвира) увеличивает его комплаентность.
Самарский государственный медицинский университет , Самара, Россия , 443099
Самарский государственный медицинский университет
Государственное учреждение здравоохранения Самарской Области Тольяттинский Кожно-венерологический диспансер, Тольятти, Россия, 445004
Государственное учреждение здравоохранения Самарской Области Тольяттинский Кожно-венерологический диспансер, Тольятти, Россия, 445004
Генитальный герпес — хроническое рецидивирующее вирусное заболевание, передаваемое преимущественно половым путем, которое вызывается вирусом простого герпеса (ВПГ) 1-го и/или 2-го типов (ВПГ-1 и/или ВПГ-2) [1].
Данное инфекционное заболевание характеризуется поражением кожи и слизистых оболочек мочеполовых органов и аноректальной области. Возбудителем генитального герпеса в большинстве случаев является ВПГ-2, однако, как показывает мировая практика, у 25—30% пациентов выявляют ВПГ-1, заражение которым происходит при орально-генитальных, генитально-анальных и орально-анальных контактах. Возможна передача инфекции бытовым путем через предметы личной гигиены. Заражение возможно как при наличии клинических проявлений болезни у полового партнера, так и при их отсутствии, что особенно важно в эпидемиологическом отношении [2].
Отличительным свойством ВПГ является его способность вызывать хроническую латентную инфекцию, т. е. способность к длительному (пожизненный) персистированию с последующей периодической реактивацией [3, 4].
По данным многочисленных исследований [5—8], распространенность генитальной герпетической инфекции неуклонно возрастает.
Генитальный герпес относят к инфекции, передаваемой половым путем (ИППП). Это наиболее распространенное эрозивно-язвенное заболевание мочеполовой системы встречается во всех популяционных группах. Инфицированность им увеличивается с возрастом: самую высокую заболеваемость регистрируют в возрастной группе 20—29 лет, второй пик заболеваемости приходится на 35—40 лет [9—11].
Основными факторами риска развития генитального герпеса являются женский пол (женщины более восприимчивы к ВПГ-2, чем мужчины), большое количество половых партнеров на протяжении жизни, пренебрежение принципами безопасного секса, рост числа гомосексуальных связей, инфицирование другими ИППП, недостаточный контроль за передачей вируса, слабый учет заболеваемости и анализ эпидемиологической ситуации [11, 12]. Кроме влияния на общее состояние здоровья, носительство ВПГ-2 значительно снижает качество жизни и опосредованно негативно влияет на репродуктивную систему [13].
Наибольшую опасность в плане распространения инфекции представляют больные, у которых рецидивирующая форма герпеса протекает в ассоциации с другими микроорганизмами урогенитального тракта (например, хламидии, уреаплазмы, микоплазмы). Эрозивно-язвенные поражения кожи и слизистых оболочек половых органов облегчают передачу других ИППП, в том числе вируса иммунодефицита человека (ВИЧ; так называемое явление эпидемиологического синергизма). Кроме того, ВПГ играет большую роль в этиологии таких заболеваний, как атопический дерматит [14].
У 20—30% больных генитальным герпесом в течение первых 2—3 лет развивается рецидив. Обострения могут быть спровоцированы разными факторами: эмоциональный и/или физический стресс, инфекционные и соматические заболевания, алиментарные состояния (голодание, избыточное употребление алкоголя), нахождение в условиях резких колебаний температуры воздуха и/или воды, резкая смена климатических поясов, медицинские манипуляции и другие [3, 15].
Рецидивирующий генитальный герпес нередко нарушает нормальную половую жизнь пациентов, препятствует созданию семьи, приводит к нервно-психическим расстройствам [2, 12, 16].
Поскольку современная медицина не располагает методами лечения, позволяющими добиться полной элиминации ВПГ из организма, лечение пациентов направлено на снижение тяжести эпизодов обострения, сокращение срока полного заживления поражений, снижение частоты и уменьшения тяжести рецидивов, предупреждение передачи инфекции половому партнеру, улучшение качества жизни пациентов [3, 15, 17].
Наиболее эффективны в лечении генитального герпеса препараты специфического противовирусного действия — ациклические нуклеозиды, блокирующие размножение ВПГ-1 и ВПГ-2. Нуклеозиды целенаправленно воздействуют на процесс размножения вируса, проникая только в пораженную клетку и не затрагивая здоровую [11].
Наиболее изученными с точки зрения принципов доказательной медицины и широко применяемыми препаратами этой группы являются ацикловир и валацикловир [18—20]. В рандомизированном исследовании с плацебо-контролем, в котором сравнивалась эффективность обоих препаратов, было показано уменьшение выраженности и продолжительности болевого синдрома [21].
Цель исследования — установление критериев эффективности лечения генитального герпеса рецидивирующей формы с использованием специфических противовирусных средств — ациклических нуклеозидов ацикловир и валацикловир (Валвир).
Материал и методы
Тяжесть и продолжительность клинических проявлений при рецидивах генитального герпеса менее выражены, чем при первичной форме.
Согласно современным клиническим рекомендациям, проведение эпизодической терапии при рецидивирующей форме герпетической инфекции рекомендуется по одной из следующих схем [1]:
— ацикловир 200 мг внутрь 5 раз в сутки в течение 5 дней;
— ацикловир 400 мг внутрь 3 раза в сутки в течение 5 дней;
— валацикловир 500 мг 2 раза в сутки в течение 5 дней;
— фамцикловир 125 мг внутрь 2 раза в сутки в течение 5 дней.
Нами было проведено исследование, целью которого было сравнение эффективности противовирусных препаратов ацикловир и валацикловир (Валвир), применяемых у больных генитальным герпесом рецидивирующей формы.
Основными критериями включения в исследование являлись возраст пациентов от 19 до 49 лет, постановка диагноза не менее чем за 1 год до включения в исследование, наличие не менее 6 рецидивов герпетической инфекции в течение последнего года до включения в исследование, наличие текущего обострения герпетической инфекции, наличие письменного информированного согласия на участие в клиническом исследовании.
Перед включением пациентов в исследование проводили изучение анамнеза (демографические данные, сведения о сопутствующих заболеваниях и о сопутствующей терапии), оценка общих показателей (частота сердечных сокращений, артериальное давление, температура тела), физикальное обследование (осмотр кожных покровов и видимых слизистых оболочек, наружный осмотр аногенитальной области), получение клинического материала для лабораторного подтверждения диагноза. Верификацию диагноза осуществляли на основании обнаружения ДНК-вирусов простого герпеса 1-го и/или 2-го типа методом полимеразной цепной реакции (ПЦР).
До назначения терапии проводили оценку субъективных и объективных симптомов герпетической инфекции (гиперемия и отечность, боль, зуд, жжение в области поражения, наличие везикулезных герпетических элементов). У пациентов обеих групп не имелось значительных различий в выраженности клинических проявлений заболевания.
Основными субъективными симптомами герпетической инфекции у пациентов 1-й группы являлись везикулезные высыпания в области поражения (100%; n=34), зуд и жжение в области наружных половых органов (88,2%; n=30), боль в области поражения (67,4%; n=23), гиперемия и отечность (58,8%; n=20).
Пациенты 2-й группы при обращении за медицинской помощью предъявляли жалобы на везикулезные высыпания в области поражения (100%; n=33), зуд и жжение (87,8%; n=29), боль (75,8%; n=25), гиперемию и отечность в области поражения (63,6%; n=21) (рис. 1).

Рис. 1. Клинические проявления рецидивирующей герпетической инфекции у обследованных пациентов, %.
Все пациенты 1-й группы, включенные в исследование, получали терапию препаратом валацикловир (Валвир) в дозе по 500 мг 2 раза в сутки в течение 5 дней.
Пациенты 2-й группы принимали препарат ацикловир по 200 мг 5 раз в сутки в течение 5 дней.
Контроль эффективности терапии осуществляли на 5-й и 14-й день после начала лечения в соответствии с критериями эффективности (уменьшение клинических проявлений инфекции, заживление поражений). В ходе наблюдения пациентам проводили обследование, включавшее осмотр кожных покровов и видимых слизистых оболочек, обследование наружных половых органов и определение признаков (симптомов) по совокупности показателей, фиксирование любых неблагоприятных явлений с момента последнего визита.
Динамика клинических симптомов у 1-й и 2-й групп отражена на рис. 2, 3.

Рис. 2. Динамика клинических симптомов у пациентов 1-й группы, %.

Рис. 3. Динамика клинических симптомов у пациентов 2-й группы, %.
Согласно полученным данным, у пациентов как 1-й, так и 2-й группы через 5 дней приема противовирусных препаратов был достигнут значительный клинический эффект, выражавшийся в уменьшении субъективных симптомов герпетической инфекции: боли, зуда и жжения в области поражений. Отсутствие везикулезных элементов было выявлено у 35,3% пациентов 1-й группы (n=12) и у 30,3% пациентов 2-й группы (n=10).
На 14-й день после начала терапии симптомы герпетической инфекции сохранялись у 1 (2,9%) пациента 1-й группы и у 2 (7,1%) — 2-й, при этом интенсивность субъективных проявлений заболевания была значительно снижена (рис. 4).

Рис. 4. Эффективность противовирусной терапии обследованных пациентов, %.
В процессе наблюдения клиническая эффективность противовирусной терапии была достигнута у 33 (97,1%) пациентов 1-й группы и у 31 (93,9%) — 2-й.
Выводы
В ходе проведенного исследования специфических противовирусных препаратов ацикловир и валацикловир (Валвир) в терапии рецидивирующей герпетической инфекции установлено, что оба препарата одинаково эффективно ускоряют разрешение эпизодов герпеса и не имеют значительных различий таких показателей, как срок заживления элементов сыпи, продолжительность болей и срок исчезновения всех симптомов заболевания.
Несомненное преимущество валацикловира (Валвир) — меньшая кратность его применения, что увеличивает его комплаентность.
Одной из нозологических форм, которую вирусы простого герпеса (ВПГ) вызывают у человека, является генитальный герпес. В настоящее время эта форма ВПГ-инфекции считается наиболее распространенной среди всех инфекций, передающихся половым путем.
Одной из нозологических форм, которую вирусы простого герпеса (ВПГ) вызывают у человека, является генитальный герпес. В настоящее время эта форма ВПГ-инфекции считается наиболее распространенной среди всех инфекций, передающихся половым путем. Генитальный герпес вызывают два серотипа вируса простого герпеса: ВПГ-1 и ВПГ-2; причем наиболее часто — ВПГ-2. Согласно данным сероэпидемиологических исследований, инфицирование ВПГ-1 выявляется у 20—40%, а ВПГ-2 — у 50—70% больных генитальным герпесом [2]. Заболевание передается преимущественно при сексуальных контактах от больного генитальным герпесом. Нередко генитальным герпесом заражаются от лиц, не имеющих симптомов заболевания на момент полового контакта или не знающих о том, что они инфицированы [5]. Эта особенность ВПГ, связанная с бессимптомным вирусоносительством, является сложной задачей, от решения которой зависит не только трудоспособность и здоровье, но и личная судьба миллионов потенциальных больных. Имеются сведения о том, что от 60 до 80% новорожденных, у которых развивается неонатальный герпес, рождаются от матерей с бессимптомным носительством [6].
ВПГ-инфекция также может быть причиной нарушения репродуктивной функции, невынашивания беременности, преждевременных родов и патологии плода. Возможно участие ВПГ в развитии онкологических заболеваний гениталий, иммунодефицитных состояний, что позволяет считать герпесвирусные инфекции важной медико-социальной проблемой практического здравоохранения [2].
Лечение хронических, часто рецидивирующих форм ВПГ-инфекции, до настоящего времени представляет определенные трудности, которые объясняются особенностями взаимодействия вируса с макроорганизмом. Жизнедеятельность вирусов герпеса основывается на следующих биологических особенностях:
- все вирусы герпеса являются внутриклеточными паразитами;
- герпесвирусы пожизненно персистируют в аксоноганглиальных структурах центральной и периферической нервной системы;
- в течение жизни человек многократно реинфицируется новыми штаммами вирусов герпеса, при этом возможно одновременное сосуществование нескольких видов и штаммов вирусов [12];
- при нарушении динамического равновесия между иммунным гомеостазом и вирусами последние переходят в активную форму [9].
Согласно данным проведенных исследований только 20% инфицированных ВПГ имеют диагностированный генитальный герпес, 60% — нераспознанный симптоматический генитальный герпес (атипичную форму) и 20% — бессимптомный герпес. В настоящее время только 27% пациентов с диагнозом генитальный герпес получают противовирусную терапию, из них треть — местное лечение [2]. По данным некоторых авторов, около 95% пациентов с клиническими проявлениями генитального герпеса вообще никак не лечатся [11].
Все разнообразие методов терапии и профилактики герпесвирусных инфекций в конечном счете сводится к трем главным подходам:
- химиотерапия;
- иммунотерапия;
- комбинация этих двух методов.
Каждый врач в своей практической работе так или иначе сталкивается с необходимостью решения этой сложной задачи, требующей тонкого индивидуального подхода к каждому пациенту, страдающему ВПГ.
Различают два способа применения противовирусных химиопрепаратов: эпизодическое назначение (при обострениях герпесвирусной инфекции по мере необходимости) и супрессивная или превентивная терапия. В первом случае препарат назначается коротким курсом (5—10 дней), во втором — ежедневный прием препарата в течение нескольких месяцев, а то и лет призван помочь не столько купировать рецидив, сколько предотвратить развитие рецидивов как таковых.
Однако за последние 10 лет увеличилось число исследований, в ходе которых было показано, что изоляты вируса простого герпеса, полученные от пациенток с продолжающимися рецидивами генитального герпеса на фоне длительной супрессивной терапии (более 4 месяцев), обладают резистентностью по отношению к ацикловиру [10].
К тому же ни ацикловир, ни другие противовирусные агенты — фамцикловир, валацикловир — не предотвращают перехода вируса в латентное состояние, возникновения рецидивов после их отмены либо передачи инфекции, а также, к сожалению, не влияют на естественное течение этой инфекции, то есть не гарантируют полного излечения. Поэтому на протяжении последних двух десятилетий ученые изыскивают методы непосредственного воздействия на иммунную систему больных генитальным герпесом с целью стимуляции специфических и неспецифических ее факторов, тем самым способствуя блокаде репродукции вируса [1].
Главной мишенью применения иммуномодулирующих препаратов служат вторичные иммунодефициты, которые проявляются частыми, рецидивирующими, трудно поддающимися лечению инфекционно-воспалительными процессами разной локализации [7]. Именно к таким процессам, требующим иммунокоррекции, и относится хроническая рецидивирующая герпесвирусная инфекция (ХРГВИ), в частности ее генитальная форма. Иммуномодуляторы назначают в комплексной терапии одновременно с противовирусными средствами.
Полиоксидоний — отечественный иммуномодулятор с широким спектром фармакологического действия, не имеющий аналогов в мире [3]. Опыт применения полиоксидония начиная с 1996 года показал его высокую клиническую эффективность в комплексном лечении многих вторичных иммунодефицитных состояний, проявляющихся хроническими, рецидивирующими, вялотекущими инфекционно-воспалительными процессами различной локализации, в том числе в ходе терапии вирусных инфекций [4].
У нас также имеется определенный позитивный опыт применения полиоксидония у пациентов, резистентных к ацикловиру [9].
Мы проводили исследование открытым методом у 50 пациентов с ХРГВИ. В исследование включались пациенты (возрастной интервал от 18 до 65 лет) мужского и женского пола с достоверным диагнозом ХРГВИ. К исследованию не допускались пациенты с гиперчувствительностью к полиоксидонию и беременные женщины. Все пациенты, включенные в исследование, находились в периоде продрома или обострения не более 48 часов от момента появления высыпаний. Обязательным условием для женщин детородного возраста было соблюдение полноценной контрацепции.
На предварительном этапе были сформированы две равнозначные группы пациентов по 25 человек. Пациенты, вошедшие в изучаемые группы, отбирались методом произвольной выборки. Все пациенты предъявляли жалобы на пузырьковые или эрозивные высыпания в области гениталий, зуд, жжение. До лечения всем пациентам проводилась ПЦР-диагностика ВПГ-2 (мазок) — положительный результат получен в 98,3 %.
Возрастной состав пациентов, страдающих генитальной формой герпесвирусной инфекции, в обеих группах был приблизительно одинаковым (43,6 года в первой группе и 38,9 — во второй), в то время как в первой группе средний возраст женщин и мужчин был несколько выше по сравнению со второй группой.
Дозировка и схемы введения. Всем пациентам производилась в/м инъекция препарата утром, под контролем врача. 1-я схема: терапия проводилась в течение 45 дней: пациенты получали по 6 мг полиоксидония в день в/м в течение 5 дней и по 6 мг в/м через день в течение 10 дней. Поддерживающая терапия — по 6 мг в/м 2 раза в неделю в течение месяца. 2-я схема: 6 мг полиоксидония в/м через день в течение 10 дней (всего 5 инъекций на курс).
Обследование проводилось до приема препарата и на 12—14-й день от начала приема препарата, а также на 3—6-й день после окончания приема препарата. Обследование включало общее клиническое, иммунологическое исследования крови, исследование мочи (общее), объективное исследование. Накануне приема препарата собирался подробный анамнез пациента. В состав исследуемых включались совершеннолетние пациенты мужского и женского пола с достоверным диагнозом ХРГВИ.
Объем сопутствующей терапии: все пациенты получали стандартную сопутствующую терапию (ацикловир по 0,2 г 5 раз в день в течение 5 дней и антиоксиданты).
Критериями оценки эффективности являлись следующие параметры: первичные критерии — время достижения полного выздоровления (полная реэпитализация); вторичные критерии — длительность ремиссии и частота рецидивов в ближайшем и отдаленном периоде после терапии полиоксидонием. С целью оценки местных симптомов проводился наружный осмотр места поражения. Оценивалось состояние кожных покровов и слизистых: наличие пузырьков, язвочек, корочек, гиперемии; выяснялись жалобы пациента (зуд, жжение, общее состояние, температура, миалгия).
На фоне лечения полиоксидонием по первой схеме длительность течения рецидива и период реэпителизации сократились в среднем с 6,44 до 3,5 дня, в то время как на фоне стандартной терапии (ацикловир и антиоксиданты) те же показатели изменились с 6,44 до 5,16 дня соответственно. После курса терапии в ближайшем и отдаленном периоде длительность рецидива и быстрота наступления реэпителизации в среднем составляла 4 дня. В процессе лечения препаратом свежие высыпания ни у одного пациента не появились. 76% (19 человек) отметили уменьшение тяжести течения рецидива; остальные — 24% (6 человек) — не отметили разницы по сравнению с периодом до получения препарата. На фоне лечения полиоксидонием по второй схеме длительность течения рецидива и период реэпителизации сократились в среднем с 6,72 до 4,24 дня вместо 6,72 — 5,04 дня соответственно. После лечения полиоксидонием в ближайшем и отдаленном периоде длительность рецидива и быстрота наступления реэпителизации в среднем также составляли 4 дня. 64 % (16 человек) отметили уменьшение тяжести течения рецидива; остальные — 36% (9 человек) — не отметили никаких изменений по сравнению с периодом до получения препарата.
Частота рецидивов у пациентов, получавших полиоксидоний по первой схеме в течение 6 месяцев после лечения, уменьшилась в среднем с 6,5 до 3 раз по сравнению с показателями ближайших шести месяцев перед получением препарата. Длительность ремиссии возросла в среднем с 27 до 75 дней. Максимальная длительность ремиссии увеличилась в среднем с 45 до 180 дней (у отдельных пациентов максимальная ремиссия достигала 190–220 дней, что связано с неравномерностью возникновения рецидивов в исследуемом временном интервале). У 84% пациентов (21 человек) отмечалось ослабление клиники течения рецидива; у 16% (4 человека) после лечения клиника не изменилась. Ухудшения течения заболевания отмечено не было. Частота рецидивов у пациентов, получавших полиоксидоний по второй схеме, в течение 6 месяцев после лечения уменьшилась в среднем с 6 до 3,6 раза по сравнению с показателями ближайших шести месяцев перед получением препарата. Длительность ремиссии возросла в среднем с 33 до 62 дней. Показатель максимальной длительности ремиссии в обеих группах вырос в среднем примерно одинаково — с 45 до 180 дней. У 72% пациентов (18 человек) отмечалось ослабление клиники течения рецидива; у 28% (7 человек) после лечения клиника не изменилась. Как и в первой группе, ухудшений течения заболевания отмечено не было.
Максимальная длительность ремиссии за период наблюдения (2 года) составила 1,9 года в первой группе (у 9 пациентов — 36 %) и 1,1 года во второй группе (у 4 пациентов — 16 %).
До лечения полиоксидонием в обеих группах частота встречаемости и выраженность местных и общих клинических проявлений ХРГВИ была выше по сравнению с теми же показателями на фоне лечения полиоксидонием.
Парентеральное (в/м) введение полиоксидония в соответствии со схемами (см. выше) не вызывало аллергических реакций, не оказывало гепатонефротоксического действия и токсического действия на кроветворные органы; пациенты отмечали хорошую переносимость препарата.
По данным общеклинических и лабораторных методов исследования, побочных эффектов и осложнений при приеме полиоксидония не было.
Использование полиоксидония в комплексной терапии пациентов с генитальной формой хронической рецидивирующей герпесвирусной инфекции является эффективным способом уменьшения клинических проявлений в фазе обострения, сокращения длительности рецидивов и заметного уменьшения их частоты в отдаленном периоде.
Раннее назначение полиоксидония способствует более быстрой реэпителизации и более стойкой ремиссии.
Использование инъекционной формы полиоксидония не вызывает аллергических реакций, а также других побочных эффектов и осложнений.
При соблюдении указанного режима дозирования препарат не обладает нефро- и гепатотоксическим действием.
А. Е. Шульженко, кандидат медицинских наук ГНЦ — Институт иммунологии МЗ РФ, Москва
При наличии герпетической инфекции следует проводить адекватную терапию с учетом характера поражения (локальная, генерализованная форма), первичного или рецидивирующего течения заболевания.
- купирование клинических симптомов, ускорение разрешения клинических проявлений, уменьшение площади поражения, снижение общей интоксикации;
- предупреждение развития острого процесса или рецидива,
- уменьшение частоты рецидивов, укорочение их длительности, увеличение временного периода между рецидивами заболевания, а также облегчение их течения;
- улучшение качества жизни пациентов;
- предупреждение развития осложнений;
- предупреждение дальнейшего распространения возбудителя, снижение риска инфицирования полового партнера или новорожденного.
Половые партнеры пациентов с герпетической инфекцией (ГИ) урогенитального тракта подлежат активному выявлению. Лечение необходимо прово дить у них при клинических проявлениях герпеса. Следует рекомендовать воздерживаться от половой жизни или использовать презервативы во время обострений. Лечение должно проводиться с учетом образа жизни и потребности в подавлении, связанной с влиянием физических и психосоциальных факторов.
Важно при этом учитывать, что достижение положительного результата при лечении генитального герпеса (ГГ) сопряжено с рядом сложностей. Полная элиминация возбудителя – вируса простого герпеса (ВПГ) – невозможна. Несмотря на достигнутые успехи в лечении ГГ, существующие методы не обеспечивают полной элиминации вирусов из организма.
Методы лечения герпетической инфекции
- применяют эффективные противовирусные химиопрепараты
- применяют средства, повышающие специфическую и неспецифическую резистентность организма (интерферон и его индукторы, иммуномодуляторы, вакцины);
- проводят серотерапию и серопрофилактику (лечение и профилактику иммунными сыворотками) с использованием специфических иммуноглобулинов человека или иммунизированных животных;
- применяют местные и антисептические средства для купирования кожно-слизистых поражений.
Противовирусная терапия генитального герпеса
- лечение первичного эпизода ГГ;
- эпизодическая противовирусная терапия (для купирования каждого отдельного эпизода обострения ГИ);
- профилактическая (превентивная или супрессивная) терапия (непрерывное лечение на протяжении определенного времени для предупреждения рецидивов и предотвращения передачи инфекции другим лицам).
Существует ряд противовирусных препаратов, способные быстро и эффективно купировать острые проявления генитального герпеса. В адекватной дозировке большинство этих препаратов одинаково эффективно уменьшают тяжесть и продолжительность обострений генитального герпеса. Однако клинический опыт их применения показал, что, облегчая выраженность симптомов болезни, они не предотвращают наступление рецидивов и, в большинстве случаев, не снижают их частоту.
Профилактическая (супрессивная) противовирусная терапия
В многочисленных исследованиях показано, что продолжительная профилактическая терапия противовирусными препаратами значительно уменьшает бессимптомное и субклиническое (в продромальный период) выделение вируса.
Изученные в настоящее время иммунопатогенетические особенности рецидивирующей герпетической инфекции убедительно указывают на нарушения клеточного иммунного ответа у данной категории больных. При герпесе развиваются иммунодефицитные состояния, обусловленные недостаточностью различных звеньев иммунной системы. Чтобы добиться нормализации иммунологических показателей у больных с данной патологией, необходимо продолжать лечение и в межрецидивный период для коррекции остаточных иммунологических нарушений.
Важным благоприятным эффектом профилактической терапии является снижение психологического давления на пациентов.
Вакцина от герпеса
Вакцино-профилактика ГГ находится в стадии научных и экспериментальных разработок. До настоящего времени не получено ни одной эффективной профилактической вакцины против ВПГ. Природа ВПГ-инфекции, заключающаяся в локальном поражении с последующим латентным периодом без системной вирусемии, приводит к тому, что даже успешная выработка специфических антител не предохраняет от последующего рецидива.
Разработанные вакцины (живые, убитые и рекомбинантные) не нашли широкого применения из-за отсутствия надежных методов оценки эффективности курсов вакцинации, критериев продолжительности вакцинации и дальнейшей реабилитации больных.
Генитальный герпес можно и нужно лечить
Лечение генитального герпеса - это многоплановая задача, сложный и длительный процесс. Правильное лечение и назначение лекарственных средств может проводиться только квалифицированным специалистом с учетом проведенной диагностики и истории болезни. Для каждого пациента терапия должна подбираться индивидуально. При тяжелом течении заболевания показано лечение в стационаре.
Результат лечения в значительной мере зависит от опыта врача, а также от терпения и тщательного выполнения пациентом рекомендаций врача. Существующий сегодня арсенал противовирусных и иммунных препаратов позволяет решить очень многие проблемы, возникающие у лиц, страдающих рецидивирующими формами ГГ с поражением гениталий, ягодиц и другими более редкими локализациями. Раннее начало лечения имеет большое значение для получения значительного противовирусного эффекта.
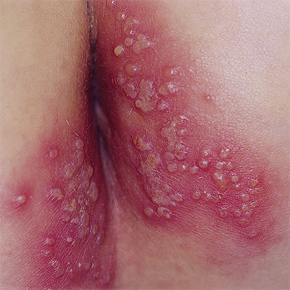
Герпетическое поражение анальной области
Спектр клинических проявлений герпетической инфекции (ГИ) весьма разнообразен. Он зависит от локализации патологического процесса и его распространенности, состояния иммунной системы больного и антигенного типа вируса. Заражение герпесом не всегда вызывает клинически выраженное заболевание, часто имеют место носительство и скрытое течение процесса.
Герпесвирусы не только способны вызывать разнообразные клинические проявления заболевания, но и провоцируют развитие частых рецидивов, а также становятся причиной осложнений. Доказано, что вирусы герпеса вызывают разнообразных нарушений в функционировании иммунной системы (иммунодефицит), которые необходимо учитывать при лечении.
Оба серотипа вируса простого герпеса (ВПГ-1 и ВПГ-2 (рус.), HSV-I и HSV-II (англ.)) могут инфицировать половые органы человека. Чаще всего герпес половых органов вызывается ВПГ-2, реже – ВПГ-1.
Первичный герпес половых органов
Первичный герпес половых органов – это первый эпизод заболевания у больного, у которого на момент проявления заболевания нет антител к ВПГ типов 1 и 2. В 20–40% случаев первичный герпес половых органов обусловлен ВПГ-1.
Первичное инфицирование может протекать бессимптомно или сопровождаться характерными признаками в местах проникновения вируса - болезненными высыпаниями на половых органах или в перианальной области, которые затем изъязвляются и сопровождаются сильной болью.
При симптомной форме заболевания первичный герпес половых органов протекает длительно (5–7 недель). В течение первой недели происходит нарастание симптоматики, затем 2-3 недели стабилизация и обратное развитие, и 2-3 недели бессимптомное слущивание (отшелушивание) участков эпителия, пораженных вирусом. Продолжительность секреции вируса при первичной инфекции может составлять до 1 месяца.
Инкубационный период обычно от 2 до 10 суток, иногда до 3 недель. Симптомы развития заболевания появляются через 3–7 дней после попадания вируса на слизистые оболочки (преимущественно половым путем): первоначально появляется локальная эритема (сильное покраснение кожи), вслед за ней – герпетические пузырьки-везикулы.
Пузырьки лопаются, образуются небольшие изъязвления, заживающие в течение несколько дней без формирования рубца. Заболевание преимущественно ограничивается входными воротами вируса и нервной тканью, иннервирующей место инокуляции.
Первичное заражение может сопровождаться увеличением лимфоузлов (лимфаденопатией), зудом и жжением при мочеиспускания (дизурией), гиперемией. При первом эпизоде заражения возможно появление общих симптомов интоксикации (среди которых повышение температуры тела, головная боль, тошнота, недомогание, миалгия, нарушения сна).
У мужчин часто встречается уретрит, сопровождающийся болью при мочеиспускании. У женщин возможен эрозивный цервицит. Возможны выделения из мочеиспускательного канала или влагалища. Нередко встречаются неврологические симптомы, обусловленные поражением крестцовых нервов (задержка мочи, запоры, парестезии). Кроме того возможны лихорадка, недомогание, головная боль, светобоязнь и ригидность затылочных мышц.
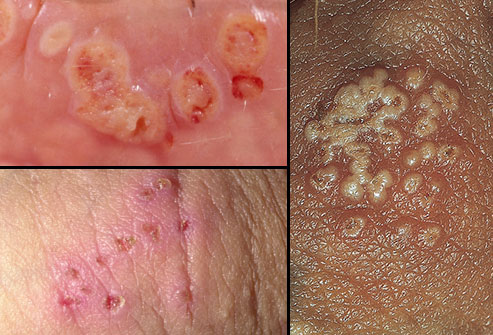
Непервичный герпес половых органов
Первый эпизод непервичного герпеса половых органов – это первый эпизод заболевания у больного, у которого на момент заболевания есть антитела к ВПГ другого типа. В большинстве случаев первый эпизод непервичного герпеса половых органов обусловлен ВПГ-2 при наличии антител к ВПГ- 1.
Первый эпизод непервичного герпеса половых органов характеризуется менее обильными высыпаниями по сравнению с первичным герпесом половых органов. В отсутствие лечения высыпания разрешаются в течение 10–14 суток. Общие симптомы при этом бывают редко. Паховый лимфаденит (воспаление паховых лимфоузлов) наблюдают редко. Выделения из мочеиспускательного канала, боль при мочеиспускании и неврологические симптомы также встречаются редко.
Рецидивирующая герпесвирусная инфекция
Герпесвирусная инфекция (ГИ) не может быть излечена полностью. Особенностью ВПГ является способность к латентному сохранению в организме после первичного инфицирования с последующей активацией и появлением клинических проявлений заболевания.
Рецидив герпеса половых органов – это второй и последующие эпизоды заболевания, обусловленные реактивацией ВПГ одного и того же типа. В большинстве случаев рецидив герпеса половых органов обусловлен ВПГ типа 2. У 90% инфицированных ВПГ-2, у которых первичный герпес или первый эпизод непервичиого герпеса проявлялся клинически, возникают рецидивы, которые также проявляются клинически.
Развитие и течение заболевания определяются состоянием иммунной системы больного. Состояние иммунодефицита увеличивает частоту рецидивов и тяжесть их протекания.
Реактивация герпетических вирусов из латентного состояния, происходящая после первичного инфицирования, проявляется при диссеминированной (генерализованной) и локализованной формах. Адекватный иммунологический ответ при этом может ограничивать инфекцию местом реактивации, а генерализованное заболевание с угрозой для жизни активно развивается на фоне иммунодефицитных состояний, особенно часто – у ВИЧ-инфицированных пациентов, реципиентов трансплантированных органов или у больных, получающих инвазивную противораковую терапию.
Рецидив герпеса половых органов характеризуется немногочисленными высыпаниями, обычно односторонними. Рецидивы, как правило, возникают на одном и том же месте. У многих больных за 1–2 суток до появления высыпаний отмечаются чувство пощипывания или жжения, покалывание, зуд, небольшие боли или чувство растяжения.
Эволюция элементов сыпи (узелок с покраснением – пузырек – гнойничок – язва – корочка) занимает 7–10 суток. Возможны атипичные язвенные высыпания. Паховый лимфаденит и неврологические симптомы бывают редко.
Бессимптомная герпесвирусная инфекция
Достаточно часто герпес половых органов (включая первичный, первый эпизод непервичного, рецидив) протекают бессимптомно, без пузырьков-везикул на коже и слизистых. При этом возможно истинное бессимптомное течение и течение с невыявленными или неправильно расцененными симптомами. У многих лиц с бессимптомным течением заболевания можно выявить минимальные или неспецифические симптомы, на которые больной не обращает внимания.
Бессимптомная инфекция встречается как у лиц, у которых никогда не было герпеса половых органов, так и у лиц, у которых уже был герпес половых органов.
- Инфекция, вызванная ВПГ-1,
- Инфекция, вызванная ВПГ-2 у лиц, инфицированных ВПГ-1,
- Нетипичная локализация (шейка матки),
- Половые особенности (у женщин чаще бессимптомные инфекции),
- Расовые отличия (у представителей негроидной расы герпес протекает легче),
- Наследственные факторы - определенные группы HLA (системы белков-антигенов).
Атипичный герпес половых органов
Выделяют атипичный герпес: в 20% всех случаев генитального герпеса специфические проявления герпетической инфекции скрыты симптоматикой сопутствующих местных инфекционных заболеваний (чаще всего кандидоза).
− рецидивирующие трещины слизистой оболочки наружных половых органов, которые самостоятельно эпителизируются в течение 4 - 5 дней;
− геморрагическая форма: единичные или множественные везикулезные элементы (пузырьки) с геморрагическим содержимым;
− абортивная форма: очаг поражения в виде зудящего пятна или папулы при отсутствии везикулезных элементов;
− субклиническая форма: кратковременное появление на слизистой оболочке наружных половых органов поверхностных трещинок, сопровождающихся незначительным зудом.
Адрес: г. Москва, Ленинский проспект, дом 82/2
Часы работы: Пн - Пт: с 10.00 до 20.00; Сб - Вс, праздники: с 11.00 до 18.00
Как нас найти (схема проезда):

Основным местом локализации первичной генитальной инфекции ВПГ у женщин является шейка матки. Чаще всего, герпетические поражения у женщин локализуются на больших и малых половых губах (68,6%), в области вульвы (41,8%), клитора (35,7%), влагалища и шейки матки (84,4%).
ВПГ был изолирован из шейки матки во время первичного заражения у 88—90 % женщин с первичной инфекцией ВПГ-2, которые имели везикулезную сыпь на наружных гениталиях, у 65 % — с повторным эпизодом инфекции ВПГ-2, и у 80 % женщин с ВПГ-1. Большинство (89 %) женщин, выделяющих вирус при первичном эпизоде заболевания, имели изменения на шейке матки.
Особенностью генитального герпеса (Herpes genitalis) женских половых органов является многоочаговость. В патологический процесс нередко вовлекаются нижний отдел мочеиспускательного канала, слизистая оболочка ануса и прямой кишки. Вовлечение в инфекционный процесс этих органов может происходить вторично, вслед за возникновением герпеса наружных гениталий, но может протекать и как изолированное поражение.
Рецидивирующая герпетическая инфекция (РГИ) может проявляться клиникой вульвовагинита и цервицита, вызывать поражения слизистой матки, труб и придатков. В 83,6 % случаев при стойких, не поддающихся терапии кольпитах, лейкоплакиях шейки матки выделяют вирус простого герпеса (ВПГ) как один из ведущих этиологических факторов заболевания.
По некоторым данным, в 66 % случаев у женщин герпетическая инфекция (ГИ) протекает атипично. Об имеющейся длительно текущей хронической ГИ можно говорить на основании особенностей клинического течения, наличия герпетического антигена в эпителиальных клетках вульвы, влагалища и периферической крови.
д) хронических часто рецидивирующих сальпингоофоритах (воспаление маточных труб и яичников) и эндометритах, не поддающихся стандартной антибактериальной терапии;
У 1–2% женщин, поступающих в гинекологическую клинику, независимо от основного заболевания, обнаруживают цитологические доказательства ВПГ-инфекции.
Герпес наружных половых органов у женщин
При рецидивирующем герпесе (РГ) наружных половых органов у женщин, очаг поражения находится в области наружных гениталий и перианальной области. Герпетические высыпания у женщин возникают на больших и малых половых губах, области лобка и промежности.
Типичная форма РГ наружных гениталий характеризуется ярко выраженными симптомами болезни, классическим развитием очага поражения (эритема, образование везикул, развитие эрозивно-язвенных элементов, эпителизация) и субъективными ощущениями (зуд, чувство жжения, болезненность, недомогание). проявляется повторяющимися пузырьковыми высыпаниями. Выраженная симптоматика позволяет врачам визуально поставить диагноз РГГ, своевременно назначить лечение и информировать больного об инфекционном характере заболевания и опасности заражения полового партнера.
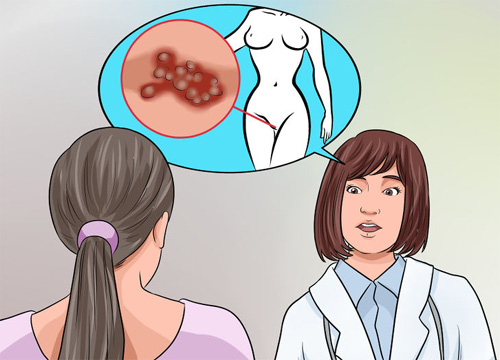
Герпес нижнего отдела урогенитального тракта, анальной области и ампулы прямой кишки
Поражение слизистых оболочек входа во влагалище, влагалища, влагалищной части шейки матки, цервикального канала, уретры, мочевого пузыря, анальной области и ампулы прямой кишки проявляется в двух клинических формах:
- очаговой, характеризующейся появлением типичных для простого герпеса слизистых оболочек везикулезно-эрозивных элементов,
- диффузной, при которой патологический процесс протекает по типу неспецифического воспаления.
Герпес верхнего отдела полового тракта (поражение матки, маточных труб).
Типичная клиническая картина герпетических поражений органов верхнего отдела мочеполового тракта проявляется симптомами неспецифического воспаления. Неспецифические герпетические поражения внутренних половых органов проявляются эндоцервицитом, эрозией шейки матки, вагинитом. Ряд авторов цервициты без наружных язв также относят к атипичным проявлениям ГГ.
Клинические проявления герпетических поражений внутренних половых органов не имеют специфических особенностей по сравнению с воспалительными процессами невирусной этиологии. Обычно больные предъявляют жалобы на выделения из влагалища, периодически появляющиеся боли в малом тазу, области проекции матки, яичников.
Герпетические поражения шейки матки
Герпетические поражения шейки матки могут носить типичный и нетипичный характер. В типичном варианте генитального герпеса – это всегда хорошо заметные множественные, довольно мелкие, с четкими границами округлые эрозии; высыпные элементы быстро минуют везикулярную стадию, в которой, кстати, эти элементы плохо различимы без применения кольпоскопии. Проблема причастности ВПГ к развитию нетипичных герпетических изменений слизистой шейки матки в настоящее время находится в стадии исследований.
При кольпоскопии в острый период герпетической инфекции шейки матки определяют изъязвление с неровными краями с сукровицей в области дна. Эволюция этого поражения идет от изъязвления с красным дном к простой эрозии до полного исчезновения в течение 3-х недель. К предшествующим изменениям относят маленькие буллезные образования, затем округлые микроэрозии с последующим формированием простых красных пятен, которые похожи на местный пятнистый кольпит.
Исследования показали, что выделение ДНК ВПГ с поверхности эрозии шейки матки в 60 % случаев сопровождается репликативной фазой ГИ (репликация и сборка вирусных частиц в инфицированных клетках). При эрозии и дисплазии шейки матки ВПГ-2 выявляется в 27,2% случаев непосредственно в соскобах со слизистой цервикального канала и сопровождается повышением титра специфических иммуноглобулинов в крови до диагностических уровней.
Особое значение влияние герпетической инфекции на состояние эпителия шейки матки имеет у женщин, длительно принимающих оральные гормональные контрацептивы. Известно, что длительный прием комбинированных стероидов в той или иной мере усиливает процессы плоскоклеточной метаплазии, а также может вызывать эффект эндоцервикальной гиперплазии, причем этот эффект в случае его развития наблюдается как в эпителии цервикального канала, так и в участках псевдоэрозии на фоне эктропиона, в полипах слизистой цервикального канала. В связи с этим прием оральных комбинированных контрацептивов может являться кофактором в развитии рака шейки матки, особенно в сочетании с герпетической инфекцией.
Герпетический цервицит
Герпетический цервицит – это воспалительный процесс, вызванный ВПГ. Для клинических проявлений герпетического цервицита характерно разнообразие проявлений — от легкой гиперемии с небольшим количеством эрозий до тяжелого некротического поражения (под эрозией шейки матки понимают дефект эпителия в результате воспаления). Цервицит диагностируется у 70-90% женщин с герпетическим поражением половых органов. Шейка матки при герпетическом эндоцервиците отечна, часто имеет эрозии, легко кровоточит при манипуляциях.
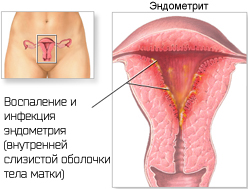
Герпетический эндометрит
Эндометрит — это воспаление внутренней (слизистой) оболочки матки (эндометрия) с поражением как функционального, так и базального слоя. Эндометрит, вызванный вирусом простого герпеса, является следствием длительной персистенции (существования) вируса в эндометрии. Герпетический эндометрит, как правило, возникает при атипичном или бессимптомном течении ГГ, типичная форма отмечается редко (~20% случаев). Клинические симптомы при вирусном поражении эндометрия чаще всего отсутствуют или проявляются нетипично, что приводит к ошибкам в диагностике и позднему началу лечения.
При герпетическомпоражении ткани нарушаются факторы местного и общего иммунитета, целостность поверхности эпителия, что приводит к созданию благоприятных условий для развития других инфекционных процессов .
Клинически герпетический эндометрит чаще проявляется во второй фазе менструального цикла или во время беременности, что, возможно, обусловлено повышением уровня простагландинов в этот период или супрессией Т-клеточного звена иммунитета, способствующих реактивации ВПГ, персистирующего в эндометрии. Субклиническая латентная внутриматочная герпетическая инфекция является важным фактором невынашивания беременности. Эндометриты ВПГ-этиологии встречаются нечасто, но эти заболевания очень опасны и могут вызвать гибель женщины и плода.
Герпес уретры и мочевого пузыря (герпетический уретрит)
Герпетический уретрит у женщин субъективно проявляется болями и резями в начале мочеиспускания, частыми позывами к мочеиспусканию. У 4,8% женщин имеет место очень болезненное мочеиспускание, или задержка мочеиспускания в результате инфекции уретры и слизистой оболочки мочевого пузыря. Нормализация функции мочевого пузыря у больных с задержкой мочеиспускания обычно происходит в течение 6–10 дней.
При осмотре наблюдаются гиперемия наружного отверстия уретры, наличие скудных слизистых выделений; при уретроскопии в передней части уретры иногда удается обнаружить мелкие поверхностные эрозии, катаральное воспаление.
Герпетический цистит
Ведущими симптомами герпетического цистита являются цисталгия, появление болей в конце мочеиспускания, дизурические явления. При герпетическом цистите появляются гематурия (кровь в моче), появление болей в конце мочеиспускания, боли в области мочевого пузыря. У женщины это может быть первым и единственным признаком ВПГ-инфицирования мочеполовой сферы. Он нередко возникает в первые 1-3 месяца после начала половой жизни или после смены полового партнера.
Герпес анальной области и прямой кишки
Очаг поражения в анальной области обычно представляет собой рецидивирующую трещину, что нередко является поводом для диагностических ошибок. Такие больные с ошибочным диагнозом "трещина заднего прохода" попадают к хирургам. Зудящая форма герпеса ануса и герпетическое поражение геморроидальных узлов, также трудны для диагностики.
Поражение анальной области может возникнуть первично как самостоятельное заболевание или вторично – в результате затекания отделяемого влагалища и мацерации слизистой оболочки ануса при наличии у пациентки герпетического кольпита, сопровождающегося обильной экссудацией.
При поражении сфинктера и слизистой оболочки ампулы прямой кишки (герпетический проктит) больных беспокоят зуд, чувство жжения и болезненность в очаге поражения, возникают мелкие эрозии в виде поверхностных трещин с фиксированной локализацией, кровоточащие при дефекации. При ректоскопии определяется катаральное воспаление, иногда эрозии.
Герпес внутренних гениталий - субклиническая и бессимптомная формы.
Для субклинической формы герпеса внутренних гениталий (влагалища, матки, яичников и т.д.) типично отсутствие у пациентки жалоб, иногда имеются указания на периодически появляющиеся необильные слизистые выделения из влагалища. При гинекологическом осмотре симптомы воспаления не выявляются. При динамическом лабораторном исследовании мазков отделяемого канала шейки матки, влагалища и уретры периодически выявляется повышенное количество лейкоцитов (до 200–250 и выше в поле зрения), свидетельствующее о наличии воспалительного процесса. При вирусологическом исследовании мазков методом иммунофлюоресценции в лейкоцитах определяется антиген ВПГ.
Бессимптомная форма герпеса внутренних гениталий характеризуется отсутствием у больных каких-либо жалоб на половую сферу, объективных клинических данных, подтверждающих воспаление. При лабораторном исследовании отделяемого урогенитального тракта выделяется ВПГ, в то время как в мазках признаков воспаления (лейкоцитоза) нет. Бессимптомная форма герпеса внутренних гениталий выявляется у 20–40% женщин, страдающих РГГ ягодицы и бедра. Это важное обстоятельство необходимо учитывать при планировании беременности у женщин с этой формой РГГ в связи с существующей вероятностью развития во время беременности осложнений ВПГ-инфекции.
Согласно данным литературы, у 83,6% женщин, страдающих не поддающимися терапии кольпитами и лейкоплакией шейки матки, ВПГ является одним из факторов заболевания. Доказано, что ВПГ может быть причиной развития эндометрита и сальпингоофорита.
Герпетический вульвовагинит
У женщин часто встречаются герпетический вульвовагинит, особенностью течения которого является нередкое присоединение отека пораженной области. Вирус герпеса могут изолированно поражать вульву и влагалище. Заражение происходит от больных. Герпетический вульвовагинит проявляется мелкими пузырьками на гиперемированной вульве. Пузырьки содержат прозрачную, а при присоединении вторичной инфекции — гнойную жидкость. Через 5—7 дней пузырьки вскрываются с образованием эрозий и язвочек, которые покрываются струпом. В начале заболевания выражены жжение, боли и зуд в области вульвы. Общие симптомы включают головную боль, озноб, повышение температуры тела.
Генитальный герпес во время беременности
Заболевание ВПГ женщин во время беременности может явиться причиной гибели плода, мертворождения, преждевременных родов. Герпесвирусы вызывают до 30% спонтанных абортов на ранних сроках беременности и свыше 50% поздних выкидышей, занимают второе место после вируса краснухи по тератогенности (развитие уродств плода).
Тяжелейшие формы неонатального герпеса развиваются при инфицировании новорожденного вирусом простого герпеса в родах. При первичном ГГ у матери инфицируется от 30% до 80% детей, при рецидивирующем герпесе – 3–5%. Инфицирование плода во время родоразрешения, если у матери в конце беременности имели место герпетические высыпания, происходит у 50% женщин, больных РГГ; при этом у 60–80% инфицированных детей развивается энцефалит.
Герпес менструальный
Менструальный герпес — это генитальный герпес (ГГ) с монотонным типом рецидивирования и тяжелым течением, характеризующийся ежемесячными обострениями инфекционного процесса до, во время или после менструации. Такое течение заболевания может стать для женщины сильнейшим психотравмирующим фактором, ограничивающим ее социальную активность и снижающим качество жизни.
Этот вариант ГИ является сложным для лечения. Поэтому разработка адекватных и эффективных способов лечения и профилактики рецидивов у больных с данными формами ГГ остается актуальной. Европейские стандарты лечения пациенток предусматривают длительную (годами) супрессивную терапию противовирусными препаратами , что не исключает повторного рецидирования ГГ и бессимптомного вирусовыделения, появления побочных эффектов и резистентности вирусов герпеса к лекарственной терапии.
Читайте также:

