Поражении шейки матки вирусом папилломы человека лечение
Обновлено: 06.05.2024
- КЛЮЧЕВЫЕ СЛОВА: шейка матки, вирус папилломы человека, скрининг, предраковое поражение, дииндолилметан, Эпигаллат, Индинол Форто, Цервикон-ДИМ
Инфицирование вирусом папилломы человека (ВПЧ) высокого онкогенного риска запускает механизм трансформации клеток слизистой оболочки и приводит к развитию рака шейки матки (РШМ). Ежегодно в мире диагностируется около 570 000 новых случаев этого злокачественного новообразования. Рост заболеваемости за последние десять лет составил 7,8%, смертности – 13,1%. Примерно в 60% случаев РШМ выявляется у женщин старше 45 лет и в 20% – у женщин старше 65 лет.
Последние годы наблюдается тенденция к росту частоты выявления РШМ в молодой популяции (шесть-семь новых случаев) и пожилой популяции – 17 случаев на 100 тыс. женщин 1 . Пик заболеваемости цервикальным раком приходится на возраст 40–49 лет. Не случайно основной целью глобальной стратегии Всемирной организации здравоохранения (ВОЗ) на период 2020–2030 гг. по ликвидации РШМ стало снижение уровня смертности от данного заболевания. В перспективе порог заболеваемости должен составлять четыре случая рака шейки матки на 100 тыс. женщин в год. Перед мировым здравоохранением поставлены задачи, которые необходимо выполнить к 2030 г. 2 :
- 90% девочек должны быть вакцинированы против ВПЧ к 15 годам;
- 70% женщин должны проходить скрининг с помощью высокопроизводительного теста к 35 годам, а затем к 45 годам;
- 90% женщин с заболеваниями шейки матки (предраком и инвазивным раком) должны получать соответствующее лечение.
Эксперты ВОЗ рекомендуют комплексный подход к профилактике РШМ и борьбе с ним. При этом алгоритм действий предусматривает наблюдение за здоровьем женщины на протяжении всей жизни. Так, в целях первичной профилактики РШМ предусмотрено не только проведение вакцинации против ВПЧ, но и информирование детей 9–14 лет о пользе здорового образа жизни, половое воспитание с учетом возраста и культуры, пропаганда использования презервативов. В свою очередь вторичная профилактика – скрининг РШМ у женщин старше 30 лет позволяет выявлять предраковые поражения на стадии, на которой они легко поддаются лечению.
Течение ВПЧ-инфекции зависит от состояния иммунной системы и может быть транзиторным, латентным и персистирующим. Около 90% случаев инфицирования ВПЧ остаются незамеченными в течение двух лет, и лишь у 10% женщин отмечается персистенция инфекции. Для персистирующей ВПЧ-инфекции характерно выявление типоспецифической ДНК ВПЧ при повторном взятии образца через 6–12 месяцев. Риск развития предракового поражения шейки матки повышен именно у женщин с персистирующим ВПЧ.
У женщин в возрасте 30–35 лет опасность персистенции ВПЧ увеличивается в десять раз по сравнению с женщинами более молодого возраста. Наиболее высокий риск персистенции ВПЧ и цервикальной интраэпителиальной неоплазии (cervical intraepithelial neoplasia – CIN) наблюдается у женщин в возрасте старше 50 лет, имеющих сексуальные отношения с молодыми мужчинами 3 .
Транзиторная (эписомальная) форма ВПЧ нередко встречается у молодых женщин. Различают транзиторную форму со стойким отрицательным ответом – вирус исчезает через 12 месяцев и нестойким отрицательным ответом – через 12 месяцев вирус сохраняется в отсутствие поражения шейки матки.
Латентная форма носительства ВПЧ характеризуется персистенцией в течение двух и более лет без изменений шейки матки. Эта форма опасна непрогнозируемым риском трансформации в дисплазию шейки матки. Интегративная форма существования ВПЧ – интеграция клеточной ДНК, сопровождающаяся тяжелым поражением шейки матки.
Транзиторная форма с нестойким отрицательным ответом относится к малым формам поражения шейки. При ВПЧ-инфекции они отличаются длительной персистенцией при нормальных цитологических результатах. Малые формы поражения шейки матки могут реализоваться в появлении атипичных клеток – дисплазии низкой LSIL (low grade SIL) и высокой HSIL степени (hight grade SIL) к концу второго года наблюдения.
У многих молодых женщин возможна самоэлиминация ВПЧ в течение двух лет. Тем не менее в 10% случаев за тот же период может наблюдаться прогрессирование до диспластических изменений цервикального эпителия второй степени (CIN II) и более. Обнаружение ВПЧ в отсутствие клинических или субклинических проявлений инфекции ассоциируется с 250-кратным увеличением риска развития РШМ 4 . В связи с этим необходимо своевременно выявлять носительство онкогенных типов ВПЧ и начинать лечение до развития предраковых поражений шейки матки.
К факторам риска персистенции ВПЧ относят:
- тип и онкогенность вируса;
- раннее начало половой жизни;
- наличие более пяти партнеров;
- паритет (количество рожденных детей) и юный возраст при рождении первого ребенка;
- наличие других инфекций, передаваемых половым путем, бактериальный вагиноз, хронические воспалительные заболевания;
- игнорирование барьерной контрацепции;
- курение;
- альтернативные виды секса;
- частые внутриматочные вмешательства;
- вторичный иммунодефицит.
Может ли CIN, ассоциированная с ВПЧ, регрессировать самостоятельно? Установлено, что дисплазия слабо выраженной степени (CIN I) регрессирует в 57% случаев, в 32% – персистирует, но инвазивный рак развивается в 1% случаев. При CIN II регрессия наблюдается в 43% случаев, персистенция – в 35%. В 22% случаев патологический процесс прогрессирует, причем инвазивный рак формируется у 5% женщин. Даже у женщин с CIN III, которая считается абсолютным предраковым состоянием, в 32% случаев возможна регрессия. HSIL – CIN II и CIN III развивается, как правило, в течение трех лет с момента инфицирования у 27% женщин 5 .
Таким образом, можно выделить два ключевых момента, связанных с ВПЧ и воспалением, – исходное наличие воспалительного процесса в шейке матки и активацию воспалительного процесса на фоне дисплазии. Данные процессы взаимосвязаны: ВПЧ способствует воспалению, воспаление – прогрессированию ВПЧ. Возникает состояние, которое называется ВПЧ-ассоциированным цервицитом. ВПЧ-ассоциированный цервицит характеризуют упорное течение с низкой эффективностью стандартных методов лечения, высокая частота дисбиотических состояний влагалища. В 30% случаев заболевание сопровождается формированием острых кондилом. При ВПЧ-ассоциированном цервиците обнаруживается сочетанная ВПЧ-инфекция из двух-трех вирусов с доминированием ВПЧ 16-го типа, а также нетяжелые атипические изменения эпителия у 19% и умеренные у 4,5% женщин 7 .
В настоящее время хорошо известно, что в развитии неопластических процессов в тканях шейки матки участвуют метаболиты эстрогенов. ВПЧ негативно влияет на обмен эстрадиола в клетках эпителия шейки матки. В норме концентрация метаболита эстрогена 2-гидрокисэстрона (2-ОНЕ1) превышает концентрацию 16-гидроксиэстрона (16-ОНЕ1). При персистенции ВПЧ в цервикальном эпителии образуется аномально высокое количество 16-альфа-ОНЕ1, что усиливает клеточную пролиферацию. Накопление же 4-гидроксиэстрона (4-ОНЕ1) на фоне ВПЧ вызывает перерождение клеток-мишеней, приводя к развитию злокачественных новообразований 8 .
Сегодня активно изучается новая концепция развития РШМ – поражение стволовых клеток в области зоны трансформации, которое приводит к быстрому прогрессированию злокачественного процесса. ВПЧ поражает полипотентные стволовые клетки под цилиндрическим эпителием эктопии, в формирующейся зоне трансформации с ее верхней границей – переходной зоной, а также в расположенном выше канале и эндоцервикальных криптах. Поэтому при поражении ВПЧ стволовых клеток быстро формируется CIN II и III, и в течение одного года или двух лет развивается РШМ.
Для диагностики патологии шейки матки используют:
- цитологическое исследование;
- ВПЧ-тестирование;
- молекулярные маркеры;
- кольпоскопическое исследование.
Биопсия и выскабливание цервикального канала обязательны при наличии цитологических и кольпоскопических признаков атипичного эпителия.
В России рекомендовано проведение скрининга для выявления патологии шейки матки. Цитологическое исследование женщинам в возрасте 21–29 лет выполняется один раз в три года, цитологический скрининг и ВПЧ-тестирование в возрасте 30–65 лет – один раз в пять лет или только цитология – ежегодно после 40 лет.
Согласно рекомендациям Американского общества кольпоскопии и патологии шейки матки и 24 международных сообществ, женщинам с выявленным ВПЧ проводят цитологический скрининг с 21 года. Существует два подхода к наблюдению за пациентками с CIN: консервативное с цитологическим исследованием, обследованием на ВПЧ, выполнением кольпоскопии и биопсии шейки матки и проведение эксцизионных процедур или аблации переходной зоны. Как правило, консервативное наблюдение рекомендуется женщинам до 24 лет, даже при наличии CIN II 10 .
По мнению российских экспертов, у молодых женщин и/или планирующих беременность пациенток с морфологически подтвержденным диагнозом LSIL (признаки ВПЧ-инфекции, койлоцитоз, CIN I) также предпочтительна выжидательная тактика с динамическим наблюдением за состоянием шейки матки в течение 18–24 месяцев в виде цитологического контроля один раз в шесть месяцев и ВПЧ-тестирования один раз в 12 месяцев. Хирургическое лечение проводится в отсутствие регрессии через 18–24 месяца.
У женщин до 25 лет с диагнозом CIN II в биоптате при р16-негативном результате иммуногистохимического исследования допустимо динамическое наблюдение с использованием цитологического контроля, ВПЧ-тестирования и кольпоскопии один раз в шесть месяцев в течение двух лет.
Женщинам старше 40 лет с CIN I в биоптате эктоцервикса целесообразно проводить петлевую эксцизию зоны трансформации 11 .
Таким образом, консервативное лечение показано:
- женщинам с малыми формами поражений ВПЧ – латентной персистирующей инфекцией, которая не исчезает через 12 месяцев персистенции;
- молодым женщинам с выявленными клетками плоского эпителия с атипией неясного значения (ASCUS), CIN I, CIN II шейки матки при p16-негативном или слабоположительном результате;
- пациенткам с хроническим цервицитом бактериальным или ВПЧ-ассоциированным;
- после хирургического лечения CIN II и CIN III для профилактики рецидива.
На сегодняшний день наиболее эффективными в терапии ВПЧ-ассоциированных поражений шейки матки признаны лекарственные средства, регулирующие работу эпигенетических механизмов. К таким препаратам относят дииндолилметан (Цервикон-ДИМ), эпигаллокатехин-3-галлат (Эпигаллат), индолкарбинол (Индинол Форто). Целесообразно также добавление к диете биологически активной добавки (БАД) Промисан, содержащей индол-3-карбинол и эпигаллокатехин-3-галлат.
Указанные препараты обладают уникальными свойствами. Они воздействуют на основные звенья патогенеза диспластических процессов шейки. На фоне эпигенетической терапии препаратами на основе индол-3-карбинола, дииндолилметана, а также БАД, содержащей эпигаллокатехин-3-галлат, при цервиците, ассоциированном с ВПЧ, происходят избирательный апоптоз и элиминация вирус-инфицированных клеток, тормозится образование агрессивных метаболитов эстрадиола, вследствие чего блокируется переход вирус-инфицированных клеток в злокачественные. Кроме того, блокируется синтез вирусного онкобелка Е7, восстанавливается активность эндогенного интерферона и повышается чувствительность к экзогенному интерферону. Восстанавливаются функциональные возможности иммунной системы шейки матки и влагалища. Эпигенетическая терапия также способствует деметилированию генов пролиферации и противоопухолевой защиты, блокаде стволовых опухолевых клеток.
В многочисленных исследованиях доказана прямая противомикробная и противовирусная активность эпигаллокатехин-3-галлата (активного компонента БАД Эпигаллат) в отношении широкого спектра возбудителей, таких как Staphylococcus aureus, Chlamydia trachomatis, Mycoplasma, Escherichia coli, герпесвирусы, аденовирусы, энтеровирусы, вирусы гепатита и гриппа. Кроме того, в последних публикациях сказано, что эпигаллокатехин-3-галлат способствует подавлению пролиферации клеток рака шейки матки, блокированию ангиогенеза 12 .
При ВПЧ-ассоциированном цервиците и CIN рекомендовано использование эпигаллокатехин-3-галлата в качестве БАД в комбинации с препаратом дииндолилметана для интравагинального введения Цервикон-ДИМ.
Лекарственный препарат Цервикон-ДИМ на основе метаболита действующего вещества индол-3-карбинола – дииндолилметана разработан для безопасной и эффективной терапии диспластических заболеваний шейки матки. Цервикон-ДИМ стимулирует апоптоз и ускоряет элиминацию инфицированных ВПЧ и трансформированных клеток, нормализует метаболизм эстрадиола в ВПЧ-инфицированных клетках, усиливает неспецифический иммунный ответ на инфекцию. Цервикон-ДИМ непосредственно воздействует на патогенез CIN и препятствует опухолевой трансформации. Дииндолилметан относится к практически нетоксичным препаратам. При интравагинальном применении Цервикон-ДИМ демонстрирует высокую местную биодоступность, при этом он практически не попадает в системный кровоток. Показанием для применения препарата Цервикон-ДИМ является лечение дисплазии (CIN) шейки матки независимо от результатов выявления папилломавирусной инфекции методом полимеразной цепной реакции. Использование препарата Цервикон-ДИМ оправданно и в случае субклинического течения ВПЧ-инфекции для профилактики развития CIN шейки матки.
Цервикон-ДИМ применяют интравагинально по 100 мг два раза в сутки, длительность курса – 3–6 месяцев. Продолжительность курса лечения определяется динамикой клинико-лабораторных показателей.
Эффективность препарата Цервикон-ДИМ подтверждена в клинических исследованиях. Так, в многоцентровом рандомизированном плацебоконтролируемом двойном слепом исследовании на фоне применения дииндолилметана в виде интравагинальных суппозиториев в дозе 200 мг (100 мг два раза в сутки) у пациенток с CIN I–II в течение 180 дней наблюдалась полная регрессия CIN 13 .
Назначая эпигенетическую терапию женщинам с ВПЧ-инфекцией, врач должен учитывать такой важный момент, как наличие дисбиоза влагалища или бактериального вагиноза. Установлена тесная взаимосвязь между инфекцией ВПЧ и обогащением бактериями. В частности, бактерии рода Sneathia ассоциируются с новообразованиями шейки матки, бактерии рода Prevotella – со стойкой инфекцией ВПЧ 14 .
Дисбиоз и бактериальный вагиноз приводят к увеличению восприимчивости к инфекции ВПЧ шейки матки, вирусной адгезии, инвазии ВПЧ в геном клетки, прогрессированию CIN. Не случайно лечение бактериального вагиноза связывают с лучшим исходом поражений шейки матки 15 .
При бактериальном вагинозе, трихомонадном и кандидозном вагините, смешанных вагинальных инфекциях применяют препарат Нео-Пенотран Форте. Суппозитории препарата Нео-Пенотран Форте содержат метронидазол, характеризующийся антибактериальным и противотрихомонадным эффектами, и миконазол, оказывающий противогрибковое действие.
В исследовании микробиологические показатели излечения на фоне терапии препаратом Нео-Пенотран Форте были получены в 100% случаев для трихомониаза, в 96,2% – для бактериального вагиноза и 90% – для кандидоза. При смешанных инфекциях общий микробиологический показатель излечения достиг 92%.
Применение препарата Нео-Пенотран Форте, содержащего метронидазол и миконазол, считается клинически доказанным медицинским подходом к лечению вагинальных инфекций с точки зрения эффективности и скорости достижения результата.
Итак, терапевтическое действие препарата Цервикон-ДИМ при дисплазии шейки матки можно усилить предварительным лечением бактериального вагиноза, совместным применением БАД Эпигаллат и иммуномодуляторов.
В частности, лечение ВПЧ-ассоциированного цервицита с CIN I на первом этапе предполагает проведение антибактериальной терапии (амоксициллин/клавуланат и джозамицин) и назначение БАД Эпигаллат 270 мг три раза в день. При наличии бактериального вагиноза или кольпита показана терапия препаратами Нео-Пенотран или Гайномакс в сочетании с пробиотиками. На втором этапе лечения к БАД Эпигаллат добавляют интравагинальный препарат Цервикон-ДИМ по одной свече два раза в сутки в течение трех месяцев. При CIN II у молодых женщин терапию препаратом Цервикон-ДИМ целесообразно сочетать с Эпигаллатом и Полиоксидонием. Как известно, Полиоксидоний воздействует на все звенья иммунитета, в том числе эффективен при наличии ВПЧ-инфекции.
Таким образом, тактика ведения пациенток с поражением шейки матки, ассоциированным с ВПЧ, должна быть комплексной с применением средств эпигенетического действия.
Что такое папилломавирусная инфекция (ВПЧ)? Причины возникновения, диагностику и методы лечения разберем в статье доктора Борисова Э. В., гинеколога со стажем в 35 лет.
Над статьей доктора Борисова Э. В. работали литературный редактор Юлия Липовская , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Папилломавирусная инфекция — это состояние, развивающееся при заражении какой-либо разновидностью вируса папилломы человека (ВПЧ). Возбудители данной группы могут существовать только в человеческом организме, поражая кожу и слизистые оболочки, приводя к появлению папиллом, бородавок, плоских и остроконечных кондилом. [1] [2] [4]
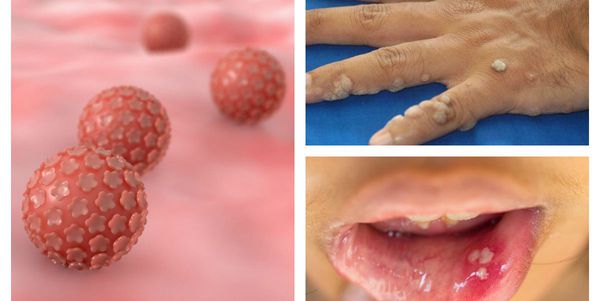
ВПЧ довольно широко распространён в человеческой популяции, особенно среди сексуально активных людей, а это свыше 80% всего населения. До недавнего времени вирусы этой группы считались относительно безобидными, вызывающими лишь косметические дефекты, но последние научные исследования показывают, что проблема гораздо серьёзнее. [9]
На сегодняшний день науке известно несколько сотен штаммов (типов) папилломавирусов . Около 40 из них преимущественно поражают аногенитальную область и передаются половым путём. Особую опасность представляют штаммы высокого онкогенного риска, так как они могут спровоцировать развитие онкологических заболеваний, в том числе рака шейки матки.
Чаще всего заражение происходит в молодом возрасте, как правило, с началом половой жизни, при этом возможно неоднократное инфицирование. Наиболее уязвимой группой в плане вероятности заражения ВПЧ и развития неблагоприятных последствий являются молодые женщины в возрасте 15-30 лет.
Помимо этого ВПЧ может перейти от инфицированной матери к ребёнку, например, при родах. Не исключается и контактно-бытовой способ передачи возбудителя, например, при соприкосновениях и даже при совместном использовании предметов личной гигиены.
К факторам риска, способствующим заражению ВПЧ, развитию хронической папилломавирусной инфекции и её переходу в предраковые состояния с потенциальным перерождением в злокачественную опухоль, относятся:
- иммунодефицит любого происхождения, в том числе вследствие ВИЧ-инфекции, лучевых поражений, применения иммунодепрессантов при трансплантации органов и тканей, лечения цитостатиками и других причин;
- подавленное состояние иммунитета во время беременности;
- раннее начало половой жизни;
- частая смена половых партнёров, незащищённый секс;
- инфицированность высокоонкогенными штаммами ВПЧ;
- заражение одновременно несколькими типами ВПЧ;
- наличие других инфекций, передающихся половым путём, например, герпесвирусной и цитомегаловирусной инфекции, вируса Эпштейна — Барр, гепатитов В и С, гонореи и трихомониаза;
- стресс, истощение, гиповитаминоз, гормональный дисбаланс;
- многократные роды и аборты;
- тяжёлые хронические заболевания, в том числе сахарный диабет;
- вредные привычки (курение, злоупотребление спиртным);
- низкий социальный статус, плохие условия жизни, неудовлетворительная интимная гигиена;
- пренебрежение регулярными профилактическими обследованиями (один из важнейших факторов риска);
- низкий уровень развития медицины в регионе проживания.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы папилломавирусной инфекции
Далеко не всегда человек догадывается о наличии в своём организме папилломавирусной инфекции, оставаясь при этом источником заражения для потенциальных партнёров. [1] [2] Дело в том, что заболевание может долгое время протекать бессимптомно: вирус скрыто существует в организме от нескольких месяцев до нескольких лет, никак себя не проявляя. Кроме того, уже имеющиеся проявления инфекции не всегда доступны для наружного обзора. Например, если папилломы, бородавки и кондиломы на открытых участках тела и поверхности гениталий ещё можно заметить самостоятельно, то патологические изменения, локализующиеся на шейке матки, сможет обнаружить только специалист в ходе осмотра с применением соответствующих инструментов.
И всё же существует несколько симптомов, которые прямо или косвенно могут указывать на наличие папилломавирусной инфекции и её неблагоприятных последствий. [3] К ним относятся:
- появление на коже и/или слизистых оболочках каких-либо разрастаний различных форм (на тонкой ножке или с широким основанием, нитевидной, округлой или плоской конфигурации, в форме цветной капусты или петушиного гребня) и размеров (от образований в несколько миллиметров до разрастаний, занимающих всю промежность);
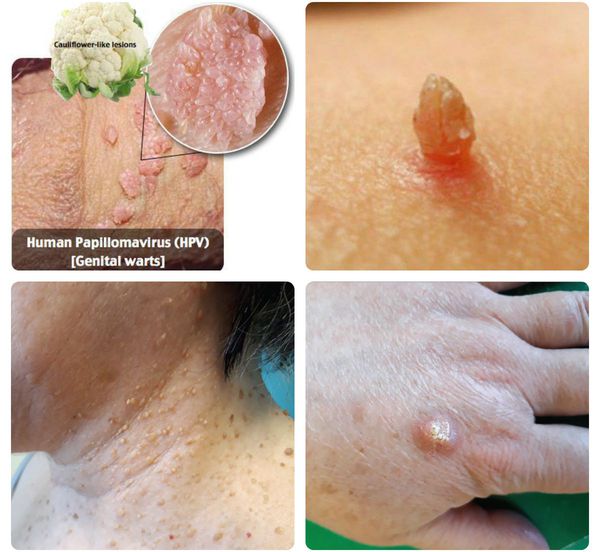
- отёчность и воспалительная инфильтрация папилломатозных разрастаний (остроконечных кондилом), их ранимость и кровоточивость, что приводит к присоединению вторичной инфекции с появлением гнойного отделяемого с неприятным запахом;
- зуд, жжение, мокнутие в области промежности, появление обильных белей, даже при отсутствии видимых патологических образований;
- межменструальные кровянистые выделения, в том числе появляющиеся в результате полового контакта:
- дискомфорт во время полового акта.
Наиболее тревожными признаками заболевания являются:
- постоянные боли в области спины и таза;
- слабость;
- беспричинная потеря веса;
- опухание одной или обеих ног.
Патогенез папилломавирусной инфекции
Заражение папилломавирусной инфекцией происходит при попадании вирусных частиц на кожу или слизистую оболочку. [1] [2] Излюбленная локализация инфекции на теле женщины — промежность, большие и малые половые губы, вульва, влагалище и шейка матки, у мужчин — половой член. Может также произойти поражение слизистой полости рта, пищевода, мочевого пузыря, трахеи, конъюнктивы и других органов и тканей.
Заражению способствуют микротравмы и потёртости. Особенно благоприятные для инфицирования условия создаются при половом акте. В 60–80% случаев достаточно однократного сексуального контакта с больным папилломавирусной инфекцией или бессимптомным носителем ВПЧ. К развитию заболевания может привести попадание в организм буквально единичных вирусных частиц.
При наличии предрасполагающих факторов (микроповреждения, слабого иммунитета и других) возбудитель проникает в эпителиальную ткань до её базального слоя. Там он прикрепляется к оболочке незрелой клетки и внедряется сначала в её цитоплазму, а затем и в ядро, где повреждает генетический аппарат. После этого начинается деление клеток с изменённым геномом, что приводит к появлению в месте внедрения вируса генитальных кондилом (образований, которые постепенно разрастаются), а, например, на шейке матки — к развитию диспластических процессов различной степени тяжести (дисплазия шейки матки).
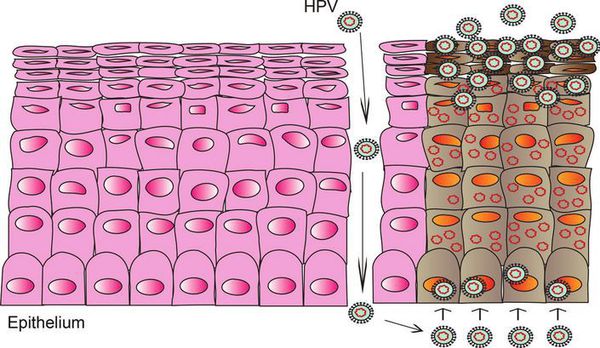
В случае ВПЧ высокого онкогенного риска определённые гены в вирусной ДНК кодируют синтез специфических белков-онкопротеинов (Е6 и Е7), которые подавляют противораковую защиту клеток. Под действием онкопротеинов нарушается стабильность генома клеток, стимулируется их размножение и снижается способность к дифференцировке — всё это со временем может привести к онкопатологии. [12]
Формирование новых полноценных вирусных частиц, способных инфицировать другого человека, происходит уже не в базальном, а в самых поверхностных слоях поражённого эпителия. Возбудитель может содержаться в слущивающихся отмирающих клетках, которые отделаются слизистой оболочкой. Таким образом они переходят к новому хозяину при тесном (сексуальном или бытовом) контакте.
Классификация и стадии развития папилломавирусной инфекции
По способности индуцировать развитие злокачественных новообразований ВПЧ подразделяют на четыре группы: [8]
- неонкогенные штаммы ВПЧ (типы 1-5);
- ВПЧ низкого онкогенного риска (типы 6, 11, 40, 42-44, 54, 61, 70, 72, 81);
- ВПЧ среднего онкогенного риска (типы 26, 31, 33, 35, 51-53, 58, 66);
- ВПЧ высокого онкогенного риска (типы 16, 18, 39, 45, 56, 59, 68, 73, 82).
Клинические формы папилломавирусной инфекции: [5]
- латентная — скрытая форма, не имеющая клинических и морфологических признаков, но обнаруживаемая иммунохимическими и молекулярно-биологическими методами;
- субклиническая — возникает у лиц с нормальным иммунитетом, определяется только специальными диагностическими методами (пробы с растворами-индикаторами, гистологические и цитологические исследования);
- манифестная — появляется у лиц с временным или стойким снижением иммунитета, в случае генитальной папилломавирусной инфекции характеризуется появлением кондилом.
Латентная инфекция может переходить в субклиническую и манифестную форму в случае возникновения предрасполагающих условий (факторов риска), но чаще всего она протекает бессимптомно, не манифестируя.
Клинические проявления папилломавирусной инфекции:
- кожные поражения: подошвенные, плоские и обычные (вульгарные) бородавки, бородавчатая эпидермодисплазия, бородавки Бютчера и небородавчатые поражения кожи;
- поражения слизистых оболочек гениталий: кондиломы, некондиломатозные поражения, карциномы;
- поражения слизистых вне гениталий: папилломатоз гортани, карциномы шеи, языка и другое.
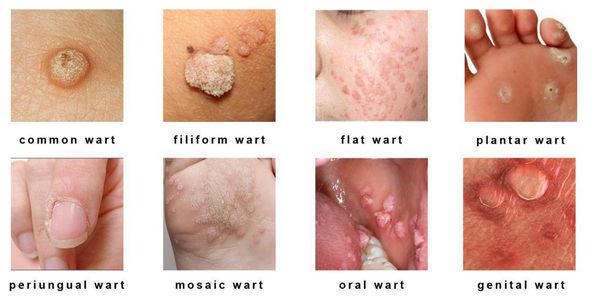
Разновидности поражений:
- экзофитные — видимые разрастания в виде папиллом и бородавок;
- эндофитные — образования, располагающиеся в толще ткани, которые не видны невооружённым глазом.
Осложнения папилломавирусной инфекции
Основными наиболее опасными осложнениями папилломавирусной инфекции являются злокачественные новообразования. Но возможны и другие серьёзные последствия:
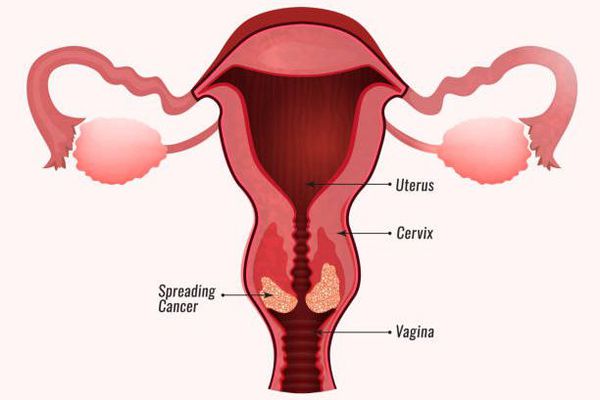
- Злокачественные новообразования заднего прохода, вульвы, полового члена и ротоглотки. Повышение риска их развития также связывают с высокоонкогенными штаммами ВПЧ. [6]
- Остроконечные кондиломы на гениталиях, папилломатоз верхних дыхательных путей (рецидивирующий респираторный папилломатоз, веррукозный ларингит). Причиной возникновения могут стать 6-й и 11-й типы вируса, несмотря на свой низкий онкогенный риск. В случае папилломатоза есть вероятность полной потери голоса, обструкции (перекрытия) гортани с развитием асфиксии. Это довольно редкое заболевание может возникать у детей, рождённых женщинами с папилломавирусной инфекцией. По разным данным, заражение может происходить как во время родов, так и внутриутробно. Как правило, респираторный папилломатоз начинает проявляться в детском и подростковом возрасте, он склонен к неоднократным рецидивам после удаления множественных папиллом, перекрывающих дыхательные пути.
- Гнойно-септические осложнения. Папилломатозные разрастания на слизистых оболочках очень ранимы, легко травмируются, и через участки мокнутия, расчёсов и потёртостей может проникать вторичная инфекция, которая в свою очередь и вызывает нагноение.
Диагностика папилломавирусной инфекции
Основные цели диагностических мероприятий: [3]
- ранняя диагностика папилломавирусной инфекции для динамического наблюдения и лечения;
- своевременное обнаружение и лечение предраковых изменений, что позволяет на 80% предотвратить развитие злокачественных новообразований;
- выявление онкологических новообразований на ранних стадиях, что в большинстве случаев даёт хороший прогноз эффективного излечения;
- решение вопроса о целесообразности вакцинации.
Для выявления папилломавирусной инфекции на сегодняшний день существует целый комплекс диагностических процедур:
- Гинекологический осмотр в зеркалах — позволяет увидеть папилломатозные разрастания (аногенитальные кондиломы) и другие изменения.
- Классический тест Папаниколау (мазки с поверхности шейки матки и стенок влагалища для цитологического исследования) — обнаруживает ранние признаки дисплазии и злокачественного перерождения.
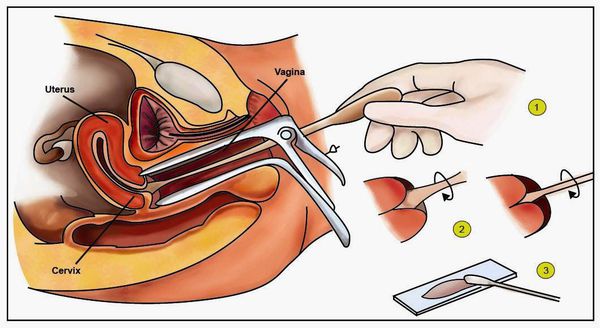
- Пробы с уксусной кислотой и раствором Люголя — выявляют участки поражения слизистой шейки матки.
- Кольпоскопия, в том числе с биопсией подозрительных участков и их гистологическим исследованием, — определяет характер имеющегося новообразования.
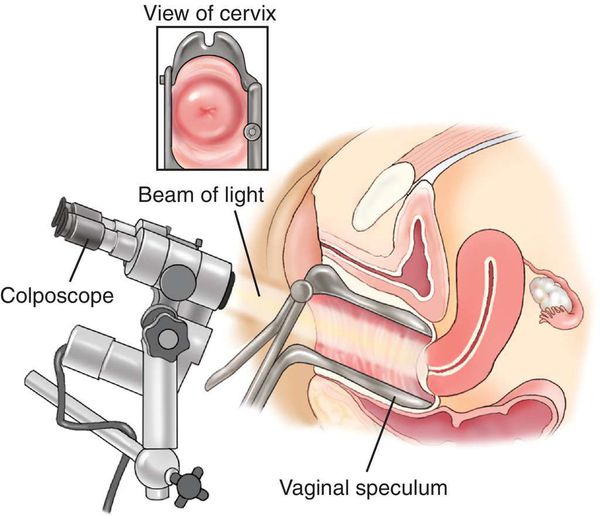
- Иммунофлюоресцентный анализ (ИФА) обнаруживает в цервикальном соскобе онкопротеины (Е7 и Е6). Этот метод достаточно новый, с его помощью можно различить носительство ВПЧ и первые признаки злокачественного перерождения в клетках, [12] оценить агрессивность данного процесса, сделать предположения относительно прогноза заболевания.
- Полимеразная цепная реакция (ПЦР) находит вирусную ДНК в биологическом материале (соскоб со слизистой), определяет тип ВПЧ, степень его онкогенности, а также количество вирусных частиц, что косвенно позволяет судить о характере течения папилломавирусной инфекции у данного пациента, возможности спонтанного излечения или высокого риска прогрессирования. Обнаружение ВПЧ с помощью этого возможно даже при латентном течении болезни, когда цитологические и гистологические методы не эффективны.
Целесообразно дополнительное обследование пациента на наличие других инфекций, передающихся половым путём, так как папилломавирус в 90% случаев с ними сочетается, и это может осложнять течение заболевания.
Лечение папилломавирусной инфекции
Лечение папилломавирусной инфекции должно быть комплексным и включать следующие составляющие: [3] [5]
- деструкцию (удаление) видимых проявлений (аногенитальных кондилом и др.);
- иммуномодулирующую терапию;
- противовирусную терапию;
- лечение сопутствующих инфекций, передающихся половым путём.
Деструктивные методы делятся на две основные группы:
- химические — с применением трихлоруксусной кислоты, а также таких препаратов, как "Солкодерм", "Колломак", "Ферезол" и др.;
- физические — хирургическое удаление, электрокоагуляция, криодеструкция, радиоволновая и плазменная коагуляция, лазеротерапия.
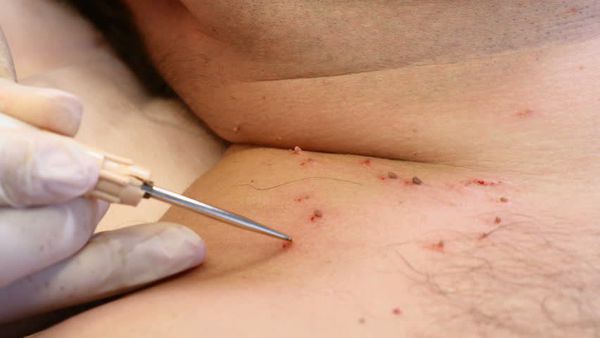
Лечение сопутствующих половых инфекций проводят до начала деструктивной терапии на фоне адекватной иммунокоррекции.
Удаление видимых проявлений папилломавирусной инфекции должно сочетаться с противовирусной терапией — как с общей, так и с применением препаратов местного действия после удаления кондилом.
Следует помнить, что успешно проведённое лечение не исключает развитие рецидивов в дальнейшем, особенно у пациентов с нарушениями иммунитета. Поэтому за ними устанавливается динамическое наблюдение в течение как минимум 1-2 лет.
Прогноз. Профилактика
В 90% случаев здоровая иммунная система человека справляется с папилломавирусной инфекцией самостоятельно за период от полугода до двух лет с момента инфицирования, после чего происходит полное выздоровление с исчезновением вируса из организма. При этом не формируется напряжённого пожизненного иммунитета, то есть человек может заразиться повторно.
В других случаях, при наличии предрасполагающих факторов, заболевание приобретает хроническую форму, склонную к длительному скрытому течению с периодическими рецидивами и возможным развитием тяжёлых осложнений.
От момента попадания вируса в организм до развития предраковых состояний и тем более возникновения рака может пройти достаточно много времени, иногда десятки лет. Поэтому регулярные профилактические обследования, своевременное выявление и лечение предраковых состояний — вполне реальный и эффективный способ избежать самого неблагоприятного варианта развития событий. [13] С этой целью Всемирная организация здравоохранения рекомендует всем женщинам старше 30 лет при первичном скрининге проходить не только “рутинное” цитологическое исследование, но и делать тест на наличие ВПЧ. [10]
Регулярное посещение гинеколога (при отсутствии каких-либо жалоб — раз в год) с проведением теста Папаниколау позволяет своевременно обнаружить начальные признаки дисплазии и предпринять все необходимые меры для предотвращения прогрессирования процесса и его перехода в онкологическое заболевание.
Использование методов барьерной контрацепции хоть и не полностью защищает от инфицирования, но несколько снижает его вероятность.
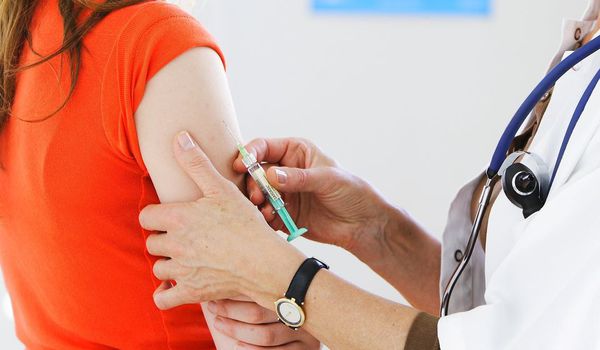
Главным методом первичной профилактики папилломавирусной инфекции считается вакцинация. [11] Современные вакцины разработаны с целью защиты от наиболее опасных, высокоонкогенных штаммов ВПЧ, ответственных за 70-80% случаев развития рака шейки матки. Стандартный курс, состоящий из трёх прививок, даёт вполне надёжную защиту.

Врач — акушер-гинеколог-эндокринолог. Стаж 21+ год. Принимает в Университетской клинике. Стоимость приема 1700 руб.
- Запись опубликована: 20.12.2018
- Reading time: 3 минут чтения
Около 660 млн. человек в мире являются носителями инфекции, вызываемой папилломавирусами. Заболевание годами может протекать бессимптомно, но при снижении иммунитета вирус активируется и болезнь проявляется.
Симптомы заражения
При инфицировании папилломавирусом на коже и слизистой появляются наросты:
- Папилломы – округлые образования, от телесного до коричневого цвета. Крепятся к различным областям на коже и слизистой.
- Бородавки – выпуклые наросты, сходные с оттенком кожи, чаще появляются на ладонях и ступнях.
- Остроконечные кондиломы – образования розового цвета, прикрепляются к эпителию половых органов или ануса.
Как можно заразиться
Болезнь передается половым путем. При однократном сексуальном контакте риск заражения составляет 60%. Использование презерватива необходимо, но это не предохраняет от болезни на 100%. Инфицироваться можно при соприкосновении с паховой областью.
Возможно заражение и бытовым способом. Для проникновения вируса достаточно наличия ранки на теле. Новорожденные инфицируются при прохождении родовых путей. Внутриутробно вирус не передается.
Типы возбудителей
Существует множество штаммов ВПЧ, отличающихся различной степенью провоцирования рака:
- HPV, низкого риска возникновения онкологии (3, 6, 11, 13, 32, 34, 40, 41, 42, 43, 44, 51, 61, 72, 73);
- HPV, среднего риска патологической трансформации эпителия (30, 35, 45, 52, 53, 56, 58);
- HPV, высокого онкогенного риска (16, 18, 31, 33, 39, 50, 59, 64, 68, 70).
У одного пациента может быть выявлено несколько разновидностей вируса.
Факторы риска
- Снижение иммунитета;
- Наличие венерических заболеваний;
- Вредные привычки (курение, алкоголизм);
- Беременность и роды (риск передачи ребенку);
- Незащищенный сексуальный контакт, частая смена половых партнеров;
- Использование средств гигиены другого человека (зубная щетка, полотенце, бритва).
Симптомы
У женщин ВПЧ поражает влагалище, шейку матки, уретру, у мужчин – головку и крайнюю плоть члена, мошонку и область ануса. Этим и обуславливаются симптомы болезни.
У мужчин и женщин возбудитель ВПЧ вызывает появление на половых органах разрастаний, похожих на цветную капусту. Эти высыпания кровоточат, болят, могут воспаляться и нагнаиваться. Бородавчатые наросты быстро увеличиваются в размерах, доставляя значительный дискомфорт. Пациенты жалуются на боль и неудобства при дефекации, мочеиспускании и интимной жизни.
У женщин вирус поражает слизистую влагалища и шейки матки. Возникает дисплазия – предраковое заболевание шейки, во время которого на ее поверхности появляются изменённые очаги слизистой. При половом контакте или поднятии тяжести возникает кровянистая мазня.
Бородавки и папилломы могут появляться в любом месте на теле. Они некрасиво выглядят, а при травмировании одеждой вызывают боль. Отрыв крупных папиллом может сопровождаться кровотечением.
У ряда пациентов заболевание приводит к раку. Этому способствует длительное протекание инфекции (10-20 лет), наличие онкогенного штамма вируса и снижение иммунитета.
ВПЧ перетекает в злокачественное состояние в 0,5 % случаев. Однако при наличии вируса риск заболеть раком шейки матки у инфицированной женщины в 300 раз выше, чем у здоровой.
Вирусная инфекция и беременность
Во время беременности папилломавирус проявляется в 30-65% случаев. Причина — снижение иммунитета в этот период.
Кондиломы на половых органах удаляют после 16-й недели, когда иммунная система матери окрепнет и снизится риск повторного возникновения заболевания.
Диагностика
- Осмотр – доктор проводит визуальный осмотр области гениталий. При ВПЧ обнаруживаются бородавки, кондиломы, папилломы. – исследование влагалища и шейки матки прибором-кольпоскопом. Гинеколог осматривает слизистую половых путей, выявляя патологические изменения.
- Цитология — мазок с шейки матки, который отправляют на цитологическое исследование с целью установить наличие атипичных и раковых клеток.
- Биопсия — забор материала (кусочка нароста), который изучается в лаборатории. Диагностика выявляет злокачественные изменения в клетках.
- ПЦР — а нализ обнаруживает фрагменты ДНК вируса в соскобе. Исследование позволяет установить тип болезни и степень онкогенного риска.
- Скрининг , определяющий риск перетекания вируса в рак. Анализ устанавливает наличие в мазке штамма заболевания с высокой онкологической перспективой.
Особой подготовки к анализам не требуется. Достаточно выполнить гигиенические процедуры и воздержаться от сексуальных контактов за пару дней до визита в клинику.
Лечение
При лечении болезни назначается курс противовирусных препаратов и средств, повышающих иммунитет.
Бородавки, кондиломы и папилломы убирают лазером, радиоволновым методом или жидким азотом. Эти современные методы не оставляют рубцов, а ткани после удаления быстро восстанавливаются.
Папилломавирусная инфекция привлекла особое внимание в последнее время в связи с ролью этой группы вирусов в развитии рака. Доказательство того, что некоторые типы вируса папилломы человека (ВПЧ) способны вызывать рак шейки матки, было отмечено Нобелевско
Папилломавирусная инфекция привлекла особое внимание в последнее время в связи с ролью этой группы вирусов в развитии рака. Доказательство того, что некоторые типы вируса папилломы человека (ВПЧ) способны вызывать рак шейки матки, было отмечено Нобелевской премией по медицине 2008 года.
Классификация
К ВПЧ-поражениям относят аногенитальные бородавки — остроконечные кондиломы, вульгарные бородавки, плоские кондиломы. Необходимо помнить, что различные виды бородавок (кондилом) — это лишь часть спектра поражений, вызванных ВПЧ. Существуют еще субклиническая и латентная формы инфекции, а также ВПЧ-ассоциированные заболевания — интраэпителиальные неоплазии (ИН) различных степеней. В частности, известно, что более чем у 60% женщин с аногенитальными бородавками имеется сопутствующая цервикальная ИН (CIN) в субклинической форме [2]. Помимо CIN с ВПЧ могут быть ассоциированы ИН вульвы (VIN), полового члена (PIN) и анальной области (AIN) [3].
В мировой практике используются различные классификации папилломавирусной инфекции и ассоциированных с ней заболеваний. Ориентировочная классификация представлена Handley J. et al. [4]:
ВПЧ-инфекция
1. Клинические формы (видимые невооруженным глазом или невидимые, но при наличии соответствующей симптоматики):
- бородавки (остроконечные кондиломы, плоские кондиломы, вульгарные бородавки);
- симптоматические ИН на ранних стадиях — койлоцитоз, дискератоз при отсутствии дисплазии (плоские кондиломы).
2. Субклинические формы (невидимые невооруженным глазом и бессимптомные, выявляемые только при кольпоскопии и/или цитологическом или гистологическом исследовании):
- асимптоматические ИН на ранних стадиях — койлоцитоз, дискератоз при отсутствии дисплазии.
3. Латентные формы (отсутствие морфологических или гистологических изменений при обнаружении ДНК ВПЧ).
Заболевания, ассоциированные с ВПЧ
Клинические и субклинические формы:
- ИН на ранних стадиях — слабо выраженная дисплазия ± койлоцитоз, дискератоз (CIN I);
- ИН на поздних стадиях — выраженная дисплазия ± койлоцитоз, дискератоз (CIN II);
- ИН на поздних стадиях — тяжелая дисплазия или карцинома in situ ± койлоцитоз, дискератоз (CIN III или CIS);
- микроинвазивная плоскоклеточная карцинома.
Эпидемиология
По оценкам Центра по контролю заболеваемости (CDC) в США ВПЧ инфицируются до 5,5 млн человек в год [5]. В Европе в год регистрируется 554 000 случаев, вызванных этими вирусами: в том числе цервикальных неоплазий легкой степени (CIN I), генитальных бородавок, цервикальных неоплазий средней и тяжелой степени (CIN II и III), рака шейки матки. Таким образом, в сутки по этой причине умирает до 40 человек [Gross et al., 2008]. По данным российских ученых папилломавирусная инфекция гениталий встречается у 44,3% женщин, обращающихся в гинекологические клиники [6].
Диагностика
Комплексная диагностика заболеваний, ассоциированных с ВПЧ, предполагает клинико-визуальный осмотр, кольпоскопическое исследование, тестирование на ВПЧ, использование цитологических и/или гистологических методов.
Лечение
Согласно существующим принципам по ведению больных с клиническими проявлениями, связанными с ВПЧ, лечение аногенитальных ВПЧ-поражений направлено на разрушение тем или иным методом папилломатозных очагов, возникающих на месте внедрения вируса. Именно такой подход приведен во всех основных рекомендациях по ведению больных с ВПЧ-инфекцией (CDC, Европейских рекомендациях, рекомендациях ВОЗ). Такой подход представлен и в рекомендациях Российского общества дерматовенерологов и косметологов.
Как для лечения клинических проявлений ВПЧ-инфекции, так и ассоциированных с ней заболеваний (в первую очередь это касается CIN II и CIN III) применяют деструктивные методы — хирургические, физические (крио-, электро- или лазеротерапия, радиоволновая хирургия) и химические. При CIN I тактика может различаться в зависимости от величины поражения шейки матки, наличия другой патологии и возможностей самой пациентки [7]. При небольшом поражении чаще рекомендуют оставить женщину под наблюдением и периодически выполнять обследования — тесты на ВПЧ, кольпоскопию, цитологию. Очень важно при этом диагностировать и лечить воспалительные, дисгормональные и другие заболевания урогенитального тракта. Большую роль в определении тактики ведения больных в этих случаях имеет желание пациентки и ее возможность регулярного посещения врача для проведения обследования.
Более эффективным методом лечения при патологии шейки матки, ассоциированной с ВПЧ, является комбинация деструкции с адъювантной противовирусной и иммуномодулирующей терапией. Применение активаторов противовирусного иммунитета позволяет повысить эффективность лечения за счет снижения частоты рецидивов, а также воздействия непосредственно на репродукцию вируса.
Помимо иммунотропного, Изопринозин обладает прямым противовирусным действием, угнетая синтез вирусов путем встраивания инозин-оротовой кислоты в полирибосомы пораженной вирусом клетки и нарушая присоединение адениловой кислоты к вирусной РНК.
Таким образом, Изопринозин прямо и косвенно, обладая противовирусным действием и оказывая влияние на противовирусный иммунитет, способен подавлять репликацию ВПЧ и образование вирусных белков. Эти эффекты могут изменять механизм взаимодействия ВПЧ и макроорганизма, препятствуя переходу вируса из транзиторной в персистирующую форму, а также влияя на клиническую манифестацию инфекции.
Одним из показаний применения препарата являются инфекции, вызванные ВПЧ: остроконечные кондиломы, папилломавирусная инфекция вульвы, вагины и шейки матки (в составе комплексной терапии).
При инфекциях, вызванных ВПЧ, Изопринозин назначают по 3 г/сут (2 таблетки 3 раза в сутки) как дополнение к местной терапии или хирургическому вмешательству в течение 14–28 дней или 5 дней в неделю последовательно в течение 1–2 недель в месяц в течение 3 месяцев.
В работе Забелева А. В. и соавт. [15] показано исчезновение атипичного эпителия после проведения курсов Изопринозина женщинам с ВПЧ-ассоциированными плоскоклеточными ИН низкой степени. Изопринозин назначали по 1 г 3 раза в сутки в течение 5 дней, 3 курса с интервалом 1 месяц.
Аналогичные результаты — улучшение морфологической картины эпителия вульвы — показаны в исследовании Sun Kuie Tay [16]. Инозин пранобекс назначали по 1 г 3 раза в сутки в течение 6 недель. Положительный эффект был достигнут у 63,5% больных, а в группе, принимавшей плацебо, — у 16,7% (рис. 1).
В другом исследовании при монотерапии Изопринозином по 3 г в сутки у 44 женщин с CIN I (длительность лечения 10 дней) и CIN II (длительность лечения 21 день) установлено, что выраженный клинический эффект наблюдался у 88,6% пациенток — полностью исчезало поражение эпителия экзоцервикса, что подтверждалось кольпоскопически и гистологически [17] (рис. 1).
Рис. 1. Сравнительная эффективность Изопринозина при лечении заболеваний, ассоциированных с ВПЧ
До лечения койлоцитоз при нормальной кольпоскопической картине был выявлен у 1367 пациенток, а после лечения — только у 71. Лечение остроконечных кондилом оказалось эффективным у 91% пациенток, комбинированное лечение CIN I — у 90%, комбинированное лечение CIN II — у 82%, лечение субклинической формы ВПЧ-инфекции — у 91% (рис. 1).
В работе Клинышковой Т. В. и соавт. [18] показана высокая частота регресса CIN I (70%) и элиминации ВПЧ (83,3%) при использовании Изопринозина в режиме монотерапии и комбинированного лечения в сочетании с деструкцией у пациенток с ВПЧ-ассоциированными поражениями шейки матки (рис. 1). Изопринозин назначали по 3 г в сутки двумя 10-дневными курсами — за 1 месяц до деструкции и с 1-го дня деструкции.
Недавно был проведен метаанализ результатов применения изопринозина [19]. Данные литературы, базирующиеся на 15 источниках, в которых описано 2369 случаев применения Изопринозина в качестве монотерапии, 3369 — в комбинации с другими методами, в сравнении с 71 наблюдением плацебо-контроля и 575 наблюдениями за традиционным лечением свидетельствуют об эффективности вспомогательной иммунотерапии Изопринозином на фоне традиционных методов при терапии генитальных поражений, ассоциированных с ВПЧ.
Интересным является факт прекращения обнаружения ВПЧ из очагов поражения в ходе проводимой комбинированной терапии с применением Изопринозина. Несмотря на то, что во многих работах говорится о полной элиминации вируса, правильнее говорить именно о прекращении выделения ВПЧ из очагов поражения или урогенитального тракта, поскольку методология диагностики заключается в исследовании соскобного материала, взятого из этих зон. Говорить в этом случае о полной элиминации ВПЧ из организма или даже из урогенитального тракта будет слишком смело и бездоказательно.
Прилепская В. Н. сообщает о прекращении выделения ВПЧ у 65,6% больных после комбинированной терапии (Изопринозин + деструкция очагов) CIN низкой степени [6]. При использовании только деструкции очагов этот результат был достигнут у 46,9% больных (рис. 2). Изопринозин назначали по 1 г 3 раза в сутки в течение 5 дней за 7–10 дней до проведения деструкции.
Похожие результаты — прекращение выделения ВПЧ у 77% больных — показаны в исследовании Шевниной И. В. (2009) при комбинированной терапии женщин с CIN и аногенитальными бородавками. Изопринозин назначали по 1 г 3 раза в сутки в течение 10 дней, затем по 0,5 грамма 3 раза в сутки в течение 20 дней.
В другом исследовании Изопринозин назначали женщинам с патологией шейки матки, ассоциированной с ВПЧ [20]. Препарат назначали после проведения обследования и противовоспалительной терапии по 3 г в сутки в течение 10 дней. Элиминация ВПЧ достигнута у 95,3% пациенток (рис. 2).
Есть и другие исследования, в которых показано прекращение выделения ВПЧ из очагов поражения у 69,6–97,8% женщин, принимавших Изопринозин [21–23] (рис. 2).
Представленные данные свидетельствуют о возможной эффективности монотерапии Изопринозином при бессимптомном вирусовыделении, когда применение деструктивных методик не показано.
Рис. 2. Воздействие Изопринозина на прекращение выделения ВПЧ из очагов поражения
Профилактика
С целью профилактики рака шейки матки и тяжелых дисплазий женщинам можно рекомендовать вакцинацию. Сегодня на российском рынке доступны две вакцины — Гардасил и Церварикс. Их эффективность с точки зрения профилактики развития рака и CIN всех степеней практически одинакова и близка к 100%. Вакцинация позволяет предотвращать не только CIN, но даже минимальные изменения морфологической картины эпителия шейки матки. Какие-либо отклонения в мазках по Папаниколау выявлялись у 42% невакцинированных и только 14% вакцинированных девочек в возрасте от 11 до 21 года при наблюдении за ними в течение 3 лет [24].
Заключение
Таким образом, основными клиническими эффектами адъювантной или самостоятельной терапии Изопринозином являются:
1) повышение эффективности деструктивных методов лечения;
2) снижение частоты рецидивов после проведенного лечения;
3) нормализация морфологической картины экзо- и эндоцервикса;
4) прекращение выделения ВПЧ из очагов поражения.
При использовании изопринозина частота побочных эффектов составляет около 10%. Сообщается о тошноте и недомогании у 5,4–8,8%, кожных аллергических реакциях у 1,7–9,1%, болях в эпигастрии у 4%, головной боли у 2,7%, сухости кожных покровов у 2%, повышении трансаминаз у 1%, повышении уровня мочевой кислоты у 1–22,2% [1, 16, 20, 21, 25].
Многочисленные исследования, проведенные во многих странах мира, в том числе и в России, показали, что при комбинации деструктивных методов с назначением Изопринозина, благодаря его двойному противовирусному и иммуномодулирующему действию, подавляющему репликацию ВПЧ, повышается эффективность терапии заболеваний шейки матки, ассоциированных с папилломавирусной инфекцией.
Литература
- Прилепская В. Н., Костава М. Н. Возможности терапии папилломавирусной инфекции // РМЖ. 2009; 17 (1): 16–19.
- Handley J. M., Maw R. D., Lawther H. et al. // Sex Transm Dis. 1992; 19: 225–229.
- Ludicke F., Stalberg A., Vassilokos P. et al. High and intermediate risk human papillomavirus infection in sexually active adolescent femails // J Pediatr Adolesc Gynecol. 2001; vol. 14 (4), p. 171–174.
- Handley J. M., Dinsmore W. // J Eur Acad Dermatol Venerol. 1994; 3 (3): 251–265.
- Armstrong G. L. et al. // Am J Epidemiol. 2001; 153: 912–992.
- Прилепская В. Н., Роговская С. И. Возможности Изопринозина в лечении хронических цервицитов и вагинитов // РМЖ. 2007; 16 (3): 14.
- Роговская С. И. Папилломавирусная инфекция у женщин и патология шейки матки. М.: ГЭОТАР-медиа, 2011, 22 с.
- Кацамбас А. Д., Лотти Т. М. Европейское руководство по лечению дерматологических болезней. МЕДпресс-информ, 2009; 84–88.
- Hersey P., Edwards A. Effect of Isoprinosine on natural killer cell activity of blood mononuclear cells in vitro and in vivo // Int J Immunopharmacol. 1984; 6: 315–320.
- Hersey P., Bindon C., Bradley M. et al. Effect of Isoprinosine on interleukin 1 and 2 production and on suppressor cell activity in pokeweed mitogen stimulated cultures of B and T cells // Int J Immunopharmacol. 1984; 6: 321–328.
- Bekesi J., Tsang P., Wallace J. et al. Immunorestorative properties of Isoprinosine in the treatment of patients at high risk of developing ARC or AIDS // J Clin Lab Immunol. 1987; 24: 155–161.
- Cillari E., Diell M., Lo Campo P. et al. Protective effect of Isoprinosine in genetically susceptible BALB/c mice infected with Leishmania major // Immunology. 1991; 74: 25–30.
- Diaz-Mitoma F., Turgonyl E., Kumar A. et al. Clinical improvement in cronic fatigue syndrome is associated with enchanced natural killer cell-mediated cytotoxicity: the results of a pilot study with Isoprinosine // J Chron Fatig Syn. 2003; 11 (2): 1–17.
- Абелевич М. М., Иванова Е. Л., Лукушкина Е. Ф. Этиопатогентическая терапия инозином пранобексом у детей с осложненным течением аллергических заболеваний // НМЖ. 2008; 1: 60–64.
- Забелев А. В., Долматова О. К., Сивоконева Е. Н. и соавт. Результаты кольпоскопического скрининга и опыт применения изопринозина в лечении паилломавирусных поражений шейки матки // Фарматека. 2005; 3: 72–75.
- Tay S. K. Efficacy of inosine pranobex oral therapy in subclinical human papillomavirus infection of the vulva: a randomized double blinde placebo-controlled study // Int J STD & AIDS. 1996; 7: 276–280.
- Потапов В. А., Демченко Т. В., Стрельцова Т. Р. и соавт. Клинико-лабораторная оценка эффективности Изопринозина в лечении папилломавирусной инфекции, ассоциированной с цервикальной интраэпителиальной неоплазией // Репродуктивное здоровье женщины. 2006; 1 (25).
- Клинышкова Т. В., Каратюк Т. И., Турчанинов Д. В. и соавт. Дифференцированный подход к ведению больных с цервикальной интраэпителиальной неоплазией с позиции прогнозирования // Гинекология. 2009; 13 (4): 40–44.
- Елисеева М. Ю., Мынбаев О. А. Вспомогательная иммунотерапия ВПЧ-ассоциированных поражений слизистых оболочек и кожи урогенитальной и перианальной локализации // Гинекология. 2009; 11 (5): 22–33.
- Линаск Л. И., Григорьева Е. Е. Опыт применения Изопринозина при заболеваниях шейки матки на фоне папилломавирусной инфекции у подростков и молодых женщин // Русский медицинский журнал. 2008; 16 (19): 1–4.
- Кедрова А. Г., Подистов Ю. И., Кузнецов В. В. и соавт. Роль противовирусной терапии в комплексном лечении больных эпителиальными дисплазиями и преинвазивным раком шейки матки // Гинекология. 2005; 7 (3): 170–174.
- Долгушина В. Ф., Ахматова А. Н., Беренда М. А. Эффективность изопринозина в лечении хронического цервицита, ассоциированного с папилломавирусной инфекцией // Фарматека. 2009; 14: 73–76.
- Макаров И. О., Шеманаева Т. В., Шешукова Н. А. Опыт применения изопринозина в лечении патологии шейки матки воспалительной этиологии // Consilium Medicum. 2010; 13 (6): 16–18.
- Gross M. et al. Human papillomavirus (HPV) vacctination and Pap smear results in adolescent girls — have we seen a difference? // J Pediatr Adolesc Gynecol. 2010; vol. 23 (2): 70–71.
- Georgala S., Katoulis A. C., Befon A. et al. Oral inosiplex in the treatment of cervical condilomata acuminate: a randomized placebo-controlled trial // BJOG. 2006; 113 (9): 1088–1091.
А. М. Соловьев*, кандидат медицинских наук, доцент
И. Н. Анискова**, кандидат медицинских наук
*МГМСУ, Москва
** ГБУЗ Центр планирования семьи и репродукции, Краснодар
Читайте также:

