Повышение печеночных ферментов при гепатите а
Обновлено: 22.04.2024
УДК 616.36-002.1-4
ББК 54.135
Лихота О.С., Цикуниб А.Д.
Адыгейский государственный университет, кафедра химии
Особенности метаболизма и маркеры биохимических нарушений в печени при гепатитах
Аннотация. В статье представлен аналитический обзор современной научной литературы, раскрывающий особенности метаболизма печени при гепатитах и обсуждены маркеры биохимических нарушений при различных по происхождению и интенсивности заболеваниях печени.
Ключевые слова: метаболизм печени, маркеры биохимических нарушений печени, гепатиты.
Likhota O. S., Tsikunib, A. D.
Adyghe state University, department of chemistry
Characteristics of metabolism and markers of biochemical disorders in the liver with hepatitis
Abstract. The article presents an analytical overview of modern scientific literature, revealing the peculiarities of the metabolism of the liver in hepatitis and discussed markers of biochemical disorders in various origins and intensity of liver diseases.
Keywords: liver metabolism, markers of biochemical disorders of the liver, hepatitis.
Печень является важнейшим органом, в котором протекают биохимические процессы, чрезвычайно значимые для организма в целом [11]. В ней синтезируются белки (альбумины, протромбин, фибриноген, другие факторы свертывания крови), липиды (холестерин), липопротеиды, образуются желчные кислоты, билирубин, желчь [2, 15]. В печени утилизируются токсические вещества, возникающие в организме и поступающие в организм (антитоксическая функция) [4, 12]. Печень синтезирует гликоген и участвует тем самым вместе с поджелудочной железой в регуляции углеводных запасов в организме [14]. Ее активная роль в пищеварении заключается в том, что желчь эмульгирует жиры и улучшает расщепление их липазой поджелудочной железы [13]. Продукты расщепления пищи (жиры, жирные кислоты, глицерин, аминокислоты, углеводы, минеральные вещества, вода, витамины) поступают через сосуды воротной вены в печень, в ней они частично депонируются, частично перерабатываются, используются и частично подготавливаются для использования другими тканями [10].
При заболеваниях печени возникают нарушения той или другой ее функции, что используется в диагностических целях. Наиболее широко выполняются в клинических лабораториях исследования нарушений пигментной, углеводной, белок образовательной функций. При острых воспалительных и токсических поражениях печени из ее ткани освобождается значительное количество внутриклеточных ферментов. Диагностическое значение приобрели исследования альдолаз, аланиновой и аспарагиновой трансаминаз(аминофераз), лактатдегидрогеназы и ее фракций, холинэстераз, аргиназы [1, 5, 9]. Печень участвует во всех этапах обмена жиров. Для нормального всасывания жира в кишечнике нужна желчь. Она выполняет функцию детергентаи эмульгатора жира, облегчает работу панкреатической липазы, улучшает всасывание жира в кишечнике. В печени синтезируются фосфолипиды в присутствии липотропных веществ, выступающих в качестве донаторов липидных групп (метионин, холин) либо фактора, способствующего синтезу фосфолипидов (витамин B12) [5]. При недостатке липотропных веществ в печени накапливаются нейтральные жиры, а количество гликогена уменьшается. При заболевании печени в ней уменьшается содержание аденозинтрифосфата, дающего энергию для синтетических процессов [10, 12].
Уровень холестерина в крови является важнейшим показателем синтеза липидов в печени. У здоровых людей в сыворотке крови содержится 3,0—6,5 ммоль/л (116—150 мг %) холестерина. При гепатитах и циррозах печени наблюдается нарушение содержания холестерина в крови: гиперхолестеринемия, по-видимому, связанная с нарушением выделительной функции печени, реже — гипохолестеринемия, связанная со снижением синтеза его в печени [3].
В печени осуществляется также синтез липопротеидов очень низкой плотности и утилизация липопротеидов высокой плотности. Хиломикроны и небольшая часть липопротеидов очень низкой плотности образуются в эпителиальных клетках тонкой кишки. Синтез и распад липопротеидов протекает при участии липопротеидлипазы, которая связывается с гепарином. Отмечено, что при циррозе печени содержание гепарина в крови снижается. Таким образом, печень участвует как в образовании липопротеидов, так и в их разрушении. При заболеваниях печени (гепатиты, начальные формы циррозов печени) имеет место дислипопротеинемия, в основном повышенное образование липопротеидов, преимущественно бета-липопротеидов [8].
Печень осуществляет переаминирование аминокислот, окисление их до пировиноградной кислоты в цикле трикарбоновых кислот, синтез белка. Все альбумины, 75—90 % альфа-глобулинов, 50 % бета-глобулинов синтезируются в печени. Здоровая печень может ежесуточно вырабатывать 13—18 г альбумина. Синтез белка происходит при участии энергии. Одной из причин снижения синтетической функции печени является уменьшение содержания в ней макроэргических соединений. При тяжелых заболеваниях печени общее количество сывороточного белка может понизиться до 40 г/л вместо 80 г/л. Значительно уменьшается содержание альбуминов (до 20 г/л вместо 40 г/л). В условиях патологии печень синтезирует глобулины с необычными свойствами (парапротеины) [6].
При острых воспалительных процессах (гепатит) повышается уровень альфа-глобулинов в 1,5—2 раза. Гамма-глобулины продуцируются лимфоцитами и клетками ретикулоэндотелиальной системы. При хронических гепатитах, протекающих с выраженными аутоиммунными процессами, содержание гамма-глобулинов в крови существенно увеличивается (до 30 %) [4].
При тяжелых нарушениях функции печени процесс дезаминирования аминокислот нарушается, что приводит к увеличению их содержания в крови и моче. Если у здоровых людей содержание аминного азота в сыворотке крови составляет 50—80 мг/л, то при тяжелых дистрофических процессах в печени оно может увеличиться до 300 мг/л (коэффициент перечисления аминного азота, выраженного в мг % или в ммоль/л составляет 0,7139). Отмечено, что при остром вирусном гепатите увеличивается содержание в сыворотке крови глютатиона, глютаминовой кислоты, метионина, фенилаланина, серина, треонина. При хронических гепатитах обнаруживаются те же изменения в содержании аминокислот в крови, но выраженные в меньшей степени [9].
Печень играет важную роль в обмене железосодержащих белков - гемоглобина, миоглобина, цитохромов и др. [7]. Образующийся при катаболизме данных белков токсичный, нерастворимый, свободный билирубин, не дающий прямой реакции с диазореактивом Эрлиха (непрямой) обезвреживается в печени под действием фермента билирубиндиглюкуронилтрансферазы путем конъюгации с глюкуроновыми кислотами с образованием билирубиндиглюкуронида (рисунок 1).

Рис. 1- Схема обезвреживания билирубина в печени.
Данная форма билирубина является уже нетоксичной, растворимой и прямой (дающей прямую реакцию с диазореактивом). Далее в норме обезвреженный билирубин активно переводится печенью в желчные капилляры, поступает в кишечник и превращается в мезобилиноген, часть которого обратно всасывается в кровь, поступает в печень и подвергается более глубокому катаболизму, а остальная часть в кишечнике превращается в основные пигменты кала и мочи и выводится из организма.
Чаще всего биохимические нарушения в печени происходят именно в пигментном обмене. Наиболее важное диагностическое и прогностическое значение имеет определение содержания общего билирубина и его различных фракций в сыворотке крови, исследование уробилина, стеркобилина, желчных пигментов в моче. Эти показатели прямо или косвенно отражают процесс превращения билирубина в печени. Так, при печеночно-клеточной или паренхиматозной желтухе, развивающейся при остром вирусном гепатите, обострении хронического гепатита, циррозе печени, алкогольном поражении печени, при воздействии ряда токсических веществ (хлорированные углеводороды, бензол и его производные, фосфор, свинец, ртуть, мышьяк, ядовитые грибы), а также некоторых лекарственных препаратов нарушаются захват, конъюгация и экскреции билирубина из клеток печени, а также, его регургитация. В результате указанных нарушений функций гепатоцита, отмечается умеренное или резкое повышение уровня общего билирубина крови (при норме не более 20,1 мкМоль/л, от 30 до 60-85 мкМоль/л при легкой форме, при 85-160 мкМоль/л появляются признаки средней тяжести, выше 170 мкМоль/л - тяжелая форма) с преобладанием прямой фракции (при норме не более 0 - 3,4 мкМоль/л), повышение уровня мезобилиногена (уробилина) в моче, снижение уровня холестерина и повышение активности аминотрансфераз, а также диспротеинемия с гипергаммаглобулинемией и снижение уровня протромбина[9].
Гепатоциты печены характеризуются высоким разнообразием ферментного состава. Ферменты печени, как и других органов, делятся на органоспецифические и неспецифические. Для печени органоспецифическими ферментами являются орнитинкарбамилтрансфераза, глютаматдегидрогеназа, фосфофруктоальдолаза, гистидаза, сорбитдегидрогеназа. Кроме того, специфическим считается пятый изофермент лактатдегидрогеназы ЛДГ5 [3].
Повреждение гепатоцитов приводит к освобождению значительного количества внутриклеточных ферментов и накоплению их в крови. В этой связи диагностическое значение приобрели трансаминазы, альдолазы и ряд других ферментов [5].
Альдолазы - групповое название ферментов, участвующих в механизмах аэробного расщепления углеводов. Сывороточная альдолаза катализирует обратное расщепление фруктозо-1,6-дифосфата на две фосфотриозы — фосфоглицериновый альдегид и монофосфатдиоксиацетона (рисунок 2).

Рис. 2- Химизм альдолазной реакции (по Северину Е.С. [11]).
Активность альдолазы в сыворотке крови повышена при остром эпидемическом гепатите и в меньшей мере- при остром токсическом гепатите. При остром вирусном гепатите 5—20-кратное возрастание активности фруктозодифосфатальдолазы наблюдается у 90 % больных. Ее увеличение происходит за 3—15 дней до появления других клинических признаков болезни. Спустя 5 дней от начала желтушного периода активность альдолазы уменьшается. Повышение активности альдолазы отмечается также при безжелтушных формах острого гепатита. У больных с хроническими воспалительными процессами в печени активность альдолазы возрастает незначительно, причем у небольшого их количества[10].
Аминотрансферазы (трансаминазы) часто используются с целью диагностики воспалительных заболеваний печени. Аминотрансферазы в организме человека осуществляют процессы переаминирования: обратного переноса аминогрупп аминокислот на кетокислоты (рисунок 3).

Рис. 3- Схема переаминированияальфа-аминокислот с альфа- кетокислотами, катализируемая трансаминазами(по Северину Е.С. [11]).
Наибольшее диагностическое значение имеет исследование активности аспартатаминотрансферазы (АсТ) и аланинаминотрансферазы (АлТ). Эти ферменты широко распространены в разных органах и тканях — печени, миокарде, скелетных мышцах, почках и др. [8]. При эпидемическом гепатите активность аминотрансфераз повышается с большим постоянством и в ранние сроки, еще до появления желтухи (рисунок 4).

Рис. 4- Динамика изменения активности аминотрансфераз при остром гепатите (по Коротяеву А.И. [8]).
При токсическом гепатите и обострении хронического активность аминотрансфераз возрастает в 3—5 раз(при норме не более 45 ЕД/л). Не столь закономерны изменения при циррозе печени[16].
Лактатдегидрогеназа (ЛДГ) — гликолитический фермент, обратимо катализирующий окисление 1-лактата в пировиноградную кислоту. Для ЛДГ в качестве промежуточного акцептора водорода требуется никотинамиддинуклеотид (рисунок 5).

Рис. 5- Химизм лактатдегидрогеназной реакции (по Григорьеву П.Я. [3]).
В сыворотке крови выявлено пять изоферментов ЛДГ. В печени содержится ЛДГ5 Фермент ингибируется мочевиной, и это свойство фермента облегчает его определение.
При вирусном гепатите активность ЛДГ4 и ЛДГ5 повышена в первые 10 дней у всех больных, степень ее повышения зависит от тяжести заболевания. Уровень активности общей ЛДГ в норме 240—480 МЕ/л. При остром вирусном гепатите активность ЛДГ в сыворотке крови увеличена в первые дни желтушного периода, и при легкой и среднетяжелой формах заболевания довольно бы¬стро возвращается к нормальному уровню. Тяжелые формы вирусного гепатита, и особенно развитие печеночной недостаточности, сопровождаются выраженным и более длительным повышением ЛДГ.При механической желтухе на первых стадиях закупорки желчных протоков активность ЛДГ в норме, на более поздних стадиях наблюдается подъем активности вследствие вторич¬ных повреждений печени.При карциномах печени или метастазах рака в печень может иметь место подъем актив¬ности ЛДГ.В стадии ремиссии при хроническом гепатите и циррозе печени активность ЛДГ в крови остается в пределах нормы или слегка повышена. При обострении процесса отмечается по¬вышение активности фермента[6].
Таким образом, анализ отечественной и зарубежной научной литературы показывает разнообразие и высокую диагностическую значимость маркеров заболеваний печени, основанных на особенностях метаболизма в гепатоцитах и специфике биохимических нарушений при гепатитах.
Примечания:
1. Апросина 3.Г. Хронический активный гепатит как системное заболевание. М.: Медицина, 1981. 248 с.
2. Гирин В.А. Гепатит: Современное лечение и профилактика. М.: Медицина, 2003. 435 с.
3. Григорьев П.Я. Клиника и диагностика хронического вирусного гепатита // Клиническая медицина. 1984. Т. 62, № 2. С. 56-61.
4. Иммунноферментный анализ в клинико-диагностических лабораториях / В.В. Долгов, Н.Г. Ракова, В.Е. Колупаев, Н.С. Рытикова. Тверь: Триада, 2011. 320 с.
5. Дмитириев Г.А., Глазко И.И. Диагностика инфекций, передаваемых половым путем. М.: БИНОМ, 2007. 320 с.
6. Казанцев А.П., Матковский В.С. Справочник по инфекционным болезням. 3-е изд., перераб. и доп. М.: Медицина, 2009. 320 с.
7. Комаров Ф.И., Коровкин Б.Ф., Меньшов В.В. Биохимические исследования в клинике. 2-е изд. Л.: Медицина, 1997. 407 с.
8. Коротяев А.И., Бабичев С.А. Медицинская микробиология, иммунология и вирусология: учеб. для мед. вузов. 4-е изд. М., 2008. 305 с.
9. Ивлев А.С., Хазанов А.И., Румянцев О.Н. Длительные холестазы у больных с дефицитом иммуноглобулина А сыворотки крови // Клиническая медицина. 2007. Т. 65, № 10. С. 131-133.
10. Мусил Я. Основы биохимии патологических процессов. М.: Медицина, 1995. 430 с.
11. Биохимия: учеб. для вузов / под ред. Е.С. Северина. М.: Гоэтар-Медиа, 2003. 779 с.
12. Guthik G. Current heratology. Chichester: John Wiley, 2004. 25 р.
13. Prognostic value of serum fibronectin concentration in alconolikcirrotic patients / S. Neveau, Th. Poynard, A. Abella, J. Rignon // Hematology. 2005. 45 р.
14. Schiff L.E.R. Diseases ot the liver. 5 th ed. Philadelphia: Lirinuott, 2012. 125 р.
15. Tietz N.W. Clinical guide to laboratory tests. Philadelphia: W. B. Saunder Company, 2003. 305 р.
16. Wallhofer H., Schmidt E., Schmidt F.W. Synopsis der Leberkrankheiter. Stuttgart: G. Thime, 2007. 75 р.
_____________________________________________________________________________________
Лихота Ольга Сергеевна, магистрант, тел. 89898090399, e-mail: Этот адрес электронной почты защищен от спам-ботов. У вас должен быть включен JavaScript для просмотра.
Likhota Olga Sergeevna, undergraduate, tel 89898090399, e-mail: Этот адрес электронной почты защищен от спам-ботов. У вас должен быть включен JavaScript для просмотра. .
Цикуниб Аминет Джахфаровна, доктор биологических наук, профессор, директор НИИ комплексных проблем АГУ, зав. лабораторией нутрициологии и экологии, 385000, г. Майкоп, ул. Гагарина, 13, 8928461725, Этот адрес электронной почты защищен от спам-ботов. У вас должен быть включен JavaScript для просмотра. .
Tsikunib Aminet Dzhakhfarovna, Head of Nutrition and Environment Laboratory, Director of Scientific Research Institute of complex Problems of Adyghe State University
Разработка нормальных границ любого биохимического показателя по определению подразумевает, что 2,5% здоровых людей не уложатся в условно нормальные рамки. Чем больше тестов используется одновременно, тем больше получаем отклонений. Во всех случаях полагается дать оценку факту, т.е. заключить, является это отклонение клинически значимым или незначимым. Естественно, что сделать это можно лишь с учетом всего индивидуального клинического контекста. В отношении конкретно печеночных тестов известно, что повышенные значения их встречаются чаще, а именно у 5% людей, не имеющих симптомов патологии печени.
Трудности у малосимптомных пациентов
Наибольшие трудности возникают у малосимптомных пациентов. Общепринятые печеночные тесты представлены в табл. 1. Если подозревается лабораторная ошибка, аномальный тест обычно повторяют. Однако получение результата нормального не исключает того, что прежнее отклонение было истинным, к тому же это может отражать естественные колебания показателя при болезни.
Таблица 1. Диагностический минимум биохимических печеночных тестов
| Печеночный тест | Клиническое значение отклонений |
| АЛТ | ↑ — Повреждение гепатоцитов |
| АСТ | ↑ — Повреждение гепатоцитов |
| Билирубин | ↑ — Холестаз, билиарная обструкция или нарушение конъюгации |
| ЩФ | ↑ — Холестаз, билиарная обструкция или инфильтративный процесс |
| 5’-нуклеотидаза | ↑ — Холестаз или билиарная обструкция |
| ГГТП | ↑ — Холестаз или билиарная обструкция |
| ЛДГ | ↑ — Неспецифическое для болезней печени повреждение гепатоцитов |
| Альбумин | ↓ — Снижение синтетической функции |
| Протромбиновое время и МНО | ↑ — Снижение синтетической функции |
Печень синтезирует 10—12 г альбумина в сутки. Содержание альбумина менее 30 г/л свидетельствует о хронизации болезни печени. Протромбиновое время отражает скорость превращения протромбина в тромбин. В печени синтезируются все факторы коагуляции, кроме VIII. Период полужизни сывороточного альбумина 20 дней, а факторов коагуляции — менее суток. Если гипоальбуминемия отражает хронизацию, то увеличение протромбинового времени может служить маркером тяжести острой дисфункции печени.
Например, при остром вирусном гепатите увеличение протромбинового времени на 5—6 сек говорит о возможности молниеносного некроза.
Билирубин формируется из гема в ретикулоэндотелиальную систему. Фракции прямого и непрямого билирубина определяют с 20-х годов прошлого столетия. Но только в 60-х годах было констатировано, что непрямой билирубин — это его неконъюгированная форма, а прямой — это комбинация моно- и диглюкуронидов билирубина (т.е. связанный). От терминов "прямой/непрямой" пора отказаться.
Основные причины гипербилирубинемии (ГБ) представлены в табл. 2. Содержание неконъюгированного билирубина в сыворотке крови отражает баланс между его продукцией и гепатобилиарной экскрецией. Неконъюгированная ГБ сама по себе не опасна, но с годами повышается риск возникновения пигментного холелитиаза. Конъюгированная ГБ отражает повреждение паренхимы печени или билиарную обструкцию, при этом значимые количества билирубина попадают в мочу. Холестаз бывает, как известно, вне- и внутрипеченочный, ГБ может не сопровождаться отклонениями активности ферментов.
Таблица 2. Основные причины гипербилирубинемии (ГБ)
| Неконъюгированная (непрямая) ГБ | Конъюгированная (прямая) ГБ |
| Синдром Жильбера | Билиарная обструкция |
| Неэффективный эритропоэз (В12-дефицит и др.) | Гепатиты |
| Гемолиз (в т. ч. при гематрансфузии) | Цирроз |
| Рассасывание обширной гематомы | Лекарства/токсины |
| | Первичный билиарный цирроз |
| Первичный склерозирующий холангит | |
| Внутрипеченочный холестаз беременных | |
| Доброкачественный рекуррентный холестаз |
Наибольшее повышение — при гепатитах Аминотрансферазы — ферменты глюконеогенеза. Аспарагиновая трансаминаза (АСТ) имеет цитозольный и митохондриальный изоэнзимы, АЛТ — цитозольный фермент. Активность трансфераз имеет околосуточные и другие колебания, меняется после физической нагрузки. Они встречаются в клетках различных тканей, причем наибольшая активность АСТ — в печени, в сердце и скелетной мускулатуре, в почках; АЛТ находится в основном в клетках печени и в меньшей степени в мышечных клетках. Повышение может быть отмечено при эндокардитах, остром инфаркте миокарда, мышечно-скелетных травмах. Наибольшее повышение имеет место при гепатитах, степень пропорциональна выраженности острого повреждения печени.
Как отдельную категорию рассматривают лиц с повышением АЛТ и АСТ выше в 1,5 и не более чем в 5 раз. Это — самая актуальная группа. К ней относятся хронические гепатиты, стеатоз, цирроз, алкогольные и другие повреждения печени.
Хроническим подъемом АЛТ или АСТ условно считают сохранение отклонений на протяжении полугода. Повреждение печени вовсе не обязательно означает некроз, это может быть обратимое состояние в форме дистрофии, т.е. повышения проницаемости клеточных мембран. Одновременное повышение АЛТ и АСТ обычно исключает лабораторную ошибку и говорит о печеночном генезе отклонения.
Для хронического алкогольного поражения печени считают характерным соотношение АСТ/АЛТ 2:1 и более плюс двойное повышение гаммаглутаминтранспептидазы (ГГТП). Резкое повышение активности ферментов редко бывает при хронической алкогольной болезни печени. Это происходит при присоединении вирусного или острого алкогольного гепатита или приема парацетамола. Более высокие трансферазы наблюдают при ишемическом гепатите и других состояниях, включая иногда и холедохолитиаз. Частая серьезная причина — гепатит С, гепатит В — теперь будет встречаться реже в результате вакцинации населения.
Чем опасна полипрагмазия
Относительно новая диагностируемая причина — жировая инфильтрация печени с воспалением или без него (стеатогепатит и гепатоз). Этот диагноз при хронических сдвигах ферментов обычно приходится ставить методом исключения. При неалкогольном стеатозе соотношение АСТ/АЛТ обычно ниже 1:1, а билирубин и альбумин нормальны.
Наследственный гемохроматоз — одна из самых частых генетических болезней с разной клинической выраженностью.
Может первично проявляться подъемом трансаминаз.
У большинства людей с изолированным умеренным подъемом АЛТ болезни печени нет. При подозрении на лекарственное средство (ЛС) как на причину его можно заменить на другой медикамент. Важно представлять, какие ЛС повреждают печень и при применении каких подъем трансаминаз имеет внепеченочные причины, ведь приходится решать вопрос о целесообразности отмены ЛС или продолжении терапии.
Наиболее актуальны сейчас ситуации, связанные с приемом статинов. Также более ¼ получающих противосудорожную терапию обнаруживают аномалии печеночных тестов. Условно неблагоприятные печеночные реакции на медикаменты разделяют на ненормальные тесты — когда показатель одного из ферментов не превышает двух норм, и поражения печени — когда один из показателей (не только трансаминаз) в два раза или более превышает верхнюю границу нормы.
Риск лекарственных поражений печени более высок при полипрагмазии, особенно в пожилом возрасте. Функциональные нарушения печени обычно нормализуются через 4—6 недель после отмены ЛС.
Печеночное или костное происхождение?
Понятие гепатотоксичности включает истинную, связанную с ЛС, токсичность, зависящую от дозы, и идиосинкразию.
Вторая — следствие индивидуальной предрасположенности. Известно более 50 микросомальных изоферментов в печеночной системе детоксикации цитохрома Р450, структура которых кодируется отдельными генами. Генетические различия каталитической активности ферментов объясняют причину развития реакций идиосинкразии к отдельным лекарствам.
Но и чрезмерное повышение активности ферментов системы цитохрома Р450 в результате их индукции (например, на фоне алкогольной интоксикации) может сопровождаться резким повышением выработки токсичных метаболитов. Первым шагом в лечении должна быть отмена ЛС, в большинстве случаев это относительно быстро приводит к существенному улучшению клинико-лабораторных данных. Но необходимо продолжать наблюдение тех больных, которые получали препараты с большим периодом полувыведения.
Причины подъема щелочной фосфатазы представлены в табл. 3. Щелочная фосфатаза (ЩФ) принадлежит к семейству цинксодержащих металлоферментов.
Таблица 3. Причины подъема щелочной фосфатазы
| Печеночные | Внепеченочные |
| Билиарная обструкция | Инфекция/воспаление |
| Первичный билиарный цирроз | Болезни костей |
| Лекарства | Застойная сердечная недостаточность |
| Инфильтративные болезни печени | Хроническая почечная недостаточность |
| Метастазы в печень | Лимфома и др. злокачественные процессы |
| Гепатиты | Ростовой скачок у подростков |
| Цирроз | Беременность (III триместр) |
| Дисфункции билиарных сфинктеров | |
| Доброкачественный рекуррентный холестаз | |
Содержится преимущественно в печени и костях, а 20% находится в стенке кишечника. ЩФ растет, когда в соответствующих тканях возрастает метаболическая активность. Так, у подростков возрастает в 2 раза по сравнению с взрослой нормой за счет костного изофермента.
При беременности в первом триместре может повыситься в два раза за счет плацентарных изоферментов и более значительно — в предродовом периоде. Период полужизни ЩФ составляет неделю, поэтому она начинает расти лишь через 1—2 дня после наступления билиарной обструкции и сохраняется повышенной несколько дней после ее разрешения.
Это нужно учитывать при повторении анализа. Изолированное повышение ЩФ может быть единственной аномалией при первичном билиарном циррозе и других болезнях, протекающих с холестазом.
Подъем ЩФ при нормальных или слегка повышенных уровнях других показателей может также указывать на инфильтративный процесс.
Каждый раз при подъеме ЩФ приходится решать вопрос, печеночное или костное она имеет происхождение.
Известно также, что ЩФ может повышаться при раках без поражения печени или костей за счет одного изофермента, который теперь называют изоэнзимом Рейгана. Фракционное определение изоферментов ЩФ позволяет установить источник повышения ее активности.
Более специфичным тестом, чем ЩФ, является определение 5’-нуклеотидазы, также из семейства фосфатаз, она существенно повышается только при болезнях печени с холестазом (также содержится и в других органах, но не в костях). Другим способом оценки источника служит определение ГГТП.
Этот фермент локализован на каналикулярной мембране гепатоцита, но также обнаруживается в почках, поджелудочной железе, кишечнике и в меньшей степени в сердечной мышце. В костях этот фермент отсутствует. Таким образом, подъем ГГТП подтверждает печеночный генез подъема ЩФ. Вообще же ГГТП повышается при многих ситуациях, например у алкоголиков. Изолированное повышение ГГТП может наблюдаться даже после эпизодического приема алкоголя на фоне противосудорожной терапии или приема варфарина. Причинами повышения ГГТП могут быть болезни гепатобилиарные, поджелудочной железы, алкогольная интоксикация, ХОБЛ, диабет, острый инфаркт миокарда, лекарства.
Сайт предоставляет справочную информацию. Адекватная диагностика и лечение болезни возможны под наблюдением добросовестного врача. У любых препаратов есть противопоказания. Необходима консультация специалиста, а также подробное изучение инструкции!
- повышение активности ферментов, постоянно присутствующих в крови
- понижение активности ферментов, постоянно присутствующих в крови
- появление в крови ферментов, которые в норме отсутствуют
- аминотрансферазы (АСТ и АЛТ)
- лактатдегидрогеназа (ЛДГ)
- щелочная фосфатаза (ЩФ)
- глутаматдегидрогеназа (ГлДГ)
- сорбитолдегидрогеназа (СДГ)
- γ-глутамилтрансфераза (ГГТ)
- фруктозо-монофосфат-альдолаза (ФМФА)
Виды ферментов – мембранные, цитоплазматические и митохондриальные
Ферменты могут располагаться в мембране, цитоплазме или митохондриях гепатоцитов. Каждый фермент имеет свое строгое место. Легко повреждаемые ферменты находятся в мембране или цитоплазме гепатоцитов. К этой группе относят – лактатдегидрогеназу, аминотрансферазы и щелочную фосфатазу. Их активность увеличивается в клинически бессимптомную фазу заболевания. При хронических повреждениях печени увеличивается активность митохондриальных ферментов (митохондрия – органелла клетки), к которым относится митохондриальная АСТ. При холестазе увеличивается активность желчных ферментов – щелочной фосфатазы.
Аланинаминотрансфераза (АЛТ, АлАТ) – норма, результат при заболеваниях печени
Нормальная активность АЛТ в крови мужчин равна 10-40 Ед/л, у женщин – 12-32 Ед/л.Различные уровни повышения активности АЛТ выявляются при острых гепатитах, циррозе печени, обтурационной желтухе и при приеме гепатотоксических препаратов (яды, некоторые антибиотики).
Резкое повышение активности АЛТ в 5-10 и более раз является несомненным признаком острого заболевания печени. Причем такое повышение выявляется еще до того как проявятся клинические симптомы (желтуха, боли и прочее). Увеличение активности АЛТ можно засечь за1-4 недели до проявления клиники и начать соответствующее лечение, не дав развиться заболеванию в полной мере. Высокая активность фермента при таком остром заболевании печени после проявления клинических симптомов держится недолго. Если нормализация активности ферментане происходит в течение двух недель, это говорит о развитии массивного повреждения печени.
Определение активности АЛТ является обязательным скрининговым тестом для доноров.
Подпишитесь на Здоровьесберегающий видеоканал


Аспартатаминотрансфераза (АСТ, АсАТ) – нормы, результат при заболеваниях печени
Максимальная активность АСТ выявлена в сердце, печени, мышцах и почках. В норме у здорового человека активность АСТ составляет 15-31 Ед/л у мужчин и 20-40 Ед/л у женщин.
Активность АСТ возрастает при некрозе печеночных клеток. Причем в данном случае имеет место прямо пропорциональная зависимость между концентрацией фермента и степенью повреждения гепатоцитов: то есть чем выше активность фермента, тем сильнее и обширнее повреждения гепатоцитов. Увеличение активности АСТ также сопровождает острый инфекционный и острый токсический гепатит (отравления солями тяжелых металлов и некоторыми лекарствами).
Соотношение активности АСТ/АЛТ называется коэффициент де Ритиса. Нормальное значение коэффициента де Ритиса равно 1,3. При повреждениях печени значение коэффициента де Ритиса снижается.
Подробную информацию о биохимическом анализе крови на фермены читайте в статье: Биохимический анализ крови
Лактатдегидрогеназа (ЛДГ) – норма, результат при заболеваниях печени
ЛДГ является широко распространенным ферментом в организме человека. Степень его активности в различных органах в убывающем порядке: почки>сердце>мышцы>поджелудочная железа>селезенка> печень>сыворотка крови. В сыворотке крови присутствует 5 изоформ ЛДГ. Поскольку ЛДГ содержится и в эритроцитах, то кровь для исследования не должна содержать следы гемолиза. В плазме крови активность ЛДГ на 40% ниже, чем в сыворотке. Нормальная активность ЛДГ в сыворотке крови составляет 140-350 Ед/л.
При каких патологиях печени увеличено содержание изоформ
В связи с широкой распространенностью ЛДГ в различных органах и тканях, повышение общей активности ЛДГ не имеет большого значения для дифференциальной диагностики различных заболеваний. Для диагностики инфекционного гепатита используют определение активности изоформ ЛДГ 4 и 5 (ЛДГ4 и ЛДГ5). При остром гепатите активность ЛДГ5 в сыворотке крови повышается в первые недели желтушного периода. Повышение совокупной активности изоформ ЛДГ4 и ЛДГ5 выявляется у всех больных инфекционным гепатитом в первые 10 суток. При желчнокаменной болезни без закупорки желчных ходов повышения активности ЛДГ не обнаружено. При ишемии миокарда происходит увеличение активности общей фракции ЛДГ за счет явления застоя крови в печени.
Щелочная фосфатаза (ЩФ) – норма, результат при заболеваниях печени
Щелочная фосфатаза располагается в мембране клеток канальцев желчных ходов. Эти клетки канальцев желчных ходов имеют выросты, которые образуют, так называемую, щеточную каемку. Щелочная фосфатаза располагается именно в этой щеточной каемке. Поэтому при повреждении желчных ходов щелочная фосфатаза высвобождается и выходит в кровь. В норме активность щелочной фосфатазы в крови колеблется в зависимости от возраста и пола. Так у здоровых взрослых людей активность щелочной фосфатазы лежит в пределах 30-90 Ед/л. Активность этого фермента повышается в периоды активного роста – при беременности и у подростков. Нормальные показатели активности щелочной фосфатазы у подростков достигают 400 Ед/л, а у беременных женщин – до 250 Ед/л.
При каких патологиях печени увеличено содержание
При развитии обтурационной желтухи активность щелочной фосфатазы в сыворотке крови возрастает в 10 и более раз. Определение активности ЩФ используют в качестве дифференциально-диагностического теста именно обтурационной желтухи. Менее значительное повышение активности щелочной фосфатазы в крови выявляется также при гепатитах, холангитах, язвенных колитах, кишечных бактериальных инфекциях и тиреотоксикозе.
Глутаматдегидрогеназа (ГлДГ) – норма, результат при заболеваниях печени
В норме глутаматдегидрогеназа присутствует в крови в небольших количествах, так как является митохондриальным ферментом, то есть, расположен внутриклеточно. Степень увеличения активности данного фермента выявляет глубину поражения печени.
Увеличение концентрации глутаматдегидрогеназы в крови является признаком начала дистрофических процессов в печени, вызванных эндогенными факторами или экзогенными. К эндогенным факторам относят опухоли печени или метастазы в печень, а к экзогенным –токсины, повреждающие печень (тяжелые металлы, антибиотики и т.д.), и инфекционные заболевания.
Коэффициент Шмидта
Совместно с аминотрансферазами рассчитывают коэффициент Шмидта (КШ). КШ = (АСТ+АЛТ)/ГлДГ. При обтурационной желтухе коэффициент Шмидта равен 5-15, при остром гепатите – более 30, при метастазах опухолевых клеток в печень – около 10.
Сорбитолдегидрогеназа (СДГ) – норма, результат при заболеваниях печени
В норме в сыворотке крови сорбитолдегидрогеназа выявляется в следовых количествах, а её активность не превышает 0,4 Ед/л. Активность сорбитолдегидрогеназы увеличивается в 10-30 раз при всех формах острого гепатита. Сорбитолдегидрогеназа является органоспецифическим ферментом, который отражает повреждение мембран гепатоцитов при первичном развитии острого процесса или при обострении хронического.
γ-глутамилтрансфераза - нормы, при каких патологиях печени увеличено содержание
Данный фермент имеется не только в печени. Максимальная активность γ-глутамилтрансферазы выявляется в почках, поджелудочной железе, печени и предстательной железе. У здоровых людей в норме концентрация γ-глутамилтрансферазы составляет у мужчин – 250-1800 нмоль/л*с, у женщин – 167-1100 нмоль/с*л. У новорожденных детей активность фермента в 5 раз выше, а у недоношенных – в 10 раз.
Активность γ-глутамилтрансферазы повышается при заболеваниях печени и желчевыводящей системы, а также при диабете. Наиболее высокая активность фермента сопровождает обтурационную желтуху и холестаз.Активность γ-глутамилтрансферазы при данных патологиях увеличивается в 10 и более раз. При вовлечении печени в злокачественный процесс происходит увеличение активности фермента в 10-15 раз, при хронических гепатитах – в 7 раз.γ-глутамилтрансфераза очень чувствительна к алкоголю, что используется для дифференциальной диагностики между вирусными и алкогольными поражениями печени.
Определение активности этого фермента является наиболее чувствительным скрининговым тестом, который предпочтительнее определения активности аминотрансфераз (АСТ и АЛТ) или щелочной фосфатазы.
Информативно определение активности γ-глутамилтрансферазы и при заболеваниях печени у детей.
Фруктозо-монофосфат-альдолаза (ФМФА) – норма, результат при заболеваниях печени
В норме в крови содержится в следовых количествах. Определение активности ФМФА используют для диагностики острого гепатита. Однако в большинстве случаев определение активности данного фермента используют для выявления профессиональной патологии у людей, которые работают с токсичными для печени химическими веществами.
При остром инфекционном гепатите активность фруктозо-монофосфат-альдолазы возрастает в десятки раз, а при воздействии токсинов в низких концентрациях (хроническом отравлении токсинами) – только в 2-3 раза.
Активность ферментов при различных патологиях печени и желчевыводящих путей
Соотношение повышений активности различных ферментов при некоторых патологиях печени и желчных путей представлены в таблице.
| Фермент | Острый гепатит | Цирроз | Холангит | Обтурационная желтуха |
| АСТ | ↑↑ | ↑ | ↑ | ↑ |
| АЛТ | ↑↑↑ | ↑ | ↑ | ↑ |
| ЛДГ | ↑↑ | – / ↑ | – | – |
| ЩФ | – | ↑ | ↑ | ↑↑↑ |
| СДГ | ↑↑↑ | ↑ (при обострении) | – | – |
| ФМФА | ↑↑ | – | – | – |
Примечание: ↑ - незначительное повышение активности фермента, ↑↑ - умеренное, ↑↑↑ - сильное повышение активности ферментов, – отсутствие изменения активности.
Подробную информацию о заболеваниях печени читайте в статьях: Гепатит ,
Итак, мы рассмотрели основные ферменты, определение активности которых может помочь в ранней диагностике или дифференциальной диагностике различных заболеваний печени. К сожалению не все ферменты используют в клинической лабораторной диагностике, снижая тем самым круг патологий, которые можно выявить на ранних стадиях. Учитывая темпы развития науки и техники, возможно, в ближайшие годы произойдет внедрение методов определения некоторых ферментов в практику лечебно-диагностических учреждений широкого профиля.
Что такое гепатит А (болезнь Боткина)? Причины возникновения, диагностику и методы лечения разберем в статье доктора Александрова Павла Андреевича, инфекциониста со стажем в 14 лет.
Над статьей доктора Александрова Павла Андреевича работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Вирусный гепатит А (Hepatitis A viruses, HAV) — острое инфекционное заболевание, вызываемое вирусом гепатита А, клинически характеризующееся синдромом общей инфекционной интоксикации, синдромом нарушения пигментного обмена, синдромами энтерита, холестаза, увеличением печени и в некоторых случая селезёнки, сопровождающееся нарушением функции печени, преимущественно доброкачественного течения.
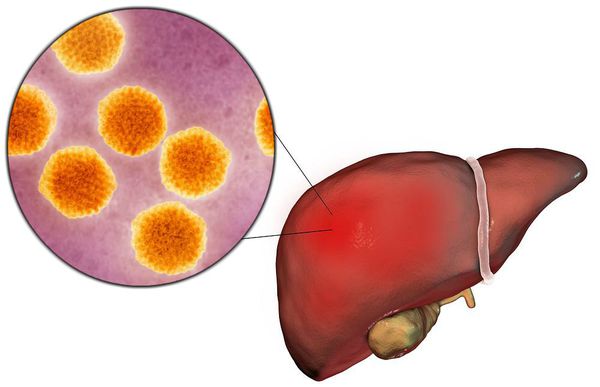
Этиология
семейство — пикорнавирусы (Picornaviridae)
вид — вирус гепатита А (HAV)
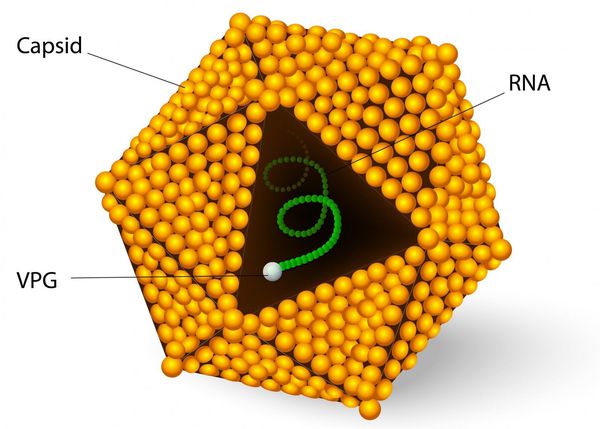
Во внешней среде очень устойчив: при температуре окружающей среды около 4°C сохраняется несколько месяцев, при 2°C — несколько лет, при замораживании очень длительно, при комнатной температуре — несколько недель. В растворе хлорсодержащих средств (0,5-1 мг/л) гибнет в течение часа, при 2,0-2,5 мг/л — в течение 15 минут, ультрафиолетовое облучение приводит к гибели в течение минуты, при кипячении сохраняется до 5 минут. В кислой среде желудка не погибает.
Наиболее значимым маркером вирусного гепатита А являются антитела класса М (анти-HAV IgM), которые образуются в начальный период заболевания и выявляются до 5 месяцев. Появление анти-HAV IgG (маркера перенесённой ранее инфекции) начинается с 3-4 недели заболевания. Антиген вируса выявляется в каловых массах за 7-10 дней до начала манифестных (явно выраженных) проявлений болезни. [1] [2] [4]
Эпидемиология
Заражение гепатитом А происходит при контакте с источником инфекции — живым человеком (больной различными формами заболевания и вирусоноситель). Больные с типичными формами являются главным источником распространения вируса (от конца скрытого и всего желтушного периодов).
Ежегодно в мире регистрируется примерно 1,5 млн случаев заболевания (количество субклинических и бессимптомных форм сложно даже представить). Смертность по миру в 2016 г., по данным ВОЗ, составила 7134 человек [10] .
Условно существует территориальное распределение по уровням инфицирования населения: высокий, средний и низкий.
Районы с высоким уровнем инфицирования это преимущественно Юго-Восточная Азия, Средняя Азия, Африка, Центральная Америка (плохие санитарные условия и низкий доход) — большинство населения к периоду взросления уже переболели и имеют иммунитет, вспышки болезни встречаются редко.
Районы со средним уровнем инфицирования — страны с переходной экономикой, развивающиеся, имеющие различия в санитарно-гигиенических условиях на территории одного региона, например Россия (большая часть населения к периоду взросления не болела и не имеет иммунитета к вирусу, возможны большие вспышки болезни).
Районы с низким уровнем инфицирования — развитые страны с высоким уровнем дохода и хорошими санитарно-гигиеническими условиями, например США, Канада, Европа, Австралия. Большинство людей не имеет иммунитета и не болела, вспышки случаются редко и чаще среди групп риска [7] .
В окружающую среду вирус выделяется преимущественно с фекалиями.
Механизм передачи: фекально-оральный (пути — водный, контактно-бытовой, пищевой), парентеральный (редко при переливании крови), половой (орально-анальный контакт).
Восприимчивость населения высокая.
Факторы риска заражения:
- высокая скученность населения;
- несоблюдение правил личной гигиены и правил хранения, обработки и приготовления продуктов питания;
- неудовлетворительное состояние объектов водоснабжения;
- бытовой очаг заболевания.
Кто находится в группе риска
- путешественники (особенно в страны жаркого климата и с плохими социальными условиями);
- гомосексуалисты;
- люди, употребляющие наркотики (любые), алкоголики;
- медработники (непривитые и не болевшие);
- бездомные;
- люди, имеющие постоянные контакты (в силу профессии или иных причин) с мигрантами из неблагополучных по гепатиту А регионов.
Характерна осенне-весенняя сезонность, повышенная привязанность к жарким южным регионам.
Иммунитет после перенесённого заболевания стойкий, пожизненный, то есть повторно заболеть нельзя [1] [3] [4] [7] [10] .
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы гепатита А
Заболевание начинается постепенно. Инкубационный период гепатита А протекает 7-50 дней.
Синдромы вирусного гепатита А:
- общей инфекционной интоксикации;
- нарушения пигментного обмена (желтуха);
- энтерита (воспаление слизистой тонкой кишки);
- холестаза (уменьшение количества желчи, поступающей в двенадцатиперстную кишку);
- гепатолиенальный (увеличение печени и селезёнки);
- отёчный;
- нарушения функции печени.
Типичное течение болезни — это желтушная форма болезни средней степени тяжести (устаревшее название — желтуха или болезнь Боткина).
Начальный период болезни (преджелтушный) имеет продолжительность от 2 до 15 дней и может протекать по нескольким вариантам:
При осмотре обнаруживается увеличение печени и, в меньшей степени, селезёнки, чувствительность края печени, повышение ЧСС (пульса), носовые кровотечения. В конце периода моча темнее, а кал становится светлее.
Следующий период (желтушный) длительностью около 7-15 дней характеризуется снижением выраженности симптомов предшествующего периода (то есть с появлением желтухи самочувствие улучшается). Усиливается желтушное окрашивание склер, кожных покровов и слизистой оболочки ротоглотки. Моча приобретает цвет тёмного пива, кал белеет. Присутствует общая слабость, недомогание, плохой аппетит, чувство тяжести и переполненности в правом подреберье, больной расчёсывает себя из-за зуда кожи (лихенификация), появляются петехии (мелкие кровоизлияния) на коже.
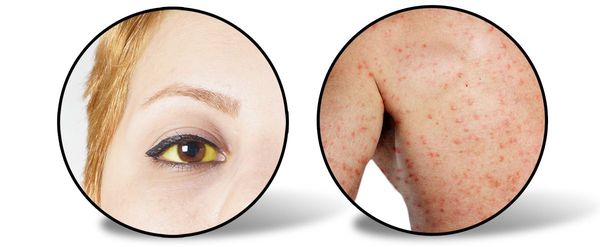
При врачебном исследовании выявляется увеличение печени и селезёнки, явственно положителен симптом Ортнера (болезненность при поколачивании ребром ладони по правой рёберной дуге), гипотония (может быть и нормотония), токсическая брадикардия (снижение ЧСС), появляются периферические отёки, возможны боли в суставах (артралгии).
Далее при благоприятном течении заболевания (которое наблюдается в большинстве случаев) происходит регресс клинической симптоматики, осветление мочи и потемнение кала, более медленное спадение желтушности кожи, склер и слизистых оболочек.
Под нетипичным течением болезни подразумеваются лёгкие безжелтушные формы гепатита А (отсутствие симптомов или лёгкая слабость без желтухи, тяжесть в правом подреберье), фульминантные формы.
Факторы, увеличивающие риск тяжёлого течения гепатита А:
Последствия для беременных
У беременных гепатит А протекает в целом несколько тяжелее, чем у небеременных. Примерно в 36 % случаев возможно развитие слабости родовой деятельности, преждевременные роды (31-37 неделя) и послеродовые кровотечения. Вирус не проникает через плаценту, то есть какого-то специфического действия на плод не оказывает. В грудном молоке вирус не содержится [1] [2] [4] [7] .
Патогенез гепатита А
Воротами для проникновения вируса является слизистая оболочка органов желудочно-кишечного тракта, где происходит его первичное размножение в эндотелиальной выстилке тонкого кишечника и мезентериальных лимфоузлах.
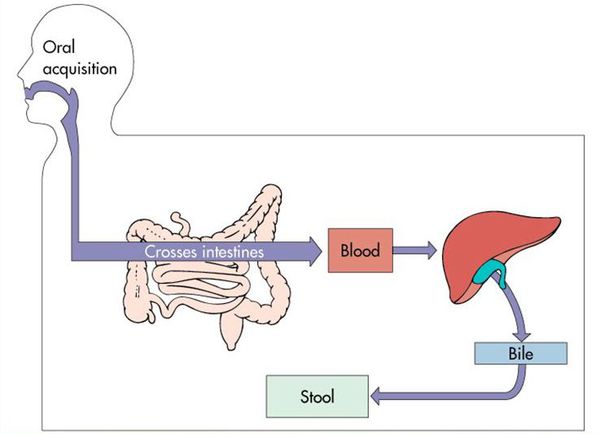
Далее происходит гематогенное распространение вирусных частиц и проникновение их в печень, где они локализуются в ретикулогистиоцитарных клетках Купфера и гепатоцитах. В результате этого происходит повреждение клеток:
- проникновение вируса в клетку;
- захват лизосомой;
- разрушение белковой оболочки вируса;
- сборка белков по программе вирусной РНК;
- встраивание этих белков в цитолемму клетки;
- образование патологических пор в оболочке клетки;
- поступление внутрь клетки ионов натрия и воды;
- баллонная дистрофия (разрушение ультраструктур клетки и образование крупных вакуолей) с последующим некрозом (его объём, как правило, ограничен);
- гибель клетки и лимфоцитарная иммунная реакция, приводящая к основному объёму поражения.
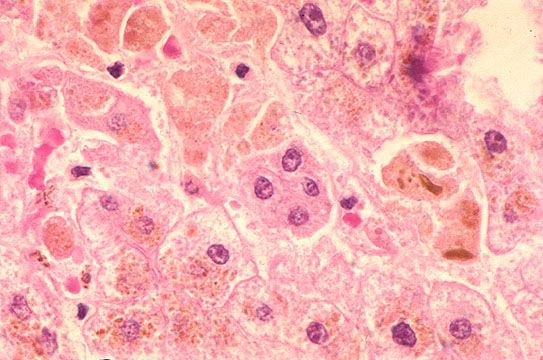
В дальнейшем вирус попадает в желчь, с ней он проникает в кишечник и выводится в окружающую среду с фекалиями. Вследствие компетентных реакций иммунной защиты размножение вируса заканчивается, и он покидает организм больного. [2] [3] [4]
Классификация и стадии развития гепатита А
По степени разнообразия проявлений выделяют две формы гепатита А:
- клинически выраженная (желтушная, безжелтушная, стёртая);
- субклиническая (инаппарантная).
По длительности течения также выделяют две формы гепатита А:
- острая циклическая (до трёх месяцев);
- острая затяжная (более трёх месяцев).
Степени тяжести гепатита А:
- лёгкая;
- среднетяжёлая;
- тяжёлая;
- фульминатная (молниеносная).
Согласно МКБ-10 (Международной классификации болезней десятого пересмотра), заболевание подразделяют на три вида:
- В15. Острый гепатит А;
- В15.0. Гепатит А с печёночной комой;
- В15.9. Гепатит А без печёночной комы. [2][4]
Осложнения гепатита А
Заболевание может привести к следующим осложнениям:
- печёночная кома (дисфункция центральной нервной системы, связанная с тяжёлым поражением печени — встречается крайне редко);
- холецистохолангит (выраженные боли в правом подреберье, нарастание желтухи и зуда кожи);
- гемолитико-уремический синдром, преимущественно у детей (гемолитическая анемия, тромбоцитопения, острая почечная недостаточность);
- развитие аутоиммунного гепатита I типа.
Гепатит А не приводит к формированию хронических форм, однако из-за выраженного воспалительного процесса возможно появление длительных резидуальных (остаточных) явлений:
- дискинезия (нарушение моторики) желчевыводящих путей;
- постгепатитная гепатомегалия (увеличение размеров печени из-за разрастания соединительной ткани);
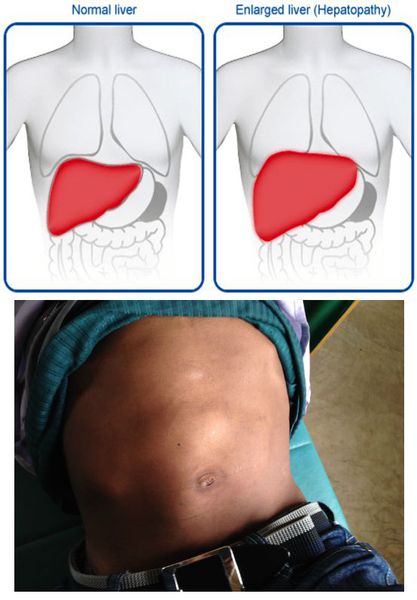
- постгепатитный синдром (повышенная утомляемость, аснено-невротические проявления, тошнота, дискомфорт в правом подреберье). [1][5]
Диагностика гепатита А
Методы лабораторной диагностики:
- Клинический анализ крови — нормоцитоз или лейкопения, лимфо- и моноцитоз, нейтропения, СОЭ в норме или снижена.
- Биохимический анализ крови — повышение общего билирубина и в большей степени его связанной фракции (реакция Эрлиха), повышение аланинаминотрансферазы и аспартатаминотрансферазы, снижение протромбинового индекса, повышение тимоловой пробы (снижение альбуминов и повышение гамма-глобулинов), повышение гамма-глутамилтранспептидазы, щелочной фосфатазы и другие показатели.
- Биохимический анализ мочи — появление уробилина и желчных пигментов за счёт прямого билирубина. Ранее, особенно в вооруженных силах, для выявления больных на начальной стадии практиковалось использование пробы Разина: утром производится опускание индикаторной полоски в мочу (при наличии уробилина она меняет цвет), и военнослужащий с подозрением на заболевание госпитализировался для углублённого обследования. Тест на уробилин становится положительным в самом начале заболевания — в конце инкубационного периода из-за болезни печёночной клетки.
- Серологические тесты — выявления анти-HAV IgM и анти-HAV IgG методом ИФА (иммуноферментного анализа) в различные периоды заболевания и HAV RNA с помощью ПЦР-диагностики (полимеразной цепной реакции) в острый период.
- Ультразвуковое исследование органов брюшной полости — увеличение печени и иногда селезёнки, реактивные изменения структуры печёночной ткани, лимфаденопатия ворот печени.
Обследование лиц, бывших в контакте с больным
Лица, контактирующие с больным вирусным гепатитом А, подлежат осмотру врачом-инфекционистом с последующим наблюдением до 35 дней со дня разобщения с больным. Наблюдение включает термометрию, осмотр кожных покровов, определение размеров печени и селезёнки, а также лабораторное обследование (АЛТ, общий билирубин, антитела классов М и G к вирусу гепатита А вначале и через три недели от первичного обследования).
Дифференциальная диагностика проводится со следующими основными заболеваниями:
- в начальный период: ;
- гастрит, гастроэнтероколит;
- полиартрит;
- энтеровирусная инфекция;
- в желтушный период: ;
- псевдотуберкулёз; ;
- желтухи другой этиологии (гемолитическая болезнь, токсические поражения, опухоли ЖКТ и другие заболевания);
- гепатиты другой этиологии (вирусные гепатиты В, С, Д, Е и другие, аутоиммунные гепатиты, болезнь Вильсона — Коновалова и т.п.) [1][2][3][4][9] .
Лечение гепатита А
Этиотропная терапия (направленная на устранение причины заболевания) не разработана.
Медикаменты
В зависимости от степени тяжести и конкретных проявлений назначается инфузионная терапия с глюкозо-солевыми растворами, обогащёнными витаминами. Показано назначение сорбентов, препаратов повышения энергетических ресурсов, при необходимости назначаются гепатопротекторы, в тяжёлых случаях — гормональные препараты, препараты крови, гипербарическая оксигенация и плазмаферез.
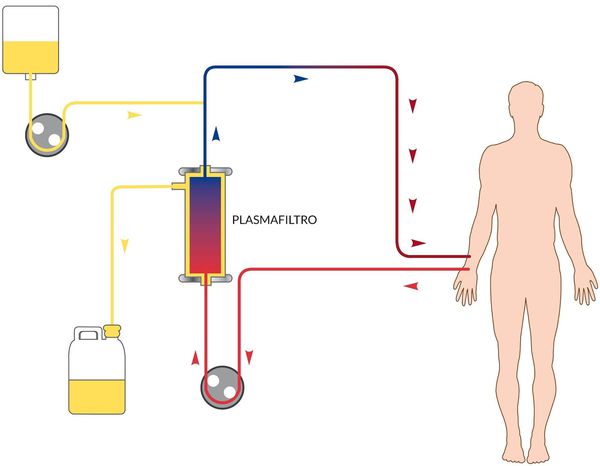
Нужна ли госпитализация
В случае лёгких форм гепатита А лечение может проводиться на дому (при наличии условий). Госпитализация потребуется, начиная со среднетяжёлых форм, лицам групп риска по тяжёлому течению, пациентам с осложнёнными формами, беременным и детям. Каких-либо особенностей при дальнейшем лечении вирусного гепатита А у детей нет.
Режим постельный или полупостельный. При гепатите А нарушаются процессы образования энергии в митохондриях, поэтому предпочтителен длительный отдых.
Лечение в стационаре и выписка
Лечение гепатита А проходит в инфекционном отделении больницы. Выписка пациентов происходит после появления стойкой и выраженной тенденции к клиническому улучшению, а также улучшения лабораторных показателей.
Критерии выписки больных:
- стойкая и выраженная тенденция к клиническому улучшению (отсутствие интоксикации, уменьшение размеров печени, регресс желтухи);
- стабильное улучшение лабораторных показателей (нормализация уровня билирубина, значительное снижение уровня АЛТ и АСТ).
При неосложнённых формах реконвалесценты (выздоравливающие больные) подлежат наблюдению в течении трёх месяцев с осмотром и обследованием не реже одного раза в месяц. [2] [3] [6]
Физиотерапия
В фазе реконвалесценции, особенно при затяжных формах болезни, возможно применение физиотерапевтических методов лечения:
- грязевых аппликаций на область правого подреберья;
- акупунктуры;
- массажа проекции области печени, желчного пузыря, желчевыводящих протоков.
Диета
Показана диета № 5 по Певзнеру — механически и химически щадящая, употребление повышенного количества жидкости и витаминов, запрет алкоголя. Исключается острое, жареное, копчёное, ограничивается кислое и соль. Все блюда готовятся на пару, тушатся, отвариваются и подаются только в тёплом виде.
Прогноз. Профилактика
Прогноз заболевания, как правило, благоприятный. Пациенты выздоравливают спустя 1-3 месяца после выписки из стационара. В редких случаях заболевание приобретает затяжной характер.
Критерии излеченности:
- отсутствие интоксикации;
- полная нормализация уровня билирубина, АЛТ и АСТ;
- нормализация размеров печени и селезёнки;
- появление в крови антител к вирусу гепатита А класса G (Anti-HAV-IgG).
Неспецифические мероприятия, позволяющие снизить количество случаев инфицирования:
- обеспечение условий и факторов потребления безопасной питьевой воды (водоснабжение);
- обеспечение и контроль за соблюдением утилизации сточных вод (канализационное хозяйство);
- контроль за качеством обследования персонала, связанного с пищевой промышленностью;
- контроль и соблюдение технологии хранения, приготовления и транспортировки пищевых продуктов и воды.
К личным профилактическим мерам относится тщательное мытьё рук после посещения туалета, смены подгузников, а также перед приготовлением или приёмом пищи.
Вакцинация
Специфическим профилактическим мероприятием является проведение иммунизации против гепатита А: практически у 100% привитых двукратно людей вырабатывается стойкий иммунитет, предотвращающий развитие заболевания. Вакцинация — это самый лучший способ предотвратить заражение.
Читайте также:

