Повышенный гемоглобин у вич инфицированных чем опасен
Обновлено: 24.04.2024
19531 04 Сентября
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
ВИЧ: причины появления, симптомы, диагностика и способы лечения.
Определение
ВИЧ (вирус иммунодефицита человека) – инфекционное хроническое заболевание, передающееся контактным путем, медленно прогрессирующее и характеризующееся поражением иммунной системы с развитием синдрома приобретенного иммунодефицита (СПИДа). СПИД – это финальная стадия ВИЧ-инфекции, когда из-за ослабленной иммунной системы человек становится беззащитным перед любыми инфекциями и некоторыми видами рака. Опасность представляют так называемые оппортунистические инфекции – заболевания, вызываемые условно-патогенной или непатогенной флорой: вирусами, бактериями, грибами, которые у здоровых людей не приводят к серьезным последствиям или протекают легко и излечиваются самостоятельно. При СПИДе они наслаиваются друг на друга, имеют затяжное течение, плохо поддаются терапии и могут стать причиной летального исхода.
Причины появления ВИЧ
Источником инфекции является человек, инфицированный ВИЧ, на любых стадиях заболевания. Вирус передается через кровь, сперму, секрет влагалища, грудное молоко.
Половой путь (незащищенный секс с инфицированным партнером) – доминирующий фактор распространения ВИЧ-инфекции.
Передача ВИЧ от матери ребенку может произойти на любом сроке беременности (через плаценту), во время родов (при прохождении через родовые пути) и грудного вскармливания (при наличии язвочек, трещин на сосках матери и во рту ребенка).
Высокий риск инфицирования существует при внутривенном введении наркотических веществ нестерильными шприцами, при переливании ВИЧ-инфицированной крови и ее препаратов, использовании медицинского и немедицинского инструментария, загрязненного биологическими жидкостями человека, инфицированного ВИЧ. Кроме того, опасность могут представлять органы и ткани доноров, используемые для трансплантации.

Попадая в кровоток, вирус проникает в Т-лимфоциты хелперы, или CD-4 клетки (рановидность лейкоцитов), которые помогают организму бороться с инфекциями. Т-хелперы имеют на поверхности так называемые CD4-рецепторы. ВИЧ связывается с этими рецепторами, проникает в клетку, размножается в ней и в конечном счете уничтожает ее. Со временем вирусная нагрузка увеличивается, а количество Т-хелперов снижается.
При отсутствии лечения через несколько лет из-за значительного снижения числа Т-хелперов появляются связанные со СПИДом состояния и симптомы.
Классификация заболевания
- Стадия инкубации - от момента заражения до появления реакции организма в виде клинических проявлений острой инфекции и/или выработки антител (специфических белков, продуцируемых в ответ на проникновение антигена, в данном случае – вируса).
- Стадия первичных проявлений клинических симптомов:
В дальнейшем продолжается активное размножение вируса и разрушение Т-лимфоцитов, развивается стадия вторичных изменений, для которой характерно прогрессирующее снижение веса, общая слабость, стойкое повышение температуры, озноб, выраженная потливость. Клинические проявления оппортунистических заболеваний обусловливают клиническую картину этой стадии: пациентов беспокоят кашель и одышка, тошнота, рвота, боли в животе, тяжелая диарея, кожные высыпания, сильные головные боли, снижение памяти и внимания и др.
Диагностика ВИЧ
Лабораторные методы исследования:
Скрининг (обследование здоровых людей) на ВИЧ должен быть проведен любому человеку, который считает, что может быть заражен, а также перед любой госпитализацией и операцией, всем беременным женщинам и их половым партнерам.
Обследование целесообразно проходить людям с высоким риском заражения ВИЧ, например, при наличии заболеваний, имеющих одинаковый с ВИЧ-инфекцией механизм передачи (вирусные гепатиты В и С, заболевания, передающиеся половым путем), лицам, имеющим регулярные незащищенные половые контакты, инъекционным наркоманам, детям, рожденным от матерей с ВИЧ-инфекцией, медицинским работникам, напрямую контактирующим с кровью на работе и др.
Существуют экспресс-тесты для скрининга ВИЧ, которые можно делать в домашних условиях. Для определения специфических антител/антигенов к ВИЧ (ВИЧ-1, 2, антиген p24) используют кровь, слюну или мочу. Точность любого экспресс-теста ниже, чем теста, проводимого в лаборатории.
Для стандартного скринингового обследования определяют антитела к ВИЧ 1 и 2 и антиген ВИЧ 1 и 2 (HIV Ag/Ab Combo) в крови с помощью иммуноферментного анализа (ИФА).
Внимание. При положительных и сомнительных реакциях, срок выдачи результата может быть увеличен до 10 рабочих дней. Синонимы: Анализ крови на антитела к ВИЧ1 и 2 и антиген ВИЧ1 и 2; ВИЧ-1 p24; ВИЧ-1-антиген, p24-антиген; ВИЧ 1 и 2 антитела и антиген p24/25, ВИЧ тест-системы 4-г.

Показатели гемоглобина при ВИЧ-инфекции часто отличаются он нормальных значений здорового человека. У инфицированных людей отклонения в большую или меньшую сторону могут указывать на прогрессирование основного заболевания или возникновение осложнений. Чтобы не допустить развития таких событий, лучше знать, какая норма гемоглобина при ВИЧ и что должно насторожить при такой патологии.
Что такое ВИЧ-инфекция

Первое время организм справляется с инфекцией, вырабатывая большое количество новых клеток взамен массовой гибели пораженных. По мере прогрессирования болезни компенсация становится недостаточной. В результате количество иммунных клеток резко снижается, что приводит к снижению иммунитета. Организм остается без надежной защиты перед негативными внешними и внутренними факторами.
Быстрая способность мутировать – одна из особенностей ВИЧ. Поэтому до сих пор не создано ни одного медикамента, способного устранить инфекцию.
Вирус попадает в организм от человека-носителя. Заражение происходит через контакт с инфицированной кровью, слюной, грудным молоком, спермой, вагинальным секретом, лимфой. При этом следует учитывать, что заражение произойдет, когда перечисленный биоматериал попадет в системный кровоток. Поэтому инфекция проникает в кровь через раны, ссадины, микротравмы слизистой рта, половых органов и т.п.
Болезнь длится от нескольких месяцев до нескольких лет. Но на протяжении всего периода, она целенаправленно разрушает иммунную систему. Проявляет себя инфекция различными симптомами. Синдром приобретенного иммунодефицита очень сильно снижает защитные силы организма. В результате к основному заболеванию часто присоединяется вторичная инфекция, появляются новообразования злокачественной природы.
Гемоглобин и другие показатели при ВИЧ

Клинический анализ крови – одновременно простой и важный метод лабораторной диагностики для выявления вируса иммунодефицита человека. У инфицированных больных серьезные изменения показателей крови может не наблюдаться долгое время. Очень часто требуется проведение других диагностических исследований.
Нормальные показатели Hb
Если инфицированный человек проходит специальный комплекс антиретровирусной терапии, то изменения в крови могут не фиксироваться в течение десятилетий. Прием лекарственных препаратов позволяет добиться стойкой ремиссии. Поэтому нормальные значения гемоглобина в крови у этих пациентов такие же, как и у здоровых людей:
- для мужчин – 130-150 г/л;
- для женщин – 120-140 г/л.
Частый спутник ВИЧ-инфекции – анемия. Такое состояние не только ухудшает качество жизни, но и становится причиной летального исхода.
Отклонения в крови при ВИЧ
Нарушения в крови могут указывать как на наличие инфекции, так и на другие процессы. Вирус иммунодефицита человека часто сопровождается следующими изменениями в лабораторных анализах крови:
На фоне нарушения работы эритроцитов очень часто снижается уровень гемо белка, что приводит к анемии.
Какое СОЭ при ВИЧ
Нормальные значения скорости соединения эритроцитов (СОЭ) у мужчин и женщин находятся в диапазоне – 2-20 мм/ч. Уровень повышается, когда в организм попадает инфекция или возникает воспалительный процесс. Изменения в большую сторону свидетельствуют о высокой активности иммунной системы. Если анализы показывают уровень СОЭ выше 50 мм/ч, то такие значения могут указывать на поражение организма вирусом иммунодефицита человека. Однако специалисты обязательно учитывают, что такие нарушения могут спровоцировать другие состояния, болезни, например:
- сердечный приступ;
- воспалительные заболевания;
- период вынашивания ребенка;
- ревматизм.
Показатель СОЭ при ВИЧ-инфекции может долгое время не изменяться и находиться в пределах нормы. Скорость соединения эритроцитов является недостаточным показателем для диагностики вируса. Необходимо получение комплексной информации о состоянии крови. Одновременное изменение уровня Hb и СОЭ должно насторожить.
Какой гемоглобин при ВИЧ должен насторожить больного

Когда уровень гемоглобина падает ниже 110-115 г/л, то это уже должно насторожить, т.к. показатели указывают на развитие анемии. Для такого состояния характерно снижение концентрации гемо белка и эритроцитов в крови. Появляются такие симптомы как головокружение, тошнота, сонливость, слабость, тахикардия, головная боль и т.п. Все эти признаки еще сильнее усугубляют ситуацию.
Заболевание выявляют у 8 инфицированных пациентов из 10. Поэтому врачи уделяют особое внимание лечению и предупреждению малокровия.
Уровень гемоглобина при ВИЧ-инфекции может не изменяться долгое время и находиться в допустимых пределах. Падение наблюдается при ухудшении состояния и отсутствии адекватной терапии. Снижение Hb требует лечения. Отсутствие терапии может существенно ухудшить качество жизни, а в некоторых случаях даже привести к смерти. Общий анализ крови не позволяет 100% выявить ВИЧ-инфекцию.
Показатели метаболизма железа определены у 86 ВИЧ-инфицированных пациентов с анемией. У 51,2 и 61,6% пациентов, соответственно, было выявлено снижение уровня сывороточного железа и коэффициента насыщения трансферрина. В соответствии с модифицированным алгоритмом G.Weiss у 30,2% пациентов со сниженным коэффициентом насыщения трансферрина диагностирована железодефицитная анемия, у 58,5% пациентов — анемия хронического заболевания (АХЗ), у 11,3% больных — сочетанный вариант анемии. Доля АХЗ была наиболее значимой у пациентов с высокой вирусной нагрузкой и клинико-лабораторными признаками иммуносупрессии. Антиретровирусная терапия сопряжена с улучшением показателей гемоглобина у всех больных с анемией хронического заболевания.
Anemia of chronic disease and HIV-infection
Indicators of iron metabolism are defined in 86 HIV-infected patients with anemia. At 51.2 and 61.6% of patients, respectively, showed a reduction in serum iron and transferrin saturation ratio. In accordance with the modified algorithm G. Weiss in 30.2% of patients with a reduced rate of transferrin saturation diagnosed with iron deficiency anemia, with 58.5% of patients — anemia of chronic disease (ACD), in 11.3% of patients — combines option anemia. The share of ACD was most significant in patients with high viral load and clinical and laboratory evidence of immunosuppression. Antiretroviral therapy involves improvements in hemoglobin in all patients with anemia of chronic disease.
Цель нашего исследования — оценить долю и значимость АХЗ в структуре анемии у пациентов с ВИЧ-инфекцией для совершенствования диагностической и лечебной тактики.
Статистическая обработка полученных данных проводилась при помощи программ СТАТИСТИКА 7.0, SPSS Statistics 17.0 и Microsoft Exell 2007.
Результаты исследования и их обсуждение
У 51,2 и 61,6% пациентов, соответственно, было выявлено снижение СЖ и КНТ ниже нормы, свидетельствующее о высокой распространенности дефицита функционального (сывороточного) железа в популяции ВИЧ-инфицированных. Для дифференциальной диагностики ЖДА и АХЗ был применен модифицированный нами алгоритм Guenter Weiss, 2005 [5] .
Изменения диагностического алгоритма заключались в следующем:
1) В отличие от автора, дифференциальная диагностика проводилась всем пациентам с уровнем КНТ менее 0,20 (т.е. ниже нормальных значений), а в оригинальной методике — при КНТ ниже 0,16.
2) Авторы методики определяли отношение концентрации РРТ к десятичному логарифму уровня ферритина только у пациентов с уровнем ферритина 30-100 нг/мл, тогда как пациенты с уровнем ферритина более 100 нг/мл автоматически были отнесены ими в группу страдающих АХЗ. У наших же пациентов с показателями ферритина выше 100 нг/мл наблюдались несомненные клинико-анамнестические и лабораторные признаки ЖДА (проявления геморрагического синдрома, крайне низкие показатели сывороточного железа и пр.). В связи с этим во избежание диагностической ошибки мы расширили показания для определения РРТ, включив в исследуемую группу всех пациентов с уровнем ферритина более 30 нг/мл.
Итоговый диагностический алгоритм анемий выглядел следующим образом (рисунок 1):
Рисунок 1. Алгоритм дифференциальной диагностики АХЗ, ЖДА и сочетанного варианта течения анемии

Из рисунка видно, что КНТ менее 0,2 был выявлен нами у 53 пациентов (62% пациентов исследуемой группы). У всех этих пациентов было проведено определение уровня ферритина. Показатель его концентрации менее 30 нг/мл выявлен у 16 пациентов; им был выставлен диагноз железодефицитной анемии, подтвержденный также другими клинико-лабораторными данными. У всех этих пациентов за исключением двоих, получающих зидовудин или ставудин, наблюдались выраженные микроцитоз и гипохромия, т.е., признаки, характерные для ЖДА (одним из побочных эффектов зидовудина и ставудина является, как известно, макроцитоз эритроцитов). Кроме того, семеро больных этой группы имели анамнестические и клинические признаки геморрагического синдрома (в т.ч., у двух — кровотечения из трофических язв, у двух женщин — дисфункциональные маточные кровотечения, у одного пациента — рецидивирующие кровотечения из геморроидальных вен, у одного — частые и обильные носовые кровотечения и у одного — кишечное кровотечение).
У пациентов с уровнем ферритина более 30 нг/мл было определено отношение РРТ к десятичному логарифму ферритина, при этом отношение менее 1,5 установлено у 31 пациента, отношение более 1,5 — у шестерых.
Мы попытались установить возможную связь разных видов анемии в группах пациентов с гендерными, клиническими и лабораторными различиями. Корреляция изучаемых показателей с полом заболевших не выявлена. Чаще всего АХЗ диагностировалась в группе больных с легкой степенью анемии (показатели Нb≥90 г/л) — у 65,7% пациентов, тогда как нарастание ее тяжести (снижение уровня Нb ниже 90 г/л) ассоциировалось с уменьшением доли больных с АХЗ до 44,4% и, соответственно, с увеличением доли пациентов с ЖДА.
Свою самостоятельную роль в генезе анемии хронического заболевания при ВИЧ-инфекции могут играть как сам вирус и оппортунистические патогены, напрямую воздействующие на процессы созревания и разрушения эритроцитов, так и образующиеся в процессе болезни провоспалительные цитокины [6, 7].
Мы проанализировали частоту АХЗ и ЖДА в подгруппах пациентов с различными уровнями вирусной нагрузки и иммуносупрессии (таблица 1).
Анемия и показатели активности инфекционного процесса у обследованных пациентов с ВИЧ-инфекцией
Анемия часто встречается у ВИЧ-инфицированных пациенток, составляя примерно 30 % в начальной бессимптомной стадии инфекции, и доходит до 80-90% при прогрессировании заболевания [5]. Применение антиретровирусной терапии и химиопрофилактики во время беременности и в родах снизили риск перинатальной передачи ВИЧ-инфекции до 1-2% [1]. Однако, несмотря на очевидный положительный эффект антиретровирусной терапии и химиопрофилактики, специалистам приходится иметь дело и с - побочными эффектами данных препаратов.
Основными причинами анемии при ВИЧ-инфекции являются:
- Снижение продукции эритроцитов вследствие неопластической инфильтрации костного мозга, инфекционного поражения костного мозга, приема антиреретровирусных лекарственных препаратов.
- Неэффективная продукция эритроцитов вследствие дефицита фолиевой кислоты и витамина В12. Во время беременности ВИЧ-инфицированные пациентки предрасположены к мальабсорбции, которая, по-видимому, вызывается самой инфекцией.
- Гемолиз эритроцитов с их значительным фагоцитозом макрофагами костного мозга и выработкой аутоантител с положительной пробой Кумбса, сниженной резистентностью эритроцитов [3,4].
Угнетение кроветворения при проведении химиопрофилактики у беременных имеет важное значение для анестезиолога-реаниматолога, так как понимание генеза данного осложнения помогает провести правильную коррекцию возникших нарушений в периоперационном периоде. Некоторые антиретровирусные препараты, особенно нуклеозидные ингибиторы обратной транскриптазы (в первую очередь зидовудин), угнетают кроветворение, эритропоэз и вызывают анемию [2]. Не стоит забывать, что зидовудин отличается выраженным миелотоксическим эффектом, в связи с чем данный препарат не назначается лицам с тяжелой анемией (Hb ? 70 г/л) а при развитии тяжелой анемии на фоне АРВТ – заменяется на другой препарат, не имеющий подобных побочных эффектов (чаще диданозин).
Для анемии, возникающей вследствие применения нуклеозидных ингибиторов обратной транскриптазы, в частности, зидовудина, характерно развитие макроцитоза (средний объем эритроцитов > 100 fl), что может быть использовано как объективный критерий угнетения кроветворения на фоне АРВТ [2]. Макроцитарная анемия, вызываемая химиопрофилактикой, не всегда связана с дефицитом витамина В12 или фолиевой кислоты, а, следовательно, не поддается лечению данными препаратами. Предстоящее оперативное родоразрешение и анемия тяжелой степени диктует необходимость отмены нуклеозидных ингибиторов обратной транскриптазы (в особенности зидовудина, ламивудина). Препаратом выбора для коррекции анемии на фоне АРВТ служит рекомбинантный эритропоэтин, предпочтительно, длительного действия, в редких случаях приходится прибегать к гемотрансфузии [7].
Согласно вышеприведенным данным, анемия является частым осложнением у ВИЧ-инфицированных беременных, принимающих антиретровирусные препараты, что ухудшает течение послеоперационного периода и предопределяет необходимость целенаправленной профилактики и лечения анемии у ВИЧ-инфицированных беременных.
Цель исследования
На основании показателей клинического анализа крови и морфологической картины эритроцитов выявить характер анемии у ВИЧ-инфицированных беременных, получающих препараты для химиопрофилактики, а также определить пути коррекции.
Материал и методы исследования
Контрольная группа (КГ) включала 139 пациенток с неосложненным течением беременности. В исследование основной группы были включены ВИЧ-инфицированные беременные с III-ей стадией заболевания, со сроком гестации 37-38 недель, которым выполнялось плановое элективное кесарево сечение. Пациентки основной и контрольной групп были сопоставимы по возрасту, сроку гестации, антропометрическим данным (табл. № 1).
Таблица 1
Некоторые характеристики больных, включенных в исследование
| Показатель | Основная группа (n=162) | Контрольная группа (n=139) |
| Возраст (годы) | 28,9±6,9 | 29,2±5,7* |
| Рост (см) | 163,9±7,28 | 162,6±6,4* |
| Вес (кг) | 75,3±5,4 | 78,4±6,3* |
| Срок гестации | 37,8±0,82 | 38,2±0,74* |
| ASA (II-III) | 85/77 | 92/47 |
Примечание: * Р> 0,05
При дальнейшем проведении исследования пациентки основной группы были рандомизированны на 2 подгруппы: I подгруппа – ВИЧ-инфицированные беременные, получающие специфическую предоперационную терапию, направленную на коррекцию анемии. С этой целью назначались внутривенные препараты железа [железа (III)-гидроксид декстран 150 мг внутривенно капельно через день)], фолиевая кислота - 10 мг/сутки, химически синтезированный активатор рецепторов эритропоэтина длительного действия (Мирцера) - 0,6 мкг/кг в/в однократно. II подгруппа – ВИЧ-инфицированные беременные, которым проводилась специфическая предоперационная терапия, однако, химически синтезированный активатор рецепторов эритропоэтина длительного действия (Мирцера) пациенткам II подгруппы не назначался. КГ была представлена пациентками с физиологическим течением беременности, сроком гестации 37-38 недель, которые не нуждались в специфической предоперационной терапии. Критерии исключения из исследования для ВИЧ-инфицированных беременных были следующие: наличие I, II, IV стадии ВИЧ-инфекции, отказ от приема антиретровирусных препаратов во время беременности, наличие тяжелых соматических заболеваний у ВИЧ-инфицированных беременных, влияющих на изучаемые показатели. Критерием исключения из исследования для беременных с физиологическим течением беременности служило наличие тяжелых соматических заболеваний, влияющих на изучаемые показатели.
У всех больных основной группы после измерения стартовых параметров и регистрации стартовых анализов проводили предоперационную подготовку в течение 7 дней. Предоперационная подготовка в контрольной группе не проводилась. Исследование пациенток ОГ и КГ проводилось на следующих этапах: I этап - исходный этап, до начала проведения предоперационной подготовки; II этап - на 7-е сутки лечения, непосредственно перед операцией; III этап - во время оперативного вмешательства, на этапе гемостаза мягких тканей; IV этап - через сутки после оперативного вмешательства;
V этап – на 5 сутки после оперативного вмешательства;
Премедикация накануне оперативного вмешательства в обеих группах была представлена рутинным назначением диазепама (10 мг в/м) и ингибитора протонной помпы омеза (20 мг перорально). Оперативное вмешательство в обеих группах проводилось в условиях в условиях спинальной анестезии маркаином с выполнением Гарвардского стандарта мониторинга.
Статистический анализ полученных данных включал описательную статистику по каждому исследуемому показателю, а также проверку гипотезы о статистической значимости различия средних значений трех групп с помощью дисперсионного анализа на уровне значимости, равном 0,05 и последующим попарным сравнением с учетом поправки Бофферони. Для сравнения частот осложнений были рассчитаны частотные характеристики выборок в обеих группах, относительный риск (ОР) и 95% доверительный интервал ОР. Вся процедура обработки данных выполнена с использованием пакета статистических программ SPSS 6.0. Различия между выборками считались достоверными при Р < 0,05.
Результаты исследования и их обсуждение
Согласно литературным данным, приём антиретровирусных препаратов, особенно нуклеозидных ингибиторов обратной транскриптазы, зачастую сопровождается угнетением кроветворения, что приводит к возникновению макроцитарной анемии. В табл. 1 представлена динамика некоторых гематологических показателей показателей на этапах исследования.
Таблица 1
Динамика некоторых гематологических показателей у обследованных нами пациенток
Примечание:
P12 - ошибка при сравнении средних значений ОГ I со средними контрольной группы;
P13 - ошибка при сравнении средних значений ОГ II со средними контрольной группы;
P23 - ошибка при сравнении средних значений ОГ I со средними ОГ II;
* - статистически значимое различие между средними основных групп и соответствующими средними контрольной группы на исходно заданном уровне 0,05 с учетом поправки Бофферони;
^- статистически значимое различие между соответствующими средними ОГ I и ОГ II на исходно заданном уровне 0,05 с учетом поправки Бофферони.
Как видно из табл. №1, на начальном этапе исследования количество эритроцитов у ВИЧ-инфицированных I подгруппы ОГ было на 30,7% ниже, чем в контрольной группе, а количество эритроцитов у пациенток II подгруппы ОГ было на 29,2% ниже по сравнению с аналогичными показателями КГ. Снижение продукции эритроцитов у ВИЧ-инфицированных беременных, скорее всего, связано с угнетением эритропоэза вследствие приема антиретровирусных препаратов. К 7 суткам лечения количество эритроцитов в I подгруппе ОГ увеличилось на 25,5% (2,75±0,46х10 12 /л на I этапе исследования против 3,69±0,41х10 12 /л на II этапе исследования), оставаясь все-таки достоверно ниже, чем у женщин с неосложненным течением беременности (P1<0,05). На III и IV этапах исследования количество эритроцитов в I подгруппе ОГ было также достоверно ниже (P1<0,01) по сравнению с показателями КГ. На V этапе исследования количество эритроцитов у пациенток I подгруппы ОГ достоверно не отличалось от изучаемого нами параметра КГ (P1>0,05). Отсутствие достоверных отличий по количеству эритроцитов у пациенток I подгруппы ОГ на 5 сутки после оперативного вмешательства мы связываем с применением активатора рецепторов эритропоэтина длительного действия. Правомерность наших суждений подтверждается и дальнейшими результатами. По сравнению с II подгруппой ОГ, количество эритроцитов у пациенток I подгруппы ОГ, начиная со II этапа исследования, было достоверно выше (3,69±0,41х10 12 /л против 2,84±0,47х10 12 /л, Р3 < 0,01), что свидетельствует о правильной тактике предоперационной подготовки.
Показательной была и динамика гемоглобина, уровень которого при поступлении был на 24,2% ниже в I подгруппе ОГ и на 23,7 % ниже во II подгруппе ОГ по сравнению с КГ. У пациенток I подгруппы ОГ величина гемоглобина, также как и количество эритроцитов в процессе лечения имела тенденцию к увеличению, составляя на 7 сутки лечения 118,3±11,2 г/л против 93,8±7,74 г/л (P1>0,05). Полученные данные свидетельствует об адекватности лечебной концепции. Сохраняющиеся статистически достоверные различия (по количеству эритроцитов и уровню гемоглобина) между I подгруппой ОГ и II подгруппой ОГ на всех этапах исследования, указывают на необходимость проведения патогенетической терапии. Препаратом выбора, на наш взгляд, является активатор эритропоэтиновых рецепторов пролонгированного действия (Мирцера), способствующий более длительной ассоциации с концевыми образованиями чувствительных нервных волокон и гарантирующий более стойкий и продолжительный эффект.
Увеличенный при поступлении средний объем эритроцитов (MCV в I подгруппе ОГ был на 28,4% выше, чем в контрольной группе; MCV во II подгруппе ОГ был на 29,2% выше по сравнению с аналогичным параметром КГ) расценивался нами как патогномоничный признак анемии при приеме антиретровирусных препаратов. Увеличение эритроцитов в объеме свидетельствует о нарушении проницаемости клеточной мембраны и указывает на готовность клеток к разрушению. Проведенная комплексная предоперационная терапия в I подгруппе ОГ способствовала значительному снижению данного параметра (88,2±9,3 fl, P1>0,05 на II-ом и последующих этапах исследования), чего нельзя сказать о показателях среднего объема эритроцитов во II подгруппе ОГ (P23
Оценивая динамику среднего содержания гемоглобина в эритроците (MCH) отметим, что при поступлении ВИЧ-инфицированных пациенток в стационар, различие с КГ по данному показателю было статистически недостоверным (28,6±3,15 fl в I подгруппе ОГ против 29,4±2,42 fl в КГ и 28,9±1,68 fl в ОГ II против 29,4±2,42 fl в КГ), что прослеживалось и на последующих этапах исследования (Р1>0,05, Р2>0,05, Р3>0,05). Тем не менее, показатель средней концентрации гемоглобина в эритроците (MCHС) на исходном этапе в I и II подгруппе ОГ был достоверно ниже, чем в контрольной группе (320,1±18,5 г/л против 345,6±18,7 г/л, P10,05). Данный факт – закономерное влияние проводимой специфической терапии, направленной на нормализацию показателей эритропоэза.
Помимо лабораторных данных, нарушения гемопоэза, обусловленные приемом антиретровирусных препаратов, иллюстрирует и морфологическая картина эритроцитов.
На рис. 1 представлены окрашенные Лейкодиф-200 эритроциты пациентки после интраоперационной кровопотери (постгеморрагическая анемия) - видны гипохромные эритроциты и выраженный анизоцитоз.
 | ||
| Рисунок 1. | Рисунок 2. | Рисунок 3. |
На рисунках 2 и 3 отражена морфологическая картина эритроцитов у ВИЧ-инфицированных пациенток, получающих антиретровирусные препараты. Так, на рис. 2 представлены эритроциты ВИЧ-инфицированной пациентки, которая получала химиопрофилактику с 32 недель беременности – эритроциты увеличены в размере, имеется выраженный анизоцитоз и гиперхромия эритроцитов. Однако, у пациентки, получающей антиретровирусные препараты с 36 недель беременности, анизоцитоз и гиперхромия эритроцитов менее выражены (рис. 3). Представленные морфологические данные подтверждают негативное влияние антиретровирусных препаратов на функцию красного кровяного ростка.
На рисунках 4 и 5 отражена микроскопическая картина эритроцитов пациентки С., которая принимала комбинацию из трех антиретровирусных препаратов с 14 недель беременности.
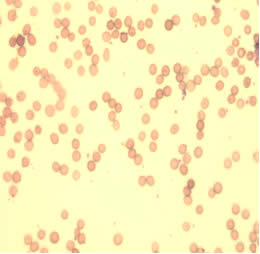 | 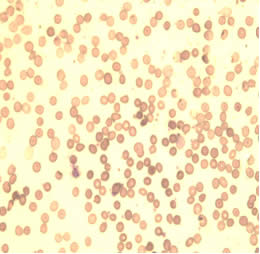 |
| Рисунок 4. | Рисунок 5. |
Практически отсутствуют клетки правильной двояковогнутой формы, характерен выраженный пойкилоцитоз, анизоцитоз, гипохромия красных кровяных телец. Среди представленных эритроцитов преобладают сфероциты, что указывает об аномалии мембраны эритроцитов, нарушении их деформируемости и готовности клеток к гемолизу. Также на рисунке 4 и 5 имеется небольшое количество кодоцитов и шистоцитов, что косвенно указывает на нарушение функции печени. Повышенная агрегационная способность эритроцитов наиболее наглядно отражена на рис. 5. Данное состояние приводит к нарушению транскаппилярного обмена, выбросу биологически активных веществ, нарушению функционирования клеток крови и транспорта кислорода.
На рис. 6 представлены эритроциты пациентки С. после проведения комплексной предоперационной подготовки с использованием стимуляторов эритропоэза. Эритроциты уменьшены в объеме, появились клетки правильной двояковогнутой формы, менее выражены анизоцитоз, пойкилоцитоз, гипохромия эритроцитов. Патологические формы эритроцитов, такие как кодоциты, сфероциты, шистоциты практически отсутствуют, что свидетельствует о появлении нормальных форм эритроцитов. Подобные эффекты достигнуты благодаря применению стимуляторов эритропоэза длительного действия (мирцера).
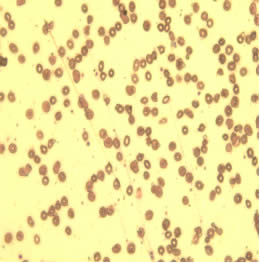 |
| Рисунок 6. |
В настоящее время доказано, что основным регулятором эритропоэза является эритропоэтин – фактор роста гликопротеиновой природы. Он контролирует пролиферацию и дифференцировку эритроидных предшественников в костном мозге и влияет на пролиферацию эритробластов, синтез гемоглобина и выход ретикулоцитов в кровь. У ВИЧ-инфицирванных беременных вследствие приема нуклеозидных ингибиторов обратной транскриптазы развивается синдром неадекватной продукции эритропоэтина и угнетение эритропоэза. Следовательно, традиционное применение препаратов железа и фолиевой кислоты в данной ситуации является недостаточным. Предпочтительнее комплексное использование активаторов эритропоэза в сочетании с препаратами железа и фолиевой кислотой. Стимулятор эритропоэза Мирцера в отличие от рекомбиантного эритропоэтина взаимодействует с эритропоэтиновыми рецепторами на клетках предшественниках костного мозга и характеризуется более длительной ассоциацией с рецептором и более быстрой диссоциацией от рецептора, что позволяет вводить препарат 1 раз в месяц. Считаем, что использование активатора эритропоэза Мирцера а сочетании с препаратами железа и фолиевой кислотой является эффективным и патогенетически обоснованным способом лечения анемии у ВИЧ-инфицированных беременных, принимающих антиретровирусные препараты.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Повышенный гемоглобин, или эритроцитоз: причины появления, при каких заболеваниях возникает, диагностика и способы лечения.
Определение
Эритроцитоз – увеличение содержания красных клеток в единице объема крови, сопровождающееся повышением уровня гемоглобина. Основными симптомами этих изменений являются головные, мышечные боли, головокружение, носовые кровотечения, быстрая утомляемость, более специфические симптомы зависят от соответствующего заболевания.
Разновидности эритроцитоза
Эритроцитоз может быть первичным и вторичным.
Первичный эритроцитоз рассматривается как самостоятельное заболевание системы кроветворения и имеет генетическую природу. В медицине он известен как врожденная полицитемия, или болезнь Вакеза. Данная патология провоцирует увеличение объема костного мозга и повышенную выработку эритроцитов и гемоглобина.
Вторичный эритроцитоз не считается отдельным заболеванием, а лишь симптомом острых или хронических болезней и состояний.
Относительный эритроцитоз является следствием обезвоживания организма, вызванного обильной диареей или рвотой.
Также повышение уровня гемоглобина может являться результатом передозировки лекарственных препаратов, курения, злоупотребления алкоголем и воздействия химических веществ (нитритов).
Абсолютный эритроцитоз является следствием усиленного эритропоэза – процесса образования красных кровяных клеток в костном мозге. Эта форма патологии всегда связана с болезнями внутренних органов или систем.
Возможные причины повышения гемоглобина
- Изменение структуры гена Jak2 V617F, отвечающего за выработку красных клеток крови.
- Неспособность крови связывать и переносить кислород к тканям.
- Снижение поступления кислорода к тканям почек (это приводит к тому, что они начинают усиленно вырабатывать гормон, отвечающий за образование эритроцитов (эритропоэтин)).
- Дефицит ферментов, отвечающих за выработку эритроцитов и их функцию переноса кислорода к тканям.
- Заболевания почек (гидронефроз, поликистоз почек, онкологические заболевания и стеноз почечной артерии).
- Заболевания легких (хронический обструктивный бронхит, бронхиальная астма, заболевания, поражающие легочную ткань, иногда неустановленной причины).
- Заболевания сердца (врожденные и приобретенные пороки сердца).
- Заболевания печени (опухоли печени).
- Заболевания головного мозга (в частности, опухоль мозжечка).
- Заболевания женской половой системы (онкологические заболевания яичников).
- Болезни эндокринной системы, поражающие надпочечники и способствующие повышению артериального давления, при которых обычно неэффективны основные препараты, используемые при гипертонической болезни (болезнь Иценко–Кушинга, феохромоцитома), а также заболевания щитовидной железы.
- Отравление угарным газом.
- Пребывание на больших высотах.
- Синдром обструктивного апноэ, характеризующийся временной остановкой дыхания во время сна.
При выявлении увеличения количества эритроцитов, гематокрита, гемоглобина в первую очередь необходимо в максимально короткие сроки обратиться к гематологу.
Для уточнения диагноза может потребоваться проведение стернальной пункции или трепанобиопсии костного мозга.
Исследование пунктатов, полученных из опухолей, предопухолевых, опухолеподобных образований различной локализации: печень, почки, лёгкие, забрюшинные опухоли, опухоли средостения, щитовидная железа, предстательная железа, яичко, яичники, лимфатические узлы, миндалины, мягкие ткани, кости. .
Читайте также:

