При вирусных гепатитах проявлением цитолитического синдрома является
Обновлено: 24.04.2024
Вирусные гепатиты представляют серьезную проблему ввиду своего широкого эпидемического распространения.
О современных подходах к диагностике, классификации и лечению этой группы заболеваний рассказывает Главный инфекционист Комитета по здравоохранению Администрации Санкт-Петербурга, д-р мед. наук, профессор Аза Гасановна Рахманова.
Хронический гепатит (ХГ) - диффузное воспаление ткани печени длительностью более 6 месяцев. ХГ как самостоятельная форма традиционно подразделяется на:
- хронический персистирующий гепатит (ХПГ);
- хронический лобулярный гепатит (ХЛГ);
- хронический активный гепатит (ХАГ).
На основе серологических и эпидемиологических исследований (преимущественно ленинградских и петербургских ученых) было доказано, что хронические гепатиты имеют вирусную этиологию. Результаты клинико-морфологических исследований показали идентичность клиники и морфологии ХГ у пациентов с маркерами различных вирусов гепатита и с неверифицированными формами. Есть данные о возникновении острых желтушных форм гепатитов среди окружения больных с циррозом печени. Это стало обоснованием лечения хронических гепатитов противовирусными препаратами. С начала 70-х годов была введена регистрация больных острым и хроническим вирусным гепатитом неверифицированной этиологии в рамках инфекционно-эпидемиологической службы (кабинеты инфекционных заболеваний поликлиник и специализированных отделений инфекционных стационаров).
Формирование классификации ХГ
С 1968 г. для прогноза и оценки тяжести течения ХГ широко использовалась клинико-морфологическая классификация J. de Groote, выделяющая формы ХПГ, ХЛГ и ХАГ. Внедрение методов определения маркеров репликации вирусов гепатита В выявило дополнительные критерии активности заболевания (репликативная и нерепликативная стадии процесса). Новые сведения, а также ненадежность морфологической классификации ХГ требовали нового диагностического подхода. Такая попытка была сделана в 1974 г. на конгрессе гепатологов в Акапулько (Мексика).
В 1994 году, в новой международной классификации (Лос-Анджелес, конгресс гастроэнтерологов) из этиологических факторов ХГ были исключены алкоголь и токсины. Таким образом, все ХГ рассматривались как вирусные, а цирроз печени связывался с активно текущим воспалительным процессом. При этом классификация 1994 года предусматривает оценку тяжести течения и прогноза ХГ на основе вирусологических, биохимических и морфологических данных. Она имеет четкую этиологическую направленность, выделяя роль как известных вирусов (В, С, D, G), так и неопределяемых и неоткрытых к настоящему времени. Цирроз печени рассматривается как стадия течения хронического гепатита.
В новой классификации существует диагноз "криптогенный хронический гепатит". С учетом вирусной этиологии ХГ, на наш взгляд, удобнее рассматривать эту форму как неопределенный вирусный хронический гепатит или хронический вирусный гепатит неверифицированной (неуточненной) этиологии. Именно этот термин употребляется в Санкт-Петербурге с 70-х годов. Самостоятельную форму аутоиммунный гепатит, на наш взгляд, целесообразнее рассматривать как проявление вирусной инфекции: исследования последних лет показали, что хронический гепатит является системным заболеванием вследствие персистенции вирусов в различных тканях организма (костный мозг, поджелудочная железа). Для хронических гепатитов В и С характерны внепеченочные проявления (аутоиммунный тиреоидит, лимфоцитарный сиаладенит, различные кожные проявления в т.ч. синдром Шенгрена). В подобном случае маркеры вирусов могут не выявляться за счет аутоиммунных реакций.
Диспансерное наблюдение хронических вирусных гепатитов в Санкт-Петербурге.
| Нозологические формы | 1997 | 1998 |
| Хронический вирусный гепатит (В, С, неверифицированный, в т.ч. и цирротическая стадия) | 14325 | 28113 |
| Носительство маркеров ВГВ | 8822 | 11611 |
| Носительство анти-ВГС антител | 5503 | 8633 |
| Всего | 28650 | 42357 |
Новые подходы к диагностике ХГ
Введение в диагностическую практику полимеразной цепной реакции (ПЦР) позволило получить достоверные данные о виремии. Это значительно повышает возможность этиологической верификации диагноза хронический вирусный гепатит с более точным выделением репликативных форм болезни. По данным Городского гепатологического центра и больницы им. С.П. Боткина (Санкт-Петербург), неверифицированный вирусными маркерами гепатит наблюдался всего у 3,3 % больных. К сожалению, в обычной клинико-эпидемиологической практике широко доступны лишь серологические методы исследований. В последнее время часто встречаются вирусные гепатиты микст-этиологии, вызываемые двумя или тремя гепатотропными вирусами. Они нередко регистрируются у лиц, получавших большое количество парентеральных манипуляций (в том числе и у наркоманов), а также - у лиц, злоупотребляющих алкоголем. В подавляющем большинстве случаев микст-гепатиты являются суперинфекцией, реже коинфекцией, с последовательной или одновременной активностью нескольких гепатотропных вирусов. При этом этиология ХВГ устанавливается для каждого периода обследования. Хронические микст-гепатиты являются основной причиной тяжелых и молниеносных форм заболевания. Они характеризуются выраженной билирубинемией (более 200 мкмоль/л) и высоким уровнем активности АЛТ (более 10 ммоль/ч*л) и часто заканчиваются смертью. По данным Специализированной клиники вирусных инфекций (Санкт-Петербург), из 16 лиц, умерших от ХВГ, только четверо были больны моногепатитом (трое с ХВГ и 1 с ХГС). С точки зрения диагностики, тактики лечения и прогноза ХГ возникает необходимость не только подтверждения наличия вирусной репликации, но и степени выраженности ведущего синдрома болезни. ХГ может длительно протекать со скудной клинической симптоматикой. Больные, в анамнезе которых отсутствовал острый гепатит, нередко считают себя практически здоровыми. Однако тщательный сбор анамнеза позволяет предполагать у большинства наличие перенесенной в прошлом безжелтушной формы заболевания. При активном опросе у них обнаруживались такие симптомы, как периодическая слабость, снижение работоспособности, плохой аппетит, ноющие боли в правом подреберье, тошнота и др. У одной трети пациентов не удалось выявить в прошлом каких-либо симптомов ХГ. Ввиду этого целесообразно выделять бессимптомные и манифестные формы ХГ с различной выраженностью клинических признаков болезни. Следует отметить, что и бессимптомные формы могут в ряде случаев быть репликативными, в особенности при ВГС инфекции. Это подтверждается результатами обследования доноров: из 28 обследованных нами практически здоровых доноров с нормальными показателями биохимических проб и наличием общих анти-ВГС антител у 20 выявлена РНК ВГС. Предлагаемый нами для широкой клинической практики модифицированный вариант международной классификации хронических вирусных гепатитов предусматривает определение:
1. Этиологии:
- хронические вирусные гепатиты В, С, D
- микст ХВГ
2. Фазы ХВГ:
- репликативная
- нерепликативная (интегративная)
3. Хронического вирусного гепатита неверифицированной (неуточненной) этиологии;
4. Степени активности:
- минимальная
- слабо выраженная
- умеренно выраженная
- выраженная
5. Стадии:
0 - без фиброза
1 - слабо выраженный перипортальиый фиброз
2 - умеренный фиброз с портопортальными септами
3 - выраженный фиброз с портопортальными септами
4 - цирроз печени (степень тяжести определяется выраженностью портальной гипертензии и печеночной недостаточности).
К сожалению, выявлять фазу репликации при хроническом неверифицированном вирусном гепатите не представляется возможным, поэтому в подобном случае в структуре диагноза следует определять фазу обострения или ремиссии. Как при верифицированном, так и при неверифицированном ХВГ необходимо определять периоды манифестации или обострения, ведущий клинический синдром и дополнительные факторы, имеющие значение для характера проявлений ХГ и его терапии: холестаз, цитолиз, или синдром аутоиммунных проявлений в различных сочетаниях. Существенно выделить ХВГ с бактериальными осложнениями как один из частых вариантов течения болезни в период обострений.
Основные направления терапии хронических вирусных гепатитов
С учетом классификации ХГ и внесенных нами дополнений комплексная терапия заболевания должна учитывать:
- степень активности патологического процесса,
- ведущий синдром болезни,
- наличие признаков цирротической стадии и фазы вирусной инфекции (интеграции или репликации).
Стандартная терапия, обязательная при любых синдромах и любой степени активности патологического процесса включает:
- Диета: стол N5, комплекс витаминов в терапевтических дозах, минеральные воды;
- Средства, нормализующие деятельность желудочно-кишечного тракта, препятствующие дисбактериозу, накоплению кишечных эндотоксинов - эубиотики (лактобиктерин, колибактерин, бифидумбактерин) и им подобные. Целесообразен прием лактулозы, энтеродеза, энтеросептола, при необходимости - ферментов (панкреатин, фестал и им подобные);
- Гепатопротекторы, обладающие метаболическими свойствами: рибоксин, цитохром С, гептрал, гепарген, сирепар, карсил, катерен, ЛИВ 52, гепалиф, эссенциале и др.;
- Лекарственные травы, обладающие противовирусным (зверобой, календула, чистотел и др.), желчегонным и спазмолитическим действием (чертополох, мята, спорыш и др.);
- Физиотерапевтические мероприятия, лечебная физкультура;
- Психосоциальная реабилитация больных ХВГ;
- Лечение сопутствующих заболеваний и состояний: симптоматические средства.
Цитолитический синдром, выявляемый при ХГ, требует коррекции путем введения белковых препаратов (альбумины), факторов свертывания (плазма, криопреципитат), обменного переливания свежегепаринизированной крови, перфузии крови через пласты гетеропечени, эмболизации печеночных сосудов, методы экстракорпоральной детоксикации и др.
Холестатический синдром купируется путем назначения абсорбентов (холестирамин, билигнин, карболен, полифепан, ваулен), а также, как показано в последние годы, препаратов ненасыщенных жирных кислот (урсофальк, хенофальк и им подобные), гемоплазмосорбции.
Аутоиммунный синдром требует назначения иммунодепрессантов: азатиоприм (имуран), депагил, кортистероиды, показана плазмосорбция. При ХГ, осложненном вторичной бактериальной инфекцией, показано применение антимикробных средств (трихопол, ампициллин и др.).
Исходя из вирусной этиологии хронических гепатитов, средствами этиотропной терапии при ХГ являются противовирусные и иммуномодулирующие средства.
Вирусная репликация - наиболее значимый критерий в прогнозе заболевания, в особенности для назначения противовирусных препаратов. Как показали наши исследования, постоянная или рецидивирующая виремия выявляется на всех этапах развития ВГВ и ВГС инфекции, в том числе при субклинической активности и даже в цирротической стадии. Испытанными средствами противовирусной терапии для лечения ХГ являются:
- Аденинарабиназид (АРА-А) в разных дозах от 5-15 мг/кг массы тела в сутки и более (даже до 200 мг/кг в сутки;
- Синтетические нуклеозиды (ингибиторы обратной транскриптазы):
- Ацикловир (зовиракс) от 1.0 до 4.0 г/сут.;
- Рибавирин от 1.0 до 2.0 г/сут.;
- Ламивудин (эпивир, 3ТС) - 150-300 мг/сут.;
Адекватные подходы к диагностике, классификации и терапии хронического гепатита должны быть включены как компоненты системы эпиднадзора.
Цитолиз при вирусном гепатите. Мезенхимально-воспалительный синдром при гепатите
Заболевания различаются по типу возбудителя, механизмам повреждения печени, клинической картине и исходам. Данная группа болезней не включает вирусные гепатиты, развивающиеся в качестве синдромов при инфекциях, вызванных EBV, CMV, Herpesvirus, Yellow fever virus и др. (так называемые гепатиты-спутники).
Гепатотропность возбудителей вирусных гепатитов объясняет сходство основных клинических проявлений заболеваний, представленных в период разгара характерными клинико-биохимическими и патоморфологическими синдромами или их сочетаниями, несмотря на то, что инфекции вызваны разными вирусами и имеют существенные различия в патогенезе.
Основным синдромом поражения печени при гепатитах является цитолиз. Цитолиз — повышение проницаемости клеточных мембран, сопровождающееся нарушением внутриклеточного метаболизма. Происходит перераспределение биологически активных веществ — выход за пределы клетки печеночно-клеточных ферментов (АлАТ, ЛДГ5 и др.) и ионов калия, проникновение в клетку жидкости и ионов натрия, кальция (отек, набухание). Диффузный цитолиз и дистрофия сопровождаются нарушениями функции печени (детоксической, белково-синтетической, пищеварительной, нарушениями пигментного обмена и др.).
![вирусный гепатит]()
Клиническая выраженность симптомов зависит от тяжести поражения и реализации мощной компенсаторной возможности органа. Типичными проявлениями диффузного цитолиза и дистрофии гепатоцитов является синдром интоксикации — астения, повышенная утомляемость, недомогание, сонливость, разбитость, головокружение. Интоксикация определяется метаболическими изменениями, обусловленными нарушением детоксической функции печени (аутоинтоксикация), обычно не сопровождается лихорадкой. С цитолизом связано нарушение пигментного обмена, что проявляется желтухой южных покровов и слизистых оболочек, потемнением мочи и ахолией кала.
Типичным признаком гепатита является увеличение размеров печени, плотновато-эластическая консистенция органа, восстановление размеров по мере обратного развития заболевания. Диспепсические жалобы обусловлены нарушением функции желчеобразования и выделения желчи, вовлечением в процесс гастродуоденальной и панкреатической зоны. Характерно снижение аппетита, тошнота, возможна рвота, ощущение дискомфорта и/или болей в эпигастральной области и правом подреберье. При тяжелой форме заболевания проявлением нарушения белково-синтетической функции печени становится геморрагический синдром, обусловленный дефицитом факторов свертывания, синтезируемых печенью (протромбин, проакцелерин, проконвертин), а также дефектами противосвертывающей системы крови.
Мезенхимально-воспалительный синдром, выраженный в большей или меньшей степени, свойственен большинству заболеваний печени и связан с реакцией ретикулоэндотелиальной системы на антигенную стимуляцию. Мезенхимально-воспалительный синдром приобретает важное значение в развитии и прогрессировании хронических гепатитов, с ним связан активный фиброгенез, формирование цирроза, портальная гипертензия и др. Лабораторными признаками мезенхимально-воспалительного синдрома являются повышение уровня глобулинов и выраженная гипергаммаглобулинемия, увеличение содержания иммуноглобулинов всех классов, изменение количества лейкоцитов в периферической крови и увеличение СОЭ, снижение сулемового титра и повышение тимоловой пробы.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.Диагностика гепатита А. Лечение и профилактика гепатита А
Диагноз гепатита А устанавливают с учетом комплекса эпидемиологических данных (развитие болезни после контакта с больным гепатитом А или пребывание в неблагополучном районе в период, соответствующий инкубации ГА), клинических проявлений (циклическое развитие заболевания с возникновением характерных синдромов) и результатов лабораторных исследований.
Наиболее постоянным лабораторным показателем, отражающим наличие гепатита (цитолитического синдрома), является 10-кратное и более повышение активности печеночно-клеточного фермента — АлАТ. Повышение активности АлАТ выявляется уже в продромальный (преджелтушный) период, сохраняется в разгар заболевания. Нормализация показателя происходит после угасания клинических проявлений заболевания.
Ранним показателем нарушения пигментного обмена является обнаружение уробилиногена и желчных пигментов в моче. Увеличение содержания билирубина в крови наблюдается при желтушной форме болезни и происходит преимущественно за счет его связанной фракции. Для ГА характерно изменение белково-осадочных проб — повышение тимоловой пробы и снижение сулемового титра. В разгар заболевания выявляется лейкопения, нейтропения, относительный лимфо- и моноцитоз, нормальная или сниженная СОЭ.
Достоверная верификация диагноза гепатита А достигается серологическими методами (РИА, ИФА и др.) путем обнаружения в крови анти-HAV-IgM в продромальный период и период разгара. Awm-HAV-IgG, обнаруживаемые в период решнвалесценции, имеют анамнестическое значение.
Дифференциальный диагноз гепатита А в продромальный период проводится с гриппом и другими ОРВИ, тифо-паратифозными заболеваниями, малярией. В период разгара ГА дифференцируют с лептоспирозом, инфекционным мононуклеозом, псевдотуберкулезом, желтой лихорадкой, а также неинфекционными желтухами — гемолитической, обтурационной, токсическими гепатитами.
![диагностика гепатита А]()
Большинство больных гепатитом А не нуждаются в активных лечебных мероприятиях. Больным следует создать благоприятные условия для функционирования поврежденной печени и самоизлечения. Это достигается щадящим режимом и рациональной диетой.
В период разгара болезни показан постельный режим. По мере улучшения состояния больного режим постепенно расширяют, ограничивая физическую активностьДиета предусматривает калорийную пишу (соответственно физиологической норме), содержащую полноценные белки, жиры (за исключением трудноперевариваемых: бараньего, свиного, говяжьего) и углеводы. Из рациона исключают продукты питания, оказьюающие неблагоприятное действие на печень и требующие ее усиленной работы (копчености, острые приправы, маринады, чеснок, грибы и др.). Объем жидкости (включая щелочные минеральные воды) составляет 2-3 литра в сутки. Рекомендуется добавление в рацион свежих овощей, фруктов и соков, богатых витаминами. Ограничение физических нагрузок и соблюдение диеты показаны в течение 6 мес после перенесенного заболевания, так как клиническое выздоровление значительно опережает патоморфологическое восстановление печеночной ткани. В это время следует исключить алкогольсодержащие напитки.
При средней тяжести и тяжелом течении проводят дезинтоксикационную терапию с применением энтеральных (полифепан, энтеродез, оралит, глююзо-содержащих и др.) и инфузионных (растворы Рингера, глюкозы, гемодез и др.) средств
В период реконвалесценции, особенно при затяжном течении ГА, назначают метаболическую терапию, включающую сбалансированное введение витаминов группы В, С, жирорастворимых А, Е, а также гепатопротекторов (легален, карсил или силибор, эссенциале). По показаниям применяют спазмолитики, желчегонные препараты (обычно холекинетики).
Профилактика. Осуществляется проведение комплекса санитарно-гигиенических и противоэпидемических мероприятий. Инфицированные лица подлежат изоляции на 28 дней Контактные лица наблюдаются и лабораторно обследуются в течение 50 дней. В очагах проводится дезинфекция.
По эпидемиологическим показаниям проводится иммунопрофилактика ГА с помощью нормального донорского иммуноглобулина (Globuman). Препарат вводят однократно внутримышечно не позже 10-14-го дня после контакта с больным. Защитное действие пассивной иммунизации ограничивается 3-5 мес. Для профилактики ГА применяют коммерческий иммуноглобулин с известным содержанием специфических антител к вирусу ГА.
В настоящее время успешно осуществляется активная иммунизация в регионах с высоким уровнем заболеваемости ГА. Вакцинопрофилактику проводят также лицам, выезжающим в эпидемиологически неблагоприятные регионы. Применяют инактивированные вакцины (Havrix, Avaxim и др.), обеспечивающие иммунитет на 10 и более лет.
М. Г. Ипатова 1, 2 к.м.н., Ю. Г. Мухина 1 д.м.н. профессор, П. В. Шумилов 1 д.м.н., профессор
1 Российский национальный исследовательский медицинский университет им. Н. И. Пирогова
МЗ РФ, Москва2 Детская Городская Клиническая Больница № 13 им. Н. Ф. Филатова, Москва
Ключевые слова: печень, синдром цитолиза, аланинаминотрансфераза, аспартатамино-трансфераза, гепатопротективные препараты
В статье изложены биохимические лабораторные показатели и их клиническое значение при заболеваниях печени, протекающих с синдромом цитолиза. Отдельное внимание уделено механизмам действия гепатопротективных препаратов, применяемых при цитолитическом синдроме.
![]()
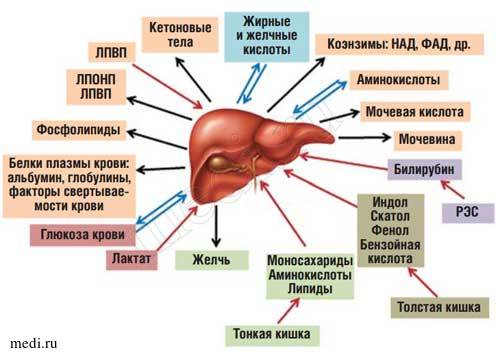
Рис. 1. Роль печени в обмене веществ.
Сокращения: ЛПВП - липопротеиды высокой плотности; ЛПОНП - липопротеиды очень низкой плотности; РЭС ретикуло-эндотелиальная система; НАД - никотинамидадениндинуклеотид; ФАД - флавинадениндинуклеотид.
Печень представляет собой центральный орган химического гомеостаза организма, где создается единый обменный и энергетический пул для метаболизма почти всех классов веществ [1]. К основным функциям печени относятся: метаболическая, депонирующая, барьерная, экскреторная, гомеостатическая и детоксицирующая [2]. Печень может обезвреживать как чужеродные экзогенные вещества, обладающие токсическими свойствами, так и синтезированные эндогенно.
Таблица 2. Причины повышения уровня аминотрансфераз
Печеночные причины
Внепеченочные причины
•Вирусные гепатиты (В, С, ЦМВ и др.)
•Хронические инфекции и паразитарные
заболевания (эхинококкоз, токсоплазмоз и др.)•Неалкогольный стеатогепатит
•Аутоиммунные заболевания печени
•Злоупотребление алкоголем
•Прием лекарственных препаратов
(статины, некоторые антибиотики, противогрибковые препараты, нестероидные
противовоспалительные препараты,
глюкокортикостероиды, другие)•Метаболические заболевания печени
(галактоземия, фруктоземия, гликогенозы,
дефицит альфа1-антитрипсина,
аминоацидопатии, нарушение цикла мочевины, нарушение окисления жирных кислот, митохондриальная гепатопатия, некоторые лизосомные заболевания (болезнь
Гоше, болезнь Ниманна-Пика, дефицит кислой липазы и др.), муковисцидоз, синдром Швахмана-Даймонда, гемохроматоз, болезнь Вильсона и др.)•врожденные и приобретенные дефекты
сосудов системы воротной вены (болезнь
Бадда-Киари и др.)•Цирроз печени
•Опухоли печени
•Патология сердца (острый инфаркт
миокарда, миокардит)•Повышенная физическая нагрузка
•Наследственные нарушения мышечного
метаболизма•Приобретенные мышечные заболевания
•Травма и некроз мышц
•Целиакия
•Гипертиреоз
•Тяжелые ожоги
•Гемолиз эритроцитов
•Нарушение кислотно-щелочного равновесия
•Сепсис
Находясь между портальным и большим кругами кровообращения, печень выполняет функцию большого биофильтра. Через воротную вену в нее поступает более 70% крови, остальная кровь попадает через печеночную артерию. Большая часть веществ, всасывающихся в пищеварительном тракте (кроме липидов, транспорт которых в основном осуществляется через лимфатическую систему), поступает по воротной вене в печень [2]. Таким образом, печень функционирует как первичный регулятор содержания в крови веществ, поступающих в организм с пищей (рис 1).
Большое разнообразие функций гепатоцитов приводит к тому, что при патологических состояниях печени нарушаются биохимические константы, отражающие изменения многих видов обмена. Поэтому стандартный биохимический анализ крови включает определение различных параметров, отражающих состояние белкового, углеводного, липидного и минерального обмена, а также активность некоторых ключевых ферментов.
Концентрация ферментов в клетках значительно выше, чем в плазме крови; в норме только очень незначительная часть определяется в крови. Наиболее частыми причинами повышения уровня ферментов в сыворотке крови являются: прямое поражение клеточных мембран, в частности вирусами и химическими соединениями, гипоксия и ишемия тканей. Иногда активность ферментов увеличивается в результате их повышенного синтеза в тканях. Определение активности тех или других ферментов в сыворотке крови позволяет судить о характере и глубине поражения различных компонентов гепатоцитов [3, 4].
Ферменты в зависимости от их локализации можно разделить на несколько групп:
1) универсально распространенные ферменты, активность которых обнаруживается не только в печени, но и в других органах – амино-трансферазы, фруктозо-1-6-дифосфатальдолаза;
2) печеночноспецифические (органоспе-цифические) ферменты; их активность исключительно или наиболее высоко выявляется в печени. К ним относятся холинэстераза, орнитин-карбамилтрансфераза, сорбитдегидрогеназа и др.;
3) клеточноспецифические ферменты печени относят преимущественно к гепатоцитам,
купферовским клеткам или желчным канальцам (5-нуклеотидаза, аденозинтрифосфатаза);4) органеллоспецифические ферменты, являются маркерами определенных органелл
гепатоцита: митохондриальные (глутаматде-гидрогеназа, сукцинатдегидрогеназа, цитохромоксидаза), лизосомальные (кислая фос фатаза, дезоксирибонуклеаза, рибонуклеаза), микросомальные (глюкозо-6-фосфатаза).Специфичность ферментов и их диагностическое значение представлено в таблице 1 [5].
Отдельное место занимает макроэнзиме-мия – редкое и крайне сложное для дифференциальной диагностики состояние, при котором происходит комплексирование молекул того или иного энзима с иммуноглобулинами или небелковыми веществами. Описаны клинические наблюдения макро-КФК-емии, макро-ЛДГ-емии, макро-АСТ-емии, макро-ГГТ-емии, макроамилаземии. Макро-энзимемии сложны для диагностики и дифференциальной диагностики и ведут к проведению инвазивных методов обследования и необоснованному лечению.
В основе выявления макроэнзимемии лежит выявление отличий молекулы макрофермента от молекулы обычного энзима. Некоторые из этих методов являются прямыми, т. е. такими, которые позволяют непосредственно определить присутствие в крови ферментного комплекса, имеющего гораздо более высокий молекулярный вес, чем молекула нормального фермента. В основу прямого метода положено разделение белков сыворотки по молекулярному весу. Другие же методы являются непрямыми, так как выявление макроэнзима в крови проводится не путем выявления самого ферментного комплекса, а основываются на выявлении какого-либо из свойств макроэнзима. Прямые тесты имеют большее диагностическое значение и влекут за собой меньше технических и диагностических ошибок.
В некоторых ситуациях повышение ферментов является физиологическим: уровень щелочной фосфатазы повышен у подростков в период вытяжения (период ускорения роста), у здоровых женщин во время третьего триместра беременности (за счет плаценты). Однако очень высокую активность щелочной фосфатазы наблюдают у женщин с преэк-лампсией, что связно с нарушением кровообращения плаценты [7].
Большое значение в диагностике заболеваний печени имеют анамнестические данные и клиническая картина заболевания. Из анамнеза следует попытаться узнать о факторах риска заболеваний печени, обращая особое внимание на семейный анамнез, прием лекарств, витаминов, растительных добавок, наркотиков, алкоголя, трансфузии препаратов крови, патологические результаты печеночных проб в прошлом и симптоматику заболеваний печени. Клиническое обследование позволяет диагностировать до 50–60% патологических состояний. Более детальная дифференциальная диагностика основана на иммунохимических методах. Они позволяют детализировать характер вирусной, а также паразитарной инфекции, определить локализацию неопластического процесса, определить этиологию аутоиммунного заболевания, уточнить вид нарушения наследственных заболеваний обмена веществ.
При патологии печени в биохимическом анализе крови выделяют 4 синдрома:
• Синдром печеночно-клеточной недостаточности
• Мезенхиально-воспалительный синдром.
В данной статье мы подробно разберем по
казатели, характерные для синдрома цитолиза.Синдром цитолиза – это синдром, обусловленный нарушением проницаемости клеточных мембран, распадом мембранных структур или некрозом гепатоцитов с выходом в плазму ферментов (АЛТ, АСТ, ЛДГ, альдолазы и др.).
АМИНОТРАНСФЕРАЗЫ: аспартатаминотрансфераза и аланинаминотрансфераза
Референтные значения: у новорожденных детей до 1 мес. – менее 80 Ед/л; от 2 мес. до 12 мес. – менее 70 Ед/л., с 1 года до 14 лет – менее 45 Ед/л, у женщин – менее 35 Ед/л, у мужчин – менее 50 Ед/л.
В клинической практике широко применяется одновременное определение уровня двух трансаминаз – аспартатаминотрансферазы (AСT) и аланинаминотрансферазы (АЛТ) в сыворотке крови.
Ферменты АЛТ и АСТ содержатся практически во всех клетках человеческого организма. Однако самый высокий уровень фермента АЛТ содержится в печени, поэтому уровень данного энзима служит специфическим маркером поражения печени. В свою очередь, АСТ помимо печени (в порядке снижения концентрации) содержится в сердечной и скелетных мышцах, почках, поджелудочной железе, легких, лейкоцитах и эритроцитах [6, 7, 8].
В печени АЛТ присутствует только в цитоплазме гепатоцитов, а АСТ – в цитоплазме и в митохондриях. Более 80% печеночной АСТ представлено именно митохондриальной фракцией [6, 7, 8].
В норме постоянство концентрации транс-аминаз в плазме крови отражает равновесие между их высвобождением вследствие физиологического апоптоза состарившихся гепатоци-тов и элиминацией. Соотношение синтеза АСТ/ АЛТ в печени равно 2,5/1. Однако при нормальном обновлении гепатоцитов уровни АСТ и АЛТ в плазме крови практически одинаковы (30–40 Ед/л) из-за более короткого периода полувыведения АСТ (18 ч против 36 ч у АЛТ).
При заболеваниях печени в первую очередь и наиболее значительно повышается активность АЛТ по сравнению с АСТ. Например, при остром гепатите, независимо от его этиологии, активность аминотрансфераз повышается у всех больных, однако преобладает уровень АЛТ, содержащейся в цитоплазме, вследствие ее быстрого выхода из клетки и поступления в кровяное русло. Таким образом, по уровню АЛТ судят о биохимической активности заболевания печени. Повышение показателя в 1,5–5 раз от верхней границы нормы свидетельствует о низкой активности процесса, в 6–10 раз – об умеренной и более 10 раз – о высокой биохимической активности. Повышение активности трансаминаз более 6 месяцев является биохимическим признаком хронического гепатита [6, 7].
Некоторые лекарственные препараты (например, вальпроевая кислота) метаболизируются в митохондриях гепатоцитов [9], поэтому ранним лабораторным маркером гепатотоксичности может быть лишь изолированное повышение АСТ.
Помимо патологии печени АСТ служит одним из ранних маркеров повреждения сердечной мышцы (повышается у 93–98% больных инфарктом миокарда до 2–20 норм); специфичность его не высока. Уровень ACT в сыворотке крови возрастает через 6–8 часов после начала болевого приступа, пик приходится на 18–24 часа, активность снижается до нормальных значений на 4–5 день. Нарастание активности фермента в динамике может свидетельствовать о расширении очага некроза, вовлечении в патологический процесс других органов и тканей, например, печени [7].
Интенсивные мышечные упражнения с чрезмерной нагрузкой также могут вызвать преходящее увеличение уровня ACT в сыворотке крови. Миопатии, дерматомиозиты и другие заболевания мышечной ткани вызывают повышение трансаминаз, преимущественно за счет АСТ.
Умеренное увеличение активности АСТ (в 2–5 раз от верхней границы нормы) отмечается при острых панкреатитах и гемолитических анемиях.
При латентных формах цирроза печени повышения активности ферментов, как правило, не наблюдают. При активных формах цирроза стойкий незначительный подъем аминотрансфераз выявляют в 74–77% случаев, и, как правило, преобладает активность АСТ над АЛТ в два и более раз.
Снижение активности АЛТ и АСТ имеет место при недостаточности пиридоксина (витамина В6), при почечной недостаточности, беременности.
Ниже приведены печеночные и внепеченочные причины повышения активности аминотрансфераз в сыворотке крови (табл. 2).
Помимо оценки уровня трансаминаз в клинической практике широко применяется коэффициент де Ритиса – отношение АСТ к АЛТ (АСТ/АЛТ). В норме значение этого кэффициента составляет 0,8–1,33. Следует отметить, что расчет коэффициента де Ритиса целесообразен только при выходе АСТ и/или АЛТ за пределы референтных значений.
У новорожденных детей соотношение АСТ/АЛТ обычно превышает 3,0, однако к пятому дню жизни снижается до 2,0 и ниже.
При поражениях печени с разрушением гепатоцитов преимущественно повышается АЛТ, коэффициент де Ритиса снижается до 0,2–0,5. При патологии сердца преобладает уровень АСТ, и коэффициент де Ритиса повышается. Однако для точной дифференциальной диагностики этот коэффициент непригоден, так как нередко при алкогольном поражении печени, неалкогольном стеатогепатите, циррозе печени также преобладает повышение АСТ и коэффициент де Ритиса составляет 2,0–4,0 и более. Значение данного коэффициента выше нормы часто наблюдается при обтурационных желтухах, холециститах, когда абсолютные значения АЛТ и АСТ невелики.
1. При остром вирусном и хроническом гепатитах, особенно на ранних стадиях, активность АЛТ выше, чем АСТ (коэффициент де Ритиса меньше 1,0). Тяжелое поражение паренхимы печени может изменить это соотношение.
2. При алкогольном гепатите и циррозе нередко активность АСТ оказывается выше, чем АЛТ (коэффициент де Ритиса больше 1,0).
3. При остром ИМ активность АСТ выше, чем АЛТ (коэффициент де Ритиса больше 1,5).
ЛАКТАТДЕГИДРОГЕНАЗА
Референтные значения ЛДГ для новорожденных – до 600 Ед/л, у детей с 1 года до 12 лет активность ЛДГ – 115 – 300 Ед/л, для детей старше 12 лет и у взрослых норма ЛДГ – до 230 Ед/л.
Лактатдегидрогеназа (ЛДГ) – гликолитический цинксодержащий фермент, обратимо катализирующий окисление L-лактата в пируват, широко распространен в организме человека. Наибольшая активность ЛДГ обнаружена в почках, сердечной мышце, скелетной мускулатуре и печени. ЛДГ содержится не только в сыворотке, но и в значительном количестве в эритроцитах, поэтому сыворотка для исследования должна быть без следов гемолиза [7].
При электрофорезе или хроматографии удается обнаружить 5 изоферментов ЛДГ, отличающихся по своим физико-химическим свойствам. Наибольшее значение имеют два изофермента – ЛДГ1 и ЛДГ5. Фракция ЛДГ1 более активно катализирует обратную реакцию превращения лактата в пируват. Она в большей степени локализуется в сердечной мышце и некоторых других тканях, в норме функционирующих в аэробных условиях. В связи с этим миокардиальные клетки, обладающие богатой митохондриальной системой, окисляют в цикле трикарбоновых кислот не только пируват, образующийся в результате протекающего в них самих процесса гликолиза, но и лактат, образующийся в других тканях. Фракция ЛДГ5 более эффективно катализирует прямую реакцию восстановления пирувата в лактат. Она локализуется преимущественно в печени, в скелетных мышцах. Последние нередко вынуждены функционировать в анаэробных условиях (при значительной физической нагрузке и быстро наступающем утомлении). Образующийся при этом лактат с кровотоком попадает в печень, в которой он используется для процесса глюконеогенеза (ресинтеза глюкозы), а также в сердце и другие ткани, где происходит его преобразование в пируват и вовлечение в цикл трикарбоновых кислот (цикл Кребса). Любое повреждение клеток тканей, содержащих большое количество ЛДГ (сердце, скелетные мышцы, печень, эритроциты), приводит к повышению активности ЛДГ и ее изо-ферментов в сыворотке крови. Наиболее частыми причинами повышения активности ЛДГ являются:
1. Поражение сердца (острый инфаркт миокарда, миокардит, застойная сердечная недостаточность); в этих случаях обычно преобладает повышение активности ЛДГ1 и/или ЛДГ2.
2. Поражение печени (острые и хронические гепатиты, цирроз печени, опухоли и метастазы печени), когда преимущественно увеличивается изофермент ЛДГ5, ЛДГ2, ЛДГ4.
3. Повреждение скелетных мышц, воспалительные и дегенеративные заболевания
скелетных мышц (преимущественно увеличение изофермента ЛДГ1, ЛДГ2, ЛДГ3).4. Заболевания крови, сопровождающиеся распадом клеток крови: острый лейкоз, гемолитическая анемия, В12-дефицитная анемия, серповидноклеточная анемия, а также заболевания и патологические состояния, сопровождающиеся разрушением тромбоцитов (массивная гемотрансфузия, эмболия легочной артерии, шок и др.). В этих случаях может преобладать повышение активности ЛДГ2, ЛДГ3.
5. Острый панкреатит.
6. Заболевания легких (пневмония и др.)
7. Инфаркт почки.
8. Опухоли (повышенный уровень ЛДГ наблюдается в 27% случаев опухолей в I стадии и в 55% – метастатических семином).
Следует помнить, что многие заболевания сердца, скелетных мышц, печени и крови могут сопровождаться повышением активности в сыворотке крови общей ЛДГ без отчетливого преобладания какого-либо из ее изоферментов.
Таблица 3. Эффективность гепатопротекторов при синдроме цитолиза (по С. В. Морозову с соавт., 2011 г. и Н. Б. Губергриц, 2012 г.) [10]
Читайте также: