Принципы микробиологической диагностики парентеральных гепатитов с
Обновлено: 26.04.2024
Гепатит С – это антропонозное вирусное заболевание с парентеральным механизмом заражения, протекающее в виде посттрансфузионного гепатита с преобладанием безжелтушных и легких форм и склонное к хронизации.
Вирус гепатита С относится к семейству Flaviviridae (лат. flavus - желтый) роду Hepacivirus (лат. hepar - печень). Вид – вирус гепатита С, Hepatitis C virus (HCV).
Вирионы вируса гепатита С имеют сферическую форму размером 55-65 нм. Геном представлен линейной плюс-РНК. Снаружи вирион окружен липидным суперкапсидом с белковыми выступами. Репродукция вируса происходит в цитоплазме инфицированной клетки.
Культуральные свойства. ВГС не культивируется на куриных эмбрионах, не обладает гемолитической и гемагглютинирующей активностью. Заражение высших приматов(шимпанзе).
Антигенная структура. Антигенами вируса являются НСсантиген (core-антиген); неструктурные белки NS2-NS5; гликопротеины оболочки gp Е1 и gp E2/NS1.
Геном представлен плюс-цепью РНК. Геном высокоизменчив. Особой гипермутабельностью обладает район, детерминирующий синтез гликопротеинов Е1 и Е2, которые обладают В-эпитом и на которые вырабатываются вируснейтрализующие антитела. Замена аминокислот в гликопротеинах изменяет антигенные свойства вируса, позволяя ему избегать нейтрализующего действия антител. Известно около 14 генотипов вируса. Наибольшее распространение имеют генотипы 1-3, наиболее вирулентным является генотип 1b.
Резистентность. Вирус во внешней среде нестоек.
Эпидемиология. Источник инфекции - инфицированный человек.
Клиника. Различают следующие периоды заболевания: 1. Инкубационный период – 6-8 недель. 2.Преджелтушный период – 1-2 недели. 3.Разгар заболевания – развитие желтухи, продолжительность – 2-3 недели. Отмечается повышение уровня билирубина, АЛТ, интоксикация, гепато- и спленомегалия. Заболевание протекает в виде острого или хронического гепатита. Часто встречаются безжелтушные формы.
Лабораторная диагностика вирусного гепатита С (ВГС) основана на определении маркеров этой инфекции: РНК вируса методом ПЦР и антител к вирусу (суммарных, отдельных классов иммуноглобулинов IgM и IgG к вирусу и отдельным вирусным белкам).
Диагностика гепатитов В и С у гематологических больных - анализы, особенности
Современная этиологическая диагностика вирусных гепатитов основана на обнаружении специфических маркеров соответствующих вирусов. Один из методов их выявления — тестирование различных антигенов вируса и антител к ним в ИФА. Наиболее прогрессивна и информативна так называемая генная диагностика: обнаружение вирусной РНК или ДНК с помощью ПЦР.
Для диагностики гепатита В в ИФА исследуют:
1) HBsAg-поверхностный антиген гепатита В, ранее называвшийся австралийским. Он указывает на факт инфицированности гепатитом В;
2) HbeAg — антиген инфекционности, свидетельствующий об активной вирусной репликации;
3) анти-НВс —антитела к ядерному антигену вируса гепатита В: класса IgM—ранние антитела острого периода, класса IgG—поздние антитела к ядерному антигену;
4) анти-НВе — антитела к HBeAg, чаще всего характеризующие прекращение активной репликации вируса (так называемая сероконверсия);
5) анти-HBs—антитела к HBsAg, обеспечивающие протективный иммунитет.
С помощью ПЦР для диагностики гепатита В тестируют ДНК вируса гепатита В — основного маркера репликации вируса.
Для диагностики гепатита С исследуют:
1) с помощью ИФА наличие анти-HCV-антител к вирусу гепатита С (для их выявления желательно использовать тест-системы второго — третьего поколения, отличающиеся большей специфичностью). Они указывают только на инфицированность вирусом гепатита С;
2) с помощью ПЦР наличие РНК вируса гепатита С — основного маркера репликации вируса.
Говоря о специфической диагностике гепатитов В и С у пациентов с онкологическими гематологическими заболеваниями (ОГЗ), следует рассмотреть вопрос о применимости стандартных подходов к выявлению различных маркеров этих вирусов у данного контингента в связи с возможным нарушением процесса антителообразования на фоне глубокой иммуносу-прессии, развивающейся в ходе полихимиотерапии (ПХТ).
Исследования, в которых сделана попытка подтвердить или опровергнуть роль антительных маркеров у пациентов с онкологическими гематологическими заболеваниями, пока единичны.
Так, в отдельных работах сообщается, что при гепатите В иммуносупрессия нарушает обычную последовательность обнаружения в сыворотке крови антигенов и антител: у больных, которые до начала ПХТ были анти-НВs-позитивными, в процессе лечения могут вновь определяться HBsAg и HBeAg, свидетельствуя о несостоятельности анти-HBs в качестве протективных антител. Угнетение механизмов, ограничивающих вирусную репликацию, ведет к тому, что виремия нередко достигает высокого уровня.
Если антитела к столбняку, дифтерии и полиомиелиту сохраняются во время и после ПХТ, то титры антител к вирусам (ветряной оспы, кори и гепатита В) резко снижаются. Это в большей мере относится к детям с лейкозами, чем с солидными опухолями. Снижение или отсутствие выработки анти-HBs отметили также R. Repp и соавт. и R. Rokicka-Milewska и соавт.. Если при гепатите В эта особенность может отразиться только на ретроспективной диагностике, то для распознавания гепатита С, основанного чаще всего на обнаружении анти-HCV с помощью ИФА, такое положение может иметь принципиальное значение, препятствуя полному и своевременному выявлению всех инфицированных.
Антитела к вирусу гепатита С (анти-HCV) вообще образуются медленно, в течение 8—15 нед от момента инфицирования, но у иммунокомпетентных лиц персистируют в организме длительно и в большинстве случаев пригодны для выявления гепатита С, являясь в настоящее время рутинным и скрининговым маркером.
Некоторые авторы, проводившие немногочисленные и небольшие по объему исследования у иммунокомпрометированных пациентов, указывают на возможность отсроченного образования антител к вирусу гепатита С и считают недостаточным использование только ИФА для диагностики данного заболевания у этого контингента пациентов. В частности, С. Cornu и соавт. обнаружили, что у 5 из 6 обследованных ими иммунокомпрометированных пациентов анти-HCV начали обнаруживаться лишь спустя 14 мес и более от момента инфицирования, установленного с помощью ПЦР.
По данным М. Arico и соавт., антительная диагностика позволяет выявить около 70 % детей с ОЛЛ, инфицированных вирусом гепатита С. Значение ПЦР в выявлении пациентов, инфицированных вирусами гепатитов В и С, продемонстрировано при обследовании турецких детей: у 13,9 % больных с онкологическими гематологическими заболеваниями диагноз гепатита В установлен только при обнаружении ДНК вируса гепатита В, а 5,8 % анти-HCV-негативных детей оказались инфицированными вирусом гепатита С при тестировании РНК.
В то же время синтез анти-НВс IgM, сопутствующий в иммунокомпетентном организме вирусной репликации и являющийся одним из ее маркеров, у пациентов с онкологическими гематологическими заболеваниями почти отсутствует, а у пациентов без онкологических гематологических заболеваний происходит их активная наработка (7,7 % против 78,6 %).
С общебиологической точки зрения, выявленные феномены ждут объяснения, а в прикладном плане они демонстрируют особенности специфической диагностики инфицированности вирусом гепатита В у больных с онкологическими гематологическими заболеваниями и необходимость поиска других подходов к распознаванию болезни. Этой цели служит использование ПЦР, которая позволяет существенно повысить выявляемость пациентов с онкологическими гематологическими заболеваниями, инфицированных вирусом гепатита В: в 16 % случаев обнаружение ДНК этого вируса было единственным маркером инфицирования.
Более того, у 50 % детей, находившихся на полихимиотерапии и позитивных по каким-либо маркерам вируса гепатита В, вирусная ДНК выявлялась в отсутствие HBeAg, т. е. была единственным показателем репликации вируса, в то время как среди детей без онкологических гематологических заболеваний подобная ситуация встречалась лишь в 14,5 % случаев, т. е. в 3,5 раза реже.
При гепатите С также не обнаружено параллелизма между выявлением анти-HCV и РНК вируса гепатита С. Весьма демонстративным было преимущество тестирования РНК перед антительной диагностикой: у 44,4 % детей с онкологическими гематологическими заболеваниями РНК вируса гепатита С оказалась единственным маркером инфицирования.
Как и при гепатите В, диагностическая значимость генных и антительных маркеров зависит от фазы ПХТ. Период интенсивного и поддерживающего лечения онкологического гематологического заболевания при гепатите С — это время абсолютной репликативной активности и резкого снижения антителообразования, способность к которому частично восстанавливается по завершении полихимиотерапии. В наших наблюдениях у 74,9 % детей это сопровождалось продолжением вирусной репликации.
Практические выводы о специфической диагностике гепатитов В и С у пациентов с онкологическими гематологическими заболеваниями сводятся к следующему:
1) рутинные подходы недостаточны для распознавания инфицированности пациентов с онкологическими гематологическими заболеваниями вирусами гепатитов В и С;
2) необходимо комплексное исследование всего известного спектра маркеров;
3) ведущую, определяющую роль в диагностике гепатитов В и С у пациентов с онкологическими гематологическими заболеваниями играет тестирование ДНК вируса гепатита В и РНК вируса гепатита С в ПЦР;
4) только путем внедрения ПЦР-диагностики в учреждениях для больных с онкологическими гематологическими заболеваниями можно обеспечить полную и своевременную диагностику гепатитов В и С;
5) обязательность обследования всех пациентов с помощью современных маркеров:
— при поступлении;
— при повышении активности АЛТ на этапах ПХТ;
— каждые 3—6 мес в ходе и в течение года после ПХТ.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Гепатит С. Вирус гепатита С. Диагностика гепатита С. Лечение гепатита С. Профилактика гепатита С.
Гепатит С обычно протекает хронически и характеризуется преимущественным развитием хронических форм гепатита с исходом в цирроз и первичную карциному печени. Вирус гепатита С включён в состав рода семейства Flaviviridae.
Резервуар возбудителя гепатита С — инфицированный человек. Основной путь передачи вируса гепатита С — парентеральный. Основное отличие от эпидемиологии вируса гепатита В — более низкая способность вируса гепатита С к передаче от беременной к плоду и при половых контактах.
Больной выделяет вирус гепатита С за несколько недель до появления клинических признаков и в течение 10 нед после начала проявлений. Заболевание чаще регистрируют в США (до 90% всех трансфузионных гепатитов) и Африке (до 25%).
Для клинической симптоматики вирусного гепатита С характерны изменение консистенции и размеров печени. При активном процессе печень обычно увеличена и болезненна при пальпации, её консистенция умеренно плотная. Другие проявления включают спленомегалию, диспепсический и астенический синдромы, желтуху, артралгии и миалгии, кардиты, васкулиты, лёгочные поражения, анемии и др. Осложнения хронического процесса — цирроз и первичная карцинома печени.

Принципы микробиологической диагностики гепатита С
Маркёры репликации вируса гепатита С — AT [IgM) к Аг вируса гепатита С и вирусная РНК. Маркёры гепатита С выявляют методами ИФА и ПЦР.
Показание для поиска AT или РНК вируса гепатита С — любое воспалительное заболевание печени. Вирусспецифические AT появляются в среднем через 3 мес и указывают на возможное инфицирование вирусом гепатита С или на перенесённую инфекцию. В серонегативный период выявляют РНК вируса гепатита С. Для подтверждения результатов ИФА, а также при обследовании пациентов, не относящихся к основным группам риска, применяют метод рекомбинантного иммуноблотинга, позволяющий эффективно исключить ложноположительные результаты ИФА.
Лечение и профилактика гепатита С
Средства этиотропной терапии гепатита С отсутствуют; при хронических инфекциях можно использовать а-ИФН. На фоне терапии ИФН у 40-70% больных отмечают стихание воспалительного процесса (на что указывает снижение содержания концентрации аминотрансфераз в сыворотке), однако по окончании курса у 40-50% пациентов наблюдают рецидив воспаления.
Средства специфической иммунопрофилактики гепатита С не разработаны.
Парентеральные гепатиты — инфекционные болезни вирусной этиологии, характеризуются поражением печени, длительным течением, вирусоносительством, часто заканчиваются острой печеночной недостаточностью, циррозом печени и первичным раком печени. Антропонозы. Передаются через кровь и половым путем.
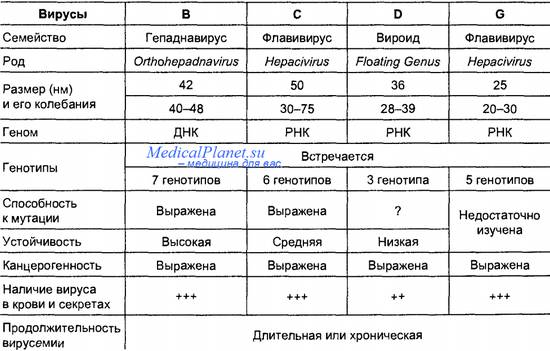
Заболевания вызывает группа вирусов, основными из которых являются вирусы гепатитов В, С, D и G.
Морфология. ВГВ — сложноорганизованный ДНК-содержащий, 2-х цепоченый, имеет дефект цепи на 30%, содержит ДНК полимеразу, вирус сферической формы, его диаметр 42—47 нм. Вирус состоит из сердцевины, построенной по кубическому типу симметрии и представляющей сердцевинный (НВс) антиген, а также липидсодержащей оболочки, несущей поверхностный HBs-антиген. Внутри сердцевины находятся ДНК, ДНК-полимераза и концевой белок — Нбе-антиген.
Культуральные свойства. ВГВ культивируется только в культуре клеток, полученной из ткани первичного рака печени в виде персистирующей инфекции, не вызывает цитопатического эффекта. В куриных эмбрионах не культивируется. Культивируется в клетках опухолей гепатоцитов. К вирусу чувствительны приматы (шимпанзе, горилла, орангутанг), которых используют в качестве экспериментальной модели.
Резистентность. ВГВ высокоустойчив к факторам окружающей среды и дезинфицирующим веществам. Температуру —20 °С выдерживает более 10 лет. При нагревании до 100 °С в течение 2—5 мин сохраняет инфекционную активность. Термоустойчивость вируса повышается, если он находится в крови. Вирус устойчив к длительному воздействию кислой среды (рН 2,3), УФ, спирта, фенола. Чувствителен к формалину, эфиру, хлорамину.
Антигенная структура. ВГВ обладает сложной антигенной структурой. В суперкапсиде вируса находится Hbs-антиген – в инкубационный и продромальный период определяется в сыворотке крови. HBc(cor) – внутренний, связан с нуклеопротеином, в крови не бывает, определяется в гепатоцитах. Hbe – при выходе из гепатоцитов, появляется чуть позже, чем Hbs в крови.
Эпидемиология. Основным резервуаром и источником инфекции является человек — больной и вирусоноситель, общее число которых в мире превышает 300 млн. Ежегодно в мире от вирусных гепатитов умирают около 2 млн человек. Россия относится к регионам с относительно высокой распространенностью гепатита В. Развитие инфекционного процесса наступает при попадании вируса в кровь. Заражение происходит при парентеральных манипуляциях. ВГВ передается трансплацентарно от матери к плоду и при прохождении плода через родовые пути. Вирус у инфицированных лиц находится во всех биологических жидкостях: крови, слюне, моче, сперме, влагалищном секрете, синовиальной, цереброспинальной жидкости, грудном молоке. В крови ВГВ появляется за 2—3 мес до проявления симптомов поражения печени и сохраняется до 5 лет после клинического выздоровления.
Патогенез. Инфекционный процесс наступает после проникновения вируса в кровь. Вирус из крови посредством эндоцитоза проникает в гепатоцит. После проникновения вируса в гепатоцит плюс-нить ДНК ДНК-полимеразой достраивается до полноценной структуры, после чего возможно развитие двух типов вирусной инфекции: интегративной и продуктивной. Интегративная инфекция сопровождается интеграцией (включением) кольцевой ДНК вируса в хромосому печеночной клетки-гепатоцита с образованием в ней провируса. При продуктивной инфекции в результате формирования новых вирусных частиц наблюдается клинически выраженный острый или хронический гепатит, маркером которого служит появление в крови анти- HBс-антител. Репликация вируса происходит в цитоплазме гепатоцитов. При этом вирус не разрушает гепатоциты, а индуцирует иммунопатологические реакции, обусловленные тем, что HBcAg, накапливающийся на поверхности гепатоцита, придает гепатоциту свойства антигенной чужеродности. В результате этого в организме формируется популяция Т-киллеров, которые, взаимодействуя с HBcAg как с рецептором, расположенным на поверхности гепатоцита, вызывают лизис клеток.
Клиника. Инкубационный период продолжается от 2 до 6 мес. Клиническая картина характеризуется симптомами поражения печени, в большинстве случаев сопровождающихся развитием желтухи. Возможны и безжелтушные формы. В 1 % случаев возникают молниеносные формы, обычно со смертельным исходом. Острый гепатит в 5—10 % случаев переходит в хронический, с развитием цирроза и носительства ВГВ. Вероятность возникновения носительства ВГВ особенно велика (в 50—90 % случаев) у детей 1-го года жизни, заразившихся от матери.
Гуморальный иммунитет, представленный главным образом антителами к Hbs-антигену, защищает гепатоциты от вируса. Клеточный иммунитет, в формировании которого основная роль принадлежит HBcAg, обеспечивает освобождение организма от инфицированных гепатоцитов. Переход острой формы болезни в хроническую связан с нарушением клеточного иммунитета, а также синтеза интерферона и интерлейкина-1.
Диагностика. Используют серологический метод и ПЦР. Методами ИФА и РИГА определяют в крови маркеры гепатита В: в инкубационный и продрому Hbs и Hbe Ag, титр Ат низкий. К концу инкубационного периода и в начале продромы появляются Ат – анти HbsIgM, потом титр этих Ат падает, и появляются HbcIgG. В период реконвалесценции, когда в крови отсутствует HbsAg, появляются Ат против HbsAg. Параллельно в этот период невысокий титр анти HbeIgM. С помощью ПЦР выявляют вирусную ДНК в крови и биоптатах печени.
Лечение. В терапии используют интерферон и ингибиторы ДН К-полимеразы.
Профилактика. Важнейшим и наиболее эффективным методом профилактики гепатита В является исключение попадания вируса при парентеральных манипуляциях и переливаниях крови. Это достигается: а) применением одноразовых шприцев, систем для переливания крови, инструментов с последующим после их использования регламентированным сбором и уничтожением; б) надежной стерилизацией инструментов в централизованных стерилизационных пунктах; в) проверкой на наличие Hbs-антигена крови доноров, а также доноров органов и тканей, используемых для трансплантации и искусственного осеменения; г) учетом всех вирусоносителей в диспансерах и лечением больных гепатитом В в специализированных отделениях инфекционных больниц. Персонал, контактирующий с кровью, обязан работать в перчатках. Группу высокого риска заражения гепатитом В составляют хирурги, гинекологи, акушеры, стоматологи, медицинские сестры, сотрудники отделений переливания крови и гемодиализа, работники лабораторий, лица, занятые в производстве иммунобиологических препаратов из донорской и плацентарной крови. Для предотвращения передачи гепатита В половым путем принимают меры, аналогичные таковым при ВИЧ-инфекции.
Специфическая профилактика осуществляется вакцинацией рекомбинантной генно-инженерной вакциной, содержащей HBs- антиген. В России разрешено применение отечественной рекомбинантной дрожжевой вакцины против гепатита В, а также аналогичной вакцины, выпущенной зарубежными фирмами.
Новорожденные, родившиеся у матерей — носителей ВГВ и больных гепатитом В, подлежат 4-кратной вакцинации. В этом случае первичное введение вакцины проводят в первые 24 ч жизни, далее — в соответствии с календарем прививок; 3-кратной вакцинации подлежат дети, в семьях которых есть носитель HBs- антигена или больной гепатитом В, а также воспитанники домов ребенка и интернатов, начиная с 4—5-месячного возраста. Среди взрослого населения 3-кратной вакцинации подвергаются лица, относящиеся к группе высокого риска заражения гепатитом В. Длительность поствакцинального иммунитета не менее 7 лет.
Вирус гепатита С (ВГС) относится к семейству Flaviviridae, роду Hepacivirus. Это РНК-содержащий вирус; имеет сферическую форму, диаметр 55—65 нм, сложно организованный. Геном вируса представлен линейной однонитчатой РНК, обладает большой вариабельностью. Известно более 10 генотипов вируса. Наиболее патогенным является генотип lb. Антигенами вируса являются сердцевинный С-протеин, гликопротеины оболочки (е-протеины 1 и 2) и неструктурные белки (NS).
Болезнь, вызываемая ВГС, широко распространена, заболеваемость нарастает с каждым годом. Природный резервуар вируса неизвестен. Экспериментальную инфекцию можно вызвать у шимпанзе. В чистом виде вирус гепатита С не выделен. Имеются успешные попытки адаптировать вирус к культуре тканей.
ВГС чувствителен к эфиру, детергентам, УФ-лучам.
Заражение ВГС аналогично заражению ВГВ. Однако для заражения ВГС требуется большая заражающая доза, чем при гепатите В. Наиболее часто ВГС передается при переливаниях крови.
Клиническое течение острого гепатита С более легкое, чем гепатита В, часто встречаются безжелтушные формы. Но несмотря на более легкое течение, в острой форме в 50 % случаев процесс переходит в хронический с развитием цирроза и первичного рака печени.
Диагностика. Диагностика серологическая: определяют антитела к вирусу гепатита С методом ИФА и ПЦР.
Лечение. Применяют интерферон и рибавирин.
Профилактика. Включает те же мероприятия, что и при гепатите В. Вакцина против гепатита В не защищает от гепатита С.
Резервуаром вируса в природе являются больные и вирусо- носители. Заражение ВГО аналогично инфицированию ВГВ. Одновременное инфицирование вирусами гепатитов В и D (ко- инфекция) приводит к развитию умеренной формы болезни. Инфицирование ВГО больных хронической формой гепатита В утяжеляет течение инфекции, приводя к развитию острой печеночной недостаточности и цирроза печени. В свободном виде ВГО в крови инфицированных им лиц не обнаруживается, его можно выявить в гепатоцитах.
Диагностика. Применяют серологический метод — определяют антитела к ВГО методом ИФА.
Лечение. Используют интерферон.
Вирус гепатита G еще мало изучен. Он относится к семейству Flaviviridae, роду Hepacivirus. Предполагают, что этот вирус обладает дефектом в сердцевинном белке и для его репликации требуется помощь вируса гепатита С.
Читайте также:

