Прививки против рака шейки матки вируса папилломы человека
Обновлено: 12.05.2024
Вакцина против ВПЧ нужна только тем, кто еще не начал половую жизнь, или это нет так? Какие бывают вакцины от ВПЧ и вызывают ли они бесплодие? Чем можно вакцинироваться, если ты живешь в России?
Сколько существует вакцин против ВПЧ и как они работают?
Кому подходит вакцина от ВПЧ?
В ВОЗ заявили, что в качестве профилактики рекомендуется делать вакцину девочкам 9–14 лет до начала половой активности. Вакцинация вторичной целевой группы: девочек от 15 лет и мальчиков рекомендуется, если она возможна, экономически эффективна и не отвлечет ресурсы от вакцинации первичной целевой группы населения.
ВПЧ и правда так опасен, что от него стоит вакцинироваться?
Ученые доказали, что онкогенные типы ВПЧ приводят к раку шейки матки. Всего есть более 100 видов ВПЧ, из них примерно 14 могут стать причиной развития рака.
ВПЧ почти невозможно обнаружить самостоятельно, так как вирус никак не влияет на функционирование организма и проходит без дополнительной терапии через несколько месяцев.
В предыдущем параграфе мы упоминали, что самые опасные онкогенные типы ВПЧ — это 18 и 16. Они ответственны за 70% случаев рака шейки матки — этот вид онкологии находится на втором месте в мире по частоте среди женщин. На первом — рак молочной железы. Также рак шейки матки сильнее всего сокращает жизнь, в среднем на 24 года. От него умирают более 300 тыс. человек в мире ежегодно.
В мире проживает 2 869 млн женщин в возрасте от 15 лет и старше, которые подвержены риску развития рака шейки матки. По текущим оценкам, каждый год 569 тыс. женщин заболевают раком шейки матки и 311 тыс. умирают от этой болезни.
В России рак шейки матки находят ежегодно у 15 тыс. человек. Наша страна находится на 13 месте по показателю заболеваемости раком шейки матки среди европейских стран.
На сколько вакцины эффективны?
Самую высокую эффективность в борьбе с ВПЧ установили у тех, кто еще не встречался с вирусом — 97–100 %.
Если же рассмотреть и тех, кто уже начал половую жизнь и встречался с ВПЧ, то эффективность вакцинации в предотвращении ВПЧ-заболеваний существенно ниже — 44–61%. Процент зависит от вакцины.
Я слышал, что вакцина может привести к бесплодию, это правда?
Нет, но миф о бесплодии до сих пор существует. Он появился после публикации исследования о сниженной вероятности забеременеть у американских девушек от 25 до 29 лет.
Спустя около шести месяцев статью отозвали, так как нашли в ней серьезные ошибки.
Какая ситуация с вакциной от ВПЧ и вакцинацией в России?
В июле этого года в России объявили о начале тестирования вакцины.
Все три вакцины от ВПЧ прошли необходимые стадии тестирования и проверки, информация об их безопасности опубликована в международных научных журналах, например, Journal of the American Medical Association и New England Journal of Medicine.
В России прививка от вируса папилломы человека не входит в Национальный календарь прививок, но для детей она может быть доступна по региональным календарям, а также по территориальным и региональным программам. Это будет бесплатно. Но для взрослых вакцина платная.
1. Кого надо вакцинировать?
Этот вопрос — предмет яростных баталий среди экспертов. Согласие достигнуто только по одному пункту: вакцинировать надо детей и подростков, в идеале — до полового дебюта, потому что вакцина может предотвратить заражение, а не прогнать уже заселившийся вирус. В октябре 2012 года ВОЗ официально внесла вакцину от ВПЧ для девочек в календарь прививок ВОЗ.
Это значит, что все страны мира, признавшие главенство ВОЗ (РФ признает), должны включить эту вакцину в свои национальные календари. Оптимальным возрастом для вакцинации в настоящее время считают 9–13 лет. В отношении вакцинации взрослых все еще существуют разногласия. В нашей стране вакцинопрофилактика рекомендована (но, увы, не обязательна) для девочек и женщин до 45 лет.

По данным на 15 мая 2018 года 1 , 80 стран мира включили ВПЧ-вакцину в свои национальные программы иммунизации для девочек. Вакцина повсеместно разрешена в США и в Японии.
2. Какие бывают вакцины против ВПЧ?
В настоящее время есть выбор из трех вариантов.

Гардасил — защищает от четырех типов ВПЧ: 16 и 18 (высокоонкогенные) + 6 и 11 (вызывают остроконечные кондиломы). Девочкам и мальчикам в возрасте 9–13 лет вводят две дозы вакцины (ввести и повторить через 6 месяцев). С 14 лет рекомендовано три введения (введение, через 2 месяца и через 6 месяцев). Возможна ускоренная программа вакцинации: введение, через месяц и еще через 3 месяца.
Если ребенок уже начал жить половой жизнью, то вакцинация проводится трехкратно вне зависимости от возраста.
К регистрации в нашей стране готовится новая вакцина Гардасил-9, которая защищает от 9 типов ВПЧ (в США разрешена с декабря 2014 года). Режим вакцинопрофилактики будет аналогичным 2 .
3. Насколько это вообще эффективно?

На сайте ВОЗ регулярно публикуются бюллетени по вакцинации, в том числе и на русском языке (май 2017 г.). Их пишут большие коллективы экспертов после тщательного изучения самой полной доказательной базы.
Современные исследования показывают, что полноценно проведенный до начала половой жизни курс вакцинации снижает риск развития ВПЧ-ассоциированного рака на 99 %. Даже однократное введение Церварикса дает 100%-ную серозащиту от ВПЧ-16 и ВПЧ-18 на 4 года 3 .
В Австралии благодаря массовой вакцинации Гардасилом уже через 3 года заболеваемость остроконечными кондиломами снизилась на 73 %, предраковых заболеваний шейки матки стало меньше на 38 %. Спустя 10 лет на материке практически не регистрируются ВПЧ-ассоциированные заболевания.
4. Нужно ли сдать анализы на ВПЧ перед вакцинацией?

Именно поэтому сейчас всё чаще говорят о необходимости вакцинации женщин, излечившихся от предраковых заболеваний шейки матки (CIN). Жизнь-то длинная, вполне возможно повторное заражение ВПЧ.
5. Могут ли быть побочные эффекты?
В настоящее время против ВПЧ вакцинированы миллионы людей во всем мире. Известно, что иногда наблюдается покраснение и болезненность в месте введения препарата. Редко встречаются небольшое повышение температуры, головная боль и головокружение, тошнота, обмороки.
Глобальный консультативный комитет ВОЗ по безопасности вакцин регулярно рассматривает данные о безопасности ВПЧ-вакцин, последнее на настоящий момент заключение было сделано в январе 2016 года: имеющиеся данные не вызывают тревоги относительно безопасности для здоровья 4 .
Несмотря на то что вакцинация является лучшим способом предотвращения ВПЧ-ассоциированных заболеваний и рака шейки матки, она не позволяет отменить рутинный цервикальный скрининг. Во-первых, некоторые редкие случаи рака шейки матки не связаны с ВПЧ. Во-вторых, защита от ВПЧ хороша, но не абсолютна. Однако по аналогии с другими прививками — привитые хотя и могут заболеть, но у них практически не бывает тяжелого течения заболевания или осложнений.
1 Data source: WHO/IVB Database, as of 15 May 2018. Map production Immunization Vaccines and Biologicals (IVB), World Health Organization.
2 Petrosky E, Bocchini JA Jr, Hariri S. et al. Use of 9-valent human papillomavirus (HPV) vaccine: updated HPV vaccination recommendations of the advisory committee on immunization practices. Centers for Disease Control and Prevention (CDC). MMWR Morb Mortal Wkly Rep 2015; 64: 300–4.
3 Safaeian M et al. Durable antibody responses following one dose of the bivalent human papillomavirus L1 viruslike particle vaccine in the Costa Rica vaccine trial. Cancer Prev Res, 2013; 6: 1242–1250.


Давайте поговорим о стоимости вакцины и так называемом анализе эффективности этой стоимости, проведенной людьми, которые умеют считать каждый цент и сравнивать данные, чтобы знать, кому от продажи очередной панацеи есть выгода: государству или производителям. Когда мы говорим о государстве, то имеем в виду следующее: насколько спонсорированная государственная программа по предупреждению чего-то или борьбе и ликвидации с чем-то финансово оправдана и выгодна всему населению страны по сравнению с бездействием или старыми методами решения проблем.
В отношении проблем, связанных с ВПЧ, сравнивают стоимость диагностики и лечения последствий ВПЧ. Например, 100 000 женщин привили от ВПЧ инфекции, и у 100 000 женщин (привитых или непривитых) провели цитологическое обследование и у некоторых выявили отклонения в мазках, провели диагностику и лечение. Что выгоднее экономически: прививать, с учетом оплаты обследования, лечения, больничных и т.д, или продолжать традиционый скрининг предрака и рака ШМ путем цитологического исследования? Оказалось, что программа прививания финансово стоит дороже, чем использование все тех же традиционных цитологических мазков для выявления рака, а также лечения рака. Ведь благодаря внедрению в практику мазка на цитологию, уровень заболеваемости раком шейки матки удалось понизить на 70% ( с 14 до 3-4 случаев на 100 000 женщин).Это колоссальный прогресс в развитых странах, который был достигнут без всяких вакцин. Государственные программы вакцинации молодого поколения могут позволить себе только богатые страны.
Мало того, комбинация прививания и скрининга молодых женщин на предраковые и раковые состояния шейки матки является не только не эффективной (не повышает уровень выявления этих состояний), но является чрезвычайно дорогостоящей, особенно для медицинских учреждений, зависящих от государственного бюджета, и для молодых женщин, где доминирует частная медицина и оплата за услуги проводится пациентами. Кому на руку в таком случае эти массовые прививания и массовые скрининги? Только тем, кто вовлечен в частный сектор медицины и создает на этом доход или тем, кто как пиявка высасывает деньги из государственных программ вакцинации, имея доступ к правительственной кормушке, а также самим производителям вакцины.
Как показывает несколько независимых анализов стоимости эффективности вакцин против ВПЧ инфекции, эта эффективность низкая на фоне высокой стоимости вакцины, как в отношении предраковых и раковых состояний шейки матки, так и в отношении генитальных бородавок. А применение вакцины для профилактики анального рака или рака головки полового члена вообще считается нерациональной.
Таким образом, важный вопрос, как долго длится защитная функция вакцины, остается спорным в соотношении с другим вопросом: насколько рационально делать прививание в раннем юношеском возрасте, если практическая эффективность вакцины составляет 3-4 года? Кроме того, оказалось, что серьезные клинические исследования по применению вакцины у подростков моложе 15 лет не поводились. Поэтому возникает еще один вопрос среди честных врачей и обеспокоенных родителей: если данных об эффективности и пользе вакцины от ВПЧ у детей до 15 лет не существует, на чем строится рациональность назначения вакцины детям 9-12 лет? По данным статистки в 44 странам мира средний возраст начала половой жизни составляет 18.4 лет. В развитых странах наметилась тенденция повышения возраста начала половой жизни: молодые люди стали осторожнее в выборе половых партнеров и потери девственности. Даже если учесть факт, что большинство городских подростков начинают половую жизнь рано, тем не менее, вопрос все тот же: насколько рационально проводить вакцинацию с 9 лет?
Сторонники вакцинации утверждают, что во многих странах половина школьников 9-12 классов (в США – около 43% в 2001 году, например) имела первый половой контакт, значит большая часть этих подростков уже инфицированы ВПЧ. В таком случае, прививка им уже не поможет. Это и есть аргументация прививания с 9 летнего возраста (3-4 класса)?
Дальше, другой вопрос: что делать в отношении профилактики ВПЧ инфекции по истечению 3-4 лет? Производители вакцины молчат. Если они начнут советовать проводить повторную вакцинацию (ревакцинацию), в ответ посыпятся протесты. Для многих известных вакцин, когда соблюден режим их использования, защита от ряда опасных инфекций длится от 10 лет и до конца жизни человека. Некоторые врачи усердно рекомендуют через 3 года вводить четвертую дозу Гардасила. Даже в своих публикациях они утверждают, что после четвертой дозы снова повышается уровень антител против ВПЧ в крови подопытных женщин. Так оно понятно, что когда вводят антиген, то появляются антитела, уровень которых снова постепенно падает. А дальше как? Снова ревакцинация?
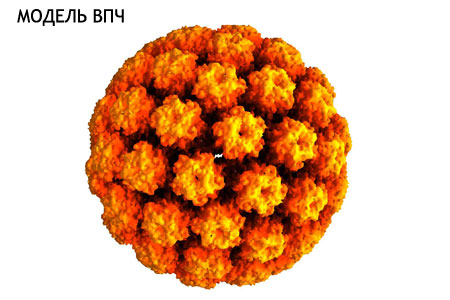
Теперь вернемся к статистике о частоте заболевания раком. С одной стороны, приведенные выше цифры могут все же напугать многих людей. С другой стороны, давайте посмотрим на эти цифры якобы с другого конца – с конца количества женщин, у которых НИКОГДА не возникнет рак шейки матки. Значит, если рак диагностируется в 3-4 случаях на 100 000 женщин от 30 до 65-70 лет, то у 99 996-99 997 женщин рака не будет. Правильно? Значит, 99.99% всех женщин никогда не будут иметь рак, даже если у них будет транзитная ВПЧ-инфекция по ходу жизни. И другая статистика, которой обычно пользуются врачи, говорит о том, что у более, чем 95% женщин никогда не возникнет рак шейки матки. Если вы умеете мыслить и сопоставите приведенные мною по ходу этой статьи статистические данные, то вы поймете, что шанс иметь этот вид рака чрезвычайно низкий. Еще ниже шансы иметь другие виды рака, как у мужчин, так и женщин, связанные с ВПЧ. Поэтому многие думающие люди, в том числе я, спрашивают: насколько рационально в таком случае прививать всех подряд девочек и женщин, если раком будут страдать единицы на фоне общей популяции разных стран, если 90% молодежи избавится от вируса папилломы человека без вредных последствий, а у оставшихся 10% с персистентной инфекцией рак шейки матки возникнет крайне редко тоже? Не лучше ли у этих 10% вовремя выявить и пролечить предраковое состояние?
Почему возник массовый психоз по отношению к вирусу папилломы человека? В 1999 году Др.Волбумерс с коллегами опубликовали статью о вирусе папилломы человека и его связи с возникновением рака шейки матки. Он предоставил данные гистологического исследования тканей шейки матки (ШМ) 932 женщин, страдающих раком шейки матки. У 99.8% этих женщин была обнаружена ДНК вируса папилломы человека. Именно эти проценты вызвали колоссальный ажиотаж среди врачей, в средствах массовой информации, а уже потом среди женщин всего мира. Однако в реальности степень вовлечения вируса папилломы человека в развитие рака ШМ ниже и составляет 75-80% случаев (в ряде публикаций до 90% случаев). Об этом мы поговорим чуть позже. Но на фоне такого открытия были сделаны очень ложные выводы, которые доминируют до сих пор: папиллома вирусная инфекция всегда, то есть в 99.8% случаев, приводит к раку шейки матки. Это неточное утверждение, и им нередко манипулируют, особенно по отношению к здоровью молодых женщин.
Теперь поговорим о вирусе папилломы человека. ВПЧ был обнаружен в 1984 году немецким ученым Харалдом цур Хаусеном, за что он получил в 2008 году Нобелевскую премию, благодаря появлению вакцины, предупреждающей развитие рака шейки матки и предраковых состояний. Вручили ученому только половину суммы премии (1.4 млн. долларов), потому что остальную часть вознаграждения отдали первооткрывателю ВИЧ, французскому вирусологу. Больше 10 лет со дня открытия ВПЧ ушло на поиск связи между этой инфекцией и раком шейки матки.
Вручение Нобелевской премии немецкому ученому повлекло серьезный мировой скандал о продажности комитета по вручению этой престижной награды, так как оказалось, что за выбором лауреатов стояла крупнейшая английская фармакологическая компания Астра-Зенека, имевшая колоссальные ставки в производстве новой вакцины от рака шейки матки и являющаяся спонсором Нобелевской организации-фонда. Пять членов комитета были платными консультантами для компании и получали большие гонорары от нее, в том числе в виде дорогостоящих, шикарных поездок заграницу. В расследование была вовлечена полиция, но Нобелевскому комитету удалось замять это дело, опять же не без помощи всемогущей фармакологической компании.
В природе существуют животные виды вируса папилломы, но на коже и слизистых человека обитают только человеческий вид этого вируса, поэтому его называют вирусом папилломы человека. Само название вируса говорит о том, что он вызывает рост бородавок (папиллом) и именно эта связь вируса с человеком известна давно – с момента его открытия.
Известно более 130 типов вируса папилломы человека. Большинство этих типов весьма безобидные и не приносят вреда человеческому телу. Все типы, которые вовлечены в возникновение генитальных бородавок и рака шейки матки, как и ряда других раков у мужчин и женщин, разделены на две основные группы – онкогенные типы низкого риска и онкогенные типы высокого риска. Больше 40 видов ВПЧ поражают аногенитальный тракт мужчин и женщин.
Помимо этой классификации существует классификация вирусов по ДНК-строению (чередованию определенных участков ДНК) на 5 классов: альфа, бета, гамма, дельта и мю. Альфа-вирусы инфицируют слизистые гениталий и ротоглоточной области и включают онкогенные типы, вызывающие рак шейки матки, поэтому изучены лучше и больше, чем другие представители ВПЧ.
Важно также знать, что выделено три вариации ВПЧ 16: Европейский (Е), Африканский (Af-1, Af-2) и Азиатский-Американский (Аа), а также три разновидности ВПЧ 18: Европейский (Е), Африканский (Af) и Азиатский-Америкоиндийский (AsAi). Забегая наперед в тему вакцинации от ВПЧ, у меня нередко возникает вопрос, на который я пока что не нашла удовлетворительного ответа: играет ли такая разновидность вирусов в создании ВПЧ-вакцины или нет? Если да, то насколько вакцина, созданная на основе одной разновидности вируса, будет эффективна в профилактике ВПЧ-инфекции в том регионе, где доминирует другой вариант вируса? Почему я задаю (фактически, сама себе) этот вопрос? Потому что такой же вопрос возникал у многих ученых, когда речь заходила о прививках против гриппа, при изготовлении которых использовались разные штаммы вирусов гриппа, но не специфичных для тех регионов, где потом продавались и внедрялись эти вакцины.
Как передаются ВПЧ? Только путем тесного телесного контакта (тело-к-телу или кожа-к-коже), что обычно происходит при половом акте, включая анальный и оральный секс. Вирус не передается через касание половых органов руками, а также через мастурбацию руками. Он также не передается через предметы интимной гигиены и сексуальные игрушки и приспособления.
Частота половых партнеров играет очень важную роль как фактор риска передачи вируса, поэтому с каждым новым партером риск заражения ВПЧ возрастает. Чем больше половых партнеров, тем выше риск заращения ВПЧ инфекцией, причем несколькими типами этого вируса. Нередко папиллома вирусную инфекцию относят к инфекциям, передающимся половым путем, потому что пик заражения ВПЧ вирусом выпадает на подростков и молодых людей, начавших и ведущих активную половую жизнь (70-80% инфицированных мужчин и женщин).
Около 10-12% женщин по всему миру заражены вирусом папилломы человека. Самая высокая частота инфицирования выпадает на страны Африки (24%), Восточной Европы (21.4%) и Латинской Америки (16.1%). Такие высокие показатели по сравнению со средне-статистическими мировыми показателями связаны с плохой гигиеной половых органов, низким уровнем использования презервативов и высоким уровнем беспорядочной половой жизни с частой сменой партнеров. До 30 лет более 70% женщин и мужчин были заражены ВПЧ хотя бы один раз в жизни, 45-50% женщин в возрасте 20-24 лет имеют ВПЧ-инфекцию. Чаще всего – это студенты училищ и высших учебных заведений. У 64% городских женщин-подростков в течение 2 лет от начала половой жизни находят ДНК вируса ВПЧ в выделениях. После первого полового акта инфекцией ВПЧ заражается почти одна треть женщин. После 30 лет уровень ВПЧ-инфекции кардинально понижается.
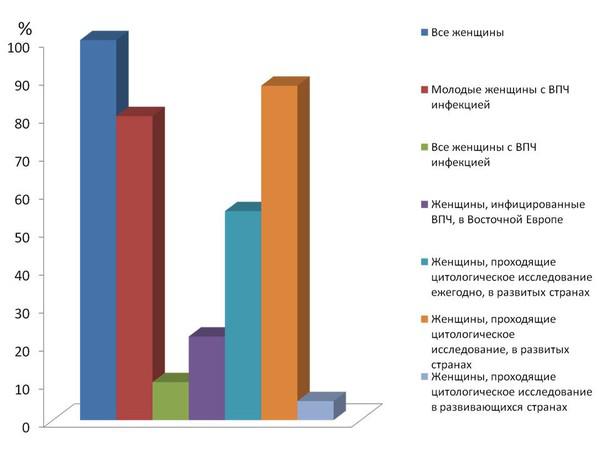
Многочисленные исследования показывают, что вирус папилломы человека исчезает и его ДНК невозможно определить во влагалищных выделениях у почти 60% женщин в течение 15 месяцев без негативных последствий для здоровья. Это важно запомнить, потому что это ключ к пониманию того, что вирус папилломы человека не так страшен, как о нем говорят многие люди, не имеющие абсолютно никаких современных знаний об этой инфекции.
Что важно помнить? Что у 90% женщин, зараженных ВПЧ, от инфекции не остается и следа в течение последующих 2 лет (чаще всего на очищение при отсутствии дисбактериоза влагалища и половых инфекций уходит три месяца). Только в 10% случаев инфекция может протекать дольше и тогда мы говорим о персистентной ВПЧ-инфекции. Но даже в таком состоянии изменения на слизистых шейки матки бывают не часто. Почему у большинства женщин происходит очищение организма от ВПЧ, а у небольшого количества инфекция продолжает прогрессировать, неизвестно. Другими словами, механизм возникновения предрака и рака шейки матки все же не изучен и не понятен. Очевидно, важную роль играет наличие факторов риска по образованию рака шейки матки, о которых мы поговорим позже, и агрессивность штаммов ВПЧ, что тоже является определенной поломкой-мутацией на уровне ДНК вируса, а также состояние защитных сил человеческого организма.
У 20% молодых девушек, никогда не имевших половых контактов через влагалище, находят ВПЧ во влагалищных выделениях и на вульве. Однако значение выявления ДНК вируса в развитии инфекционного процесса в таких случаях не выяснено до конца.
ВПЧ-инфекция также может быть вовлечена в развитие рака прямой кишки (точнее, ануса) и диагностируется приблизительно в 1.6 на 100 000 мужчин и женщин по всему миру. В 93% случаев находят ВПЧ 16 и 18. У бисексуальных мужчин и геев шанс развития анального рака в 17 раз выше, чем у гетеросексуальных мужчин.
Однако в отношении рака врачей и женщин интересует обнаружение интраэпителиального поражения высокой степени (тяжелой дисплазии), что есть предрак, и рака. 3-10% ДНК-положительных и 0,7% ДНК-отрицательных женщин имеют изменения в цитологическом мазке в виде умеренной и тяжелой дисплазий плоскоклеточного эпителия. Таким образом, на то огромное количество зараженных ВПЧ-женщин, показатели изменений в цитологическом мазке низкие. Другими словами, давайте все же не будем делать из мухи слона, пугая женщин развитием рака шейки матки у всех, у кого обнаружена эта инфекция.
Как диагностируется ВПЧ-инфекция? На современном этапе обследования существует три основных метода определения специфических типов ВПЧ в организме человека: (1) методы гибридизации, (2) методы полимеразной цепной реакции и (3) методы insitu гибридизации. У каждой группы методов есть свои преимущества и ограничения. Чаще всего используют метод полимеразной цепной реакции (ПЦР), которым определяют наличие ДНК вируса ВПЧ во влагалищных выделениях, то есть тип вируса. Методом гибридизации можно определить группы высокого и низкого риска, но не конкретный тип вируса. Если ваш врач ищет вирусы ВПЧ в крови или по анализу крови заявляет вам об инфицировании ВПЧ, гоните такого врача в шею.
Конечно, в сыворотке крови можно обнаружить антитела к ВПЧ, однако определяют их не с целью диагностики этой инфекции, а в экспериментальных целях, чтобы узнать, возникает ли иммунитет после перенесенной инфекции ВПЧ, а также как реагируют защитные силы организма на введение вакцины. Многих женщин, как и врачей, интересует вопрос: возникает ли длительная или пожизненная защита после того, как произошло заражение ВПЧ и организм очистился от вируса, или возможно повторное заражение одним и тем же типом ВПЧ? Как раз ответную защитную реакцию можно определить по уровню определенных антител в сыворотке крови, но результаты в этом направлении исследований пока что не утешительны. Очевидно, что женщины и мужичины могут заражаться ВПЧ несколько раз. Если снова находят один и тот же тип вируса у ДНК-отрицательного человека, который раньше имел ДНК-положительный результат, неизвестно, произошло ли повторное заражение или реактивация старой инфекции, которую в скрытом состоянии известными науке методами диагностики определить до этого не удавалось.
Читайте также:

