Пробиотики в лечении гепатита в
Обновлено: 24.04.2024
Е.А. Чихачева, Л.А. Тетерина, П.В. Селиверстов, В.П. Добрица, В.Г. Радченко
СЗГМУ им. И.И. Мечникова (каф. внутренних болезней и нефрологии), Санкт-Петербург
На сегодняшний день установлена роль микрофлоры в под держании здоровья организма-хозяина, которую выполняют индигенные представители нормальной микрофлоры кишеч ника. Под воздействием многих факторов, таких как климати ческие условия, загрязнение окружающей среды, образ жиз ни, нормофлора меняется в количественном и качественном отношениях.
Бактериологическими методами установлено, что наруше ние микрофлоры кишечника (дисбиоз) характеризуется зна чительным ростом численности микробов в просвете тонкой кишки (более 10 5 КОЕ/мл) и изменением микробного соста ва толстой кишки (снижение количества бифидо- и лакто бактерий, увеличение численности условно патогенной ми крофлоры).
Во-первых, было установлено, что поверхность слизистой оболочки тонкой кишки, так же как и других отделов кишеч ника, покрыта микроорганизмами. Формирование подобной биопленки обеспечивается способностью микроорганизмов к адгезии, то есть к прилипанию к мембранам. Количество их на поверхности слизистой оболочки тонкой кишки на 6 поряд ков превышает содержание их в полости кишки. Существен ную долю микробиоты тощей кишки (1,3-10 10 КОЕ/г) состав ляют аэробные и анаэробные актиномицеты и близкие к ним микроорганизмы.
Во-вторых, происходит существенное изменение доли эубактерий (род Eubacterium) среди других микроорганизмов кишечника (27% в тощей и 16% в ободочной кишке), а также их видовое изменение. Концентрация стрептомицетов, родококков и других представителей Actinomycetales в десятки раз увеличивается и/или уменьшается.
В-третьих, при некоторых болезнях происходит увеличе ние в десятки раз концентрации маркеров лактобацилл и би фидобактерий. Это побуждает к дифференцированному при менению широко распространенных пробиотиков на основе этих бактерий.
Клинические проявления дисбиоза в значительной степе ни определяются локализацией дисбиотических изменений. Различают дисбиоз тонкой кишки (синоним: синдром избы точного бактериального роста в тонкой кишке) и дисбиоз тол стой кишки.
Известно, что микробиота реализует свои функции в соста ве микробно-тканевого комплекса, образованного микроколо ниями бактерий и продуцируемыми ими экзополисахаридами; слизью; эпителиальными клетками слизистой оболочки и их гликокаликсом, а также клетками стромы слизистой оболочки. Структурная связь бактерий пристеночных колоний и кишеч ного эпителия реализуется посредством специфических рецеп торов на клетках слизистой оболочки, к каждому из которых адгезируются определенные виды бактерий. Последние содержат на своей поверхности лектины, ответственные за специфи ческую адгезию к эпителию. Своеобразие рецепторов генети чески детерминировано у каждого индивидуума.
В микробных сообществах, относящихся к нормальной ми крофлоре человека, эволюционно сформировались межклеточ ные кооперации, представляющие систему трофических и энер гетических взаимосвязей внутри кишечного микробиоценоза. Практически ни один биосубстрат, находящийся в распоряже нии того или иного микробного эпитопа, не используется толь ко в интересах одной популяции микроорганизмов (Верхов цева Н.В., Осипов Г.А., 2004; Steven R. Gill et al., 2006). Таких сложных цепочек существует огромное множество.
Кишечная микрофлора и печень являются основными си стемами, при взаимодействии которых осуществляются про цессы детоксикации организма. Микробиота в составе био пленки первой вступает в контакт со всеми субстанциями, по ступающими в организм с пищей, водой или воздухом атмос феры. Она трансформирует химические вещества в нетокси ческие конечные продукты либо в промежуточные соедине ния, легко разрушаемые в печени и удаляемые из организма. Нарушение взаимодействия печени и кишечника приводит к взаимным функциональным и структурным изменениям в них самих и в организме в целом. Вследствие этого гепатоэн- теральную регуляцию различных органических и неоргани ческих соединений можно без преувеличения причислить к кардинальным гомеостатическим механизмам. Сниженная де токсикационная функция микрофлоры при дисбиозе кишеч ника увеличивает нагрузку на ферментативные системы пече ни, что способствует возникновению в ней метаболических и структурных изменений. Обсемененность кишечника услов но патогенной и патогенной микрофлорой у больных хрони ческими заболеваниями печени ускоряет нарушение присте ночного пищеварения, тормозит синтез витаминов группы В, нарушает гепатоэнтеральную циркуляцию с образованием токсичных веществ, повышает проницаемость эпителия сте нок кишечника для бактерий, токсических продуктов, микро- и макромолекул. Иными словами, возникает порочный круг, который поддерживает взаимоотягощающее поражение как кишечника, так и печени. В то же время нарушения процес сов синтеза и экскреции компонентов желчи при заболевани ях печени могут привести к нарушению качественного и ко личественного состава микробиоты кишечника и в конечном итоге к нарушениям функционирования внутренних органов и развитию поливалентных клинических проявлений разви тия внутренней микробной дисгармонии.
В настоящее время выделяют три направления коррекции нарушений микробиоценоза кишечника у пациентов с хрони ческими заболеваниями печени:
Пробиотики — препараты или продукты питания, содержа щие живые штаммы нормальной кишечной микрофлоры. Важ ным механизмом их действия является антагонистический эф фект в отношении патогенных штаммов кишечной микрофло ры, обусловленный действием метаболитов нормальных бак терий, основными из которых являются короткоцепочечные ЖК и молочная кислота.
К микроорганизмам, на основе которых создаются пробио тики, предъявляются следующие требования:
- микроорганизм должен быть идентифицирован до вида по фено- и генотипическим признакам, должна быть исследо вана генетическая характеристика штамма, в том числе внехромосомные факторы наследственности;
- штамм должен относиться к виду, не вызывающему за болеваний человека, то есть должен быть авирулентным, апатогенным, безопасным для людей;
- свойства штамма должны быть стабильными при куль тивировании, в процессе производства и длительного приме нения на лабораторных животных;
- штамм должен проявлять антагонистическую активность к патогенным и условно патогенным микроорганизмам, при этом не должен угнетать представителей нормальной микро флоры; желательна хромосомная устойчивость к терапевтиче ским дозам антибиотиков;
- штаммы должны быть стабильны по биологическим свой ствам на всех стадиях процесса получения препаратов и при хранении их в регламентированные сроки.
Микробиологические критерии выбора терапевтически ак тивного пробиотика включают:
- высокую жизнеспособность бактериального штамма про биотика и быстрый переход штамма из анабиоза в метаболи чески активное состояние;
- антагонизм к патогенным возбудителям заболеваний па циента (бактериям, вирусам, грибам, микоплазмам и др.);
- отсутствие антагонизма и симбиоз с нормальной полез ной микрофлорой человека;
- отсутствие антагонизма нормальной микрофлоры к штам му пробиотика;
- адгезивная способность у штаммов пробиотиков и непро должительное время нахождения их в организме человека.
В настоящее время используются препараты и пищевые до бавки, содержащие различные микроорганизмы: бифидобак терии (Bifidobacterium bifidum, B. infantis, B. longum, B. breve, B. adolescentis, B. lactis, B. animals), лактобациллы (Lactobacil lus GG, L. acidophilus, L. plantarum, L. casei spp. rhamnosus, L. bre vis, L. helveticus, L. delbrueckii spp. bulgaricus, L. gasseri, L. fem— ientum, L. lactis), лактококки (Lactococcus spp. cremonis L. lactis spp. Lactis), кишечную палочку (Escherichia coli), энтерококки (Enterococcus faecium, E. faecalis), стрептококки (Streptococ cus salivarium spp. thermophilus, S. faecium, S. cremoris, S. lactis), пропионибактерии (Propionibacterium acnes), бациллы (Bacillus subtilis), грибы-сахаромицеты (Saccharomyces boulardii). Про биотики могут содержать как монокультуру, так и несколько видов микроорганизмов (симбиотики).
Методы исследования
- психометрическое определение качества жизни (КЖ) с помощью опросника SF-36;
- исследование клинического анализа периферической крови с определением количества тромбоцитов, гемоглобина, эритроцитов, лейкоцитов, СОЭ; биохимическое исследование сыворотки крови: опре деление общего белка, альбумина, концентрации общего би лирубина, активности аланинаминотрансферазы (АлАТ) и аспартатаминотрансферазы (АсАТ), щелочной фосфатазы (ЩФ), Y-глутамилтранспептидазы (ГГТП), общего холестери на, ЛПНП, ЛПВП, триглицеридов (ТГ)

Рис. 1. Этиологическая структура пациентов с хроническими заболеваниями печени.

Рис. 2. Изменение микрофлоры толстой кишки у больных хроническими заболеваниями печени.
- мочевины, креатинина, калия, глюкозы крови, протромбинового индекса (ПТИ), фибриногена;
- бактериологическое исследование кала;
- исследование состава микробных маркеров в крови мето дом газовой хроматографии — масс-спектрометрии для опре деления дисбиоза.
Характеристика исследуемой группы пациентов, режим и дозы назначения препарата
Нами были обследованы 30 больных с хроническими за болеваниями печени. Возрастной состав пациентов от 35 до 64 лет.
Линекс получали 20 пациентов, которые и составили основ ную группу, в группу сравнения были включены 10 пациентов с хроническими заболеваниями печени.
Группы были сопоставимы по полу, возрасту, этиологиче ской структуре, тяжести и степени активности патологиче ского процесса.
Этиологическая структура пациентов с хроническими за болеваниями печени представлена на рис. 1.
Распределение больных в зависимости от нозологии: 14 па циентов с неалкогольной жировой болезнью печени (НАЖБП) на стадии стеатогепатита (46,7%), с перекрестным синдромом (ПС): ПБЦ / аутоиммунный гепатит — 7 (23,4%), хрониче ский вирусный гепатит В (ХВГВ) — 4 (13,3%), хронический вирусный гепатит С (ХВГС) — 3 (18,8%), алкогольный гепа тит (АГ) — 2 пациента (6,6%).
С целью коррекции метаболических нарушений пациентам обеих групп назначался двухнедельный курс инфузионной те рапии, включающей раствор Рингера — ежедневно внутривенно капельно — 500,0, тиамина бромид (витамин В1) 3% раствор — ежедневно внутримышечно — 2,0, пиридоксина гидрохлорид (витамин В6) 5% раствор — ежедневно внутримышечно — 2,0, аскорбиновую кислоту (витамин С) 5% раствор — ежедневно внутривенно струйно — 3,0. Внутрь назначался гепатопротектор из группы эссенциальных фосфолипидов по стандартной схеме в течение 4 недель.
У всех больных в клинической картине заболевания пре обладали расстройство стула, частота поноса не превышала 3-6 раз в сутки. У 9 больных стул был необильный, кашицео бразной консистенции с примесью слизи, сочетался с метео ризмом, вздутием, урчанием и болями в животе. Остальные пациенты отмечали склонность к запорам.
У всех исследуемых преобладали проявления астеновегетативного синдрома (слабость, утомляемость, сонливость), сниже ние аппетита, боли ноющего характера в правом подреберье.
Было установлено, что нарушения кишечного микробио ценоза (КМ) выявлялись у всех обследованных как методом масс-спектрометрии, так и при посеве кала на дисбиоз.
У всех пациентов при посеве кала на дисбиоз отмечалось уменьшение на 2-3 порядка по сравнению с существующими нормативами содержания анаэробных микроорганизмов (бифи добактерий, лактобактерий, бактероидов, пептострептококков, эубактерий), относящихся к симбионтным микроорганизмам. На этом фоне наблюдалось повышенное содержание условно патогенных аэробных микроорганизмов (лактозоотрицатель ных эшерихий, клебсиелл и энтеробактерий, стафилококков, аэробных бацилл и дрожжеподобных грибов) в среднем до уровня 4-5 lgKOE/r. Количество нормальной кишечной па лочки находилось в границах допустимых значений, а содер жание энтерококков оказалось несколько сниженным.
У больных, получавших Линекс, происходило восстановле ние микрофлоры толстой кишки. Так, снижение степени дисбиоза наблюдалось у 19 человек (63,3%). Также наблюдалось повышение количества бифидобактерий, лактобактерий и об щего количества эшерихий (рис. 2).
Отмечалась также тенденция к уменьшению количества услов но патогенных штаммов (Klebs. pneumon., Enterobac. cloacae), p < 0,05, и патогенного штамма стафилококка золотистого.

Рис. 3. Динамика микробных маркеров на фоне терапии Линексом по данным масс-спектрометрии.

Рис. 4. Изменение активности аминотрансфераз и содержание билирубина в течение 4 недель у больных хроническими заболеваниями печени.
до (6,79 ± 0,32) и с (6,28 ± 0,98) до (6,22 ± 1,20) lgKOE/r соот ветственно (p > 0,05).
Анализ микробного состава фекалий методом ГХ-МС у боль ных ХЗП, принимавших Линекс, показал различные отклоне ния в составе микрофлоры. Прежде всего, у всех больных до назначения Линекса выявлено многократное в снижение обще го содержания бактерий в крови, дефицит колонизации лакто-, бифидо-, пропионобактерий и эубактерий при одновременном росте условно патогенной микрофлоры (рис. 3).
Использование Линекса у больных с хроническими забо леваниями печени сопровождалось выраженным снижением клинико-биохимической активности.
Отмечено более выраженное снижение активности амино трансфераз в группах больных, получавших Линекс, по сравне нию с контрольной группой, через 4 недели (табл. 1).
При этом более выраженная динамика снижения показате лей цитолиза отмечалась у больных с хроническим вирусным и токсическим гепатитом по сравнению с группой стеатогепатита и перекрестным синдромом.
Изменения активности ГГТП было отмечено у пациентов с токсическим поражением печени. Выраженных изменений активности щелочной фосфатазы (ЩФ) при приеме Линекса не наблюдалось.
На фоне приема Линекса в течение 4 недель у 6 человек с хро ническим вирусным и токсическим гепатитом также отмечалось достоверное (p < 0,05) снижение активности аминотрансфераз (АСТ, АЛТ) и билирубина, тогда как достоверного снижения ЩФ и ГГТП (p >0,05) отмечено не было (рис. 4.)
За время наблюдения побочных эффектов, явлений не переносимости препарата или нежелательных явлений получено не было. Все пациенты отмечали хороший клини ческий эффект.
Таблица 1. Динамика биохимических показателей пациентов с хроническими заболеваниями печени на фоне проводимой терапии.
| Биохимические показатели | Основная группа, n = 20 | p | Группа сравнения, n = 10 | p | ||
| До лечения | После лечения | До лечения | После лечения | |||
| АЛТ, Ед./л | 93,0 ± 7,0 | 53,0 ± 6,0 | p < 0,05 | 89,0 ± 8,2 | 78,0 ± 7,1 | p > 0,05 |
| АСТ, Ед./л | 137,0 ± 11,0 | 64,0 ± 14,1 | p < 0,05 | 128,0 ± 6,0 | 112,0 ± 8,0 | p > 0,05 |
| Билирубин, мкмоль/л | 62,0 ± 8,0 | 32,0 ± 7,1 | p < 0,05 | 35,0 ± 5,0 | 32,0 ± 4,0 | p > 0,05 |
| ГГТП, Ед./л | 252,0 ± 13,2 | 188,0 ± 12,0 | p < 0,05 | 153,0 ± 44,0 | 151,0 ± 40,0 | p > 0,05 |
| ЩФ, Ед./л | 351,0 ± 35,0 | 297,0 ± 44,0 | p > 0,05 | 246,0 ± 21,0 | 236,0 ± 24,0 | p > 0,05 |

Рис. 5. Динамика показателей качества жизни у больных хроническими заболеваниями печени на фоне терапии Линексом.
Следовательно, в результате курса лечения Линексом нор мализуются показатели фекальной микрофлоры и исчезают признаки бактериального обсеменения тонкой кишки. Изме нения микрофлоры слизистой оболочки тонкой кишки носят более глубокий характер и нормализуются медленнее. Поэто му лечение должно продолжаться и после наступления кли нической ремиссии.
Заключение
Обнаруженные тенденции к нормализации эубиоза дают основание рекомендовать применение Линекса не только до наступления клинической ремиссии, то есть нормализации стула и других симптомов, свойственных дисбиозу, но и после ее наступления. Таким образом, для получения полной карти ны нарушения микрофлоры как тонкой, так и толстой кишки необходимо совмещать методы диагностики: бактериологиче ский метод и масс-спектрометрию, что позволяет рациональ но строить проводимую терапию.

Вирусный гепатит С — тяжелое заболевание, при котором организм требует дополнительной поддержки. В частности, страдает микрофлора кишечника, от восстановления которой во многом зависит успех терапии. Специалисты рекомендуют принимать пробиотики для нормализации работы органов ЖКТ. К выбору препаратов следует подойти максимально ответственно.

Врач-гепатолог высшей категории, доктор медицинских наук. Оказывает бесплатные консультации по лечению Гепатита С в проекте "Мой Гепатит".
Что такое пробиотики?
Пробиотики — это препараты, содержащие живые микроорганизмы. При употреблении в умеренных дозах они приносят пользу организму, в ткани которого внедряются. Чаще всего пробиотики используются в качестве дополнительных биологических добавок для поддержки функциональности пищеварительной системы. Используются как в терапевтических, так и в профилактических целях.
Естественные пробиотики содержатся в продуктах из следующего списка:
- Натуральный йогурт
- Квашеная капуста
- Кефир.
- Кимчи.
- Темпе.
Согласно с нормативами ГОСТ Р 52349-2005 “Продукты пищевые и функциональные”, пробиотики относятся к функциональным биологическим сегментам, полезных для любого нетоксигенного (не вырабатывающего собственного яда) организма. Для достижения эффекта принимать их следует регулярно, не реже 1 раза в день. Применение пробиотиков обеспечивает нормализацию микрофлоры кишечника.
Как правильно выбрать пробиотики?

К выбору пробиотиков следует подойти максимально ответственно. Важно помнить, что различные колонии бактерий влияют на разные свойства человеческого организма. Поэтому при выборе определите цель приема препаратов:
- Избавление от запора. Улучшить перистальтику кишечника и обеспечить беспрепятственное прохождение каловых масс помогут бактерии типа Lactis. Кроме того, слабительным воздействием отличаются колонии L.plantarum, L.rhamnosus, L.acidophilus, L.reuteri и B.animalis.
- Избавление от диареи. Нормализовать стул помогут бактерии классов B.coagulans и S.boulardii и комбинация Lactobacillus и Bifidobacterium.
- Снижение веса. Для похудения и при диетическом питании рекомендуется отдать предпочтения комбинациям Lactobacillus rhamnosus и Bifidobacterium lactis, Lactobacillus gasseri и Lactobacillus rhamnosus.
- Улучшение работы мозга. Для улучшения памяти и других важных функций головного мозга рекомендуется применять Bifidobacterium breve, Lactobacillus rhamnosus, Bifidobacterium infantis, Bifidobacterium longum и Lactobacillus helveticus.
- Укрепление иммунной системы. В этих целях рекомендованы колонии Bifidobacterium longum, Lactobacillus gasseri и Bifidobacterium bifidum.
Существуют пробиотики и для общего укрепления организма. К таковым относятся Bifidobacterium bifidum. Колонии этих бактерий обеспечивают выработку жирных кислот, снижают уровень стресса, способствуют продуцированию серотонина и нормализации гормонального фона.
Зачем нужны пробиотики при гепатите?
При вирусном гепатите С функции печени угнетаются. Железа не может полноценно выводить токсины из организма, выработка желчи замедляется. При тяжелых формах ВГС возможен гормональный дисбаланс. Все это приводит к таким нарушениям, как:
- Расстройства органов желудочно-кишечного тракта: диарея, запоры, приступы тошноты и рвоты.
- Депрессивное состояние, проблемы со сном, спутанность сознания.
- Нарушение функциональности почек, поджелудочной железы и других внутренних органов.
Пробиотики при гепатите применяются с целью детоксикации организма и стабилизации работы ЖКТ. Дозированное употребление живых бактериальных колоний обеспечивает улучшение общего состояния пациента. Применение пробиотиков позволяет бороться с такими неприятными проявлениями гепатита, как тошнота, несварение и изменения психического состояния.

Какие препараты можно принимать?
Пробиотики при гепатите можно получать из еды. При диете №5, рекомендованной при данном диагнозе запрещены квашеная капуста, кимчи, темпе и многие другие продукты, насыщенные ферментами и живыми бактериями. Но употребление кефира и натурального йогурта больным с гепатитом С принесет большую пользу. Это поможет нормализовать кишечную микрофлору и устранить развивающиеся проблемы с ЖКТ.
Из препаратов с пребиотиками при гепатите С рекомендованы:
- Бифидумбактерин
- Линекс
- Филак Форте
- Энтерол
- Эффидижест
Все перечисленные выше пребиотики не препятствуют процессу лечения вирусного гепатита С. При этом улучшается состояние органов пищеварительного тракта, что приводит к быстрой всасываемости поступающих питательных и лекарственных веществ. Рассмотрим особенности каждого из препаратов по отдельности.
Бифидумбактерин и Линекс при гепатите
Бифидумбактерин — препарат, в состав которого входят колонии бактерий Bifidobacterium bifidum. Обладает общеукрепляющими свойствами, положительно влияет на пищеварение и обменные процессы. Бифидумбактерин при гепатите применяется в качестве профилактического средства для развития инфекции в кишечнике.
Препарат повышает иммунитет и способствует борьбе с гепатовирусом. Бифидумбактерин при гепатите следует принимать по 2 пакетика-саше 1-2 раза в сутки.
Линекс — лекарственное средство на основе порошка Либенина. В состав 1 г препарата входят:
- Lactobacillus acidophilus — 300 мг.
- Bifidobacterium infantis — 300 мг.
- Enterococcus faecium — 300 мг.
- Вспомогательные вещества: картофельный крахмал и лактоза.
Линекс при гепатите С применяется для нормализации микрофлоры кишечника. В день следует принимать по 1 капсуле 3 раза в день.
Хилак Форте и Энтерол при гепатите
Хилак Форте при гепатите С применяется для нормализации микрофлоры кишечника и устранения аллергических высыпаний. Пробиотик выпускается в виде прозрачного мутноватого раствора с нейтральным или вишневым вкусом. Хилак Форте при гепатите следует применять по 40-60 капель в день. Лекарство содержит следующие колонии живых бактерий:
- Escherichia coli
- Streptococcus faecalis
- Lactobacillus acidophilus
Энтерол при гепатите применяется в качестве противомикробного, противоглистного и противодиарейного средства. Выпускается в виде капсул или порошка. Каждая доза препарата содержит 250 мг бактерий Saccharomyces boulardii. Взрослым пациентам рекомендуется принимать по 1 единице лекарства в сутки. Энтерол при гепатите нормализует пищеварение и обеспечивает защиту от обезвоживания.
Эффидижест при гепатите
Эффидижест — натуральная биологическая добавка, основанная на колониях молочных бактерий. Базу препарата составляет сухое сырье в естественной закваске. Препарат выпукается в виде мерных саше. Эффидижест при гепатите применяется, как средство для нормализации пищеварения. Важно учитывать, что БАД запрещен к приему лицам с аллергией на лактозу или фруктозу.
Эффидижест при гепатите следует принимать 2 раза в день. Порошок растворяется в 1/2 стакана теплой воды и выпивается в процессе приема пищи.
Заключение
Пробиотики при гепатите — дополнительное средство лечения, способствующее быстрому восстановлению пищеварительной функции организма. Однако перед приемом убедитесь в том, что у вас нет аллергии на перечисленные выше средства. В этих целях примите небольшую дозу пробиотика и проследитеза реакциями организма. Если в течение 2 часов не проявятся неприятные симптомы — все в порядке.
Важно учесть, что при вирусном гепатите С любые формы самолечения недопустимы. Перед приемом пробиотиков посоветуйтесь со специалистом. Получить бесплатную консультацию гепатолога можно по ссылке→
Грачева Н.М., Щербаков П. Т, Аваков А.А., Мацулевич Т.В.
Военно-медицинский журнал № 5, 1999 г., С.51-57.
До настоящего времени острые кишечные инфекции (ОКИ) бактериальной и вирусной природы — шигеллез, сальмонеллез, кампилобактериоз, ротавирусные гастроэнтериты и другие — занимают значительную долю в общей структуре инфекционной заболеваемости. Так, по данным Федерального центра Госсанэпиднадзора МЗ РФ, инфекционная заболеваемость в Российской Федерации в 1997 г. на 100 тыс. населения составила: сальмонеллезом — 40.7, шигеллезом – 56.8, ОКИ, вызванными установленным возбудителем, — 61.4, неустановленным возбудителем — 240.6.
В последние годы по сравнению с данными 1989-1991гг. наблюдается рост заболеваемости военнослужащих шигеллезом и другими ОКИ.
Известно, что ОКИ нередко ведут к развитию воспалительных и дистрофических процессов в желудочно-кишечном тракте (ЖКТ), вторичных ферментопатий, дисбактериоза кишечника и к формированию хронических болезней и дискинезий органов пищеварительной системы.
В последние годы отмечается тенденция к отходу от широкого применения химиотерапевтических средств, особенно антибиотиков, в лечении ОКИ. В связи с этим возрастает практическая значимость патогенетической терапии, в частности пробиотиками, обладающими антагонистической активностью к широкому спектру патогенных и условно-патогенных бактерий, воздействующих на местные факторы иммунитета, иммунологическую реактивность и общую неспецифическую резистентность макроорганизма.
ББФ относится к комбинированным бифидосодержашим препаратам. Механизм его действия отличен от аналогичных пробиотиков. Препарат состоит из искусственно созданных микроколоний, каждая из которых является агрегатом Bifidobacterium bifldum (штамм 1), сорбированных на частицах активированного угля. Микроколонии интенсивно адгезируются на эпителии слизистой оболочки, обеспечивая ускоренное заселение кишечника бифидобактериями.
Процесс адгезии и последующей колонизации слизистой оболочки кишечника, как и биотический (репродуктивный) потенциал микробных клеток, а следовательно, и воздействие на многие физиологические функции макроорганизма, зависит от исходной концентрации вводимой суточной дозы бифидобактерий. Высокие дозы препарата, превышающие фармакопейные в 1000 раз, не оказывают токсического влияния на органы и ткани макроорганизма. Доказано, что ББФ местно не действует раздражающе и относится к нетоксичным веществам.
Под нашим наблюдением находились 103 взрослых больных обоего пола: 62 пациента (опытная группа) получали большие дозы ББФ (30 больных ОКИ, 11 — с хроническими болезнями ЖКТ, 21 — вирусным гепатитом В) и 41 пациент (группа сравнения, или контрольная) — обычные дозы бифидумбактерина . (20 больных ОКИ, 21 больной вирусным гепатитом В).
ББФ применяли по 45 доз на 1 прием 2 — 3 раза в день. Содержимое пакетиков смешивали в 50 мл кипяченой охлажденной воды. Больные принимали препарат во время еды или сразу после приема пищи.
Обычный бифидумбактерин применяли в соответствии с инструкцией к препарату — по 5 доз 2 раза в день за 30 мин до приема пищи. Продолжительность терапии ББФ составляла 5-7 дней у больных ОКИ и вирусным гепатитом В и 10-14 дней при хронических заболеваниях ЖКТ с выраженными явлениями дисбактериоза кишечника.
ББФ применяли курсами аналогичной продолжительности. Наряду с пробиотиками больные получали базисное патогенетическое лечение, включавшее средства пероральной и парентеральной регидрадаиии, дезинтоксикационную терапию, десенсибилизирующие препараты, витамины и симптоматические средства. Больным антибактериальные препараты не назначали. Оценивали данные клинических наблюдений, лабораторных, бактериологических и морфологических исследований.
Клинические испытания (табл.1) показали, что в опытной группе больных ОКИ, получавших большие дозы ББФ на фоне проводимой терапии, отчетливо наблюдалась положительная клиническая динамика: исчезали боли и урчание в животе, прекращалась диарея, улучшалось общее состояние. У больных ОКИ, получавших обычные дозы бифидумбактерина, также проявлялась сходная положительная клиническая динамика.
Сроки исчезновения основных клинических симптомов при острых кишечных инфекциях на фоне лечения большими дозами бифидумбактерина форте (n =30) и обычными дозами бифидумбактерина в порошке
Сравниваемый препарат, дозы
Срок исчезновения клинических симптомов
В то же время в опытной группе при купировании диспептических явлений отмечались достоверно более короткие сроки нормализации стула, прекращения болей и урчания в животе, чем у больных группы сравнения, что указывает на значительно лучшую клиническую эффективность больших доз ББФ.
У всех больных вирусным гепатитом В в сравниваемых группах до начала лечения пробиотиками на фоне клинико-лабораторных проявлений гепатита имелись симптомы поражения ЖКТ, которые обусловливались явлениями дисбактериоза кишечника: метеоризмом, неприятными ощущениями в животе, неустойчивым стулом и болями при пальпации по ходу кишечника.
У больных вирусным гепатитом В опытной группы на фоне лечения большими дозами ББФ отмечалась положительная клиническая динамика: нормализовался стул, исчезали диспептические явления. Положительная клиническая динамика наблюдалась и у больных группы сравнения. Однако сроки исчезновения названных клинических проявлений у пациентов опытной группы были достоверно короче, чем у больных группы сравнения, что также указывает на более выраженную клиническую эффективность больших доз ББФ при купировании симптомов дисфункции ЖКТ при вирусном гепатите В (табл. 2).
Сроки исчезновения основных клинических симптомов при вирусном гепатите В на фоне лечения большими дозами бифидумбактерина форте (n=1) и обычными дозами бифидумбактерина в порошке (n=21), сут (x± m)
Сравниваемый препарат, дозы
Срок исчезновения клинических симптомов
Известно, что при болезнях органов пищеварения с высокой частотой выявляются в той или иной степени выраженные нарушения микробной экологии ЖКТ. Нередко они становятся причиной различных дисфункций, вызывающих жалобы и требующих проведения соответствующей терапии. Имеющийся клинический опыт свидетельствует о хорошей терапевтической эффективности бактерийных биологических препаратов при хронических болезнях ЖКТ. Однако для достижения клинического и бактериологического эффекта требуются, как правило, длительные курсы лечения.
Большие дозы ББФ мы применяли курсом 14 дней у больных с сочетанной гастроэнтерологической патологией — хроническими гастритами, язвенной болезнью двенадцатиперстной кишки, хроническими колитами с выраженными клиническими симптомами кишечной дисфункции и явлениями дисбактериоза кишечника. Пациенты получали ББФ на фоне базисной терапии, соответствующей диагнозу основного заболевания, включавшей антациды, препараты висмута, Н2-блокаторы гистамина, ферментные препараты и симптоматические средства.
Как показали наши наблюдения включение больших доз ББФ в комплексную терапию указанных пациентов оказывало положительный терапевтический эффект при купировании диспептических явлений и соответствующих жалоб и существенно улучшало результаты лечения.
Большие дозы ББФ хорошо переносились больными. Лишь у одного пациента из этой группы на фоне лечения появились боли в животе и выраженный метеоризм, что потребовало отмены препарата.
Как показали бактериологические исследования (табл. 3), у больных ОКИ после курса лечения большими дозами ББФ отмечаются положительные сдвиги в составе кишечной микрофлоры. Это проявляется достоверным уменьшением частоты больных с выраженным дисбактериозом IV степени и возрастанием числа больных с нормальными показателями кишечной микрофлоры и слабо выраженными дисбиотическими проявлениями I степени.
Состояние микрофлоры кишечника при острых кишечных инфекциях до и после лечения большими дозами бифидумбактерина форте (n=30) и обычными дозами бифидумбактерина в порошке (n=20), % (p± m)
Испытуемый препарат, дозы
Состояние микрофлоры кишечника
Бифидумбактерин форте, большие
Бифидумбактерин в порошке, обычные
Примечание. Значимость различий сравниваемых показателей по критерию Стьюдента несущественна — Р>0,05*, существенна — P<0,05**, Р<0,01***
У пациентов группы сравнения состояние микробиоценоза кишечника после лечения было существенно хуже: несмотря на некоторые положительные тенденции в составе кишечной микрофлоры, достоверной разницы между показателями до и после лечения при указанной продолжительности курса лечения (3-5 дней при ОКИ) выявить не удалось. Это свидетельствует о более высокой бактериологической эффективности применения больших доз ББФ у больных ОКИ, их влиянии на микробиоценоз кишечника по сравнению с обычными дозами бифидумбактерина.У больных вирусным гепатитом В, получавших пробиотики более длительными курсами, до 7-10 дней, также отчетливо прослеживались отмеченные особенности (табл. 4).выраженные положительные изменения в состоянии микрофлоры кишечника, свидетельствовавшие о нормализующем влиянии указанного препарата на микробиоценоз.
Состояние микрофлоры кишечника при вирусном гепатите В до (n =21) и после (n=21)лечения большими дозами бифидумбактерина форте и обычными дозами бифидумбактерина в порошке, % (p± m)
Испытуемый препарат, дозы
Состояние микрофлоры кишечника
Бифидумбактерин форте, большие
Бифидумбактерин в порошке, обычные
Примечание. Значимость различий сравниваемых показателей по критерию Стьюдента несущественна — Р>0,05*, существенна — P<0,001**
Изучение динамики количественного содержания различных видов микроорганизмов — индигенной (постоянной) микрофлоры, представителей патогенных и условно-патогенных бактерий — у всех пациентов, получавших большие дозы ББФ, показало, что наиболее часто увеличивалось количество бифидобактерий: 66,7% — при вирусном гепатите В и 90,9% — при хронических болезнях ЖКТ. Одновременно у этих больных увеличивалось количество эшерихий (соответственно 13,7 и 36,4%) и лактобактерий (соответственно 26,7 и 28,8%). Количество эшерихий и лактобактерий в процессе лечения большими дозами ББФ часто не изменялось и оставалось без динамики при нормальных показателях или показателях нижних границ нормы. Обращает внимание, что в 3,3 — 23,3% случаев лактобактерии и эшерихии на фоне лечения оставались без положительной динамики: количественные показатели были сниженными, а в отдельных случаях лишь несколько снижались. В отношении динамики условно-патогенных бактерий: лучшие результаты (прекращение бактериовыделения) отмечены при хронических заболеваниях ЖКТ и назначении больших доз ББФ наиболее длительными курсами — до 14 дней, а также при вирусном гепатите В (курс лечения 7-10 дней). Хуже результаты оказались в группе больных ОКИ, получавших наиболее короткие курсы препарата — 3—5 дней.
Таким образом, количественные изменения индигенной микрофлоры ЖКТ на фоне лечения большими дозами ББФ в первую очередь относятся к бифидобактериям и в меньшей степени — к эшерихиям и лактобактериям. По мере увеличения продолжительности лечения положительные сдвиги в составе как индигенной микрофлоры, так и условно-патогенных бактерий становятся более отчетливыми.
Для оценки эффективности терапии проводили эндоскопическое исследование со взятием биоптатов слизистой оболочки толстой кишки (СОТК). Морфологические исследования выполнены при ОКИ и хронических болезнях ЖКТ и у здоровых на 49 биоптатах СОТК: 16 — от больных ОКИ в разгаре болезни и в острый период до начала лечения, 9 -после лечения большими дозами ББФ (опытная группа), 10 — после лечения обычными дозами бифидумбактерина (группа сравнения), 8 — после базисной терапии (контрольная группа), 6 — от здоровых лиц (норма). СОТК изучена гистологическим, гистохимическим, морфометрическим, бактериоскопическим и статистическим методами.
У больных ОКИ в разгар болезни в СОТК гистологически выявлялась картина острого катарального и катарально-геморрагического колита. При этом 70,8% учитываемых морфометрических показателей отличались от нормальных.
Включение высоких доз ББФ в комплексную терапию пациентам с ОКИ способствовало уменьшению толщины СОТК. В поверхностном и криптальном эпителии под влиянием лечения снижалось содержание межэпителиальных лимфоцитов, эозинофильных и нейтрофильных гранулоцитов. В герминативных зонах эпителия кишечных желез повышались митотическая активность и число желудочно-кишечных эндокриноцитов. Такая терапия способствовала сохранению повышенной плотности воспалительного клеточного инфильтрата в собственной пластинке СОТК за счет увеличения в последнем содержания плазматических клеток, тогда как количество макрофагов и нейтрофильных гранулоцитов в нем значительно снижалось.
Мы убедились, что включение ББФ в комплексное лечение положительно влияло на процессы репарации СОТК, переводя острый катарально-геморрагический колит в острый катаральный колит в стадии завершения патологического процесса.
ББФ положительно влиял на репарацию эпителиального пласта СОТК, устранял в ней выраженность воспаления, а также стимулировал действие факторов неспецифической и специфической местной зашиты.
Сравнивая морфометрические показатели СОТК двух аналогичных групп больных ОКИ, получавших в комплексной терапии разные пробиотики (коммерческий бифидумбактерин и ББФ), нами выявлены существенные различия по 40,9% учитываемых объективных параметров.
ББФ лучше, чем бифидумбактерин, предохранял поверхностный эпителий от проникновения в него эозинофильных гранулоцитов. В герминативных зонах эпителия крипт стимулировал митотическую активность и трансформацию стволовых клеток в желудочно — кишечные эндкриноциты, предохраняя последние от дегрануляции. В собственной пластинке СОТК он увеличивал число плазматических клеток, продуцирующих местно антитела. В то же время этот препарат препятствовал инфильтрации стромы нейтрофильными гранулоцитами. Следовательно, включение в комплексную терапию больных ОКИ высоких доз ББФ действует значительно лучше на репаративные процессы в СОТК, чем бифидумбактерин в обычных дозах.
При сопоставлении морфометрических показателей СОТК у больных ОКИ, у которых в комплексную терапию ББФ в высоких дозах, с таковыми показателями адаптированной нормы, установлено, что препарат способствовал в исследуемые сроки нормализации 50% объективных параметров. Под влиянием базисного лечения с включением в неё ББФ нормализовались толщина слизистой облочки и высота поверхностного эпителия.
Приведенное сравнение свидетельствую о том, что под влиянием терапии с включением в нее ББФ лучше восстанавливается эпителиальный пласт СОТК, чем её собственная пластинка.
После назначения ББФ в комплексную терапию хронических болезней ЖКТ отмечалась тенденция к повышению высоты поверхностного эпителия СОТК с уменьшением в нем дистрофических изменений. В кишечных железах увеличивалось содержание бокаловидных клеток, которые интенсивно продуцировали слизь с высоким содержанием в ней сульфомуцинов.
Полученные нами результаты свидетельствуют о том, что при включении ББФ в комплексную терапию упомянутых больных значительно активируются процессы репарации в СОТК.
ВЫВОДЫ
Гепатит В – неизлечимое хроническое пожизненное заболевание. Течение заболевания не сопровождается выраженными симптомами. Можно много лет не подозревать наличие у себя вируса и только при случайном обследовании его обнаружить. Иногда при длительном заболевании могут быть боли в суставах, усталость, снижение работоспособности, бессонница. Часто пациенты жалуются на тяжесть в правом подреберье.
Для диагностики хронического вирусного гепатита В достаточно одного маркера – HВsAg положительный. Его делают обычно при любом обращении в лечебное учреждение, например, при подготовке к операции, беременности, ЭКО и др. Этот показатель означает, что в печени присутствует вирус гепатита В. Он останется там навсегда.
Однако, это совсем не означает, что с вирусом ничего нельзя сделать и необратимые изменения в печени (цирроз и первичный рак печени) неизбежны. Вирусный гепатит В – это контролируемое заболевание, значит, если его держать под контролем, то можно прожить долгую жизнь с нормальной здоровой печенью. Больше того, вирусный гепатит В не всегда надо лечить противовирусными препаратами!
Если вирус обнаружен впервые, необходимо пройти полное обследование с целью получить полную информацию о вашем вирусе и о состоянии печени. Вирусологические маркеры гепатита В позволяют выяснить активность и агрессивность вируса, наличие у него мутаций устойчивости к препаратам, посчитать количество вируса в крови, определить его генотип.
Кроме того, крайне важно сделать анализ на гепатит D, который может попасть в организм вместе с вирусом В. Этот вирус отличается высокой агрессивностью и быстро вызывает в печени фиброз с исходом в цирроз. Лечение вируса гепатита D назначается сразу при его обнаружении – препаратами интерферона.
Состояние печени оценивается разными методами: УЗИ, биохимическими показателями, эластометрия (ФиброМакс, ФиброТест) – степень фиброза печени по шкале МЕТАВИР – F0 здоровая печень, F4 цирроз.
В зависимости от результатов этого обследования принимаются разные решения:
если вирус не активный и не представляет угрозы для жизни, печень в хорошем состоянии, то противовирусное лечение НЕ НАЗНАЧАЕТСЯ;
если вирус активный и печень уже поражена вирусом, то врач обязан назначить противовирусные препараты для того, чтобы остановить разрушительные процессы в печени и вернуть ее в здоровое состояние.
Во всех случаях пациент должен быть информирован о том, как контролировать вирусный гепатит в течение всей его жизни. Основными параметрами контроля является состояние печени по данным эластометрии (ФиброТеста, ФиброМакса) – то есть степень фиброза, а также активность вируса – его количество в крови. Желательно находиться под наблюдением квалифицированного гепатолога, который сможет вовремя принимать правильные решения, если ситуация изменится.
К сожалению, для вирусного гепатита В нет единого стандарта лечения и принятия решения о его назначении. Именно поэтому так важно своевременно обследоваться и консультироваться у специалиста, который умеет лечить вирусный гепатит В.
Как лечить гепатит В?
Цель лечения гепатита В
Полное удаление вируса гепатит В из организма невозможно, так как ДНК вируса встраивается в геном хозяина. В то же время, вирус не всегда опасен и не всегда требует лечения. Лечение необходимо только в том случае, если вирус активный и в печени происходят изменения, которые могут привести ее к циррозу.
Цель терапии хронического гепатита B (ХГВ) — предотвратить прогрессирование болезни в цирроз, тем самым повысить качество и продолжительность жизни.
При наличии цирроза целью лечения становится предотвращение декомпенсации цирроза и развития терминального поражения печени, первичного рака печени и смерти.
Эта цель может быть достигнута при стойком подавлении репликации HBV. Параллельное подавлению репликации вируса и уменьшение воспалительного процесса в печени снижает риск цирроза печени и рака печени.
Схемы лечения и противовирусные препараты для лечения ХГВ
Единого стандартного лечения вирусного гепатита В нет. Решения принимаются индивидуально в зависимости от вирусологических показателей и степени поражения печени.
В настоящее время существует две разные стратегии лечения: курсовое применение интерферонов-альфа, в том числе пегилированных, или аналогов нуклеозидов/нуклеотидов (АН).
Нуклеозидные аналоги: ламивудин, телбивудин, энтекавир.
Нуклеотидные аналоги: адефовир и тенофовир.
Преимуществом лечения интерферонами является то, что курс лечения ограничен и составляет 1 год. Кроме того, не развивается устойчивость вируса к интерферону, и стойкий вирусологический ответ сохраняется долго и после курса терапии. Возможно также полное удаление вируса с формированием иммунитета (образованием anti-HBsAg), хотя это происходит примерно в 20-30 % случаев.
В то же время, существенным недостатком этой тактики являются серьёзные побочные действия, а также необходимость подкожного введения, которые значительно снижают переносимость и мотивацию пациента к лечению.
Препараты интерферона противопоказаны при декомпенсированном циррозе, обусловленном HBV-инфекцией, аутоиммунным заболеванием, а также пациентам с неконтролируемой тяжелой депрессией и психозами и во время беременности.
Энтекавир и тенофовир обладают мощным противовирусным свойством и характеризуются высоким генетическим барьером к развитию резистентности. Их длительное применение не вызывает развития у вируса мутации устойчивости (резистентности) к препарату. Поэтому они могут уверенно использоваться в качестве монотерапии первой линии.
Ламивудин, телбивудин и адефовир рекомендуется применять для лечения ХГВ только при недоступности более мощных АН или же при развитии непереносимости более активных препаратов.
Ламивудин относится к недорогим препаратам, но длительная монотерапия очень часто сопровождается мутацией вируса и развитием резистентности. Адефовир менее эффективен и дороже тенофовира. Резистентность к нему возникает чаще.
Телбивудин — мощный ингибитор репликации HBV, но к нему быстро развивается резистентность у пациентов с высоким исходным уровнем ДНК HBV или с определяемым уровнем ДНК HBV через 6 мес. лечения. Частота резистентности к телбивудину относительно невелика у пациентов с низким исходным уровнем виремии (< 2 x 108 МЕ/мл у HBeAg-позитивных и < 2 x 106 МЕ/мл у HBeAg-негативных пациентов), ДНК HBV у которых не определяется через 6 мес. терапии.
Курсовая терапия пегилированным интерфероном
Пациенту должна быть предоставлена полная информация о достоинствах, нежелательных явлениях и недостатках терапии интерфероном по сравнению с АН, чтобы он мог участвовать в принятии решения о выборе препарата.
Длительное лечение аналогами нуклеозидов/нуклеотидов
Эта стратегия необходима у HBeAg-позитивных пациентов без HBe-сероконверсии и у HBeAg-негативных пациентов. Такая же стратегия рекомендуется у больных с циррозом печени, независимо от статуса по HBeAg или формирования HBe-сероконверсии во время лечения. В качестве монотерапии первой линии должны использоваться наиболее мощные препараты с оптимальным профилем резистентности, т. е. тенофовир и энтекавир.
При монотерапии тенофовиром и энтекавиром в течение 3 лет и более удается поддерживать вирусологическую ремиссию у большинства больных.
При приеме любого препарата необходимо достижение и поддержание отрицательного уровня ДНК HBV, подтвержденного методом ПЦР в реальном времени. Кроме того, необходимо контролировать состояние печени в процессе лечения (биохимические показатели, УЗИ, ФиброМакс эластометрия, ФиброТест).
Поскольку полного удаления вируса достичь не удается, рекомендуется пожизненный контроль активности вируса и состояния печени.
Вирусный гепатит Б – это инфекционное заболевание печени, широко распространенное в мире. Его опасность заключается в том, что поражение печени, вызванное вирусом, может привести к тяжелым последствиям – циррозу и раку.
В случае, когда лечение пациента с диагнозом вирусный гепатит Б было назначено не своевременно или не было назначено вовсе, развитие болезни приводит к разрушению печени, причем не заметно для пациента. Именно по этой причине необходимо своевременно обратиться к специалисту гепатологу.
Чем раньше начато лечение гепатита Б / В, тем лучше его прогноз и выше вероятность сохранить здоровую печень на долгие годы.
- усталость, повышенная утомляемость
- тяжесть в правом подреберье
- тошнота, потеря аппетита
- желтуха, желтый цвет кожи и пожелтение склеры глаза
- светлый цвет кала
- темный цвет мочи
- боли в суставах
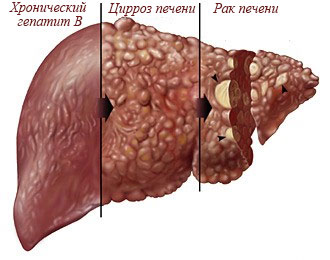
Рис.1 - Стадии развития хронического гепатита В
На сегодняшний день нет противовирусных препаратов, которые могли бы гарантировать выздоровление и полное удаление вируса из организма. Однако, терапия, дающая возможность сохранить здоровье печени надолго, существует и уже сейчас помогает миллионам пациентов с вирусом гепатита В. Подробнее о лечении гепатита Б / В и контроле над вирусом
Формы вирусного гепатита Б
Вирус гепатита В поражает печень в острой или хронической форме. При острой форме заболевания в течение 6 месяцев после заражения появляются характерные симптомы - желтизна кожи, тошнота, темная моча, повышенная утомляемость, температура, абдоминальные боли. Иногда острое течение вирусного гепатита В приводит к развитию печеночной недостаточности со смертельным исходом. У 15-20 % острый вирусный гепатит переходит в хроническую, бессимптомную форму, 30% из них — с прогрессирующим течением, из них в 70% случаев приводящим к циррозу печени в течение 2—5 лет. Гепатит В является высоким риском смерти от цирроза и гепатоцеллюлярной карциномы (рака печени).
Как можно заразиться вирусным гепатитом Б?
Гепатит В может попасть в кровь при различных медицинских манипуляциях — хирургических операциях, переливании крови, лечении зубов. Также заразиться можно при пирсинге, нанесении татуировок, при введении наркотиков внутривенно, а также половым путем. Вероятность заражения от полового партнера составляет 30%. Кроме того, возможно заражение ребенка от инфицированной матери во время беременности и родов.
Обследования на вирус гепатита Б
Поскольку хронический вирусный гепатит В протекает бессимптомно, диагностика возможна только лабораторными методами. Основной показатель наличия вируса – антитела к поверхностному антигену – HbsAg.
Для острого гепатита характерно наличие антител класса IgM к ядерному антигену – anti-HBcor IgM, маркер высокого уровня активности и заразности вируса – HBeAg. Главным показателем опасности вируса является вирусная нагрузка, которая определяется методом ПЦР с количественной оценкой концентрации вируса в мл крови – HBV-ДНК.
Для опредения в крови вируса гепатита В необходимо сдать три анализа :
- HBsAg — показывает наличие или отсутствие вируса в настоящее время;
- Анти-HBcor – показывает наличие или отсутствие вируса в прошлом;
- Анти-HBs – показывает наличие или отсутствие защитных антител.
- Стоимость комплексного обследования — 1850 руб.
Запишитесь на бесплатную консультацию для назначения обследования и возможности вакцинации. АНОНИМНО.
- с 9:00 до 17:30 по будням
- с 9:00 до 15:00 в субботу
Возможен ли бытовой путь передачи вируса гепатита В?
Контактно-бытовым путем вирус гепатита В не передается. Для окружающих пациент не опасен. Подробнее о том как передается гепатит В (Б)
Насколько заразен вирус гепатита В?
Вирус гепатита В очень заразен. Кроме того, он устойчив во внешней среде и может сохраняться в ней в течении целой недели.
Гепатитом В болеет более 2 миллионов человек в мире, а носителей вируса около 350 миллионов. 1 миллион человек ежегодно погибает от этого заболевания. Острый вирусный гепатит В отмечается у 4 миллионов человек в год.
В развитых странах болеет в основном взрослое население. Дети до 9 лет защищены прививкой, которую им делают по закону в первые часы после рождения.
Что происходит после проникновения вируса гепатита В в кровь?
Вирус гепатита В попадает в печень, внутрь печеночных клеток (гепатоцитов), и начинает там размножаться. Это приводит к гибели гепатоцитов, повреждению тканей печени и, при отсутствии своевременного лечения, циррозу.
Как протекает гепатит В?
Гепатит В может быть острым и хроническим.
Острый гепатит наступает через короткое время после заражения (до 6 месяцев) и проявляется чаще всего выраженными симптомами: температурой, ознобом, тошнотой, желтухой. Он продолжается 6-8 недель и может закончится либо выздоровлением с формированием естественного иммунитета, либо переходом гепатита в хроническую форму. При этом хроническая форма может быть как неактивной, без размножения вируса, так и активной.
В первом случае противовирусное лечение не требуется, но необходим контроль заболевания, во втором случае может возникнуть необходимость в противовирусных препаратах.
Хронический гепатит В остается пожизненным диагнозом
Течение хронического гепатита В и его исход зависят от скорости прогрессирования заболевания. Более чем в половине случаев болезнь прогрессирует очень медленно, а риск развития цирроза и рака печени довольно низок.
При активно прогрессирующем заболевании, риск развития цирроза и рака печени составляет около 20 %, однако при злоупотреблении алкоголем он намного выше.
Поскольку оценить характер течения и опасность прогрессирования гепатита Б может только специалист, во избежании необратимых последствий необходимо, как можно раньше, обращаться к гепатологу для уточнения тактики лечения и контроля над вирусным гепатитом В.
Когда появляются первые признаки гепатита B?
Инкубационный (скрытый) период составляет от 3-х недель до 6 месяцев. Симптомы появляются у 70 % заболевших, чаще всего это усталость, повышенная утомляемость, желтуха, темная моча, светлый кал, боли в суставах.
Что может сопровождать вирусный гепатит В?
Для вирусного гепатита В также характерны внепеченочные проявления – поражения сосудов, почек, боли в суставах.
Какие анализы подтверждает наличие вирусного гепатита В?
HbsAg — положительный. Лабораторные маркеры вирусного гепатита В появляются в среднем через 4 недели после заражения. Кроме того в крови значительно увеличиваются биохимические показатели АЛТ и АСТ, при желтушной форме также повышается билирубин.
Как протекает острый вирусный гепатит В?
Острый вирусный гепатит В может иметь одну из трех форм: безжелтушную форму, желтушную с признаками холестаза и затяжную форму.
При безшелтушной форме характерно легкое течение заболевания с невысокими биохимическими показателями.
Желтушная форма сопровождается желтухой, интоксикацией, выраженными биохимическими изменениями показателей крови.
При холестатической форме острого гепатита Б значительно выражены признаки функционального поражения печени.
Вирус гепатита D / Д – возможная опасная сочетанная инфекция
Вирус гепатита В может сопровождаться вирусом гепатита D (Д, дельта-вирус) , который практически всегда вызывает в печени необратимые изменения (цирроз), поэтому во всех случаях выявления гепатита Б необходимо проводить исследование на вирус гепатита D.
Какие обследования надо делать при остром вирусном гепатите В?
К лабораторным маркерам вирусного гепатита В относятся следующие: HBsAg, anti-HBcor JgM, anti-HBcor JgG, HBeAg, anti-HBe, anti-HBs и HBV-ДНК.
Разные сочетания этих маркеров дают различную информацию, в том числе о давности заболевания, активности вируса, возможном выздоровлении. Анализы на гепатит В.
Отдельно необходимо провести оценку состояния печени. Для этого выполняют биохимический анализ крови с показателями АЛТ, АСТ, ГГТП, щелочная фосфатаза, общий белок и белковые фракции, билирубин, Также проводится УЗИ органов брюшной полости.
Какими препаратами лечат острый вирусный гепатит В?
При остром вирусном гепатите В противовирусные препараты не назначаются. Лечение направлено на детоксикацию и восстановление печени.
Каких результатов лечения вирусного гепатита В можно ожидать?
Большинство пациентов с острым вирусным гепатитом В выздоравливает. Если острый вирусный гепатит переходит в хроническую форму, полное выздоровление происходит крайне редко. Современные препараты позволяют рассчитывать на полное выздоровления в 10-15% случаев.
Как правило целью лечения хронического вирусного гепатита В является снижение вирусной нагрузки и предотвращение перехода гепатита в цирроз или рак печени.
Какие препараты используются для лечения хронического вирусного гепатита В?
В настоящее время нет противовирусных препаратов для лечение гепатита В, которые могут обеспечить полное удаление вируса. Поэтому существующие в мире противовирусные препараты – аналоги нуклеозидов (нуклеотидов) применяются с целью подавить репликацию вируса, чтобы остановить или замедлить развитие цирроза, сократить риск рака печени и увеличить продолжительность и качество жизни пациентов с вирусным гепатитом В. К таким препаратам относятся энтекавир, тенофовир и другие препараты. В ряде случаев назначается альфа-интерферон.
В настоящее время идет разработка нового препарата – МЕРКЛЮДЕКС.
Выбор схемы терапии проводит квалифицированный гепатолог в зависимости от результатов полного обследования. Обследование позволяет установить не только степень поражения печени, но и активность и агрессивность вируса у конкретного человека.
Кому может быть назначена противовирусная терапия при гепатите В.
Для назначения противовирусной терапии необходимы серьезные основания. Поводом для начала терапии является высокий уровень ДНК HBV в крови, повышенная активность печеночных ферментов и умеренно или сильно выраженный фиброз (больше F2 по шкале МЕТАВИР).
Длительность терапии не может быть меньше, чем 5 лет. Иногда курс лечения назначается пожизненно, если степень поражения печени близка к циррозу, или цирроз уже сформирован. Противовирусные препараты представляют собой таблетки, которые хорошо переносятся и редко вызывают лекарственную устойчивость. Препараты обладают противофиброзным действием (обратное развитие фиброза).
Решение о назначении терапии должен принимать врач-гепатолог после соответствующего обследования. По рекомендациям Европейской ассоциации по изучению печени, все пациенты с циррозом печени должны получать лечение независимо от уровня виремии, также как и пациенты с семейным анамнезом по раку печени и циррозу.
Пациентам с уровнем виремии больше 20 000 МЕ в мл крови и АЛТ в 2 раза превышающим норму лечение назначается независимо от степени фиброза.
Пожизненный контроль при лечении
Если оснований для применения противовирусной терапии гепатита Б нет, то необходим регулярный контроль, не реже 1 раза в год. Под контролем должна быть вирусная нагрузка и состояние печени по биохимическим данным и степени фиброза
Побочные действия препаратов
Препараты интерферона имеют выраженные побочные действия (см. лечение вирусного гепатита С ). Однако, преимуществом этой схемы лечения является ограниченный по срокам курс лечения (1 год).
Аналоги нуклеозоидов выраженными побочными действиями не обладают. Крайне редко отмечается головная боль.
Заразна ли кровь пациента, прошедшего курс противовирусной терапии?
После курса терапии противовирусными препаратами вирус сохраняется в организме, поэтому кровь пациента заразна.
Как нельзя лечить вирусный гепатит В?
К сожалению, препаратов, позволяющих быстро и гарантированно получить выздоровление, не существует и в ближайшее время не ожидается. Однако, при правильном и вовремя начатом лечении сохранить здоровье печени удается в подавляющем большинстве случаев. Подробнее о лечении гепатита В
Как можно защититься от гепатита В?
Для профилактики гепатита В в мире уже больше 20 лет делают прививки. Вакцина вводится в мышцу плеча по стандартной схеме: после первой вакцинации через месяц вторая и через 5 месяцев после этого – третья.
Есть ли у вакцины побочные действия?
Крайне редко (примерно в 2 % случаев) возможно легкое повышение температуры.
Нужно ли специальное обследование для того, чтобы сделать прививку?
Прежде, чем вакцинироваться, необходимо пройти вирусологическое обследование, (анализы для прививки) подтверждающее отсутствие вируса не только в данный момент, но и в прошлом: HBsAg, anti-HBcor, anti-HBs.
Только при отрицательных значениях этих лабораторных показателей можно делать прививку.
Через полгода после вакцинации необходимо оценить результат прививки, сделав анализ anti-HBs количественный. Если титр составляет больше 100 МЕ/мл, можно считать себя защищенным от гепатита В.
Иммунитет сохраняется от 5 до 8 лет.
Кому нужно делать прививку от гепатита Б?
Всем. Учитывая легкость заражения, необходимость в вакцинации является актуальной для всех. По закону, согласно нормативным документам Минздрава, всем новорожденным делают первую прививку в течение 12 часов после рождения, вторую – в один месяц, третью – в шесть месяцев.
Детям, рожденным от инфицированной матери, прививку делают по особой схеме.
Читайте также:

