Проблемы при лечении гепатита с
Обновлено: 11.05.2024
Для цитирования: Подымова С.Д. ГЕПАТИТ С: СОВРЕМЕННЫЕ ПОДХОДЫ К ДИАГНОСТИКЕ И ЛЕЧЕНИЮ. РМЖ. 1996;1:1.
После идентификации в 70-е годы вирусов гепатитов А и В перед клиницистами и вирусологами возникла проблема выявления этиологического фактора большого количества сывороточных гепатитов, при которых отсутствовали маркеры инфицирования вышеуказанными вирусами. Длительное время диагноз устанавливался методом исключения, и этот тип гепатита был известен как гепатит ни А ни В. В 1989 г. Houghton и соавт. идентифицировали вирус гепатита С (HCV), и это название пришло на смену термину "гепатит ни А ни В с парентеральным механизмом передачи".
HCV представляет собой РНК-содержащий флавивирус диаметром 30 - 38 нм, покрытый липидной оболочкой. На 5 '-конце расположен терминальный участок, содержащий 329-341 нуклеотид, на 92% гомологичный у различных типов HCV. Этот участок, по-видимому, отвечает за трансляцию генома, и его консервативность позволяет использовать его для выявления РНК HCV с помощью полимеразной цепной реакции (ПЦР). Вирусный геном также содержит предполагаемый ядерный (core) участок р22, два участка, кодирующие гликопротеины оболочки (Е1и Е2) и четыре неструктурных (NS) участка, кодирующих ферменты, играющие роль в репликации вируса.
Выделяют по меньшей мере 6 генотипов HCV, классификация которых базируется на анализе 5'-терминальг ного участка неструктурного региона NS5. Географическое распределение генотипов неравномерно, в частности, в Северной Африке распространен генотип 4, в Северной и Центральной Европе - генотипы 2 и 3, в ЮгоВосточной Азии и на Дальнем Востоке - 1, 2 и 6[30].
Хронизация гепатита С отмечается в 50 - 80% случаев перенесенной острой инфекции, причем у 20% больных в течение 5 лет развивается цирроз, на фоне которого нередко наблюдается развитие гепатоцеялюлярной карциномы [1, 2, 25]. Учитывая достаточно широкое распространение HCV (от 0,5% в Северной Европе до 2% в Тайване), диагностика и этиотропная терапия гепатита С являются важной медикскюциальной проблемой.
Диагностика
Выявление антител к HCV. Наибольшее распространение благодаря своей надежности и чувствительности получил иммуноферментный метод (enzyme linked immunosorbent assay, ELISA). Тест-система первого поколения (ELISA-1) выявляла антитела к антигену С100. В дальнейшем были получены новые клоны РНК HCV, продуцирующие другие вирусные антигены для обнаружения соответствующих антител (см. таблицу ), и появились второе и третье поколения тест-систем ELISA. Будучи значительно более чувствительной и специфичной по сравнению с тест-системами предыдущих поколений, ELISA-3 широко используется для скрининга доноров. Важно, что ELISA-3 позволяет выявлять антитела к NS5-pemoHy, так как до 5% вирусоносителей имеют в крови только данный тип антител, вследствие чего при использовании первых поколений ELISA получают ложноотрицательные результаты.
ELISA-3 дает почти 100% гарантию выявления носителей анти-HCV при скрининге доноров и диагностике вирусных заболеваний печени. Однако в двух случаях антитела могут не быть обнаружены. Во-первых, антиHCV в крови могут появляться в срок до 6 мес после инфицирования (в среднем через 12 нед), т.е. в определенный период течения инфекции имеется так называемое "серологическое окно". Во-вторых, антитела могут не быть обнаружены у больных, получавших иммуносупрессивную терапию (например, после трансплантации органов). Кроме того, несмотря на высокую специфичность ELISA-3 (99,7%), возможны также ложноположительные результаты.
Таблица
Тест-система
Для исключения ошибки используют подтверждающие тесты, такие как рекомбинантный иммуноблоттинг (recombinant immunoblot assay, RIBA), и, реже, анализ синтетических пептидов (Inno-Lia). При использовании RIBA антигены HCV наносят раздельно на полоски нитроцеллюлозы и инкубируют с сывороткой больного. При наличии соответствующих антител происходит их визуализация. Тест-система третьего поколения (RIBA-3), широко распространенная в Европе, содержит синтетические пептиды c o re-региона и NS4 и рекомбинантные NS3 и NS5 (см. таблицу). Результаты RIBA считаются положительными при выявлении антител более чем к одному региону HCV [30].
У большей части RIBA-положительных больных вирус находится в состоянии репликации, что подтверждает обнаружение у 75 - 80% из них РНК HCV. Отсутствие РНК при наличии анти-HCV может быть обусловлено элиминацией вируса после перенесенной инфекции, уровнем виремии ниже порога чувствительности ПЦР, либо это может означать, что результат анализа на наличие антител является ложноположительным. А.Alberti и соавт. [3] отмечена связь между отсутствием РНК HCV у анти-HCV положительных больных и отсутствием воспалительных изменений в биоптатах печени, что, по-видимому, является свидетельством элиминации вируса. Однако вирусная РНК может не выявляться у больных после курса противовирусной терапии; в таких случаях не исключены ее наличие в подпороговых титрах или персистенция вируса в тканях, делающая его недоступным для детекции. Следовательно, лиц, положительных по анти-HCV, даже при отсутствии признаков виремии, необходимо рассматривать как потенциально опасных в плане заражения HCV.
Рекомбинантные белки, используемые в тест-системах ELISA и RIBA [32].
Выявление вирусной РНК. Определение наличия в сыворотке РНК HCV необходимо для:
1 ) подтверждения инфекции HCV у анти-HCV положительных пациентов или при подозрении на инфицирование при отсутствии антител к вирусу;
2) ранней диагностики острого гепатита;
3) контроля за перинатальной передачей вируса;
4) определения показаний к назначению противовирусной терапии;
5) контроля за эффективностью противовирусной терапии [30].
Наибольшее распространение получила ПЦР, заключающаяся в синтезе множества копий ДНК на основе вирусной РНК при помощи обратной транскриптазы с последующим электрофорезом в полиакриламидном геле [15]. С помощью ПЦР можно обнаруживать РНК как в сыворотке, так и в биоптатах печени. В последнее время получает распространение количественное определение РНК, для которого применяются такие методики, как анализ серийных разведений и амплификация разветвленной ДНК [ 16].
Следует отметить, что последний метод, позволяющий наиболее точно определить степень виремии, является менее чувствительным (его чувствительность составляет около 70% таковой ПЦР) и, следовательно, одновременно с ним необходимо использовать ПЦР.
Реже применяют другие методики, такие как лигазная цепная реакция и изотермическая амплификация нуклеиновых кислот.
В настоящее время основным препаратом для лечения гепатита С, как и других вирусных гепатитов, является интерферон (ИФН). По современным представлениям, выделяют два типа ИФН. К типу 1 относятся a - и b -ИФН, к типу II - g -ИФН. Подразделение на типы обусловлено различной биологической ролью: если a - и b -ИФН свойственна в основном противовирусная активность, то g -ИФН (имукин) является универсальным эндогенным иммуномодулятором. Наибольшее распространение в качестве средства этиотропной терапии вирусных гепатитов получил a -ИФН, как нативный (получаемый из культуры лейкоцитов человека), так и рекомбинантный; различий в терапевтической эффективности между этими формами не обнаружено. Реже встречаются работы, посвященные применению b -ИФН.
Высокая частота хронизации гепатита С побуждает к поиску средств воздействия на вирус в острой фазе инфекции. При использовании ИФН для лечения остро го гепатита С получают неоднозначные результаты. М.
Omata и соавт. [23] лечили b -ИФН 14 больных в течение 30 дней, общая доза составила 52 ME. Ремиссия наступила у II, остальным был назначен повторный курс ИФН. Через 3 года наблюдения активность АЛТ оставалась повышенной у 1 больного (в контрольной группе нормализовалась только у 3). Больные, у которых отмечалась биохимическая ремиссия, стали также негативными по РНК HCV [24]. Еще в трех исследованиях с использованием рекомбинантных a -2a (роферон) и ( a -2b (интрон А) ИФН показано снижение частоты хронизации гепатита, но в двух из них результаты были статистически недостоверными [3, 7, 31]. Окончательный вывод, снижает ли терапия ИФН частоту хронизации острого гепатита С, можно будет сделать на основе результатов длительного наблюдения.
Основным показанием к назначению ИФН при хроническом гепатите С является обнаружение в сыворотке вирусной РНК. Дополнительными критериями являются повышение уровня сывороточных трансаминаз не менее чем в 1,5 раза и гистологическая картина хронического гепатита. К основным факторам, определяющим хороший ответ на ИФН, относятся: молодой возраст, гетеросексуальная ориентация, отсутствие ВИЧинфекции, парентеральное заражение вирусом, небольг шая продолжительность заболевания, отсутствие гистологических признаков перехода в цирроз, отсутствие биохимического синдрома холестаза, слабовыраженный аутоиммунный компонент. Наряду с вышеперечисленными прогностическими факторами в последние годы большое значение придается низким исходным титрам РНК HCV и генотипу вируса [9, 15, 27, 29].
Разные генотипы HCV обладают различной чувствительностью к ИФН. Наиболее чувствительным считается генотип 3 (до 70% положительных результатов лечения ИФН). Существенно меньшей чувствительностью обладает генотип 2. Генотип 1 (распространенный в Северной Европе), особенно подтип 1Ь, характеризуется тяжелым течением и резистентносью к противовирусной терапии; данный подтип распространен на Дальнем Востоке и в Японии [ 18, 30]. Однако, по другим данным, генотип вируса не является значимым фактором, определяющим ответ на ИФН. Решающее значение имеют титры РНК HCV, выявленные перед началом лечение [II, 14]. При низких титрах РНК быстро наступает стойкая серологическая и биохимическая ремиссия. Некоторые авторы отмечают корреляцию между генотипом вируса и степенью виремии. Так, М. Omata и соавт. [23] у инфицированных вирусом с генотипом 2 наблюдали более высокие титры РНК HCV, чем у инфицированных вирусом с генотипами 3 и 4, что коррелировало с худшим ответом на лечение ИФН. Y. Kobayashi и соавт. [15] указывают на высокую частоту инфицирования вирусами с различными генотипами, что снижает значение идентификации генотипа HCV и выводит на первое место количественное определение виремии [ 15 ].
Средние дозы ИФН составляют 3-5 ME 3 раза в неделю на протяжении 6 мес., хотя некоторые авторы указывают, что более низкие дозы (от I ME) также могут быть эффективны [12, 21]. Основным критерием успешности лечения служит исчезновение из сыворотки вирусной РНК, что также коррелирует с нормализацией или снижением уровня трансаминаз и улучшением результатов гистологического исследования биоптатов печени [8,21,25,26,33]. Положительный эффект отмечается в среднем у 50% больных, из них у половины в течение полугода после окончания лечения происходит рецидив [4, 6, 11, 30]. Имеются данные, что 12-месячный курс с последовательным снижением дозы имеет ряд преимуществ [19]. P. Jouet и соавт. [ 13] провели исследование с участием 108 больных хроническим гепатитом С, у части из которых имелись признаки цирроза. Больным 1-й группы ИФН назначали по обычной схеме (3 ME 3 раза в неделю в течение 6 мес), 2-й - в течение 12 мес с постепенным снижением дозы (по 3 ME 3 раза в неделю в течение 6 мес, по 2 ME следующие 3 мес и по 1 ME еще 3 мес). Через 6 мес после окончания лечения ремиссия сохранялась в среднем у 13,5% больных 1-й группы и у 28,6% больных 2-й группы; при отсутствии цирроза частота стойкой ремиссии была значительно выше .
В качестве возможного механизма резистентности к ИФН рассматриваются изменения структуры гипервариабельного региона (ГВР), находящегося на 5'конце гена E2/NSI РНК HCV, который является мишенью иммунологического надзора и играет важную роль в персистенции вируса. Отсутствие эффекта от назначения ИФН может быть обусловлено "ускользанием" от иммунного ответа хозяина структурно измененного ГВР. Эволюция ГВР может происходить непосредственно в процессе лечения ИФН [10] .
Большое количество больных с хроническими вирусными поражениями печени, резистентных к терапии ИФН, а также высокая частота рецидивов диктуют необходимость поиска комбинаций ИФН с другими противовирусными средствами. Не останавливаясь подробно на каждой из них, следует отметить, что во многих исследованиях выявлена их невысокая эффективность. R. Mtiller [20] на основании анализа контролируемых клинических испытаний делает вывод об отсутствии преимуществ комбинированной противовирусной терапии перед монотерапией ИФН. В то же время в последние годы снова стали появляться данные о выраженном положительном эффекте комбинаций ИФН с рибавирином при повторном курсе у ИФН-резистентных больных. S .
Brillanti и соавт. [5] проводили дифференцированное лечение двух групп больных, не давших положительного ответа на 6-месячный курс a -ИФН. 1-й группе было продолжено введение ИФН в прежней дозировке (3 ME 3 раза в неделю) в течение следующих 6 мес, больным 2-й группы к ИФН добавили 800 мг рибавирина per os. В обеих группах отмечено значительное снижение уровня трансаминаз, однако через 9 мес после окончания лечения биохимическая ремиссия сохранялась только у пациентов 2-й группы. Исчезновение РНК HCV наблюдалось у 40% больных 2-й группы и лишь у 1 больного 1-й группы. Положительный ответ на комбинированную терапию коррелировал с уменьшением воспалительно-некротических изменений в печени [5]. Обнадеживающие результаты получены G. Mazella и соавт. [17] при комбинированном лечении ИФН и урсодезоксихолевой кислотой (УДХК) (600 мг УДХК ежедневно и ИФН в обычной дозировке) больных хроническим гепатитом С, резистентных к ИФН. Ремиссия наблюдалась у 13 из 29 больных, в том числе у 7 на протяжении 6-месячного периода наблюдения. В контрольной группе, продолжавшей монотерапию ИФН, только у 2 отмечена нестойкая ремиссия. Положительный эффект обусловлен, по-видимому, иммуномодулирующим влиянием УДХК, которая, таким образом, потенциировала действие ИФН .
Кроме комбинации с противовирусными препаратами, некоторые авторы предлагают проведение короткого курса терапии глюкокортикостероидами с последующим назначением ИФН [20]. Теоретически эффективность такого лечения может быть обусловлена усилением репликации вируса на фоне иммуносупрессии и последующим ее подавлением ИФН .

К врачу-инфекционисту обратилась 45-летняя женщина с положительным результатом анализа на антитела к гепатиту С.
Жалобы
Никаких симптомов болезни и других проблем со здоровьем пациентка не испытывала. Боли в желудочно-кишечном тракте не было.
Анамнез
При подготовке к операции пациентка прошла необходимые обследования, среди которых был обязательный анализ на вирусные гепатиты. Анализ на гепатит оказался С положительным.
За последние полгода женщина не посещала стоматологов и других операций не делала. Длительное время ходила к мастеру маникюра в один и тот же салон красоты.
Обследование
- общее состояние удовлетворительное;
- печень в пределах нормы (гладкая и эластичная, выступает на 1 см из-под края рёберной дуги);
- кожа и слизистые оболочки чистые, нормального цвета;
- язык влажный с небольшим беловатым налётом на корне;
- дыхание в лёгких в норме, без хрипов;
- живот мягкий, безболезненный, не вздут;
- стул и мочеиспускание в норме.
Так как ранее у пациентки выявили антитела к гепатиту С, а ВИЧ и гепатит В не подтвердились, женщину направили на дообследование:
- биохимический анализ крови — все показатели в норме;
- общий анализ крови — уровень тромбоцитов снижен до 150х10⁹/л;
- развёрнутый анализ крови на гепатит В — антитела не выявлены;
- анализ на антитела к гепатиту С — положительный;
- анализ крови методом ПЦР (полимеразной цепной реакции) — обнаружена РНК гепатита С, генотип 3а;
- УЗИ органов брюшной полости — печень увеличена, структура неоднородная (диффузная), найдены признаки хронического холецистита;
- фибросканирование — обнаружен фиброз (рубцевание) печени 1-й степени по шкале METAVIR.
Диагноз
Хронический вирусный гепатит С минимальной биохимической активности, генотип 3а и фиброз печени 1-й степени.
Лечение
Чтобы наблюдать за течением болезни, пациентку поставили на диспансерный учёт. Ей рекомендовали регулярно посещать инфекциониста и пройти противовирусную терапию.
Женщина исправно принимала противовирусные препараты и вовремя сдавала контрольные анализы. Уже через две недели анализ ПЦР на РНК дал отрицательный результат.
По прошествии полного курса лечения все показатели биохимического и общего клинического анализа крови также были в пределах нормы.
Пациентка оставалась под наблюдением врача в течение трёх месяцев после лечения. По истечению этого срока она сдала контрольные анализы ещё раз — все показатели были в норме.
С учётом проведённой терапии, низкого уровня фиброза печени и устойчивого положительного вирусологического ответа на лечение женщину сняли с учёта.
Заключение
Поэтому пациенты должны быть аккуратны при выборе стоматологической клиники, салона красоты или других заведений, связанных с инвазивными процедурами, например нанесением татуировок, проколами для пирсинга и др.
У нас в стране нет обязательного обследования на вирусные гепатиты, но его желательно периодически проходить всем жителям, особенно тем, кто входит в группу риска.
Актуальность. Проблема этиотропного лечения хронического вирусного гепатита С (ХВГС), несмотря на большое количество исследований, по-прежнему остается актуальной и до конца не решена.
Эффективность лечения по данным разных исследователей не превышает 46-51% у больных ХВГС с 1-м генотипом и 70-80% у больных ХВГС с не 1-м генотипом 3. Так же ограничивают их применение высокая стоимость препаратов и большое количество побочных эффектов от проводимой терапии. Целью проведения этиотропной терапии ХВГС является подавление вирусной репликации, эрадикация вируса из организма и, соответственно, прекращение инфекционного процесса. Даже отсутствие вирусологического эффекта при специфической терапии приводит к замедлению прогрессирования заболевания, стабилизации или регрессии патологических изменений в печени, предупреждению формирования цирроза печени и первичной гепатоцеллюлярной карциномы, а также повышению качества жизни.
Оценку эффективности специфического лечения осуществляют на основании нескольких критериев: вирусологического (исчезновение рибонуклеиновой кислоты (РНК) вируса из сыворотки крови), биохимического (стойкая нормализация уровня ферментов печени) и морфологического (уменьшение индекса гистологической активности и стадии фиброза).
В целом около 5% больных [1,5] вынуждены отказаться от специфического противовирусного лечения в начале курса из-за многочисленных побочных эффектов, а 20% не доводят его до конца.
Побочные эффекты интерферона (ИФН) и рибавирина иногда вынуждают временно или постоянно снижать их дозы или отменять препараты. Некоторыми исследователями [5] показано, что для достижения устойчивого вирусологического ответа (УВО) необходимо получение не менее 2/3 дозы ИФН и рибавирина, поэтому эффективность комбинированной противовирусной терапии (КПВТ) напрямую зависит от наличия побочных эффектов и возможностью их коррекции.
Некоторые побочные эффекты не требуют медикаментозной терапии, так как носят легкий или среднетяжелый характер, другие - тяжелый и угрожающий жизни характер, при этом необходима специфическая коррекция. Как правило, после окончания терапии большинство побочных эффектов полностью исчезает без применения симптоматической терапии.
Проблема побочных эффектов на фоне проводимой КПВТ остается до конца не изученной, несмотря на проведенные многочисленные исследования.
Основными побочными явлениями, описанными в литературе, являются: гематологические изменения; гриппоподобный, диспепсический, неврологический и астеновегетативный синдромы; аутоиммунные поражения; снижение массы тела; выпадение волос; огрубение кожи; аллергические реакции различной степени выраженности; местная реакция в области введения интерферонов.
Таким образом, проблема побочного действия комбинированного противовирусного лечения ХВГС, его влияние на достижение УВО является актуальной в настоящее время.
Целью данного исследования было изучение побочных явлений КПВТ в зависимости от схемы лечения, сопутствующих заболеваний, влияние на достижение УВО. Для достижения поставленной цели были сформулированы следующие задачи: оценить переносимость КПВТ пациентами с различными схемами терапии, выявить частоту побочных эффектов КПВТ и взаимосвязь их с достижением УВО.
Материалы и методы. В исследование были включены 50 пациентов с установленным диагнозом ХВГС, которые получали КПВТ. Диагноз был подтвержден согласно общепринятым методикам.
Из исследования исключались пациенты с микст-инфекцией (вирусный гепатит В, ВИЧ-инфекция) а так же наличием сопутствующей патологии печени (первичный билиарный цирроз, болезнь Вильсона-Коновалова, синдром Бадда-Киари, гемохроматоз, аутоиммунный гепатит, дефицит альфа-1 антитрипсина) и предшествующего специфического противовирусного лечения по поводу ХВГС, больные с наличием любого из общепринятых противопоказаний для проведения КПВТ.
Продолжительность лечения составила 48 недель для пациентов, инфицированных генотипом 1в вирусного гепатита С или при наличии у больного цирроза печени; 24 недели для пациентов, инфицированных генотипом 2 и 3а. Согласно рекомендациям по ведению пациентов с ХВГС, КПВП включала комбинацию стандартного (Интрон или Альтевир 3 млн МЕ 3 раза в неделю) или пегилированного (ПегИнтрон 120 мкг или Пегасис 180 мкг в неделю) ИФН и рибавирина в дозировке 800-1200 мг в зависимости от массы тела.
Устойчивый вирусологический ответ (УВО) определялся как отсутствие РНК вируса в сыворотке крови спустя 24 недели после окончания КПВТ. Больные находились под наблюдение в течение терапии на базе Воронежской областной клинической инфекционной больницы и поликлиник Воронежа. Все пациенты были разделены на 2 группы: получающие в составе КПВТ стандартные ИФН – 52,0% (26 человек) или пегилированные ИФН – 48,0% (24 человек). Пациенты были сопоставимы по возрасту и полу: средний возраст составил 40,3 ±10,4, количество мужчин - 57,1%, женщин 42,9%. Распределение по группам показано в табл. 1.
Таблица 1. Характеристика пациентов в исследуемых группах

При анализе полученных результатов использовались описательные методы математической статистики с применением пакета программ Microsoft Excel 2010. Достоверность различий оценивалась методами непараметрической статистики, статистически значимыми считались различия результатов при р≤0,05.
Результаты. При анализе эпидемиологических данных выяснено, что в большинстве случаев (34% случаев) ХВГС выявлен случайно, без клинических проявлений. Одинаковое количество пациентов (по 8 человек - 19,2%) обследовались по поводу диспепсических жалоб и длительного повышения печеночных ферментов. У 30 % пациентов в анамнезе отмечались неоднократные операции или переливание крови; употребление внутривенных наркотиков - у 16% человек. Длительность заболевания до начала противовирусной терапии составила в 1 группе 3±1,4 лет, во 2 группе 5±3,4лет. Степень фиброза по Metavir в среднем составил в 1 группе 1±0,85 балла, во второй группе выше - 1,9±1,5 баллов.
Соотношение генотипов вируса гепатита С, определенных до начала КПВТ, показано в табл. 2.
Таблица 2. Соотношение генотипов вирусного гепатита С

Среди всех пациентов УВО определялся в большинстве случаев - 80,0%, при применении обоих видов терапии, но при этом достоверных различий между группами по этому признаку не выявлено. Эффективность терапии в 1 группе составила 75,1%, во 2 группе - 78,2%. Отсутствие вирусологического ответа в половине случаев связано с отменой препаратов из-за развития выраженных побочных эффектов (прогрессирование неврологической симптоматики с развитием энцефалопатии в 1 группе, длительная некупируемая лихорадка во 2 группе).
Частота побочных эффектов в общей выборке была достаточно высокой - 72,3% среди всех пациентов, при этом в 1 и 2 группе нежелательные явления встречались с одинаковой частотой (69,1% и 73% соответственно).
На протяжении всей терапии у большинства пациентов встречался астеновегетативный синдром в виде выраженной слабости, усталости, нарушения сна, при этом значительно чаще эти проявления отмечали пациенты 2 группы - принимающие пегилированные ИФН (30,7%), что в 2,1 раза чаще, чем во 1 группе (66,6%). Снижение настроения, появление раздражительности, неконтролируемой агрессии при опросе отмечали 23,0% пациентов 1 группы и 25,0% пациентов 2 группы. Данные жалобы чаще встречались на 24±2 неделе терапии. Описанная в литературе депрессия, индуцированная КПВТ, среди данной выборки не встречалась. Для выявления депрессии у всех пациентов применялся опросник Цунга в начале и при завершении КПВТ.
Гриппоподобный синдром, проявляющийся лихорадкой до 38±0,85?С, миалгией, артралгией, выявлен достоверно чаще в у пациентов 1 группы (38,4%), чем у 2 группы (30,1%). Длительность лихорадки составляла в среднем 14±2 недель, первый подъем температуры всегда сопровождал начало КПВТ. Лихорадка купировалась применением препаратов НПВС в стандартных дозировках.
Жалобы со стороны желудочно-кишечного тракта в виде снижения аппетита, тошноты, периодической диареи, боли, вздутия в животе отмечались у 34,6% пациентов 1 группы, что в 2,08 раза чаще, чем во 2 группе (16,6%) .Желтуха на фоне КПВТ встречалась у 2 человек в каждой группе (по 8,3% и 7,6% соответственно).
Снижение веса в среднем на 10,5±5,1 кг, регистрируемое к концу КПВТ, встречалась в 2,3 раза чаще у пациентов 1 группы (19,2%) чем у пациентов среди пациентов 2 группы (8,3%).
Выпадение волос, жалобы на сухость кожи, зуд кожи регистрировались редко: в 1 группе у 2 человек (7,6%среди группы), во 2 группе чаще - у 3 человек(12,5%).
Обострение имеющихся сопутствующих соматических заболеваний встречались в обеих группах приблизительно с одинаковой частотой (30,1% и 27,6% соответственно). Чаще всего встречались обострения хронического панкреатита, язвенной болезни желудка, сахарного диабета.
Частота манифестации впервые выявленных соматических заболеваний на фоне проведения КПВТ имеет прямую корреляционную связь с используемыми препаратами, то есть значительно чаще выявляется при применении ИФН короткого действия, чем пролонгированных форм. При этом в 1 группе на фоне КПВТ манифестировали псориаз (7,6%), аутоиммунный тиреодит (15,3%). А во 2 группе выявлялись гипотиреоз и сахарный диабет (по 4,1% пациентов).
Гематологические осложнения встречались в обеих группах. Анемия, регистрируемая в виде снижения гемоглобина ниже 110г/л, встречалась чаще всего в середине терапии (24±3недели КПВТ). Во второй группе анемия выявлена достоверно чаще – в 2,4раза чаще (38,4%случаев), чем в 1 группе (16% случаев). Эритропоэтин для коррекции анемии применялся в 4 случаях (8%), у остальных коррекции анемии не требовалось.
Среди пациентов обеих групп при наличии анемии УВО встречается в 49,7% случаев, при отсутствии анемии достоверно реже (в 1,35 раз) - у 36,6% пациентов. Таким образом, наличие анемии, в сочетании с другими факторами можно считать предиктором эффективности КПВТ.
Напротив, частота тромбоцитопении на фоне КПВТ коррелировала с отсутствием УВО. Пациенты со снижением уровня тромбоцитов в 1,8 раз реже достигали УВО. Среди всех пациентов тромбоцитопения встречалась только у 8,0% пациентов, что реже, чем по литературным данным. В обеих группах частота данного побочного действия была одинаковой.
Выводы
1. Эффективность терапии с применением препаратов пегилированных или стандартных интерферонов оказалась сходной.
2. Гематологические нежелательные эффекты выявлены достоверно чаще при использовании пегилированных ИФН в составе противовирусной терапии.
3. Гриппоподобный на фоне КПВТ встречались достоверно чаще у пациентов, получающих стандартные ИФН.
5. Выявлена зависимость между достижением устойчивого вирусологического ответа и величиной снижения уровня гемоглобина.
Список использованных источников:
1. Беляева Н.М., Турьянов М.Х., Рабинович Э.З. Комбинированная терапия гепатита С рибавирином и альфа-интерфероном: Пособие для врачей. - М.: РМАПО. – 2002.
2. Громова Н.И. и Богомолов Б.П. Клиническая эффективность этиотропной терапии хронического вирусного гепатита С// Клин. мед. - 2003.-№1. - С.48.
3. Ивашкин В.Т. Комбинированное лечение хронического гепатита В// Российский журнал гастроэнтерологии, гепатологии, колопроктологии. 1998. №5. С. 57-60.
4. Ferenci P., Fried M., Shiffman M. et al. Predicting sustained virological responses in chronic hepatitis C patients treated with peginterferon alfa-2a// J. Hepatol. – 2005. – Vol. 43. – P. 425–433.
5. Fried M.W. Side effects of therapy of hepatitis C and their management. Hepatology. 2002. - P.237-244
6. Князькина О.В., Каган Ю.Д., Скачков М.В. Микробиоценоз кишечника у больных хроническим вирусным гепатитом С и его лечение// Врач-аспирант, №3.4(52), 2012. – С.579-586.
7. Пирогова И.Ю., Пышкин С.А. Неинвазивная диагностика стадии фиброза у пациентов с хроническими гепатитами В и С// Врач-аспирант, №2(45), 2011. – С. 21-27.
8. Попов С.С., Попов С.Ф. Динамика биохимических показателей гепато-билиарной системы рабочих основных цехов металлургического завода, инфицированных вирусами гемоконтактных гепатитов В и С// Врач-аспирант, №6(55), 2012. – С.55-61.
9. Рихсиева Г.М. Особенности клинико-иммунологических показателей детей, больных острыми вирусными гепатитами А и В, родившихся от матерей, злоупотребляющих алкоголем// Врач-аспирант, №4.4(47), 2011. – С. 675-681.
10. Рюмин А.М., Корочкина О.В., Соболевская О.Л. Закономерности естественного течения хронического гепатита В// Врач-аспирант, №4.1(53), 2012. – С. 214-223.
Подписано в печать: 01.02.2013
Справка: что такое гепатит С
Вирусные гепатиты — это инфекционные заболевания, поражающие печень. Существуют разные вирусные гепатиты (их обозначают латинскими буквами). Симптомы заболеваний могут быть схожими (а чаще всего их вообще нет), но их возбудители по-разному распространяются и влияют на организм человека. Например, гепатит А — это кратковременная инфекция, а В и С могут протекать десятилетиями, незаметно повреждая печень. С распространением гепатитов А и В успешно борются с помощью прививок, а вот против гепатита С вакцины не существует.
Заражение вирусом гепатита С обычно происходит через контакт с кровью инфицированного человека:
- через шприц у лиц, употребляющих инъекционные наркотики (по статистике это наиболее распространенный способ заражения);
- при незащищенном сексе (риск выше при более травматичных формах, например, анальном сексе);
- через нестерильные медицинские инструменты (например, при экстренных вмешательствах в ограниченных условиях, при стоматологических процедурах и др.);
- через предметы личного пользования (например, бритву);
- при нарушении условий переливания крови (встречается редко, так как компоненты и доноры крови проходят тщательный отбор и обследование);
- от инфицированной матери новорожденному.
Основной способ диагностики гепатита С — анализ крови. Поэтому сложно назвать реальное количество людей, которые являются носителями этого вируса. В 2021 году некоторые эксперты говорили о том, что в России гепатитом С могут быть заражены около 5,7 млн человек.
— Как гепатит С лечили раньше?
— Сначала для терапии использовали рибавирин — неспецифический противовирусный препарат, у которого есть немало побочных эффектов. Потом его стали использовать в комбинации с препаратами интерферона, задача которого — усилить иммунный противовирусный ответ в организме. Но и у интерферона есть побочные явления и нередко — противопоказания к применению. Существуют заболевания, при которых применение интерферона невозможно или дает очень высокие риски осложнений. Зачастую приходилось выбирать, кому из больных проводить терапию по этой схеме, а кому отказывать. Эффективность тоже была заведомо невысокой, можно даже сказать, мы играли в лотерею. Переносимость интерферона, сопутствующие заболевания, риск нежелательных явлений, изменение показателей крови, стадия цирроза печени и в целом состояние печени на момент лечения — от всего этого зависело, можно ли было назначать лечение. Плюс мы выявляли у пациентов определенные генетические показатели, при которых его применение заведомо могло быть малоэффективным.
— Таких пациентов совсем не лечили?
— Гепатопротекторы бесполезны при гепатите?
— Итак, старая схема давала высокие риски, побочные эффекты и низкую эффективность. Что удалось изменить в новых рекомендациях?
— Принципиальный момент, который, наверное, будет самым важным для всех нас — и для пациентов, и для врачей, — возможность назначать терапию на любой стадии хронического гепатита С. Не запущенные стадии, как было раньше, когда у пациента уже возникали фиброз и цирроз печени. Сейчас у нас единственное показание к лечению, как и во всем мире, что мне очень приятно, — это сам факт выявления вируса гепатита С в крови. Поэтому врачам теперь не нужно решать, кому назначать противовирусную терапию, а кому — нет.
— Терапию теперь можно проводить сразу после того, как вирус обнаружили в крови?
— По современным российским рекомендациям это нужно сделать не позднее трех месяцев после обнаружения вируса в крови — возможно начать терапию сразу, иногда понаблюдать 6–12 недель. Это можно делать, потому что в определенных случаях организм побеждает вирус сам. Процент таких больных действительно есть, хотя он намного ниже, например, чем в случаях с гепатитом В (он реже становится хроническим).
— Мы убрали это слово, сейчас такого подхода нет. Конечно, приоритет все равно дается пациентам с циррозом печени или с другими рисками (например, с раком печени и вирусным гепатитом или поражением других органов). Пациенты после после пересадки печени получают лечение незамедлительно, так как инфицирование нового органа наступает неизбежно.
— Схема лечения тоже изменилась?
— Это еще один принципиальный момент, над которым мы целенаправленно работали. Из рекомендаций исчезли препараты интерферона. Это влечет за собой целый ряд позитивных изменений. Как я уже говорил, интерферон многими пациентами переносится тяжело, возникают побочные эффекты, и результаты невысоки, особенно при циррозе печени.
Теперь мы перешли полностью на таблеточные схемы, их эффективность приближается к 100%. Это позволяет бюджетным медицинским учреждениям больше не тратить деньги на закупку интерферона, а закупать только таблеточные формы лекарств и использовать безинтерфероновые высокоэффективные схемы. При этом нужно сказать, что большая часть тех препаратов, которые есть в мире и, в частности, в западных странах, присутствуют и в России.
— Новые схемы лечения эффективнее прежних?
— Они перекрывают все существующие в России типы вирусов гепатита С. Это так называемая пангенотипная схема: когда одна таблетка, одна комбинация препаратов, может вылечить все типы вирусов. К примеру, в России встречаются в основном три типа вируса гепатита С (1а, 1b, 3), и их раньше по разным причинам не всегда удавалось лечить эффективно, особенно на стадии цирроза. Сейчас эта проблема уже не имеет значения. Во всем мире принята следующая концепция упрощенного подхода к лечению: выявляют вирус, но не определяют ни его количество, ни его разновидность, для того чтобы выбрать конкретный препарат. Вместо этого назначают лекарства, которые одинаково эффективны при разных вариантах инфекции.
У Юлии два высших образования, она работала врачом, на психоактивные вещества зарабатывала сама. О том, что у нее гепатит, узнала в женской консультации, когда забеременела. Ребенок был долгожданный, и она не согласилась на предложение врача сделать аборт. Тогда, в 2002 году, информации было немного, ей помогло медицинское образование — начала читать книги о гепатите и о передаче гепатита при родах.
по теме

Лечение
АBC — азбука гепатита
Дмитрий Карсаков несколько раз был в тюрьме, тоже употреблял наркотики. О том, что у него гепатит, узнал, когда попал в больницу на операцию. По его словам, тогда он отреагировал очень спокойно, даже не придал этому значения, ведь у него уже был ВИЧ.
В поликлинике он ругался с врачами, просил убрать этот красный треугольник, ведь на картах не должно быть никаких пометок о диагнозах пациента. Свое право он отстоял, треугольник убрали, но врачи все равно ему сказали, что болезнь не лечится.

Юлия шевченко, фото из личного архива.
Азбука гепатита
Всего в мире насчитывается семь разновидностей гепатитов — A, B, C, D, E, F и G. Вообще гепатит — это общее название воспалительных заболеваний печени, которые могут быть вызваны разными причинами: отравлением (токсический гепатит), атакой клеток печени собственной иммунной системой (аутоиммунный гепатит). Но чаще всего, говоря об этой болезни, имеют в виду поражение клеток печени особыми вирусами.
В то же время разные вирусные гепатиты — совершенно разные болезни, каждый из них вызывается своим возбудителем, могут различаться пути передачи, способы лечения и профилактики. Общее у них только одно — мишенью во всех случаях является печень.

Дмитрий Карсаков, фото из личного архива.
После освобождения ее пригласили на тренинг, где были социальщики, работающие с ВИЧ-позитивными людьми и наркопотребителями. Она этим загорелась и сейчас помимо основной работы старшим специалистом в кредитной компании волонтерит в организации, помогающей наркозависимым. Считает, что ее опыт и история могут уберечь других от ошибок, которые когда-то совершила она сама.
Дмитрий узнал про свой статус в 1997 году. Он тоже употреблял наркотики и неоднократно попадал за это в колонии. Через несколько лет у него обнаружили и ВИЧ.
по теме
Лечение
Гепатит и стоматология: стоит ли бояться врачей?
Когда его везли по этапу, посадили в камеру к другим заключенным с такими же диагнозами. По его словам, сотрудники ФСИН к ним не заходили и старались как можно меньше контактировать, даже закрывали глаза на какие-то нарушения.
Когда мужчина вышел в 2011 году, ему предложили лечение интерферонами. Он согласился. Через три месяца лечения начались жесткие побочные эффекты: диарея, температура и так далее.
Помогло ему, что лечение заканчивалось как раз к концу весны. Друзья выводили Дмитрия на природу, помогали, поддерживали, это помогло ему вернуться в нормальное состояние. Уже осенью он решил, что станет помогать другим.
После того, как узнала в женской консультации во время беременности, что гепатит есть и у нее, самое сложное было — принять и научиться с этим жить. По ее словам, самая страшная мысль — что болезнь может передаться ребенку.
Оставалось лишь ждать окончания беременности и только потом начинать лечение. Анна отмечает, что сама она человек брезгливый, и если бы тогда узнала, что в ее окружении есть человек с гепатитом, не стала бы к нему подходить.
Анна считает, что ей повезло, она не чувствовала негатива от близких или врачей. Хотя до сих пор к ней регулярно обращаются девушки, которые узнают о гепатите во время беременности и сталкиваются с неадекватной реакцией на диагноз.
Лечение и стигма
по теме

Лечение
Преодолевая темноту: борьба с гепатитом С в Украине
Эксперт объясняет, что многие носители гепатита в России — это люди, употребляющие инъекционные наркотики. Но зависимость не делает их менее нуждающимися в помощи и лечении. Он убежден, что снизить уровень инфицирования среди наркопотребителей можно лишь одним действенным способом — расширять программы по работе с людьми из групп риска. Однако, по его словам, с каждым годом в стране таких программ становится все меньше.
Существует несколько способов лечения гепатита С: интерфероновыми схемами, современными безинтерфероновыми схемами и дженериками. Первый вариант самый древний, дешевый, но в то же время с очень тяжелыми побочными эффектами.
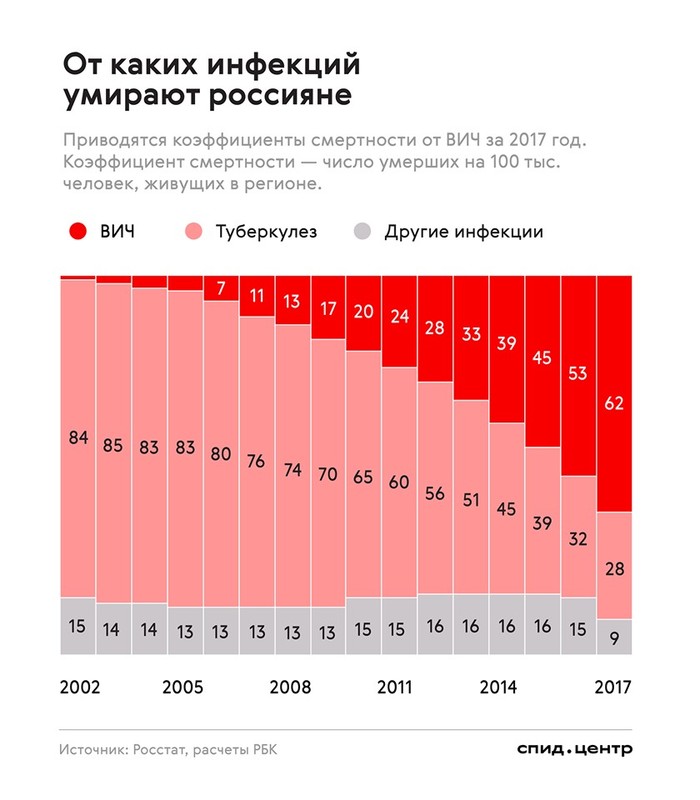
Весь мир сейчас лечит гепатит С с помощью новых схем, в состав которых больше не входит интерферон, а базовый препарат — софосбувир (Совальди) недоступен для большинства россиян в силу своей дороговизны. По подсчетам Международной коалиции по готовности к лечению, стоимость курса лечения гепатита С такой схемой (софосбувир + даклатасвир) составляет 582 000 рублей за 12 недель.
Из-за дороговизны в 2017 году государство обеспечило этими лекарствами лишь 1,5 % нуждающихся россиян. Несмотря на то, что софосбувир попал в список ЖНВЛП (жизненно необходимых и важнейших лекарственных препаратов), это лекарство так и не вошло в рекомендации Минздрава для лечения вирусного гепатита С. Более того, ведомство не предусмотрело возможности закупок софосбувира на 2019 год.
В феврале 2019 года общественники в очередной раз просили правительство закупить софосбувир, но его все еще нет в закупках Министерства здравоохранения.
Читайте также:

