Профилактическая вакцина от вич
Обновлено: 16.04.2024
Егор Воронин — нью-йоркский вирусолог, специалист в области вакцинопрофилактики. Более двадцати лет он занимался исследованиями ВИЧ, его эволюцией и репликацией. С 2018 по 2020 год он возглавлял биотехнологическую компанию Worcester HIV Vaccine, занимающуюся разработкой вакцины от ВИЧ. В своем блоге shvarz Егор публикует массу интересных фактов о вакцинах, ВИЧ, о вирусах в целом, а в последние полтора года и о новом коронавирусе: он умеет рассказывать простым языком о сложном.
— Наверное, тот факт, что сейчас все следят за вакцинами, позволит объяснить это проще.
— Это единственная проблема?
— Нет. Вторая проблема: как мы все уже знаем в отношении коронавируса — созданные против него вакцины хорошо предотвращают тяжелое течение болезни и смерть, но гораздо хуже защищают от заражения. Для COVID-19, как все же быстротечной болезни, это нормально: даже если вирус попадет в привитый организм, он не вызовет тяжелую болезнь, организм силами иммунной системы быстро его поборет, и человек скоро выздоровеет, вирус исчезнет.
С ВИЧ же совершенно другая ситуация. Он приспособлен к тому, чтобы жить в организме очень долго и ускользать от иммунной системы годами. Если мы не предотвратили его попадание в организм, то без терапии он будет в нем реплицироваться и в конце концов вызовет СПИД. Будучи привитыми от коронавируса, вы можете все равно им заразиться, но лишь чуть-чуть поболеете или даже не заметите, что вирус был, организм его вычистит, — а с ВИЧ это не работает. На ранних этапах разработки вакцин пытались измерять их эффективность именно по способности предотвращать не заражение ВИЧ, а последующее развитие СПИДа, но сейчас уже ясно, что если ВИЧ попал в организм, то без терапии СПИД неизбежно разовьется. Значит, в отношении ВИЧ нам нужна вакцина, которая будет полностью предотвращать само попадание вируса в организм, а это гораздо более высокая планка.
— Но с точки зрения обывателя все кажется просто: есть вирус ВИЧ, он выделен и хорошо известен. Так возьмите его, убейте, и убитый, обезвреженный вирус введите человеку — пусть организм вырабатывает иммунный ответ. Ведь так делались все классические вакцины. На каком этапе оказалось, что с ВИЧ это не работает?
— Над вакциной от ВИЧ работают уже не первый десяток лет. При этом были сделаны какие-то побочные открытия, которые можно применять в других областях? Например, в нынешней борьбе с коронавирусом?
— Попытки создать вакцины от ВИЧ начались сразу же, как только вирус был впервые выделен. Пытались сделать вакцины на основе убитого вируса, на основе рекомбинантных белков, продолжают активно работать над векторными вакцинами. А когда появился COVID-19, практически все мои коллеги, кто занимался вакцинами от ВИЧ, перекинулись в область коронавируса. Я смотрю на научные статьи о коронавирусе — там все знакомые имена.
Я уже упоминал, что технология стабилизации спайкового белка была разработана для ВИЧ, это был один из главных прорывов в вакцинологии за последние десять лет, и она нашла отличное применение в вакцинах от COVID-19.
Известный вирусолог Барни Грэм, который занимался именно стабилизацией вирусного белка у ВИЧ и у респираторно-синцитиального вируса, сыграл важную роль в разработке одной из самых популярных в мире вакцин от COVID-19 компании Moderna.
Мишель Нуссенцвайг, который выделил нейтрализующие антитела к коронавирусу, разработал технологию выделения этих антител в ходе многолетних исследований антител к ВИЧ и вирусу иммунодефицита обезьян. Памела Бьоркман, ведущий специалист Caltech по структуре вирусных белков, раньше изучала в том числе и ВИЧ.
— Это известные имена, но применяются ли отработанные на ВИЧ методики?
— Сами методы тестирования на нейтрализующие антитела были разработаны для ВИЧ, а теперь применяются для COVID-19. В области тестирования вакцин существует огромная сеть клинических центров и лабораторий и в США, и в Африке, и по миру — она была создана для ВИЧ-инфекции, после начала пандемии ее просто взяли и перепрофилировали под коронавирус, а заведуют ею те же самые ученые.
С другой стороны, технологии, нашедшие применение в вакцинах от COVID-19, сейчас интересуют и исследователей ВИЧ: технология мРНК вакцин разрабатывалась и для ВИЧ, но сейчас работы в этой области существенно активизировались.
— Кто-нибудь из российских ученых занимается разработками вакцины от ВИЧ?
— В России разработки вакцин от ВИЧ ведутся, но их немного. Есть три исследовательские группы: в Москве, Петербурге и в Новосибирске. У них есть определенные наработки, но пока они не прошли дальше первой фазы испытаний.
Вопрос в большей мере этический. Раз уж существуют эффективные методы предотвращения ВИЧ-инфекции, то нельзя не делать их доступными участникам клинических испытаний. Но если мы предоставляем их всем участникам клинических испытаний (и плацебо-группе, и группе, получающей вакцину), то количество новых инфекций будет чрезвычайно мало в обеих группах, и эффективность вакцины будет невозможно измерить. Или придется делать испытания еще обширнее и еще длинней, что еще больше повысит их стоимость.
Перспективы разработки вакцины от ВИЧ тают с каждым днем именно потому, что сложно их тестировать, не подвергая людей риску заразиться в ситуации, когда есть готовые способы избежать этого риска. Но нельзя сказать, что ученые полностью потеряли надежду. Уже ведутся активные обсуждения новых подходов к проведению клинических испытаний ВИЧ-вакцин в будущем.
Какие вакцины уже есть

Однако трудности не останавливают исследователей, и работа над созданием вакцины идет на протяжении многих лет.
Вторая группа препаратов, на которую делаются большие ставки, — использование нейтрализующий антител широкого спектра действия (bNAbs). bNAbs вырабатываются b-клетками. В отличие от обычных антител, bNAbs реагируют с консервативными эпитопами вируса, обеспечивая защитный иммунитет против подавляющего большинства штаммов ВИЧ. Эксперименты на макаках показали эффективность — у них bNAbs предотвращали заражение.
В 2016–2018 годах в двух исследованиях AMP (Antibody Mediated Prevention) было рандомизированно более 4600 участников для приема VRCO1 и плацебо. Исследование не показало снижение передачи ВИЧ в целом, но его эффективность составила 75% в группе участников, подвергшихся воздействию вируса, чувствительного к VRCO1. Результаты в целом подтверждают принцип, что bNAbs могут быть эффективными и приемлемыми в странах с низким уровнем дохода.
Новые направления разработки вакцин
Российские разработки вакцины от ВИЧ
Согласно презентации Анны Вадимовны, исследования специфической активности на лабораторных животных показали, что они эффективно стимулируют необходимый иммунный ответ.
Стоит ли ждать эффективную вакцину?
По мнению Покровской, в ожидании действенной вакцины не стоит забывать про уже известные методы профилактики ВИЧ.
Четвертая Международная научно-практическая конференция PROHIV проходит 20–21 сентября 2021 года. В ней участвуют медики, ученые, активисты и ВИЧ-положительные люди. Эксперты обсуждают инновационные решения по профилактике, диагностике, лечению ВИЧ и не только. Присоединиться к конференции можно по ссылке (необходимо зарегистрироваться).
Перед тем как говорить о вакцине против ВИЧ, стоит начать с более общего вопроса: что мы понимаем под прививками и вакцинами с научной точки зрения?
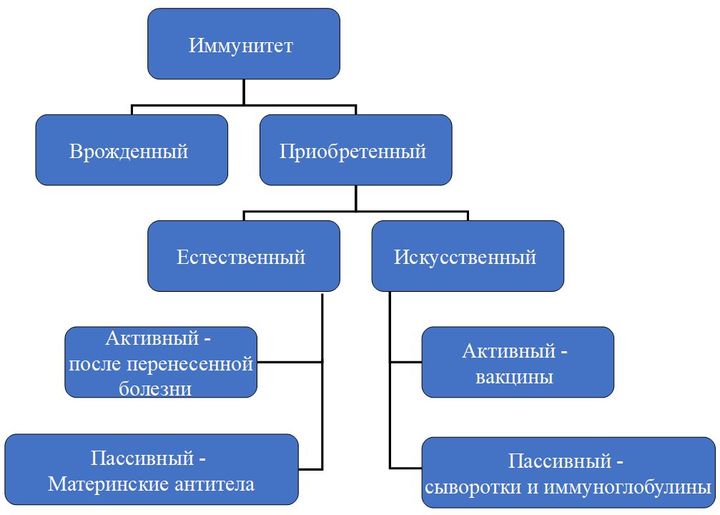
По механизму возникновения иммунитет делится на два вида: врожденный и приобретенный. Первый есть у каждого человека с рождения, он выработан эволюционно. Благодаря нему человек не болеет многими болезнями, которыми, например, страдают животные.
Второй возникает в течение жизни и у каждого может отличаться в зависимости от того, с какими возбудителями человеку довелось встретиться.
по теме
Лечение
Как устроен иммунитет: Объясняем по пунктам
Приобретенный иммунитет может быть активным (он возникает вследствие реакции организма на перенесенную болезнь, присутствие возбудителя в организме), а может быть пассивным, когда антитела, например, передаются от матери ребенку во время беременности.
Именно по этим антителам, как правило, и ставится диагноз, если мы пользуемся экспресс-тестами. В случае с ВИЧ существует и пассивный иммунитет. Но при передаче вируса от матери ребенку, к сожалению, он не обладает достаточным защитным эффектом.
Еще одно направление — это искусственный иммунитет. Он тоже бывает активным и пассивным. Пассивный — это иммуноглобулины, выработанные либо у лабораторных животных, либо у других иммунизированных лиц, и сыворотки. Активный же достигается собственно путем вакцинации.
Вакцины бывают профилактические (защитные) и лечебные. Они различаются по типу воздействия на организм и по своим результатам.
Пассивный иммунитет возникает быстрее, сразу после того, как в организм ввели чужие антитела. Однако он бывает совсем недолговременным. Активный иммунитет держится долго, чаще — пожизненно, но и возникает не сразу.
Иммунный ответ: как это все работает?
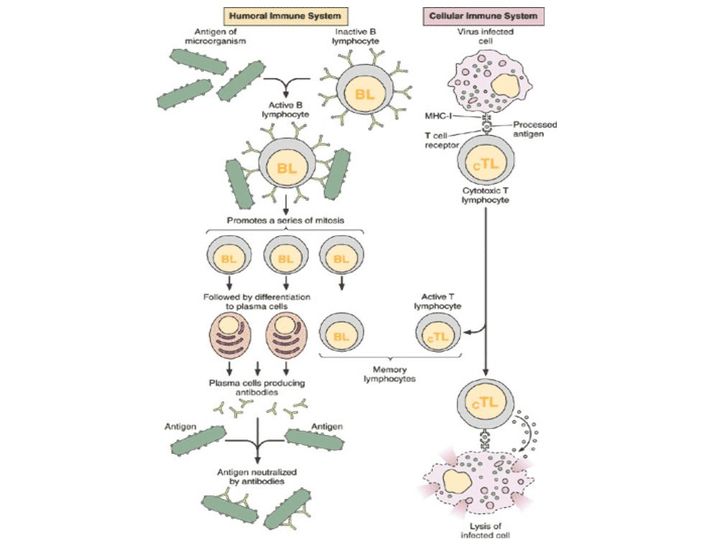
Ученые обычно говорят о гуморальном и клеточном иммунитете. Принцип работы гуморального заключается в следующем: в нашем организме есть специальные клетки — лимфоциты. Они постоянно циркулируют в крови и проверяют все, что попадается им на пути, по принципу свой/чужой.
по теме

Лечение
Гид по вакцинам. Когда и какую прививку сделать? А главное: надо ли вообще прививаться? (Спойлер: конечно, надо)
Например, антитела к ВИЧ-инфекции появляются где-то через месяц после заражения, соответственно, все это время вирус может циркулировать в организме. Почему они неэффективны? Во-первых, потому что появляются слишком поздно.
Во-вторых, потому что вирус, с которым мы имеем дело, очень изменчив. Если даже В-клетки обнаружили его антиген, выработали к нему антитела, способные нейтрализовать заразу, то за время, которое ушло на все это, сам вирус успевает мутировать и оказаться неуязвимым для выработанного организмом оружия.
Когда мы говорим о клеточном иммунитете, речь идет об уничтожении тех вирусов, которые преодолели гуморальный барьер и успели забраться в саму клетку.
Клетки CD4 частично регулируют весь процесс и выполняют функцию клеток памяти. Их принято называть хелперами. CD8 — собственно занимаются уничтожением, за это их зовут киллерами.
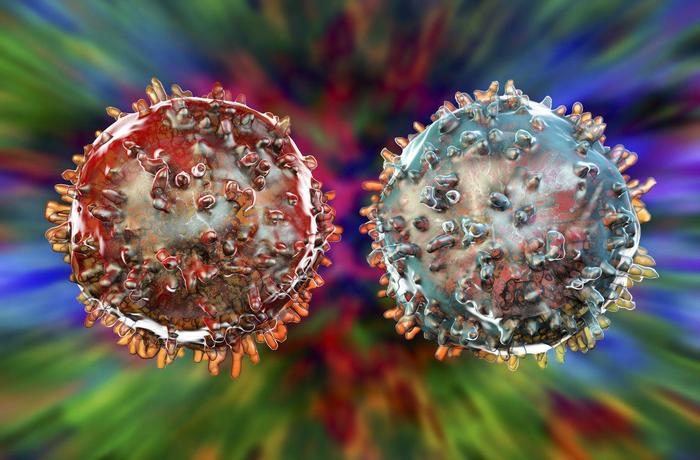
ВИЧ — единственный вирус, который поражает не просто клетки организма, а собственно клетки иммунной системы. Той самой, которая с вирусом должна, по идее, бороться.
Именно поэтому против ВИЧ-инфекции иммунитет не может сработать так, как это было бы с любым другим вирусом.
Какие возникают трудности при создании вакцины против ВИЧ?
На данный момент в рамках более ста испытаний уже протестировано более сорока видов вакцин с участием тысяч добровольцев, и есть целая система, в которой регистрируются все исследования по вакцинации от ВИЧ.
Последнее время в разного рода СМИ регулярно появляется информация, что той или иной компанией разрабатывается новая вакцина против ВИЧ. Однако обнадеживающих результатов не так уж и много. Почему?

Ученые разрабатывают и испытывают терапевтические вакцины против ВИЧ, чтобы замедлить развитие ВИЧ и его переход в СПИД, а лечение людей этими вакцинами в идеале могло бы поддерживать неопределяемый уровень вирусной нагрузки (Н=Н) без регулярной антиретровирусной терапии (АРТ). (АРТ является рекомендуемой стратегией лечения ВИЧ-инфекции, она представляет собой прием определенной комбинации различных лекарств от ВИЧ для предотвращения размножения ВИЧ. В настоящее время человек с ВИЧ должен постоянно принимать препараты АРТ, чтобы поддерживать вирусную нагрузку на неопределяемом уровне.)
Терапевтическая вакцина против ВИЧ также снижает вероятность передачи ВИЧ другим людям.
Существуют ли терапевтические вакцины против ВИЧ, одобренные FDA?
К настоящему моменту FDA (Управление по санитарному надзору за качеством пищевых продуктов и медикаментов, агентство Министерства здравоохранения США) не одобрило к использованию ни одну терапевтическую вакцину против ВИЧ, но исследования продолжаются. Получить терапевтическую вакцину против ВИЧ можно, только став участником клинических испытаний.
Чем терапевтическая вакцина против ВИЧ отличается от профилактической?
Профилактическая вакцина против ВИЧ вводится ВИЧ-отрицательным людям с целью предотвращения ВИЧ-инфицирования. Вакцина учит иммунную систему человека распознавать ВИЧ и эффективно бороться с ним в случае, если вирус попадет в организм человека.
Терапевтическая вакцина против ВИЧ вводится людям, которые уже инфицированы ВИЧ. Цель терапевтической вакцины против ВИЧ — усилить иммунный ответ человека на ВИЧ, который уже находится в организме человека.
Где можно узнать о клинических испытаниях терапевтических вакцин против ВИЧ?
Список клинических испытаний терапевтических вакцин против ВИЧ приведен в базе данных ClinicalInfo в разделе кратких сведений об исследованиях ClinicalTrials.gov. Чтобы просмотреть дополнительную информацию об исследовании, нужно щелкнуть на названии исследования.
В настоящее время одной из наиболее перспективных терапевтических вакцин является вакцина с новым иммуногеном HTI, обнадеживающие результаты исследования которой были представлены на Конференции по ретровирусам и оппортунистическим инфекциям в марте 2021 года.
В ходе испытаний ряда терапевтических вакцин было обнаружено, что они помогают в течение длительного времени после прекращения антиретвовирусной терапии удерживать вирусную нагрузку на очень низком уровне.
Об окончательных результатах говорить еще очень рано, но вакцины с HTI, очевидно, смогут в перспективе войти в комплексную схему лечения по достижению функционального излечения (длительной супрессии ВИЧ без необходимости в использовании антиретровирусной терапии).
По словам доктора Беатрисы Моте из испанского Научно-исследовательского института СПИДа ИрсиКайша, у некоторых участников испытаний, которые пришли в исследование с неопределяемой вирусной нагрузкой и прервали лечение после получения ряда вакцин, произведенных с помощью различных технологий, вирусная нагрузка удерживалась на очень низком уровне в течение полугода.
В своем заявлении президент Международного сообщества борьбы со СПИД — профессором Адееба Камарулзаман отметил, что:
По сути, терапевтические вакцины призваны заставить иммунную систему обычного человека с ВИЧ работать подобно иммунной системе элитного контролера.
Исследователи создали целый ряд вакцин с HTI с использованием различных технологий. В одной из них ДНК ВИЧ доставляется напрямую, в другой используется модифицированный вирусный вектор осповакцины Анкара (MVA), а в третьей используется вектор аденовируса шимпанзе (ChAdOx1), аналогичный тому, который использовался в вакцине AstraZeneca от COVID-19.
Методика и итоги исследования
Участники I/IIa фазы исследования начали прием антиретровирусной терапии в течение полугода после ВИЧ-инфицирования, имели неопределяемый уровень вирусной нагрузки на протяжении не менее одного года и удерживали количество клеток CD4 выше 400 в течение не менее шести последних месяцев. Среди 45 участников была 1 женщина, и большинству было около 35 лет.
Вначале 30 участников были случайным образом распределены для проведения вакцинации, а 15 получили соответствующие инъекции плацебо. Группа вакцинированных получила три дозы иммуногена HTI, доставленные посредством ДНК-вектора (в самом начале, через 4 и через 8 недель), а затем две дозы векторной вакцины MVA (через 12 и 20 недель). Большинство участников позже получили векторную вакцину с аденовирусом шимпанзе (две дозы с интервалом 12 недель) и последнюю бустерную вакцину MVA.
После вакцинации участникам предлагали прервать лечение на 24 недели под строгим медицинским контролем. У них еженедельно брали кровь для измерения вирусной нагрузки, и они немедленно возобновляли прием антиретровирусных препаратов, если количество копий РНК ВИЧ поднималось выше заранее установленного порога (выше 100 000 в любой момент или держалось выше 10 000 в течение более чем 8 недель), а также если количество клеток CD4 падало ниже 350.
Почти все участники вакцинированной группы показали сильный и выраженный Т-клеточный ответ на пептиды ВИЧ, доставляемые вакцинами HTI, и сила этих реакций определила длительность периода отказа от лечения. У всех участников в обеих группах отмечалось снижение количества ДНК ВИЧ, формы генетического материала ВИЧ в долгоживущем вирусном резервуаре, из-за которого ВИЧ так трудно искоренить.
У всех из 41 участника, решивших прервать лечение, возвратная виремия возникала, как и ожидалось, в течение 2–3 недель после отказа от терапии. Но в группе вакцинированных новое значение уровня вирусной нагрузки было ниже.
Среди 32 участников, у которых отсутствовал благоприятный генетический профиль (аллели HLA класса I), обуславливающий естественный контроль над ВИЧ, 8 получателей вакцины (40%) и 1 получатель плацебо (8%) смогли отказаться от антиретровирусных препаратов на 22 недели. Из-за пандемии COVID-19 два человека решили возобновить лечение, несмотря на низкую вирусную нагрузку.
У 5 получателей вакцины и 1 получателя плацебо вирусная нагрузка сохранялась на уровне ниже 2000, несмотря на прерывание лечения. Но даже такая низкая вирусная нагрузка может привести к неблагоприятным последствиям для здоровья из-за хронической стимуляции иммунной системы и воспаления. Более того, люди с обнаруживаемой вирусной нагрузкой могут передавать ВИЧ половым путем; по этой причине решил возобновить лечение один участник исследования.
Вакцинация по описанной выше схеме хорошо переносилась участниками, побочные эффекты проявлялись лишь в слабой или умеренной форме. В группе вакцинированных участники чаще жаловались на мышечные боли, чем в группе плацебо.
По мнению д-ра Моте, вакцины с HTI могут стать основой для комбинированной схемы лечения с целью достижения функционального излечения от ВИЧ. Она добавила, что антиретровирусную терапию крайне важно начинать как можно раньше, пока вирусный резервуар все еще мал, или же придется комбинировать вакцину с другими агентами, которые помогают уменьшить резервуар.
В рамках исследования AELIX-003 (NCT04364035), которое сейчас проводится в Испании, действие вакцин с HTI изучается в сочетании с весатолимодом от Gilead Sciences — агонистом TLR7, который помогает сокращать вирусные резервуары (GS-9620).
Подчеркивая, что об окончательных результатах говорить еще рано, многие эксперты согласились с тем, что результаты этих исследований можно назвать многообещающими.
Если вы нашли ошибку, пожалуйста, выделите фрагмент текста и нажмите Ctrl+Enter.

Некоторые из наиболее важных достижений медицины прошлого столетия были связаны с разработкой вакцин для защиты от вирусов, таких как:
Но один вирус все еще сопротивляется тем, кто хочет создать вакцину для защиты от него: ВИЧ.
Впервые ВИЧ был выявлен в 1984 году. Министерство здравоохранения и социальных служб США объявило тогда, что они надеются получить готовую вакцину в течение двух лет.
Однако, несмотря на многочисленные испытания возможных вакцин, по-настоящему эффективная вакцина все еще недоступна. Почему так трудно победить эту болезнь? И на каком этапе мы находимся в этом процессе?
Препятствия на пути к вакцинации против ВИЧ
Очень трудно разработать вакцину против ВИЧ, потому что он отличается от других типов вирусов. ВИЧ не соответствует типичным подходам к вакцинации в нескольких аспектах:
Иммунная система, которая борется с болезнью, не реагирует на вирус ВИЧ. Она вырабатывает антитела к ВИЧ, но они только замедляют развитие болезни. Они не останавливают ее.
Вакцины, как правило, предназначены для того, чтобы имитировать иммунную реакцию выздоровевших людей
Однако почти ни один человек не выздоровел после заражения ВИЧ. В результате нет иммунной реакции, которую могли бы имитировать вакцины.
Вакцины защищают от болезней, а не от инфекций
ВИЧ — это инфекция, пока она не прогрессирует до стадии 3, или СПИДа. При большинстве инфекций вакцины дают организму больше времени, чтобы самостоятельно избавиться от инфекции, прежде чем начнется заболевание.
Однако ВИЧ имеет длительный бессимптомный период, прежде чем он переходит в СПИД. В течение этого периода вирус скрывается в ДНК человека с вирусом. Организм не может найти и уничтожить все скрытые копии вируса, чтобы вылечиться. Таким образом, вакцина, позволяющая выиграть больше времени, не будет работать с ВИЧ.
Убитые или ослабленные вирусы ВИЧ не могут быть использованы в вакцине
Большинство вакцин производится с убитыми или ослабленными вирусами. Однако убитый ВИЧ плохо работает, чтобы вызвать иммунный ответ в организме. Любая живая форма вируса слишком опасна для использования.
Вакцины обычно эффективны против редко встречающихся заболеваний
К ним относятся дифтерия и гепатит В. Но люди с известными факторами риска ВИЧ-инфекции могут ежедневно подвергаться воздействию ВИЧ-инфекции. Это означает, что есть больше шансов получить инфекцию, которую вакцина не может предотвратить.
Большинство вакцин защищают от вирусов, попадающих в организм через дыхательную или желудочно-кишечную системы
Больше вирусов проникает в организм этими двумя путями, поэтому у нас больше опыта борьбы с ними. Но ВИЧ проникает в организм чаще всего через половые органы или кровь. У нас меньше опыта защиты от вирусов, которые проникают в организм таким образом.
Большинство вакцин тщательно тестируются на животных
Это помогает гарантировать, что они, вероятно, будут безопасными и эффективными, прежде чем их испытают на людях. Однако подходящей модели испытания для ВИЧ-инфекции на животных не существует. Ни одно исследование, проведенное на животных, не показало, как люди отреагируют на тестируемую вакцину.
Вирус ВИЧ быстро мутирует
Вакцина нацелена на вирус определенной формы. Если вирус изменится, вакцина может больше не действовать на него. ВИЧ быстро мутирует, поэтому трудно создать вакцину, которая будет работать против него.
Профилактические и терапевтические вакцины
Несмотря на эти препятствия, исследователи продолжают попытки найти вакцину. Существует два основных типа вакцин: профилактические и терапевтические. Исследователи ищут и те, и другие вакцины против ВИЧ-инфекции.
Большинство вакцин являются профилактическими, что означает, что они предотвращают заболевание человека. Терапевтические вакцины, с другой стороны, используются для усиления иммунного ответа организма на борьбу с болезнью, которая у человека уже есть. Терапевтические вакцины также считаются методами лечения.
Терапевтические вакцины исследуются для нескольких состояний, таких как:
Теоретически вакцина против ВИЧ должна иметь две цели. Во-первых, ее должно быть можно вводить людям, у которых нет ВИЧ, чтобы предотвратить заражение вирусом. Это сделало бы ее профилактической вакциной.
Но ВИЧ также является хорошим кандидатом для терапевтической вакцины. Исследователи надеются, что терапевтическая вакцина против ВИЧ может снизить вирусную нагрузку человека.
Типы экспериментальных вакцин
Исследователи пробуют множество различных подходов к разработке вакцины против ВИЧ. В настоящее время изучаются возможные вакцины как для профилактического, так и для терапевтического применения.
В настоящее время исследователи работают со следующими типами вакцин:
- Пептидные вакцины используют небольшие белки от ВИЧ, чтобы вызвать иммунный ответ.
- Рекомбинантные субъединицы белковых вакцин используют более крупные участки белков от ВИЧ.
- Живые векторные вакцины используют другие вирусы, кроме ВИЧ, для переноса генов ВИЧ в организм, чтобы вызвать иммунный ответ. В вакцине против оспы используется этот метод.
- Вакцины с вирусоподобными частицами используют неинфекционный аналог ВИЧ, который содержит некоторые, но не все белки ВИЧ.
- Вакцины на основе ДНК используют ДНК ВИЧ для запуска иммунного ответа.
Препятствия на пути клинических испытаний
Исследование вакцины против ВИЧ, известное как исследование HVTN 505, закончилось в октябре 2017 года. В нем изучали профилактический подход, в котором использовалась живая векторная вакцина.
Ослабленный вирус простуды под названием Ad5 был использован для запуска иммунной системы, чтобы распознать (и, таким образом, быть в состоянии бороться) белки ВИЧ. Для участия в исследовании было набрано более 2500 человек.
Исследование было прекращено, когда исследователи обнаружили, что вакцина не предотвращает передачу ВИЧ и не снижает вирусную нагрузку. Фактически, 41 человек, принимавший вакцину, заразился ВИЧ, в то время как только 30 человек, принимавших плацебо, заразились им.
Нет никаких доказательств того, что вакцина сделала людей более склонными к заражению ВИЧ. Однако с предыдущей неудачей в 2007 году Ad5 в исследовании под названием STEP исследователи начали беспокоиться о том, что все, что заставляет иммунные клетки атаковать ВИЧ, может увеличить риск заражения вирусом.
Надежда из Таиланда и Южной Африки
Эта комбинированная вакцина оказалась безопасной и в какой-то степени эффективной. Эта комбинация снизила скорость передачи инфекции на 31 процент по сравнению с плацебо-инъекцией.
31-процентного сокращения недостаточно для широкого применения этой вакцинной комбинации. Однако этот успех позволяет исследователям изучить, почему вообще был какой-либо профилактический эффект.
В ходе последующего исследования надежный источник под названием HVTN 100 протестировал модифицированную версию режима RV144 в Южной Африке. В HVTN 100 используется другой усилитель, чтобы усилить вакцину. Участники исследования также получили еще одну дозу вакцины по сравнению с людьми из RV144.
В группе из примерно 200 участников исследование HVTN 100 показало, что вакцина улучшает иммунный ответ людей, связанный с риском ВИЧ-инфекции. Основываясь на этих многообещающих результатах, в настоящее время проводится более крупное последующее исследование под названием HVTN 702. Исследование HVTN 702 проверит, действительно ли вакцина предотвращает передачу ВИЧ.
Исследование HVTN 702 также пройдет в Южной Африке и привлечет около 5400 человек. Исследование HVTN 702 является многообещающим, потому что это первое крупное испытание вакцины против ВИЧ за последние семь лет. Многие люди надеются, что это приведет к нашей первой вакцине против ВИЧ. Результаты ожидаются в 2021 году.
Другие текущие испытания
Нынешнее испытание вакцины, начавшееся в 2015 году, связано с международной инициативой по вакцинации против СПИДа (IAVI). В этом испытании профилактической вакцины участвуют люди из:
В ходе испытания была принята стратегия живой векторной вакцины, использующая вирус Сендай для переноса генов ВИЧ. Также используется комбинированная стратегию со второй вакциной для усиления иммунного ответа организма. Сбор данных из этого исследования завершен. Результаты ожидаются в 2022 году.
Еще одним важным подходом, изучаемым в настоящее время, является использование векторной иммунопрофилактики.
При таком подходе вирус, не являющийся ВИЧ, отправляется в организм, чтобы проникнуть в клетки и произвести так называемые широко нейтрализующие антитела. Это означает, что иммунный ответ будет нацелен на все штаммы ВИЧ. Большинство других вакцин нацелены только на один штамм.
В настоящее время IAVI проводит подобное исследование под названием IAVI A003 в Великобритании. Исследование завершилось в 2018 году, и результаты ожидаются в ближайшее время.
Будущее вакцин против ВИЧ
Согласно отчету за 2018 год, в 2017 году на исследования вакцины против ВИЧ было потрачено 845 миллионов долларов. И на сегодняшний день было протестировано более 40 потенциальных вакцин.
Мы медленно продвигаемся к созданию действенной вакцины. Но с каждой неудачей мы узнаем все больше сведений, которые могут быть использованы в новых попытках.
Перевод: Наталья Исаева
Если вы нашли ошибку, пожалуйста, выделите фрагмент текста и нажмите Ctrl+Enter.
Читайте также:

