Профилактика пневмоцистной пневмонии у вич инфицированных у детей
Обновлено: 15.04.2024
СПИД у детей – заболевание, которое начинается с инфицирования ребенка вирусом иммунодефицита человека (ВИЧ), который поражает клетки множества систем и органов (прежде всего, иммунной и нервной), сопровождается проявлением множества инфекций.
В Украине и России типичен эпидемический тип распространения рассматриваемой болезни. Эпидемические темы на сегодняшний день замедлились, они детально описаны в UNAIDS/WHO, 2008. Множество пациентов с ВИЧ и СПИДом не догадываются о своем диагнозе. Или же родители скрывают статус больного ребенка. Потому все врачи должны знать симптомы поражения организма ребенка ВИЧ, чтобы распознать их, даже если пациент обратился за помощью касательно других жалоб.
ВИЧ/СПИД передается детям такими путями:
- на протяжении периода кормления грудью
- парентеральными путями (инъекции и манипуляции с применением мединструментов; переливание крови, ее компонентов и препаратов; при трансплантации органов)
- половым путем (подростки)
Если беременная мать не применяла профилактические меры, то частота передачи ВИЧ ребенку составит 15-30/100.
Классификация стадий СПИД у детей согласно ВОЗ:
- начальная (острая);
- персистирующая генерализованная лимфаденопатия;
- СПИД-ассоциированный комплекс;
- развёрнутый СПИД.
Что провоцирует / Причины СПИДа у детей:
СПИД провоцирует вирус иммунодефицита человека (ВИЧ), который относят к семейству ретровирусов. Выделяют два его типа: ВИЧ-1 и ВИЧ-2. Вирусная частица представляет собой ядро в окружении оболочки. В ядре содержатся РНК и ферменты: интеграза, обратная транскриптаза, протеаза.
Патогенез (что происходит?) во время СПИДа у детей:
Согласно исследователю Монтанье, ВИЧ, который вызывает СПИД, угнетает рост и размножение Т-клеток (среди них и Т-хелперы), что приводит к нехватке их в организме. В начале болезни происходит активирование гуморального иммунитета – повышается секреция IgA,G,M. Но истощение и этого звена иммунной защиты происходит в короткие сроки. Ребенок теперь не защищен перед влиянием окружающей среды. Среди гипотех возникновения СПИДа лидируют две. Первая говорит о том, что носители вируса СПИДа – африканские зеленые мартышки, и вирус трансформировался, став патогенным для человека. Согласно второй гипотезе, в Т-клетках человека вирус находился уже давно, но был в дремлющем состоянии, а потом активировался по каким-то причинам.
Симптомы СПИДа у детей:
У детей СПИД может быть врожденным или приобретенным.
Виды врожденного СПИДа у детей (по симптомам):
- дизморфический синдром (его находят у ребенка, мать которого была инфицирована; проявляется гидроцефалией, микроцефалией, кальфицикацией мягких тканей мозга, симптомами энцефалопатии)
- СПИД-ассоциированный комплекс (проявления, которые встречаются при этом комплексе в сочетаниях или по-одиночке: длительные лихорадочные состояния с выраженным потоотделением, генерализованная лимфоаденопатия, длительные диареи неопределяемого генеза, гепатоспленомегалия, экзантемы непонятных причин)
- собственно СПИД (проявляется инфекциями и онкологическими проявлениями)
Приобретенные ВИЧ инфекции у детей
При приобренном ВИЧ/СПИД у детей происходят тяжелые изменения в центральной нервной системе:
- прогрессирующая энцефалопатия с развитием судорожного синдрома
- задержки психического развития
- оппортунистические инфекции
Онкология при приобретенном СПИДе у детей проявляется:
-
(это доброкачественная эпидермальная опухоль, которая базируется на коже или слизистой пищеварительного тракта)
- выпячиванием кожных покровов
- гирляндообразными пятнами синюшного оттенка
- плотными тестоватыми массами на поверхности слизистой оболочки
- гиперемированными или синюшными полипами очень больших размеров
- симптомами кишечной непроходимости у ребенка
СПИД поражает в организме ребенка:
- периферические лимфоузлы (увеличиваются)
- печень и селезенку
- синдром истощения
- нарушение темпов физического развития
- кожу (вызывает ксероз, пятнисто-папуллезные высыпания, васкулиты)
- слюнные железы (вызывая паротит)
- дыхательную систему (лимфоидная интерстициальная пневмония)
- центральную нервную систему (ВИЧ-энцефалопатия)
- сердечно-сосудистую систему (вызывает сердечную недостаточность и кардиопатию)
- почки (появляется почечная недостаточность, нефротический синдром, протеинурия,)
- пищеварительный тракт (у детей возникает синдром мальабсорбции)
- гематологическую систему (появляется тромбоцитопения, лейкопения, анемии)
Синдром истощения при СПИДе называется вастинг-синдромом. Он помогает в диагностике рассматриваемого заболевания. Масса тела ребенка снижается на 10% и больше. Диарея длится дольше месяца, становясь хронической. Наблюдается документированная лихорадка постоянная или интермиттирующая – также месяц и более. При вастинг-синдроме у детей прогнозируют летальный исход.
Паротит при СПИДе у детей наблюдают у 2–14 % маленьких пациентов. Это поражение слюнных желез, при котором припухают околоушные железы. Могут быть также дополнительные симптомы: боль во рту и ксеростомия. Пальпация определяет эластичность желез, болевых ощущений нет, кожа над железами неизменна. При надавливании на железу из протока выделяется прозрачная слюна.
В других случаях у ребенка возникает бактериальный паротит, в большинстве случаев он односторонний, после выздоровления рецидивирует. При нем есть местная болезненность, повышенная температура и гиперемия кожи. При пальпации железа плотная, возникает боль, при ее массировании из протока выделяется гной.
Атопический дерматит при СПИДе у детей может проявляться эритематозной сыпью на коже щек. Но этот симптом может говорить не только о ВИЧ/СПИД у детей.
Ксероз — патологическая сухость кожи. Является частым осложнением иммунодефицита, в том числе СПИДа. Фиксируют множественные чешуйки на коже лица и всего тела. Ребенок может жаловаться на зуд и сухость кожи.
Лимфоидная интерстициальная пневмония прогрессирует медленно, поражает дыхательные пути. Происходит диффузная инфильтрация межальвеолярных перегородок и лимфатических сосудов зрелыми, преимущественно СD8 Т-лимфоцитами, плазматическими клетками и гистиоцитами. Болезнь развивается в том числе под влиянием вируса Эпштейна — Барр. Симптомы появляются, как правило, у детей от 2 до 3 лет. Ребенок кашляет, у него есть одышка (быстро прогрессирует), быстро утомляется.
При лимфоидной интерстициальной пневмонии возникают также:
- гепатоспленомегалия
- генерализованная лимфаденопатия
- увеличение околоушных слюнных желез
На последней стадии развития этого проявления СПИД у детей появляются признаки хронической гипоксии. Рентген обнаруживает двусторонние сетчато-узловые или очаговые альвеолярные инфильтраты, наиболее выраженные в нижних долях.
Тромбоцитопения бывает более чем у трети детей и подростков, зараженных ВИЧ. Количество тромбоцитов в некоторых случаях может спонтанно становиться нормальным, но в большинстве случаев без лечения тромбоцитопения сохраняется и прогрессирует. Легкая форма тромбоцитопении чаще всего проходит без симптомов. Но геморрагический синдром наблюдают, когда число тромбоцитов снижается до 20 000–50 000 мкл–1.
Оппортунистические инфекции при СПИД у детей:
- микозы
- пневмоцистная пневмония
- герпесвирусные инфекции
- бактериальные инфекции, в том числе туберкулез и атипичные микобактериозы
- опухоли
- паразитозы
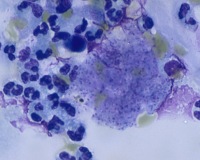
Пневмоцистная пневмония — самое частое из СПИД-индикаторных заболеваний. Возбудитель: Pneumocistis jiroveci. Начало болезни внезапное, болезнь развивается на протяжении 2-4 недель. Типичны такие симптомы:
Рентгенографические методы находят повышение прозрачности легочных полей и двусторонние диффузные интерстициальные изменения. Для подтверждения диагноза нужно обнаружить возбудитель с помощью микроскопии окрашенных мазков из содержимого носоглотки, мокроты, бронхоальвеолярной жидкости.
Кандидозный стоматит — молочница, часто бывает у детей с ВИЧ/СПИД. Бывает при низком количестве лимфоцитов СD4. На слизистой обнаруживаются красные очаги и белый налет, в углах рта формируются покраснения и трещины. Во рту у ребенка может быть боль и жжение.

Стоматит - одна из оппортунистических инфекций ВИЧ/СПИД у детей и подростков
Контагиозный моллюск при СПИДе у детей проявляется высыпаниями – полусферическими папулами, имеющими вдавление в центре. Чаще всего они локализируются на лице.
Бактериальные поражения кожи при ВИЧ у детей требуют длительной антибиотикотерапии. Обнаруживаются такие заболевания:
- абсцессы
- фолликулит
- везикулопустулез
- фурункулез
Ветряная оспа при СПИДе протекает более тяжело, чем при нормальном иммунитете у ребенка. Форма может быть буллезной или генерализированной.
Диагностика СПИДа у детей:
Врачи собирают анамнез, проводят осмотр, обращая внимания на типичные проявления СПИД у детей, проводят лабораторные исследования. К СПИД-маркерным инфекциям относят две группы. В первой группе находятся такие болезни:
- криптоспоридиоз с диареей более 1 месяца пищевода, трахеи, бронхов, легких
- системная герпетическая инфекция более 1 месяца
- цитомегаловирусная инфекция у больных старше 1 месяца
- лимфома головного мозга
- саркома Капоши
- токсоплазмоз ЦНС у лиц старше 1 месяца
- пневмоцистная пневмония
- диссеминированная микоплазменная инфекция
Ко второй группе СПИД-маркерных инфекций относят:
- ВИЧ - энцефалопатию
- сочетанные или рецидивирующие бактериальные инфекции у детей до 13 лет
- диссеминированный микобактериоз
- саркому Капоши у больных любого возраста
- дистрофию непонятной этиологии
- сальмонеллезную септицемию
- внелегочный туберкулез
Лабораторная диагностика СПИДа у детей
- исследование Т-лимфоцитов
- исследование периферической крови
- иммунология крови
- исследование иммуноглобулинов
- серологическое исследование
Лечение СПИДа у детей:
Детям при СПИДе (врожденном или приобретенном) необходима долгая противоинфекционная терапия. При наличии опухолей часто нужны хирургические методы лечения. Иммунозаместительная терапия заключается в пересадке костного мозга или переливании лимфоцитарной массы. Необходимов иммуномодуляторов (гамма-интерферон, интерлейкин 2), который стимулируют образование Т-хелперов.
Врачи назначают препараты, которые стимулируют продукцию продукцию Т-хелперов и действуют на фермент обратную транскриптазу вируса:
Эффект от приема этих препаратов наблюдается у детей с ВИЧ/СПИД только при постоянном приеме. Среди побочных действий выделяют привыкание организма (как следствие – лекарство не действует) и тяжелые реакции. В Японии проходит клиническую апробацию препарат киностатин-72, ингибитор протеаз вируса СПИД. При пероральном приеме, согласно полученным данным, отмечается значительное снижение титра антител к ВИЧ.
Сегодня разрабатываются новые методы и средства для лечения СПИДа у детей, подростков и взрослых. Надежду дает метод генной инженерии. В больную клетку имплантируется клетка-предшественник и создается возможность изменить генетическую программу заболеваний клетки.
Прогноз при СПИДе во всех случаях неблагоприятный.
Профилактика СПИДа у детей:
Первичные профилактические меры заключаются в тестировании крови доноров на наличие ВИЧ, чтобы пациентам не были перелиты зараженные препараты. Следует применять обеззараженные инструменты при проведении различных медманипуляций и хирургических операций. Также среди профилактических мер выделяют пропаганду здоровых сексуальных отношений с единственным партнером и применением контрацепции. Этот метод актуален для подростков. Но уроки сексуального воспитания проводятся также в некоторых школах.
Если о диагнозе ВИЧ/СПИД стало известно беременной женщине, ей рекомендуется прервать беременность, поскольку есть большой риск передачи инфекции ребенку. Во второй половине беременности возможен курс терапии азидотимидином. Это уменьшает риск рождения зараженного малыша с 50% до 25%.
В случае рождения ребенка от зараженной матери, прибегают к кесаревую сечению, чтобы не было горизонтального заражения. Ребенка после рождения следует отлучить от груди матери с ВИЧ/СПИД. Если женщина хочет иметь ребенка от ВИЧ - инфицированного мужа, то возможно искусственное оплодотворение сперматозоидами, прошедшими специальную обработку.
На сегодняшний день нет специфической вакцины, которая защищала бы детей и взрослых от ВИЧ/СПИД. Причины в том, что при вакцинации невозможно получить адекватный иммунный ответ; выделено несколько серотипов ВИЧ; риск непредсказуемых последствий в организме вакцина может стать опасной для акцептора.
Американской ВИЧ-ассоциацией была разработана система рекомендаций по охране прав детей с ВИЧ:
- Решение о посещении ребенка с таким диагнозом школы или другого коллектива детей должны принимать коллегиально председатель мэрии по здравоохранению, представители социальных служб, медработники, родители и педагоги.
- Следует оценивать физические и соматическое состояние ребенка, когда выносят решении о посещении им детского коллектива.
- При решении вопроса об усыновлении отказных детей обязательное исследование на ВИЧ-инфицированность.
- Изоляции подлежат дети с серьезными психическими отклонениями и наличием мокнущих поверхностей тела.
- Должно происходить регулярное медицинское освидетельствование ВИЧ-инфицированного.
- Весь персонал работающий с этими детьми должен ежегодно проходить специальную подготовку, экзамен.
- ВИЧ-инфицированные дети имеют все права, указанные в Конституции.
- Дети с ВИЧ/СПИД имеют право на врачебную тайну.
К каким докторам следует обращаться если у Вас СПИД у детей:
Вас что-то беспокоит? Вы хотите узнать более детальную информацию о СПИДа у детей, ее причинах, симптомах, методах лечения и профилактики, ходе течения болезни и соблюдении диеты после нее? Или же Вам необходим осмотр? Вы можете записаться на прием к доктору .
Пневмоцистная пневмония – это тяжелая форма интерстициального легочного воспаления, вызываемая пневмоцистами и развивающаяся на фоне выраженных иммунодефицитных состояний. Клиническое течение характеризуется нарастающей одышкой, непродуктивным кашлем, фебрильной лихорадкой, болями в груди, развитием сердечно-легочной недостаточности. Диагноз ставится на основании рентгенологических признаков, состояния иммунного статуса, лабораторной идентификации патогена в крови, БАЛ, мокроте, биоптате (ПЦР, серологические тесты, РНИФ). Для этиотропной терапии используются сульфаниламидные, противопротозойные, иммуномодулирующие средства.
МКБ-10


Общие сведения
Пневмоцистная пневмония (ПП) относится к оппортунистическим инфекциям, поражающим лиц с иммунодефицитом и иммуносупрессией. При этом большинство людей с нормальным уровнем иммунитета переносит пневмоцистную инфекцию в виде ОРВИ. Антитела к возбудителю имеют около 90% взрослого населения, около 10% являются бессимптомными носителями пневмоцист – именно они представляют наибольшую угрозу для иммунокомпрометированных пациентов. Пневмоцистная пневмония является самой тяжелой клинической формой пневмоцистоза.

Причины
Характеристика возбудителя
Pneumocystis jirovecii – микроорганизм, вызывающий пневмоцистную пневмонию и другие виды пневмоцистоза у человека. До недавнего времени пневмоцисты считались простейшими, однако в 1988 г. на основании ряда характерных генетических, морфологических и биохимических признаков были отнесены к грибам семейства актиномицетов. Пневмоцисты обладают тропизмом к легочной ткани, весь их жизненный цикл протекает внутри альвеол и проходит 4 стадии:
- Трофозоит. Представляет собой вегетативную стадию P. Jirovecii. Имеет амебоидную форму, диаметр 1-5 мкм, одно ядро и тонкую двухслойную мембрану. Прикрепляется к альвеолоцитам, где увеличивается в размерах и делится.
- Прециста. Имеет овальную форму, диаметр 5 мкм. В ранней стадии содержит одно ядро, окруженное митохондриями, на поздней – 2-6 ядер с мембранами.
- Циста. Зрелая циста округлой формы, с 3-слойной стенкой, диаметром 7-8 мкм. Внутри цисты содержится четное количество (обычно 8 шт.) внутрицистных телец ‒ спорозоитов.
- Спорозоит. При разрыве зрелых цист из них высвобождаются спорозоиты, часть которых обладает одинарным набором хромосом (являются гаплоидными). Сливаясь, они вновь образуют трофозоиты, и жизненный цикл патогена повторяется.
В описанном цикле различают две фазы: неполовую, или асексуальную (деление трофозоита), и половую, или сексуальную (спорозоит-трофозоит-прециста-циста).
Пути передачи
Источниками P. jirovecii являются носители (бессимптомные или больные ОРЗ) и больные пневмоцистной инфекцией. В 30% случаев выявляется вовлеченность в эпидемический процесс медицинских работников. При кашле и чихании носители выделяют мелкодисперсный аэрозоль, содержащий патогены. Заражение восприимчивого макроорганизма происходит при вдыхании контаминированного воздуха (воздушно-капельным, воздушно-пылевым путем). Воротами для входящей инфекции служат дыхательные пути. Редко реализуется трансплацентарный путь передачи.
Характерны внутрисемейные и внутрибольничные эпидемические вспышки пневмоцистной пневмонии. Последние чаще происходят в отделениях недоношенных, домах престарелых, инфекционных стационарах. Пик детской заболеваемости пневмоцистной пневмонией приходится на конец лета – начало осени, взрослые болеют круглогодично.
Группы риска
Пневмоцисты являются типичными оппортунистами, поскольку вызывают манифестную инфекцию только при выраженном дефиците клеточного и гуморального иммунитета у определенного контингента пациентов. К группам риска по заболеваемости пневмоцистной пневмонией относятся:
- ВИЧ-инфицированные и больные СПИДом;
- пациенты с ЦМВ-инфекцией;
- недоношенные дети и младенцы с ЗВУР;
- дети, страдающие гипотрофией, рахитом;
- больные, получающие иммуносупрессивную терапию (по поводу лейкозов, миеломной болезни, других видов рака, трансплантации органов, коллагенозов);
- пациенты с первичными иммунодефицитами, болезнями крови (анемией, полицитемией), туберкулезом, патологией почек.

Патогенез
Пневмоцисты присутствуют в дыхательных путях здоровых людей, но вызывают пневмоцистную пневмонию только у лиц с нарушением гуморального и клеточного звена иммунитета. Экспериментально доказано, что ведущую роль в механизме пневмоцистоза играет снижение Т-хелперов (критическим является снижение СД4+ лимфоцитов ˂300-200 клеток/мкл), увеличение количества цитотоксических лимфоцитов СД8+.
P. Jirovecii с помощью особых выростов – филоподий – прикрепляется к альвеолоцитам первого порядка и альвеолярным макрофагам. Клеточной адгезии также способствуют гликопротеины пневмоцистов, которые взаимодействуют с фосфолипидами, апопротеинами, мукополисахаридами, сурфактантом альвеолярного эпителия. В условиях иммунокомпрометации цисты размножаются, используя сурфактант-ассоциированные белки, выделяют токсические метаболиты.
Происходит разрушение альвеолоцитов, заполнение альвеол пенистым экссудатом, содержащим большое количество пневмоцист на разных стадиях развития, воспалительные клетки, детрит. Интерстициальная ткань инфильтрируется плазматическими клетками. Развивается интерстициальная плазмоклеточная пневмония. Межальвеолярные перегородки гипертрофируются, что приводит к резкому снижению диффузии газов (альвеолярно-капиллярный блок), формированию дыхательной недостаточности и тяжелой гипоксии.
Классификация
В соответствии с патоморфологическими критериями в современной пульмонологии выделяют три стадии пневмоцистной пневмонии:
- I стадия. Происходит прикрепление пневмоцист к альвеолярной стенке. Воспалительная реакция и клинические проявления отсутствуют.
- II стадия. Отмечается десквамация альвеолоцитов, увеличение числа возбудителей в форме цист в макрофагах. В эту стадию появляются начальные клинические проявления пневмоцистной пневмонии.
- III стадия. Развивается альвеолит, плазмоцитарная инфильтрация интерстиция, гигантские скопления пневмоцист в макрофагах и альвеолах. Соответствует разгару заболевания.
Этапы развития пневмоцистной пневмонии:
- отечная фаза ‒ длится 7-10 дней, характеризуется нарастанием симптоматики;
- ателектатическая фаза ‒ продолжается в течение 4-х недель, сопровождается выраженной легочной недостаточностью;
- эмфизематозная фаза – имеет различную длительность, знаменуется обратным развитием симптоматики.
Симптомы пневмоцистной пневмонии
Инкубационный период вариабелен – от 7-10 дней до 2-4 недель (у больных СПИДом – до 10 недель). В отечную стадию клинические признаки пневмоцистной пневмонии легко спутать с обычной респираторной инфекцией. Симптомы нарастают постепенно: вначале беспокоит слабость, недомогание, субфебрилитет. Затем появляется одышка при умеренной нагрузке, боли в грудной клетке, сухой кашель.
В ателектатической стадии лихорадка принимает фебрильный характер, усиливается интоксикационный синдром (отсутствие аппетита, снижение веса, потливость по ночам). Кашель становится коклюшеподобным, постоянным, особенно беспокоит в ночное время суток. Одышка до 30-50 дыхательных движений в минуту выражена в покое. Отмечаются бледность кожных покровов с носогубным цианозом, тахикардия. В этот период пациент может погибнуть от сердечно-легочной недостаточности (СЛН).
У выживших пациентов наступает эмфизематозная стадия. Температура тела снижается, дыхательные расстройства исчезают. В исходе пневмоцистной пневмонии формируется эмфизема легких, легочное сердце. Пневмоцистная пневмония часто протекает в ассоциации с туберкулезом легких.
Четкая стадийность при пневмоцистозе прослеживается в основном у детей раннего возраста. У ВИЧ-инфицированных болезнь имеет стертое затяжное течение, у ВИЧ-негативных лиц с иммунодефицитом – более активное, с быстрым нарастанием СЛН.
Осложнения
Типичными осложнениями, развивающимися в разгар болезни, являются пневмоторакс, подкожная эмфизема, пневмомедиастинум, возникающие вследствие разрыва мелких кистозных образований. Возможно развитие абсцедирующей пневмонии. Эти состояния еще более усугубляют дыхательную недостаточность, повышают летальность. При значительном подавлении иммунитета может произойти генерализация пневмоцистной инфекции с мультиорганным поражением печени, селезенки, ЖКТ, щитовидной железы, органов зрения и слуха, лимфоузлов, костного мозга.

Диагностика
Из-за неспецифичности и стертости симптоматики существенной проблемой является гиподиагностика пневмоцистной пневмонии. Иногда патология диагностируется только посмертно. Все больные с подозрением на ПП должны быть в срочном порядке проконсультированы врачом-пульмонологом, инфекционистом. При выставлении диагноза опираются на следующие данные:
Дифференциальная диагностика
Комплексное клинико-лабораторное, рентгенологическое и бронхологическое обследование позволяет отличить пневмоцистную пневмонию от других поражений легких:
- легочного кандидоза;
- криптококковой пневмонии;
- цитомегаловирусной пневмонии;
- микоплазменной пневмонии;
- хламидийной пневмонии;
- туберкулеза легких;
- респираторного криптоспоридиоза;
- саркомы Капоши;
- бактериальной пневмонии.
Лечение пневмоцистной пневмонии
Стандартные антибактериальные средства при ПП неэффективны. В настоящее время препаратами первой линии считаются комбинированные сульфаниламиды, оказывающие противомикробное, бактерицидное и противопротозойное действие. Могут назначаться как перорально, так и внутривенно. Курс лечения составляет 1-3 недели.
При выраженных токсических эффектах и резистентности подбираются другие антибиотики, активные в отношении пневмоцист (линкозамиды, противолепрозные, противомалярийные, антипротозойные препараты). Из-за массовой гибели патогенов в первые дни терапии состояние пациентов с пневмоцистной пневмонией может ухудшиться, в связи с чем целесообразно назначение кортикостероидов.
Прогноз и профилактика
Смертность от пневмоцистной пневмонии достигает 50% среди недоношенных детей, 25-40% ‒ среди больных СПИДом. У 10-30% иммунокомпрометированных пациентов через несколько месяцев после излечения возникают рецидивы ПП. При отсутствии лечения летальность 100%.
Профилактическая работа реализуется в двух направлениях: эпидемиологическом и медикаментозном. Первый аспект предполагает широкое тестирование на пневмоцистную инфекцию представителей групп риска: пациентов с ВИЧ, онкопатологией, иммунодефицитами, недоношенных детей, сотрудников роддомов и стационаров. Второе направление – это фармакопрофилактика пневмоцистной пневмонии у лиц с количеством СД4+ клеток ˂200. Она заключается в приеме сульфаниламидов в профилактических дозах длительными курсами.
1. Пневмоцистная пневмония. Этиология, патогенез, клиника, дифференциальная диагностика, лечение (лекция)/ Боровицкий В.С.// Проблемы медицинской микологии. – 2012.
2. Пневмоцистная пневмония: исторические, эпидемиологические, клинико-морфологические аспекты/ Марковский В. Д., Плитень О. Н., Мирошниченко М. С., Мирошниченко А. А.// Annals of Mechnikov Institute, - 2012. - №3.
3. Особенности пневмоцистной пневмонии у ВИЧ-инфицированных лиц/ Пузырёва Л.В., Сафонов А.Д., Мордык А.В.// Медицинский вестник Северного Кавказа. – 2016. – Т.11, №3.
4. Пневмоцистоз. Современное состояние проблемы/ Каражас Н.В.// Альманах клинической медицины. – 2010.
Пневмоцистоз – оппортунистическая инфекция дыхательных путей, чаще поражающая детей раннего возраста, а также лиц с ослабленным иммунитетом. Пневмоцистоз может протекать в форме ОРЗ, ларингита, обструктивного бронхита, обострения ХЗЛ, интерстициальной пневмонии. Диагностика пневмоцистоза основана на обнаружении пневмоцист в мокроте и бронхиальном секрете с помощью микроскопии и ПЦР; данных гистологического исследования биоптатов бронхов; рентгенографии и КТ легких, сцинтиграфии, спирографии. Для проведения противопневмоцистной терапии используются препараты сульфаметоксазол+триметоприм, пентамидин, комбинация триметоприма с дапсоном и другие схемы лечения.
МКБ-10
Общие сведения
Пневмоцистоз – легочная инвазия, вызываемая пневмоцистами и протекающая преимущественно в виде пневмоцистной пневмонии. Пневмоцистоз является иммунодефицит-ассоциированным инфекционным заболеванием, которым чаще всего болеют недоношенные дети, а также пациенты с первичными и вторичными иммунодефицитами. Смертельную опасность пневмоцистоз представляет для больных ВИЧ/СПИДом: при отсутствии лечения заболевание неизбежно заканчивается летальным исходом. Пневмоцистоз может возникать как спорадическая или внутрибольничная инфекция в отделениях педиатрии, гемобластозов, пульмонологии, противотуберкулезных инфекционных стационарах.

Причины пневмоцистоза
На сегодняшний день вопрос с видовой принадлежностью возбудителя пневмоцистоза окончательно не решен. В течение длительного времени микроорганизм Pneumocystis Carinii относили к простейшим класса споровиков. Однако в настоящее время доминирует точка зрения, что пневмоцисты занимают промежуточное положение между низшими и высшими грибами. В своем развитии пневмоцисты претерпевают 4 стадии: трофозоита, предцисты, цисты и спорозоита, протекающие на альвеоцитах. При разрыве оболочки созревшей цисты из нее выходят спорозоиты, которые проникают в легочные альвеолы, запуская очередной цикл стадийного развития пневмоцист новой генерации.
Источником эпидемиологической опасности выступает инвазированный человек (больной или носитель), выделяющий спорозоиты с частицами слизи во внешнюю среду при кашле или чихании. Передача возбудителей пневмоцистоза происходит по аспирационному механизму, воздушно-капельным, воздушно-пылевым, ингаляционным или аэрогенным путями. Считается, что среди клинически здоровых лиц до 10% являются носителями пневмоцист, однако у людей с нормально функционирующей иммунной системой инвазия протекает бессимптомно. Риску заболеваемости манифестными формами пневмоцистоза, главным образом, подвержены недоношенные новорожденные; дети с гипогаммаглобулинемией, гипотрофией, рахитом; больные ВИЧ/СПИДом и туберкулезом; пациенты, получающие иммуносупрессивную терапию по поводу коллагенозов, злокачественных новообразований, гематологических и лимфопролиферативных заболеваний, трансплантации органов и пр.
Пневмоцистоз развивается при снижении количества СД4+ клеток (Т-хелперов) в 4 и более раз по сравнению с нормой и достижении уровня менее 200 клеток в 1 мкл. При нарушении клеточного и гуморального иммунитета пневмоцисты начинают активно размножаться в альвеолах, вызывая развитие реактивного альвеолита, образование пенистого альвеолярного экссудата, содержащего пневмоцисты, лейкоциты, клеточный детрит и фибрин. При прогрессировании патологического процесса возникают участки ателектазов в легких, буллезное вздутии легочной ткани, что сопровождается нарушением вентиляции и газообмена, развитием дыхательной недостаточности.
Симптомы пневмоцистоза
В клиническом течении пневмоцистоза выделяют отечную (1-7 недель), ателектатическую (около 4-х недель) и эмфизематозную стадии. У части больных пневмоцистоз может протекать в виде ларингита, обструктивного или астматического бронхита, бронхиолита; в остальных случаях развивается пневмоцистная пневмония.
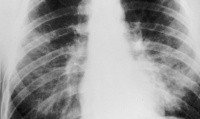
Инкубационный период пневмоцистоза занимает от 10 дней до 2-5 недель. Проявления отечной стадии развиваются постепенно и на ранних этапах включают в себя субфебрилитет, слабость, вялость. В конце первого периода присоединяется сухой кашель, тахипноэ, одышка. Признаками развивающегося пневмоцистоза у грудных детей может служить вялое сосание, отказ от кормления, плохая прибавка в массе тела, цианоз носогубного треугольника. Рентгенологические изменения в легких в отечной стадии пневмоцистоза отсутствуют; аускультативно определяется жестковатое дыхание, мелко- и среднепузырчатые хрипы; перкуторно - тимпанит в верхних отделах грудной клетки.
В ателектатической стадии пневмоцистоз может осложниться развитием пневмоторакса, экссудативного плеврита, легочного сердца, отека легких, а в случае присоединения бактериальной или грибковой инфекции – абсцессом легких. Летальные исходы в этот период обычно обусловлены дыхательной и сердечной недостаточностью. Третья, эмфизематозная стадия пневмоцистоза характеризуется уменьшением одышки и улучшением общего состояния больных. В исходе пневмоцистоза развивается эмфизема легких, сопровождающаяся значительным снижением показателей функции внешнего дыхания.
Диагностика
Клинические, физикальные и рентгенологические данные при пневмоцистозе не являются патогномоничными, что затрудняет своевременную диагностику заболевания. Между тем, пневмоцистную пневмонию всегда следует исключать у иммунокомпрометированных пациентов. С целью верификации пневмоцистоза проводится комплекс лабораторных и инструментальных исследований.
Для подтверждения диагноза пневмоцистоза выполняется бронхоскопия с забором бронхиального секрета, трансбронхиальная биопсия легкого, сцинтиграфия легких с галлием-67. Для лабораторной детекции P.carinii микроскопически исследуются окрашенные мазки мокроты, бронхиальный и трахеальный аспират; выполняется гистологическое исследование биоптатов, исследование мокроты методом ПЦР. Проводится иммунологическая диагностика: определение титра противопневмоцистных IgG и IgM в сыворотке крови с помощью РИФ и ИФА. Дифференциальную диагностику пневмоцистоза необходимо проводить с цитомегаловирусной, хламидийной, уреаплазменной, бактериальной пневмонией, туберкулезом легких, саркомой Капоши и др.
Лечение пневмоцистоза
Лечение пневмоцистоза проводится в стационаре. Лица с иммунодефицитом и недоношенные дети должны быть помещены в отдельные стерильные палаты с ламинарным воздушным потоком. В большинстве случаев для проведения специфической фармакотерапии пневмоцистоза используется комбинированные препараты (сульфаметоксазол+триметоприм, триметоприм+дапсон), пентамидин, эфлорнитин, атоваквон в течение 2-3 недель. Для устранения побочных эффектов терапии назначают фолиевую кислоту, глюкокортикоиды. Проводится инфузионная терапия (введение гамма-глобулина, солевых растворов, глюкозы, плазмы крови, альбумина и др.), кислородотерапия. У больных ВИЧ-инфекцией этиотропная терапия пневмоцистной пневмонии сочетается с высокоактивной антиретровирусной терапией.
Прогноз
Выживаемость при пневмоцистозе составляет 75-90%, а при повторном развитии пневмоцистной пневмонии – 60%. У 25-60% ВИЧ-инфицированных в течение года отмечаются рецидивы заболевания, поэтому больные нуждаются в проведении противорецидивного курса химиотерапии.
Среди недоношенных детей смертность от пневмоцистной пневмонии составляет 50%, но рецидивов практически не наблюдается. При пневмоцистной пневмонии у взрослых, не страдающих СПИДом, прогноз более благоприятный и определяется тяжестью фонового заболевания. У больных СПИДом при отсутствии лечения пневмоцистной пневмонии всегда приводит к летальному исходу. При поздней диагностике летальность при первичном эпизоде - около 40%, своевременно начатое лечение позволяет снизить летальность до 25%. Однако даже через несколько месяцев возможны рецидивы (от 10 до 30%) пневмоцистной пневмонии. Лечение рецидивов проходит значительно труднее, так как у 50 - 80% больных развиваются выраженные побочные реакции на бактрим и пентамидин, и летальность увеличивается уже до 60%.
Эпидемиология пневмоцистной пневмонии.
Пневмоцисты широко распространены среди многих видов диких и домашних животных. Их выявляют у мышей, крыс, хорьков, кроликов, крупного рогатого скота, свиней, собак и др. Спонтанное носительство P. carinii считается обычным явлением. По морфологическим признакам пневмоцисты от разных видов животных почти идентичны. Иммунологические, цитохимические и генетические методы исследований последних лет свидетельствуют об отличиях между P. carinii, выделенными от различных видов животных. Так, антитела к P. carinii, которые образуются у одного вида животных, перекрестно не реагируют с антигенами P. carinii других видов животных. Хромосомы пневмоцист от человека, мышей, хорьков сходны по размерам, но имеют индивидуальный кариотип. В экспериментальных условиях попытки передачи пневмоцист от человека и различных видов животных другим видам животных, даже иммунодефицитным, закончились неудачей. Это свидетельствует о строгой видовой специфичности P. carinii. Циркуляция возбудителя среди людей происходит без дополнительных хозяев.
Пневмоцистоз человека - антропоноз. Источник инфекции - человек.
Основной механизм передачи - капельный. Главное место локализации патологического процесса при пневмоцистозе - дыхательные органы. При кашле, который является наиболее частым симптомом болезней органов дыхания, образуется мелкодисперсный аэрозоль. Его частицы не оседают, а находятся во взвешенном состоянии. Заражение пневмоцистами происходит при вдыхании воздуха, контаминированного возбудителем. Выявить цисты в воздухе и других объектах внешней среды до настоящего времени не удавалось. Только с помощью молекулярно-биологических исследований в образцах воздуха помещений, где находились больные пневмоцистозом, были обнаружены генетические носители (фрагменты ДНК) пневмоцист.
При тяжелых формах иммунодефицита у ВИЧ-инфицированных больных циркуляция пневмоцист может происходить в кровеносной системе. Имеются указания на возможность выявления фрагментов ДНК пневмоцист в крови и внутренних органах вне иммуносупрессии. Учитывая возможность пребывания возбудителя в кровеносной системе, фактором передачи, очевидно, может быть кровь. Пропагативная форма, обеспечивающая персистенцию P. carinii в организме хозяина и сохранение в окружающей среде, морфологически не описана.
Исследования показали, что число цист P. carinii у отдельных больных с неспецифическими заболеваниями легких колеблется в широких пределах - от 5 до 1500 цист в 1 мл мокроты, а по средним показателям в отдельных контингентах - от 140 ± 45 до 235 ± 30. Из-за невозможности выделения возбудителя из внешней среды сроки выживаемости пневмоцист в воздухе, других объектах не определены.
Существует возможность возникновения вспышек пневмоцистоза. В литературе описаны вспышки в стационарах для детей раннего возраста, в детском туберкулезном санатории, домах ребенка, школах, интернатах. Они характеризовались растянутостью во времени (1,5 - 2,5 мес. с момента выявления первых случаев), втягиванием в эпидемический процесс большого количества больных (34 - 84%) и медицинского персонала (38 - 75%), полиморфизмом клинических проявлений пневмоцистоза, преобладанием среди зараженных пневмоцистами лиц носителей, а у больных с клиническими проявлениями - регистрацией случаев пневмоцистной пневмонии, особенно у детей раннего возраста.
Исследования, проведенные среди ВИЧ-отрицательных и ВИЧ-положительных больных с неспецифическими заболеваниями легких и медицинских работников отделенния СПИДа и пульмонологических отделений, показали, что зараженность P. carinii больных колеблется от 28% до 84%, количество выделяемых цист в мокроте - от 155 до 330 в 1 мл. Зараженность P. carinii медицинских работников, обследованных по клиническим показаниям (наличие кашля, мокроты, патологии дыхательных путей), - 100%, число выделяемых пневмоцист - 165 цист в 1 мл мокроты. Учитывая частое и длительное пребывание больных в стационаре, назначение им инвазивных методов исследования (бронхо-, трахеоскопия), переуплотненность палат и отсутствие боксированных помещений, а также значительную зараженность P. carinii медицинского персонала, можно предположить возможность легкой передачи пневмоцистоза в отделениях. Его можно рассматривать как внутрибольничную инфекцию с капельным механизмом передачи.
Распространенность пневмоцистной пневмонии.
Пневмоциста является условно-патогенным возбудителем, ее патогенные свойства проявляются только при угнетении естественной резистентности организма, в частности, при иммуннодефиците разного происхождения.
По данным литературы, пневмоцистная пневмония чаще всего регистрируется у детей раннего возраста, несовершенство иммунитета у которых обусловлено недоношенностью, дефектами иммунной системы (гипо- или агаммаглобулинемия), проявлениями рахита, пороками сердца, цитомегаловирусной инфекцией. Большинство исследователей связывают пневмоцистоз с детским возрастом. P. carinii выявляли у 10 - 40% обследованных детей в странах Европы и у 7% - в странах Африки. Однако допускается, что действительная зараженность пневмоцистами выше. По данным серологических исследований (РИФ, ИФА, метод встречного электрофореза), в США из 120 здоровых детей в возрасте до 1 года 33% имели AT к P. carinii, в возрасте 3-4 лет - 83%. В Дании исследование в РИФ сывороток 300 детей выявило AT к P. carinii у 20% детей до 1 года, у 33% - в возрасте 1 года, у 58% -2 лет, у 75% - 3 - 5 лет, и у 71% - 11 - 15 лет.
Основными группами риска развития пневмоцистной пневмонии являются взрослые и дети с системными заболеваниями крови и соединительной ткани, онкологические больные, реципиенты трансплантированных органов, пациенты с другими болезнями, для лечения которых используют иммуносупрессивную терапию (кортикостероиды, цитостатики, облучение).
Частота развития пневмоцистной пневмонии в группе больных с гемобластозами составляет в среднем 2%. Она зависит от характера заболевания (при лимфопролиферативных процессах - до 9%), от вида препаратов, их количества, дозы, длительности терапии. После трансплантации костного мозга пневмоцистная пневмония развивалась у 0,7 - 15% пациентов. У взрослых с неоплазмами на аутопсии пневмоцистоз выявлен у 5% умерших. К группам риска заражения пневмоцистами и развития пневмоцистной пневмонии относятся лица пожилого возраста, больные диабетом.
Многочисленные данные литературы свидетельствуют о персистенции пневмоцист в иммунокомпетентном организме человека и животных без развития выраженных форм болезни
Лишь иммунодефицит ведет к размножению возбудителя и развитию патологии. Есть также мнение, что состояние бессимптомного носительства P. carinii для человека вообще не характерно, так как не у каждого человека с иммунодефицитом развивается клинический пневмоцистоз. Этот вопрос нуждается в углубленном изучении.
Читайте также:

