Производство вакцины от вич
Обновлено: 25.04.2024
Егор Воронин — нью-йоркский вирусолог, специалист в области вакцинопрофилактики. Более двадцати лет он занимался исследованиями ВИЧ, его эволюцией и репликацией. С 2018 по 2020 год он возглавлял биотехнологическую компанию Worcester HIV Vaccine, занимающуюся разработкой вакцины от ВИЧ. В своем блоге shvarz Егор публикует массу интересных фактов о вакцинах, ВИЧ, о вирусах в целом, а в последние полтора года и о новом коронавирусе: он умеет рассказывать простым языком о сложном.
— Наверное, тот факт, что сейчас все следят за вакцинами, позволит объяснить это проще.
— Это единственная проблема?
— Нет. Вторая проблема: как мы все уже знаем в отношении коронавируса — созданные против него вакцины хорошо предотвращают тяжелое течение болезни и смерть, но гораздо хуже защищают от заражения. Для COVID-19, как все же быстротечной болезни, это нормально: даже если вирус попадет в привитый организм, он не вызовет тяжелую болезнь, организм силами иммунной системы быстро его поборет, и человек скоро выздоровеет, вирус исчезнет.
С ВИЧ же совершенно другая ситуация. Он приспособлен к тому, чтобы жить в организме очень долго и ускользать от иммунной системы годами. Если мы не предотвратили его попадание в организм, то без терапии он будет в нем реплицироваться и в конце концов вызовет СПИД. Будучи привитыми от коронавируса, вы можете все равно им заразиться, но лишь чуть-чуть поболеете или даже не заметите, что вирус был, организм его вычистит, — а с ВИЧ это не работает. На ранних этапах разработки вакцин пытались измерять их эффективность именно по способности предотвращать не заражение ВИЧ, а последующее развитие СПИДа, но сейчас уже ясно, что если ВИЧ попал в организм, то без терапии СПИД неизбежно разовьется. Значит, в отношении ВИЧ нам нужна вакцина, которая будет полностью предотвращать само попадание вируса в организм, а это гораздо более высокая планка.
— Но с точки зрения обывателя все кажется просто: есть вирус ВИЧ, он выделен и хорошо известен. Так возьмите его, убейте, и убитый, обезвреженный вирус введите человеку — пусть организм вырабатывает иммунный ответ. Ведь так делались все классические вакцины. На каком этапе оказалось, что с ВИЧ это не работает?
— Над вакциной от ВИЧ работают уже не первый десяток лет. При этом были сделаны какие-то побочные открытия, которые можно применять в других областях? Например, в нынешней борьбе с коронавирусом?
— Попытки создать вакцины от ВИЧ начались сразу же, как только вирус был впервые выделен. Пытались сделать вакцины на основе убитого вируса, на основе рекомбинантных белков, продолжают активно работать над векторными вакцинами. А когда появился COVID-19, практически все мои коллеги, кто занимался вакцинами от ВИЧ, перекинулись в область коронавируса. Я смотрю на научные статьи о коронавирусе — там все знакомые имена.
Я уже упоминал, что технология стабилизации спайкового белка была разработана для ВИЧ, это был один из главных прорывов в вакцинологии за последние десять лет, и она нашла отличное применение в вакцинах от COVID-19.
Известный вирусолог Барни Грэм, который занимался именно стабилизацией вирусного белка у ВИЧ и у респираторно-синцитиального вируса, сыграл важную роль в разработке одной из самых популярных в мире вакцин от COVID-19 компании Moderna.
Мишель Нуссенцвайг, который выделил нейтрализующие антитела к коронавирусу, разработал технологию выделения этих антител в ходе многолетних исследований антител к ВИЧ и вирусу иммунодефицита обезьян. Памела Бьоркман, ведущий специалист Caltech по структуре вирусных белков, раньше изучала в том числе и ВИЧ.
— Это известные имена, но применяются ли отработанные на ВИЧ методики?
— Сами методы тестирования на нейтрализующие антитела были разработаны для ВИЧ, а теперь применяются для COVID-19. В области тестирования вакцин существует огромная сеть клинических центров и лабораторий и в США, и в Африке, и по миру — она была создана для ВИЧ-инфекции, после начала пандемии ее просто взяли и перепрофилировали под коронавирус, а заведуют ею те же самые ученые.
С другой стороны, технологии, нашедшие применение в вакцинах от COVID-19, сейчас интересуют и исследователей ВИЧ: технология мРНК вакцин разрабатывалась и для ВИЧ, но сейчас работы в этой области существенно активизировались.
— Кто-нибудь из российских ученых занимается разработками вакцины от ВИЧ?
— В России разработки вакцин от ВИЧ ведутся, но их немного. Есть три исследовательские группы: в Москве, Петербурге и в Новосибирске. У них есть определенные наработки, но пока они не прошли дальше первой фазы испытаний.
Вопрос в большей мере этический. Раз уж существуют эффективные методы предотвращения ВИЧ-инфекции, то нельзя не делать их доступными участникам клинических испытаний. Но если мы предоставляем их всем участникам клинических испытаний (и плацебо-группе, и группе, получающей вакцину), то количество новых инфекций будет чрезвычайно мало в обеих группах, и эффективность вакцины будет невозможно измерить. Или придется делать испытания еще обширнее и еще длинней, что еще больше повысит их стоимость.
Перспективы разработки вакцины от ВИЧ тают с каждым днем именно потому, что сложно их тестировать, не подвергая людей риску заразиться в ситуации, когда есть готовые способы избежать этого риска. Но нельзя сказать, что ученые полностью потеряли надежду. Уже ведутся активные обсуждения новых подходов к проведению клинических испытаний ВИЧ-вакцин в будущем.
Перед тем как говорить о вакцине против ВИЧ, стоит начать с более общего вопроса: что мы понимаем под прививками и вакцинами с научной точки зрения?
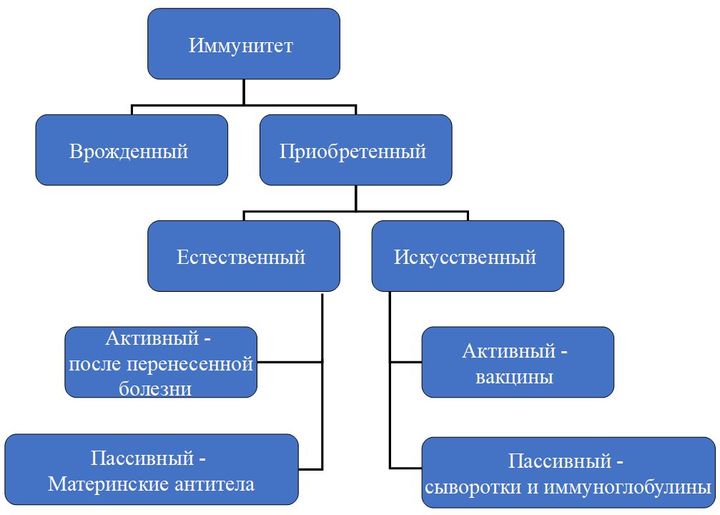
По механизму возникновения иммунитет делится на два вида: врожденный и приобретенный. Первый есть у каждого человека с рождения, он выработан эволюционно. Благодаря нему человек не болеет многими болезнями, которыми, например, страдают животные.
Второй возникает в течение жизни и у каждого может отличаться в зависимости от того, с какими возбудителями человеку довелось встретиться.
по теме
Лечение
Как устроен иммунитет: Объясняем по пунктам
Приобретенный иммунитет может быть активным (он возникает вследствие реакции организма на перенесенную болезнь, присутствие возбудителя в организме), а может быть пассивным, когда антитела, например, передаются от матери ребенку во время беременности.
Именно по этим антителам, как правило, и ставится диагноз, если мы пользуемся экспресс-тестами. В случае с ВИЧ существует и пассивный иммунитет. Но при передаче вируса от матери ребенку, к сожалению, он не обладает достаточным защитным эффектом.
Еще одно направление — это искусственный иммунитет. Он тоже бывает активным и пассивным. Пассивный — это иммуноглобулины, выработанные либо у лабораторных животных, либо у других иммунизированных лиц, и сыворотки. Активный же достигается собственно путем вакцинации.
Вакцины бывают профилактические (защитные) и лечебные. Они различаются по типу воздействия на организм и по своим результатам.
Пассивный иммунитет возникает быстрее, сразу после того, как в организм ввели чужие антитела. Однако он бывает совсем недолговременным. Активный иммунитет держится долго, чаще — пожизненно, но и возникает не сразу.
Иммунный ответ: как это все работает?
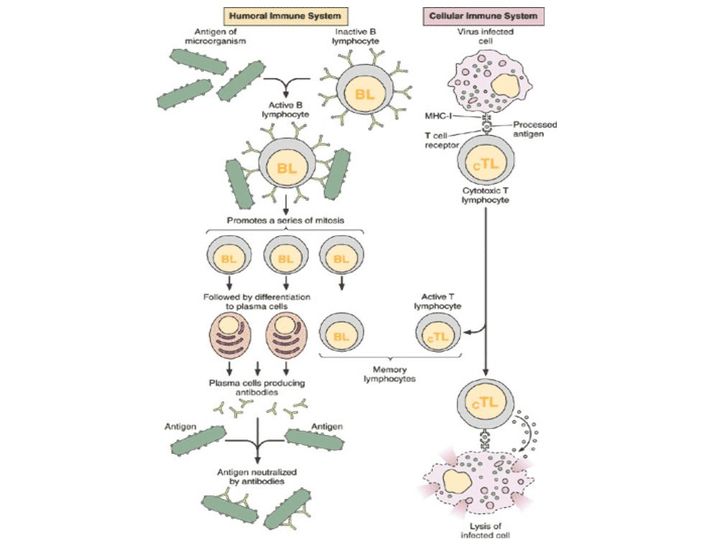
Ученые обычно говорят о гуморальном и клеточном иммунитете. Принцип работы гуморального заключается в следующем: в нашем организме есть специальные клетки — лимфоциты. Они постоянно циркулируют в крови и проверяют все, что попадается им на пути, по принципу свой/чужой.
по теме

Лечение
Гид по вакцинам. Когда и какую прививку сделать? А главное: надо ли вообще прививаться? (Спойлер: конечно, надо)
Например, антитела к ВИЧ-инфекции появляются где-то через месяц после заражения, соответственно, все это время вирус может циркулировать в организме. Почему они неэффективны? Во-первых, потому что появляются слишком поздно.
Во-вторых, потому что вирус, с которым мы имеем дело, очень изменчив. Если даже В-клетки обнаружили его антиген, выработали к нему антитела, способные нейтрализовать заразу, то за время, которое ушло на все это, сам вирус успевает мутировать и оказаться неуязвимым для выработанного организмом оружия.
Когда мы говорим о клеточном иммунитете, речь идет об уничтожении тех вирусов, которые преодолели гуморальный барьер и успели забраться в саму клетку.
Клетки CD4 частично регулируют весь процесс и выполняют функцию клеток памяти. Их принято называть хелперами. CD8 — собственно занимаются уничтожением, за это их зовут киллерами.
ВИЧ — единственный вирус, который поражает не просто клетки организма, а собственно клетки иммунной системы. Той самой, которая с вирусом должна, по идее, бороться.
Именно поэтому против ВИЧ-инфекции иммунитет не может сработать так, как это было бы с любым другим вирусом.
Какие возникают трудности при создании вакцины против ВИЧ?
На данный момент в рамках более ста испытаний уже протестировано более сорока видов вакцин с участием тысяч добровольцев, и есть целая система, в которой регистрируются все исследования по вакцинации от ВИЧ.
Последнее время в разного рода СМИ регулярно появляется информация, что той или иной компанией разрабатывается новая вакцина против ВИЧ. Однако обнадеживающих результатов не так уж и много. Почему?

ТАСС, 4 февраля. Американские молекулярные биологи создали белковую молекулу, которая заставляет организм животных и людей вырабатывать антитела ко всем разновидностям ВИЧ, и успешно проверили ее работоспособность в опытах на мышах. Результаты исследования опубликовал научный журнал Nature Communications.
Какая инфекция помогла Кутузову и почему забраковали вакцину от ВИЧ? Тест об эпидемиях и нашей борьбе с ними

"Наше открытие проложило дорогу для быстрой разработки вакцин от ВИЧ, которые заставляют иммунитет человека вырабатывать антитела, обладающие широким профилем действия. Это резко ускорит разработку высокоэффективных прививок от вируса иммунодефицита", - рассказал один из авторов исследования, доцент Института Вистара (США) Дэниел Калп.
ВИЧ проникает в иммунные клетки человека, используя белки, которыми покрыта его оболочка. Структура этих молекул, а также связанных с ними нитей сахаров быстро меняется по мере размножения вируса, что вынуждает иммунитет участвовать в своеобразной "гонке вооружений", постоянно вырабатывая новые наборы антител. В конечном итоге в ней почти всегда побеждает вирус, если пациент не принимает антиретровирусных лекарств.
В этом случае примерно через 3-4 года после заражения ВИЧ иммунная система приспосабливается к вирусу и начинает синтезировать так называемые антитела широкого профиля действия. Эти молекулы могут распознавать и нейтрализовать сразу несколько разновидностей вируса, соединяясь с критически важными участками в структуре тех белков, которые ВИЧ использует для проникновения в клетки.
Основа для вакцины от ВИЧ
Калп и его коллеги выяснили, что этого можно добиться при помощи созданной ими сложной белковой молекулы, которая состоит из нескольких фрагментов оболочки ВИЧ. Она активно взаимодействует с иммунными клетками и заставляет их вырабатывать антитела, которые соединяются с так называемым C3V5-участком, особой областью на поверхности оболочки ВИЧ, почти не меняющейся по мере его эволюции.
Ученым удалось значительно упростить и удешевить производство данной вакцины при помощи ДНК-молекулы, которая кодирует в себе все необходимые фрагменты оболочки вируса. Как показали опыты на мышах, эту нить ДНК можно вводить в клетки грызунов, что будет заставлять их вырабатывать большое число подобных антигенов. Это привлекает внимание иммунных клеток и заставляет их вырабатывать универсальные антитела к ВИЧ.
Что интересно, простое введение белковых компонентов оболочки ВИЧ в организм мышей не приводило к появлению значимых количеств антител, способных присоединяться к участку C3V5. Это свидетельствует о том, что взаимодействия между фрагментами вирусной оболочки играют важную роль в формировании универсальных антител к ВИЧ, что необходимо учитывать при последующей разработке вакцин.
По словам Калпа и его коллег, в ближайшее время ученые попытаются создать новые вариации подобных белков и проверят, можно ли повысить эффективность текущего прототипа вакцины при помощи точечных модификаций структуры белка. Эти опыты, как надеются исследователи, это приведет к созданию первых полноценных вакцин от ВИЧ уже в ближайшее время.
— Какие на данный момент существуют разработки препаратов против ВИЧ? Насколько в этом направлении продвинулись зарубежные коллеги?
Есть еще обширный пласт просто химиопрепаратов, которые разрабатываются для ВИЧ-пациентов. Этими препаратами кормят пациентов на протяжении всей жизни со всеми вытекающими последствиями.
— Самые перспективные исследования сейчас с чем связаны?
— Связаны с генной терапией, в первую очередь, когда вводятся гены, которые разным способом действуют на инфекцию. В нашем случае мы говорим о так называемой внутриклеточной иммунизации, когда гены вводят в клетку и эта клетка становится устойчивой к вирусу: он не может в нее зайти или не может в клетке размножаться. Варианты зависят от гена. Делаем такую вот иммунизированную клетку, которая для вируса недоступна.
— Можете немного подробнее рассказать, как это работает?
— Есть доказательства, что этот механизм эффективен?

— Как можно повторить такой случай излечения?
— В чем принципиальная разница между нашей разработкой и американской?
— Комплексным подходом?
— Совершенно верно. Аналогичный подход используется сейчас при терапии ВИЧ — антиретровирусная терапия комбинированная, и она помогает. В генной терапии такой же подход — недостаточно перекрыть один какой-то путь вирусу. Мы сейчас задумываемся о том, что мы к этому препарату будем добавлять еще один ген, который еще дополнительно подстрахует. Мы считаем, что в генной терапии тоже три гена будут успешны.
— По доклиническим испытаниям есть два основных направления: мы должны показать эффективность и безопасность этого лекарственного препарата. С безопасностью тут все понятно: есть серия тестов, они одинаковые для химических препаратов и для биологических, таких как наш, мы их все успешно прошли, доказали, что препарат безопасен и в больших дозах не вызывает никаких побочных эффектов. В том, что касается эффективности, сложнее, потому что для каждого препарата нужна своя модель. Например, животные, которые болеют этой болезнью, чтобы мы их вылечили и показали, что препарат работает. С ВИЧ сложно, поскольку моделей готовых нет, а на человеке не можем проводить.
— Но на клетках уже есть результаты?
— На данный момент мы показали эффективность препарата на клетках. Есть клетки, их можно заразить.
Можно у человека взять его лимфоциты, посадить в пробирку. Если к ним добавить вирус, вирус начинает размножаться — клетки дохнут. На такой системе in vitro мы показали, что когда мы обрабатываем препаратом клетки, то потом на них вирус практически не растет.
— Может быть, не 100% сейчас, но очень сильное снижение вируса, практически до нуля. При этом есть еще некоторые моменты, которые мы могли бы улучшить, а именно — доставку препарата. Поскольку когда мы обрабатываем препаратом клетки, то он попадает не во все клетки. Поэтому мы сейчас работаем над улучшением доставки, поскольку от этого улучшится и эффективность препарата.
— На какой стадии сейчас исследования на животных?
— Второй вопрос в том, что нужно все-таки провести исследования in vivo, то есть на каких-нибудь животных. Тут проблема такая, что в принципе есть модель мышей, специально разработанная, так называемые гуманизированные мыши. Их можно заразить вирусом, и он будет себя вести в них, как в теле человека, потому что у этих мышей — человеческие клетки крови, лимфоциты и так далее. Но в нашей стране их, к сожалению, нет. Их можно привезти, но их транспортировка требует особых условий, потому что они изначально не имеют иммунной системы. Если все это сложить, то получается, что мыши стоят очень и очень дорого.
— А сколько таких мышей надо?
— Необходимо не менее 50 животных и отлаженная методика гуманизации. Каждая мышь стоит 300—500 евро, но еще больше стоит работа по гуманизации, содержанию мышей, заражению их вирусом.
— То есть сейчас все уперлось в отсутствие возможности провести доклинические исследования на животных моделях?
— Конечно, прежде чем выйти на клинические испытания, хотелось бы больше быть уверенными, что он у нас in vivo работает. На тех тестах, которые мы уже провели, видно, что он хорошо себя ведет, хотелось бы еще убедиться в этом на животных моделях. Кроме того, мы сейчас подали проект на совместное финансирование с немецкими коллегами, которые работают с такими мышами. Ждем сейчас, будет им это интересно или нет. Если будет интересно, то со следующего года мы начнем проверять уже на этих мышах. С другой стороны, идет строительство собственного вивария в ЦНИИ эпидемиологии, где будут созданы все условия для содержания таких мышей, для их гуманизации, чтобы мы могли сами уже это делать, не зависеть ни от кого, потому что на самом деле заказ таких исследований за рубежом — это очень дорого.
— На какой стадии сейчас исследования по редактированию генома?
— Это более безопасное, хотя и пока менее эффективное воздействие. Тем не менее у нас сейчас более или менее хорошо работает система изменения генома CRISPR-Cas. Есть еще вторая система, которая может что-то прицельно в геноме вырезать, что-то прицельно вставлять и делать уже направленные изменения. Тут более или менее все ясно, потому что изменять надо ген CCR5, и это мы уже делаем. Но поскольку препарат нам нужен комплексный, мы ищем способы, как бы нам вместо этого CCR5 встроить гены, которых нам не хватает для того, чтобы клетка была полностью защищена. Уже работы идут, но есть нюансы. Я думаю, что к тому моменту, когда у нас появятся собственные мыши в виварии, мы уже будем готовы испытывать, и сразу выберем лучшее, и с ним уже будем готовиться к клиническим испытаниям.
— Когда нам ожидать регистрации препарата?
— То есть это через несколько лет?
— Это не следующий год, это лет через пять, по оптимистичным прогнозам. В среднем до 10 лет проходит. Опять-таки клинические испытания — это деньги, производство препарата — это тоже деньги. С другой стороны, мы рассчитываем, что это будет революция, потому что с химиопрепаратами для антиретровирусной терапии уже более или менее все понятно — они работают, но это пожизненно, дорого и токсично для организма.
Читайте также:

