Противовирусные препараты лечение эндометрита
Обновлено: 26.04.2024
Воспалительные заболевания женских половых органов занимают одно из ведущих мест в структуре гинекологической патологии и составляют 60-65%. Хронический рецидивирующий эндометрит (ХРЭ) встречается у женщин преимущественно в репродуктивном возрасте и ведет к нарушению менструальной, секреторной и генеративной функций. Частота хронического эндометрита по данным разных авторов варьирует в широких пределах — от 0,2% до 66,3%, в среднем составляя 14%. Среди женщин репродуктивного возраста, страдающих циклическими нарушениями менструальной функции, частота данного заболевания составляет 53,2%.
Тенденцию к увеличению частоты ХРЭ многие авторы связывают с широким использованием внутриматочных спиралей (ВМС), ростом числа искусственных абортов, изменениями в этиологии воспалительных заболеваний матки и придатков. Частыми осложнениями данного воспалительного заболевания являются осложненное течение беременности, родов и послеродового периода, а также вторичное бесплодие и привычное невынашивание беременности. В последнее время отмечается увеличение числа мало-и асимптомных форм эндометрита, склонность к хроническому и длительному течению с частыми рецидивами, быстрому развитию осложнений.
Немаловажную роль в развитии нарушений репродуктивной функции имеют иммунологические изменения при ХРЭ, в т. ч. увеличение числа макрофагов (CD68) в эндометрии больных, выраженный клеточный и медиаторный дисбаланс в эндометрии на фоне хронического воспаления, подавление фагоцитарной активности лейкоцитов, количественное содержание lg классов М, G и А в эндометриальном секрете в 100 раз превышает показатели здоровых женщин, при умеренном их снижении в сыворотке крови.
Следовательно, наряду с воздействием на возбудителя и сам воспалительный процесс, первостепенное место в программе лечения ХРЭ должны занимать идентификация структурных и/или функциональных нарушений в иммунной системе и коррекция этих нарушений.
Возникает вопрос, какой вид иммуномодулятора целесообразней выбрать для лечения и профилактики вторичных иммунодефицитов у лиц с хроническими воспалительными заболеваниями (ХВЗ). Как известно, элиминация большинства инфекционных агентов осуществляется именно клетками фагоцитарной системы, поэтому иммуномодуляторы, воздействующие на клетки моноцитарно-макрофагальной системы, являются оптимальным выбором для активации противоинфекционного иммунитета и показаны к применению при наличии хронического инфекционно-воспалительного процесса.
Полиоксидоний ®
Иммуномодулятор последнего поколения Полиоксидоний ® — физиологически активное высокомолекулярное соединение, сополимер N-окси-1,4-этиленпиперазина и (Г\1-карбоксиэтил)-1,4-этиленпиперазиния бромида с молекулярной массой 60-100 kD.
Препарат оказывает активирующее влияние на неспецифическую резистентность организма, фагоцитоз, гуморальный и клеточный иммунитет. Установлено, что Полиоксидоний ® действует на все звенья фагоцитарного процесса: активирует миграцию фагоцитов, усиливает клиренс чужеродных частиц из кровотока, повышает поглотительную и бактерицидную активность фагоцитов. Стимулируя иммунные реакции, Полиоксидоний ® не нарушает естественные механизмы их торможения и не истощает резервные возможности кроветворной системы.
Иммуномодулирующие свойства Полиоксидония ® проявляются также и в индукции синтеза цитокинов (IL-1 бета, IL-6, TNF-альфа и IFN-альфа), но только при их исходно низких или средних уровнях. Полиоксидоний ® усиливает исходно сниженную цитотоксичность NK-клеток, усиливает образование антител.
Детоксицирующие свойства Полиоксидония ® связаны с его высоким молекулярным весом и наличием на поверхности молекул большого количества различных активных групп. Поэтому он активно адсорбирует на своей поверхности циркулирующие в крови как растворимые токсические субстанции, так и микрочастицы.
Антиоксидантные свойства Полиоксидония ® проявляются в перехвате в водной среде активных форм кислорода, Н2Ог, ОН-; уменьшении концентрации каталитически активного Fe2+.
Материалы и методы
За время лечения проводилось несколько осмотров: до лечения, сразу и через один месяц после лечения. Динамическое наблюдение за репродуктивной функцией осуществлялось в течение трех лет. Всем пациенткам проводились общеклинические, иммунологические, специальные гинекологические, микроскопические исследования отделяемого из цервикального канала, микробиологическая и диагностика методом полимеразной цепной реакции (ПЦР) биоптата эндометрия, УЗИ, исследование сосудов малого таза, гистероскопия с морфологическим, бактериологическим и ПЦР-исследованиями прицельно взятого эндометрия. В ходе лечения проводился динамический контроль общего анализа крови, иммунологических и биохимических показателей с применением статистических методов обработки результатов.
Кроме ХРЭ у пациенток имелись сопутствующие гинекологические заболевания: миома матки — 22,2%, вторичное бесплодие — 25,1%, привычное невынашивание — 14,1%, варикозное расширение вен малого таза — 5,9%. Сочетанная сопутствующая гинекологическая патология выявлена в 20,7% случаев.
Следует отметить, что положительная динамика, выражавшаяся в значительном уменьшении или полном исчезновении клинических симптомов ХРЭ при проведении лечения, в 1-й подгруппе наблюдалась на 2-3 сутки от начала лечения, во 2-й подгруппе — на 4-6 день, а в 3-й — на 5-7 день от начала терапии (рис.).
Рис. Сроки наступления положительной динамики на фоне различных схем терапии
Таблица. Оценка клинических проявлений на фоне проведенной терапии
| Симптомы | Клиника | До лечения | 1 подгруппа (комплексная терапия) | 2 подгруппа (монотерапия) | 3 подгруппа (стандартная терапия) | ||||
| Абс. | % | Абс. | % | Абс. | % | Абс. | % | ||
| Боли | Периодические боли внизу живота с усилением перед или в первые дни менструации | 135 | 100 | 2 | 4,0*** | 2 | 5,0*** | 5 | 11,1** |
| Бели | 135 | 100 | 3 | 6,0*** | 3 | 7,5*** | 7 | 15,5** | |
| Слизисто-гнойные | 100 | 74 | 0 | 0,0*** | 0 | 0,0*** | 1 | 2,2*** | |
| Слизистые | 35 | 26 | 3 | 6,0* | 3 | 7,5** | 6 | 13,3* | |
| Без запаха | 49 | 36,3 | 3 | 6,0* | 3 | 7,5** | 6 | 13,3* | |
| С неприятным запахом | 86 | 63,7 | 0 | 0,0*** | 0 | 0*** | 1 | 2,2** | |
| Нарушение менструального цикла | 75 | 55,5 | 2 | 4,0** | 3 | 7,5** | 7 | 15,5* | |
| Меноррагия | 27 | 19,9 | 0 | 0,0* | 0 | 0,0** | 1 | 2,2* | |
| Метроррагии | 3 | 2,3 | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 | |
| Олигоопсоменорея | 5 | 3,7 | 1 | 2,0 | 1 | 2,5 | 2 | 4,4 | |
| Альгодисменорея | 40 | 29,6 | 1 | 2,0* | 2 | 5,0* | 4 | 8,9* | |
| Нарушения репродукции | Вторичное бесплодие | 34 | 25,0 | 1 | 2,0* | 2 | 5,0* | 10 | 22,2 |
| Привычное невынашивание | 19 | 4,1 | 1 | 2,0* | 1 | 2,5* | 6 | 13,3 | |
| Изменение либидо | 28 | 20,7 | 2 | 4,0* | 2 | 5,0** | 3 | 6,6* | |
| Аноргазмия | 4 | 2,9 | 1 | 2,0 | 1 | 2,5 | 2 | 4,4 | |
| Вагинизм | 3 | 2,2 | 1 | 2,0 | 1 | 2,5 | 0 | 0,0 | |
| Диспареуния | 21 | 15,6 | 0 | 0,0** | 0 | 0,0** | 1 | 2,2* | |
| Другие симптомы | Общая утомляемость | 19 | 14,1 | 1 | 2,0* | 4 | 4,4* | 2 | 10,0 |
| Слабость | 27 | 19,9 | 1 | 2,0** | 2 | 5,0* | 7 | 15,5 | |
| Дизурические проявления | 34 | 25,0 | 1 | 2,0* | 3 | 7,5* | 10 | 22,2 | |
| Примечание. Статистическая значимость различий с данными до лечения обозначена: * р < 0,05; ** р < 0,01 ;*** р < 0,001. | |||||||||
При анализе динамики количества белей у больных ХРЭ было установлено, что на фоне комплексной терапии на 3-4 сутки от начала лечения этот симптом сохранялся у 6% пациенток, на фоне монотерапии — у 7,5%, а в 3-й группе — у 15,5%. Выраженный положительный эффект при использовании Полиоксидония ® как в комплексной, так и в монотерапии проявлялся полным исчезновением таких симптомов, как мено-и метроррагии, в то время как на фоне стандартной терапии такой симптом, как меноррагия, сохранялся у 2,2% пациенток. Альгодисменорея, наблюдавшаяся до лечения у 29,6% больных ХРЭ, сохранялась после комплексной терапии у 2% пациенток, на фоне монотерапии — у 5%, а при использовании стандартной схемы лечения — у 8,9% женщин.
На фоне комплексной терапии было отмечено значительное уменьшение дизурических нарушений в 12,5 раза после окончания лечения (при монотерапии уменьшение в 3,3 раза), в группе пациенток со стандартным лечением этот показатель практически не изменился и наблюдался у 22,2% (до лечения у 25%).
У больных ХРЭ в нашем исследовании вторичное бесплодие отмечалось в 25% случаев. При анализе репродуктивного анамнеза в течение трех лет после окончания лечения, нами было обнаружено восстановление репродуктивной функции: на фоне комплексной терапии — вторичное бесплодие сохранялось лишь у 2% женщин; при использовании монотерапии — сохранялось у 5% пациенток; при использовании стандартной терапии — у 22,2% больных, что показывает отсутствие влияния традиционной схемы лечения на репродуктивную функцию. Привычное невынашивание, составлявшее 14,1% до лечения в первой подгруппе, сократилось до 2,0%, во второй — до 2,5%, в третьей подгруппе осталось без изменений — 13,3%.
При оценке эффективности различных схем терапии на основе осмотра в зеркалах, УЗИ и эндоскопического исследования было обнаружено существенное уменьшение признаков хронических воспалительных изменений слизистой полости матки после применения Полиоксидония ® как в комплексной, так и в монотерапии.
При сравнительном анализе клеточного звена иммунного статуса сразу после окончания лечения обращает на себя внимание нормализация числа Т-лимфоцитов, восстановление нормального соотношения субпопуляций и, как следствие, нормализация иммунорегуляторного индекса при использовании всех схем терапии.
При использовании Полиоксидония ® наблюдается существенное повышение стимулированной микробицидной активности нейтрофилов, приводящее к повышению коэффициента стимуляции НСТ.
Причем монотерапия Полиоксидонием ® оказывает более выраженный стимулирующий эффект, чем в комплексе с этиотропными химиопрепаратами. Стандартная терапия не оказывает существенного влияния на показатели фагоцитарной активности нейтрофилов.
При анализе показателей гуморального и фагоцитарного звеньев иммунной системы через один месяц после окончания курса лечения отмечаются существенные различия в группах, получавших разные схемы терапии. У пациенток, которым проводилась комплексная терапия, наблюдается нормализация всех показателей. На фоне монотерапии Полиоксидонием ® отмечается увеличение содержания иммуноглобулинов и циркулирующих иммунных комплексов (ЦИК). Стимулированная микробицидная активность у этих пациенток также повышена.
Таким образом, сочетание этиотропной и иммуномодулирующей терапии с применением иммуномодулятора Полиоксидоний ® позволяет достичь выраженной и устойчивой положительной динамики клинической картины, лабораторных и инструментальных методов исследования, показателей всех звеньев иммунного статуса, восстановить репродуктивную функцию достоверно чаще и быстрее, чем при стандартной терапии.
Выводы
Иммунологическая недостаточность при ХРЭ характеризуется преимущественным нарушением Т-клеточного иммунитета, перераспределением иммунорегулирующих субпопуляций, недостаточностью фагоцитарного звена.
Включение в комплексную терапию хронического рецидивирующего эндометрита иммуномодулятора Полиоксидония ® способствует быстрому купированию клинических симптомов, нормализации морфологической структуры и эхографической картины эндометрия, полной элиминации или снижению активности инфекционных агентов и нормализации показателей иммунного статуса, восстановлению репродуктивной функции, что значительно повышает эффективность традиционной терапии.
Хронический эндометрит встречается у женщин преимущественно в репродуктивном возрасте и ведет к нарушению менструальной, секреторной и генеративной функций. На сегодняшний день продолжается активный поиск оптимального и эффективного комплекса мероприятий
Chronic endometritis is common among women in their reproductive age and leads to malfunction of menstrual, secretory and generative function. Currently, active search of optimal and efficient complex of measures for the treatment of this disease is proceeded. All the well-known, including the most modern methods of treatment of chronic endometritis, are presented in this article.
Хронический воспалительный процесс в эндометрии является одной из основных причин невынашивания беременности, бесплодия, неудачных попыток экстракорпорального оплодотворения (ЭКО). Лечение хронического эндометрита представляет собой достаточно сложную, но очень важную задачу, особенно у женщин с бесплодием и репродуктивными потерями в анамнезе [1].
Лечение хронического эндометрита — непростая задача. Сложности ведения больных связаны со следующими причинами. Преобладание стертых форм заболевания и отсутствие специфических клинических симптомов. Хроническое воспаление в любой ткани имеет волнообразно-прогрессирующий характер, поэтому при отсутствии адекватного лечения повреждение ткани во времени (за счет каскада вторичных повреждений) всегда имеет нарастающий характер. Сложности идентификации микробных агентов в эндометрии, особенно при вирусной инвазии, приводят к проблеме выбора этиотропных препаратов. В ходе лечения возможна смена ведущего микробного фактора (например, на представителя условно-патогенной микрофлоры). Элиминация повреждающего агента из эндометрия часто не приводит к самовосстановлению ткани, особенно при длительности заболевания более 2 лет, поэтому с целью устранения каскада вторичных повреждений ткани необходимы целенаправленные терапевтические мероприятия. Контроль эффективности лечебных мероприятий на основании динамики клинических симптомов и неинвазивных методов исследования не дает точных представлений о восстановлении рецептивности эндометрия [2].
Таким образом, лечение хронического эндометрита (ХЭ) должно быть комплексным, этиологически и патогенетически обоснованным, поэтапным и базироваться на результатах максимально тщательного и точного обследования состояния эндометрия. Большинство ученых сходятся во мнении о целесообразности проведения комплексной терапии ХЭ в два этапа [3].
Сущность первого этапа заключается в элиминации повреждающего эндометрий микробного фактора и/или снижении активности вирусной инвазии посредством проведения этиотропной терапии антибиотиками широкого спектра действия, анаэробными средствами и/или противовирусными препаратами [4, 5]. При стерильных посевах эндометрия или невозможности проведения микробиологического исследования у пациенток с признаками ХЭ допустимо проведение эмпирической антибактериальной и противовирусной терапии препаратами широкого спектра действия со сменой групп препаратов в течение нескольких курсов в случае необходимости.
Столкнувшись с проблемой лекарственной резистентности и роста числа нежелательных лекарственных реакций, в последние годы возобновился интерес клиницистов во многих странах мира к использованию фагов с лечебной и профилактической целью. Некоторые предлагают вводить в полость матки поливалентный бактериофаг в сочетании с инфракрасным лазером накожно, что позволяет реализовать антимикробный эффект путем специфического направленного действия на большой спектр возможных возбудителей воспалительного процесса в полости матки в отсутствие значительного системного влияния, а также добиться иммуномодулирующего эффекта, улучшить гемодинамику в органах малого таза и стимулировать рецепторную активность эндометрия [6].
Цель второго этапа лечения ХЭ заключается в восстановлении морфофункционального потенциала эндометрия путем устранения результатов вторичных повреждений ткани — коррекции фиброзирующих и склеротических процессов, последствий ишемии, восстановлении гемодинамики и активности рецепторного аппарата эндометрия. Характер терапии ХЭ на данном этапе зависит от морфологического состояния эндометрия и наличия сочетанной гинекологической патологии. Первый аспект сводится к выраженности воспалительной реакции и наличию обширных участков склероза и/или атрофии в эндометрии, что определяется длительностью течения ХЭ и приводит к нарушению рецептивности эндометрия при продолжительности заболевания более 2 лет.
Научно доказаны морфофункциональные изменения эндометрия у всех женщин с неудачными попытками ЭКО в анамнезе. При обнаружении у таковых совпадений в 3 и более локусах системы генов тканевой совместимости (HLA) II класса целесообразным является проведение подготовительных мероприятий с использованием иммуноглобулинотерапии [7].
Второй этап терапии нередко является продолжительным (2–3 мес), но очень важным, так как позволяет добиться завершения воспалительного процесса — регенерации поврежденной слизистой оболочки тела матки. Для этого используют различные варианты метаболической терапии, преформированные физические и бальнеологические факторы, гормональные препараты, иммуномодуляторы [8–10]. Многие авторы отмечают важность включения в данный этап лечения препарата Лонгидаза, что значительно повышает эффективность терапии и купирование клинической симптоматики [11, 12].
Задачами физиотерапии при ХЭ являются улучшение гемодинамики органов малого таза, стимуляция функции рецепторов, ускорение процессов регенерации эндометрия, повышение иммунологических свойств.
Зарубежные авторы отмечают высокую эффективность в лечении гипопластичного эндометрия внутриматочным введением гранулоцитарного колониестимулирующего фактора (Г-КСФ), препарата Филграстим [19–21]. Механизм его действия в отношении пролиферации и дифференцировки клеток эндометрия до конца не ясен. По имеющимся на сегодняшний день данным, Г-КСФ повышает концентрацию в эндометрии тромбоцитарного фактора роста эндотелиальных клеток, играющего ключевую роль в стимуляции ангиогенеза [22, 23]. Такая же положительная корреляция наблюдалась при изучении концентраций интегрина альфа-V/бета-3. Как известно, интегрины задействованы во всех стадиях имплантации, наибольшая концентрация интегрина альфа-V/бета-3 совпадает с максимальной рецепторной активностью эндометрия. Данный гликопротеин выделяется железистыми эпителиальными клетками после 19?го дня цикла при открытии окна имплантации. В нескольких работах было показано, что недостаток интегрина альфа-V/бета-3 характерен для женщин с тонким эндометрием и встречается также у пациенток, перенесших многочисленные безуспешные попытки ЭКО [24]. Внутриматочные перфузии Г-КСФ сопровождаются увеличением толщины эндометрия в течение 72 часов после применения, что определяет кратность его введения в первой фазе менструального цикла вплоть до овуляции [25–27].
Исследованиями М. Malinova и соавт. уставлен положительный эффект на рост эндометрия в циклах ЭКО у бесплодных женщин вагинального или орального приема вазодилятаторов типа силденафила цитрата совместно с кломифеном цитратом [28, 29].
С целью подготовки эндометрия к программе вспомогательных репродуктивных технологий (ВРТ) и преодоления проблемы недостаточной толщины и рецептивности эндометрия в клиниках мира используются разные методики лечения, такие как гистероскопия с адгезиолизисом, эстрогены, агонисты гонадотропин-релизинг-гормона, Аспирин, витамин Е, пентоксифиллин, L-аргинин, β-блокаторы типа атенолола, глюкокортикоиды и дигидроэпиандростендион [30, 31]. Крайне интересны работы последних лет, связанные с применением антагонистов рецепторов окситоцина, индол-3 карбинола и интерферона [32, 33].
Некоторыми авторами с целью увеличения толщины эндометрия при низком уровне сосудисто-эндотелиального фактора роста (СЭРФ) в сыворотке крови предложено в состав комплексной предгестационной подготовки вводить метилпреднизолон в дозировке 8 мг в сутки с 1?го по 25?й день менструального цикла, что ведет к увеличению уровня СЭРФ и соответственно толщины эндометрия [34].
В последние годы широко изучаются возможности клеточной терапии стволовыми клетками в регенеративной медицине. Одними из наиболее перспективных являются мезенхимальные стволовые клетки, происходящие из костного мозга, пуповинной крови, жировой ткани. Описан новый источник таких клеток — менструальная кровь. Среди преимуществ их использования: доступность, неинвазивный способ получения исходного материала, а также отсутствие иммунных реакций при аллогенном применении. Отсутствие спонтанной трансформации при длительном культивировании клеток — важный фактор, подтверждающий безопасность использования метода.
Появляются работы, посвященные применению эндометриальных мезенхимальных стволовых клеток в лечении синдрома Ашермана. После их введения наблюдалась неоваскуляризация стенки матки, сопровождающаяся утолщением эндометрия, достаточным для успешной имплантации и вынашивания беременности. В случаях отсутствия ответа эндометрия на гормональную терапию внутриматочное введение мезенхимальных стволовых клеток в начале менструального цикла непосредственно после кюретажа может решить задачу роста эндометрия и в последующем способствовать наступлению беременности в программе ЭКО. Подобные публикации пока носят характер описания единичных случаев. Тем не менее следует признать высокий потенциал клеточных технологий в преодолении невосприимчивости тонкого эндометрия и связанных с ней бесплодия и невынашивания беременности.
Важным методом коррекции нарушения трофики является применение прямых метаболических активаторов, что приводит к усилению тканевого обмена, активации энергетических процессов в клетках, устранению последствий гипоксии в ткани, в том числе угнетению анаэробного гликолиза и стабилизации цикла Кребса в аэробных параметрах функционирования. С этой целью используются комплексные метаболические препараты, длительность приема которых должна составлять не менее 3–4 недель. Ярким представителем данной группы препаратов является депротеинизированный гемодериват крови телят.
Аутоплазменное лечение хронического эндометрита нашло широкое применение как в России, так и за рубежом. В нашей стране применяется парацервикальное введение аутоплазмы. Иностранные авторы сообщают об успешном лечении хронического эндометрита при внутриматочном введении PRP-плазмы (Platelet Rich Plasma) [35, 36].
Из нетрадиционных методов лечения хронического эндометрита применяют контрастный массаж, иглорефлексотерапию, йоготерапию. Кроме положительного воздействия последнего метода лечения на эндометрий авторы отмечают снижение депрессии и уровня стресса, что очень важно, так как сам по себе стресс способен провоцировать гемодинамические нарушения, способствовать поддержанию высокого уровня провоспалительных цитокинов в эндометрии [37, 38].
Дискуссионными остаются вопросы о целесообразности использования в комплексном лечении ХЭ циклической гормональной терапии. В настоящее время считается, что при ХЭ оправдано только дифференцированное назначение гормонотерапии при наличии гипофункции яичников или ановуляции [39]. Потенциал к патологической регенерации ткани, который таит в себе хроническое воспаление, при назначении циклической заместительной гормональной терапии может быть усилен и реализован [40]. Хотя некоторые авторы отмечают успешность лечения гипопластичного эндометрия циклическими гормональными препаратами [41–43].
В предполагаемом фертильном цикле, особенно при проведении стимуляции функции яичников, обосновано применение эстрогенных препаратов. При этом трансдермальные формы эстрогенов обладают рядом преимуществ перед оральным приемом эстрадиола ввиду высокой по сравнению с оральным приемом биодоступности, создания постоянной концентрации в кровотоке, отсутствия конверсии в неактивные метаболиты и возможности легкого варьирования дозы. Справедливости ради надо отметить, что препараты эстрадиола могут назначаться и на этапе подготовки к фертильному циклу в случаях, когда причиной тонкого эндометрия является овариальная недостаточность. Эстрогены назначаются по 21?дневной схеме, в течение последних десяти дней их сочетают с прогестинами (дидрогестерон 10–20 мг/сут, микронизированный прогестерон 200 мг/сут, раствор прогестерона 1% — 2 мл или 2,5% — 1 мл внутримышечно через день). Реакция эндометрия в индивидуальных случаях значительно отличается, поэтому возможность увеличивать или уменьшать дозу становится принципиальным фактором успеха подготовки эндометрия к фертильному циклу и обусловливает предпочтение в пользу трансдермальных форм эстрогенов [44–46].
Недостаточная эффективность гормональной терапии эстрогенами объясняется сниженной рецептивностью тонкого эндометрия и сохраняет актуальность поиска дополнительных путей увеличения его роста.
Задача улучшения ростовых функций эндометрия оказывается непростой для решения, так как экзогенные эстрогены усиливают пролиферативные процессы с одновременной активацией воспалительной реакции, что неблагоприятно для последующего наступления и течения беременности.
Критериями эффективности проведенной терапии являются: купирование клинических симптомов заболевания при их наличии, восстановление эхографической картины эндометрия, улучшение васкуляризации эндометрия при допплерометрии сосудов матки, элиминация или снижение активности инфекционного агента, восстановление морфологической структуры эндометрия, восстановление функционального состояния эндометрия, нормализация менструального цикла с полноценной лютеиновой фазой [48].
Проводится контрольная аспирационная биопсия эндометрия на 7–11 день менструального цикла не ранее чем через 2–3 мес после лечения с последующим морфологическим и бактериологическим исследованиями состояния эндометрия.
Хронический эндометрит является клинически значимой нозологической формой с позиций репродуктологии и требует обязательной диагностики и лечения у женщин с патологией репродуктивной системы, а также при использовании программ вспомогательных репродуктивных технологий. Комплексная этиопатогенетическая терапия хронического эндометрита позволяет восстановить нарушенный тканевый гомеостаз и рецептивность эндометрия, что приводит к восстановлению репродуктивной функции.
Литература
Е. В. Козырева* , 1 , кандидат медицинских наук
Л. Ю. Давидян**, доктор медицинских наук, профессор
* ГУЗ УОКБ, Ульяновск
** ФГБОУ ВПО УлГУ, Ульяновск

- бактерии — наиболее частый виновник эндометрита. Выделяются специфичные и неспецифичные возбудители: к первым относятся хламидии, уреаплазмы, бледная трепонема сифилиса, микобактерии туберкулеза, ко вторым — синегнойная и кишечная палочка, стрептококки, стафилококки;
- грибки: чаще заболевание вызывают так называемые актиномицеты на фоне сниженного иммунитета;
- определенные виды вирусов;
- зачастую к развитию болезни приводит столкновение сразу нескольких возбудителей.

Возбудители проникают в матку двумя путями: восходящим и нисходящим. В первом случае бактерии попадают в полость из влагалища через шейку матки. Нисходящий путь бывает гематогенным или лимфогенным: иными словами, если в организме уже запущен какой-то воспалительный процесс, возбудитель попадает в матку через кровь или лимфу.
На развитие и течение воспаления влияет ряд провоцирующих факторов:
- Механическое повреждение (травмы) слизистой: аборты, выскабливание дна матки, кесарево сечение, вагинальные обследования с введением гинекологических инструментов.
- При менструации отторгается поверхностный слой эндометрия и формируется раневая (уязвимая) поверхность. К развитию эндометрита приводит и незащищенный секс во время месячных: заражение проходит по восходящему пути.
- Снижение местного или общего иммунитета на фоне врожденного или приобретенного иммунодефицита: прием иммунодепрессантов, ВИЧ, гиповитаминоз, нарушения питания. В этом случае возможно как восходящее, так и нисходящее заражение.
Другие, не менее опасные факторы — появление в полости матки остатков плаценты после кесарева сечения или родов, а также наличие там децидуальной (отпадающей) ткани, сгустков крови, плодного яйца. Поэтому аборт (особенно в нестерильных условиях) и выскабливание могут привести к воспалению.
Симптомы эндометрита матки
Лейкоциты — клетки иммунной системы — вырабатывают медиаторы воспаления простагландины. Этот процесс проявляется в ряде симптомов:
- у пациенток наблюдается отек, так как повышается проницаемость стенок сосудов, и потому плазма крови выходит в межклеточное вещество;
- боль появляется из-за того, что простагландины раздражают чувствительные нервные окончания и сдавливают их вследствие отека;
- застой крови усиливается в области воспаления из-за сужения (спазма) венозных сосудов и ухудшения оттока крови. Внешне реакция проявляется в виде покраснения воспаленного участка;
- в попытках защититься организм вырабатывает антитела и увеличивает активность лейкоцитов, из-за чего поднимается температура. Подъем только на 0,1° С может усилить активность нашего иммунитета в 10 раз.
При эндометрите проявляется острое либо хроническое воспаления: первое характеризуется яркой симптоматикой, второе нередко протекает бессимптомно. Острый воспалительный процесс чаще связан с воздействием сразу нескольких микроорганизмов. Реже слизистая оболочка поражается изолированно: обычно воспаляется мышечная оболочка матки наравне с развитием миоэндометрита.
При остром эндометрите симптомы проявляются на 3-4 день: повышается температура, наблюдается слабость, головная боль и боль внизу живота, гнойные и (или) кровянистые выделения. Острая стадия длится от 8 до 10 дней и полностью проходит при правильном и своевременном лечении. Если же этого не произошло, острая форма может перетечь в хроническую.
Хронический эндометрит легко не заметить: часто женщины узнают о заболевании только на приеме у гинеколога или при планировании беременности. Наиболее яркий симптом заболевания — нарушение менструального цикла. Температура у пациенток обычно нормальная, иногда бывают ноющие боли в пояснице и внизу живота. Поэтому окончательный диагноз ставится только на основе гистологического исследования эндометрия.
При обсуждении репродуктологии важнее говорить о хроническом эндометрите (ХЭ). Острая патология замечается почти сразу и потому оперативно устраняется. А вот хроническая фаза требует долгого лечения в течение нескольких месяцев, ведь при такой форме заболевания эндометрий сильно видоизменяется, не может трансформироваться и обновляться.
Чаще всего болезнь проявляется у женщин от 26 до 35 лет. Национальный центр контроля заболеваемости сообщает, что каждый год в США регистрируют около 1 млн воспалительных заболеваний органов малого таза. В России такие диагнозы ставятся от 28 до 34 % пациенток гинекологии. При хроническом эндометрите часто развивается бесплодие или привычное невынашивание беременности: до 65 % и до 70 % случаев соответственно. Плодное яйцо не может прикрепиться к измененному эндометрию, из-за чего беременность не наступает или протекает неудачно.
Клинические проявления хронического эндометрита таковы:
- аномальные маточные кровотечения и выделения из половых путей;
- синдром тазовых болей;
- диспареуния (болезненный половой акт);
- бесплодие и/или неудачные ЭКО, привычное невынашивание беременности;
- преждевременные роды.
Однако единого мнения насчет клинической картины хронического эндометрита не существует. Даже при явных симптомах невозможно понять, какова глубина функциональных и структурных изменений эндометрия.

Лечение эндометрита у женщин разного возраста
Симптомы и лечение эндометрита у женщин мало связаны с возрастом. После 40 лет острый эндометрит обычно проявляется более ярко: на это влияют изменения гормонального фона из-за предстоящего климакса. Переход острой формы в хроническую в этом возрасте происходит намного быстрее, однако формат лечения в 25 и 45 лет не различается.
Борьба с заболеванием — сложная, но важная задача, особенно у женщин, переживших выкидыш или неудачное ЭКО. Чтобы поставить точный диагноз и подобрать индивидуальное лечение, врачи МЦРМ собирают детальный анамнез. Необходимо выяснить информацию о менструальной функции, течении и исходе беременностей, абортах и выкидышах. Это позволит верно диагностировать патологию и подготовить эндометрий к беременности с помощью специально подобранных препаратов.
В комплексное лечение входят антибиотики широкого спектра с высокой способностью проникновения в клетку, а также (в зависимости от вида возбудителя) противогрибковые (антимикотики) и противовирусные препараты, местные комбинированные лекарства, системная энзимотерапия (применение ферментов) и физиотерапия в момент реабилитации. Для профилактики кандидоза на фоне антибиотиков назначаются противогрибковые препараты.
Следующий этап — гормональная терапия: комбинированные оральные контрацептивы. Во вторую фазу цикла при планировании беременности врач назначает прогестерон. Лечение начинается с первого дня менструации.
Перед назначением препаратов в нашей клинике проходит комплексная диагностика:
- ультразвуковое исследование органов малого таза;
- гистероскопия — осмотр внутренней оболочки матки (в сочетании с лапароскопией или изолированно);
- исследование эндометрия (получение материала во время гистероскопии, раздельного диагностического выскабливания или аспирационной биопсии);
- иммуногистохимическое и микробиологическое исследование эндометрия;
- ПЦР (фемофлор-скрининг): метод выявит патогенную микрофлору и причины развития воспалительного процесса.
После диагностики мы подбираем индивидуальное лечение. На первом этапе необходимо уничтожить инфекционного агента, на втором — восстановить функционал эндометрия: благодаря лечению устраняются повреждения, завершается регенерация, восстанавливается локальная гемодинамика (движение крови в сосудах) и активность рецепторов эндометрия.
В стенах клиники мы много лет разрабатывали схемы, которые помогают наиболее эффективно бороться с заболеванием. Прежде всего на весь период лечения (два-три менструальных цикла) прописываются следующие препараты:
- Монофазные комбинированные оральные контрацептивы (Ярина, Джес, Жанин, Фемоден и др.).
- Витаминотерапия: Фемибион, Ангиовит или Элевит (одна капсула в сутки).
- Иммунотерапия: Вобэнзим — три капсулы три раза в день за 30 минут до приема пищи.
Препараты в первый месяц лечения:
1. При обнаружении патогена по результатам фемофлор-скриннинга с первого дня менструального цикла назначается антибактериальная либо противовирусная терапия — в зависимости от вида возбудителя. Если в результате фемофлор-скрининга патоген не найден, антибиотики пить не нужно!
2. Также важна поддержка нормальной флоры желудочно-кишечного тракта и влагалища, поэтому:
- первый и последний дни приема антибиотиков назначается Дифлюкан: 150 мг перорально.
- Препараты, регулирующие равновесие кишечной микрофлоры, на выбор:
- Бифиформ — одна капсула 3 раза в день во время еды в течение трех недель,
- Аципол — две капсулы 3 раза в день на протяжении трех недель,
- Энтерол — по одной капсуле 2 раза в сутки 10 дней.
- Лактожиналь — по одной свече во влагалище на ночь в течение двух недель;
- Лактагель — по одному тюбику во влагалище на протяжении двух недель;
- Вагинорм-С — одна вагинальная капсула в течение 12 дней.
Препараты во второй месяц лечения:
1. Активная иммунотерапия: 10 дней после менструации принимается Генферон — 250 тыс. ед. два раза в сутки интравагинально.
2. Препараты, которые активируют обмен веществ в тканях, улучшают трофику (питание клеток) и стимулируют процесс регенерации: Актовегин — одно драже 3 раза в сутки перед приемом пищи на протяжении 30 дней.
3. Физиотерапевтические методы благоприятно влияют на пораженные ткани, помогают снять воспалительные процессы, улучшить состояние сосудов и эндометрия.
Хронический эндометрит и беременность
Как уже было сказано ранее, при хроническом эндометрите часто наблюдается бесплодие или привычное невынашивание беременности. Необходимо, чтобы слой эндометрия постоянно регенерировался: только тогда зародыш будет успешно имплантирован в матку. При хроническом эндометрите регенерация невозможна из-за воспалительного процесса, поэтому плодное яйцо не может закрепиться на эндометрии.
Даже если это происходит, беременность редко оказывается успешной: риск выкидыша сохранится на протяжении вынашивания. Такую беременность сопровождают нарушения и осложнения: в частности, возбудители заболевания могут поразить ткани плода, что приведет к его гибели.
Нарушение развития эмбриона — еще одно возможное последствие беременности при эндометрите. Поврежденному эндометрию не хватает поступления крови из-за застоя: ткань не получает кислород, витамины, питательные вещества и не передает их эмбриону. Из-за этого ребенок может родиться с патологиями. Кроме того в несколько раз повышается вероятность рождения раньше срока, может нарушиться формирование плаценты, так что при планировании беременности следует немедленно начать лечение этого заболевания.
В общей сложности выкидыши и бесплодие из-за хронического эндометрита связаны сразу с несколькими причинами:
- Нарушение морфологии эндометрия, из-за чего оплодотворенная яйцеклетка не закрепляется в матке и выходит вместе с выделениями — в таком случае женщина может даже не знать, что была беременна.
- Проблемы с синтезом прогестерона: этот гормон поддерживает состояние беременности, утолщая эндометрий и подготавливая слизистую матки. При хроническом эндометрите прогестерон вырабатывается слабо, а беременность прерывается на раннем сроке.
- Мужские сперматозоиды инактивируются уже при зачатии. При воспалении фагоцитарные клетки организма уничтожают чужеродные тела, за которые принимают и сперматозоиды.
Поэтому перед планированием беременности необходимо пройти полный курс лечения от эндометрита: в таком случае вероятность забеременеть может возрасти до 100 %. В случае с ЭКО основная проблема связана именно с закреплением половых клеток в матке, поэтому для эффективности стоит сделать несколько попыток подсадить оплодотворенную яйцеклетку. Помимо приема препаратов необходимо поберечь себя: постараться исключить стрессы, ограничить физическую нагрузку и не поднимать тяжести.
Что такое эндометрит? Причины возникновения, диагностику и методы лечения разберем в статье доктора Делеске И. А., гинеколога со стажем в 9 лет.
Над статьей доктора Делеске И. А. работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов и шеф-редактор Лада Родчанина
![Делеске Инна Александровна, гинеколог, гинеколог-эндокринолог - Волгоград]()
Определение болезни. Причины заболевания
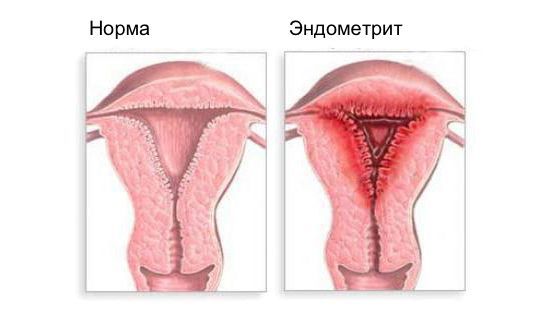
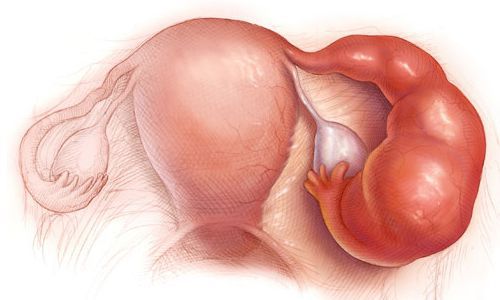
Эндометрит — это воспаление внутреннего слоя матки (эндометрия), которое приводит к изменению его функций. Возникает в результате заражения этой области микробами, вирусами и грибковыми инфекциями.
Эндометрит — одно из наиболее распространенных гинекологических заболеваний. По данным зарубежных источников, распространенность эндометрита составляет 20% в популяции, отечественные авторы указывают до 60-70%, чаще всего болеют женщины репродуктивного возраста [9] [11] . Стабильный рост заболеваемости отмечается последние 20-30 лет [1] [10] . Часто встречается в сочетании с ранним началом половой жизни, отсутствием контрацепции, абортами, наличием хронических воспалительных заболеваний нижнего отдела репродуктивного тракта. [7] [8] .
![Эндометрит и норма]()
Эндометрит часто является причиной бесплодия, привычного невынашивания (два и более выкидыша в анамнезе), нарушения менструального цикла, осложнений беременности, родов и послеродового периода, неудачных попыток ЭКО, гиперпластических заболеваний эндометрия и сексуальных проблем [1] .
Чем эндометрит отличается от эндометриоза
Эндометриоз — это разрастание эндометриоидной ткани. Эндометриоз может поражать полость матки, её оболочки, маточные трубы, яичники, брюшину и области вне половых органов. Эндометритом же называют воспаление внутреннего слоя матки.
Причины эндометрита
В женском репродуктивном тракте присутствуют различные микроорганизмы, среди которых преобладают Lactobacillus spp. Эндометрит чаще ассоциирован с чрезмерным размножением бактерий Enterobacter, Enterococcus, Streptococcus, Staphylococcus, Ureaplasma, Mycoplasma.
Эндометрит вызывают также вирусные инфекционные агенты: вирус герпеса, цитомегаловирус, вирус папилломы человека, энтеровирусы и аденовирусы.
Возможен эндометрит специфической этиологии: гонорейный, туберкулезный, актиномикотический (грибковая инфекция) и неспецифический. [8] [7] [10] .
Риск развития эндометрита увеличивают:
- манипуляции в полости матки — аборты, выскабливания, метросальпингография (контрастное рентгенологическое исследование полости матки и проходимости фаллопиевых труб), введение внутриматочного контрацептива, инсеминация (введение спермы), ЭКО;
- заболевания мочевыделительной системы;
- операции на органах малого таза;
- послеродовые гнойно-воспалительные осложнения;
- другие гинекологические заболевания (хронический сальпингоофорит, цервицит, гиперплазия эндометрия, полип эндометрия);
- частая смена половых партнеров;
- незащищенные половые связи;
- предшествующие прерывания беременности;
- кесарево сечение до 28 недель гестации;
- длительный безводный период в родах;
- ручное отделение плаценты;
- инвазивные исследования для пренатальной диагностики;
- длительное ношение внутриматочного контрацептива.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы эндометрита
Воспаление может протекать в острой и хронической форме. Чаще всего симптомы эндометрита появляются на четвёртый день после инфицирования. При острой форме эндометрита отмечаются общие симптомы воспаления, такие как слабость, быстрая утомляемость, повышение температуры тела, изменения в общем анализе крови (сдвиг лейкоцитарной формулы влево и повышение СОЭ).
К локальным симптомам острого эндометрита можно отнести:
- периодические умеренные или острые тянущие боли внизу живота, иногда отдающие вниз спины и в пах;
- жидкие гноевидные выделения из половых путей с неприятным запахом (возможно с примесью крови);
- диспареуния (боль при половом акте).
При отсутствии правильного и своевременного лечения эндометрита в течении 10 дней возможен переход в хронический воспалительный процесс. При этом держится повышенная температура, появляются новые симптомы:
- нарушение менструального цикла, мажущие кровянистые выделения в середине цикла;
- привычное невынашивание беременности;
- серозно-гнойные выделения из половых путей;
- ноющие боли внизу живота;
- боль во время секса [3][5][8] .
Течение острого послеродового эндометрита более тяжёлое, проявляется в следующих симптомах:
![Лохии]()
Эндометрит при беременности
Эндометрит препятствует имплантации плодного яйца, из-за чего оно может отторгнуться полностью или возникнет нарушение процессов имплантации. В дальнейшем это может привести к выкидышу или замершей беременности.
Если воспалительный процесс усиливается, может развиться хориоамнионит — воспаление плаценты, которое приводит к разрыву плодных оболочек, излитию околоплодных вод и преждевременным родам.
Чтобы избежать возможных осложнений, женщинам с хроническим эндометритом при планировании беременности необходимо пройти комплексное лечение.
Патогенез эндометрита
На начальном этапе воспаления инфекционный агент (бактерии, вирусы или грибки) внедряется в слизистую оболочку матки. Начинается выработка медиаторов воспаления, которая приводит к нарушению микроциркуляции крови в его очаге. Миграция лейкоцитов в зону повреждения, активация нейтрафилов и макрофагов ведёт к активной выработке цитокинов и перекиси водорода, запуску перекисного окисления липидов с повреждением мембран клеток. В это время на фоне повышенной выработки цитокинов и факторов роста происходит деградация матрикса клеток. Нарушение микроциркуляции крови приводит к развитию локальной ишемии и гипоксии ткани, которые затем активируют процессы склерозирования. При длительной стимуляции иммунной системы происходит её истощение и появление аутоиммунных реакций.
В 95% случаев эндометрит является первичным — патогенные микроорганизмы попадают в полость матки восходящим путём, при половом контакте или гинекологических манипуляциях . В 5% случае эндометрит носит вторичный характер: инфекция попадает в эндометрий гематогенным путем, либо же лимфогенным или нисходящим путём (с верхних отделов репродуктивного тракта).
При длительности воспалительного процесса более 2 месяцев можно расценивать его как хронический процесс. Развиваются изменения в структуре и функции ткани, происходит нарушение пролиферации (деления клеток) и физиологической циклической трансформации эндометрия. В связи с этим возможно нарушение нормальной имплантации эмбриона при беременности.
Существует аутоиммунная теория патогенезе хронического эндометрита. Она говорит о том, что при длительном воздействии инфекционного агента на иммунную систему происходит вторичное повреждение эндометрия. При этом нарушается процесс апоптоза (запрограммированной гибели клетки) [11] .
Классификация и стадии развития эндометрита
Эндометрит можно разделить на острую и хроническую форму.
Острый эндометрит возникает при абортах, диагностических манипуляциях, выскабливании, развивается быстро, воспаление сопровождается острыми или ноющими болями и повышением температуры. Наиболее частый путь инфекции при нём — восходящий. Распространение инфекции из влагалища в верхние отделы репродуктивного тракта происходит при несостоятельности барьера шейки матки. Воспаление может локализоваться в эндометрии, а также переходить на миометрий. При несвоевременном и неполноценном лечении возможно развитие пельвиоперитонита (воспаление оболочки брюшины в области малого таза).
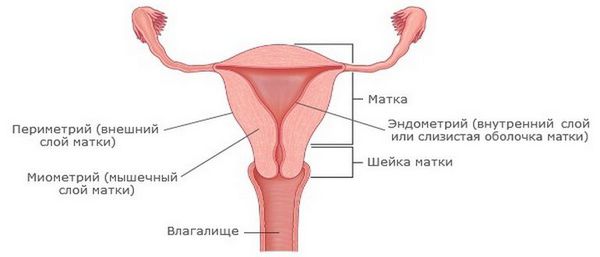
Отдельно выделяется острый послеродовый эндометрит — начинается на 2-4 сутки после родов, ему может предшествовать хориоамнионит (инфицирование оболочек плода и жидкости).
![Строение матки]()
При хроническом эндометрите симптоматика сглажена. Характерны периодические обострения и рецидивы после переохлаждения и воспаления другой локализации урогенитального тракта.
По клиническим проявлениям эндометрит подразделяется на клиничеcки выраженную и субклиническую форму.
По характеру воспалительного процесса эндометрит можно разделить на:
- Катаральную форму (поражение поверхностных слоев слизистой оболочки матки и выделение слизистого экссудата).
- Катарально-гнойную форму.
- Гнойную форму.
- Некротическую форму.
- Гангренозную форму.
По морфологическим признакам:
- Атрофический эндометрит — наблюдается атрофия желез эндометрия, фиброз стромы, инфильтрация лимфоидными элементами;
- Кистозный эндометрит — сдавление протоков желез фиброзной тканью, образование кистозных элементов в эндометрии;
- Гипертрофический эндометрит — характеризуется гипертрофией желез эндометрия в результате хронического воспаления [5] .
Осложнения эндометрита
Осложнения у эндометрита могут быть достаточно серьёзными.
Метротромбофлебит (тромбоз тазовых вен) развивается через 2-3 недели от начала заболевания эндометритом. Пациентки отмечают общие симптомы воспаления, сохраняющуюся повышенную температуру тела, тянущие или острые боли внизу живота, выделения из половых путей [1] [2] .
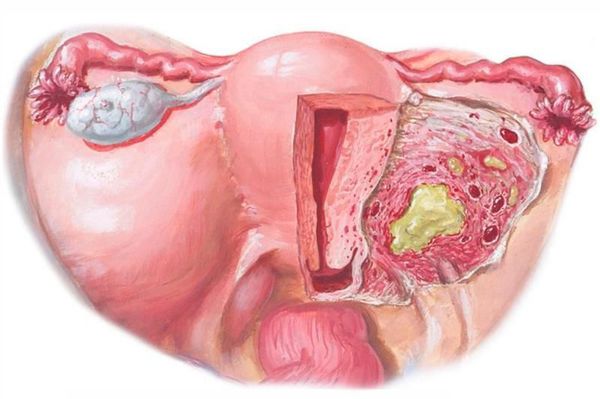
Параметрит — воспаление околоматочной клетчатки. После внедрения инфекционного возбудителя в параметрий возможно образование диффузного воспалительного инфильтрата. При отсутствии лечения происходит нагноение и переход в хроническое течение. При переходе на всю клетчатку развивается пельвиоцеллюлит (воспаление клетчатчки малого таза) [2] [9] [10] .
![Параметрит]()
Пельвиоперитонит — воспаление выходит за пределы матки, в процесс вовлекаются листки брюшины. Пациентки отмечают резкое повышение температуры, симптомы интоксикации, тошноту, рвоту, интенсивные боли внизу живота (основная локализация ниже пупка), симптом раздражения брюшины ( резкое усиление боли в животе при быстром надавливании и снятии руки).
Сальпингоофорит — воспалительный процесс в маточных трубах и яичнике. Наиболее частые осложнения при несвоевременном лечении: пиовар (гнойное воспаление яичника) и туюоовар (формирование единого гнойного конгламерата из воспаленного яичника и маточной трубы). Все вышеперечисленные осложнения требуют оперативного лечения [2] [9] [10] .
![Сальпингоофорит]()
Другими осложнениями могут быть бесплодие, нарушение менструального цикла, выкидыши, внематочная беременность, спаечный процесс в малом тазу [1] [2] [3] .
В некоторых случаях возникает септический шок — угрожающее жизни осложнение, в условиях которого критически нарушается кровоснабжение тканей и клеточный метаболизм. Главные симптомы сепсиса — высокие показатели температуры тела, симптомы интоксикации, снижение давления и тахикардия, изменения в общих анализах крови, обильное потоотделение, спутанность сознания [8] [9] .
Диагностика эндометрита
Диагностика хронического эндометрита должна быть основана на комплексном подходе анализа жалоб пациентки, анамнеза, симптомов, результатов эхографических исследований, лабораторной диагностики, данных морфологического исследования эндометрия и иммунного статуса.
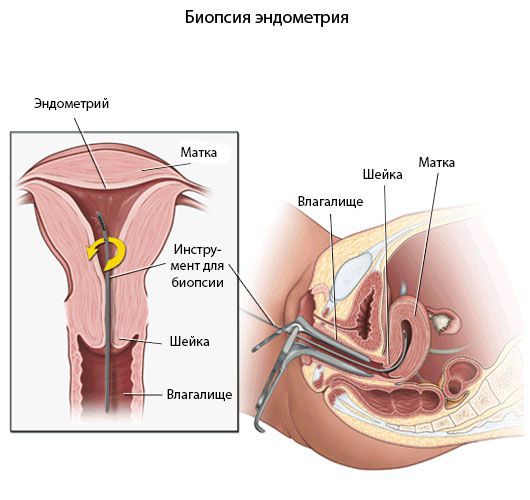
Пайпель-биопсия эндометрия
Хронический эндометрит диагностируют прежде всего с помощью морфологического исследования [8] .
Гистологический материал получают при выскабливании стенок полости матки под контролем гистероскопа или пайпель-биопсии. Пайпель-биопсия — это получение гистологического материала с помощью тонких канюль при аспирации (удалении) эндометрия. Данный метод имеет большую диагностическую ценность в амбулаторных условиях.
![Пайпель-биопсия]()
Критериями хронического эндометрита является наличие очаговых или диффузных лимфоидных инфильтратов, склероз стенок спиральных артерий, фиброз стромы и наличие плазматических клеток. При этом к абсолютным признакам хронического эндометрита относят плазматические клетки.
Микробиологическое исследование
Микробиологические посевы используются для выявления возбудителя воспалительного процесса.
Иммуногистохимическое исследование
Иммуногистохимическое исследование при эндометрите заключается в исследовании биоптата слизистой оболочки матки с целью определения мембранного белка, который является маркером плазматических клеток. Информативность гистологического исследования при этом возрастает до 85-90%, можно установить и иммунный характер повреждения эндометрия [5] [7] [8] .
УЗИ при эндометрите
При эхографии (УЗИ) хронический эндометрит определяют по:
- изменениям в структуре эндометрия;
- участкам повышенной эхогенности различной формы и величины в зоне М-Эхо;
- наличию сниженной эхогенности в эндометрии;
- наличию жидкости в полости матки;
- присутствию мелких кальцинатов 1-3 мм в эндометрии;
- участкам фиброза в эндометрии разной степени;
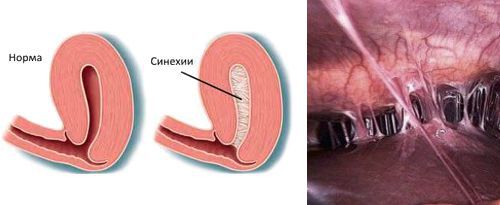
- наличию внутриматочных синехий.
![Внутриматочные синехии]()
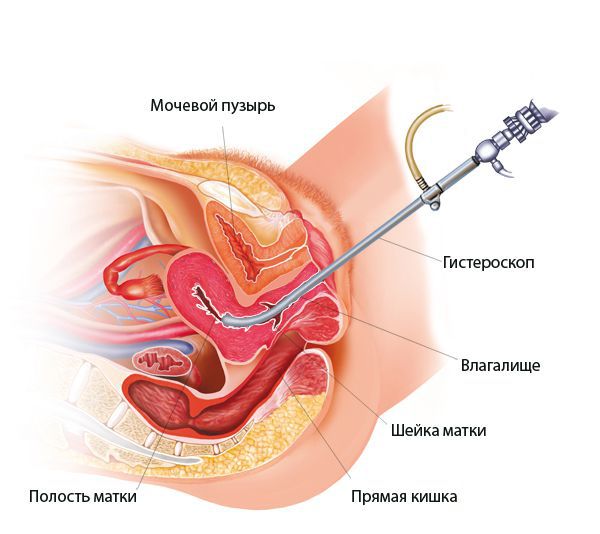
Гистероскопия при эндометрите
При гистероскопии определяются следующие признаки хронического эндометрита: гиперемия слизистой оболочки матки, неровномерная толщина эндометрия, полипообразные образования, кровоизлияния, очаговая гиперплазия эндометрия.
![Гистероскопия]()
Лечение эндометрита
Лечение эндометрита на первом этапе заключается в устранении бактериального или грибкового возбудителя, а для эндометрита вирусной этиологии — снижении вирусной нагрузки [7] . Для этого проводят комплексное лечение, включающее в себя антибактериальную терапию, анаэробные средства, противовоспалительные и противовирусные лекарственные средства [5] [6] [8] .
Второй этап заключается в восстановлении рецептивности эндометрия и его функциональности. Успешное восстановление рецепторного аппарата эндометрия должно происходить без снижения пролиферации (размножения, разрастания) клеток. Устраняются последствия ишемии, склеротические процессы, восстановливается отток крови. Длительность и объёмы терапии зависят от тяжести воспалительного процесса и сопутствующей гинекологической патологии. После проведения основных этапов лечения необходим курс реабилитации (физио-терапевтическое лечение) [7] [8] [10] .
Иммуностимулирующую терапию применяют при комплексном лечении хронического эндометрита, если выявлена вирусная инфекция: вирус папилломы человека, герпеса, Эпштейна — Барр, цитомегаловирус.
Гормональную терапию используют для подготовки эндометрия, чаще всего перед ЭКО. Для применения гормональных препаратов необходимо гистологическое подтверждение патологии эндометрия.
Контрольные критерии эффективности терапии хронического эндометрита:
- допплерометрическое исследование сосудов матки с ЦДК во 2 фазу менструального цикла;
- определение ангиогенных факторов;
- клиническое улучшение.
Рекомендации по диагностике и лечении эффективны лишь у половины больных, а частота рецидивов остается на уровне 25 % [13] .
Прогноз. Профилактика
При своевременном и полноценном лечении прогноз благоприятный. Пациентки отмечают улучшение состояния в течении двух суток. При запоздалом лечении эндометрита возможно развитие септического шока.
Читайте также: