Противовирусные препараты при гнойничках
Обновлено: 23.04.2024
Фурункулы – это болезненные, воспаленные, заполненные гноем полости в коже. Размер фурункула может быть от горошинки до грецкого ореха. Хотя фурункулы могут возникать на любом участке тела, чаще всего они возникают в тех областях, где есть волосяной покров и где происходит трение, например: шея, подмышки, пах, лицо, грудь, ягодицы и т.д.
Карбункулы – это особенно крупные фурункулы или несколько рядом расположенных фурункулов, которые обычно более глубокие и болезненные. При подозрении на карбункул обязательно проконсультируйтесь с врачом, т.к. воспаление может проникнуть в кровоток, и тогда вам могут понадобиться антибиотики.
Причины возникновения фурункула
Фурункулы возникают, когда бактерии проникают в волосяной фолликул. Кожная ткань вздувается и появляется красная, наполненная гноем, болезненная припухлость. Пока фурункул не вскроется и не опорожнится (содержащийся в нем гной не выйдет), фурункул будет болеть, и к нему будет неприятно прикасаться.
Cимптомы
Если у фурункула не формируется головка или не наблюдается улучшения в течение трех дней, или если фурункул очень болезненный, с большим количеством гноя, если возникающая боль мешает движению, или если фурункул возник в области лица, позвоночника или в ректальной зоне, если при этом повышается температура или видны красные полоски, расходящиеся от фурункула (лимфангит), а также при частом появлении (фурункулез) даже небольших фурункулов следует обязательно обратиться к врачу
Осложнения
- распространение фурункулов на другие части тела;
- септицемия (заражение крови).
Что можете сделать Вы
Мойте руки с антибактериальным мылом, прежде чем прикасаться к фурункулу и после контакта с фурункулом (неважно, с ранкой или гнойной головкой).
Мягко нанести на пораженную область антибактериальное средство 3-4 раза в день. Наложите теплый компресс на 15 минут 3-4 раза в день для облегчения боли и ускорения созревания гнойной головки. Затем следует закрыть фурункул толстым слоем марли и держать повязку сухой. Ни в коем случае не царапайте и не ковыряйте фурункул, не выдавливайте и не вскрывайте фурункул самостоятельно, т.к. это может разнести инфекцию. Если фурункул открылся сам, осторожно удалите гной, затем тщательно обработайте это место перекисью водорода. Потом наложите сухую повязку. Повторяйте процедуры каждый день до полного заживления. Примите обезболивающее, чтобы облегчить боль и уменьшить воспаление. Не используйте безрецептурные препараты (кремы, мази), содержащие антибиотики без консультации врача. Никогда не пытайтесь сами вскрыть фурункул без разрешения врача.
Тщательно мойте руки перед приготовлением пищи, т.к. бактерии из фурункула могут вызвать заражение пищи. Диабетикам при возникновении фурункула следует немедленно обратиться к врачу.
Что может сделать врач для лечения фурункула
Ваш врач может вскрыть фурункул, сделав небольшой надрез хирургическим лезвием, так, чтобы гной мог выйти, удалить гной и наложить сухую повязку. При необходимости выписать подходящие антибиотики (в т.ч. и мази). При частых фурункулах (фурункулез) назначить анализы (в т.ч. чтобы убедиться, что у вас нет сахарного диабета).
Профилактические меры
Принимайте ванну или душ хотя бы раз в день. Не царапайте зудящее место на коже, т.к. это может спровоцировать попадание инфекции в поврежденное место.
Наносите антисептический лосьон, чтобы не допустить попадания инфекции.
Р-р д/местн. и наружн. прим. масляный 20%: 5 мл, 10 мл, 15 мл, 20 мл, 30 мл или 50 мл фл., 15 мл, 20 мл или 25 мл фл.-капельн.
М.А.Гомберг, д.м.н., профессор, А.М.Соловьев, к.м.н., доцент, МГМСУ, Москва
В последнее время папилломавирусная инфекция привлекает особое внимание в связи с ролью этой группы вирусов в развитии рака. В 2008 г. Нобелевской премией по медицине было отмечено доказательство того, что некоторые типы вируса папилломы человека (ВПЧ) способны вызывать рак шейки матки. По Handley J.M., et al. (1994), к ВПЧ-поражениям относят: клинические формы — аногенитальные бородавки (остроконечные кондиломы, вульгарные бородавки), симптоматические внутриэпителиальные неоплазии на ранних стадиях при отсутствии дисплазии (плоские кондиломы); субклинические формы — бессимптомные внутриэпителиальные неоплазии при отсутствии дисплазии; латентные формы (отсутствие морфологических или гистологических изменений на фоне обнаружения ДНК ВПЧ).
Лечение аногенитальных ВПЧ-поражений, согласно существующим принципам по ведению больных с клиническими проявлениями, связанными с ВПЧ, должно быть направлено на разрушение тем или иным методом папилломатозных очагов, возникающих на месте внедрения вируса. Во всех основных рекомендациях по ведению больных с ВПЧ-инфекцией — CDC, Европейских рекомендациях, рекомендациях ВОЗ, и в том числе в рекомендациях РОДВ, приведен именно такой подход.
Роль вирусов папилломы человека (ВПЧ) в развитии множества доброкачественных и злокачественных новообразований кожи и слизистых оболочек не вызывает сомнений. Полагают, что все 500тыс. случаев рака шейки матки, ежегодно диагностируемые в мире, вызваны генитальной ВПЧ-инфекцией (Bulletin Word Health Organization, 2007).
В различных клинических рекомендациях и протоколах подробно описываются методы лечения именно клинических проявлений ВПЧ, но обходится стороной вопрос так называемого вирусоносительства или бессимптомного выделения вируса. Причем вопросу тактики врача при бессимптомном выделении вируса у пациента ВПЧ уделяется мало внимания не только в практических рекомендациях, но и в научно-исследовательской литературе.
Мы предлагаем свой подход к этой проблеме.
Прежде всего мы исходим из того, что наш долг — ставить во главу угла интересы пациента. Если он встревожен наличием ВПЧ и желает избавиться от этой инфекции, мы должны постараться успокоить его и обсудить все имеющиеся в настоящее время возможности лечения. В противном случае нам будет трудно рассчитывать на доверие с его стороны.
Мы считаем, что такое обсуждение должно состоять из 3 частей.
1. Информирование пациента относительно характера течения и последствий инфекции.
2. Методы профилактики рака шейки матки (при выявлении вируса у женщин).
3. Возможности воздействия на ВПЧ с целью его элиминации.
1. ИНФОРМИРОВАНИЕ ПАЦИЕНТА
При первом же визите необходимо рассказать человеку о возможных рисках, связанных с инфицированием ВПЧ. Однако консультирование нужно проводить очень осторожно, чтобы не спровоцировать у человека развитие психоневроза и канцерофобии.
Пациент с выявленным ВПЧ должен знать о своей потенциальной заразности для неинфицированных лиц, поэтому ему надо рекомендовать использовать презерватив при половых контактах и обязательно информировать своего полового партнера о вирусоносительстве.
Следует проинформировать пациентов о том, что возможно самостоятельное исчезновение ВПЧ. Известно, что у лиц более молодого возраста вероятность исчезновения вируса с течением времени выше, чем у лиц старше 25 лет.
2. ПРОФИЛАКТИКА РАКА ШЕЙКИ МАТКИ (ПРИ ВЫЯВЛЕНИИ ВИРУСА ПАПИЛЛОМЫ ЧЕЛОВЕКА У ЖЕНЩИН)
Всем женщинам, инфицированным ВПЧ, следует провести кольпоскопическое исследование, в том числе с окраской раствором Люголя или раствором уксусной кислоты, а также цитологические тесты по Папаниколау. Периодичность обследований обсуждается с гинекологом в зависимости от степени онкогенности выявленных вирусов и результатов кольпоскопии и цитологии. Цитологические исследования следует проводить не реже, чем 1 раз в 6 месяцев. Для женщин старше 26 лет этот подход является практически единственным способом профилактики рака шейки матки.
Имеются публикации об эффективности российского препарата индинол для профилактики рака шейки матки у женщин, инфицированных ВПЧ. Однако контролированных плацебо-исследований не проводилось.
3.ВОЗДЕЙСТВИЕ НА ВПЧ
Наиболее дискуссионным является вопрос о воздействии на выделение вируса, поэтому остановимся на нем подробнее. Врач, безусловно, должен информировать пациента о том, что в настоящее время нет методов, позволяющих достоверно и с высокой степенью вероятности устранить вирус из организма.
Необходимость проведения лечебных мероприятий обсуждается индивидуально с каждым пациентом. Желательно, чтобы врач принимал решение о проведении лечения с целью устранения ВПЧ в отсутствие клинических проявлений только после подписания пациентом информированного согласия, во избежание возможных последующих недоразумений.
Теоретически, учитывая локализацию вируса в эпителиальных клетках и то, что происходит постоянное слущивание эпителия, можно предположить, что ВПЧ может исчезнуть вместе со старыми эпителиальными клетками. Видимо, именно этим объясняются случаи самопроизвольного исчезновения ВПЧ. Между тем очевидно, что элиминации ВПЧ из организма с гораздо большей эффективностью можно добиться при активизации противовирусного иммунитета, ингибирующего размножение ВПЧ и его внедрение в другие клетки. Доказать возможность достижения такого результата на практике можно только путем проведения соответствующих специальных исследований.
Потенциально возможны 3 способа инфицирования: от матери к ребенку (трансплацентарно; во время родов, в том числе путем кесарева сечения; возможно — через слюну или грудное молоко), посредством передачи вируса воздушно-капельным или контактно-бытовым путями. Cчитается, что ВПЧ-инфекция передается в основном половым путем, что объясняет ее широкую распространенность среди сексуально активного населения. В частности, в США ежегодно диагностируют 6,2 млн новых случаев генитальной ВПЧ-инфекции (Steinbrook R., 2006).
Повышение функциональной эффективности противовирусного иммунитета является основным способом, который предположительно может помочь в устранении вируса из организма или уменьшить его активность. Этого можно достичь как неспецифическими, так и специфическими методами.
К неспецифическим относят различные способы укрепления защитных сил организма, так называемый здоровый образ жизни: правильное питание, профилактический прием витаминов, биологически активных добавок.
Отдельный вопрос — проведение гомеопатического лечения. Но поскольку об этих способах часто упоминается в научно-популярной литературе, в рамках данной статьи мы их комментировать не будем.
Установлено, что при применении интерферонов снижается количество вирусной ДНК (по данным ПЦР) у пациентов в очагах поражения [Arany I., et al., 1995].
Интерферон применяют местно и системно (подкожно, внутримышечно, внутривенно или ректально).
В большинстве исследований была показана невысокая эффективность наружного применения интерферона [Keay S., et al, 1988] при наличии клинических проявлений, а при лечении больных с субклиническими очагами ВПЧ-инфекции и цервикальных неоплазиях (ЦИН) были получены обнадеживающие результаты [Gross G., 1996].
По данным различных авторов, при системном применении альфа-интерферона в дозе от 1,5 до 3 млн МЕ внутримышечно или подкожно через день в течение 4 недель в качестве монотерапии у 11—100% пациентов наблюдается полное исчезновение бородавок [Gross G., et al., 1986; Zwiorek L., et al., 1989], что свидетельствует о возможном ингибирующем влиянии препаратов интерферонов на ВПЧ.
При системном применении интерферонов побочными эффектами обычно являются гриппоподобные состояния, выраженность которых зависит от полученной дозы [Handley, et al., 1994]. Эти побочные явления можно ослабить приемом нестероидных противовоспалительных препаратов.
Считается возможным самостоятельное исчезновение ВПЧ. Известно, что у лиц более молодого возраста вероятность исчезновения вируса с течением времени выше, чем у лиц старше 25 лет.
На российском рынке представлен широкий выбор интерферонов различных производителей, как отечественных, так и зарубежных, — генферон, виферон, кипферон, реаферон, роферон-А, интрон А, реальдирон и т.д. Предпочтительнее назначать рекомбинантные, а не человеческие интерфероны.
При назначении интерферонов надо учитывать не только частые побочные реакции, но и то, что их введение может подавлять синтез собственных эндогенных интерферонов. Поэтому в отсутствие клинических проявлений интерфероны применяют только в том случае, когда о целесообразности такого назначения свидетельствуют результы исследования иммунного статуса. Следует также отметить и высокую стоимость качественных препаратов интерферона.
Воздействовать на противовирусный иммунитет можно с помощью индукторов эндогенного интерферона и других активаторов иммунитета. На российском фармацевтическом рынке представлено много иммуноактивных препаратов, которые, согласно инструкции производителя или рекомендациям исследователей, можно применять для комбинированного лечения аногенитальных бородавок (в сочетании с различными деструктивными методами). На основании этого их можно рекомендовать для противовирусной терапии при отсутствии клинических проявлений.
Гепон — синтетический олигопептид, состоящий из 14 аминокислотных остатков, относится к группе иммуномодуляторов. Препарат показан для повышения эффективности иммунной защиты от инфекций, лечения и профилактики оппортунистических инфекций, вызванных бактериями, вирусами или грибами. Гепон оказывает иммунофармакологическое и противовирусное действие:
У больных с ослабленной иммунной системой гепон:
Так, например, после удаления очагов ВПЧ-поражений любым деструктивным методом, аппликации гепона (от 3 до 6 аппликаций через день) позволяют ускорить процесс заживления и снизить уровень рецидивирования. Системно препарат применяют по 2 мг перорально 3 раза в неделю. Курс можно повторять с интервалом в 1 неделю [Соловьев А.М., 2003].
Изопринозин (инозин пранобекс) — противовирусное средство с иммуномодулирующими свойствами. Препарат, индуцируя созревание и дифференцирование Т-лимфоцитов и Т1-хелперов, потенцируя индукцию лимфопролиферативного ответа в митогенных или антиген-активных клетках, нормализует дефицит или дисфункцию клеточного иммунитета. Изопринозин моделирует цитотоксичность Т-лимфоцитов и натуральных киллеров, функцию Т8-супрессоров и Т4-хелперов, а также повышает количество иммуноглобулина G и поверхностных маркеров комплемента. Препарат повышает синтез интерлейкина-1 (ИЛ-1) и интерлейкина-2 (IL-2), регулирует экспрессию рецепторов IL-2, существенно увеличивает секрецию эндогенного γ-интерферона и уменьшает продукцию интерлейкина-4 в организме. Изопринозин усиливает действие нейтрофильных гранулоцитов, хемотаксис и фагоцитоз моноцитов и макрофагов. Кроме этого, он оказывает прямое противовирусное действие, угнетая синтез вирусов путем встраивания инозин-оротовой кислоты в полирибосомы пораженной вирусом клетки и нарушая присоединение адениловой кислоты к вирусной и-РНК. Одним из показаний для применения препарата являются инфекции, вызванные вирусом папилломы человека: остроконечные кондиломы, папилломавирусная инфекция вульвы, вагины и шейки матки (в составе комплексной терапии).
Для женщин старше 26 лет цитологическое исследование слизистой шейки матки, проводимое 2 раза в год, является практически единственным способом профилактики рака шейки матки.
В литературе описаны различные схемы и результаты применения изопринозина.
При инфекциях, вызванных ВПЧ, изопринозин назначают по 3 г/сут (2 таблетки 3 раза в сутки) как дополнение к местной терапии или хирургическому вмешательству на протяжении 14—28 дней для пациентов с низкой степенью риска или 5 дней в неделю последовательно в течение 1—2 недель в месяц в течение 3 мес для пациентов с высокой степенью риска.
Известно о зарубежном опыте применения инозин пранобекса в качестве терапии, дополняющей деструкцию аногенитальных бородавок [Davidson-Parker J., et al., 1988]. Препарат назначали по 1 г 3 раза в сутки в течение 14—28 дней.
В работе Забелева А.В. и соавт. (2005) показано исчезновение атипичного эпителия у женщин с ВПЧ-ассоциированными плоскоклеточными интраэпителиальными поражениями низкой степени после проведения курсов лечения изопринозином. Препарат назначали по 1 грамму 3 раза в сутки в течение 5 дней, 3 курса с интервалом в 1 месяц. В исследовании, проведенном Sun Kuie Tay (1996), показаны аналогичные результаты — улучшение морфологической картины эпителия вульвы. Инозин пранобекс назначали по 1 г 3 раза в сутки в течение 6 недель. Положительный эффект был достигнут у 63,5% больных, тогда как в группе, принимавшей плацебо, только у 16,7%. О прекращении выделения ВПЧ у 65,6% больных после проведения комбинированной терапии (изопринозин + деструкция очагов) ЦИН низкой степени сообщает Прилепская В.Н. (2007). При использовании только деструкции очагов этот результат был достигнут у 46,9% больных. Изопринозин назначали за 7—10 дней до проведения деструкции по 1 г 3 раза в сутки в течение 5 дней. В исследовании Шевниной И.В. (2009) показаны похожие результаты — прекращение выделения ВПЧ у 77% больных при комбинированной терапии женщин с ЦИН и аногенитальными бородавками. Изопринозин назначали по 1 г 3 раза в сутки в течение 10 дней, затем по 0,5 г 3 раза в сутки в течение 20 дней.
Для решения поднятой в этой статье проблемы интересным является факт прекращения обнаружения ВПЧ из очагов поражения в ходе проводимой комбинированной терапии с применением иммуномакса. При проведении вирусологического обследования пациентов до лечения в среднем у 70% выявлялся ВПЧ в очагах поражения. После проведенного комбинированного лечения в ходе контрольного наблюдения у 45% больных было отмечено прекращение выделения ВПЧ [Перламутров Ю.Н. и соавт., 2003]. Полученные результаты свидетельствуют, что проведение терапии иммуномаксом влияет на противовирусный иммунитет и приводит к прекращению не только рецидивов, но и выделения ВПЧ из очагов поражения. В связи с этим в перспективе иммуномакс можно будет использовать не только для лечения остроконечных кондилом, но и для предотвращения вирусовыделения у больных без клинических проявлений инфекции.
ПРОТИВОВИРУСНЫЕ ПРЕПАРАТЫ С ИММУНОМОДУЛИРУЮЩИМ ДЕЙСТВИЕМ
Панавир — растительный полисахарид, полученный из растения Solanum tuberosum, относится к классу высокомолекулярных гексозных гликозидов сложного строения с молекулярной массой 1000 кД. В настоящее время в России он является одним из самых популярных препаратов, использующихся для противовирусной терапии. Причем лечение папилломавирусной инфекции является лишь одним из показаний к его применению.
После однократной инъекции панавира в 2,7—3 раза повышается уровень лейкоцитарного интерферона, что соответствует воздействию терапевтических доз интерферона [Колобухина и соавт., 2005].
Повышение функциональной эффективности противовирусного иммунитета является основным способом, который предположительно может помочь в устранении вируса из организма или уменьшить его активность.
Со степенью распространенности неопластического процесса связывают эффективность препарата в отношении прекращения вирусовыделения [Иванян А.Н. и соавт., 2004]. Так, после проведения комплексного лечения у пациенток с 1-й степенью распространенности процесса вирус не выявлялся в 90,5%, при 2-й степени — в 71,1%, при 3-й степени — в 39,6%, при 4-й степени — в 9,4% случаев. Достоверное снижение вирусной нагрузки с 398,2 RLU до 176,2 RLU (p<0,05) через 1 месяц после окончания монотерапии панавиром ВПЧ-инфекции отмечает Мелехова Н.Ю. (2005).
Продолжаются исследования противовирусной активности панавира с целью установления мишени, объясняющей его высокую противовирусную активность, а также по расширению показаний к его применению. Но уже сейчас можно говорить о том, что он является одним из наиболее перспективных противовирусных агентов с доказанным иммуномодулирующим действием.
В этой статьей мы начали дискуссию о целесообразности попытки устранения папилломавирусной инфекции при отсутствии ее клинических проявлений. Существующие рекомендации по наблюдению таких пациентов могут не удовлетворить тех из них, которые хотели бы получить квалифицированную помощь в устранении этой инфекции. Поэтому мы предлагаем 3-х этапную тактику ведения таких больных: консультирование, цитологический контроль у женщин и использование противовирусных препаратов с иммуномодулирующим действием.
Действующее вещество: осельтамивира фосфат - 39,4 мг (в пересчете на осельтамивир - 30,0 мг).
Вспомогательные вещества: крахмал кукурузный прежелатинизированный, повидон К30, натрия кроскармеллоза, тальк, натрия стеарилфумарат.
Капсула твердая желатиновая № 4:титана диоксид, желатин.
1 капсула 45 мг содержит :
Действующее вещество: осельтамивира фосфат - 59,1 мг (в пересчете на осельтамивир - 45,0 мг).
Вспомогательные вещества: крахмал кукурузный прежелатинизированный, повидон К30, натрия кроскармеллоза, тальк, натрия стеарилфумарат.
Капсула твердая желатиновая № 3: титана диоксид, желатин.
1 капсула 75 мг содержит :
Действующее вещество: осельтамивира фосфат - 98,5 мг (в пересчете на осельтамивир - 30,0 мг).
Вспомогательные вещества: крахмал кукурузный прежелатинизированный, повидон К30, натрия кроскармеллоза, тальк, натрия стеарилфумарат.
Капсула твердая желатиновая № 1: титана диоксид, желатин.
Описание
Твердые капсулы, корпус и крышечка капсулы непрозрачные, от белого или почти белого цвета до белого с желтоватым оттенком цвета.
Содержимое капсул - порошок или уплотненная порошковая масса от белого или почти белого цвета до белого с желтоватым оттенком цвета.
Фармакотерапевтическая группа
Код АТХ
Фармакодинамика:
Механизм действия
Противовирусный препарат. Осельтамивир является пролекарством его активный метаболит (осельтамивира карбоксилат ОК) - эффективный и селективный ингибитор нейраминидазы вирусов гриппа типа А и В - фермента катализирующего процесс высвобождения вновь образованных вирусных частиц из инфицированных клеток их проникновения в неинфицированные клетки эпителия дыхательных путей и дальнейшего распространения вируса в организме.
Тормозит рост вируса гриппа in vitro и подавляет репликацию вируса и его патогенность in vivo уменьшает выделение вирусов гриппа А и В из организма. Концентрация ОК необходимая для ингибирования нейраминидазы 50% (IC50) составляет 01-13 нМ для вируса гриппа А и 26 нМ для вируса гриппа В. Медиана значений IC50 для вируса гриппа В несколько выше и составляет 85 нМ.
Клиническая эффективность
В проведенных исследованиях осельтамивир не оказывал влияния на образование противогриппозных антител в том числе на выработку антител в ответ на введение инактивированной вакцины против гриппа.
Исследования естественной гриппозной инфекции
В клинических исследованиях проведенных во время сезонной инфекции гриппа пациенты начинали получать осельтамивир не позднее 40 ч после появления первых симптомов гриппозной инфекции. 97% пациентов были инфицированы вирусом гриппа А и 3% пациентов - вирусом гриппа В. Осельтамивир значительно сокращал период клинических проявлений гриппозной инфекции (на 32 ч).
У пациентов с подтвержденным диагнозом гриппа принимавших осельтамивир тяжесть заболевания выраженная как площадь под кривой для суммарного индекса симптомов была на 38% меньше по сравнению с пациентами получавшими плацебо.
Более того у молодых пациентов без сопутствующих заболеваний осельтамивир снижал примерно на 50% частоту развития осложнений гриппа требующих применения антибиотиков (бронхита пневмонии синусита среднего отита).
Были получены четкие доказательства эффективности препарата в отношении вторичных критериев эффективности относящихся к антивирусной активности: осельтамивир вызывал как укорочение времени выделения вируса из организма так и уменьшение площади под кривой "вирусные титры-время".
Данные полученные в исследовании по терапии осельтамивиром у пациентов пожилого и старческого возраста показывают что прием осельтамивира в дозе 75 мг 2 раза в сутки в течение 5 дней сопровождался клинически значимым уменьшением медианы периода клинических проявлений гриппозной инфекции аналогичным таковому у взрослых пациентов более молодого возраста однако различия не достигли статистической значимости.
В другом исследовании пациенты старше 13 лет больные гриппом имевшие сопутствующие хронические заболевания сердечно-сосудистой и/или дыхательной систем получали осельтамивир в том же режиме дозирования или плацебо. Отличий в медиане периода до уменьшения клинических проявлений гриппозной инфекции в группах осельтамивир и плацебо не было однако период повышения температуры при приеме осельтамивира сокращался примерно на 1 день.
Доля пациентов выделяющих вирус на 2-ой и 4-ый день становилась значительно меньше. Профиль безопасности осельтамивира у пациентов группы риска не отличался от такового в общей популяции взрослых пациентов.
Лечение гриппа у детей
У детей в возрасте 1-12 лет (средний возраст 53 года) имевших лихорадку (≥ 378 °С) и один из симптомов со стороны дыхательной системы (кашель или ринит) в период циркуляции вируса гриппа среди населения было проведено двойное слепое плацебо- контролируемое исследование. 67 % пациентов были инфицированы вирусом гриппа А и 33% пациентов - вирусом гриппа В. Осельтамивир (при приеме не позднее 48 ч после появления первых симптомов гриппозной инфекции) значительно снижал продолжительность заболевания (на 358 ч) по сравнению с плацебо. Продолжительность заболевания определялась как время до купирования кашля заложенности носа исчезновения лихорадки возвращения к обычной активности.
В группе детей получавших осельтамивир частота острого среднего отита снижалась на 40% по сравнению с группой плацебо. Выздоровление и возвращение к обычной активности наступало почти на 2 дня раньше у детей получавших осельтамивир по сравнению с группой плацебо.
В другом исследовании участвовали дети в возрасте 6-12 лет страдающие бронхиальной астмой; 536% пациентов имели гриппозную инфекцию подтвержденную серологически и/или в культуре. Медиана продолжительности заболевания в группе пациентов получавших осельтамивир значительно не снижалась. Но к последнему 6-му дню терапии осельтамивиром объем форсированного выдоха за 1 сек (OФB1) повышался на 108% по сравнению с 47% у пациентов получавших плацебо (р = 00148).
Профилактика гриппа у взрослых и подростков
Профилактическая эффективность осельтамивира при естественной гриппозной инфекции А и В была доказана в 3 отдельных клинических исследованиях III фазы. На фоне приема осельтамивира гриппом заболели около 1% пациентов. Осельтамивир также значительно уменьшал частоту выделения вируса и предотвращал передачу вируса от одного члена семьи к другому.
Взрослые и подростки которые были в контакте с больным членом семьи начинали прием осельтамивира в течение двух дней после возникновения симптомов гриппа у членов семьи и продолжали его в течение 7 дней что достоверно уменьшало частоту случаев гриппа у контактировавших лиц на 92%.
У лиц пожилого и старческого возраста находившихся в домах для престарелых 80% из которых были привиты перед сезоном когда проводилось исследование осельтамивир достоверно снижал заболеваемость гриппом на 92%. В том же исследовании осельтамивир достоверно (на 86%) уменьшал частоту осложнений гриппа: бронхита пневмонии синусита. Пациенты принимали препарат в течение 42 дней.
Профилактика гриппа у детей
Профилактическая эффективность осельтамивира при естественной гриппозной инфекции была продемонстрирована у детей от 1 года до 12 лет после контакта с заболевшим членом семьи или с кем-то из постоянного окружения. Основным параметром эффективности была частота лабораторно подтвержденной гриппозной инфекции. У детей получавших осельтамивир в форме порошка для приготовления суспензии для приема внутрь в дозе от 30 до 75 мг 1 раз в день в течение 10 дней и не выделявших вирус исходно частота лабораторно подтвержденного гриппа уменьшилась до 4% (2/47) по сравнению с 21% (15/70) в группе плацебо.
Профилактика гриппа у лиц с ослабленным иммунитетом
Резистентность
У всех пациентов-носителей OK-резистентного вируса носительство имело временный характер не влияло на элиминацию вируса и не вызывало ухудшения клинического состояния.
Абсцесс – ограниченное капсулой скопление гноя, возникающее при острой или хронической очаговой инфекции и приводящее к тканевой деструкции в очаге (нередко с перифокальным отеком).
Абсцессы кожи и подкожной клетчатки: фурункул, карбункул. Staphylococcus aureus.
Фурункул – острое гнойно-некротическое воспаление волосяного фолликула и окружающих его тканей. В дальнейшем воспаление переходит на сальную железу и окружающую соединительную ткань. Наиболее часто наблюдается на участках кожи, подвергающихся загрязнению (предплечья, тыл кисти) и трению (задняя поверхность шеи, поясница, ягодичная область, бедра). Вызывается чаще Staphylococcus aureus, реже Staphylococcus pyogenes albus.
Фурункулез – множественное поражение фурункулами.
Карбункул – острое гнойно-некротическое воспаление нескольких волосяных фолликулов и сальных желез с образованием обширного некроза кожи и подкожной клетчатки. Карбункул чаще развивается на задней поверхности шеи, межлопаточной и лопаточной областях, на пояснице, ягодицах, реже на конечностях. Возбудители – Staphylococcus aureus или стафило-стрептококковая инфекция, реже стрептококк.
Код протокола: 09-101е "Абсцесс кожи, фурункул и карбункул других локализаций. Другие уточненные инфекции кожи и подкожной клетчатки"
Период протекания
Длительность лечения составляет 9 дней.
Факторы и группы риска
Истощение, гиповитаминоз, тяжелые общие заболевания, болезни обмена веществ (сахарный диабет, ожирение), загрязнение кожи и микротравмы.
Диагностика
Критерии диагностики
При фурункуле – болезненный конусовидный инфильтрат с формирующимся гнойным стержнем, на вершине инфильтрата отмечается небольшое скопление гноя с черной точкой (некроз) в центре. Пустула обычно прорывается и подсыхает, а на 3-7 сутки инфильтрат гнойно расплавляется и некротизированные ткани в виде стержня вместе с остатками волоса выделяются с гноем.
При карбункуле - вначале появляется небольшой воспалительный инфильтрат с поверхностной пустулой, который быстро увеличивается в размере. Напряжение тканей приводит к возникновению резких болей при пальпации, а также распирающей, рвущей, самостоятельной боли. Кожа в области инфильтрата приобретает базовый оттенок, напряжена, отечна. Эпидермис над очагом некроза прорывается в нескольких местах, образуется несколько отверстий ("сито"), из которых выделяется густой зеленовато-серый гной. В отверстиях видны некротизированные ткани. Отдельные отверстия сливаются, образуя большой дефект в коже, через который вытекает много гноя и отторгаются некротические ткани. Температура повышается до 40 С, отмечается значительная интоксикация (тошнота и рвота, потеря аппетита, сильная головная боль, бессонница, изредка бред и бессознательное состояние).
Лечение
При фурункуле операция выполняется редко. Однако при плохом отторжении гнойно-некротического стержня кожа рассекается острым скальпелем. Рассекать фурункул нельзя, так как гнойная инфекция может распространиться на окружающие ткани. Категорически запрещается выдавливать содержимое фурункула и делать массаж в области очага воспаления.
При карбункуле если консервативное лечение не эффективно, показанием для операции является нарастание интоксикации. Операция проводится под наркозом и заключается в крестообразном рассечении карбункула через всю толщу некроза до жизнеспособных тканей с иссечением некротических тканей и вскрытием затеков. Повязки с гипертоническим раствором натрия хлорида, мазью Вишневского или другим антисептиком.
Для вскрытия абсцесса выбирают самый короткий путь с учетом анатомических образований. Можно вначале пунктировать абсцесс, а затем по игле рассечь ткани. Удалив гной, разрез расширяют и иссекают некротические ткани. Полость обрабатывают растворами антисептиков и дренируют марлевыми тампонами с антисептиками, протеолитическими ферментами, антибиотиками, а также резиновыми дренажами. При плохом дренировании из основного разреза делают контрапертуру. Первые 2-3 дня рану перевязывают ежедневно и, когда она очистится от гноя и некротических тканей, переходят на редкие мазевые повязки. В некоторых случаях можно иссечь абсцесс в пределах здоровых тканей и наложить первичные швы с активной аспирацией из раны, что ускоряет ее заживление и позволяет добиться хорошего косметического эффекта.
Обосновано применение витаминов, обладающих противовоспалительным и иммуномодулирующим действием, улучшающих обмен веществ: аскорбиновая кислота 5% -2,0 в/м №10-15, поливит по 1 др. х 3 раза в день, 10 дней.
Антибиотики с учетом чувствительности микрофлоры:
- феноксиметилпенициллин – 0,25 г 4 раза/сут (при стрептококковой инфекции);
- амоксициллин/клавуланат – 0,375-0,625 г 3 раза/сут.;
- цефалексин 0,5-1,0 г 4 раза/сут.;
- цефуроксим аксетил – 0,5 г 2 раза/сут во время еды;
- эритромицин 0,5 г 4 раза/сут.;
- оксациллин 1-2 г 4-6 раз/сут. в/в, в/м;
- цефазолин 1-2 г 3 раза/сут. в/в, в/м;
- фузидиевая кислота 0,5-1 г 3 раза/сут. внутрь;
- цефтриаксон 1, 0 г 1 раз/сут. в/м.
- итраконазол оральный раствор 400 мг\сут – 7 дней (профилактика кандидоза).
Местно - 2% мазь или крем на основе мупироцина, 2% мазь или крем на основе натриевой соли фузидиевой кислоты.
Учитывая упорное течение заболевания, развитие воспалительного процесса в дерме и сенсибилизацию организма назначаются десенсибилизирующие средства: тиосульфат натрия 30% - 10,0 в/в ежедневно №10-15.
При гнойничковых заболеваниях имеет место нарушение периферического кровообращения и обмена веществ, в связи с чем назначается никотиновая кислота 1% 1,0 в/м №10-15 (улучшает углеводный обмен, микроциркуляцию, оказывает сосудорасширяющее действие и улучшает регенеративные свойства ткани). Назначаются препараты способные адсорбировать токсины: активированный уголь – 6 таб. утром натощак 10 дней.
Для уменьшения возбудимости ЦНС применяют успокаивающие средства – настойка пустырника по 20 кап. х 3 раза в день в течение месяца.
Учитывая, что в патогенезе существенное значение имеют иммуннодефицитные состояния, снижение реактивности организма назначают иммуномодуляторы – метилурацил 500 мг х 3 раза в день - 10 дней; метронидазол по 250 мг х 3 раза в день - 10 дней. С целью коррекции поражений поджелудочной железы, печени и желчевыводящих путей, при нарушении факторов неспецифической защиты и наличии сопутствующей патологии назначается панкреатин по 1 капс. х 4 раза в день, 10 дней.
С целью улучшения реологических свойств крови и микроциркуляции - декстран 400 мл в/в 1 р. в день, курсовая доза 800 мл. Наружно назначают бактерицидные, антисептические препараты – мази с антибиотиками, растворы анилиновых красителей (метиленовый синий, калия перманганат, перекись водорода), противовоспалительные - для улучшения трофики кожи.
Перечень основных медикаментов:
1. *Аскорбиновая кислота раствор для инъекций 5%, 10% в ампуле 2 мл, 5 мл
2. Феноксиметилпенициллин 500 мг табл.
3. *Амоксициллин+клавулановая кислота таблетка 625 мг; раствор для инъекций 600 мг во флаконе
4. *Цефалексин 250 мг, 500 мг табл., капс.; суспензия и сироп 125 мг, 250 мг/5 мл
5. *Цефуроксим 250 мг, 500 мг табл.; порошок для приготовления инъекционного раствора во флаконе 750 мг
6. *Эритромицин 250 мг, 500 мг табл; пероральная суспензия 250 мг/5 мл
7. *Цефазолин порошок для приготовления инъекционного раствора 1000 мг
8. *Цефтриаксон порошок для приготовления инъекционного раствора 250 мг, 500 мг, 1000 мг во флаконе
9. *Итраконазол оральный раствор 150 мл – 10 мг\мл
10. *Натрия тиосульфат раствор для инъекций 30% 5 мл, 10 мл в ампуле
11. *Никотиновая кислота 50 мг табл.; раствор в ампуле 1% 1 мл
12. *Активированный уголь 250 мг табл.
13. Настойка пустырника 30 мл, 50 мл фл.
14. *Метилурацил 10% мазь
15. *Метронидазол 250 мг табл; раствор для инфузий 0,5 во флаконе 100 мл
16. *Панкреатин таблетка, капсула с содержанием липазы не менее 4 500 ЕД
17. *Декстран раствор для инфузий во флаконе 200 мл, 400 мл
18. *Метиленовый синий раствор спиртовый 1% во флаконе 10 мл
19. *Калия перманганат водный раствор 1:10 000
20. *Перекись водорода раствор 3% во флаконе 25 мл, 40 мл
Критерии перевода на следующий этап: заживление операционной раны.
* – препараты, входящие в список основных жизненно важных лекарственных средств
Материалы предназначены исключительно для врачей и специалистов с высшим медицинским образованием. Статьи носят информационно-образовательный характер. Самолечение и самодиагностика крайне опасны для здоровья. Автор статей не дает медицинских консультаций: клинический фармаколог — это врач только и исключительно для врачей.
Врага, как известно, надо знать в лицо. Просторы интернета принесли вот такое симпатичное фото нашего противника.
Данного возбудителя невозможно перепутать ни с чем, особенно, когда процесс зашел далеко. Практически все отделение будет в курсе наличия такого больного из-за непередаваемого аромата, разносящегося из его пораженных областей.
Pseudomonas aeruginosa бывает дикой, ее нам приносят пациенты из внешнего мира и нашей, госпитальной, которая живет внутри больничных отделений (чаще хирургических и реанимационных) и вызывает тот самый суеверный ужас практически у всех, обремененных медицинским образованием.
Синегнойная палочка является вольным жителем тех мест, где тепло и влажно. Она живет в прудах (дикая), в раковинах, в банках с фурацилином и другими дезенфектантами, диализных жидкостях и наркозных аппаратах в стационарах.
А потому, если в отделение что-то такое выросло, борьба с синегнойной инфекцией должна начинаться со смены сантехники (старой на новую) и линолеума вокруг раковины. С отказа от фурацилина, со сроком изготовления более суток и с просушивания трубок аппаратуры для вентиляции легких.
Больной у нас тоже теплый и, как и любой человек, на 70% состоит из воды. А еще у него множество вольных открытых пространства – мокнущие раневые поверхности, ожоговые раны, свищевые ходы, пролежни, цистостомы, трахеостомы, катетеры. То есть все те условия, которые палочка очень любит. А еще теплой и влажной поверхностью у нас является роговица глаза и если промедлить с лечением – этот самый глаз можно потерять за несколько часов.
- Гангренозную пневмонию
- Эмпиему
- Наружный отит
- Инфекции глаз (особенно после травм и хирургических вмешательств)
- Фурункулез (после горячих ванн)
- Септицемию
- Эндокардит
- Менингит
- Часто инфицирует ожоговые поверхности, свищевые ходы, изъязвленные пролежни.
Синегнойная инфекция развивается чаще всего на фоне иммуносупрессии или массированной антимикробной терапии, так как сам возбудитель природно устойчив абсолютному большинству антибактериальных препаратов, а массовая гибель конкурентов, дает ей селективное преимущество. Кстати, основными препаратами, селектирующими в отделениях Pseudomonas aeruginosa являются цефалоспорины третьего и четвертого поколений.
- на руках
- на общих полотенцах в ординаторских, процедурных и манипуляционных (многоразовых)
- на фонендоскопах
- на мобильных телефонах
- на авторучках, которые у нас торчат из карманов и т.д.
И достаточно в отделении появиться одному пациенту с этим возбудителем, а персоналу забыть о путях распространения – к вечеру все 100% пациентов будут обсеменены этим возбудителем. А дальше как повезет… пациентам…
Если инфицирование все-таки произошло, и у пациента возникла синегнойная инфекция, чем же мы будем ее лечить?
В этом списке нет цефоперазона и цефоперазона/сульбактама, о которых нам с института говорят, что они антисинегнойные. Дело в том, что единственным действительно антисинегнойным цефалоспорином является цефтазидим, а данные о якобы высокой чувствительности к цефоперазону и цефоперазону сульбактаму существуют только в России, так как нет ни одной рекомендации по использованию этих препаратов ни в США, ни на medscape.com, ни на EUCAST. Более того, эти источники не дают даже критериев определения чувствительности Pseudomonas aeruginosa к этим препаратам. И откуда взялись наши российские выводы о высокой чувствительности вообще не понятно. Более того, комбинация Цефоперазон/сульбактам существует только в 2-х странах – России и Турции. FDA в свое время очень быстро отменила его регистрацию.
Цефалоспорин третьего поколения. Препарат с явной и очень высокой антисинегнойной активностью. Первые несколько лет после появления он был самым мощным препаратом против грам(-) флоры. Однако в связи с увеличением количества как госпитальных, так и внебольничных беталактамаз расширенного спектра (БЛРС), его значение было пересмотрено и сейчас он используется в качестве индикатора для выявления БЛРС у грам(-) бактерий. Проще говоря, если кишечная палочка или клебсиелла устойчивы к цефтаздиму, то любой, сколь угодно большой диаметр зоны на чашке Петри вокруг диска с цефотаксимом или цефтриаксоном в расчет уже не принимаются.
Если антибиотикограммы еще нет, но есть пациент предлеченный цефтазидимом без эффекта, то не нужно выбирать ему препарат среди III генерации цефалоспоринов, по причине того, что использование их будет бесполезным, при этом, если пациента с грамотрицательной инфекцией лечили цефалоспоринами 2-3-й генерации, то вполне допустима терапия цефтазидимом, потому что, во-первых, он активен против синегнойки, а во вторых бета-лактамаза цефуроксимаза, рушит все цефалоспорины, но не цефтазидим.
Еще одной особенностью цефтазидима является его возможность создавать высокие концентрации в ликворе, проникая через гематоэнцефалический барьер, поэтому его используют для лечения менингитов, вызванных грамотрицательной микрофлорой, при условии чувствительности к нему возбудителей.
3. Карбопенемы обладают антисинегнойной активностью, но она слабее чем у цефтазидима и анисинегнойными они стали только из-за того, что существует Эртапенем, у которого нет никакой антисинегнойной активности. Да, применять можно, но только в комбинации с другими антисинегнойными препаратами.
4. Амикацин, как и все аминогликозиды, обладает более мощным бактерицидным действием, чем бета-лактамы и минимальным количеством аллергических реакций. Но он должен нами рассматриваться, как и другие антисинегнойные препараты, как препарат резерва и не использоваться широко в стационаре. Другие аминогликозиды прекрасно отработают Гр (-) флору и без него, нам важно сохранить чувствительность нашей, местной синегнойки к нему как можно дольше.
Дозируем амикацин, как вы помните, на килограмм массы тела и детям и взрослым и обязательно с учетом клиренса креатинина. (подробнее о дозировании смотрите обзорную статью по аминогликозидам, которая располагается по этой ссылке /vracham/Informatsiya-dlya-spetsialistov/Antibiotikoterapiya/Obzory-antibiotikov-razlichnyh-grupp/Obzory-antibiotikov-razlichnyh-grupp_411.html)
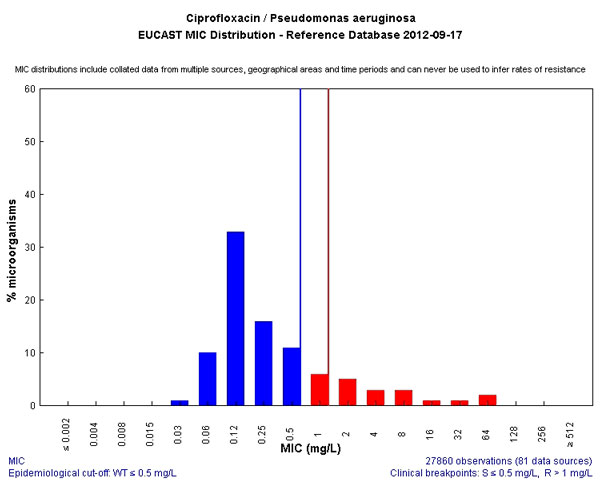
И, к сожалению, препарат, который нам скоро уничтожат коллеги из поликлинического звена, потому что назначают его направо и налево. Да и в стационарах коллеги грешат его необоснованным назначением, так как он относительно дешев и более чем доступен из-за огромного количества дженериков. Как результат, нам уже приходится использовать дозировки не 400 мг в сутки, а 800-1200 мг. И, слава богу, что механизм резистентности нам это еще позволяет. Является одним из самых безопасных антисинегнойных препаратов, а потому беречь его мы должны как самое дорогое.
Он может использоваться в стационаре в случаях не синегнойной инфекции только тогда, когда другим способом помочь пациенту невозможно.
Это препарат такого же глубокого резерва как амикацин. И может использоваться только под контролем клинического фармаколога в отличие от других фторхинолонов.
И один из самых страшных моих, и не только моих, кошмаров – это панрезистентная синегнойная палочка. Это та палочка которая устойчива абсолютно ко всем известным на данный момент антимикробным средствам и здесь мы совершенно бессильны. А потому наша основная цель состоит в том, чтобы не дать ей у нас в стационаре появиться. Для этого требуется соблюдать несложные правила асептики, а именно, мыть и обрабатывать руки после каждого пациента, менять перчатки, обрабатывать фонендоскопы и к пациентам с гнойным воспалением не заходить с мобильниками и чем либо еще, что мы можем схватить руками, сами того не замечая. Ну и никаких общих полотенец в ординаторских и сестренских.
Читайте также:

