Противовирусные препараты при скв
Обновлено: 25.04.2024
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Васкулиты: причины появления, симптомы, диагностика и способы лечения.
Определение
Причины возникновения васкулитов
Причины развития васкулитов точно пока не известны. Выделяют первичные системные васкулиты, являющиеся самостоятельными заболеваниями, и вторичные, которые развиваются на фоне других болезней.
В основе формирования первичных васкулитов лежат генетические дефекты, а пусковыми факторами становятся латентные (скрыто протекающие) инфекционные процессы (гепатит В, парвовирус, стафилококк, микобактериоз, ОРВИ), иммунная гиперчувствительность к некоторым лекарственным препаратам (антибактериальным, противовирусным, ингибиторам АПФ, аминазину и др.), гиперсенсибилизация к некоторым соединениям, входящим в состав табака, и пр.
Вторичные системные васкулиты возникают как синдром при различных заболеваниях, например, при инфекционном эндокардите, ревматоидном артрите, при некоторых опухолевых процессах, инфекционных поражениях, при лекарственной болезни.
В основе развития системных васкулитов лежат различные патологические механизмы, например, повреждающее действие циркулирующих иммунных комплексов (ЦИК). Иными словами, при попадании в организм антигена (им может быть любой микробный агент, лекарственное вещество, собственный измененный белок) к нему присоединяется соответствующий иммуноглобулин. Вместе они образуют иммунный комплекс. Эти комплексы начинают циркулировать по организму, осаждаются на внутренней стенке сосудов и вызывают воспаление. Чем больше этих комплексов и чем дольше они циркулируют в крови, тем сильнее повреждается сосудистая стенка. Способствует повреждению повышение внутрисосудистого давления, замедление тока крови, нарушения баланса в работе иммунной системы.
Другими патологическими механизмами, лежащими в основе васкулитов, является выработка тромбоцитами и клетками внутренней стенки сосудов (эндотелия) провоспалительных цитокинов и появление в крови аутоантител – белков, которые ведут себя агрессивно по отношению к собственным антигенам организма. Эти аутоантитела могут оказывать прямое повреждающее действие на эндотелий (антиэндотелиальные антитела), на цитоплазму нейтрофилов (АНЦА – антинейтрофильные цитоплазматические антитела), способствовать активации каскада свертывающей системы крови (антифосфолипидные аутоантитела).
Классификация васкулитов
Существует большое количество классификаций системных васкулитов, из которых основной на сегодняшний день является та, в основе которой лежит калибр пораженных сосудов и основные механизмы их поражения:
1. Васкулит с поражением сосудов крупного калибра:
- артериит Такаясу (неспецифический аортоартериит),
- гигантоклеточный артериит (болезнь Хортона) и ревматическая полимиалгия.
- узелковый полиартериит,
- болезнь Кавасаки.
3.1. Васкулиты, ассоциированные с антинейтрофильными цитоплазматическими антителами (АНЦА):
- микроскопический полиангиит,
- гранулематоз с полиангиитом (Вегенера),
- эозинофильный гранулематоз с полиангиитом (Черджа- Строс).
- заболевания, ассоциированные с антителами к базальной мембране клубочка почек (синдром Гудпасчера),
- криоглобулинемический васкулит
- IgA-ассоциированный васкулит (геморрагический васкулит, пурпура Шенлейна-Геноха),
- гипокомплементемический уртикарный васкулит (анти-C1q васкулит).
- кожный лейкоцитокластический ангиит,
- кожный артериит,
- первичный васкулит центральной нервной системы,
- изолированный аортит,
- другие.
- васкулит при системной красной волчанке,
- ревматоидный васкулит,
- саркоидный васкулит,
- другие.
- криоглобулинемический васкулит, ассоциированный с вирусом гепатита С,
- васкулит, ассоциированный с вирусом гепатита В,
- аортит, ассоциированный с сифилисом,
- лекарственный иммунокомплексный васкулит,
- лекарственный АНЦА-ассоциированный васкулит,
- паранеопластический васкулит,
- другие.
Симптомы системного васкулита зависят от того, какие сосуды поражены. При вовлечении сосудов кожи появляются симметричные высыпания (в первую очередь на голенях), склонные к отеку, кровоизлияниям, некрозу. Может развиться гангрена.
На слизистых оболочках также могут появляться геморрагические высыпания, язвы и некрозы.
Ишемический синдром при васкулитах проявляется перемежающейся хромотой – болью в икроножных мышцах, возникающей при ходьбе и вынуждающей человека сделать остановку и подождать, пока боль утихнет (встречается также в других мышцах ног, сопровождается онемением и похолоданием конечностей, может наблюдаться и при поражении верхних конечностей). Кроме того, может развиваться ишемическая полинейропатия, ишемические поражения центральной нервной системы, асимметрия пульсации артерий.
Системные васкулиты характеризуются вовлечением в патологический процесс разных органов и систем. Поражения сосудов сердечно-сосудистой системы могут приводить к недостаточному кровоснабжению сердечной мышцы, миокардитам, поражению внутренней оболочки сердца – эндокарда, и околосердечной сумки – перикарда. Возникают различные нарушения ритма и проводимости, повышается риск развития острого инфаркта миокарда и сердечной недостаточности.
Поражение бронхолегочной системы включает появление в легких уплотнений (инфильтратов), развитие инфарктной пневмонии, бронхоспазма, плеврита.
Почечные васкулиты становятся следствием поражения почечных артерий. Например, при узелковом периартериите в почках возникают множественные безболевые инфаркты (гибель части почки в результате закупорки артерии), что приводит к почечной недостаточности. Поражение почечных артерий может закончиться стойкой злокачественной артериальной гипертензией. Некоторые васкулиты протекают с развитием тяжелого гломерулонефрита – воспалением почечных клубочков.
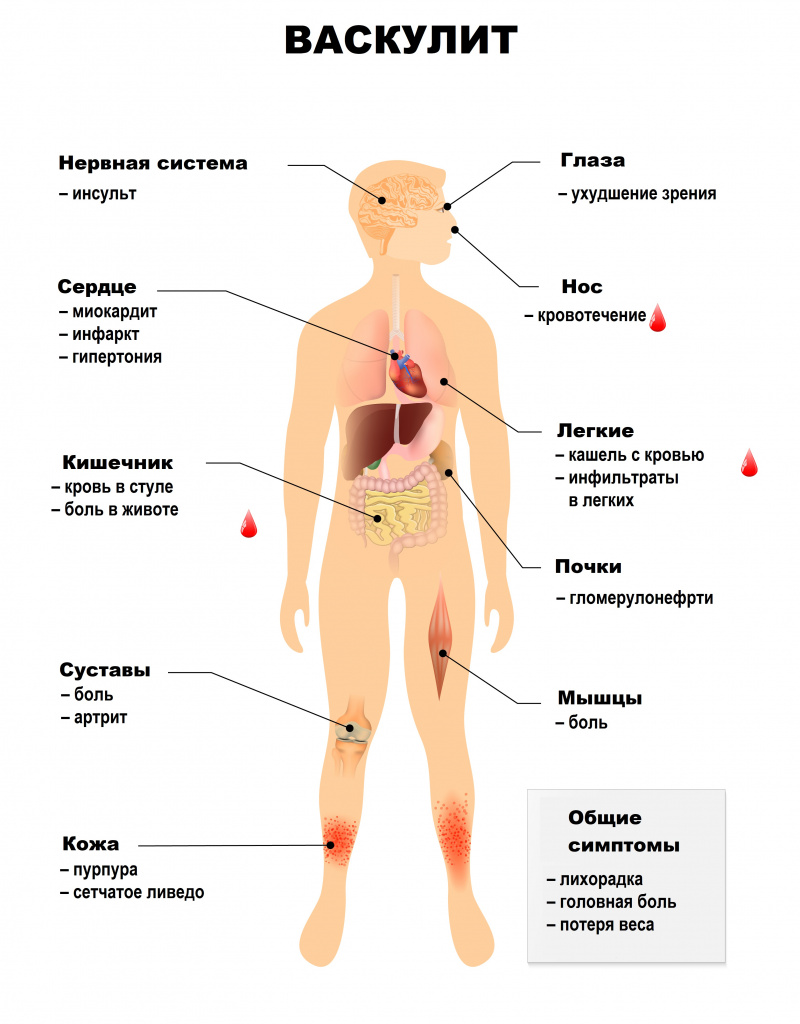
Абдоминальный синдром при васкулитах сопровождается болью в животе в сочетании с диспепсическими расстройствами (чувством распирания, вздутием), тошнотой, рвотой, язвами в желудке и кишечнике, может развиться опасное осложнение – тромбоз брыжеечных артерий, кровоснабжающих кишечник.
Поражение нервной системы проявляется множественными невритами, патологией центральной нервной системы с психозами, зрительными расстройствами, острыми нарушениями мозгового кровообращения.
Для геморрагического васкулита (пурпуры Шенлейна-Геноха) типично поражение кожи, кишечника, почек, суставов. Поражение кожи проявляется геморрагическим синдромом – множественными кровоизлияниями на стопах, голенях, бедрах, ягодицах, плечах, предплечьях, вокруг пораженных суставов. Но особенно они выражены на внутренней поверхности предплечий, бедер, голеней, в местах расположения ремня брюк, ремешка часов. О кровоизлияниях в кишечнике свидетельствуют колики, тошнота, рвота, стул с кровью.
Для криоглобулинемического васкулита характерно поражение кожи и клубочков почек. Появляется мелкоточечная или сливная геморрагическая пурпура чаще в области нижних конечностей, ягодиц, поясницы. Одновременно у больных возникают мигрирующие боли в мелких суставах кистей и в коленных суставах.
Гранулематоз Вегенера проходит с вовлечением дыхательных путей и тяжелым гломерулонефритом, приводящим к декомпенсированной почечной недостаточности и часто является причиной смерти больного.
Эозинофильный гранулематоз с полиангиитом (Черджа-Строс) протекает с поражением респираторного тракта, придаточных пазух носа, аллергией. Характерным признаком является развитие гиперэозинофильной бронхиальной астмы. Почки при этом васкулите, как правило, не страдают.
При узелковом периартериите поражаются в основном артерии среднего калибра – образуются аневризмы, тромбы, кровотечения из-за разрыва аневризм, велик риск инфаркта пораженных органов и тканей. Больные испытывают сильную боль в мышцах (чаще ног), мигрирующие боли в крупных суставах, наблюдается поражение кожи, желудочно-кишечного тракта и сердца.
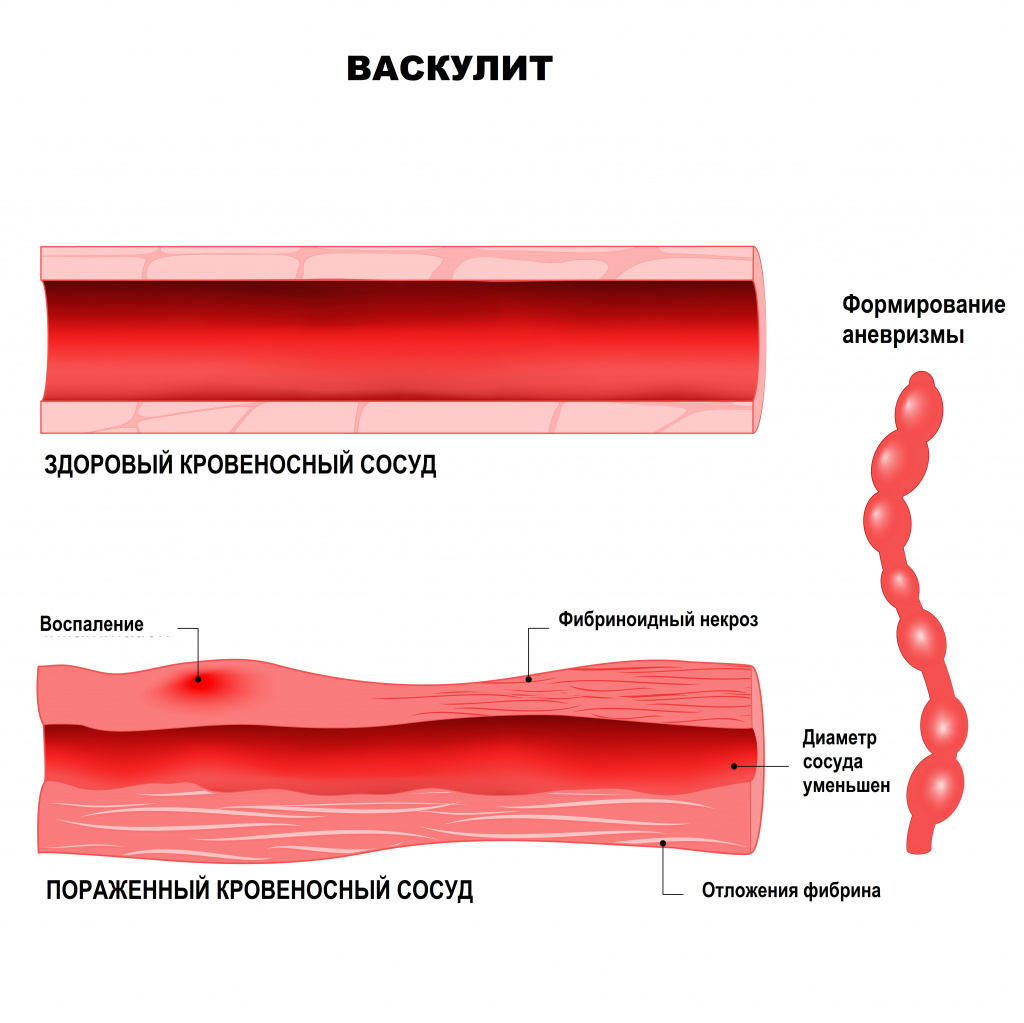
При микроскопическом полиангиите страдают мелкие сосуды. Для заболевания характерны кожные проявления, полиневрит, воспалительные процессы в дыхательных путях, а также некротизирующий гломерулонефрит.
Болезнь/синдром Кавасаки часто встречается у детей и сопровождается лихорадкой, воспалением слизистых оболочек, кожи, лимфатических узлов и различных систем, прежде всего сердечно-сосудистой, что проявляется тахикардией, аритмией, могут возникать аневризмы и сужения коронарных артерий, миокардит, перикардит, поражение клапанного аппарата.
При болезни Такаясу, или неспецифическом аортоартериите страдают суставы (преимущественно верхних конечностей) и кожа с развитием язв. Характерным является синдром дуги аорты – он включает поражение подключичных артерий, которое проявляется болями, мышечной слабостью, зябкостью рук, резким уменьшением или полным отсутствием пульса на лучевых артериях, и стеноз сонных артерий. Кроме того, возникает симптоматическая артериальная гипертензия (из-за сужения почечных артерий), повышается давление в легочной артерии, сужаются артерии сердца вплоть до развития инфаркта, наблюдается перемежающаяся хромота.
При гигантоклеточном височном артериите страдает аорта и отходящие от нее крупные артерии. Характерным признаком является воспаление височной артерии, вызывающее постоянную, очень интенсивную головную боль, обычно с одной стороны головы.
Диагностика васкулита
Для большинства системных васкулитов нет специфических лабораторных тестов. Внимание уделяется клинической картине заболевания с выявлением характерных для того или иного васкулита симптомов.
Затем врач выясняет системность патологического процесса, на которую могут указывать такие симптомы как повышение температуры, снижение массы тела, боль в мышцах и суставах, анемия, увеличение СОЭ.
Потом определяется, первичный или вторичный характер носит заболевание, после чего требуется клиническое и инструментальное подтверждение поражения сосудов.
Для этой цели применяются методы инструментальной и рентген-диагностики:
Ультразвуковое сканирование артерий верхних конечностей в комплексной диагностике сердечно-сосудистых заболеваний.
Системная красная волчанка (СКВ)-одно из наиболее распространенных хронических аутоиммунных системных (не-органоспецифических) заболеваний, которое характеризуется диффузным поражением соединительной ткани и сосудов; относится к группе так называемых больших коллагенозов.
Частота СКВ в разных странах варьирует; например, в Северной Америке и Европе она в среднем составляет 40 случаев на 100 000 населения. Однако установлено, что чернокожее население Америки и население Испании поражается чаще и заболевание у них протекает тяжелее.
Женщины болеют СКВ гораздо чаще (9:1); до 80% женщин страдают СКВ в детородном периоде. У детей и лиц пожилого возраста частота возникновения СКВ составляет приблизительно 1 случай на 100000 населения с соотношением женщины : мужчины – 3:1.
Довольно часто у больных СКВ кроме признаков этого заболевания имеются также признаки другой патологии соединительной ткани – ревматоидного артрита и склеродермии.
Иммунопатогенез. Развитие СКВ сопряжено с воздействием генетических факторов и факторов окружающей среды, которые приводят к развитию нарушений иммунной регуляции, модификации аутоантигенов, срыву толерантности и развитию аутоиммунного ответа.
Роль генетических факторов подтверждается следующими данными:
- Доказано, что СКВ развивается у 30% монозиготных близнецов и только у 5% дизиготных;
- Установлена ассоциация между предрасположенностью к СКВ и генами HLA DR2/DR3,Gm-аллотипом и особенностями строения альфа-цепи Т-клеточного антигенраспознающего рецептора;
- Существуют специальные инбредные линии мышей, у которых СКВ-подобное заболевание развивается спонтанно;
- Выявлено, что предрасположенность к заболеванию СКВ кодируется более, чем 6 генами, расположенными на различных хромосомах.
Роль факторов окружающей среды подтверждается следующими данными:
- У 30% больных отмечается фоточувствительность кожи, которая проявляется развитием сыпи после пребывания на солнце;
- Установлено, что под влиянием гидралазина, прокаинамида, фенитоина, гидантои-на, изониазида, хлорпромазина, D-пеницилл амина и др. развивается лекарственно-индуцированный СКВ-синдром;
- Хорошо известны случаи индукции СКВ после перенесенных инфекций.
Роль гормональных факторов подтверждается более высокой частотой встречаемости СКВ у женщин по сравнению с мужчинами (соотношение 9:1).
Роль аутоантител, иммунных комплексов и дефицита комплемента подтверждается следующими данными:
- Увеличением концентрации IgG в сыворотке крови больных;
- Наличием аутоантител к аутологичным и чужеродным антигенам;
- Выявлением циркулирующих иммунных комплексов у 80% больных;
- Снижением концентрации С2, С4 и СЗ в сыворотке крови больных;
- Снижением количества рецепторов к комплементу (CR1) на эритроцитах;
- Отложением IgG, М, СЗ и С4 в капиллярах почечных клубочков и кожи.
Нарушения Т- и В-лимфоцитов у больных СКВ Т-лимфоциты:
- Лимфопения, развивающаяся под влиянием антилимфоцитарных антител, в том числе, анти-Т-антител;
- Снижение количества и функции супрессорных клеток;
- Снижение количества “наивных” Т-лимфоцитов (CD4V8 CD45RA+);
- Снижение количества Т-клеток памяти (CD4\8 CD29. CD45RO+);
- Увеличение количества активированных Т-клеток (CD4+DR+).
- Поликлональная активация В-лимфоцитов;
- Увеличение чувствительности к стимулирующим цитокиновым сигналам;
- Нарушение цитокинового профиля у больных СКВ включает снижение способности моноцитов продуцировать ИЛ-1, а также снижение способности Т-лимфоцитов отвечать на ИЛ-2.
При активации заболевания обнаружено также повышение уровня цитокинов, контролирующих дифференцировку В-лимфоцитов и продукцию гуморальных антител: ИЛ-6, ИЛ-4, ИЛ-5. Одним из чувствительных показателей, свидетельствующих об активации СКВ, является повышение в сыворотке крови количества растворимых рецепторов к ИЛ-2.
Иммунные комплексы. У больных с активной стадией СКВ доказано повышение уровня циркулирующих иммунных комплексов, которые, откладываясь в сосудах, вызывают воспаление тканей.
В физиологических условиях антитела, которые продуцируются в ответ на микробную инфекцию, формируют циркулирующие иммунные комплексы. Последние после связывания с сывороточным комплементом фиксируются на эритроцитах за счет наличия на мембране эритроцитов рецептора к СЗb. В дальнейшем иммунные комплексы попадают в печень и селезенку, где выводятся из крови.
При СКВ за счет различных нарушений создаются условия для персистенции циркулирующих иммунных комплексов (ЦИК) в высоких титрах. Это приводит к тому, что иммунные комплексы откладываются в нелимфоидных тканях, например, в клубочках почки или в сосудах кожи. Их отложение в тканях приводит к активации комплемента, хемотаксису полиморфонуклеарных лейкоцитов, которые высвобождают медиаторы воспаления, что обусловливает повреждение сосудов и развитие васкулита.
Таким образом, основные клинические проявления СКВ объясняются следующими иммунными механизмами:
- Наличие ЦИК, в состав которых входят антиядерные антитела; последние, откладываясь в микроциркуляторном русле, приводят к развитию васкулопатий и, как следствие, к повреждению тканей.
- Наличие аутоантител к клеткам крови приводит к лейко-, лимфо-, тромбопении и анемии.
- Наличие антифосфолипидных антител приводит к развитию так называемого антифос-фолипидного синдрома.
Клиника. Наиболее частыми ранними проявлениями СКВ являются полиартрит и дерматит. Следует учитывать, что; 1) в принципе любой из симптомов СКВ может быть первым проявлением заболевания; 2) может пройти много месяцев или даже лет, прежде чем будет установлен окончательный диагноз СКВ. Кроме упомянутых полиартрита и дерматита, к ранним симптомам СКВ, на которые следует обращать внимание, относят хроническую усталость, различные расстройства сознания, аффекты, включая тревогу и депрессии, перикардит, тромбоцитопению, анемию, лейко- и лимфопению. В последующем появляются признаки поражения почек и центральной нервной системы.
Диагноз. Критерии диагностики СКВ и других болезней соединительной ткани, разработаны Американской ревматологической ассоциацией и включают 11 пунктов. Для их лучшего запоминания F. Graziano и R. Lemanske (1989) предлагают использовать мнемонический прием, выделив первые буквы каждого пункта таким образом, что образовалось новое словосочетание – SOAP BRAIN MD (SOAP-мыло; BRAIN-мозг; MD – medical doctor):
- S – серозиты, плевральные или перикардиальные;
- 0–оральные (или назофарингеальные) изъязвления слизистой оболочки, которые можно выявить при обследовании;
- А–артриты, неэрозивные, с вовлечением двух и более суставов, с наличием болезненности, припухлости и выпотом;
- Р–фоточувствительность (photosensitivity), приводящая к появлению сыпи после пребывания на солнце;
- В–кровь (blood): гемолитическая анемия, лейкопения ( < 400 в 1 мл), лимфопения (< 1500 мм3), тромбоцитопения (< 100 000 в 1 мл);
- R – почки (renal): протеинурия (>0,5 г/день) или цилиндрурия;
- А – антитела антиядерные;
- I – иммунные тесты: анти-dsДНК-антитела, анти-Sm-антитела, ложноположительная реакция на сифилис, LE-клетки;
- N – неврологические нарушения: судорожные припадки или психозы, не связанные с приемом лекарственных средств или с такими метаболическими нарушениями как уремия, электролитный баланс или кетоацидоз;
- М – сыпь (malar) с фиксированной эритемой в виде бабочки в носогубной области;
- D – дискоидная сыпь с появлением эритематозных пятен.
Диагноз считается подтвержденным при наличии 4 из 11 критериев.
Лабораторная диагностика. Ниже приведены лабораторные признаки, которые могут помочь в диагностике СКВ, и указана в процентах частота их выявления у нелеченных больных.
Лабораторные признаки СКВ
Антитела к dsДНК > 80% (ds – двуспиральная) Антиядерные антитела (высокие титры; IgG)— 95% Повышение уровня IgG в сыворотке крови – 65% Снижение уровня СЗ и С4 компонентов комплемента – 60% Антитромбоцитарные антитела – 60% Криоглобулинемия – 60%
Антитела к экстрагируемым ядерным антигенам:
Антитела к фосфолипидам – 30—40%
ревматоидный фактор (низкие титры) – 30%
Биопсия кожи, выявляющая наличие отложений IgG, СЗ и С4— 75%
Увеличение СОЭ – 60%
Волчаночный антикоагулянт – 10-20%
Ложноположительная реакция Вассермана— 10%
Повышение уровня С-реактивного белка, нормального до присоединения инфекции (информативный тест для выявления присоединившейся инфекции)
По мнению Н. Chapel, M. Haeney (1995), определение LE-клеток является неспецифическим, очень нечувствительным и устаревшим методом.
При лабораторном обследовании больного обнаруживаются различные гематологические, серологические и биохимические нарушения, которые являются непосредственным следствием заболевания, обусловлены его осложнениями или вторичны и связаны с лечением.
Многие тесты (например, уровень иммуноглобулинов, уровень компонентов комплемента, наличие аутоантител) сами по себе не дают права устанавливать диагноз и должны интерпретироваться в контексте индивидуальной клинической картины.
Одним из характерных иммунологических лабораторных признаков СКВ является наличие в циркулирующей крови аутоантител, направленных к различным компонентам клетки: ядерным, мембранным структурам, сывороточным белкам. Доказано, что эти аутоантитела во многом определяют клинические особенности манифестирования СКВ. Их участие в патогенезе СКВ может быть связано либо с прямым повреждающим действием на клетку, либо с индукцией иммунной дисрегуляции, которая уже, в свою очередь, приводит к развитию заболевания.
Антиядерные (или антинуклеарные) аутоантитела реагируют с ядерными антигенами и обнаруживаются более чем у 95% больны х. Лу чше всего они выявляются с помощью метода не прямой иммуно-флюоресценции. В качестве субстратов используются различные клетки, например перевиваемой клеточной линии НЕр2 и др. При определении антиядерных аутоантител этим методом самым ответственным моментом является установление характера флуоресцентного свечения. Различают три основных вида свечения: гомогенное, кольцевидное (в виде ободка) и гранулярное (крапчатое).
Гомогенное свечение вызывают аутоантитела к dsДHK, гистонам и дезоксирибонуклеопротеинам. Гранулярное свечение вызывают аутоантитела, направленные к экстрагируемым ядерным антигенам— Sm, UT-RNP, Scl 70 (ДНК топоизомеразы 1), SS-A/Ro, SS-B/La и др. Кольцевидное свечение обнаруживается у небольшого количества больных с СКВ, осложненной гепатитом, цитопенией, васкулитом. Хотя метод непрямой иммуно-флюоресценции является очень чувствительным, однако его специфичность невелика, поэтому он используется в основном как скрининговый.
Аутоантитела к ДНК встречаются чаще всего у больных с СКВ. Различают аутоантитела к нативной (двуспиральной – ds) ДНК и од-носпиральной (ss) ДНК. Для их выявления в настоящее время используются следующие методы: радиоиммунологический, ELISE и имму-нофлюоресцентный. аутоантитела к ss-ДНК обнаруживаются при различных воспалительных и аутоиммунных заболеваниях, поэтому их выявление имеет небольшую диагностическую ценность. Напротив, высокие титры аутоантител к ds-ДНК весьма специфичны (98%) для СКВ и часто отражают активность заболевания. Однако они обнаруживаются только у 60% больных с СКВ. аутоантителам к ds-ДНК принадлежит патогенная роль в развитии СКВ, а их наличие часто ассоциируется с ранним вовлечением почек в патологический процесс. Их определение весьма целесообразно для мониторинга за активностью заболевания и эффективностью терапии.
Аутоантитела к негистоновым структурам.
1. аутоантитела к Sm (Smith) антигену и рибону-клеопротеиновым антигенам. Термин “экстрагируемые ядерные антигены” (ENA) включает два антигена – Sm и ядерный рибонуклеопротеин (nRNP). Эти антигены состоят из пяти различных уридилат – обогащенных рибонуклеопротеинов, которые связаны с белками. Они формируют функциональную единицу – сплайсеосому, которая участвует в посттрансляционном изменении мДНК. У больных с СКВ к этим функциональным единицам развиваются специфические аутоанти-тела. аутоантитела к U1-RNP получили название антиUIRNP аутоантитела; антитела к комплексу UI-U5RNP названы анти-Sm аутоантитела. Для выявления этой гетерогенной группы аутоантител используют метод иммунодиффузии (Оухтерлони), количественную иммунофлюоресценцию и иммунопреципитацию. аутоантитела к UI-RNP и Sm обнаруживаются у 40-50% и 10-30% больных СКВ соответственно. Ayто-Sm-антитела очень специфичны для СКВ. аутоантитела к UI-RNP обнаруживаются у больных с СКВ, у которых одновременно выявляется синдром Рейно и миозит либо склеродермия и полимиозит. Как правило, у больных с анти-UI-RNP аутоантителами не выявляют анти-ds-ДНК антитела, основное заболевание протекает нетяжело, поражение почек выявляется нечасто.
Вопрос о титрах, в которых выявляются антинуклеарные антитела, очень сложен с точки зрения диагностической ценности. Известно, что в разных лабораториях очень варьируют разведения нормальных сывороток (т. е., собственно титры), при которых антинуклеарные антитела продолжают определяться. Поэтому нужно придерживаться следующего правила: если титры антител в сыворотке крови больных менее, чем в 2 раза превышают титры антител в сыворотке крови здоровых лиц (в контроле), такие результаты следует считать сомнительными. Например, если в сыворотке здоровых лиц титр антител 1:16, то результаты исследования сыворотки больных с титрами антител 1:32 и даже 1:64 следует считать сомнительными. Чем выше титр антител, тем более высокая информативность их определения для постановки диагноза. Следует учитывать, что приблизительно у 2% здорового населения эти антитела могут выявляться в низких титрах.
Диагноз СКВ легко устанавливается, если больной имеет 3 или 4 типичных симптома, таких как характерная сыпь, тромбоцитопения, серозит или нефрит, антинуклеарные антитела. Однако, к сожалению, на практике чаще всего приходится иметь дело с такими жалобами, как артралгия или неспецифические проявления артрита, нечетко выраженные симптомы со стороны центральной нервной системы, в анамнезе – кожная сыпь или феномен Рейно и слабоположительный тест на антинуклеарные антитела. В таких случаях диагноз может быть предварительным и такой больной должен находиться под наблюдением врача.
Одним из дополнительных иммуногенетических признаков, в некоторых случаях позволяющих верифицировать диагноз, является определение HLA-фенотипа больного. Установлено, что продукция тех или иных антител у больных СКВ ассоциируется с определенными HLA-антигенами .Лекарственно-индуцированная СКВ. Описано достаточно большое количество случаев, когда в результате приема того или иного лекарственного средства у больных развивались расстройства, напоминающие СКВ. Одним из таких классических лекарственных средств является прокаинамид. Характерные клинические особенности такого СКВ-синдрома состоят в сравнительно умеренной выраженности симптомов, включающих артралгию, макуло-папулезную сыпь, серозит, лихорадку, анемию и лейкопению. аутоантитела при этой форме СКВ имеют определенные особенности: 1) антинуклеарные антитела, если они выявляются, то дают гомогенное свечение при иммунофлюоресцентном исследовании; 2) как правило, выявляются антигистоно-вые антитела; 3) антитела к нативной ДНК при лекарственно-индуцированной СКВ никогда не выявляются.
После отмены подозрительного препарата симптоматика исчезает через 4-6 недель, однако аутоантитела продолжают выявляться еще 6-12 месяцев.
Следует упомянуть об антифосфолипидных антителах, которые обнаруживаются приблизительно у 30% больных с СКВ. Они являются причиной различного рода тромбоэмболиче-ских осложнений, таких как инсульт, тромбоз полой (портальной) вены, тромбофлебит, эмболия легочной артерии на разном уровне и др. Наличие у больных СКВ антифосфолипидных антител во многом определяет исход заболевания. Вместе с тем, риск тромбоэмболических осложнений не у всех больных с такими антителами одинаков. Риск выше в тех случаях, когда одновременно с антифосфолипидньми антителами выявляются функциональные нарушения в системе свертывания крови. Наличие у больных СКВ антифосфолипидных антител может быть причиной положительной реакции Вассермана. Отсюда следует, что если без видимой причины выявляется положительная реакция Вассермана, то следует заподозрить наличие антифосфолипидных антител как ранний признак СКВ.
Наличие антифосфолипидных антител у женщин (в том числе и без СКВ) может быть причиной возникновения привычных выкидышей, поэтому в том случае, если в анамнезе у женщины повторяются выкидыши во втором триместре беременности, следует сделать анализ на антифосфолипидные антитела (несколько подробнее об этом см. раздел “Иммунология репродукции”).
У больных СКВ очень высок риск развития инфекционных осложнений, которые довольно часто являются причиной смерти. Чаще всего это наблюдается у больных с поражением почек и цент ра льной нервной системы, которым при ходится на значать высокие дозы гликокортикоидов и цитостатиков; при этом инфекционные осложнения вызываются оппортунистической инфекцией. Однако и у более сохранных больных СКВ склонность к инфекциям (например, системные поражения, вызванные нейсерией, сальмонеллой, грамположительными кокками) повышена. Причина этого – антителоиндуцированная лейкопения и дисфункция гранулоцитов, снижение уровня комплемента, так называемая функциональная аспления и др.
Лечение. К сожалению, стандартного лечения, которое подошло бы любому больному СКВ, не существует. В каждом отдельном случае, с учетом индивидуальной клинической картины, степени тяжести заболевания и лабораторных показателей определяется та или иная тактика лечения. Из общих рекомендаций можно отметить следующие:
- Включение в диету ненасыщенных жирных кислот;
- Запрет курения;
- Регулярная программа физических упражнений;
- Поддержание идеальной массы тела;
- Использование фотопротекторов, включая отказ от пребывания на солнце в середине дня.
При выявлении СКВ основное лечение должно быть направлено на решение двух задач:
- предотвращение антигенных стимулов или влияния факторов окружающей среды, которые могли бы послужить пусковыми механизмами активации заболевания;
- контроль за продукцией аутоантител с помощью иммуносупрессивных воздействий.
Следует учитывать, что некоторые лекарственные средства, а также вакцины могут быть причиной обострения заболевания. Часто обострение развивается после инфекций, инсоляции, стрессов и других воздействий факторов окружающей среды.

В журнале Rheumatology 06 октября 2017 г. опубликовано руководство по лечению системной красной волчанки у взрослых, подготовленное Британским обществом ревматологии.
Клинические и серологические признаки о вероятном диагнозе системной красной волчанки (СКВ):
1) СКВ является мультисистемным аутоиммунным заболеванием. Диагноз требует наличия комбинации клинических признаков и наличия как минимум одной связанной иммунологической патологии. При подозрении на СКВ необходимо проведение тестов крови, включая тесты на серологические маркеры.
2) Антинуклеарные антитела (ANA) присутствуют у около 95% пациентов с СКВ. Если тест негативен, то имеется низкая вероятность наличия СКВ у пациента. Положительный тест ANA имеется у около 5% взрослых и изолированно имеет низкую прогностическую ценность при отсутствии клинических признаков аутоиммунной ревматической болезни.
3) Наличие антител к двухцепочечной ДНК (анти-dsDNA), низкий уровень комплемента или анти-Sm (Smith) – антитела являются высокопрогностичным признаком диагноза СКВ у пациентов с соответствующими клиническими признаками. Анти Ro/La – антитела, и анти RNP – антитела являются менее специфичными маркерами СКВ, так как они обнаруживаются при других аутоиммунных ревматических болезнях и при СКВ.
4) Необходимо проведение теста на синдром антифосфолипидных антител у всех пациентов с СКВ изначально, особенно с отклонениями беременности в анамнезе, либо с артериальными/венозными тромботическими событиями. Подтверждающими тестами на антифосфолипидный синдром являются положительный волчаночный антикоагулянт, антитела к кардиолипину (IgG и IgM) и/или анти-бета-2 гликопротеин-1 (IgG и IgM) при проведении тестов 2 раза с как минимум 12 недель между тестированием.
Обследование пациентов с СКВ:
1) Клинические проявления у пациентов с СКВ зависят от активности болезни, поражений, токсичности препаратов или наличия сопутствующих заболеваний. По активности болезни, очень важно убедиться является ли это из-за активного воспаления или тромбоза, что и будет обусловливать стратегию лечения.
2) Клиническая оценка пациентов с СКВ должна включать тщательный анамнез и обзор систем, полный клинический осмотр и мониторинг основных показателей состояния организма, общий анализ мочи, лабораторные тесты, оценка состояния здоровья и качества жизни, и измерение активности болезни и степени повреждений с применением стандартных инструментов оценки СКВ. При наличии показаний необходимо проводить методы визуализации, биопсию почек и других тканей.
3) Активность болезни категоризуется на легкую, умеренную и тяжелую с периодами обострений. Легкой активностью болезни является клиническая стабильность без жизне-угрожающего вовлечения органов, с основным проявлением в виде артрита, кожно-слизистых поражений и легкого плеврита. У пациентов с умеренной активностью болезни имеются более серьезные проявления. При тяжелой активности болезни имеются жизне-угрожающие или орган-угрожающие проявления.
1) Пациенты с СКВ должны проходить мониторинг на регулярной основе на проявления болезни, токсичность препаратов и сопутствующие заболевания.
2) Пациенты с активной болезнью должны проходить контрольные осмотры как минимум каждые 1 - 3 месяца с измерением АД, общего анализа мочи, функции почек, анти-dsDNA антитела, уровень комплемента, С-реактивный белок, развернутый общий анализ крови, и печеночные тесты. Пациенты со стабильной болезнью с низкой активностью или в ремиссии могут проходить мониторинг менее часто, например каждые 6 - 12 месяцев.
3) Наличие синдрома антифосфолипидных антител связано с тромботическими событиями, повреждениями и неблагоприятными исходами при беременности. При отрицательном предыдущем тестировании, необходимо повторное тестирование до беременности или операции, либо при наличии новых тяжелых проявлений или сосудистых событий.
4) Анти-Ro/La антитела связаны с неонатальной СКВ (включая врожденной блокадой сердца) и должны быть проверены до беременности.
5) Пациенты с СКВ имеют повышенный риск сопутствующих болезней, таких как атеросклеротическая болезнь, остеопороз, аваскулярный некроз, злокачественных новообразований и инфекций. Необходимо проводить исходную и ежегодную оценку модифицируемых факторов риска, включая гипертонию, дислипидемию, диабет, высокий индекс массы тела и курение.
6) Иммуносупрессивная терапия может приводить к токсическим проявлениям. Необходимо проводить тщательный мониторинг препаратов путем лабораторных тестов и клинической оценки согласно руководствам по мониторингу препаратов.
Лечение легкой СКВ:
1) Лечение легкой орган-не-угрожающей СКВ включают болезнь-модифицирующие препараты гидроксихлорохин и метотрексат, и короткие курсы НПВС для контроля симптомов. Данные препараты позволяют избегать либо снижать дозу кортикостероидов.
2) Для поддерживающей терапии может понадобиться применение преднизолона в низкой дозе ≤ 7,5 мг/день . Возможно применение средств местного применения при кожных проявлениях и внутрисуставных инъекций при артритах.
3) Солнцезащитный крем с высоким SPF UV-A и UV-B является важным в лечении и профилактике вызываемых ультра-фиолетовым излучением поражений кожи. Необходимо информировать пациентов об избегании солнца и ношении соответствующей защитной одежды.
Лечение умеренной СКВ:
1) При лечении умеренной СКВ применяют более высокие дозы преднизолона (до 0,5 мг/кг/день), либо в/м иди в/в дозы метилпреднизолона. Для контроля активной болезни часто необходимы иммуносупрессивные препараты, позволяющие избежать стероиды. Данные препараты также снижают риск повреждений в длительном периоде.
2) Метотрексат, азатиоприн, микофенолата мофетил, циклоспорин и другие ингибиторы кальциневрина должны быть рассмотрены в случаях артрита, кожных поражений, серозитов, васкулите или цитопениях, если гидроксихлорохин оказался недостаточным.
3) В рефрактерных случаях можно рассмотреть возможность применения белимумаба или ритуксимаба.
Лечение тяжелой СКВ:
1) Пациенты с тяжелой СКВ, включая с поражением почек и нейро-психиатрическими проявлениями, нуждаются в тщательном обследовании для исключения других причин, включая инфекции. Лечение зависит от этиологии (воспалительной и/или тромботической) и необходимо соответствующее лечение с применением иммуносупрессии и/или антикоагуляции соответственно.
2) Иммуносупрессивные режимы при тяжелой активной СКВ включают в/в метилпреднизолон или пер-оральный преднизолон в высоких дозах (до 1 мг/кг/день) для приведения к ремиссии, либо изолированно, или как чаще бывает, в составе протокола лечения с другим иммуносупрессивным препаратом.
3) Микофенолата мофетил или циклофосфамид применяются при большинстве случаев волчаночного нефрита и при рефрактерных тяжелых случаях болезни без поражения почек.
4) Можно рассмотреть возможность применения биолоджиков белимумаба или ритуксимаба на индивидуальной основе, когда у пациентов неэффективны или непереносимы другие иммуносупрессивные препараты.
5) Внутривенные иммуноглобулины и плазмаферез могут быть рассмотрены для пациентов с рефрактерной цитопенией, тромботической тромбоцитопенической пурпурой, быстро ухудшающемся остром галлюциногенном состоянии и катастрофической формой антифосфолипидного синдрома.
По препаратам смотрите таблицу 1.
Подробнее смотрите в прикрепленном файле.
Посмотреть другие обзоры
Автор обзора
Автор обзоров мировой медицинской периодики на портале MedElement - врач общей практики, хирург Талант Иманалиевич Кадыров.
Закончил Киргизский Государственный медицинский институт (красный диплом), в совершенстве владеет английским языком. Имеет опыт работы хирургом в Чуйской областной больнице; в настоящий момент ведет частную практику.
Регулярное повышение квалификации: курсы Advanced Cardiac Life Support, International Trauma Life Support, Family Practice Review and Update Course (Англия, США, Канада).

Новость
Автор
Редакторы
Системная красная волчанка — это мультифакторное заболевание, развивающееся на основе генетического несовершенства иммунной системы и характеризующееся выработкой широкого спектра аутоантител к компонентам клеточного ядра. Молекулярно-генетические основы болезни изучены довольно плохо, в связи с чем специфического лечения до сих пор не создано, а в основе проводимой в клинике патогенетической терапии лежат иммунодепрессанты — глюкокортикостероиды и цитостатики. И вот, после более чем 50 лет попыток разработать специфическое лечение волчанки, произошел сдвиг: Управление по контролю за качеством пищевых продуктов и лекарств США официально утвердило в качестве лекарства от волчанки препарат Бенлиста (Benlysta) на основе моноклональных антител, специфически блокирующих B-лимфоцит-стимулирующий белок (BLyS).
Системная красная волчанка (СКВ) — одно из самых распространённых аутоиммуных заболеваний, в основе которого лежит генетически обусловленное комплексное нарушение иммунорегуляторных механизмов. При заболевании происходит образование широкого спектра аутоантител к различным компонентам ядра клеток и формирование иммунных комплексов. Развивающееся в различных органах и тканях иммунное воспаление приводит к обширным поражениям микроциркуляторного кровяного русла и системной дезорганизации соединительной ткани [1], [2].
Патогенез СКВ

Рисунок 1. Патогенез СКВ
Волчанка во многом связана с нарушениями на уровне пролиферации различных клонов В-клеток, активируемых многочисленными антигенами, в роли которых могут выступать медицинские препараты, бактериальная или вирусная ДНК и даже фосфолипиды мембраны митохондрий. Взаимодействие антигенов с лейкоцитами связано либо с поглощением антигенов антиген-презентирующими клетками (АПК), либо с взаимодействием антигена с антителом на поверхности В-клетки.
В результате поочередной активации то T-, то B-клеток увеличивается продукция антител (в том числе, аутоантител), наступает гипергаммаглобулинемия, образуются иммунные комплексы, чрезмерно и неконтролируемо дифференцируются Т-хелперы. Разнообразные дефекты иммунорегуляции, свойственные СКВ, связаны также с гиперпродукцией цитокинов Th2-типа (IL-2, IL-6, IL-4, IL-10 IL-12).
Одним из ключевых моментов в нарушении иммунной регуляции при СКВ является затрудненное расщепление (клиренс) иммунных комплексов, — возможно, вследствие их недостаточного фагоцитоза, связанного, в частности, с уменьшением экспрессии CR1-рецепторов комплемента на фагоцитах и с функциональными рецепторными дефектами.
Распространённость СКВ колеблется в пределах 4–250 случаев на 100 000 населения; пик заболеваемости приходится на возраст 15–25 лет при соотношении заболевших женщин к мужчинам 18:1. Наиболее часто заболевание развивается у женщин репродуктивного возраста с увеличением риска обострения во время беременности, в послеродовом периоде, а также после инсоляции и вакцинации.
СКВ часто становится причиной инвалидности. В развитых странах в среднем через 3,5 года после постановки диагноза 40% больных СКВ полностью прекращают работать, — в основном, в связи с нейрокогнитивными дисфункциями и повышенной утомляемостью. К потере трудоспособности чаще всего приводят дискоидная волчанка и волчаночный нефрит.
Клинические проявления СКВ чрезвычайно разнообразны: поражение кожи, суставов, мышц, слизистых оболочек, лёгких, сердца, нервной системы и т.д. У одного пациента можно наблюдать различные, сменяющие друг друга варианты течения и активности заболевания; у большинства больных периоды обострения заболевания чередуются с ремиссией. Более чем у половины больных есть признаки поражения почек, сопровождающиеся ухудшением реологических свойств крови [4].
Поскольку молекулярные и генетические механизмы, лежащие в основе заболевания, до сих пор как следует не изучены, специфического лечения волчанки до недавнего времени не существовало. Базисная терапия основана на приёме противовоспалительных препаратов, действие которых направлено на подавление иммунокомплексного воспаления, как в период обострения, так и во время ремиссии. Основными препаратами для лечения СКВ являются:
- глюкокортикоиды (преднизолон, метилпреднизолон);
- цитостатические препараты (циклофосфамид, азатиоприн, метотрексат, мофетила микофенолат, циклоспорин).
Исследователи, желая специфически блокировать BLyS, сделали ставку на человеческое моноклональное антитело, разработанное совместно с английской биотехнологической фирмой Cambridge Antibody Technology, и названное белимумаб (belimumab). В начале марта 2011 года американское Управление по контролю за качеством пищевых продуктов и лекарственных препаратов (FDA) впервые за 56 лет одобрило препарат, предназначенный для специфического лечения системной красной волчанки. Эти препаратом стал Бенлиста — коммерческое название антитела белимумаба, производством которого уже занимается компания GlaxoSmithKline. До того FDA одобряла для терапии СКВ гидроксихлорохин — лекарство от малярии; было это в 1956 году.
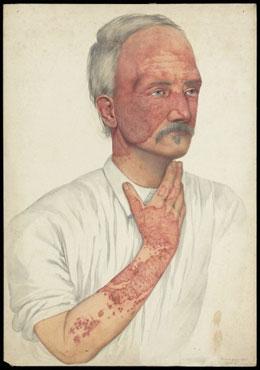
Рисунок 2. Человек, больной системной красной волчанкой (акварель 1902 года кисти Мэйбл Грин). Свое название заболевание получило ещё в средневековье, когда людям казалось, что характерная волчаночная сыпь на переносице напоминает волчьи укусы.
Целенаправленная терапия
Следующие на очереди
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Системная красная волчанка: причины появления, симптомы, диагностика и способы лечения.
Определение
Системная красная волчанка (СКВ) – это хроническое аутоиммунное заболевание неустановленной этиологии, при котором иммунная система организма становится гиперактивной и поражает здоровые ткани.
СКВ характеризуется генерализованным поражением микроциркуляторного русла и системной дезорганизацией соединительной ткани с кожными, суставными и висцеральными изменениями.
Заболеваемость СКВ составляет порядка 40-50 случаев на 100 000 населения в год. Заболевание наиболее часто развивается в течение второго и третьего десятилетий жизни у девушек и молодых женщин. Около 20% пациентов заболевают в возрасте до 16 лет.
Причины появления системной красной волчанки
Волчанка является аутоиммунным заболеванием, но точная причина возникновения болезни неясна.
Иммунная система защищает организм и борется с антигенами, такими как вирусы, бактерии и микробы. Это происходит благодаря синтезу белков, называемых антителами.
Когда человек страдает аутоиммунным заболеванием, таким как красная волчанка, иммунная система не может отличить чужеродные вещества (или антигены) от клеток собственного организма.
В результате иммунная система направляет антитела как против здоровой ткани, так и против антигенов. Это вызывает воспаление и повреждение тканей.
Поскольку точные причины возникновения системной красной волчанки до сих пор не обнаружены, ученые выдвигают теории и делают предположения. На первое место они ставят генетическую предрасположенность. Ученым удалось определить более 60 локусов (местоположений определенного гена на генетической или цитологической карте хромосомы) предрасположенности к СКВ, которые можно разделить на несколько групп. Интересно, что многие локусы риска являются общими для СКВ и других аутоиммунных заболеваний.
Одним из механизмов, запускающих аутоиммунный ответ, является ультрафиолетовое излучение, поскольку после воздействия солнечного света у пациентов на коже часто проявляются покраснения и сыпь.
Развитие болезни, по-видимому, может спровоцировать и вирусная инфекция. Нельзя исключать, что в этом случае аутоиммунные реакции возникают из-за молекулярной мимикрии вирусов — феномена сходства вирусных антигенов с собственными молекулами организма.
Гормональная теория развития СКВ может объяснить тот факт, что, во-первых, у женщин заболевание отмечается в 10 раз чаще, чем у мужчин, а во-вторых, симптомы обычно появляются в фертильном возрасте - от 15 до 45 лет и только 20% - после 50 лет.
Классификация заболевания
По характеру течения:
- острое;
- подострое;
- хроническое.
- высокая;
- умеренная;
- минимальная.
В классификации учитываются общие проявления, такие как лихорадка, поражение кожи, суставов, неврологические нарушения, воспаление оболочки сердца и легких, нарушения в кровеносной системе, поражение почек.
Симптомы системной красной волчанки
Симптомы системной красной волчанки могут быть весьма разнообразны, поэтому перечислим основные:
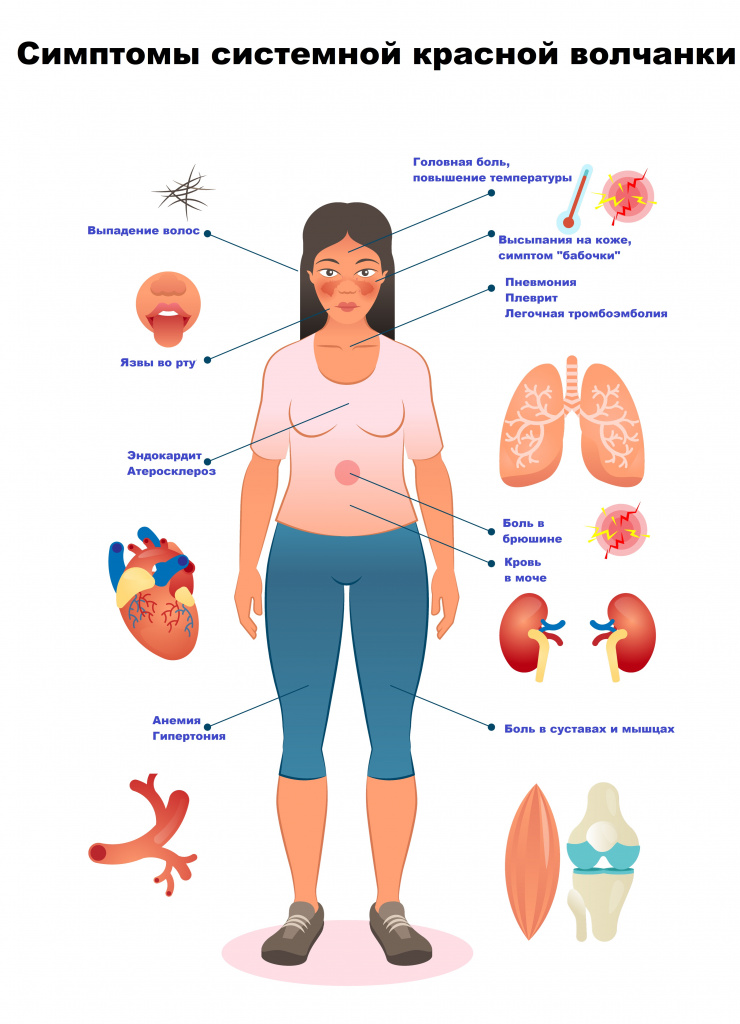
Диагностика системной красной волчанки
В первую очередь при постановке диагноза врач должен обращать внимание на жалобы и характерные симптомы заболевания. Для уточнения диагноза и оценки степени поражения потребуются следующие лабораторные и инструментальные обследования:
-
Клинический анализ крови с развернутой лейкоцитарной формулой.
Синонимы: Общий анализ крови, ОАК. Full blood count, FBC, Complete blood count (CBC) with differential white blood cell count (CBC with diff), Hemogram. Краткое описание исследования Клинический анализ крови: общий анализ, лейкоформула, СОЭ См. также: Общий анализ – см. тест № 5, Лейкоцит.
Читайте также:

