Противовирусный препарат при перитоните
Обновлено: 26.04.2024
По степени распространенности воспалительного процесса в брюшной полости выделяют:
1. Отграниченный (местный) перитонит (занимает до 2-х из девяти анатомических областей брюшной полости).
2. Распространенный перитонит (занимает три и более анатомических области живота):
По характеру экссудата: серозный, серозно-фибринозный и гнойный перитонит.
Диагностика.
Диагноз перитонита должен быть установлен на основании первичного физикального обследования.
В ходе обследования пациента в приемном отделении на основании клинико-инструментального обследования следует установить возможные причины перитонита.
В приемном отделении в экстренном порядке производят общий клинический анализ крови, биохимический анализ крови, коагулограмму, общий анализ мочи; определяют группу крови и резус-фактор; выполняются ЭКГ, рентгенография грудной клетки в прямой проекции и обзорная рентгенография брюшной полости (у лежачих больных – в латеропозиции), УЗИ брюшной полости (оценка наличия газа и жидкости в брюшной полости, дилатация кишечных петель, перистальтика); по показаниям проводятся консультации врачами терапевтических специальностей.
Лечебная тактика.
Диагноз перитонита является показанием к экстренному оперативному вмешательству. Больной подлежит экстренному оперативному вмешательству в течение 1 часа с момента установления диагноза.
Больным с выраженными явлениями интоксикации, синдромными расстройствами и с тяжелыми сопутствующими заболеваниями показано проведение кратковременной (в течение 1,5-2 часов) предоперационной подготовки в условиях реанимационного отделения. Вопрос о необходимости и объеме предоперационной подготовки больного к хирургическому вмешательству решается совместно хирургом и анестезиологом.
Любое оперативное вмешательство по поводу перитонита необходимо выполнять под эндотрахеальным наркозом.
Доступ.
- при клинической картине отграниченного перитонита,
- при необходимости проведения дифференциального диагноза (острый панкреатит, мезентериальный тромбоз),
- в случае диагностированных до операции аппендицита, холецистита и перфоративной язвы.
- при клинической картине распространенного перитонита,
- при лапароскопической находке, исключающей возможность выполнения оперативного приема лапароскопическим доступом, показано выполнение конверсии к срединной лапаротомии.
Хирургическая тактика.
Обязательными этапами оперативного вмешательства при перитонита являются:
- Забор материала для микробиологического исследования;
- Полная и планомерная ревизия брюшной полости;
- Эвакуация экссудата;
- Устранение источника перитонита;
- Санация брюшной полости;
- Назо-интестинальная интубация – по показаниям;
- Дренирование брюшной полости;
- Формирование лапаростомы для последующих программных санаций – по показаниям.
Радикальное устранение источника перитонита предусматривает:
- удаление воспаленного органа (аппендэктомия, холецистэктомия);
- герметичное ушивание перфораций и свежих сквозных ранений полых органов;
- резекцию органа (при язве, опухоли, травмах или нарушении мезентериальногокровобращения); - формирование колостомы (илеостомы) для выключения из пассажа пораженных участков толстой кишки.
При отсутствии условий для радикальной ликвидации источникаинфицирования возможна его локализация (отграничение тампонами в брюшной полости), экстраабдоминизация органа.
Формирование межкишечных анастомозов на воспаленных участках кишечных петель при гнойном перитоните противопоказано. В таких случаях целесообразно выведение концевых кишечных стом, включая, при необходимости и тощую кишку.
При правосторонней гемиколэктомии вопрос о формировании первичного илеотрансверзоанастомоза или формировании илеостомы решается индивидуально в зависимости от состояния стенки подвздошной кишки.
При резекции левой половины толстой кишки формируется одноствольная колостома.
При выраженном парезе и расширении кишечных петель более 4-5 см показано проведение декомпрессии пищеварительной трубки путем назоинтестинальной интубации на всем протяжении тонкой кишки широким 2-х канальным (неприсасывающимся) силиконовым зондом.Одновременно с установкой назо-интестинального зонда устанавливается назо-гастральный зонд.
Введение тампонов в брюшную полость допустимо только при невозможности радикального устранения источника перитонита и в целях гемостаза.
Варианты завершения операции:
· распространенный фибринозно-гнойный или каловый перитонит;
· признаки анаэробного инфицирования брюшной полости;
· тяжелый абдоминальный сепсис, септический шок;
· основное заболевание (его осложнение), не позволяющее одномоментно ликвидировать или локализовать источник перитонита;
· сопутствующее заболевание или состояние, не позволяющее выполнить адекватный объем операции;
· синдром интраабдоминальной гипертензии;
· состояние лапаротомной раны (гнойно-некротический процесс), не позволяющее ушить брюшную полость.
· прогрессирование перитонита (неустраненный первичный источник, появление нового источника, недиагностированный источник, третичный перитонит);
· осложнение основного заболевания, требующее хирургической коррекции (абсцесс, флегмона, кровотечение в брюшную полость или ЖКТ, ранняя спаечная кишечная непроходимость);
· возникновение или осложнение в послеоперационном периоде конкурирующего заболевания, требующего хирургического вмешательства (кровотечение из гастродуоденальных язв, деструктивный панкреатит, перфорация острых и стресс-язв, острое нарушение мезентериального кровотечения);
· осложнения, связанные с нарушением техники хирургического вмешательства, манипуляции (ятрогенные повреждения, несостоятельность ЖКА, несостоятельность культи или кровотечение вследствиесоскальзывание лигатуры, клипсы, инородные тела брюшной полости).
- изоляция органов брюшной полости от париетальной брюшины и лапаротомной раны перфорированной полиэтиленовой пленкой;
- сведение краев операционной раны отдельными редкими кожными швами с оставлением диастаза краев раны в 5 – 10 см; после каждой санации швы накладывать в новых местах;
Критерии окончания режима программируемых санаций:
· гарантированная ликвидация или локализация источника перитонита;
· отсутствие неудалимых очагов некроза и гнойных очагов;
· прозрачный серозный экссудат;
· наличие перистальтики тонкой кишки;
· отсутствие распространенного гнойно-некротического поражения операционной раны или передней брюшной стенки, исключающее возможность одномоментной хирургической коррекции.
Антибактериальная терапия начинаться непосредственно после установления диагноза перитонита. Первая доза антибактериального препарата вводится перед оперативным вмешательством. До получения результатов микробиологического исследования экссудата брюшной полости применяется "эмпирическое" назначение антибиотиков со спектром действия, включающим грамотрицательные бактерии в сочетании с анаэробными микроорганизмами:
- цефалоспорины (цефоперазон 4 г/сутки) + аминогликозиды (тобрамицин, сизомицин, амикацин 150 мг - 2 г/сутки) + метронидазол (1500 мг/сутки);
- офлоксацины (ципрофлоксацин 800 мг/сут) + метронидазол (1500 мг/сутки);
- карбаценемы (меропенем 3-6 г/сутки) в виде монотерапии.
После получения результатов микробиологических исследований необходима коррекция антибиотикотерапии по чувствительности микрофлоры.
Патогенетическая посиндромная терапия.
1. Инфузионно-трансфузионная терапия проводится с целью ликвидации дефицита жидкости и электролитов, коррекции КЩС с учетом показателей гомеостаза, гемодинамики, темпа диуреза в режиме умеренной гемодилюции (Ht 27-32%), при необходимости - форсированный диурез. Суточный объем инфузии 3000-3500 мл/сутки при темпе диуреза 80-100 мл/час. При восполненном ОЦК в отсутствие гипопротеинемии и снижении диуреза - стимуляция фуросемидом до 2 мг/кг/сутки. Коррекция анемии препаратами крови - при снижении гемоглобина ниже 100 г/л.
2. Коррекция метаболических нарушений:
- нормализация белкового и углеводного обменов;
- использование энергетических материалов в виде растворов декстрозы, концентрированной глюкозы (с введением адекватного количества инсулина), солей калия, коферментов (витаминов);
- введение антигистаминных средств;
- введение ингибиторов протеаз.
3. Коррекция агрегатного состояния крови, профилактика ДВС-синдрома:
- улучшение реологии крови путем создания гемодилюции и применения дезагрегантов (трентал 30-50 мл/сутки, курантил 6-8 мл/сутки, ацетилсалициловая кислота 0,5 г/сутки);
- гепаринотерапия (наиболее рационально постоянно дозированное введение гепарина 20000-30000 ед./сутки под контролем АЧТВ и тромбинового времени);
- препараты крови, содержащие факторы свертывания и фибринолиза;
- профилактика цитотоксического эффекта, мембраностабилизирующий эффект - даларгин (0,6-0,8 мг/сутки), дексазон 16-32 мг/сутки.
4. Коррекция иммунологического статуса:
- пассивная иммунизация гипериммунными плазмами и сыворотками;
- использование иммуномодуляторов (т-активин, тималин, миелопид) и препаратов неспецифической иммунокоррекции (дибазол, аскорбиновая кислота);
- ультрафиолетовая и лазерная обработка крови.
5. Постоянная декомпрессия тонкого кишечника при малых цифрах разряжения (10-20 мм. вод. ст.) с проведением кишечного лаважа растворами электролитов (СЭР - солевым электролитным раствором) в объеме 1000-1500 мл/сутки.
6. Коррекция состояния сердечно-сосудистой системы:
7. Респираторная терапия, профилактика бронхолегочных осложнений:
8. Активные методы детоксикации следует использовать при II и III степени эндогенной интоксикации:
- методом выбора считать проведение плазмафереза с момента стабилизации гемодинамики (целесообразен забор плазмы 500-1000 мл с возмещением адекватным количеством донорской плазмы и альбумина);
- в случае выраженной нефропатии целесообразно проведение гемодиализа или гемодиафильтрации;
- УФО крови (объем облученной крови 300-500 мл).
9. Обезболивание в послеоперационном периоде:
- перидуральная анальгезия растворами анестетиков, наркотических анальгетиков;
- традиционное обезболивание: наркотические и ненаркотические анальгетики.
10. Коррекция энергетического потенциала путем:
- регуляции кислородного и углеводного обменов (адекватная функция дыхания, улучшение микроциркуляции, снятие инсулиновой резистентности);
Противовирусные препараты существуют двух основных типов: один тип нацелен на клеточные органеллы, которые вирусы используют с целью их репликации, в то время как другие нацелены на некоторую специфическую активность вирусной инфекции и репликацию. Препараты, которые повреждают клеточные органеллы, имеют наименьшую вероятность быть эффективными, поскольку они имеют тенденцию оказывать негативный эффект как на клетку, так и на вирус. Наиболее полезные противовирусные методы лечения включают препараты, которые направлены на специфические регионы вирусного генома, которые регулирует ключевые процессы инфекции или репликации.
Коронавирус кошек имеет различные гены, которые схожи по активности с генами вируса иммунодефицита человека типа 1, включая РНК – зависимую полимеразу и вирусные протеазы. Ретровирусная протеаза является другой важной целью для вируса иммунодефицита человека типа 1 и комбинация ингибиторов реверсной транскриптазы, протеазы и интегразы эффективно подавляет вирус иммунодефицита человека типа 1 при хронической субклинической инфекции у большинства пациентов.
На основании опыта использования других ингибиторов вирусных протеаз, схожие препараты разрабатываются против основной протеазы (3CL), кодируемой как коронавирусами, так и норовирусами (Kimetal., 2013). Многие из структурных протеинов коронавируса сначала транскрибируются с РНК как полипротеины, которые расщепляются протеазами на компоненты. Хотя предполагается, что клеточные протеазы играют важную роль в расщеплении полипротеинов вируса инфекционного перитонита кошек, предварительные invitro тесты показали, что ингибиторы 3CL протеаз эффективны в ингибировании репликации вируса инфекционного перитонита кошек на уровнях, которые не токсичны для клеток (Kimetal., 2013).
Лекарственный препарат chloroquine, который использовался для лечения малярии, как было показано, ингибирует репликацию вируса инфекционного перитонита кошек invitro и имеет противовоспалительные эффекты (Takanoetal., 2013b). Он был протестирован при экспериментальной инфекции инфекционного перитонита кошек; хотя клинические оценки кошек в группах, леченных chloroquine, были лучше, чем оценки у кошек в группе без лечения chloroquine, уровни аланинаминотрансферазы увеличивались в группе кошек, леченных chloroquine, указывая на неблагоприятный токсический эффект.
Также показано, что циклоспорин А обладает активностью, направленную против коронавируса кошек. Pfefferle et al. (2011) продемонстрировали, что ряд иммунофиллинов сильно взаимодействует с коронавирусным неструктурным белком 1 (Nsp1) и что ингибиторы циклофиллина, такие как циклоспорин А, блокируют репликацию коронавирусов всех родов, включая человеческий, кошачий и птичий. Это подтверждает роль клеточных иммунофиллинов (циклофиллинов) в репликации коронавируса. Авторы предположили, что неиммуносупрессивные производные циклоспорина А не только служат в качестве ингибиторов широкого спектра новых коронавирусов человека, но также более широкораспостраненных коронавирусных патогенов человека и домашних животных.
Способность циклоспорина А ингибировать репликацию коронавируса кошек в культуре клеток подтверждена, но она не тестировалась in vivo (Tanaka et al., 2013). Проблема с антивирусными препаратами, такими как хлороквин или циклоспорин, состоит в том, что они работают при помощи путей, общих для клеток и вирусов. Коронавирусы используют нормальные клеточные пути для усиления их собственной репликации и противовирусные эффекты препаратов, таких как хлороквин и циклоспорин не могут быть отделены от других их эффектов на клетки и, поэтому, на хозяина. Для примера, противовирусная активность хлороквина in vivo уступала активности in vitro и наблюдались токсические эффекты у хозяина (Takano and colleagues (2013a) и Takano et al., 2013b).
Raaben et al. (2010) исследовали роль убиквитин –протеазной системы на различных этапах цикла коронавирусной инфекции с использованием ингибиторов убиквитина, таких как MG132, эпоксимицин и велкад. Эти соединения нарушают вход и последующий синтез РНК и экспрессию протеина вируса гепатита мышей, вируса инфекционного перитонита кошек и коронавируса, вызывающего тяжелый острый коронавирусный респираторный синдром. Сборка и выпуск вириона, судя по вирусу гепатита мышей, не были нарушены. Экспрессия белка вируса снижались в клетках, в которых содержание убиквитина уменьщалось. В этих условиях чувствительность клеток к вирусной инфекции не изменялась, за исключением важной роли убиквитинирования для входа
Это исследование показало, что убиквитин-протеазная система была вовлечена на многочисленных этапах цикла коронавирусной инфекции и идентифицировало ее как потенциальную цель лекарственных препаратов для лечения коронавирусной инфекции. Однако, должно быть отмечено, что в последующем исследовании не было найдено, что убиквитин-протеазная система вовлечена в цикл репликации коронавируса, вызывающего тяжелый острый респираторный синдром, что сохраняет неясность о вовлечении ее у вирусов гепатита мышей и вируса инфекционного перитонита кошек(Schneideretal., 2012).
Liuetal. (2013)разработали 5 перекрывающихся пептидов, которые были способны ингибировать репликацию вируса инфекционного перитонита кошек, с использованием одного из 5 пептидов в концентрации
Ряд препаратов имеет как противовоспалительную, так и иммуносупрессирующую активность. Преднизолон и алкилирующие препараты, такие как циклофосфамид использовались для ослабления клинических симптомов у кошек с инфекционным перитонитом, но не имеется доказательств, что они влияют на исход заболевания. В большей степени, чем использование этого менее специфичного терапевтического подхода, было уделено внимание попыткам ингибировать специфические цитокины, считающиеся важными в патогенезе инфекционного перитонита кошек. Ингибиторы тканевого фактора некроза (TNF) использовались в течение некоторого времени для ослабления некоторых симптомом инфекционного перитонита кошек.
Одним из наиболее популярных из этих препаратов является пентоксифиллин (Fischer et al., 2011).Пентоксифиллин широко использовался при инфекционном перитоните кошек, вследствие его использования для контролирования васкулитов у человека, поскольку васкулит является важным компонентом патофизиологии инфекционного перитонита кошек. Исследование 23 кошек с доказанным инфекционным перитонитом кошек было недостаточным для выявления влияния пентоксифиллина на время выживания, качество жизни или какие - либо ассоциированные с инфекционным перитонитом кошек клинические или лабораторные параметры (Fischer et al., 2011).
Иммуностимулятор полипренил(Polyprenyl ) является новейшим растительным экстрактом, по утверждениям, удлиняющий жизнь у некоторых кошек со слабо выраженными формами сухого инфекционного перитонита кошек1. Текущая популярность использования этого биологического агента основана на исследовании трех кошек, одна из которых, как сообщается, была вылечена от инфекционного перитонита кошек после длительного лечения ( Legendreand Bartges, 2009). Однако, все три кошки имели невыпотное заболевание, локализованное в одном брыжеечном лимфоузле, две кошки имели субклиническое заболевание и были здоровы в начале исследования, а третья кошка имела только слабо выраженное заболевание. Авторы сообщали, что лечение не дало эффекта у кошек с более тяжелой формой заболевания, такой как выпотной инфекционный перитонит кошек, хотя результаты не были представлены к этому времени. Авторы также не считают, что кошки с таким локализованным заболеванием могут потенциально подвергаться спонтанной ремиссии.
Последующие испытания полипренила, которые исключали кошек с выпотной формой инфекционного перитонита кошек и кошек с тяжелым заболеванием (преимущественно вследствие сухой формы инфекционного перитонита кошек) показали только 5% выживаемость в течение года. Поэтому, нет доказательств, что полипренил оказывает лечебный эффектв при инфекционном перитоните кошек в любой форме и нет доказательств, что он может значительно увеличивать продолжительность жизни, даже у кошек со слабовыраженной формой заболевания.
Должно быть подчеркнуто, что использование всех таких биологических иммуностимуляторов для лечения инфекционного перитонита кошек является нелицензированным, поскольку большинство из них было условно лицензировано или лицензировано для использования у кошек с вирусной лейкемией кошек или вирусным иммунодефицитом кошек или, в случае с полипренилом, герпесвирусом кошек. Кроме того, эти соединения могут быть дорогими, с отсутствием доказательств значительной пользы. Режим дозирования для таких препаратов часто неопределен и часто основывается больше на ограничении денежных затрат для владельцев за счетн назначения маленьких доз или менее частого лечения.
Заболевание, похожее на инфекционный перитонит кошек, у домашних хорьков
Эпизоотический катарральный энтерит, вызванный новым коронавирусом, был сначала описан у домашних хорьков в США в 1993 г.(Murray et al., 2010) В последующем, заболевание, идентичное по проявлениями сухой форме инфекционного перитонита кошек, также было описано ы США (Murray et al., 2010) Вирус, вызывающий эпизоотический катаральный энтерит (ECE) был назван ECE вирус (ECEV), в то время как вирус, вызывающией заболевание, похожее на инфекционный перитонит кошек, стало называться системным коронавирусом хорьков (FRSCV). Эти инфекции, в последующем, наблюдались у домашних хорьков в Японии и Европе (Michimae et al, 2010, Wise et al, 2010 и Provacia et al, 2011). Генетический анализ ECEVs и FRSCVs показал, что оба коронавируса были близко связаны, но были генетически уникальны (Wise et al., 2010). Интересно, что функциональные мутации гена ORF 3c, напоминающие мутации вируса инфекционного перитонита кошек, наблюдались у 2/3 изолятов FRSCV от хорьков, но не имелись в ECEVs.
Тот факт, что коронавирус хорьков существует в различных генетических формах показывает, что коронавирусы существуют у видов в течение некоторого времени. Новый коронавирус хорьков развивался, что наиболее вероятно, за счет мутирования, которое вызывает инфекционный перитонит? Поскольку хорьки становятся все более популярны в качестве домашних животных, они сталкиваются с теми же факторами риска, с которыми сталкивались кошки, когда они становились все более популярны в качестве домашних животных? Аналогичные мутации ответственны за системное заболевание как у коронавирусов кошек, так и коронавирусов хорьков? Эти вопросы остаются без ответа.
Заключение
Диагностика инфекционного перитонита кошек не должна быть трудной. Это заболевание, в основном, встречается у котят и молодых кошек, находящихся в окружении значительного количества кошек, таких как приюты, спасательные организации для кошек/котят или питомники. Представленные данные анамнеза и симптомы при физикальном обследовании, при выпотной или при сухой форме, относительно стереотипны и результаты стандартного общего анализа крови, показатели сывороточного белка, альбумина и глобулина часто подтверждают подозрения, возникшие после получения анамнеза и выполнения физикального обследования. Желтого цвета, слизеподобный воспалительный перитонеальный (или превральный ) выпот характерен для выпотной формы заболевания, в то время как неврологические симптомы, увеит и массы в илеоцекальном регионе, почках и мезентериальных лимфоузлах характерны для сухой формы инфекционного перитонита кошек.
Титры антител против коронавируса могут вводить в заблуждение в диапазоне 1:25–1:1600, но из значение все более актуально при более высоких титрах. Макро и и микроскопические находки при посмертном исследовании часто недооцениваются и им следует придавать большее значение. Иммуногисохимия и RT-PCR в реальном времени очень полезны для идентификации антигена вируса инфекционного перитонита кошек в пораженных тканях или выпотах и, если все сделано правильно, могут обеспечить окончательный диагноз. Чашей Грааля для диагностики инфекционного перитонита кошек является простой тест крови, который бы выявлял вирус инфекционного перитонита кошек, ассоциированный с активным заболеванием, а не кишечную форму коронавируса или мутантов кишечной формы, которые неспособны вызывать инфекционный перитонит кошек.
В настоящее время не имеется эффективного лечения инфекционного перитонита кошек и смертность крайне высока. Однако, тот факт, что в очень редких случаях некоторые кошки спонтанно выздоравливают при наличии хорошего поддерживающего ухода, является достаточным стимулом, чтобы владельцы пытались пробовать применять различные альтернативные методы лечения, которые рекламируются, главным образом, в Интернете. Многие из этих видов лечения дороги. Важно, чтобы такие способы лечения были адекватно тестированы на адекватном количестве кошек с подтвержденном заболеванием и был использован рандомизированный, плацебо –контролируемый и двойной слепой способ.
Наиболее перспективные способы лечения будут, вероятно, включать препараты, которые специфически нацелены на вирусные белки, важные для вирусной репликации. Коронавирусы имеют большие геномы с многими потенциальными генами – мишенями и, надеюсь, безопасные и эффективные противовирусные препараты будут созданы. Предполагается, что такие препараты могут быть разработаны в качестве ответвления научных исследований, направленных на изучение новых и высокофатальных коронавирусных инфекций у человека.
Перитонит – локальное или диффузное воспаление серозного покрова брюшной полости – брюшины. Клиническими признаками перитонита служат боль в животе, напряжение мышц брюшной стенки, тошнота и рвота, задержка стула и газов, гипертермия, тяжелое общее состояние. Диагностика перитонита основывается на сведениях анамнеза, выявлении положительных перитонеальных симптомов, данных УЗИ, рентгенографии, вагинального и ректального исследований, лабораторных тестов. Лечение перитонита всегда хирургическое (лапаротомия, санация брюшной полости) с адекватной предоперационной и послеоперационной антибактериальной и дезинтоксикационной терапией.
МКБ-10
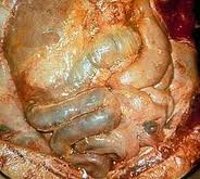
Общие сведения
Перитонит – тяжелое осложнение воспалительно-деструктивных заболеваний органов брюшной полости, сопровождающееся выраженными местными и общими симптомами, развитием полиорганной недостаточности. Летальность от перитонита в гастроэнтерологии составляет 20-30%, а при наиболее тяжелых формах достигает 40-50%.
Брюшина (peritoneum) образована двумя переходящими друг в друга серозными листками - висцеральным и париетальным, покрывающими внутренние органы и стенки брюшной полости. Брюшина является полупроницаемой, активно функционирующей мембраной, выполняющей множество важных функций: резорбтивную (всасывание экссудата, продуктов лизиса, бактерий, некротических тканей); экссудативную (выделение серозной жидкости), барьерную (механическая и противомикробная защита органов брюшной полости) и др. Важнейшим защитным свойством брюшины является ее способность к отграничению воспаления в брюшной полости благодаря фиброзным спайкам и рубцам, а также клеточным и гуморальным механизмам.

Причины перитонита
Этиологическим звеном при перитоните выступает бактериальная инфекция, в большинстве случаев представленная неспецифической микрофлорой желудочно-кишечного тракта. Это могут быть грамотрицательные (энтеробактер, кишечная палочка, протей, синегнойная палочка) и грамположительные (стафилококки, стрептококки) аэробы; грамотрицательные (фузобактерии, бактероиды) и грамположительные (эубактерии, клостридии, пептококки) анаэробы. В 60-80% наблюдений перитонит вызывается ассоциацией микробов – чаще кишечной палочкой и стафилококком. Реже развитие перитонита бывает обусловлено специфической микрофлорой – гонококками, гемолитическим стрептококком, пневмококками, микобактериями туберкулеза. Поэтому для выбора рационального лечения перитонита первостепенное значение имеет бактериологический посев содержимого брюшной полости с определением чувствительности выделенной микрофлоры к антибактериальным препаратам.
В соответствии с этиологией различают первичные (идиопатические) и вторичные перитониты. Для первичных перитонитов характерно проникновение микрофлоры в брюшную полость лимфогенным, гематогенным путем или по фаллопиевым трубам. Непосредственное воспаление брюшины может быть связано с сальпингитами, энтероколитами, туберкулезом почек или гениталий. Первичные перитониты встречаются нечасто – в 1-1,5% случаев.
В клинической практике гораздо чаще приходится сталкиваться с вторичными перитонитами, развивающимися вследствие детсруктивно-воспалительных заболеваний или травм брюшной полости. Наиболее часто перитонит осложняет течение аппендицита (перфоративного, флегмонозного, гангренозного), прободной язвы желудка или 12-перстной кишки, пиосальпинкса, разрыва кисты яичника, кишечной непроходимости, ущемления грыжи, острой окклюзии мезентериальных сосудов, болезни Крона, дивертикулита, флегмонозно-гангренозного холецистита, панкреатита, панкреонекроза и др. заболеваний.
Посттравматический перитонит развивается вследствие закрытых и открытых повреждений органов брюшной полости. Причинами послеоперационных перитонитов могут служить несостоятельность анастомозов, дефекты наложения лигатур, механическое повреждение брюшины, интраоперационное инфицирование брюшной полости, гемоперитонеум при неадекватном гемостазе. Отдельно выделяют канцероматозные, паразитарные, гранулематозные, ревматоидные перитониты.
Классификация
По этиологии различают бактериальные и абактериальные (асептические, токсико-химические) перитониты. Последние развиваются в результате раздражения брюшины агрессивными неинфекционными агентами (желчью, кровью, желудочным соком, панкреатическим соком, мочой, хилезной жидкостью). Абактериальный перитонит довольно быстро принимает характер микробного вследствие присоединения инфекционных возбудителей из просвета ЖКТ.
В зависимости от характера перитонеального выпота различают серозный, фибринозный, геморрагический, желчный, гнойный, каловый, гнилостный перитонит.
По клиническому течению перитониты делятся на острые и хронические. С учетом распространенности поражения по поверхности брюшины различают отграниченный (местный) и диффузный перитонит. К вариантам местного перитонита относят поддиафрагмальный, аппендикулярный, подпеченочный, межкишечный, тазовый абсцессы. О диффузном перитоните говорят, когда воспаление брюшины не имеет тенденции к ограничению и четких границ. По степени поражения брюшины диффузные перитониты подразделяются на местные (развивающиеся в одной анатомической области, вблизи от источника инфекции), распространенные (охватывают несколько анатомических областей) и общие (при тотальном поражении брюшины).
В развитии перитонита принято выделять раннюю фазу (до 12 часов), позднюю (до 3-5 суток) и конечную (от 6 до 21 дня от начала заболевания). В соответствии с патогенетическими изменениями различают реактивную, токсическую и терминальную стадии перитонита. В реактивную стадию перитонита (24 часа от момента поражения брюшины) отмечается гиперергическая реакция на раздражение брюшины; в эту фазу максимально выражены местные проявления и менее выражены общие симптомы. Токсическая стадия перитонита (от 4 до 72 часов) характеризуется нарастанием интоксикации (эндотоксическим шоком), усилением и преобладанием общих реакций. В терминальной стадии перитонита (позднее 72 часов) происходит истощение защитно-компенсаторных механизмов, развиваются глубокие нарушения жизненно важных функций организма.
Симптомы перитонита
В реактивном периоде перитонита отмечаются абдоминальные боли, локализация и интенсивность которых определяются причиной воспаления брюшины. Первоначально боль имеет четкую локализацию в области источника воспаления; может иррадиировать в плечо или надключичную область вследствие раздражения нервных окончаний диафрагмы гнойно-воспалительным экссудатом. Постепенно боли распространяются по всему животу, становятся незатихающими, теряют четкую локализацию. В терминальном периоде в связи с параличом нервных окончаний брюшины болевой синдром становится менее интенсивным.
Характерными симптомами перитонита служат тошнота и рвота желудочным содержимым, которые в начальной стадии возникают рефлекторно. В более поздние сроки перитонита рвотная реакция обусловлена парезом кишечника; в рвотных массах появляется примесь желчи, затем - содержимое кишечника (фекальная рвота). Вследствие выраженного эндотоксикоза развивается паралитическая кишечная непроходимость, клинически проявляющаяся задержкой стула и неотхождением газов.
При перитоните, даже в самой ранней стадии, обращает на себя внимание внешний вид больного: страдальческое выражение лица, адинамия, бледность кожных покровов, холодный пот, акроцианоз. Пациент принимает вынужденное положение, облегчающее боль – чаще на боку или спине с поджатыми к животу ногами. Дыхание становится поверхностным, температура повышенная, отмечается гипотония, тахикардия 120-140 уд. в мин., не соответствующая субфебрилитету.
Диагностика
Изменения в общем анализе крови при перитоните (лейкоцитоз, нейтрофилез, увеличение СОЭ) свидетельствуют о гнойной интоксикации. Лапароцентез (пункция брюшной полости) и диагностическая лапароскопия показаны в неясных для диагностики случаях и позволяют судить о причине и характере перитонита.
Лечение перитонита
Выявление перитонита служит основанием для экстренного хирургического вмешательства. Лечебная тактика при перитоните зависит от его причины, однако во всех случаях в ходе операции придерживаются одинакового алгоритма: показано выполнение лапаротомии, проведение изоляции или удаления источника перитонита, осуществление интра- и послеоперационной санации брюшной полости, обеспечение декомпрессии тонкой кишки.
Послеоперационное ведение пациентов с перитонитом включает инфузионную и антибактериальную терапию, назначение иммунокорректоров, переливание лейкоцитарной массы, внутривенное введение озонированных растворов и др. Для противомикробной терапии перитонита чаще используется комбинация цефалоспоринов, аминогликозидов и метронидазола, обеспечивающая воздействие на весь спектр возможных возбудителей.
С целью стимуляции перистальтики и восстановления функций ЖКТ показано назначение антихолинэстеразных препаратов (неостигмина), ганглиоблокаторов (димеколония йодид, бензогексония), антихолинэргических средств (атропина), препаратов калия, физиопроцедур (электростимуляции кишечника, диадинамотерапии).
Прогноз и профилактика
Успех лечения перитонита во многом зависит от срока выполнения операции и полноты объема послеоперационной терапии. Летальность при разлитом перитоните достигает 40% и более; гибель пациентов наступает от гнойной интоксикации и полиорганной недостаточности.
Поскольку большинство перитонитов являются вторичными, их профилактика требует своевременного выявления и лечения основной патологии - аппендицита, язвы желудка, панкреатита, холецистита и др. Предупреждение послеоперационного перитонита включает адекватный гемостаз, санацию брюшной полости, проверку состоятельности анастомозов при абдоминальных операциях.
Перитонит — это воспаление брюшины, которая покрывает внутреннюю брюшную стенку и покрывает органы в брюшной полости, — обычно вызванное бактериальной или грибковой инфекцией.
Причины
Выстилка живота (брюшина) покрывает внутренние органы, такие как почки, печень и кишечник. Если слизистая оболочка инфицируется, внутренние органы, которые она покрывает, также могут быть повреждены.
Чаще всего это происходит из-за таких вещей, как:
- разрыв язвы желудка
- разрыв аппендикса
- проблемы с пищеварением, такие как болезнь Крона или дивертикулит
- панкреатит
- хирургическое повреждение желудка
- воспалительные заболевания органов малого таза
- цирроз печени
Редко, если бактерии попадают в оборудование для перитонеального диализа, используемое для лечения людей с почечной недостаточностью, это также может вызвать инфекцию.
Симптомы
Перитонит может быть опасным для жизни, если его своевременно не лечить. Немедленно обратитесь к врачу, если у вас:
- боль в животе или болезненность
- вздутие живота или ощущение полноты в животе
- лихорадка
- тошнота и рвота
- потеря аппетита
- диарея
- жажда
- усталость
- путаница в голове

Если вы проходите перитонеальный диализ, симптомы перитонита также могут включать:
- Мутная диализная жидкость
- Белые пятна, нити или сгустки (фибрин) в диализной жидкости
Немедленно обратитесь за медицинской помощью, если у вас появились настолько сильные боли в животе, что вы не можете сидеть спокойно или найти удобное положение.
Позвоните врачу или обратитесь за неотложной медицинской помощью, если у вас сильная боль в животе после несчастного случая или травмы.
Диагностика
Важно сразу выяснить, есть ли у вас перитонит. Это может очень быстро привести к серьезным проблемам со здоровьем.
Перитонит часто диагностируется путем анализа образца инфицированной жидкости, взятой из живота (брюшной полости).
Другие тесты на перитонит могут включать:
- рентген брюшной полости
- анализы крови и мочи
- компьютерная томография
- МРТ
Как лечить?
Если у вас диагностирован перитонит, вам потребуется лечение в больнице, чтобы избавиться от инфекции. Это может занять от 10 до 14 дней.
Лечение обычно включает введение антибиотиков в вену (внутривенно).
Если у вас перитонит, вызванный лечением диализом почек, антибиотики могут быть введены непосредственно в слизистую оболочку желудка.
Помощь с приемом пищи во время лечения
Питательная трубка может быть введена в ваш желудок через нос или помещена в желудок с помощью хирургической операции.
Если питательную трубку использовать нельзя, жидкие питательные вещества можно вводить непосредственно через вену.
Профилактика
Часто перитонит, связанный с перитонеальным диализом, вызывается микробами вокруг трубки (катетера). Если вы проходите перитонеальный диализ, выполните следующие действия для предотвращения перитонита:
- Вымойте руки, в том числе под ногтями и между пальцами, прежде чем прикасаться к катетеру.
- Каждый день очищайте кожу вокруг катетера антисептиком.
- Надевайте хирургическую маску во время обмена диализной жидкости.
Если у вас раньше был перитонит или если у вас скопление перитонеальной жидкости из-за такого заболевания, как цирроз печени, ваш врач может назначить антибиотики для профилактики перитонита.
Читайте также:

