Протокол лечения вирусного гепатита с беларусь
Обновлено: 23.04.2024
Вирусный гепатит C (HCV) – это инфекционное заболевание печени, развивающееся в результате инфицирования вирусом гепатита С. Передача данного вируса осуществляется с кровью, например, при переливании крови или ее препаратов, введении наркотических и иных веществ, при котором не соблюдаются правила стерилизации медицинского инструментария. Группами риска для заражения вирусным гепатитом С являются больные, которым переливали кровь, больные гемофилией и наркоманы. Возможен также и половой путь передачи, но он встречается значительно реже по сравнению с парентеральным (внутривенным) путем. В редких случаях вирус гепатита С может передаваться от матери к ребенку в период беременности и родов. Это происходит в том случае, если беременная женщина переносит гепатит С в острой форме или у неё обострение хронического гепатита С.
Гепатит С может быть острым или хроническим.
Острый гепатит −это воспалительный процесс в печени, который возникает в течение первых 6 месяцев после инфицирования вирусом гепатита С. Для большинства людей, острый гепатит С приводит к хронической инфекции.
Хронический гепатит С является долгосрочной болезнью, которая возникает, когда вирус гепатита С остается в теле человека. Хроническая форма может продолжаться всю жизнь и привести к серьезным проблемам печени, включая цирроз (рубцевание печени) или рак печени. Примерно у 75% -85% людей, инфицированых вирусом гепатита С, развивается хроническая инфекция.
Другой особенностью вирусного гепатита С является крайне медленное его прогрессирование. Так, хронический гепатит может развиваться спустя 10 лет после инфицирования, а цирроз или злокачественное перерождение клеток печени – спустя несколько десятилетий.
Большинство людей, инфицированных хроническим гепатитом С, не имеют никаких симптомов и не догадываются о своем заболевании. Часто эту инфекцию выявляют случайно при обращении к врачу по другому поводу. Повышенному риску инфицирования вирусом гепатита С подвержены:
- Потребители внутривенных форм наркотиков;
- Пациенты, получавшие донорскую кровь, продукты крови или органы (особенно до 1992 года, когда тестирование на данную инфекцию не проводилось, гемодиализ);
- Люди, сделавшие пирсинг, прокалывание ушей или татуировки нестерильными инструментами;
- Медицинские работники, работающие с пациентами, позитивными к вирусу гепатита С;
- ВИЧ-инфицированные лица;
- Дети, рожденные от матерей, инфицированных вирусом гепатита С.
Маркеры гепатита С
Антитела (маркеры) вируса гепатита С (анти-HCV) – первый анализ, который необходимо сделать при подозрении на инфицированность гепатитом С.Антитела к гепатиту C – это не сам вирус, а белки, вырабатываемые иммунной системой, в ответ на попадание вируса в организм. Антитела бывают разных классов и могут выявляться долго, иногда пожизненно, даже при отсутствии самого вируса. Если этот анализ отрицательный, то гепатитом Вы никогда не болели. Исключение составляют только случаи недавнего инфицирования (не более 6 месяцев). В течение этого времени антитела могут еще не появиться в крови. Положительный же тест на определение антител означает, что организм имел контакт с вирусом. По разным причинам (у беременных женщин, у пациентов с некоторыми инфекциями, при наличии некоторых особенностей иммунной системы) этот анализ может давать ложно-положительные (анализ положительный, но инфекции на самом деле нет) и ложно-отрицательные результаты (анализ отрицательный, но инфекция на самом деле есть). Именно поэтому для более точной диагностики гепатита С выполняются другие исследования.
Антитела к индивидуальным белкам вируса гепатита С (спектр) – это специфические антитела к отдельным структурным и неструктурным белкам вируса гепатита С. Их определяют для суждения о вирусной нагрузке, активности инфекции, риске хронизации, разграничении острого и хронического гепатита, степени поражения печени.
Подтверждение наличия антител к вирусу гепатита С – метод выявления инфицированности гепатитом С посредством обнаружения в крови специфических антител, образующихся к белкам вируса гепатита С (сore, NS1 NS2, NS3, NS4, NS5) с целью подтверждения предварительных исследований на гепатит С при получении положительных или сомнительных результатов в исследовании на определение антител к вирусному гепатиту С. Исследование считается положительным, если выявляются антитела к 2 или более белкам вируса гепатита С.
Выявление антител к вирусу гепатита С не позволяет определить различия между текущей инфекцией и перенесенной инфекцией. Для подтверждения диагноза активной инфекции гепатита С необходимо сделать анализ на наличие РНК методом полимеразно-цепной реакции.
Определение РНК вирусного гепатита С
ОПРЕДЕЛЕНИЕ РНК ВИРУСА ГЕПАТИТА С методом ПЦР – основной метод диагностики, позволяющий непосредственно выявить генетический материал вируса гепатита С в сыворотке крови и тканях человеческого организма. Это исследование помогает подтвердить инфицирование и дает информацию об активности и скорости размножения вирусов в организме. Выявление РНК HCV в крови при положительных результатах ИФА (определение антител к HCV) подтверждает наличие гепатита С у пациента. ПЦР – диагностика – основной метод для диагностики ранних (острых) форм гепатита С, при которых в крови еще не определяются антитела.
КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ РНК ВИРУСА ГЕПАТИТА С – это тест на определение количества единиц РНК вируса гепатита С, которые присутствуют в определенном объеме крови (обычно это 1 мл, что соответствует 1 кубическому сантиметру). Это количество выражается в цифрах, единицы измерения – копии/мл. Данный тест используется при оценке эффективности лечения.
ГЕНОТИПИРОВАНИЕ РНК ВИРУСА ГЕПАТИТА С – это анализ на определение генетической вариации вируса гепатита С. Существует более 10 генотипов вируса гепатита С, но для клинической практики достаточно определять 5, наиболее распространенных в Беларуси, типов : 1a, 1b, 2,3а/3b. Выявление генотипа (генотипирование) важно для определения продолжительности лечения, что весьма актуально учитывая широкий спектр побочных действий интерферона и низкую переносимость этого препарата больными.
Лечение вирусного гепатита С
По данным ВОЗ в настоящее время доступ к лечению гепатита С улучшается, но остается ограниченным. В 2015 г. из 71 миллиона человек с инфекцией ВГС в мире 20% (14 миллионов) знали о своем диагнозе. В 2015 г. лечение начали 7,4% людей с поставленным диагнозом (1,1 миллиона человек). В 2016 г. лечение получали на 1,76 миллиона человек больше, и глобальный охват лечением гепатита С возрос до 13%. Для достижения цели по охвату лечением 80% нуждающихся в нем людей к 2030 г. необходима значительная активизация усилий.
Ну, а каждый здоровый человек должен осознать высокую опасность, которую несет в себе вирус гепатита С и предпринимать все доступные для человека меры профилактики, чтобы не оказаться инфицированным вирусом гепатита С.
Что такое гепатит А (болезнь Боткина)? Причины возникновения, диагностику и методы лечения разберем в статье доктора Александрова Павла Андреевича, инфекциониста со стажем в 14 лет.
Над статьей доктора Александрова Павла Андреевича работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Вирусный гепатит А (Hepatitis A viruses, HAV) — острое инфекционное заболевание, вызываемое вирусом гепатита А, клинически характеризующееся синдромом общей инфекционной интоксикации, синдромом нарушения пигментного обмена, синдромами энтерита, холестаза, увеличением печени и в некоторых случая селезёнки, сопровождающееся нарушением функции печени, преимущественно доброкачественного течения.
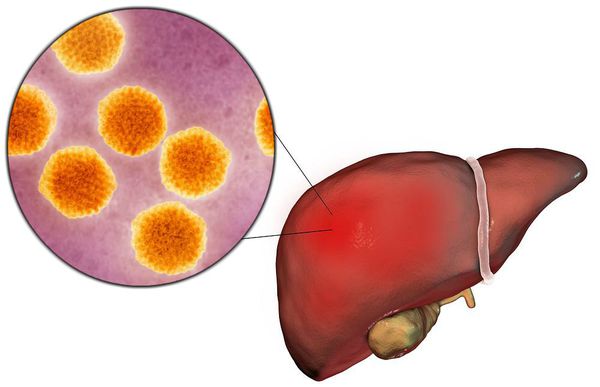
Этиология
семейство — пикорнавирусы (Picornaviridae)
вид — вирус гепатита А (HAV)
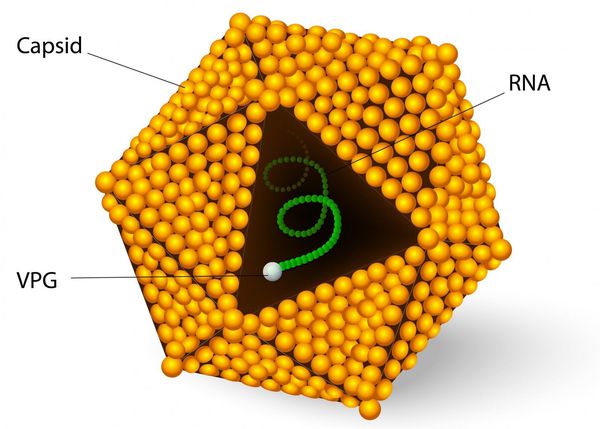
Во внешней среде очень устойчив: при температуре окружающей среды около 4°C сохраняется несколько месяцев, при 2°C — несколько лет, при замораживании очень длительно, при комнатной температуре — несколько недель. В растворе хлорсодержащих средств (0,5-1 мг/л) гибнет в течение часа, при 2,0-2,5 мг/л — в течение 15 минут, ультрафиолетовое облучение приводит к гибели в течение минуты, при кипячении сохраняется до 5 минут. В кислой среде желудка не погибает.
Наиболее значимым маркером вирусного гепатита А являются антитела класса М (анти-HAV IgM), которые образуются в начальный период заболевания и выявляются до 5 месяцев. Появление анти-HAV IgG (маркера перенесённой ранее инфекции) начинается с 3-4 недели заболевания. Антиген вируса выявляется в каловых массах за 7-10 дней до начала манифестных (явно выраженных) проявлений болезни. [1] [2] [4]
Эпидемиология
Заражение гепатитом А происходит при контакте с источником инфекции — живым человеком (больной различными формами заболевания и вирусоноситель). Больные с типичными формами являются главным источником распространения вируса (от конца скрытого и всего желтушного периодов).
Ежегодно в мире регистрируется примерно 1,5 млн случаев заболевания (количество субклинических и бессимптомных форм сложно даже представить). Смертность по миру в 2016 г., по данным ВОЗ, составила 7134 человек [10] .
Условно существует территориальное распределение по уровням инфицирования населения: высокий, средний и низкий.
Районы с высоким уровнем инфицирования это преимущественно Юго-Восточная Азия, Средняя Азия, Африка, Центральная Америка (плохие санитарные условия и низкий доход) — большинство населения к периоду взросления уже переболели и имеют иммунитет, вспышки болезни встречаются редко.
Районы со средним уровнем инфицирования — страны с переходной экономикой, развивающиеся, имеющие различия в санитарно-гигиенических условиях на территории одного региона, например Россия (большая часть населения к периоду взросления не болела и не имеет иммунитета к вирусу, возможны большие вспышки болезни).
Районы с низким уровнем инфицирования — развитые страны с высоким уровнем дохода и хорошими санитарно-гигиеническими условиями, например США, Канада, Европа, Австралия. Большинство людей не имеет иммунитета и не болела, вспышки случаются редко и чаще среди групп риска [7] .
В окружающую среду вирус выделяется преимущественно с фекалиями.
Механизм передачи: фекально-оральный (пути — водный, контактно-бытовой, пищевой), парентеральный (редко при переливании крови), половой (орально-анальный контакт).
Восприимчивость населения высокая.
Факторы риска заражения:
- высокая скученность населения;
- несоблюдение правил личной гигиены и правил хранения, обработки и приготовления продуктов питания;
- неудовлетворительное состояние объектов водоснабжения;
- бытовой очаг заболевания.
Кто находится в группе риска
- путешественники (особенно в страны жаркого климата и с плохими социальными условиями);
- гомосексуалисты;
- люди, употребляющие наркотики (любые), алкоголики;
- медработники (непривитые и не болевшие);
- бездомные;
- люди, имеющие постоянные контакты (в силу профессии или иных причин) с мигрантами из неблагополучных по гепатиту А регионов.
Характерна осенне-весенняя сезонность, повышенная привязанность к жарким южным регионам.
Иммунитет после перенесённого заболевания стойкий, пожизненный, то есть повторно заболеть нельзя [1] [3] [4] [7] [10] .
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы гепатита А
Заболевание начинается постепенно. Инкубационный период гепатита А протекает 7-50 дней.
Синдромы вирусного гепатита А:
- общей инфекционной интоксикации;
- нарушения пигментного обмена (желтуха);
- энтерита (воспаление слизистой тонкой кишки);
- холестаза (уменьшение количества желчи, поступающей в двенадцатиперстную кишку);
- гепатолиенальный (увеличение печени и селезёнки);
- отёчный;
- нарушения функции печени.
Типичное течение болезни — это желтушная форма болезни средней степени тяжести (устаревшее название — желтуха или болезнь Боткина).
Начальный период болезни (преджелтушный) имеет продолжительность от 2 до 15 дней и может протекать по нескольким вариантам:
При осмотре обнаруживается увеличение печени и, в меньшей степени, селезёнки, чувствительность края печени, повышение ЧСС (пульса), носовые кровотечения. В конце периода моча темнее, а кал становится светлее.
Следующий период (желтушный) длительностью около 7-15 дней характеризуется снижением выраженности симптомов предшествующего периода (то есть с появлением желтухи самочувствие улучшается). Усиливается желтушное окрашивание склер, кожных покровов и слизистой оболочки ротоглотки. Моча приобретает цвет тёмного пива, кал белеет. Присутствует общая слабость, недомогание, плохой аппетит, чувство тяжести и переполненности в правом подреберье, больной расчёсывает себя из-за зуда кожи (лихенификация), появляются петехии (мелкие кровоизлияния) на коже.
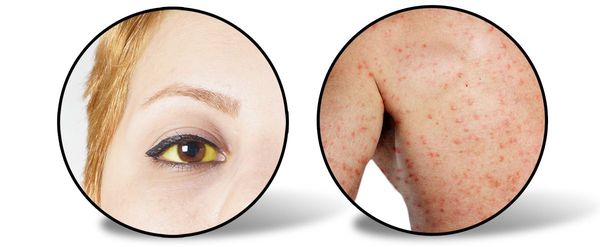
При врачебном исследовании выявляется увеличение печени и селезёнки, явственно положителен симптом Ортнера (болезненность при поколачивании ребром ладони по правой рёберной дуге), гипотония (может быть и нормотония), токсическая брадикардия (снижение ЧСС), появляются периферические отёки, возможны боли в суставах (артралгии).
Далее при благоприятном течении заболевания (которое наблюдается в большинстве случаев) происходит регресс клинической симптоматики, осветление мочи и потемнение кала, более медленное спадение желтушности кожи, склер и слизистых оболочек.
Под нетипичным течением болезни подразумеваются лёгкие безжелтушные формы гепатита А (отсутствие симптомов или лёгкая слабость без желтухи, тяжесть в правом подреберье), фульминантные формы.
Факторы, увеличивающие риск тяжёлого течения гепатита А:
Последствия для беременных
У беременных гепатит А протекает в целом несколько тяжелее, чем у небеременных. Примерно в 36 % случаев возможно развитие слабости родовой деятельности, преждевременные роды (31-37 неделя) и послеродовые кровотечения. Вирус не проникает через плаценту, то есть какого-то специфического действия на плод не оказывает. В грудном молоке вирус не содержится [1] [2] [4] [7] .
Патогенез гепатита А
Воротами для проникновения вируса является слизистая оболочка органов желудочно-кишечного тракта, где происходит его первичное размножение в эндотелиальной выстилке тонкого кишечника и мезентериальных лимфоузлах.
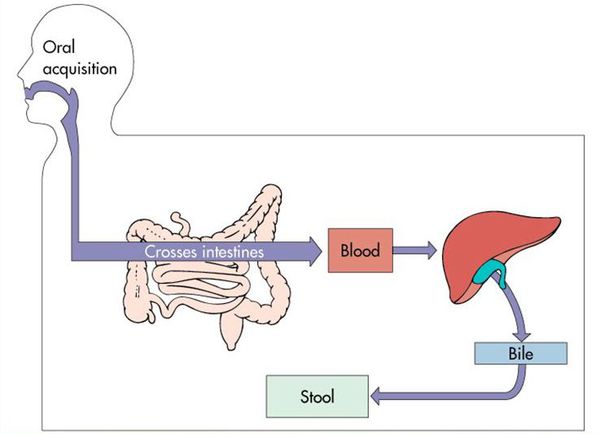
Далее происходит гематогенное распространение вирусных частиц и проникновение их в печень, где они локализуются в ретикулогистиоцитарных клетках Купфера и гепатоцитах. В результате этого происходит повреждение клеток:
- проникновение вируса в клетку;
- захват лизосомой;
- разрушение белковой оболочки вируса;
- сборка белков по программе вирусной РНК;
- встраивание этих белков в цитолемму клетки;
- образование патологических пор в оболочке клетки;
- поступление внутрь клетки ионов натрия и воды;
- баллонная дистрофия (разрушение ультраструктур клетки и образование крупных вакуолей) с последующим некрозом (его объём, как правило, ограничен);
- гибель клетки и лимфоцитарная иммунная реакция, приводящая к основному объёму поражения.
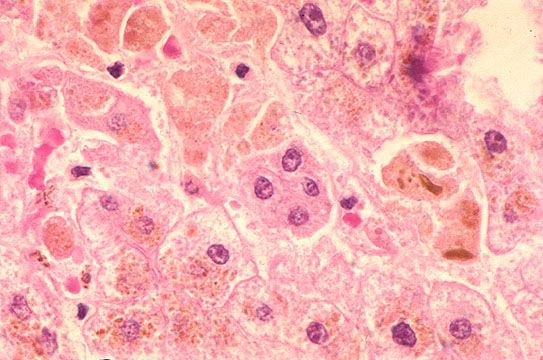
В дальнейшем вирус попадает в желчь, с ней он проникает в кишечник и выводится в окружающую среду с фекалиями. Вследствие компетентных реакций иммунной защиты размножение вируса заканчивается, и он покидает организм больного. [2] [3] [4]
Классификация и стадии развития гепатита А
По степени разнообразия проявлений выделяют две формы гепатита А:
- клинически выраженная (желтушная, безжелтушная, стёртая);
- субклиническая (инаппарантная).
По длительности течения также выделяют две формы гепатита А:
- острая циклическая (до трёх месяцев);
- острая затяжная (более трёх месяцев).
Степени тяжести гепатита А:
- лёгкая;
- среднетяжёлая;
- тяжёлая;
- фульминатная (молниеносная).
Согласно МКБ-10 (Международной классификации болезней десятого пересмотра), заболевание подразделяют на три вида:
- В15. Острый гепатит А;
- В15.0. Гепатит А с печёночной комой;
- В15.9. Гепатит А без печёночной комы. [2][4]
Осложнения гепатита А
Заболевание может привести к следующим осложнениям:
- печёночная кома (дисфункция центральной нервной системы, связанная с тяжёлым поражением печени — встречается крайне редко);
- холецистохолангит (выраженные боли в правом подреберье, нарастание желтухи и зуда кожи);
- гемолитико-уремический синдром, преимущественно у детей (гемолитическая анемия, тромбоцитопения, острая почечная недостаточность);
- развитие аутоиммунного гепатита I типа.
Гепатит А не приводит к формированию хронических форм, однако из-за выраженного воспалительного процесса возможно появление длительных резидуальных (остаточных) явлений:
- дискинезия (нарушение моторики) желчевыводящих путей;
- постгепатитная гепатомегалия (увеличение размеров печени из-за разрастания соединительной ткани);
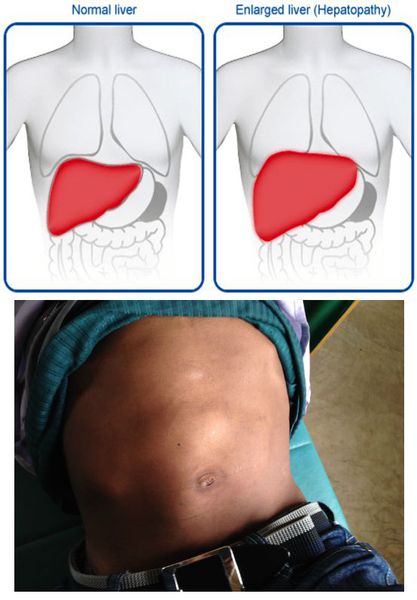
- постгепатитный синдром (повышенная утомляемость, аснено-невротические проявления, тошнота, дискомфорт в правом подреберье). [1][5]
Диагностика гепатита А
Методы лабораторной диагностики:
- Клинический анализ крови — нормоцитоз или лейкопения, лимфо- и моноцитоз, нейтропения, СОЭ в норме или снижена.
- Биохимический анализ крови — повышение общего билирубина и в большей степени его связанной фракции (реакция Эрлиха), повышение аланинаминотрансферазы и аспартатаминотрансферазы, снижение протромбинового индекса, повышение тимоловой пробы (снижение альбуминов и повышение гамма-глобулинов), повышение гамма-глутамилтранспептидазы, щелочной фосфатазы и другие показатели.
- Биохимический анализ мочи — появление уробилина и желчных пигментов за счёт прямого билирубина. Ранее, особенно в вооруженных силах, для выявления больных на начальной стадии практиковалось использование пробы Разина: утром производится опускание индикаторной полоски в мочу (при наличии уробилина она меняет цвет), и военнослужащий с подозрением на заболевание госпитализировался для углублённого обследования. Тест на уробилин становится положительным в самом начале заболевания — в конце инкубационного периода из-за болезни печёночной клетки.
- Серологические тесты — выявления анти-HAV IgM и анти-HAV IgG методом ИФА (иммуноферментного анализа) в различные периоды заболевания и HAV RNA с помощью ПЦР-диагностики (полимеразной цепной реакции) в острый период.
- Ультразвуковое исследование органов брюшной полости — увеличение печени и иногда селезёнки, реактивные изменения структуры печёночной ткани, лимфаденопатия ворот печени.
Обследование лиц, бывших в контакте с больным
Лица, контактирующие с больным вирусным гепатитом А, подлежат осмотру врачом-инфекционистом с последующим наблюдением до 35 дней со дня разобщения с больным. Наблюдение включает термометрию, осмотр кожных покровов, определение размеров печени и селезёнки, а также лабораторное обследование (АЛТ, общий билирубин, антитела классов М и G к вирусу гепатита А вначале и через три недели от первичного обследования).
Дифференциальная диагностика проводится со следующими основными заболеваниями:
- в начальный период: ;
- гастрит, гастроэнтероколит;
- полиартрит;
- энтеровирусная инфекция;
- в желтушный период: ;
- псевдотуберкулёз; ;
- желтухи другой этиологии (гемолитическая болезнь, токсические поражения, опухоли ЖКТ и другие заболевания);
- гепатиты другой этиологии (вирусные гепатиты В, С, Д, Е и другие, аутоиммунные гепатиты, болезнь Вильсона — Коновалова и т.п.) [1][2][3][4][9] .
Лечение гепатита А
Этиотропная терапия (направленная на устранение причины заболевания) не разработана.
Медикаменты
В зависимости от степени тяжести и конкретных проявлений назначается инфузионная терапия с глюкозо-солевыми растворами, обогащёнными витаминами. Показано назначение сорбентов, препаратов повышения энергетических ресурсов, при необходимости назначаются гепатопротекторы, в тяжёлых случаях — гормональные препараты, препараты крови, гипербарическая оксигенация и плазмаферез.
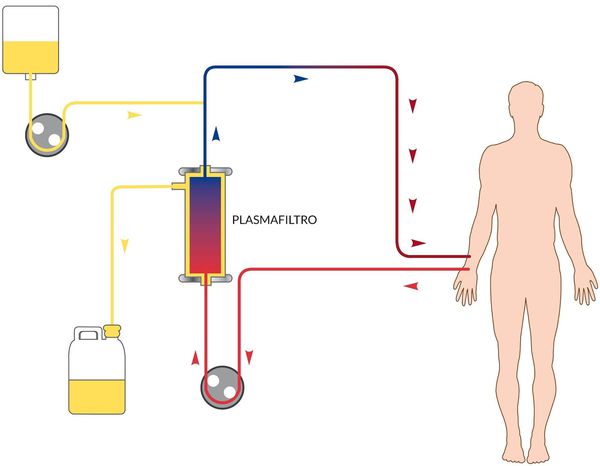
Нужна ли госпитализация
В случае лёгких форм гепатита А лечение может проводиться на дому (при наличии условий). Госпитализация потребуется, начиная со среднетяжёлых форм, лицам групп риска по тяжёлому течению, пациентам с осложнёнными формами, беременным и детям. Каких-либо особенностей при дальнейшем лечении вирусного гепатита А у детей нет.
Режим постельный или полупостельный. При гепатите А нарушаются процессы образования энергии в митохондриях, поэтому предпочтителен длительный отдых.
Лечение в стационаре и выписка
Лечение гепатита А проходит в инфекционном отделении больницы. Выписка пациентов происходит после появления стойкой и выраженной тенденции к клиническому улучшению, а также улучшения лабораторных показателей.
Критерии выписки больных:
- стойкая и выраженная тенденция к клиническому улучшению (отсутствие интоксикации, уменьшение размеров печени, регресс желтухи);
- стабильное улучшение лабораторных показателей (нормализация уровня билирубина, значительное снижение уровня АЛТ и АСТ).
При неосложнённых формах реконвалесценты (выздоравливающие больные) подлежат наблюдению в течении трёх месяцев с осмотром и обследованием не реже одного раза в месяц. [2] [3] [6]
Физиотерапия
В фазе реконвалесценции, особенно при затяжных формах болезни, возможно применение физиотерапевтических методов лечения:
- грязевых аппликаций на область правого подреберья;
- акупунктуры;
- массажа проекции области печени, желчного пузыря, желчевыводящих протоков.
Диета
Показана диета № 5 по Певзнеру — механически и химически щадящая, употребление повышенного количества жидкости и витаминов, запрет алкоголя. Исключается острое, жареное, копчёное, ограничивается кислое и соль. Все блюда готовятся на пару, тушатся, отвариваются и подаются только в тёплом виде.
Прогноз. Профилактика
Прогноз заболевания, как правило, благоприятный. Пациенты выздоравливают спустя 1-3 месяца после выписки из стационара. В редких случаях заболевание приобретает затяжной характер.
Критерии излеченности:
- отсутствие интоксикации;
- полная нормализация уровня билирубина, АЛТ и АСТ;
- нормализация размеров печени и селезёнки;
- появление в крови антител к вирусу гепатита А класса G (Anti-HAV-IgG).
Неспецифические мероприятия, позволяющие снизить количество случаев инфицирования:
- обеспечение условий и факторов потребления безопасной питьевой воды (водоснабжение);
- обеспечение и контроль за соблюдением утилизации сточных вод (канализационное хозяйство);
- контроль за качеством обследования персонала, связанного с пищевой промышленностью;
- контроль и соблюдение технологии хранения, приготовления и транспортировки пищевых продуктов и воды.
К личным профилактическим мерам относится тщательное мытьё рук после посещения туалета, смены подгузников, а также перед приготовлением или приёмом пищи.
Вакцинация
Специфическим профилактическим мероприятием является проведение иммунизации против гепатита А: практически у 100% привитых двукратно людей вырабатывается стойкий иммунитет, предотвращающий развитие заболевания. Вакцинация — это самый лучший способ предотвратить заражение.
Ключевые слова
Об авторе
Список литературы
1. Blach S. (2017) Global prevalence and genotype distribution of hepatitis C virus infection in 2015: a modelling study. The Lancet Gastroenterology & Hepatology, vol. 2, no 3, pp. 161–176.
2. Razavi H. (2017) Hepatitis C virus prevalence and level of intervention required to achieve the WHO targets for elimination in the European Union by 2030: a modelling study. The Lancet Gastroenterology & Hepatology, vol. 2, no 5, pp. 325–336.
3. Pimpin L. (2018) Burden of liver disease in Europe: Epidemiology and analysis of risk factors to identify prevention policies. Journal of Hepatology, vol. 69, no 3, pp. 718–735.
4. Sarrazin C. (2017) Late relapse versus HCV reinfection in patients with sustained virologic response after sofosbuvir-based therapies. Clinical Infectious Diseases: An Official Publication of the Infectious Diseases Society of America, vol. 64, no 1, pp. 44–52.
5. Carrat F. (2019) Clinical outcomes in patients with chronic hepatitis C after direct-acting antiviral treatment: a prospective cohort study. Lancet (London, England), vol. 393, no 10179, pp. 1453–1464.
6. Mandorfer M. (2020) Changes in Hepatic Venous Pressure Gradient Predict Hepatic Decompensation in Patients Who Achieved Sustained Virologic Response to Interferon-Free Therapy. Hepatology (Baltimore, Md.), vol. 71, no 3, pp. 1023–1036.
7. Mauro E. (2018) Portal pressure and liver stiffness measurements in the prediction of fibrosis regression after sustained virological response in recurrent hepatitis C. Hepatology (Baltimore, Md.), vol. 67, no 5, pp. 1683–1694.
8. Arase Y. (2013) Effect of type 2 diabetes on risk for malignancies includes hepatocellular carcinoma in chronic hepatitis C. Hepatology (Baltimore, Md.), vol. 57, no 3, pp. 964–973.
9. Bruno S. (2016) Survival of patients with HCV cirrhosis and sustained virologic response is similar to the general population. Journal of Hepatology, vol. 64, no 6, pp. 1217–1223.
10. Nahon P. (2017) Eradication of Hepatitis C Virus Infection in Patients With Cirrhosis Reduces Risk of Liver and Non-Liver Complications. Gastroenterology, vol. 152, no 1, pp. 142–156.e2.
11. Kanwal F. Risk of Hepatocellular Cancer in HCV Patients Treated With. 1005.e1.
12. Calvaruso V. (2018) Incidence of Hepatocellular Carcinoma in Patients With HCV-Associated Cirrhosis Treated With Direct-Acting Antiviral Agents. Gastroenterology, vol. 155, no 2, pp. 411–421.e4.
13. Kanwal F. (2020) Long-Term Risk of Hepatocellular Carcinoma in HCV Patients Treated With Direct Acting Antiviral Agents. Hepatology (Baltimore, Md.), vol. 71, no 1, pp. 44–55.
14. Caviglia G.P. (2015) Chronic hepatitis C virus infection and lymphoproliferative disorders: mixed cryoglobulinemia syndrome, monoclonal gammopathy of undetermined significance, and B-cell non-Hodgkin lymphoma. Journal of Gastroenterology and Hepatology, vol. 30, no 4, pp. 742–747.
15. Younossi Z.M. (2017) Hepatitis C Infection: A Systemic Disease. Clinics in Liver Disease, vol. 21, no 3, pp. 449–453.
16. Mahale P. (2018) The effect of sustained virological response on the risk of extrahepatic manifestations of hepatitis C virus infection. Gut, vol. 67, no 3, pp. 553–561.
17. Pawlotsky J.-M. (2018) EASL Recommendations on Treatment of Hepatitis C. Journal of Hepatology, vol. 0, no 0.
18. Pawlotsky J.-M. (2020) EASL recommendations on treatment of hepatitis C: Final update of the series. Journal of Hepatology, vol. 73, no 5, pp. 1170–1218.
19. Karpov I.A. (2019) Diagnostika i lechenie pacientov (vzrosloe naselenie) s hronicheskimi virusnymi gepatitami B i C: klin. protokol, utv. Postanovleniem M-va zdravoohranenija Resp. Belarus’ no 19 ot 19.03.19 [Diagnostics and treatment of patients (adult population) with chronic viral hepatitis B and C: clinical protocol approved by the Decree of the Ministry of health of the Republic of Belarus no 19 of March 19, 2019]. Minsk, 30 p.
20. Andrews J. (2013) GRADE guidelines: 14. Going from evidence to recommendations: the significance and presentation of recommendations. Journal of Clinical Epidemiology, vol. 66, no 7, pp. 719–725.
21. (2017) EASL Recommendations on Treatment of Hepatitis C 2016. Journal of Hepatology, vol. 66, no 1, pp. 153–194.
Появление новых препаратов прямого противовирусного действия – это возможность полной победы над гепатитом С. В клинических испытаниях и по данным клинической практики эффективность лечения этими препаратами составляет от 80 до 99%, а нежелательные явления – минимальные.
Препараты прямого противовирусного действия для лечения хронического вирусного гепатита С
Для назначения курса лечения необходимо обследование, а во время лечения контроль эффективности и безопасности лечения в соответствии с рекомендациями Европейской ассоциации по изучению печени.
По механизму действия все препараты представляют собой ингибиторы различных протеаз вируса: NS3, NS4, NS5A, NS5B. Разные сочетания препаратов позволяют получить выздоровление, с вероятностью в ряде случаев до 100%. Среди препаратов есть пангенотипические, то есть эффективные для всех генотипов, и препараты, действующие только на определенные генотипы вируса (1а, 1в, 2а/b, 3а/в).
СОФОСБУВИР – ингибитор NS5В – следует принимать в дозе 400 мг (1таблетка) один раз в сутки. Применяется только в комбинации с другими препаратами ППВД или с рибавирином и интерфероном.
Софосбувир выводится в основном (60%) почками с мочой, поэтому назначение его требует осторожности у пациентов с заболеваниями почек.
Софосбувир вступает в межлекарственные взаимодействия с многими препаратами, поэтому следует внимательно относиться сопутствующим заболеваниям и корректировать прием препаратов, назначенных для лечения этих заболеваний.

ЛЕДИПАСВИР – ингибитор NS5B - доступен в комбинации с софосбувиром(400 мг софосбувира и 90 мг ледипасвира). Доза для приема – 1 таблетка в день независимо от приема пищи.
Так как ледипасвир взаимодействует с другими лекарственными препаратами, следует соблюдать меры предосторожности с частым контролем функции почек. Кроме того, важно учитывать прием пациентами статинов и препаратов в схеме антиретровирусной терапии (ВИЧ).
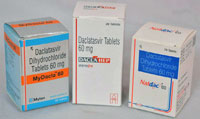
ДАКЛАТАСВИР – ингибитор NS5А – применяется 1 таблетка 60 мг в день в комбинации с другими препаратами ППВД, в том числе с софосбувиром, или рибавирином с интерфероном. Многочисленные лекарственные взаимодействия даклатасвира требуют внимательного отношения при его назначении и соответствующего контроля при его применении.
ВИКЕЙРА ПАК – комплексный препарат, включающий 4 действующих вещества (ритонавир, усиливающий действие паритапревира, омбитасвир и дасабувир). Рекомендуемая доза 1 раз в суткиво время еды 2 таблетки ритонавира/паритапревира/омнитасвира, а также дасабувир 2 раза в сутки. При назначении следует учитывать многочисленные лекарственные взаимодействия, а также класс цирроза.
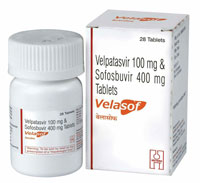
ВЕЛПАТАСВИР – ингибитор NS5А, 1 раз в день 100 мг. Эффективен для всех генотипов вируса. Препарат применяется в комбинации с софосбувиром и воксилапревиром – ВОСЕВИ. Показана его эффективность при перелечивании пациентов с неудачной терапией и формированием мутаций.
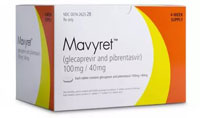
МАВИРЕТ – комбинация глекапревира с прибрентасвиром у пациентов с любым генотипом, рекомендован также для перелечивания, так как мутации не влияют на результат лечения.
СИМЕПРЕВИР – ингибитор NS3/4А - следует принимать одну капсулу 150 мг в сутки. Пациентам, принимающим симепривир, нужно с осторожностью лечиться другими препаратами, в частности антиретровирусными.
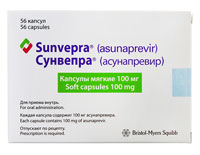
АСУНАПРЕВИР – ингибитор NS3/4A протеазы, применяется 100 мг 2 раза в день. Препарат назначается в комбинации с даклатасвиром, а также в схемах с рибавирином и интерфероном.
НАРЛАПРЕВИР – ингибитор NS3 протеазы (отечественный препарат), 200 мг 1 таблетка в день, применяется в комбинации с рибавирином и интерфероном, с обязательным включением в схему лечения ритонавира. Есть ряд ограничений при единовременном применении с другими лекарственными препаратам. Противопоказанием является цирроз печени класса В и С.
Схемы лечения препаратами прямого противовирусного действия хронического вирусного гепатита
Выбор наиболее эффективной схемы для пациента проводится врачом гепатологом обязательно с учетом степени поражения печени (есть ограничения при высоком классе цирроза), генотипа вируса и сопутствующих хронических заболеваний, так как большинство препаратов имеет выраженные межлекарственные взаимодействия. Иногда необходимо учитывать опыт предыдущего неудачного лечения препаратами интерферона, так как это повышает вероятность исходных мутаций устойчивости к препаратам у вируса, снижающую возможность выздоровления.
Длительность терапии зависит от степени поражения печени и наличия компенсированного или декомпенсированного цирроза. Стандартный курс – 12 недель, при циррозе может быть увеличен до 24 недель.
Возможно назначение дополнительно к схеме лечения рибавирина у пациентов с циррозом и с отрицательными прогностическими факторами ответа на лечение.
Для лечения пациентов с генотипом 1 (1а и 1в) существует 4 рекомендованные схемы препаратов прямого противовирусного действия:
Софосбувир+Ледипасвир
Софосбувир+Симепревир
Софосбувир+Даклатасвир
Софосбувир+Велпатасвир
Викейра Пак ( генотип 1в – 12 недель, генотип 1а – 24 недели).
Даклатосвир + Аунапревир – 24 недели
Для лечения пациентов с генотипом 2 и 3 существует две безинтерфероновые схемы, которые могут применяться также и при других генотипах – пангенотипические схемы.
Софосбувир+даклатасвир
Софосбувир +велпатасвир
Новые все более эффективные и безопасные препараты прямого противовирусного действия вводятся в клиническую практику постоянно. Информация о них регулярно появляется на нашем сайте.
Лечение новыми препаратами. Мнение специалиста
Кажущаяся простота и доступность лечения новыми препаратами, к сожалению, приводит к самолечению.
Лечение назначают продавцы препаратов по телефону и скайпу, без учета сопутствующих заболеваний, что может проявиться в побочных действиях, иногда смертельно опасных.
Неправильно подобранные схемы лечения и отсутствие правильного контроля безопасности во время лечения – основная причина неудач, связанных с генетическими изменениями вируса и формированием устойчивости вируса к препаратам
Диагностическим тестом при гепатите С служит определение антител к вирусу методом ИФА (анти-HCV). Если антитела к HCV обнаружены, необходимо определять РНК HCV чувствительным методом молекулярной диагностики.
В случае положительного результата на антитела и отрицательного результата определения РНК-HCV необходимо выполнять повторные исследования для подтверждения выздоровления.
Цель лечения вирусного гепатита С
Цель лечения – полное удаление вируса и предупреждение заболеваний печени и внепеченочных заболеваний, включая воспалительно-дегенеративные поражения, фиброз, цирроз, рак печени и тяжелые внепеченочные проявления.
Контрольный показатель эффективности лечения
Устойчивый вирусологический ответ (УВО) – отсутствие вируса (определяемой РНК-HCV) через 12 и 24 недели после окончания лечения. Исследование необходимо проводить чувствительным методом молекулярной диагностики с нижним порогом определения 15 МЕ/мл и менее.
Результаты исследований с долгосрочным наблюдением показали, что УВО соответствует окончательному излечению от гепатита в 99% случаев.
У пациентов с циррозом и выраженным фиброзом исследования РНК-HCV следует продолжать и после получения УВО.
Обследование перед началом терапии (подробнее. )
Исключение других причин поражения печени
Прежде всего необходимо исключить другие факторы, влияющие на течение заболевания: наличие гепатотропных вирусов – гепатита В, ВИЧ, алкоголизма, аутоиммунного заболевания печени, поражение печени генетическими и метаболическими заболеваниями: гемахроматоз, сахарный диабет или ожирение, токсическое поражение печени и другие.
Оценка степени поражения печени.
Поскольку от стадии фиброза зависит вероятность выздоровления, прежде всего, необходимо выявление цирроза или выраженного фиброза. В настоящее время убедительно показана возможность оценки степени фиброза не инвазивными методами:
эластометрия / эластография (на аппарате фиброскан),
фибромакс и фибротест (по показателям крови)
Наиболее информативным является совместное определение степени фиброза (по крови и на аппарате фиброскан), что полностью заменяет биопсию.
Пациентам с циррозом необходимо исключать гепатоцеллюлярную карциному (первичный рак печени), а также осложнение цирроза – выраженную портальную гипертензию с расширением вен пищевода и желудка. С этой целью важно до начала терапии провести ЭГДС (гастроскопию).
Для оценки состояния печени проводится биохимическое обследование крови с определением структурных (АЛТ, АСТ, ГГТ) и функциональных показателей (альбумин, общий белок, белковые фракции, фракции липидов), а также общий клинический анализ крови.
Определение характеристик вируса.
Для назначения противовирусной терапии необходимо определить вирусную нагрузку и генотип вируса.
Количественное определение вируса должно проводиться чувствительным методом.
Генотипы устанавливаются методами, позволяющими достоверно определить подтип вируса (например, 1а и 1в), так как они влияют на выбор терапии.
Определение генетических характеристик пациента.
Определение генотипа интерлейкина 28В не потеряло своего прогностического значения.
Противопоказания для применения препаратов прямого противовирусного действия.
Абсолютных противопоказаний к применению препаратов прямого противовирусного действия нет.
Следует соблюдать меры предосторожности при лечении препаратом софосбувир пациентов с заболеваниями почек и сердца.
Пациентам с декомпенсированным циррозом класса В и С противопоказана комбинация препаратов Викейра Пак.
Продолжается исследование безопасности препарата симепревир для пациентов с декомпенсированным циррозом.
Показания к лечению: кого следует лечить?
Все пациенты с компенсированным и декомпенсированным хроническим гепатитом С являются кандидатами на лечение, если они не имеют противопоказаний.
Не имеет значения, получали они ранее терапию или нет.
Приоритет в лечении определяется стадией фиброза. В первую очередь следует назначать терапию пациентам с фиброзом F3-F4 по шкале METAVIR.
Пациентам с декомпенсированным циррозом (класс В и С по шкале Чайлд-Пью) лечение должно быть назначено незамедлительно. Желательно проводить его в условиях отделения трансплантологии.
К группе высокого приоритета относятся также пациенты, коинфецированные ВИЧ и гепатитом В, а также с клинически значимыми внепеченочными проявлениями, такими как васкулит, сопровождающийся криоглобулинемией.
Пациентам с умеренным фиброзом F2 назначение лечения оправдано, однако при необходимости оно может быть отложено (например, по материальным соображениям).
Время начала терапии у пациентов без проявлений или с легким течением заболевания (F0-1) и без внепеченочных симптомов определяется индивидуально.
Препараты прямого противовирусного действия, доступные в Европе.
СОФОСБУВИР – следует принимать в дозе 400 мг (1 таблетка) один раз в сутки.
Софосбувир выводится в основном (80%) почками с мочой, поэтому назначение его требует осторожности у пациентов с заболеваниями почек.
Возможны межлекарственные взаимодействия с многими препаратами, поэтому следует внимательно относиться к сопутствующим заболеваниям и корректировать прием препаратов, назначенных для лечения этих заболеваний.
ЛЕДИПАСВИР – доступен в комбинации с софосбувиром (400 мг софосбувира и 90 мг ледипасвира). Доза для приема – 1 таблетка в день независимо от приема пищи.
Так как ледипасвир может взаимодействовать с другими лекарственными препаратами, следует соблюдать меры предосторожности, с частым контролем функции почек. Кроме того, важно учитывать прием пациентом статинов и препаратов в схеме антиретровирусной терапии.
СИМЕПРЕВИР – следует принимать 1 капсулу 150 мг 1 раз в сутки. Пациентам, принимающим симепревир, противопоказаны некоторые препараты, в том числе антиретровирусные.
ДАКЛАТАСВИР – 1 таблетка 60 мг 1 раз в сутки. Многочисленные лекарственные взаимодействия даклатасвира требуют внимательного отношения при его назначении и соответственно контроля при его применении.
ВИКЕЙРА ПАК – комплексный препарат, включающий 4 действующих вещества (ритонавир, усиливающий действие паритапревира, омбитасвир и дасабувир).
Рекомендуемая дозировка 1 раз в сутки во время еды 2 таблетки ритонавира/паритапревира/омнитасвира, а также дасабувир 2 раза в сутки. При назначении следует учитывать многочисленные лекарственные взаимодействия и класс цирроза.
Варианты лечения различных групп пациентов.
Для лечения хронического гепатита С противовирусными препаратами прямого действия существует несколько различных схем, эффективность и безопасность которых проверена во многих клинических испытаниях.
Выбор комбинаций лекарственных средств осуществляется врачом и зависит от генотипа и подтипа вируса, тяжести заболевания печени, результатов предшествующей терапии.
Длительность терапии зависит от степени поражения печени и наличия компенсированного или декомпенсированного цирроза. Стандартный курс терапии – 12 недель, при циррозе может быть увеличен до 24 недель.
Возможно назначение дополнительно к схеме лечения препарата рибавирин у пациентов с циррозом и с отрицательными прогностическими факторами ответа на лечение, например, при содержании тромбоцитов менее 75х10^3/мкл.
Для лечения пациентов с генотипом 1 (1а и 1в) существует 4 рекомендованные схемы препаратов прямого противовирусного действия:
Для лечения пациентов с генотипом 2 существует только одна безинтерфероновая схема: софосбувир+даклатасвир в течение 12 недель.
Пациентов с циррозом, ранее уже получавших или не получавших терапию, следует лечить также 12 недель.
Для лечение пациентов, инфицированных HCV генотипа 3, пока существует только одна схема безинтерфероновой терапии: софосбувир +даклатасвир. Ледипасвир в отношении HCV генотипа 3 значительно менее эффективен, чем даклатасвир, поэтому схемы с применением ледипасвира для этого генотипа не рекомендованы.
Пациентам с HCV генотипа 3 с циррозом, получавшим или не получавшим ранее терапию, следует назначать эту схему лечения с добавлением рибавирина и длительностью курса 24 недели.
Контроль лечения
В процессе лечения необходимо контролировать эффективность и безопасность (побочные нежелательные эффекты).
Контроль эффективности лечения основан на регулярном определении уровня РНК HCV с использованием чувствительных количественных методов.
РНК HCV следует определять до начала терапии, через 2 недели, а затем через 4, 8 и 12 недель, а также через 12 и 24 недели после окончания курса лечения.
Прекращение терапии вследствие ее бесперспективности при лечении препаратами прямого противовирусного действия правилами НЕ предусмотрено.
Контроль безопасности лечения
Схемы лечения препаратами прямого противовирусного действия хорошо переносятся. Случаи выраженных нежелательных явлений, требующих отмены препаратов, отмечены редко.
Однако, во время терапии необходимо контролировать проявления токсичности других препаратов, применяемых для лечения сопутствующих заболеваний, а также проявления лекарственных взаимодействий. При лечении схемами, содержащими софосбувир, необходимо контролировать состояние почек.
Наиболее часто отмечаются утомляемость и головная боль.
Лечение следует безотлагательно прекратить при обострении гепатита (АЛТ выше нормы в 10 раз).
Тактика лечения пациентов с ожирением и метаболическим синдромом
При выявлении у пациентов с HCV сопутствующего поражения печени в результате метаболического синдрома (неалкогольная жировая болезнь печени - стеатоз) необходимо провести дополнительное обследование на показатели обменных и гормональных нарушений, характерных для этого заболевания.
Рекомендуется для оценки степени поражения печени использовать исследование крови – Фибромакс, которое дает возможность оценить отдельно степень поражения печени вирусом и отдельно метаболическим синдромом.
Тактика лечения зависит от степени поражения печени в целом, и отдельно каждым повреждающим фактором. Лечение противовирусными препаратами может быть назначено сразу, а дальнейшее лечение метаболического синдрома после получения УВО.
Если степень поражения печени вирусом значительно меньше, чем метаболическим синдромом, возможно начинать противовирусную терапию после лечения метаболического синдрома.
В случаях наличия сопутствующих заболеваний печени необходимо ставить целью лечения не только получение УВО, но и сохранение и восстановление печени, пострадавшей от других патологических факторов.
Читайте также:

