Проявление гепатита в стоматологии
Обновлено: 15.04.2024
С. И. Потапова, И. И. Соколова, Т. Е. Гурьева, Харьковский государственный медицинский университет.
Цель настоящей статьи — привлечь внимание стоматологов к некоторым эпидемиологическим вопросам вирусного гепатита В [ВГВ], связанным со здоровьем как стоматологического больного, так и врача.
Гепатит относится к группе заболеваний вирусной этиологии с характерным механизмом передачи инфекционного агента. Заражение происходит при переливании крови и ее компонентов, различных инвазивных лечебно-диагностических манипуляциях.
Фундаментальные научные исследования последних десятилетий послужили основанием для пересмотра сложившихся представлений о вирусных гепатитах. Одновременно возник целый ряд новых проблем, представляющих теоретический интерес и имеющих важное практическое значение. К ним следует отнести и проблему профессионального заражения медицинских работников.
Результаты проведенных в этом направлении исследований не вызывают в настоящее время сомнений в том, что медицинские работники любого профиля представляют собой группу высокого риска заражения [5, 6], однако наиболее высокие показатели инфицирования наблюдаются у сотрудников отделений гемодиализа, хирургов и медицинских сестер [7, 8], отмечается также высокий риск заражения стоматологов, особенно хирургов [9, 10].
Изучение условий заражения медицинских работников показало, что оно осуществляется в лечебных учреждениях преимущественно через кровь.
Однако неоспоримо доказано, что слюна, слезная жидкость, вагинальный секрет, сперма, моча, грудное молоко также могут содержать вирус гепатита В и стать причиной заражения. Чаще всего полный набор маркеров ВГВ обнаруживается в крови инфицированных лиц. Поэтому при контакте с кровью источника ВГВ риск заражения значительно выше, чем с другими его выделениями, так как в крови вирус находится в наиболее полноценном состоянии и в высокой концентрации [11]. С кровью ВГВ может сохраняться во внешней среде при комнатной температуре продолжительное время (до 7 мес.) [12].
При анализе анамнестических данных об оперативных вмешательствах, переливаниях крови было установлено, что эти факторы риска заражения с одинаковой частотой отмечались у медицинских работников как с выявленными маркерами вируса ГВ, так и без них, что указывает на профессиональный характер заражения ВГВ [13].
К сожалению, применявшиеся до недавнего времени санитарно-противоэпидемические методы не обеспечивают полного предохранения медицинского персонала от этого заболевания. ВГВ опасен своим распространением, часто вызывает хронические формы поражения печени — хронический гепатит, цирроз печени, инфицированность ВГВ повышает риск сочетанного заражения вирусом гепатита Д. Кроме того, фатальная форма ВГВ встречается у 1% больных острым ВГВ и остается проблемой, далекой от разрешения [14].
Возникновение ВГВ у стоматологов объясняется следующими причинами: постоянный контакт врача со средами — носителями вируса, слюной и особенно кровью; частые царапины, порезы и другие повреждения рук в связи с работой режуще-колющими инструментами; воздушно-капельная передача инфекции за счет чрезвычайно близкого и длительного контакта с больным, а также образования аэрозольного облака при работе на скоростных бормашинах и при использовании ультразвуковой техники для снятия зубных отложений.
Профилактика ВГВ у стоматологических больных заключается, прежде всего, в совершенствовании традиционных мер асептики и антисептики. Большое значение имеет дезинфекция и предстерилизационная обработка инструмента.
При выборе дезинфицирующих средств необходимо учитывать, что для дезинфекции стоматологических инструментов допускается применение только таких дезинфицирующих средств, которые обладают бактерицидным, вирулицидным, фунгицидным и спороцидным действием. Не допускается использовать для дезинфекции стоматологических инструментов дезинфицирующие средства І-ІІ класса опасности, а также средства, не обладающие вирулицидным действием, а для дезинфекции поверхностей помещений — средства, обладающие только статическим действием, то есть действием, только задерживающим рост микроорганизмов.
Учитывая обширность перечня разрешенных для применения дезинфицирующих средств и разнообразие их действующих веществ и концентраций, условий растворимости в воде, способов применения, времени экспозиции, влияния на обрабатываемые объекты и т. п., прежде всего, обращают на себя внимание препараты целевого назначения, которые максимально учитывают особенности обеззараживания изделий медицинского назначения. Препарат Абактерил-Актив соответствунт всем заявленным требованиям.
Наиболее надежными методами стерилизации, рекомендуемыми для стоматологии, являются автоклавирование (при 120°C в течение 15 мин.) и суховоздушная стерилизация (при 180°C в течение 1 часа).
Одной из действенных мер борьбы с ВГВ является применение инструментов разового пользования (шприцев, пульпэкстракторов, эндодонтических инструментов, разделительных пластинок и др.).
Руки врача-вирусоносителя, даже обработанные самым тщательным образом, при их случайном повреждении могут стать источником инфекции. Поэтому перчатки являются лучшим средством защиты больного от ВГВ.
Выявление вирусоносителей среди лиц стоматологических профессий (врачи, сестры, санитарки) — еще одно из направлений профилактики.
Профилактика ВГВ у стоматологов, как и у пациентов, сводится к прекращению трансмиссии ВГВ. Сюда относятся следующие мероприятия: стерилизация всех инструментов, профилактика повреждений рук, применение перчаток и хирургических масок.
Эти предосторожности особенно важны при работе с контингентами, имеющими высокую вероятность заболевания ВГВ (наркоманы, больные туберкулезом и др.), и с лицами, переболевшими ВГВ.
Проведенный скрининг наглядно свидетельствует о высоком уровне инфицированности ВГВ медицинского персонала лечебно-профилактических учреждений (ЛПУ) и требует проведения мероприятий по созданию специфического протективного иммунитета [15].
Специфическая иммунопрофилактика против ВГВ медперсонала ЛПУ — важнейшая задача современного здравоохранения.
Преимущество подобной вакцины в том, что она совершенно безопасна, прекрасно дозируется и введение ее доз четко контролируется; вакцинация практически не имеет противопоказаний, поскольку вакцина не имеет животного белка (исключение составляют беременность, острые инфекционные заболевания, повышенная температура в момент вакцинации).
Если во время медицинских манипуляций произошло инфицирование сотрудника кровью больного или вирусоносителя ВГВ, то следует как можно раньше ввести иммуноглобулин против ВГВ (не позднее 24 часов от момента возможного заражения), а затем, не позднее 7 дней — вакцину против ГВ, т. е. провести экстренную вакцинацию. Ревакцинацию проводят через 1 и 6 месяцев.
При проведении плановой вакцинации против ГВ надо помнить, что она эффективна только в случае трехкратной прививки (либо по укороченной схеме — 0-1-2 мес., либо по стандартной (более предпочтительной) схеме — 0-1-6 мес.).
Учитывая выше изложенное, можно сделать следующие выводы: распространение ВГВ может быть связано со стоматологическими вмешательствами; медицинские работники стоматологического профиля имеют высокий риск профессионального инфицирования вирусом гепатита В; заражение сотрудников стоматологических учреждений осуществляется преимущественно при контакте с кровью и ротовой жидкостью пациентов; ВГВ необходимо считать профессиональным заболеванием медицинского персонала стоматологического профиля; обеспечение высокого уровня специфического протективного иммунитета путем вакцинации следует рассматривать как основное направление профилактики ВГВ среди медицинских работников; регулярное обследование персонала стоматологических учреждений может позволить выявить очаги ВГВ; совершенствование методов асептики и антисептики в ЛПУ стоматологического профиля — необходимая мера профилактики ВГВ.
Гепатит С — вирусное заболевание, в основном передающееся через кровь. Чаще всего инфицирование им случается при использовании нестерильных медицинских инструментов. А поскольку само заболевание в течение первых месяцев протекает бессимптомно, в большинстве случаев оно переходит в хроническую форму еще до того, как бывает диагностировано.
Нелеченый гепатит может привести к фиброзу, циррозу печени, поражению суставов, снижению интеллектуальных функций и работоспособности. Особенно тяжелыми последствиями он грозит обернуться в сочетании с ВИЧ.
Как и ВИЧ, вирус передается в том числе половым путем, и пусть этот способ инфицирования для него нехарактерен, в отличие от вируса иммунодефицита, вирус гепатита намного более устойчив ко внешней среде. В каком-то смысле гепатит С — чемпион по выживанию: в высохшей крови при комнатной температуре вирус сохраняет жизнеспособность до 16 часов (тот же ВИЧ умирает в таких условиях почти мгновенно). А уничтожение вируса гепатита С достигается только стерилизацией.
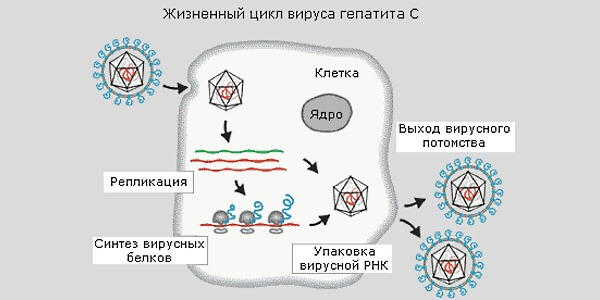
Если в конце 90-х в России распространение гепатита напрямую коррелировало с употребления внутривенных наркотиков, сегодня эпидемиологическая картина совсем другая: вирус обнаруживается у 3—4 % населения, включая маленьких детей.
Причем вероятность инфицироваться гепатитом, даже если вы не употребляете инъекционных наркотиков, не занимаетесь незащищенным сексом, вам не переливали кровь, все равно остается весьма высокой. А одним из мест, где можно заразиться гепатитом, остается кабинет стоматолога.
Инерция скупости
Если вероятность инфицироваться ВИЧ у стоматолога весьма невелика, то, как утверждают западные исследования гепатита, в случае с этим заболеванием все обстоит намного серьезнее.
Традиционно врач-стоматолог препарирует ткань зуба турбинным наконечником, чтобы поставить пломбу. Ротор вращает бор, вставленный в наконечник, со скоростью 300 000 оборотов в минуту, а сам ротор приводится в движение сильным потоком сжатого воздуха. Собственно эта турбина и издает тот характерный звук, который у нас ассоциируется со стоматологическим кабинетом.
При препарировании зуба наконечник всегда загрязняется биологическими жидкостями: кровью, гноем, слюной. Но настоящая проблема в том, что при прекращении подачи воздуха в турбинном наконечнике возникает эффект аспирации: давление в воздушном канале становится куда ниже, чем в зоне турбины, и биологические жидкости засасываются в воздушный канал.

Когда вы садитесь в кресло стоматолога или усаживаете туда своего ребенка, врач при вас надевает стерильные перчатки и распечатывает стерильный лоток с инструментами.Но турбинный наконечник часто остается прежним.
Когда стоматолог приступает к работе, он уже стоит в установке. К сожалению, в большинстве российских стоматологических клиник наконечник распечатывают из стерильной упаковки в начале смены, а стерилизуют в самом конце — и это в лучшем случае.
Так, недавний опрос 467 стоматологов, проведенный исследователями, показал, что 19 % российских врачей, большая часть которых имеют специализацию по ортопедии и стаж работы от 10 до 19 лет, не считают необходимым стерилизовать мелкий стоматологический инструментарий между пациентами.
Отчасти это связано с тем, что, когда турбинные наконечники появились на рынке в 90-е годы, они стоили очень дорого и врачи не могли себе позволить принимать каждого пациента с отдельным наконечником. Сегодня турбинный наконечник стоит 2500—4000 рублей, что для стоматологической клиники немного, но инерционность мышления специалистов берет свое.
Вакуум знаний
Впрочем, паниковать не стоит. Профессор кафедры инфекционных болезней и эпидемиологии МГМСУ имени А. И. Евдокимова Ирина Шестакова на вопрос нашего сайта отвечает, что реально оценить вероятность такого заражения достаточно сложно. И риск не так уж и велик, как это может показаться на первый взгляд.
по теме

Лечение
АBC — азбука гепатита
Ее коллега Юрий Крестинский, директор центра развития здравоохранения московской школы управления Сколково, не так оптимистичен. До трети случаев заражения гепатитами происходят через стоматологию, маникюры, педикюры, либо через парикмахерские услуги, например, такие как бритье опасными и старомодными лезвиями, которые во многих странах запрещены, подчеркивает он.
Вопрос контроля
Как демонстрируют данные уже упомянутого опроса, 2 % врачей-стоматологов со стажем работы более 30 лет допускают повторное использование игл и карпул с анестетиком для анестезии после стерилизации. Более четверти врачей-стоматологов не изучали вопросы инфекционного контроля при получении постдипломного образования и на курсах повышения квалификации. Более 30 % из них открыто признаются, что не обладают достаточными знаниями о заболеваниях, переносимых кровью.
В результате 51 % детских стоматологов не используют 2 пары перчаток при работе с пациентом, у которого подобный диагноз установлен. 25 % врачей-стоматологов городских стоматологических поликлиник не используют крафт-пакеты для стерилизации и хранения инструментов.
Каков итог, стоит ли бояться стоматологов? Конечно, не стоит. Общий вывод, который можно сделать в этом случае: не стесняйтесь и не бойтесь перестраховываться — требуйте, чтобы стоматолог при вас распечатывал все инструменты и доставал их из стерильной упаковки.
Не верьте пустым заявлениям, помните, что дезинфекция никогда не заменяет стерилизацию и что инфекции, передающиеся через кровь, обходятся слишком дорого. Так что лучше выглядеть в глазах стоматолога занудой, чем в один непрекрасный день узнать, что у вас гепатит С.
Что такое гепатит Б? Причины возникновения, диагностику и методы лечения разберем в статье доктора Александрова Павла Андреевича, инфекциониста со стажем в 14 лет.
Над статьей доктора Александрова Павла Андреевича работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
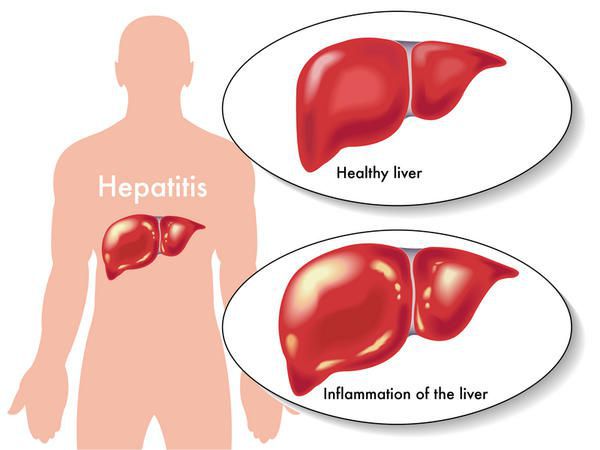
Вирусный гепатит В (Б) — острое и хроническое инфекционное заболевание, вызываемое вирусом гепатита В, с гемоконтактным механизмом передачи (через кровь), протекающее в различных клинико-морфологических вариантах, и возможным развитием цирроза печени и гепатоцеллюлярной карциномы. Всего в мире, по самым скромных оценкам, инфицировано более 250 млн человек.
Этиология
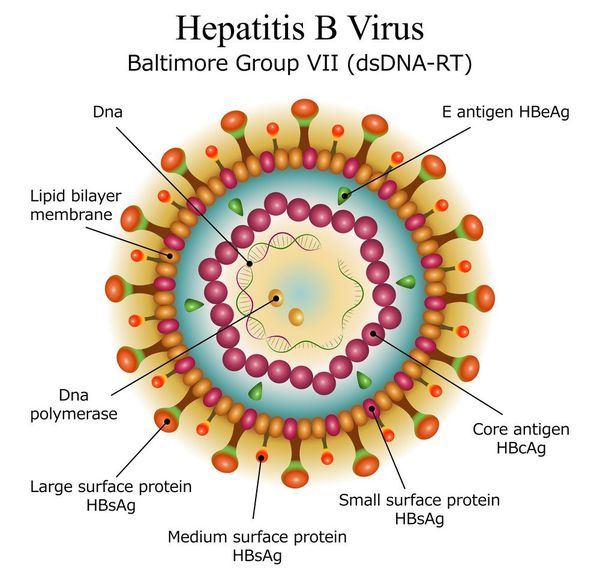
вид — вирус гепатита В (частица Дейна)
Развитие вируса гепатита Б происходит в гепатоцитах (железистых клетках печени). Он способен к интеграции в ДНК человека. Имеются 9 генотипов вируса с различными подтипами — генетическая изменчивость позволяет вирусу образовывать мутантные формы и ускользать от действия лекарств.
Имеет ряд собственных антигенов:
- поверхностный HbsAg (австралийский). Появляется за 15-30 дней до развития болезни, свидетельствует об инфицировании (не всегда). Антитела к HbsAg выявляются через 2-5 месяцев от начала заболевания, а сам HbsAg исчезает из крови (при благоприятном течении процесса);
- сердцевинный HbcorAg (ядерный, коровский). Появляется в инкубационном периоде и совместно с ним появляются антитела (HbcorAb). Длительное присутствие HbcorAg в крови свидетельствует о вероятной хронизации процесса (неадекватный иммунный ответ);
- антиген инфекциозности и активного размножения вируса (HbeAg). Появляется совместно с HbsAg и отражает степень инфицированности. Его продолжительная циркуляция в крови является свидетельством развития хронизации процесса, а антитела к нему являются благоприятным прогностическим признаком (не всегда, но по меньшей мере указывают на возможность более благоприятного процесса, срок их циркуляции после выздоровления окончательно не определён, но не более пяти лет после благоприятного разрешения процесса);
- HbxAg — регулятор транскрипции, способствует развитию гепатокарциномы.
Вирус гепатита В чрезвычайно устойчив к действию всевозможных естественных факторов окружающей среды, инактивируется при 60 °C за 10 часов, при 100 °C за 10 минут, при оптимальной температуре сохраняется до 6 месяцев, при автоклавировании погибает за 5 минут, в сухожаровом шкафу — через 2 часа, 2% раствор хлорамина убивает вирус за 2 часа. [1] [3]
Эпидемиология
Источник инфекции — только человек, больной острой или хронической формой инфекции.
Механизм передачи: гемоконтактный и вертикальный (от матери к ребёнку), не исключается трансмиссивный механизм передачи (например, при укусах комаров в результате раздавливания и втирания инфицированного тела комара в поврежденную ткань человека).
Пути передачи: половой, контактно-бытовой, гемотрансфузионный (например, при переливании крови или медицинских манипуляциях). Восприимчивость всеобщая. Заболеваемость — 30-100 человек на 100 тысяч населения (зависит от страны). Летальность от острых форм — до 2%. После перенесённого острого заболевания при условии выздоровления иммунитет стойкий, пожизненный.
Для заражения характерна малая заражающая доза (невидимые следы крови). [1] [2]
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы гепатита Б
Инкубационный период гепатита В длится от 42 до 180 дней (следует иметь в виду, что наличие клинической симптоматики характеризует лишь незначительную долю всех случаев заболевания).
Начало постепенное. Характерные синдромы:
- общей инфекционной интоксикации (проявляется как астеноневротический синдром);
- холестатический (нарушение секреции желчи);
- артрита;
- нарушения пигментного обмена (появление желтухи при уровне общего билирубина свыше 40 ммоль/л);
- геморрагический (кровоточивость кровеносных сосудов);
- экзантемы;
- отёчно-асцитический (скопление жидкости в брюшной полости);
- гепатолиенальный (увеличение печени и селезёнки).
При первых признаках гепатита B нужно обратиться к доктору.
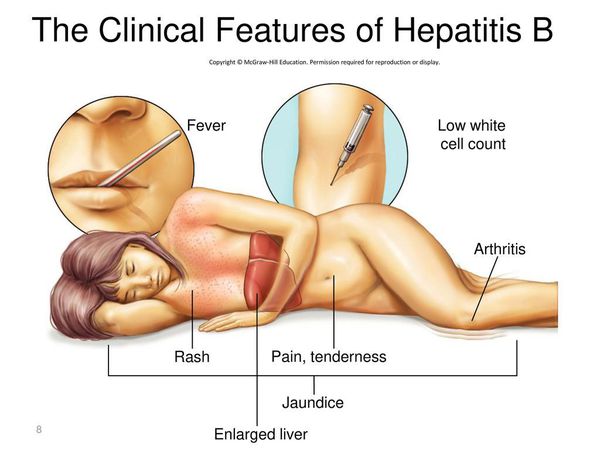
Первые признаки гепатита B
Начальный (преджелтушный) период продолжается 7-14 дней. Чаще протекает по многообразному типу с болевыми ощущениями в различных суставах по ночам и утром, уртикарными высыпаниями, астеновегетативными проявлениями (снижение аппетита, апатия, нервозность, слабость, разбитость, повышенная утомляемость). Изредка развивается синдром Джанотти-Крости — симметричная, яркая пятнисто-папулёзная сыпь. Не исключены умеренные диспептические явления (расстройства пищеварения). К концу периода происходит потемнение мочи, обесцвечивание кала.
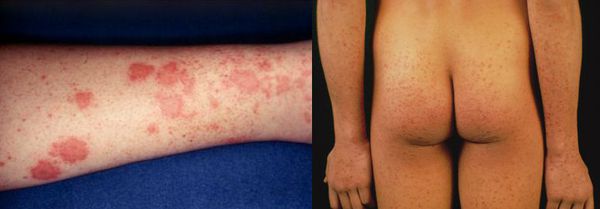
Желтушный период
Этот период продолжительностью около одного месяца характеризуется возникновением желтушного окрашивания кожи (различных оттенков) на фоне продолжающегося или ухудшающегося общего состояния. Характерна длительность и стойкость симптоматики. Появляется тяжесть и болезненность в правом подреберье, горечь во рту, тошнота, выражённый зуд кожи (практически не снимаемый никакими средствами). На фоне усиления астеноневротического компонента появляются геморрагические проявления, урежение пульса, гипотензия, отёки (отражает степень интоксикации и нарушения функций печени).
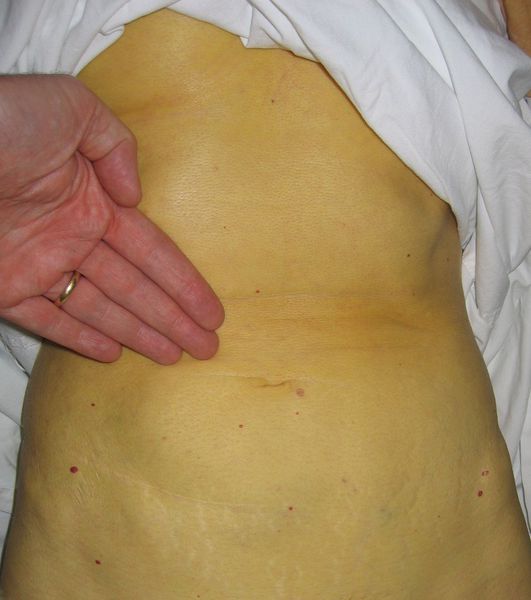
Выздоровление
Следующим этапом в развитии болезни является нормализации общего состояния, спадение желтухи и реконвалесценция, которая в зависимости от конкретной ситуации и состояния иммунной системы может закончиться как выздоровлением, так и движением развития заболевания в хроническое течение, характеризующееся маловыраженой неусточивой симптоматикой, преимущественно в виде слабости, периодического дискомфорта в правом подреберье, бурно сигнализирующим лишь на стадии цирроза и полиорганных осложнений.
- гепатиты другой этиологии;
- желтухи другой этиологии (например, гемолитическая болезнь, токсическое поражение, опухоли);
- малярия; ;
- лептоспироз;
- ревматоидный артрит.
Гепатит В у беременных
Острый гепатит характеризуется более тяжёлым течением у беременной, возникновении повышенного риска преждевременных родов, аномалий развития плода на ранних сроках и кровотечений. Вероятность передачи при острой форме зависит от сроков беременности: в первом триместре риск 10% (но более тяжёлые проявления), в третьем триместре — до 75% (чаще бессимптомное течение после родов). У большинства детей при заражении во внутриутробном и постнатальном периодах происходит хронизация инфекции. [1] [3] [6]
Патогенез гепатита Б
С движением кровяной массы вирус попадает в печеночную ткань, где локализуется в гепатоцитах и теряет свою протеиновую сферу в лизосомах. Происходит выход вирусной ДНК с последующим ресинтезом аномальных протеинов LSP, а параллельно образование новых частиц Дейна.
В процессе эволюции вирусчеловеческого взаимодействия возможно развитие двух вариантов:
При репликативном пути происходит следующее: белки LSP совместно с HbcorAg вызывают увеличение продукции гамма-интерферона, что приводит к активации главного комплекса гисотсовместимости (HLA), проистекает преобразование молекул гистосовместимости 1 и 2 классов, в результате чего клетка становиться для организма враждебной в антигенном формате.
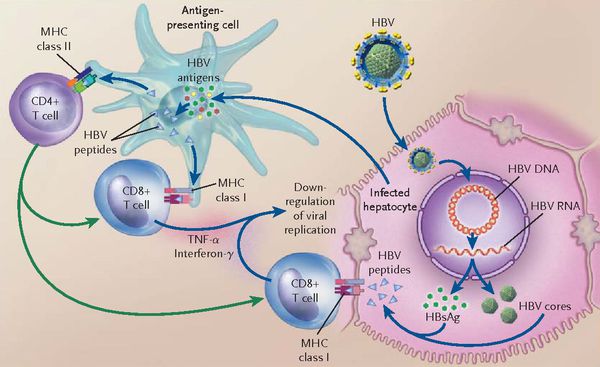
Антигенпрезентирующие макрофаги содействуют изменению В-лимфоцитов в плазматические клетки и экспрессии ими агрессивных белков-антител к посторонним антигенам. В итоге на поверхности печёночных клеток формируются вирусспецифические иммунные комплексы (антиген + антитело + фракция комплемента С3в).
В динамике может реализоваться два сценария:
- в первом варианте запуск каскада комплимента ведёт к появлению в составе иммунных комплексов агрессивной фракции С9 (мембранатакующий комплекс) — наблюдается значительный некроз гепатоцитов без участия лимфоцитов (молниеносная форма гепатита В);
- при альтернативной варианте (наблюдающимся в большинстве случаев) каскад комплемента в силу иммуноиндивидуалистических свойств не активируется — тогда идёт умеренное разрушение Т-киллерами меченых антителами заражённых вирусом гепатоцитов. Образуются ступенчатые некрозы с образованием на месте гибели гепатоцитов соединительной ткани — рубцов (то есть острый гепатит В при плохом иммунном ответе постепенно переходит в хронический).
Непременным атрибутом патогенеза является формирование иммунопатологического процесса. Гибель гепатоцитов, инфицированных вирусом гепатита В, следует за счёт иммунокомпетентных частиц, Т-киллеров и макрофагальных элементов.
Серьёзным значением является нарушение свойств мембраны клеток печени, что сопровождается экскрецией (выделением) лизосомальных ферментов, разрушающих гепатоциты. Сообразно этому, гибель гепатоцитов происходит за счёт иммунокомпетентных клеток, лизосомальных ферментов и противопечёночных гуморальных аутоантител, то есть острая болезнь наступает (и благоприятно заканчивается) только при хорошем иммунитете, а при плохом идёт хронизация.
При тяжёлом цитолитическом синдроме (массивные некрозы гепатоцитов) возникает гипокалиемический алкалоз, острая печёночная недостаточность, печёночная энцефалопатия (ПЭП), церебротоксическое действие, нарушение функции обмена нервной ткани. [2] [3] [6]
Классификация и стадии развития гепатита Б
По цикличности течения:
- острый;
- острый затяжной;
- хронический.
По клиническим проявлениям:
- субклинический (инаппарантный);
- клинически выраженный (желтушный, безжелтушный, холестатический, фульминантный).
По фазам хронического процесса:
Группы риска хронического гепатита B
Хроническим гепатитом чаще страдают дети младше шести лет. При заражении в первый год жизни он развивается в 80–90 % случаев, от года до шести лет — в 30–50 %, у взрослых без сопутствующих заболеваний — менее чем в 5 %. [7]
Осложнения гепатита Б
Чем опасен гепатит Б
Заболевание может привести к острой печёночной недостаточности (синдрому острой печеночной энцефалопатии).
Выделяют четыре стадии болезни:
Диагностика гепатита Б
Многообразие форм, тесная взаимосвязь с иммунной системой человека и зачастую достаточно высокая стоимость исследований часто затрудняют принятие конкретного решения и диагноза в стационарный отрезок времени, поэтому во избежание роковых (для больного) ошибок следует подходить к диагностике с учётом всех получаемых данных в динамическом наблюдении:
- общеклинический анализ крови с лейкоцитарной формулой (лейкопения, лимфо- и моноцитоз, уменьшение СОЭ, тромбоцитопения);
- общий анализ мочи (появление уробилина);
- биохимический анализ крови (гипербилирубинемия в основном за счёт связанной фракции, повышение уровня АЛТ и АСТ, ГГТП, холестерина, щелочной фосфатазы, снижение протромбинового индекса, фибриногена, положительная тимоловая проба);
- маркеры гепатита В: HbsAg, HbeAg, HbcorAg, HbcorAb IgM и суммарные, HbeAb, anti-Hbs, ПЦР в качественном и количественном измерении);
- УЗИ органов брюшной полости, КТ и МРТ диагностика;
- фиброскан (применяется для оценки степени фиброза). [3][4]
Скрининг при хроническом гепатите
Пациентам с хроническим гепатитом В рекомендуется не реже чем раз в полгода проходить обследование: УЗИ органов брюшной полости, клинический анализ крови, АЛТ, АСТ, тест на альфа-фетопротеин. Скрининг позволяет вовремя заметить обострение болезни и начать специфическую терапию.
Лечение гепатита Б
Лечение острых форм гепатита В должно осуществляться в стационаре (учитывая возможность быстрых и тяжёлых форм болезни), хронических — с учётом проявлений.
Диета и режим при гепатите В
В острый период показан постельный режим, печёночная диета (№ 5 по Певзнеру): достаточное количество жидкости, исключение алкоголя, жирной, жареной, острой пищи, всё в мягком и жидком виде.
Медикаментозная терапия
При лёгкой и средней тяжести острого гепатита этиотропная противовирусная терапия (ПВТ) не показана. При тяжёлой степени и риске развития осложнений назначается специфическая противовирусная терапия на весь период лечения и возможно более длительное время.
В лечении хронических форм гепатита показаниями к назначению ПВТ является наличие уровня DNA HBV более 2000 МЕ/мл (при циррозе печении независимо от уровня), умеренное и высокое повышение АЛТ/АСТ и степени фиброза печёночной ткани не менее F2 по шкале METAVIR, высокая вирусная нагрузка у беременных женщин. В каждом конкретном случае показания определяются индивидуально, в зависимости от выраженности процесса, временной тенденции, пола, планирования беременности и другого.
Существует два пути противовирусного лечения:
- терапия пегилированными интерферонами (имеет ряд существенных противопоказаний и серьёзных побочных эффектов — не менее 12 месяцев);
- нуклеозидно-аналоговой терапии NA (используются препараты с высоким порогом резистентности вируса, длительно — не менее пяти лет, удобство применения, хорошая переносимость).
В отдельных случаях может рассматриваться применение комбинированной терапии.
Из средств патогенетической терапии в острый период используются внутривенно вводимые растворы 5% глюкозы, дезинтоксикантов, антиоксидантов и витамины. Показан приём энтеросорбентов, ферментных препаратов, при выраженном холестазе применяются препараты Урсодезоксихолевой кислоты, при тяжёлом течении — глюкокортикостероиды, методы аппаратного плазмофереза.
В хронической стадии заболевания при наличии соответствующей активности процесса и невозможности назначения ПВТ может быть показан приём групп гепатопротекторов и антиоксидантов. [1] [3]
Прогноз. Профилактика
Основное направление профилактики на сегодняшний день — это проведение профилактической вакцинации против гепатита В в младенческом возрасте (в том числе усиленная вакцинация детей, рождённых от матерей с гепатитом В) и далее периодические ревакцинации раз в 10 лет (или индивидуально по результатам обследования). Достоверно показано, что в странах, где была введена вакцинация, резко сократилось количество вновь выявленных случаев острого гепатита В.
Вторая составляющая стратегии профилактики включает обеспечение безопасности крови и её компонентов, использование одноразового или стерилизованного инструментария, ограничение числа половых партнёров и использование барьерной контрацепции. [1] [2]
Кафедра акушерства и гинекологии с курсом пренатальной диагностики Смоленской государственной медицинской академии
Влияние острого вирусного гепатита В на состояние слизистой оболочки рта и пародонта
Журнал: Стоматология. 2016;95(6‑2): 34‑35
Кучумова Е.Д., Петрова С.В. Влияние острого вирусного гепатита В на состояние слизистой оболочки рта и пародонта. Стоматология. 2016;95(6‑2):34‑35.
Kuchumova ED, Petrova SV. . Stomatologiya. 2016;95(6‑2):34‑35. (In Russ.).
Кафедра акушерства и гинекологии с курсом пренатальной диагностики Смоленской государственной медицинской академии
Актуальность. В последние годы все больше внимания уделяется проявлению общесоматической патологии во рту, и зачастую именно врач-стоматолог может определить начальные стадии многих заболеваний и предупредить изменения со стороны органов и тканей рта при помощи профилактических методов.
Цель исследования — изучить влияние острого вирусного гепатита В (МКБ-10, код В16) на состояние слизистой оболочки рта и пародонта.
Результаты. Желтушность твердого и мягкого неба, а также протоков парных слюнных желез выявлены у всех пациентов (100%) как в 1-е, так и во 2-е посещение. Геморрагии на мягком небе и вестибулярной поверхности губ отмечаются в 94% в 1-е посещение и в 80% — во 2-е. Мелкие сливающиеся эрозии, покрытые налетом желтушного оттенка, отмечены в 77 и 30% при первичном и повторном наблюдении соответственно. Десквамация эпителия спинки языка, сочетающаяся с атрофией сосочков на боковой поверхности, отмечена у всех обследуемых (100%) при первичном наблюдении и 80% при повторном. Среднее значение индекса OHI-S (1,1) при первичном осмотре свидетельствует о хорошем уровне гигиены рта, однако при повторном осмотре среднее значение этого индекса (2,0) отражает ухудшение последней. Значение индекса РМА при первичном осмотре свидетельствует о выраженной распространенности и интенсивности процесса (среднее значение — 43,5%), при повторном осмотре также отмечено дальнейшее распространение патологического процесса и увеличение его тяжести (среднее значение — 58,5%). Значение индекса кровоточивости по Saxer & Műhleman при первичном осмот-ре в 90% случаев отражает наличие кровоточивости при приеме пищи и/или чистке зубов, на что так же указывают пациенты. При повторном осмотре отмечается заметное снижение кровоточивости, в 60% случаев кровоточивость появляется не раньше, чем через 30 c.
Вывод. При остром вирусном гепатите В наблюдаются изменения со стороны слизистой оболочки рта и пародонта. Кровоточивость десен зависит от динамики основного заболевания и снижается при получении пациентом стандартной схемы лечения основного заболевания. В связи с ухудшением показателей гигиенических индексов за период наблюдения необходима коррекция комплекса мероприятий по индивидуальной гигиене рта. Требуется совместная работа врача-инфекциониста и врача-стоматолога при ведении пациентов с вирусным гепатитом В уже на ранних стадиях развития данного заболевания.
ВПП — внепеченочное поражение
ИК — иммунные комплексы
КГС — криоглобулинемический синдром
МКГН — мезангиокапиллярный гломерулонефрит
ПВТ — противовирусная терапия
РФ — ревматоидный фактор
СКГ — смешанная криоглобулинемия
СШ — синдром Шегрена
ТИН — тубулоинтерстициальный нефрит
УП — узелковый полиартериит
ФА — фиброзирующий альвеолит
ХГВ — хронический гепатит В
ХГН — хронический гломерулонефрит
ХГС — хронический гепатит С
ЦП — цирроз печени
ЩЖ — щитовидная железа
HBV — вирус гепатита В
HCV — вирус гепатита С
Изучение хронических вирусных поражений печени выявило широкий спектр внепеченочных проявлений хронического гепатита В (ХГВ), а впоследствии, при открытии вируса гепатита С, и хронического гепатита С (ХГС).
В России ведущая роль в изучении системности поражения при вирусных заболеваниях печени принадлежит исследованиям, проведенным в клинике им. Е.М. Тареева: изучение хронического активного гепатита как системного заболевания (З.Г. Апросина, 1974 г., 1981 г.), внепеченочных поражений при ХГС (Т.М. Игнатова, 2000 г.; А.В. Русских, 2004 г.; С.Ю. Милованова, 2005 г.; С.Ю. Карпов, 2005 г.) и ХГВ (А.А. Ильянкова, 2001 г.; Д.Т. Абдурахманов, 2003 г.; М.М. Ибрагимова, 2004 г.; П.Е. Крель, 1995 г.; С.В. Тэгай, 2003 г.; А.В. Русских, 2004 г.), поражения системы крови (Л.А. Гусейнова, 1981 г.), поражения легких (А.С. Дроздова, 1989 г.), синдрома Шегрена (Т.Н. Лопаткина, 1980 г.; О.В. Чернецова, 2004 г.), поражения почек (А.В. Потапова, 1989 г.; Е.Н. Косминкова, 1992 г.), системных васкулитов при вирусных гепатитах (Е.Н. Семенкова, 1994).
В развитии внепеченочных поражений основное значение имеют иммунные реакции, возникающие в ответ на репликацию вирусов гепатита В (HBV) или С (HCV) в печени, в тканях лимфоидного и нелимфоидного происхождения. Предположения о наличии внепеченочной локализации репликации HBV или HCV возникли в связи с наблюдением случаев быстро развивающегося острого гепатита у пациентов с вирусным циррозом печени (ЦП) после пересадки здоровой донорской печени, что объяснялось внепеченочной локализацией вирусов [1]. Помимо иммунных нарушений в возникновении системных поражений имеет значение прямое цитопатическое действие вирусов гепатита, при этом часто внепеченочное поражение (ВПП) служит единственным проявлением вирусной инфекции и может определять прогноз и тактику лечения заболевания.
Особенности ХГВ с ВПП. У 10—20% больных ХГВ [2]встречаются ВПП, которые включают широкий спектр поражений различных органов и систем.
Поражения кожи, наблюдаемые при острых и хронических болезнях печени, обусловленные HBV, весьма вариабельны и включают макулярные, макулопапулезные, папуловезикулярные высыпания, рецидивирующую крапивницу, петехии, пурпуру, узловатую эритему, скарлатиноподобную сыпь, гангренозную пиодермию, витилиго, гиперпигментацию и изъязвления в области нижних конечностей, аллергический капиллярит, пурпуру Шенлейна—Геноха [3—7].
Смешанная криоглобулинемия (СКГ) встречается у 3—17% больных ХГВ, может проявляться кожной пурпурой, артритами и/или артралгиями, поражением почек, синдромом Рейно [5, 6, 8, 9].
Поражение почек при ХГВ протекает в 3 формах — хронический гломерулонефрит (ХГН), тубулоинтерстициальный нефрит (ТИН), а также при HBV-ассоциированном узелковом полиартериите (УП) [10—16]. Частота поражения почек при ХГВ составляет 14%, в том числе ХГН 12,6%, ТИН 1,4% [11]. В клубочках выявляются депозиты различных антигенов HBV, у отдельных больных в ткани почки обнаружена ДНК HBV [13]. Иммунные комплексы (ИК) могут активировать комплемент и вызывать поражение клубочков путем формирования мембраноатакующих комплексов и дальнейшего каскада реакций, таких как индукция протеаз, оксидативное повреждение и разрушение цитоскелета нефрона [14].
УП—системный васкулит с поражением средних и мелких артерий. В патогенезе HBV-ассоциированной формы важную роль играют циркулирующие ИК, содержащие вирусные белки [15]. По данным Е.Н. Семенковой, инфицирование HBV выявляется в 56,9% случаев УП. [16] Отмечено, что почти все случаи УП, ассоциированного с HBV, связаны с инфекцией HBV дикого типа, характеризующейся HBe-антигенемией и выраженной репликацией HBV. Предположительно повреждение почек происходит в результате отложения вирусных ИК HBeAg-HBeAb [15].
В целом хроническая инфекция HBV вызывает широкий спектр ВПП, в генезе которых имеют значение как иммунокомплексные реакции, так и реакции гиперчувствительности замедленного типа. ВПП ХГВ могут длительно маскировать поражение печени, являясь ведущими клиническими признаками болезни и нередко определяющими прогноз заболевания. Однако с введением программ массовой вакцинации против HBV инфицированность населения начала снижаться. Открытие HСV в 1989 г. положило начало активному изучению обширного спектра ВПП при этой инфекции.
Особенности ХГС с ВПП. Согласно различным исследованиям у 40—74% пациентов, инфицированных HСV, может быть хотя бы одно ВПП за время течения болезни [17—19]. Более того, часто внепеченочные симптомы служат первыми проявлениями инфекции HCV в отсутствие у ряда больных признаков поражения печени. Для ХГС характерно развитие ВПП преимущественно иммунокомплексного генеза, в первую очередь обусловленных СКГ, которая наблюдается у 19—56% больных [18—21]. Только у небольшой группы больных ХГС с СКГ (менее 15%) имеются клинические проявления — криоглобулинемический синдром (КГС) [21, 22]. Распространенность СКГ повышается при более продолжительной персистенции HCV в организме и чаще наблюдается у женщин на 2—3-м десятилетии болезни. В некоторых исследованиях показано, что длительность инфекции HCV у больных ХГС со СКГ почти в 2 раза больше, чем у пациентов без СКГ [20], у 40% больных со СКГ выявляют признаки ЦП.
Установлено, что HCV имеет высокий тропизм к мононуклеарам периферической крови, которые могут служить его резервуаром и местом репликации. HCV связывается с лигандом CD81 на поверхности В-лимфоцитов через белок Е2, что приводит к их активации. На первом этапе продуцируются только поликлональные криоглобулины (КГ), затем доминирующий клон В-клеток начинает продуцировать моноклональные иммуноглобулины. СКГ является причиной системного васкулита с поражением сосудов мелкого и среднего калибра с возможным вовлечением в патологический процесс различных органов и систем [18, 23, 24]. Известно, что при ХГС васкулиты могут быть обусловлены не только СКГ, но и (со значительно меньшей частотой) — иммунными комплексами, не обладающими свойствами преципитировать на холоде, т.е. не содержащими ревматоидный фактор (РФ) класса IgM [18, 25, 26].
Поражение кожи в 95% случаев представлено васкулитом от пурпуры (лейкоцитокластический васкулит) и петехий на нижних конечностях до выраженных некротических язв. Биопсия кожи выявляет иммунокомплексный васкулит мелких сосудов с мононуклеарной инфильтрацией, в 40% случаев определяются антитела к HCV [19].
У больных ХГС без СКГ по сравнению с больным с СКГ пурпура характеризуется меньшей распространенностью и отсутствием язвенно-некротических изменений кожи [27]. Синдром Рейно при ХГС часто проявляется на ранней стадии КГС, некрозы фаланг пальцев, как правило, не наблюдаются [10]. Однако при высоком криокрите частота развития последних увеличивается [27].
Поражение почек при СКГ, связанной с инфекцией HCV, наблюдается в 35—60% случаев. Наиболее часто встречающийся тип гломерулонефрита, ассоциированного с СКГ, — мезангиокапиллярный гломерулонефрит (МКГН). РНК HCV определяется в сыворотке у 81% больных МКГН с СКГ против 25% случаев некриоглобулинемического МКГН. В почечной паренхиме экспрессируются рецепторы CD81 и SR-B1, с помощью которых HCV связывается с мембраной клетки и проникает внутрь путем эндоцитоза [29]. Поражение почек может наблюдаться в дебюте заболевания у 20% больных ХГС. У 25% пациентов при инфекции HCV развиваются протеинурия нефротического уровня (>3 г/сут), отеки, артериальная гипертония и гипокомплементемия; у 30% в дебюте отмечаются остронефритический синдром и острая почечная недостаточность (олигурическая в 5% случаев). У 55% больных наблюдаются только легкая гематурия, протеинурия и начальные стадии почечной недостаточности. При биопсии почки обнаруживаются иммунокомплексные депозиты IgG, IgM с активностью РФ и компонент С3-комплемента. Наиболее характерной гистологической картиной при световой микроскопии являются капиллярные тромбы, состоящие из преципитированных КГ. Менее часто HCV вызывает фокальный сегментарный гломерулярный склероз или мембранозный, или пролиферативный гломерулонефрит [30]. Картина ассоциированного с HCV некриоглобулинемического МКГН существенно не отличается по клиническим и морфологическим признакам от таковой при идиопатическом МКГН [31].
У 30% больных клиническое течение поражения почек при ХГС замедлено, и функция почек остается сохранной многие годы. В 20% случаев болезнь характеризуется рецидивирующими эпизодами остронефритического синдрома. Менее чем 15% больных требуется диализ в связи с развитием терминальной стадии почечной недостаточности [19, 30].
В основном это мононевропатия, а также поражение периферической нервной системы, ассоциированное с УП, которое обычно представлено асимметричной полиневропатией с ведущими моторными нарушениями [19, 27].
Поражение легких. Описано вовлечение сосудов легких (легочный васкулит) в рамках СКГ, проявляющееся легочными инфильтратами, альвеолярным кровотечением [18]. Имеется ряд наблюдений фиброзирующего альвеолита (ФА) у больных ХГС, в том числе с морфологическим подтверждением и обнаружением РНК HCV в ткани легкого [28]. В некоторых регионах мира (Италия, Япония) частота выявления инфекции HCV у больных ФА составляет 13—14%, что значительно выше, чем в целом в популяции [32]. Эти данные, а также результаты исследований бронхоальвеолярной жидкости у больных ХГС, выявляющих повышенное содержание лимфоцитов и эозинофилов, позволили обсуждать пусковую роль HCV в развитии альвеолита [18]. В то же время в Англии частота инфекции HCV у больных ФА оказалась невысокой (1,6%) и роль HCV в его патогенезе ставится под сомнение [33]. По данным Клиники им. Е.М. Тареева, частота поражения легких была выше у больных без СКГ (11,3%), чем с КГ (6,3%). В группе пациентов, у которых КГ не обнаруживались, поражение легких характеризовалось развитием ФА, у больных с КГ наблюдалась картина легочного васкулита [27].
Поражение сердца. Описаны наблюдения хронического миокардита на фоне инфекции HCV. Поражение миокарда, ассоциированное с инфекцией HCV, может быть обусловлено следующими причинами: 1) прямое (вирусное) воздействие на миокард; 2) непрямой (иммунологический) путь; 3) апоптоз клеток, вызванный внутренними и внешними сигналами [34]. Выявлена репликация HCV в миокарде. Кроме того, высказано предположение о прямом повреждающем действии на миокард core-белка HCV. Непрямой иммуноопосредованный путь повреждения миокарда осуществляется при участии В-, Т-клеток и макрофагов. Обнаружение цепей (+) и (–) РНК HCV в ткани миокарда у больных миокардитом, дилатационной миокардиопатией и цепи (+) РНК HCV в миокарде больных гипертрофической кардиомиопатией, сочетающихся с инфекцией HCV, позволяют обсуждать возможность репликации HCV в ткани миокарда, а также роль реакций клеточного иммунитета на тканевые антигены вируса и индуцированные им аутоантигены, роль иммунных комплексов в патогенезе поражения миокарда. Кроме того, не исключается роль цитокинов (продуцируемых активированными вирусом иммуноцитами), которые путем повышения продукции оксида азота вызывают отрицательный инотропный эффект и повреждение сердечной мышцы [35].
Поражение суставов. Артралгии и/или артриты встречаются у 21—74% больных ХГС [19, 24], могут наблюдаться как в рамках КГС, так и в отсутствие СКГ. Описано 2 вида поражения суставов: полиартрит мелких суставов, подобный ревматоидному артриту, который встречается очень редко и имеет мягкое течение, и неэрозивный олигоартрит с вовлечением средних и крупных суставов, часто интермиттирующего течения, как правило, связанный с криоглобулинемией. РФ в сыворотке крови выявляется в 50—80% случаев. Антитела к циклическому цитруллиновому пептиду обнаруживаются менее чем у 6% больных с артритом, ассоциированным с HCV, что можно использовать для дифференциальной диагностики ревматоидного артрита и поражения суставов в рамках инфекции HCV [19].
Синдром Шегрена (СШ). У 14—77% больных ХГС выявляются морфологические признаки лимфоцитарного сиалоаденита, а также поражение слезных желез (у 26—50%), морфологические изменения малых слюнных желез характеризовались небольшой воспалительной инфильтрацией и распространенным фиброзом [36, 37]. Клинически ксерофтальмия и ксеростомия протекают мягко или отсутствуют у 73,8% больных, наибольшая клиническая выраженность СШ отмечалась у больных ХГС с КГ [37]. Наличие СШ у больных с инфекцией HCV является фактором риска развития злокачественной В-клеточной лимфомы, особенно при сочетании со СКГ [38].
Поражение щитовидной железы (ЩЖ). Прямая связь между инфекцией HCV и заболеванием ЩЖ до конца не установлена, однако поражение ЩЖ (особенно гипотиреоз) у больных ХГС встречается чаще, чем в общей популяции. Примерно у 13% больных, инфицированных HCV, выявляется гипотиреоз и у 25% обнаруживаются антитиреоидные антитела. В 30% случаев поражение ЩЖ выявляется в ходе противовирусной терапии (ПВТ).
В связи с этим остается открытым вопрос, является ли нарушение функции ЩЖ индуцированным HCV или нежелательным эффектом ПВТ. Возможно, ПВТ вызывает развитие нарушения функции ЩЖ de novo или обостряет существующее субклиническое поражение ЩЖ [39, 40].
Инфекция HCV и неходжкинская В-клеточная лимфома. В настоящее время доказана этиологическая роль HCV в развитии КГ II типа, представляющей собой доброкачественное лимфопролиферативное заболевание, в основе которого лежит клональная (IgMκ) пролиферация В-лимфоцитов. У отдельных больных ХГС доброкачественная лимфопролиферация трансформируется в злокачественную. У 8—10% больных с СКГ II типа развивается В-клеточная лимфома. Показана высокая распространенность инфекции HCV и при моноклональной иммуноглобулинопатии, обусловленной пролиферацией других (не продуцирующих СКГ) клонов лимфоцитов, а также значительная (до 11%) частота обнаружения моноклональной иммуноглобулинопатии у больных ХГС. HCV персистирует в иммунокомпетентных клетках кроветворной системы, но не способен к интеграции в геном клетки хозяина. Процесс лимфомогенеза при инфекции HCV рассматривается как длительный многостадийный процесс, в основе которого лежит патологическая пролиферация клеток, сочетающаяся с повреждением их генома. Патологическая пролиферация связывается со снижением порога активации В-лимфоцитов, обусловленной взаимодействием HCV со специфическими рецепторами В-клеток (CD81), а также подавлением вирусом апоптоза. В В-лимфоцитах при инфекции HCV повышается экспрессия белка bcl-2 вследствие транслокации t(14;18), играющего важную роль в подавлении апоптоза. Показано также, что core-белок HCV регулирует транскрипцию с-myc и что bcl-2 и c-myc взаимодействуют друг с другом в процессе лимфомогенеза. Гистологически наиболее распространены фолликулярная лимфома, В-клеточная хроническая лимфоцитарная лейкемия/лимфома из малых лимфоцитов, лимфоплазмоцитарная лимфома и лимфома маргинальной зоны. Среди последних описана особая ассоциация инфекции HCV с MALT-лимфомой [18, 41, 42]
Таким образом, при ХГС многообразие ВПП инфекции обусловлено в первую очередь смешанной криоглобулинемией и характеризуется развитием у ряда больных КГС с поражением кожи, суставов, мышц, почек и других органов и систем. Особенностью доброкачественной лимфопролиферации, свойственной ХГС, является возможность трансформации в злокачественную с развитием В-клеточной лимфомы. Как и при ХГВ, внепеченочные проявления ХГС создают трудности при дифференциальном диагностике ХГС, определяя у отдельных больных неблагоприятный прогноз криоглобулинемического васкулита, поражения почек, В-клеточной лимфомы.
Лечение больных ХГВ и ХГС с системными проявлениями. Адекватный подход к лечению хронических вирусных гепатитов с ВПП включает две независимые, но тесно связанные цели. Первая — эрадикация вируса или снижение вирусной нагрузки с помощью этиотропной ПВТ. Вторая — патогенетическое лечение аутоиммунных нарушений с использованием иммуносупрессивной терапии и/или плазмафереза с целью контроля образования иммунных комплексов.
По мнению большинства исследователей, для лечения инфекции хронической HBV оптимальна комбинированная терапия: использование препаратов, различающихся по механизму действия, — сочетание α-интерферона (ИФН-α) с аналогами нуклеоз(т)идов, сочетание нескольких аналогов нуклеоз(т)идов. Преимуществом ИФН-α является более низкая частота рецидивов после отмены препарата, а аналогов нуклеоз(т)идов — отсутствие нежелательных эффектов, в том числе иммуностимулирующего действия, что обусловливает его применение у больных с выраженными ВПП и декомпенсированным ЦП. В ряде случаев при выраженных системных поражениях оправданно применение иммуносупрессивной терапии, несмотря на активирующее влияние глюкокортикостероидов на репликацию HВV [6, 43—46].
Лечение больных ХГС со СКГ направлено на подавление вирусной репликации и угнетение В-клеточной пролиферации. Эрадикация HCV при ПВТ приводит к исчезновению СКГ и регрессу клинических проявлений, но некоторые больные ХГС не отвечают на ПВТ, у ряда пациентов отмечаются выраженные нежелательные эффекты лечения. Применение глюкокортикостероидов при хроническом вирусном гепатите с аутоиммунными нарушениями может приводить к увеличению вирусной нагрузки. В то же время известно, что интерферонотерапия может вызывать усугубление таких ВПП инфекции HCV, как периферическая невропатия, миокардит, тубулоинтерстициальный нефрит, полимиозит. Недавно предложено использовать ритуксимаб (химерные моноклональные антитела к CD20) в качестве анти-В-клеточной терапии у больных ХГС с криоглобулинемией, не отвечающих на ПВТ [47, 48]. Его действие связано с быстрым, но обратимым, угнетением CD20+ В-клеток в периферической крови [49, 50]. Ряд исследований свидетельствуют об эффекте ритуксимаба у больных ХГС с периферической невропатией и комбинации ритуксимаба и плазмафереза у больных ХГС с криоглобулинемическим васкулитом [47, 51], а также об эффективности ритуксимаба и ПВТ у больных ХГС с криоглобулинемическим гломерулонефритом и сосудистой пурпурой [23, 52].
Таким образом, лечение больных хроническими вирусными гепатитами с ВПП не разработано, представляет серьезные проблемы и нуждается в дальнейшем изучении и определении тактики.
Читайте также:

