Путь прохождения вируса в клетку хозяина называют
Обновлено: 22.04.2024
Мы кратко рассмотрели структуру вирионов гриппа и процесс кодирования вирусными РНК одного и более белков. Теперь обратимся к размножению вирусов гриппа.
Вирусы – это исключительно внутриклеточные паразиты, они не могут воспроизводиться вне клетки. Появление новых инфекционных частиц должно протекать внутри клетки. Войдя в клетки, вирусы начинают паразитировать в структуре хозяина для воспроизводства вирусного потомства. Все события, происходящие в инфицированной вирусом клетке, называются инфекционным циклом, или вирусной репликацией. Вирусологи искусственно разделяют инфекционный цикл на несколько стадий, чтобы проще было его изучить. Эти стадии включают прикрепление и вхождение вириона, трансляцию мРНК в белок, репликацию генома (создание большего количества РНК или ДНК), скопление новых частиц и выход частиц из клетки. Мы рассмотрим каждую из названных стадий, а затем обсудим, как вирус гриппа инфицирует нас и вызывает болезнь.
Остановимся на первой стадии – прикреплении вириона к клетке. Возьмем обычную клетку, с которой, я уверен, знаком каждый. Но не будет лишним повториться.
Рисунок 10.
Слева показан клеточный белок, прикрепленный к цитоплазматической мембране. Снизу изображена внутренняя часть клетки – цитоплазма. Часть белка пересекает мембрану, и также видны части цитоплазматической и внеклеточной сторон. Сферы – это сахара, прикрепленные ко множеству белков (белок + сахар = гликопротеин). Сиаловая кислота всегда является последним сахаром в цепи, которая прикрепляется к белку. Справа показана химическая структура сиаловой кислоты; следующий сахар (справа) – галактоза. Вирионы гриппа прикрепляются к клеткам, когда HA захватывает очень маленькую сиаловую кислоту.
Сахар в сравнении с HA в действительности очень мал – он подходит к небольшому кармашку на острие шипа. На рис. 11 изображена молекулярная модель, демонстрирующая, как HA прикрепляется к аналогу сиаловой кислоты. Шаровидный конец HA показан в верхней части рис. 11. Маленькие красные и белые сферы показывают места будущего прикрепления сиаловой кислоты – кармашки на верхнем конце HA.
Рисунок 13.
Процесс вхождения вируса гриппа в клетки – наиболее понятный из всех известных механизмов проникновения вирусов. После прикрепления вириона к сиаловой кислоте, имеющей рецепторы на поверхности клетки, вирус-рецепторный комплекс входит в клетки посредством эндоцитоза – процесса, в ходе которого клетки обычно берут молекулы из внеклеточной жидкости. Пока эндосомальные везикулы, содержащие частицы вируса, движутся к ядру клетки, их pH понижается. Это изменение в pH завершает клеточный канал, закачивающий протоны (H+) в везикулу. Когда эндосомальная pH достигает 5,0, вирусный белок HA подвергается конформационной перестройке. Это изменение подвергает пептид слияния на HA короткой гидрофобной последовательности, вставляющей его в эндосомальную мембрану, которая от этого сливается с вирусной оболочкой. Когда это происходит, вирусные РНК проникают в цитоплазму. Затем они транспортируются в ядро клетки, где начинается размножение.
В вирионе гриппа вирусные РНК не оголены, поскольку к ним прикреплены вирусные белки, включая белок M1. Этот белок образует оболочку, лежащую в основе липидной мембраны вириона. К сожалению, если вирусные РНК прикрепляются к белку M1, когда выходят из вириона, они не могут достичь ядра. Для решения этой проблемы вирион гриппа имеет в своей мембране несколько копий белка, называемого M2. Этот вирусный белок образует канал в мембране, который активно закачивает протоны из эндосомы во внутреннюю часть вириона. Данные протоны понижают pH внутри вириона, освобождая вирусные РНК от M1. В этом случае РНК могут войти в ядро.
Ионный канал M2, являющийся мишенью для противовирусных адамантанов, показан на рис. 14. Эти образования забивают канал и не позволяют протонам закачиваться в вирион. В присутствии адамантанов вирусным РНК нужно прикрепляться к M1, отчего они не могут достичь ядра. Поэтому вирусная репликация подавляется. Устойчивость к адамантанам возможна при изменении в аминокислотах, прокладывающих канал M2. Такие изменения не дают лекарству забить канал.
Рисунок 15.
На рис. 15 сферический конец белка HA, который прикрепляется к рецепторам клетки, изображен сверху, а вирусная мембрана – снизу. Для наглядности помечен только сайт расщепления HA. Нерасщепленная форма белка называется HA0; после расщепления клеточным ферментом образуются два белка, называемые HA1 (синий) и HA2 (красный). Две субъединицы остаются вместе на поверхности вирусной частицы. Новая амино(N)-концевая область HA2, образовавшегося при расщеплении, содержит последовательность гидрофобных аминокислот, называемых пептидом слияния. Во время вхождения вируса гриппа в клетки пептид слияния вставляется в эндосомальную мембрану и вызывает слияние вирусной и клеточной оболочек. Следовательно, вирусные РНК гриппа могут войти в цитоплазму. Процесс слияния описан в предыдущем параграфе.
Если белок HA не расщеплен, чтобы образовать HA1 и HA2, слияния не происходит. Поэтому вирусы гриппа с нерасщепленным HA не заразны. Расщепление вирусного HA происходит после того, как вновь синтезированные вирионы выходят из клетки. Вирусы гриппа эффективно размножаются в яйцах из-за присутствия протеазы в аллантоисной жидкости, способной расщеплять HA. Однако репликация многих штаммов вируса гриппа в культурах клеток требует добавления в среду соответствующей протеазы (как привило, трипсина).
У людей репликация вируса гриппа ограничена дыхательными путями, потому что это единственный участок, где производится протеаза, расщепляющая HA. Однако белок HA высокопатогенных штаммов H5 и H7 вируса птичьего гриппа может расщепляться протеазами, производимыми во многих различных тканях. В результате эти вирусы способны размножаться во многих органах птиц, включая селезенку, печень, легкие, почки и мозг. Это свойство объясняет способность штаммов H5N1 вируса птичьего гриппа размножаться вне дыхательных путей человека.
Подобно белкам HA высокопатогенных вирусов H5 и H7, HA штамма вируса гриппа 1918 г. может также расщепляться повсеместно присутствующими клеточными протеазами. Следовательно, вирус может размножаться в культурах клеток без добавления трипсина.
Белки HA H5 и H7 имеют множество основных аминокислотных остатков на сайте расщепления HA1-HA2, которые делают возможным расщепление посредством широко представленных протеаз. Но HA вируса гриппа H1 1918 г. не обладал этим свойством. Также N1 1918 г. не был в состоянии привлечь протеазы, которые расщепляли бы HA, т. е. не было механизма, позволяющего штамму A/WSN/33 вируса гриппа размножаться в клетках без трипсина. Понимание того, как белок HA вируса H1 1918 г. мог быть расщеплен протеазами – основной в понимании высокой патогенности данного штамма.
Рекомендуемая литература.
Chaipan, C., Kobasa, D., Bertram, S., Glowacka, I., Steffen, I., Solomon Tsegaye, T., Takeda, M., Bugge, T., Kim, S., Park, Y., Marzi, A., &Pohlmann, S. (2009). Proteolytic Activation of the 1918 Influenza Virus Hemagglutinin Journal of Virology, 83 (7), 3200-3211 DOI:10.1128/JVI.02205-08.
Главная задача биологии — это развитие представлений у человека о живых организмах, о многообразии видов, обо всех закономерностях развития живых существ, а также об их взаимодействии с окружающей природой. Предмет основы безопасности жизнедеятельности (ОБЖ) позволяет получить знания и умения, которые помогут сохранить жизнь и здоровье в опасных ситуациях. Эти ситуации всегда возникают неожиданно, но, тем не менее, большинство из них предсказуемы и к ним можно подготовиться заранее. ОБЖ учит нас предвидеть возможные опасности и минимизировать потери от той или иной ситуации. Сегодня мы сталкиваемся с новым видом вирусной опасности COVID-19,о котором поговорим с точки зрения биологии и ОБЖ.
Что такое вирус?
Вирус — это неклеточный инфекционный агент. Сегодня нам известно около 6 тысяч различных вирусов, но их существует несколько миллионов. Вирусы не похожи друг на друга и могут иметь как форму сферы, спирали, так и форму сложного асимметричного сплетения. Размеры вирусов варьируются от 20 нм до 300 нм.
Как устроен вирус?
В центре агента находится генетический материал РНК или ДНК, вокруг которого располагается белковая структура — капсид.
Капсид служит для защиты вируса и помогает при захвате клетки. Некоторые вирусы дополнительно покрыты липидной оболочкой, т.е. жировой структурой, которая защищает их от изменений окружающей среды.
Вирусолог Дэвид Балтимор объединил все вирусы в 8 групп, из которых некоторые группы вирусов содержат 1-2 цепочки ДНК. Другие же содержат 1 цепочку РНК, которая может удваиваться или достраивать на своей матрице ДНК. При этом каждая группа вирусов производит себя в различных органеллах зараженной клетки.
Вирусы имеют определенный диапазон хозяев, т.е. он может быть опасен для одних видов и абсолютно безвреден для других. Например, оспой болеет только человек, а чумкой только некоторые виды плотоядных. Вирус не способен выжить сам по себе, поэтому активируется только в хозяйской клетке, используя ее ресурсы и питательные вещества. Цель вируса — создание множества копий себя, чтобы инфицировать другие клетки!
Как вирус попадает в организм?
- через физические повреждения (например, порезы на коже)
- путём направленного впрыскивания (к примеру, укус комара)
- направленного поражения отдельной поверхности (например, при вдыхании вируса через трахею)
- к эпителию слизистых оболочек (это например вирус гриппа)
- к нервной ткани (вирус простого герпеса)
- к иммунным клеткам (вирус иммунодефицита человека)

Геном вируса встраивается в одну из органелл или цитоплазму и превращает клетку в настоящий вирусный завод. Естественные процессы в клетке нарушаются, и она начинает заниматься производством и сбором белка вируса. Этот процесс называется репликацией. И его основная цель — это захват территории. Во время репликации генетический материал вируса смешивается с генами клетки хозяина — это приводит к активной мутации самого вируса, а также повышает его выживаемость. Когда процесс репликации налажен, вирусная частица отпочковывается и заражает уже новые клетки, в то время как инфицированная ранее клетка продолжает производство.
Выход вируса
Вирус создал множество собственных копий, клетка оказывается изнуренной из-за использования ее ресурсов. Больше вирусу клетка не нужна, поэтому клетка часто погибает и новорожденным вирусам приходится искать нового хозяина. Это и есть заключительная стадию жизненного цикла вируса.
Скорость распространения вирусной инфекции
Размножение вирусов протекает с исключительно высокой скоростью: при попадании в верхние дыхательные пути одной вирусной частицы уже через 8 часов количество инфекционного потомства достигает 10³, а концу первых суток − 10²³.
Вирусная латентность
Как вирус распространяется?
- воздушно-капельный (кашель, чихание)
- с кожи на кожу (при прикосновениях и рукопожатиях)
- с кожи на продукты (при прикосновениях к пище грязными руками вирусы могут попасть в пищеварительную и дыхательную системы)
- через жидкие среды организма (кровь, слюну и другие)
Почему с вирусами так тяжело бороться?
Сегодня людям уже удалось победить некоторые вирусы, а некоторые взять под жесткий контроль. Например, Оспа (она же черная оспа). Болезнь вызывается вирусом натуральной оспы, передается от человека к человеку воздушно-капельным путем. Больные покрываются сыпью, переходящей в язвы, как на коже, так и на слизистых внутренних органов. Смертность, в зависимости от штамма вируса, составляет от 10 до 40 (иногда даже 70%), На сегодняшний день вирус полностью истреблен человечеством.
Кроме того, взяты под контроль такие заболевания, как бешенство, корь и полиомиелит. Но помимо этих вирусов существует масса других, которые требуют разработок или открытия новых вакцин.
Коронавирус
Виновником эпидемии, распространяющейся сегодня по миру, стал коронавирус, вирусная частица в 0,1 микрона. Свое название он получил благодаря наростам на своей структуре, своеобразным шипам. Внутри вируса спрятан яд, с помощью которого он подчиняет себе зараженный организм. Этот вирус воздействует не только на человека, но и на птиц, свиней, собак и летучих мышей. В настоящий момент выделяют от 30 до 39 разновидностей коронавирусной инфекции. Но для человека патогенно всего 6. И как любой другой вирус COVID-19 мутирует.

К наиболее распространенным симптомам COVID-19 относятся повышение температуры тела, сухой кашель и утомляемость. К более редким симптомам относятся боли в суставах и мышцах, заложенность носа, головная боль, конъюнктивит, боль в горле, диарея, потеря вкусовых ощущений или обоняния, сыпь и изменение цвета кожи на пальцах рук и ног. Как правило, эти симптомы развиваются постепенно и носят слабо выраженный характер. У некоторых инфицированных лиц болезнь сопровождается очень легкими симптомами.
Сколько же может жить этот вирус вне организма? Все зависит от типа вируса и от той поверхности, на которую вирусы попали. В качестве примера было рассмотрено 3 вируса, по которым велись исследования. Изучали время, на которое может задерживаться вирус на различных поверхностях. Данные приведены в таблице.

Поскольку пока не изобретено вакцины от COVID-19, в целях защиты от инфекции самым важным для нас является соблюдение гигиены.
Гигиена — раздел медицины, изучающий влияние жизни и труда на здоровье человека и разрабатывающая меры (санитарные нормы и правила), направленные на предупреждение заболеваний, обеспечение оптимальных условий существования, укрепление здоровья и продление жизни.
Сегодня следует соблюдать определенные правила гигиены:
- Соблюдение режима труда и отдыха, не допускающего развития утомления и переутомления.
- Выполнение условий, обеспечивающих здоровый и полноценный сон (свежий воздух, отсутствие шума, удобная постель, оптимальная продолжительность).
- Правильное здоровое питание в соответствии с потребностями организма.
- Комфортный микроклимат в жилище (температура, влажность и подвижность воздуха, естественная и искусственная освещенность помещений).
- Содержание в чистоте тела и тщательный уход за зубами.
- Спокойное и корректное поведение в конфликтных ситуациях.

Вирус (лат. virus - яд) - неклеточная форма жизни, мельчайшие болезнетворные микроорганизмы, не видимые в микроскоп. Они значительно меньше бактерий: легко проходят через бактериальные фильтры.
Вирусы способны размножаться только внутри живых клеток, до проникновения в них вирусы не имеют признаков жизни: пассивно перемещаются во внешней среде, ожидая встречи с клеткой-мишенью.
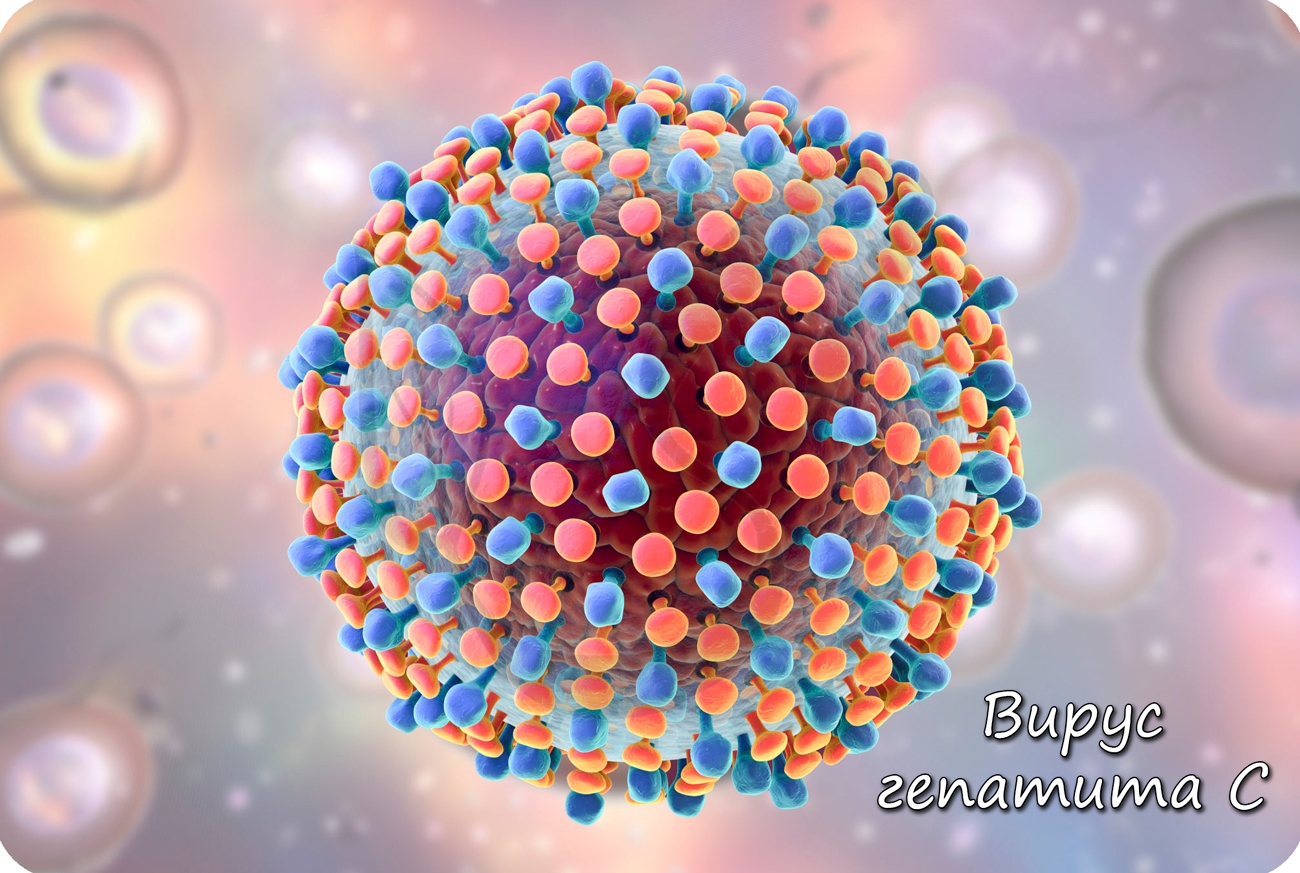
В 1892 году Ивановский Д.И. в ходе изучения мозаичной болезни табака обнаружил, что болезнь вызывается мельчайшими субстанциями, которые проходят через бактериальный фильтр, то есть были меньше бактерий. Вирусы впервые увидели в электронный микроскоп в 1939 году (спустя 19 лет со смерти Ивановского), однако считается, что именно Ивановский положил начало вирусологии как науке.

- Наличие наследственности и изменчивости
- Способность к репродукции (воспроизведению себе подобных)
-
Неживое (инертное) состояние
Вне клетки хозяина находятся в неживом состоянии, ожидая внедрения. Вирусы - облигатные внутриклеточные паразиты.
У вирусов отсутствует обмен веществ с внешней средой (метаболизм).
Не имеют клеточной мембраны, ограничивающих их от внешней среды, и, соответственно, клеточного строения.
У вирусов отсутствует половое размножение и деление. Попав в живую клетку, вирус встраивает свою нуклеиновую кислоту (РНК/ДНК) в наследственный материал клетки-мишени. В результате клетка начинает синтезировать вирусные белки (новые вирусы): так увеличивается численность вирусов.
Вирусы не растут, не увеличиваются в размерах. Стратегия их жизни - безудержное размножение.
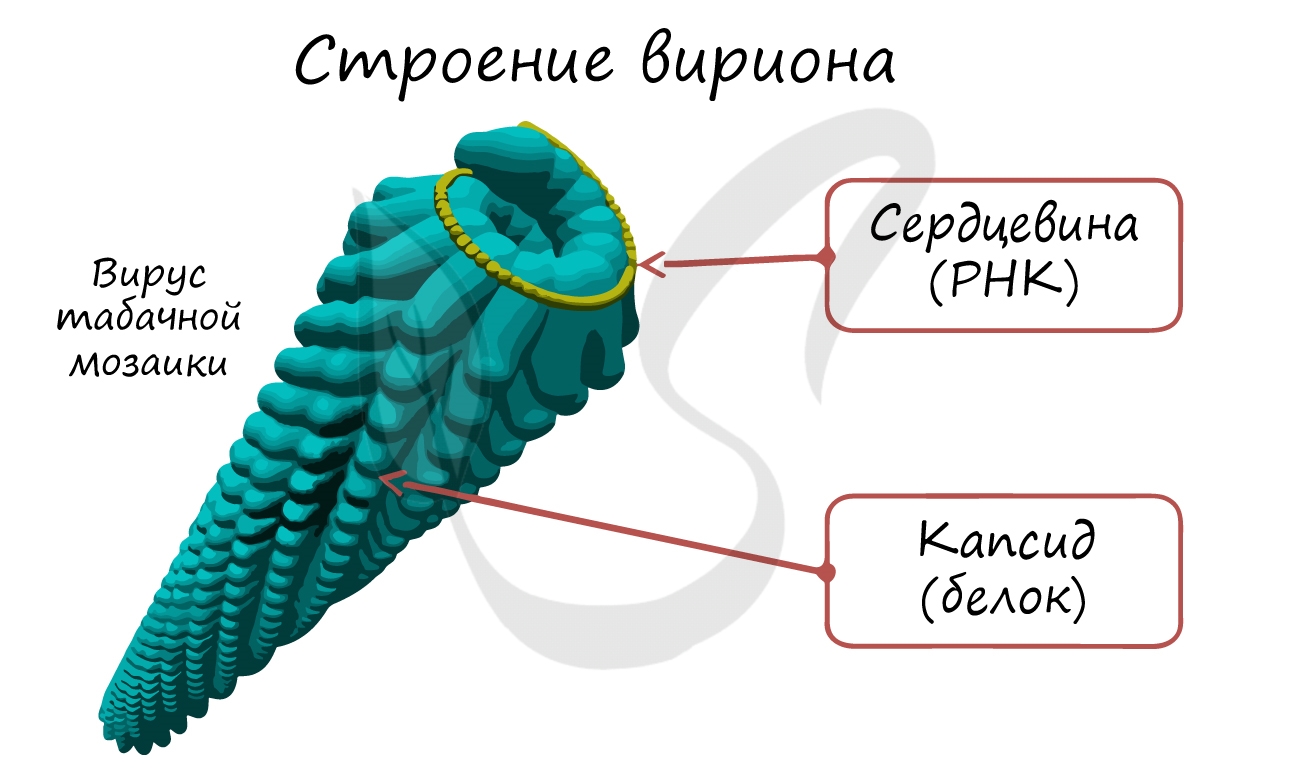
Если мы заглянем в клетку, инфицированную вирусом, то от вируса мы увидим только один элемент - его нуклеиновую кислоту (ДНК/РНК). Во внешней среде вирусы существуют в виде вирионов - полностью сформированных вирусных частиц, состоящих из белковой оболочки (капсида) и нуклеиновой кислоты внутри.
Носителем наследственной информации у вирусов может быть ДНК, РНК. В связи с этим все вирусы подразделяются на ДНК- и РНК-содержащие.
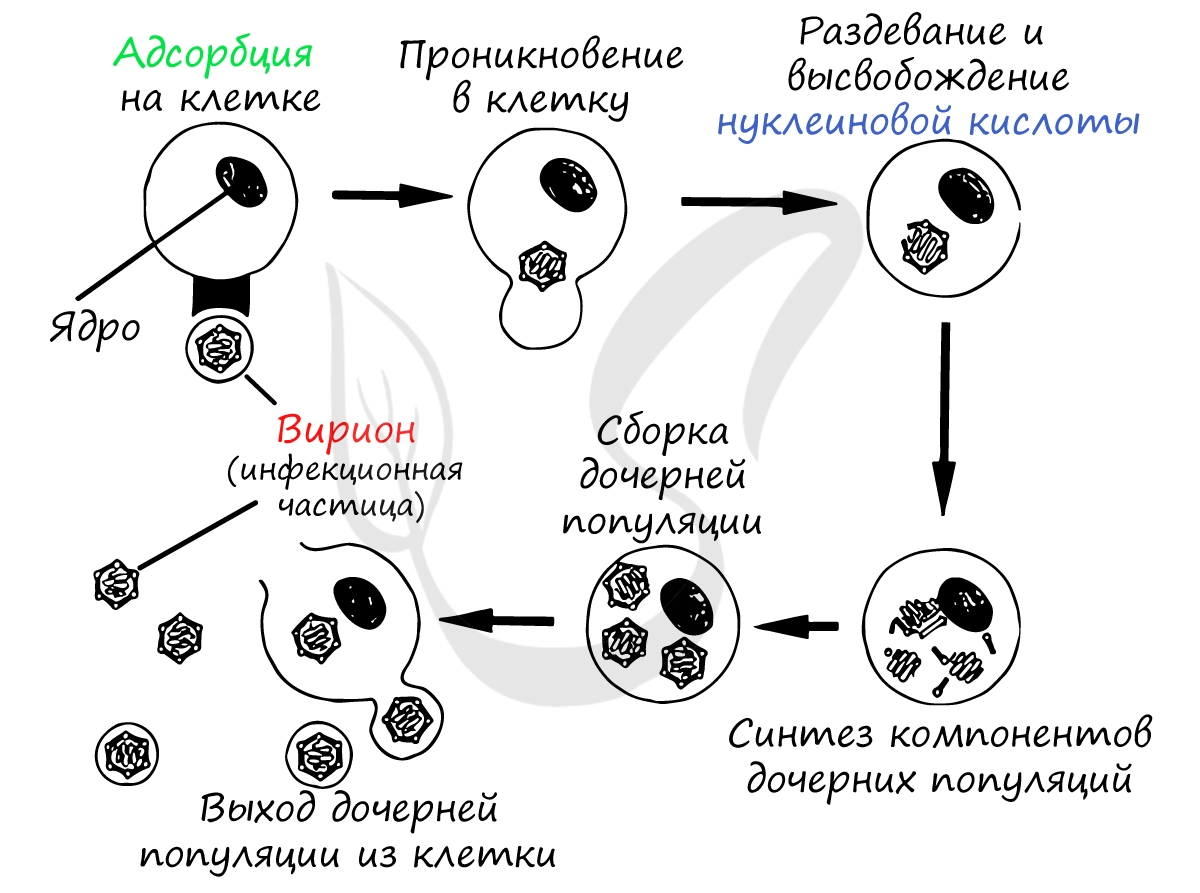
Взаимодействие вируса с клеткой
Найдя клетку, на поверхности которой есть подходящий рецептор, вирус взаимодействует с ним и прикрепляется к мембране клетки. Путем эндоцитоза (образование вакуоли) вирус проникает внутрь клетки, выходит из вакуоли в цитоплазму. Наследственный материал (ДНК/РНК) вируса реализуется по схеме: ДНК ↔ РНК → белок.
Проникнув внутрь клетки (инфицировав ее), вирус реализует собственный генетический материал (ДНК/РНК) путем синтеза вирусного белка на рибосомах клетки хозяина. Клетка даже и не подозревает, что вирус встроил в ее РНК/ДНК свой генетический код - она принимает его как свой собственный, а в результате синтезирует вирусные белки.
Образовавшиеся белки объединяются в вирусные частицы, которые могут выходить из клетки разными путями. Вирионы вирусов гепатита C выходят из клетки путем почкования (экзоцитозом), при таком варианте клетка долгое время остается живой и служит для продукции новых вирионов.
Известен и другой механизм выхода вирионов из клетки: взрывной, при котором оболочка клетки разрывается, и тысячи вирионов отправляются инфицировать новые клетки. Такой способ характерен для аденовирусов, ротавирусов.
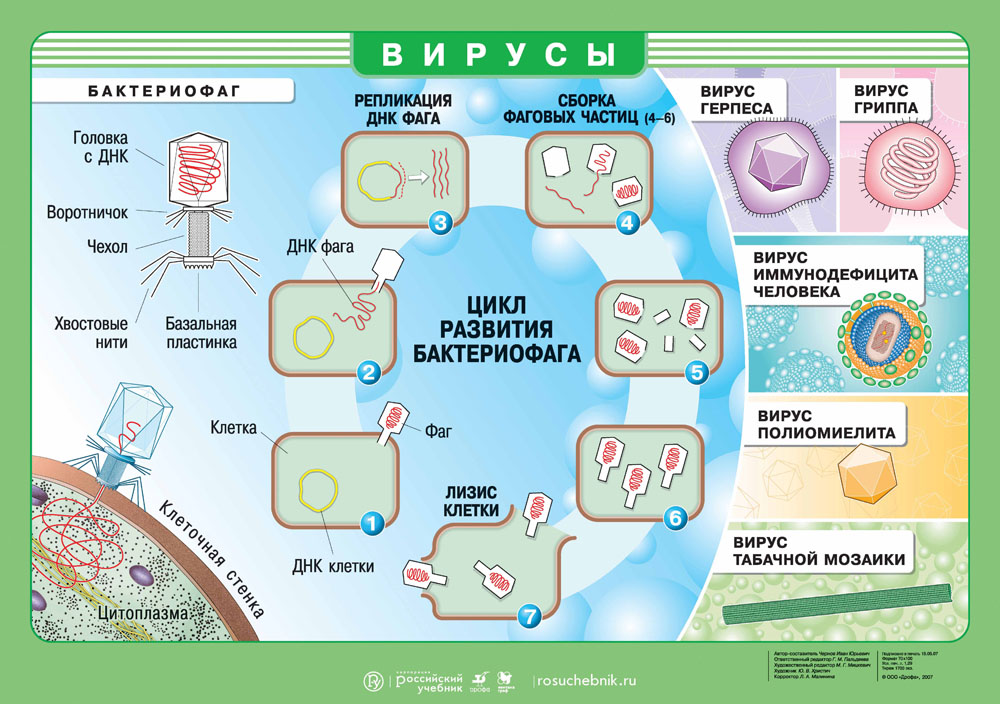
Бактериофаги ("бактерия" + греч. phag(os) — пожирающий)
Это уникальная группа вирусов, инфицирующая только бактерии. Бактериофаг имеет капсид, с содержащимся внутри наследственным материалом - ДНК (реже РНК), протеиновым хвостом. Бактериофаги открыты в 1915 году и с тех пор активно применяются в ходе генетических исследований.
Ниже вы можете видеть типичное строение бактериофага. Бактериофаг напоминает шприц, который протыкает стенку бактерии и впрыскивает внутрь нее свою нуклеиновую кислоту.
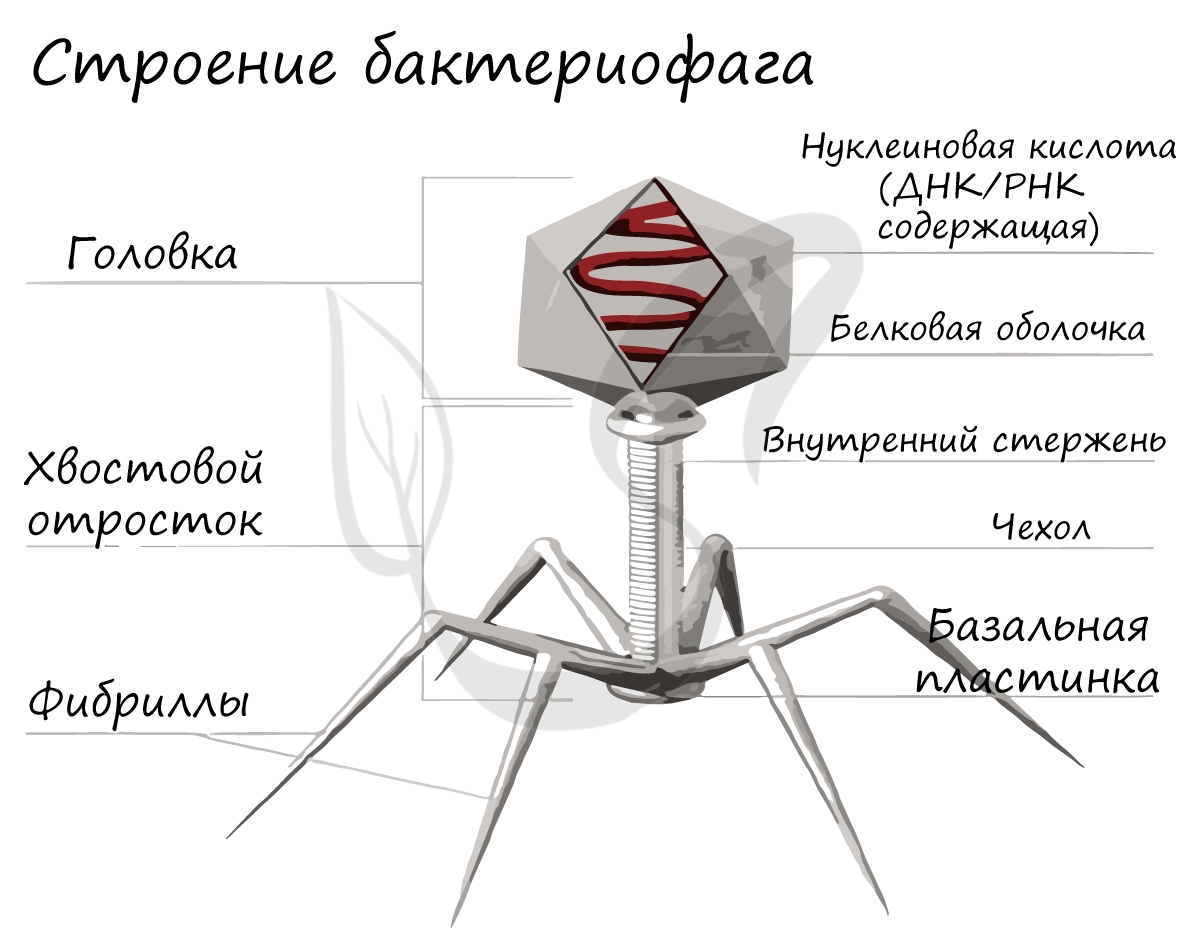
Бактериофаги успешно применяются в медицине для лечения многих заболеваний. Это высокоэффективные, дорогостоящие препараты, которые помогают, например, нормализовать микрофлору кишечника при бактериальных инфекциях.
Вирусные инфекции
Вирусы вызывают множество заболеваний человека и животных. Некоторые из них неизлечимы даже на современном этапе развития медицины, например бешенство. К вирусным инфекциям относятся грипп, корь, свинка, СПИД (вызванный ВИЧ), полиомиелит, желтая лихорадка, онковирусы.
Такая группа, как онковирусы, потенцируют развитие опухолей в организме. К ВИЧ и онкогенным вирусам не существует специфических антител, что затрудняет процесс создания вакцины. В то же время против ряда вирусных инфекций: корь, ветряная оспа созданы вакцины, создающие стойкий пожизненный иммунитет.
Клетки вырабатывают защитный белок - интерферон. Это вещество подавляет синтез новых вирусных частиц, приводит к повышению температуры тела (например, при гриппе).

Вирус иммунодефицита человека (ВИЧ) представляет для организма большую опасность. Он размножается в T-лимфоцитах - клетках крови, которые выполняют иммунную функцию. С гибелью T-лимфоцитов разрушается иммунная система, становится невозможным сопротивление организма бактериями, вирусам и грибам, что в отсутствии лечения приводит к вторичным инфекциям.
Риск заражения ВИЧ присутствует при гемотрансфузии (переливании крови), половом акте. Инфекция также может быть передана от ВИЧ инфицированной матери к плоду.

Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.

Но и Дженнер не имел представления о том, что является причиной заболевания оспой. В XIX веке все болезнетворные организмы и вещества без разбора называли вирусами. Лишь благодаря опытам отечественного биолога Дмитрия Иосифовича Ивановского прекратилась эта путаница! Он пропускал экстракт заражённых табачной мозаикой 1 растений через бактериальные фильтры, сквозь которые не проходят даже самые мелкие бактерии. Выяснилось, что экстракт оставался по-прежнему заразным для других растений. Значит, возбудителями табачной мозаики были организмы, меньшие по размеру, чем бактерии; их назвали фильтрующимися вирусами. Вскоре бактерии перестали называть вирусами, а сами вирусы выделили в отдельное царство живых организмов. Дмитрий Ивановский же во всём мире по праву считается основателем вирусологии — науки о вирусах.

Рис. 2. Дженнер прививает Джеймса Фиппса от оспы
Но что мы пока поняли про вирусы? Только то, что они меньше бактерий. Чем же вирусы так не похожи на другие организмы? И почему понадобилось вдруг их выделять в отдельное царство? А вот почему. В отличие от других живых организмов, вирусы не имеют клеточного строения, а значит, и всех характерных для клетки структур. А ещё они единственные, кто не умеет самостоятельно производить белок, главный строительный материал всего живого. Поэтому их размножение невозможно вне заражённой клетки. Из-за этого многие учёные не без оснований считают вирусы внутриклеточными паразитами.
Жертвами различных вирусов становятся представители всех без исключения существующих царств живых организмов! Так, есть вирусы растений — вирус табачной мозаики (рис. 3, слева), вирус мозаики костра (это растение изображено на рисунке 3, справа), вирус желтухи свёклы, вызывающий иногда даже эпидемии. Кстати, в растение вирус просто так не проникнет. Заражение происходит при травмах растительных тканей. Типичный пример: тля пьёт сок из стебля и для этого протыкает покровные ткани — а вирус тут как тут.

Рис 3. Слева: листья табака, поражённые вирусом табачной мозаики. Справа: костёр (лат. Brómus) — род многолетних травянистых растений семейства Злаки. Если посмотреть на заросли костра в ветреную погоду, его крупные метёлки, склоняясь под ветром то в одну, то в другую сторону, отсвечивают красноватым светом в солнечных лучах, очень напоминая языки пламени. Отсюда, вероятно, и произошло русское название этого растения
Грибы тоже поражаются вирусами, вызывающими, например, побурение плодовых тел у шампиньонов или изменение окраски у зимнего опёнка. Причиной многих опасных заболеваний животных и человека тоже служат вирусы: вирус гриппа, ВИЧ (вирус иммунодефицита человека), вирус Эбола, вирус бешенства, герпеса, клещевого энцефалита и т. д.
Есть даже вирусы, поражающие бактерии, их называют бактериофагами 2 . Так, в конце XIX века исследователи из Института Пастера заметили, что вода некоторых рек Индии обладает бактерицидным действием, то есть способствует снижению роста бактерий. И достигалось это благодаря присутствию в речной воде бактериофагов.

Рис. 4. Слева: вирус табачной мозаики. В центре: вирус мозаики костра похож на футбольный мяч (справа)

Рис. 5. Слева направо: вирус герпеса, аденовирус А человека, бактериофаг

Рис. 6. Маленькие вирусы-спутники внутри гигантского мимивируса
Но не стоит думать, что вирусы причиняют исключительно вред другим организмам! Так, исследователи из Пенсильванского университета показали, что безвредный для человека вирус AAV2, встречающийся почти у всех людей, убивает самые разные виды раковых клеток. При этом здоровые клетки организма вирус не заражает.
А совсем недавно стало известно, что вирусы тоже болеют. Мимивирус, поражающий амёбу Acanthamoeba polyphaga, сам страдает от другого вируса-спутника (рис. 6). Он, кстати, так и называется — Спутник. Этот вирус-спутник использует механизмы воспроизводства мимивируса для собственного размножения, мешая ему нормально развиваться в клетке амёбы. По аналогии с бактериофагами, он был назван вирофагом, то есть пожирающим вирусы. Можно сказать, что присутствие вируса-спутника в амёбе обеспечивает ей больше шансов на выживание в борьбе с мимивирусом.

Что день грядущий мне готовит?
Мир непредсказуем. Эту простую истину в той или иной степени испытал на себе каждый, но есть те, для кого неопределенность будущего представляет собой каждодневную головную боль: это биржевые игроки, фанаты игры на тотализаторе, не объяснившиеся влюбленные и все живые существа, планирующие оставить потомство. Родители всегда немного похожи на генералов, хорошо готовых к уже прошедшим войнам, поэтому неудивительно, что, отпуская потомство в большой мир, они оказываются не в состоянии предсказать ожидающие его опасности. Да что мы — даже наши гены бессильны в этом вопросе.
Самая простая и очевидная из этих стратегий — пластичность, то есть способность подстраивать свое развитие под окружающие обстоятельства. Если растение периодически теребить рукой, имитируя ветер или наличие преграды, оно вырастет невысоким и распластанным по земле, если же оставить его в покое, то оно вытянется ввысь. Разделенные близнецы могут вырасти очень непохожими друг на друга. И так далее. Итак, большинство организмов в той или иной степени обладает пластичностью, и это прекрасно, но есть, однако, и некоторые проблемы.
Во-первых, пластичность может быть затратной сама по себе (подробно это обсуждается, например, в статье J. R. Alud et al., 2009. Re-evaluating the costs and limits of adaptive phenotypic plasticity). Все-таки, чтобы один и тот же организм мог идти по самым разным путям развития, в его геноме, клетках, органах и т. д. уже должна существовать машинерия для реализации этих направлений развития.
Немного этимологии
Говоря строго, бет-хеджинг — это стратегия, позволяющая снизить дисперсию (вариацию) собственного репродуктивного успеха за счет уменьшения среднего репродуктивного успеха. Причем если говорить совсем уж формально, то речь идет об уменьшении геометрического среднего. Я думаю, нет смысла вдаваться во все эти детали, поэтому переформулирую определение чуть более вольно. Бет-хеджинг — это стремление организма уменьшить возможный разброс числа успешных потомков за счет снижения средней численности этих потомков.
Представьте себе два растения: одно из них за три репродуктивных сезона произвело 4 + 3 + 4 взошедших семени, а второе — 100 + 0 + 0. Заметно, что одно из этих растений дает стабильный, но небольшой приплод, а у другого то густо, то пусто. Кажется, что второе растение должно оказаться в эволюционном выигрыше, поскольку в целом производит больше потомков, но давайте представим себе, что в первый год условия были благоприятные, а во второй и третий — засушливые. Тогда может так получиться, что потомки второго растения (вспомним, что они унаследовали гены своего родителя!) дадут мало потомства или не дадут никакого, в то время как потомки первого растения будут потихоньку размножаться. Тогда картина становится чуть менее однозначной. Если же предположить, что наши растения короткоживущи, а засушливые годы продолжатся, то второе растение и все его потомки могут вообще потерпеть эволюционную катастрофу, и их линия вымрет. Таким образом, может оказаться, что менее плодовитое, но более приспособленное к различным окружающим условиям растение может оказаться фаворитом на долгой эволюционной дистанции.
Каким же образом первое растение может добиться такой впечатляющей стабильности? Существуют как минимум две стратегии бет-хеджинга (см. Olofsson et al., 2009. Bet-hedging as an evolutionary game: the trade-off between egg size and number):

Долгое время основным объектом исследования бет-хеджинга были однолетние растения, живущие в пустынях и полупустынях. Со временем выяснилось, что и другие живые существа могут использовать бет-хеджинг при формировании своей стратегии размножения (см. M. E. Evans, J. J. Dennehy, 2005. Germ banking: bet-hedging and variable release from egg and seed dormancy). Так, размер выводка у птиц может определяться желанием родителей подстраховаться на случай неподходящих условий. Покоящиеся яйца многих планктонных животных, способные сотни лет пролежать в иле, тоже могут считаться попыткой распылить ставки. В последнее время выяснилось, что и вирусы не пренебрегают бет-хеджингом.
В своей работе группа американских ученых выяснила, какие механизмы ответственны за формирование стратегии бет-хеджинга у цитомегаловируса (ЦМВ) — одного из самых распространенных вирусов в человеческой популяции (рис. 1).
Вирионы цитомегаловируса: оппортунисты и радикалы
Цитомегаловирус, также известный под названием вирус герпеса человека 5-го типа, представляет собой двухцепочечную ДНК, погруженную в плотную белковую оболочку — капсид — и окруженную тегументом. ДНК этого вируса содержит довольно много генетического материала, в котором закодировано много вирусных белков, а потому цитомегаловирус имеет весьма гибкий жизненный цикл (рис. 3), в ходе которого может переключаться с одной стратегии эксплуатации хозяина на другую (подробнее об этих стратегиях рассказано немного ниже).


Рис. 3. Упрощенная схема литического цикла цитомегаловируса в клетке. Частицы вируса проникают в клетку, оставляя часть белков своего тегумента, включая pp71, в цитоплазме. Затем ДНК вируса поступает в ядро, где с него считывается множество копий. Уже в ядре формируется капсид вируса, вокруг которого в цитоплазме клетки-хозяина собираются белки тегумента и гликопротеины мембраны. После этого новорожденные вирионы покидают клетку, готовые к новым свершениям. На врезке: схема устройства вирусной частицы ЦМВ. Источники изображений: T. Crough and R. Hanna, 2009. Immunobiology of Human Cytomegalovirus: from Bench to Bedside и T. Manandhar et al., 2019. Battle between Host Immune Cellular Responses and HCMV Immune Evasion, с изменениями
ЦМВ способен переноситься самыми разными путями, включая передачу через слюну, при переливании крови, половом контакте, а также переходить от матери к ребенку еще в утробе или при кормлении грудью (T. Crough and R. Hanna, 2009. Immunobiology of Human Cytomegalovirus: from Bench to Bedside). Поэтому неудивительно, что этим вирусом заражена большая часть человечества. ЦМВ вообще-то вирус мягкий, предпочитающий не вступать в жесткую конфронтацию со своим хозяином. Инфекция, как правило, протекает бессимптомно, реже ее первичное проявление ограничивается мышечной болью, тонзиллитом, небольшим жаром и/или легким воспалением печени. После этого вирус остается в организме человека, но надолго уходит в тень, лишь периодически напоминая о себе, пользуясь временным ослаблением иммунитета хозяина из-за других инфекций, стресса или воспаления (T. Crough and R. Hanna, 2009). Однако существуют категории граждан, для которых ЦМВ может представлять серьезную угрозу. Обычно это люди с ослабленным или еще не сформировавшимся иммунитетом, например недавно перенесшие трансплантацию органов, носители ВИЧ и новорожденные. Считается, что ЦМВ — основная причина врожденных неврологических расстройств (таких, например, как глухота), а порой цитомегаловирусная инфекция может привести и к смерти ребенка. Хотя случаи тяжелого течения инфекции довольно редки, широкое распространение вируса в человеческой популяции приводит к заметному числу жертв ЦМВ в абсолютном выражении.
Каким же образом генетически идентичные вирусные частицы могут различаться по стратегиям взаимодействия с клеткой хозяина? Как определяется, какая частица будет активной, а какая латентной? Вот здесь и выступает на сцену бет-хеджинг.
Бет-хеджинг на вирусный манер
Чтобы придумать, как обнаружить бет-хеджинг у ЦМВ, и показать, как он работает, группе американских исследователей пришлось решить последовательно несколько задач. Во-первых, им нужно было узнать, есть ли существенные различия в количестве молекул белков рp71 и pp150 в разных частицах вируса (по аналогии с семенами растений: если у какого-нибудь вида вы обнаруживаете сильную вариацию в толщине покровов, то это может навести вас на мысль, что растение использует бет-хеджинг, чтобы приноровиться к разным условиям ). Для этого использовалась флуоресцентная микроскопия сверхвысокого разрешения (см. Super-resolution microscopy): вирусы, как правило, настолько малы, что в обычный световой микроскоп их не увидишь. Я не буду здесь рассказывать о том, что такое микроскопия сверхвысокого разрешения, — это увело бы нас слишком далеко от темы сегодняшнего разговора, — зато в общих чертах изложу сущность флуоресцентного метода.


В ходе анализа выяснилось, что число молекул белка pp71 в разных клетках действительно, сильно отличалось, причем разброс был гораздо больше, чем у белка pp150 или белка, взятого в качестве контроля. Более того, оказалось, что различия между клетками по интенсивности средней флуоресценции вирусных частиц невелики, а значит, за разброс были ответственны именно различия между частицами вируса. Другими словами, исследователи исключили вероятность того, что на концентрацию белка pp71 могут заметно повлиять клетки-хозяева. Всё говорило о том, что вирус целенаправленно способствует синтезу частиц с разным количеством этого белка. Напомню, что белок pp71, как предполагалось, отвечает за активацию более агрессивной стратегии цитомегаловируса, заключающейся в активном производстве частиц вируса в ядре и цитоплазме клеток хозяина.
Оказалось, что вирусные частицы с повышенным содержанием pp71 (pp71 HI ) активно размножаются в клетках хозяина в разы чаще, чем вирионы с нормальным количеством этого белка (pp71 WT ). Вирусные частицы, богатые pp71, заражали больше клеток в культуре, чем то же количество нормальных частиц, и их требовалось меньше для достижения сходной эффективности заражения (рис. 5).


Однако и на Солнце есть пятна.
Как выяснилось, именно избыток белков pp71 мешает вирусным частицам перейти на легальное положение. Механизм происходящего, видимо, таков. Проникая внутрь ядра клетки хозяина, ДНК цитомегаловируса деликатно оставляет за дверью, то есть в цитоплазме, большую часть белков своего капсида и тегумента, в том числе и белок pp71. Тем не менее некоторое его количество все-таки проникает в ядро, и то, по какому пути пойдет развитие инфекции — литическому (пути активного размножения вируса) или латентному, — зависит именно от концентрации белка pp71 в ядре клетки. Если его много, то вероятность перехода вируса в спящее состояние невелика.


Что в итоге?
Авторы статьи провели очень интересное и детальное исследование различных репродуктивных стратегий цитомегаловируса, продемонстрировали любопытный пример бет-хеджинга у вирусов и показали, что базовые эволюционно-экологические стратегии могут сходным образом работать как в макро- так и в микромире.
Источник: Sonali Chaturvedi, Jonathan Klein, Noam Vardi, Cynthia Bolovan-Fritts, Marie Wolf, Kelvin Du, Luwanika Mlera, Meredith Calvert, Nathaniel J. Moorman, Felicia Goodrum, Bo Huang, and Leor S. Weinberger. A molecular mechanism for probabilistic bet hedging and its role in viral latency // Proc Natl Acad Sci USA. 2020. V. 117 (29). P. 17240–17248. Doi: 10.1073/pnas.1914430117.
Читайте также:

