Распространение вирусов и пути заражения животных
Обновлено: 24.04.2024
Не все знают, что большая часть биологических угроз для человека скрыта внутри животных и растений, часто являющихся переносчиками чуждых нам вирусов, бактерий, грибков и паразитов. В основном эти болезнетворные организмы распространяются только среди определённых видов, не угрожая жизни человека.
Но иногда болезни всё же разрушают барьеры между животными и людьми, переходя в категорию зоонозных инфекций. При достаточной мобильности носителей, такие ранее неизвестные заболевания быстро распространяются между людьми, при определённых условиях даже приводя к пандемии – точь-в-точь, как это
с китайским коронавирусом.
Но почему такие вспышки случаются не так часто, и по какому принципу происходит переход инфекций в зоонозный вид?
Всё дело в повторении, а точнее – в продолжительном вторжении в естественную среду обитания животных и растений.
Эрозия среды обитания является одной из главных причин того, что вирусы начали разрушать стены между людьми и животными. Так, например, вирус Nipah, обнаруженный в Малайзии и Бангладеш, распространился от плодоядных летучих мышей к свиньям и людям, когда местные фермеры посадили фруктовые сады рядом со свинофермами. Вирус, вызывающий COVID-19, скорее всего, произошёл из схожих условий. Генетические исследования показали, что вирус напоминает уже известную инфекцию, распространявшуюся среди летучих мышей. По мнению специалистов, в звене передачи также присутствовал как минимум ещё один вид змей или ящеров, но эта история пока что остаётся под вопросом.
Но как тогда происходит переход?
Для того, чтобы болезнь совершила скачок, человек должен войти в прямой контакт с жизнеспособным вирусом. Поедание мяса кажется наиболее вероятным способом подхватить инфекцию, но специалисты относятся к этому скептически.
Зато весь процесс, происходящий перед приготовлением – а именно охота и убийство, сдирание шкур и разделка мяса – часто приводит к плачевным результатам. И если мы можем избежать контакта с крупными животными, то отдельной головной болью медиков останется то великое множество болезней, переносимых комарами, блохами, другими насекомыми и клещами. Все они часто входят в контакт как между собой, так и с людьми и животными, повышая вероятность передачи зоонозных инфекций.
Для вируса, вызывающего COVID-19, уязвимым рецептором оказался ACE2.
Знание того, какой рецептор уязвим для вируса, позволяет ученым узнать, какие типы клеток и какие виды животных вирус может заразить. ACE2 разделяют кошки, хорьки и свиньи, что заставляет ученых полагать, что эти виды также восприимчивы для инфекции. Внутри клетки существует еще больше барьеров, препятствующих заражению вирусом. Когда Колин Пэрриш, профессор вирусологии в колледже ветеринарной медицины Корнельского университета, проанализировал результаты научных исследований по вирусам ВИЧ и гриппа, он обнаружил, что они преодолели ряд из пяти или шести барьеров, чтобы запустить эпидемию в новом хозяине. По его мнению, новый коронавирус преодолел примерно такое же количество препятствий.
Даже внутри человеческой клетки вирус находится лишь на полпути к эпидемии или вспышке болезни. Выход из клетки и заражение другого хозяина представляет для вируса новый набор проблем.
Несмотря на то, как много ученые знают о том, как болезни перескакивают от животных к людям, разнообразие и сложность жизни на Земле затрудняет выявление развивающихся пандемий.
К сожалению, все эти познания не увеличивают наш шанс на успешную борьбу с уже появившимися инфекциями. Но новая эпидемия COVID-19 в очередной раз указывает нам на опасности, таящиеся за вторжением в естественную природную среду.
Несмотря на то, что многие из видов зоонозных инфекций распространяются практически без участия человека, минимизация разрушения окружающих нас экосистем в перспективе останется одним из главных залогов сокращения риска появления новых заболеваний – по-крайней мере, так считают специалисты. А нам остаётся лишь ждать спада текущей пандемии, а затем приложить все усилия к тому, чтобы она не повторилась.
Главная задача биологии — это развитие представлений у человека о живых организмах, о многообразии видов, обо всех закономерностях развития живых существ, а также об их взаимодействии с окружающей природой. Предмет основы безопасности жизнедеятельности (ОБЖ) позволяет получить знания и умения, которые помогут сохранить жизнь и здоровье в опасных ситуациях. Эти ситуации всегда возникают неожиданно, но, тем не менее, большинство из них предсказуемы и к ним можно подготовиться заранее. ОБЖ учит нас предвидеть возможные опасности и минимизировать потери от той или иной ситуации. Сегодня мы сталкиваемся с новым видом вирусной опасности COVID-19,о котором поговорим с точки зрения биологии и ОБЖ.
Что такое вирус?
Вирус — это неклеточный инфекционный агент. Сегодня нам известно около 6 тысяч различных вирусов, но их существует несколько миллионов. Вирусы не похожи друг на друга и могут иметь как форму сферы, спирали, так и форму сложного асимметричного сплетения. Размеры вирусов варьируются от 20 нм до 300 нм.
Как устроен вирус?
В центре агента находится генетический материал РНК или ДНК, вокруг которого располагается белковая структура — капсид.
Капсид служит для защиты вируса и помогает при захвате клетки. Некоторые вирусы дополнительно покрыты липидной оболочкой, т.е. жировой структурой, которая защищает их от изменений окружающей среды.
Вирусолог Дэвид Балтимор объединил все вирусы в 8 групп, из которых некоторые группы вирусов содержат 1-2 цепочки ДНК. Другие же содержат 1 цепочку РНК, которая может удваиваться или достраивать на своей матрице ДНК. При этом каждая группа вирусов производит себя в различных органеллах зараженной клетки.
Вирусы имеют определенный диапазон хозяев, т.е. он может быть опасен для одних видов и абсолютно безвреден для других. Например, оспой болеет только человек, а чумкой только некоторые виды плотоядных. Вирус не способен выжить сам по себе, поэтому активируется только в хозяйской клетке, используя ее ресурсы и питательные вещества. Цель вируса — создание множества копий себя, чтобы инфицировать другие клетки!
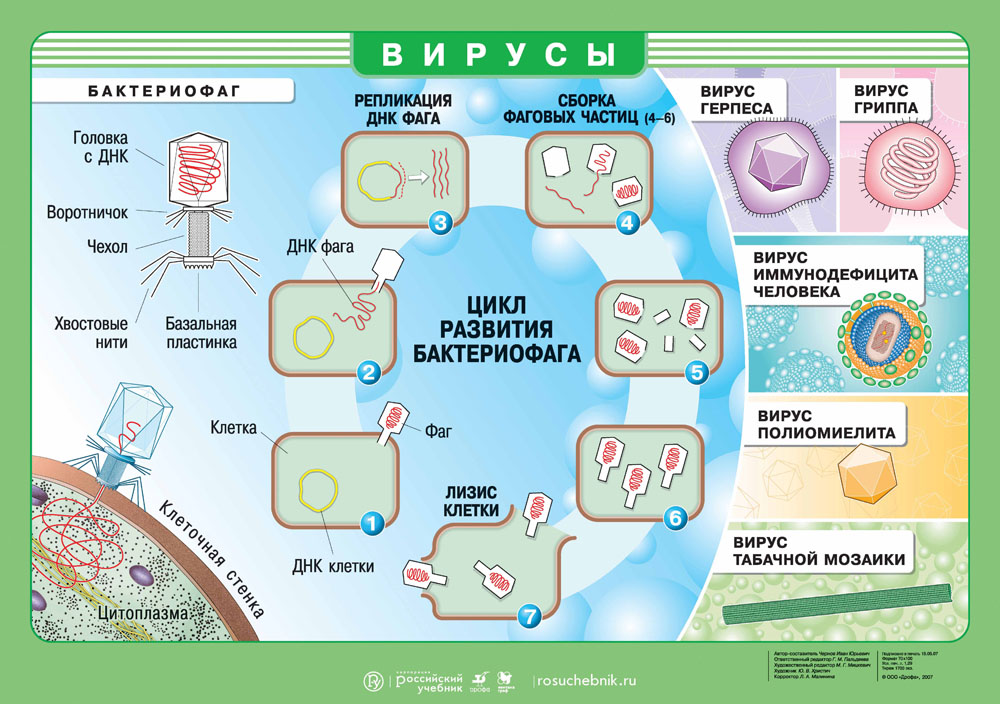
Как вирус попадает в организм?
- через физические повреждения (например, порезы на коже)
- путём направленного впрыскивания (к примеру, укус комара)
- направленного поражения отдельной поверхности (например, при вдыхании вируса через трахею)
- к эпителию слизистых оболочек (это например вирус гриппа)
- к нервной ткани (вирус простого герпеса)
- к иммунным клеткам (вирус иммунодефицита человека)

Геном вируса встраивается в одну из органелл или цитоплазму и превращает клетку в настоящий вирусный завод. Естественные процессы в клетке нарушаются, и она начинает заниматься производством и сбором белка вируса. Этот процесс называется репликацией. И его основная цель — это захват территории. Во время репликации генетический материал вируса смешивается с генами клетки хозяина — это приводит к активной мутации самого вируса, а также повышает его выживаемость. Когда процесс репликации налажен, вирусная частица отпочковывается и заражает уже новые клетки, в то время как инфицированная ранее клетка продолжает производство.
Выход вируса
Вирус создал множество собственных копий, клетка оказывается изнуренной из-за использования ее ресурсов. Больше вирусу клетка не нужна, поэтому клетка часто погибает и новорожденным вирусам приходится искать нового хозяина. Это и есть заключительная стадию жизненного цикла вируса.
Скорость распространения вирусной инфекции
Размножение вирусов протекает с исключительно высокой скоростью: при попадании в верхние дыхательные пути одной вирусной частицы уже через 8 часов количество инфекционного потомства достигает 10³, а концу первых суток − 10²³.
Вирусная латентность
Как вирус распространяется?
- воздушно-капельный (кашель, чихание)
- с кожи на кожу (при прикосновениях и рукопожатиях)
- с кожи на продукты (при прикосновениях к пище грязными руками вирусы могут попасть в пищеварительную и дыхательную системы)
- через жидкие среды организма (кровь, слюну и другие)
Почему с вирусами так тяжело бороться?
Сегодня людям уже удалось победить некоторые вирусы, а некоторые взять под жесткий контроль. Например, Оспа (она же черная оспа). Болезнь вызывается вирусом натуральной оспы, передается от человека к человеку воздушно-капельным путем. Больные покрываются сыпью, переходящей в язвы, как на коже, так и на слизистых внутренних органов. Смертность, в зависимости от штамма вируса, составляет от 10 до 40 (иногда даже 70%), На сегодняшний день вирус полностью истреблен человечеством.
Кроме того, взяты под контроль такие заболевания, как бешенство, корь и полиомиелит. Но помимо этих вирусов существует масса других, которые требуют разработок или открытия новых вакцин.
Коронавирус
Виновником эпидемии, распространяющейся сегодня по миру, стал коронавирус, вирусная частица в 0,1 микрона. Свое название он получил благодаря наростам на своей структуре, своеобразным шипам. Внутри вируса спрятан яд, с помощью которого он подчиняет себе зараженный организм. Этот вирус воздействует не только на человека, но и на птиц, свиней, собак и летучих мышей. В настоящий момент выделяют от 30 до 39 разновидностей коронавирусной инфекции. Но для человека патогенно всего 6. И как любой другой вирус COVID-19 мутирует.

К наиболее распространенным симптомам COVID-19 относятся повышение температуры тела, сухой кашель и утомляемость. К более редким симптомам относятся боли в суставах и мышцах, заложенность носа, головная боль, конъюнктивит, боль в горле, диарея, потеря вкусовых ощущений или обоняния, сыпь и изменение цвета кожи на пальцах рук и ног. Как правило, эти симптомы развиваются постепенно и носят слабо выраженный характер. У некоторых инфицированных лиц болезнь сопровождается очень легкими симптомами.
Сколько же может жить этот вирус вне организма? Все зависит от типа вируса и от той поверхности, на которую вирусы попали. В качестве примера было рассмотрено 3 вируса, по которым велись исследования. Изучали время, на которое может задерживаться вирус на различных поверхностях. Данные приведены в таблице.

Поскольку пока не изобретено вакцины от COVID-19, в целях защиты от инфекции самым важным для нас является соблюдение гигиены.
Гигиена — раздел медицины, изучающий влияние жизни и труда на здоровье человека и разрабатывающая меры (санитарные нормы и правила), направленные на предупреждение заболеваний, обеспечение оптимальных условий существования, укрепление здоровья и продление жизни.
Сегодня следует соблюдать определенные правила гигиены:
- Соблюдение режима труда и отдыха, не допускающего развития утомления и переутомления.
- Выполнение условий, обеспечивающих здоровый и полноценный сон (свежий воздух, отсутствие шума, удобная постель, оптимальная продолжительность).
- Правильное здоровое питание в соответствии с потребностями организма.
- Комфортный микроклимат в жилище (температура, влажность и подвижность воздуха, естественная и искусственная освещенность помещений).
- Содержание в чистоте тела и тщательный уход за зубами.
- Спокойное и корректное поведение в конфликтных ситуациях.

Распространение вирусов животных. Вертикальная передача, горизонтальная (контактная, векторная с помощью переносчиков, капельная, через наружные покровы, трансмиссивная, парентеральная). Особенности эпидемиологии вирусных инфекций. Распространение вирусов растений. Вертикальная передача, трансплантационная (при прививках), контактная, векторная (с помощью переносчиков).
Пути распространения вирусов в биосфере
Экологическая ниша вирусов — это многокомпонентная система взаимосвязанных элементов, включающая клетку, организм, популяцию хозяина, переносчиков, другие вирусы и внешнюю среду. Для сохранения вируса как биологического вида необходима его последовательная передача от хозяина к хозяину. Передача происходит по горизонтальному и вертикальному направлениям, что имеет место не только в популяциях человека и животных, но и среди бактерий, насекомых, растений, грибов.
Горизонтальная передача — рассеивание возбудителей среди восприимчивых хозяев с использованием различных механизмов и путей, во многом определяемых средой обитания и особенностями жизнедеятельности организма-хозяина.
Вертикальная передача — это передача возбудителя от родителей потомству, которая также может осуществляться различными путями, и предполагает сохранение вируса в ряду поколений.
Бактериофаги в природных условиях встречаются в тех местах, где есть чувствительные бактерии (в воде, почве, выделениях человека и животных), которые инфицируются вирусом при случайных контактах и распространяются водными потоками или путями, используемыми хозяином. Применение бактериофагов в качестве лечебных препаратов значительно увеличило интенсивность циркуляции вирусов бактерий в биосфере. Возможно распространение бактериофагов воздушным путем, что создает определенные трудности при работе с бактериальными культурами в научно-исследовательских лабораториях.
Вирусы растений могут распространяться в процессе размножения хозяев (с пыльцой, семенами), где важную роль играют природные факторы (дождь, ветер, птицы). Человек распространяет вирусы растений при использовании зараженного посадочного материала (вегетативные побеги, семена), а также при использовании зараженной земли. Однако основными переносчиками фитопатогенных вирусов являются их промежуточные хозяева (насекомые, клещики, нематоды, фитопатогенные грибы).
Вирусы насекомых инфицируют хозяина в процессе его питания и размножения. Различают трасспермальную, трансовариальную и трансстадийную (в процессе метаморфоза) передачи вируса. Распространяются вирусы в процессе миграций насекомых.
Распространение вирусов позвоночных осуществляется с использованием механизмов, которые реализуются различными путями, и часто включают внешнюю среду и промежуточных хозяев вируса. Важную роль в распространении вирусов играют миграционные процессы, наблюдаемые среди людей и животных.
Распространение вирусов в человеческой популяции имеет свои особенности. В соответствии с четырьмя основными типами локализации возбудителя в организме (дыхательные пути, желудочно-кишечный тракт, кровь, наружные покровы) выделены несколько механизмов передачи вирусов.
Трансмиссивный механизм — передача с помощью биологических переносчиков. При любом варианте такой передачи вирус черпается переносчиком из внутренних сред донора и внедряется во внутреннюю среду реципиента.
Парентеральный механизм — передача вирусов через кровь. Вирусы, циркулирующие в крови, могут передаваться в процессе переливаний крови, при использовании загрязненных шприцев и других медицинских инструментов (искусственный путь), в процессе сексуальных контактов (половой путь) и другими путями.
Алиментарный (энтеральный) механизм — вирус проникает через слизистые оболочки органов пищеварения. Разновидностью алиментарного механизма является фекально-оральный механизм передачи вируса.
Аэрогенный механизм — входными воротами инфекции являются слизистые органов дыхания. Реализуется воздушно-капельным или пылевым путем.

Контактный механизм — реализуется через кожные покровы. Такой механизм передачи могут использовать очень немногие вирусы. Так, например, вирус бешенства может проникать в организм животного и человека при ослюнении кожных покровов. Слюна собак содержит гиалуронидазу, которая облегчает проникновение вируса в кровь через кожу.
Вертикальный механизм — передача вирусов от матери плоду во время вынашивания и родов. Возбудитель может передаваться через плаценту, через околоплодные воды и оболочки, при прохождении плода через родовые пути матери.
Вирус бешенства покрыт оболочкой, содержит одну спираль РНК, принадлежит к семейству рабдовирусов. Нейровирулентность вируса бешенства обусловлена связыванием гликопротеидов вируса с ацетилхолиновыми рецепторами.
Эпидемиология
Клинические проявления
Диагностика
Специфический диагноз бешенства определяется выделением вируса в культуре из слюны или ткани головного мозга путем заражения мышей; обнаружением вируса бешенства в инфицированных тканях (контактные мазки роговицы, биопсия кожи и головного мозга) реакцией флюоресценции антител и по 4кратному росту титра нейтрализующих антител. Если больные получили постконтактную профилактику бешенства, титр сывороточных антител интерпретировать сложнее, но в ликворе антитела отсутствуют или есть лишь в низком титре (< 1 : 64).
Лечение и профилактика
Принятие решения о проведении постконтактной профилактики бешенства определяется комплексом факторов. Если человек контактировал со слюной или иной жидкостью организма животного, больного бешенством, животное следует поймать, умертвить, а его головной мозг — обработать флюоресцирующими антителами. При положительном ответе контактному человеку вводят иммуноглобулин и вакцину. Если здоровое домашнее животное укусило человека, оно должно быть изолировано и находиться под наблюдением в течение 10 дней. При появлении признаков заболевания или отклонений в поведении, исследуют мозг животного. Если животное, укусившее человека, не заболело, вероятно, оно не является переносчиком бешенства. Когда животное недоступно для обследования, но может быть переносчиком бешенства (летучая мышь, енот, скунс, лиса), контактному проводят курс лечения. Постконтактная профилактика включает локальную обработку раны (тщательное промывание водой с мылом, столбнячный анатоксин, антибиотики), пассивную иммунизацию (человеческий антирабический иммуноглобулин, 20 ЕД/кг, 50% Дозы вводится внутримышечно в дни 0й, 3й, 7й, 14й и 28й после контакта). Может применяться лошадиная антисыворотка для пассивной иммунизации в дозе 4U ЕД/кг, но при сывороточной болезни больше подходит человеческая антисывоРотка. Предконтактную профилактику проводят лицам с высоким риском заражения (ветеринары, спелеологи, лаборанты и владельцы животных). Три дозы вакцины вводят внутримышечно по 1 мл или 0,1 мл внутрикожно в 0й, 7й и 28й дни.
Эффективность вакцинирования следует проверить серологически после ее проведения, а затем каждые 2–6 лет в зависимости от риска инфицирования. Если титрнтител падает ниже 1: 5, вводят живую вакцину 1 мл внутримышечно или 0,1 мл Утрикожно. Постконтактная профилактика для тех, кто получал предконтактную профилактику, состоит из 2 доз вакцины 1 мл внутримышечно в 0й и 3й дни.
Таблица 691 Основные клинические синдромы при арбовирусных инфекциях, передающихся кровососущими насекомыми
| Синдром | Вирус |
| Энцефалит — асептический менингит | Восточный энцефалит лошадей, энцефалит СентЛуис, западный асептический энцефалит лошадей, калифорнийский энцефалит, венесуэльский энцефалит, японский энцефалит, поуссан, лихорадка Рифт-Валли |
| Артралгии, артриты Геморрагическая лихорадка | Чикунгунья, Росс-Ривер, лихорадка Западного Нила Денге, желтая лихорадка, омская геморрагическая лихорадка, конгокрымская геморрагическая лихорадка, хантаан |
| Недомогание, миалгии | Флеботомная лихорадка, колорадская клещевая лихорадка |
Эпидемиология
Поскольку арбовирусная инфекция, вызывающая энцефалит, передается кровососущими насекомыми, инфекционные заболевания возникают в разгаре сезона москитов, с поздней весны до ранней осени. В табл. 692 представлена характеристика 4 основных арбовирусов, вызывающих энцефалит в США.
Клинические проявления
В разных возрастных группах симптоматика арбовирусных энцефалитов существенно различается. У детей до 1 года единственным постоянным симптомом является внезапное начало лихорадки, часто с судорогами, локальными или генерализованными. Выбухание родничка, ригидность конечностей и патологические рефлексы достаточно типичны. У детей 5–14 лет головная боль, лихорадка, сонливость часто опережают на 2–3 дня рвоту, тошноту, мышечные боли, фотофобию и, несколько реже, судороги. У детей обычно отмечается картина серьезной болезни, заторможенность, часто ригидность затылочных мышц и тремор рук при произвольных движениях. У взрослых первыми признаками являются: острое начало болезни, тошнота, рвота и выраженная головная боль (обычно в лобных отделах), затем в течений 24 ч следует нарушение сознания. Наиболее значимые неврологические симптомы нарушения сознания от незначительных отклонений, выявляемых при обследовании, до комы. Другие признаки: тремор (особенно часто у лиц старше 40 лет), патология черепных нервов и рефлекторные нарушения (усилены ладонноподбородочный рефлекс, сосательный и другие оральные рефлексы). Лихорадка и неврологическая симптоматика сохраняются от нескольких дней до месяцев, чаще 4–14 дней. Вслед за снижением лихорадки на протяжении нескольких дней следует улучшение состояния, несмотря на возникновение необратимых анатомических изменений.
| Этиология | Географ. преобладание в США | Город, село | Возраст | Пол (лет) | Специф. признаки | Летальность (%) | Ост. явл-я |
| Калифорнийский энцефалит | Средний Запад | Сельская местность | 5–10 | М | Судороги | 2 | Судороги (у 25 % больных в острой фазе), поведенческие проблемы у 15 % больных |
| Восточный энцефалит лошадей | Восточное побережье | Обе зоны | < 5 | М | В ликворе может быть > 1000 лейкоцитов в 1 мкл | 50 | У детей до 10 лет эмоциональная лабильность, отставание в развитии, судороги |
| Энцефалит СанЛуи | Восток и Средний Запад | Обе зоны | >3—5 | М | Дизурия | 2–12 | Атаксия, расстройства речи у 5 % больных |
| Западный энцефалит лошадей | Везде | Обе зоны | >5 | М | Нет | 3 | У детей до 3 мес. нарушение поведения, судороги |
Диагностика
В ликворе обнаруживается плеоцитоз, обычно несколько сотен клеток в 1 мкл, иногда и более 1000 клеток/1 мкл, первоначально с нейтрофильным сдвигом, сменяющимся через несколько дней преобладанием лимфоцитов. Содержание белка в ликворе обычно несколько повышено и может возрасти еще больше; уровень глюкозы не изменен. Специфический диагноз основан на выделении вируса или на повышении титра сывороточных антител при сравнении в острой фазе и на этапе выздоровления.
Лечение
Лихорадка Денге
Вирусы Денге относят к группе флавовирусов четырех серотипов.
Эпидемиология
Клинические проявления
Вирус Денге часто вызывает инаппарантные инфекции. По начальным симптомам они разделяются на три группы: классическая Денге, ГЛД и умеренно выраженная атипическая форма.
Классическая лихорадка Денге. После инкубационного периода в 5–8 дней отмечается короткий продром с умеренно выраженным конъюнктивитом, насморком, за ним через несколько часов следует острое начало с сильнейшей головной болью, ретроорбитальной болью, болями в спине (особенно в поясничном отделе), нижних конечностях и суставах. Частые симптомы: боли в глазных яблоках, анорексия и слабость, кашель нехарактерен. Кожные сыпи, различные по характеру, выраженности и распространению, отмечаются весьма часто, как и лимфаденопатия. Лихорадка может быть двухфазной. Она обычно длится 5–6 дня и критически прерывается.
Атипичная лихорадка Денге. Ее симптомы включают лихорадку, анорексию, головную боль, миалгию. Возможна мимолетная сыпь, лимфаденопатии нет. Симптоматика обычно сохраняется менее 72 ч.
ГЛД. Заболевание начинается внезапно со слабовыраженной фазы длительностью 2–4 дня, состоящей из лихорадки, кашля, фарингита, головной боли, анорексии, тошноты, рвоты и боли в животе, которая может быть довольно сильной. В отличие от классической лихорадки Денге миалгия, артралгия и боли в костях нехарактерны. Геморрагические симптомы включают положительный тест со жгутом, петехии, пурпуру, экхимозы, носовые кровотечения, кровоточивость десен, рвоту с кровью, мелену, увеличение печени, тромбоцитопению, гемоконцентрацию и увеличение гематокрита на 20% и больше. Диагноз шокового синдрома Денге (ШСД) ставят при появлении частого, слабого пульса, снижении пульсового давления до 20 мм рт. ст. и ниже или понижении АД с появлением холодной, влажной кожи и тревоги.
Диагностика
Первичное выделение вируса в культуре можно осуществить, инокулировав кровь больного в первые 3–5 дней заболевания в тело москита или в культуру клеток его тканей. Серологическую диагностику проводят на парных сыворотках (РТГА и РСК); при первичной инфекции образуются антитела класса IgM.
Лечение
Поддерживающее. Глюкокортикоиды неэффективны. Применение гепарина при ДВС противопоказано.
Ареновирусы
Ареновирусы представляют собой группу РНКвирусов, паразитирующих на грызунах. При внутриутробном заражении животных или в периоде новорожденное наличие вирусов в организме не сопровождается клиническими проявлениями, не вызывает иммунной реакции и может быть передано дальше по цепочке.
Лимфоцитарный хориоменингит
Эпидемиология
Мыши являются первичным хозяином при лимфоцитарном хориоменингите (ЛXM), который распространен повсеместно. Человек инфицируется после контакта с инфицированным грызуном; пути передачи, скорее всего, респираторный и контакт с инфицированными экскрементами животных.
Клинические проявления
Чаще всего клиника напоминает гриштоподобный синдром. У некоторых больных болезнь протекает двухфазно с картиной вторичного асептического менингита или энцефалита. Типична лихорадка. Слабость, миалгия (особенно в поясничном отделе), ретроорбитальная головная боль, фотофобия, анорексия, тошнота, головокружение отмечены более чем у 50% больных. При физикальном обследовании обнаруживают кожную сыпь, фарингит без экссудации, умеренно выраженную шейную или затылочную лимфаденопатию, аллопецию и симптомы менингизма. Боли в яичках или картина явного орхита, обычно одностороннего, и боли в области околоушной слюнной железы дают основание для дифференциальной диагностики заболевания с инфекционным паротитом. Больные с асептическим менингитом обычно выздоравливают без осложнений. У 25–30% больных с энцефалитом остаются неврологические осложнения.
Диагностика
В течение 1й недели болезни отмечаются лейкопения и тромбоцитопения. У больных с признаками менингита в ликворе обычно обнаруживают несколько сотен клеток в 1 мкл, преимущественно лимфоциты. У половины больных в ликворе находили более 100 клеток в 1 мкл. Уровень белка в ликворе несколько повышен; в отличие от других вирусных менингитов у 2–7% больных ЛХМ уровень глюкозы остается низким. Вирус ЛХМ можно выделить из ликвора или из крови при соблюдении персоналом мер самозащиты 3го уровня. Диагностический путь — РИФ инфицированных клеток, фиксированных на срезах для микроскопирования. Применяют и серологические методы; антитела появляются к 7—10му дню. Нейтрализующие антитела появляются на 68й неделе, титр их медленно растет и остается высоким на протяжении лет.
Лечение
Специфического лечения не существует.
Лихорадка Ласса
Эпидемиология
Лихорадка Ласса — высококонтагиозное вирусное заболевание, описанное после вспышки, возникшей в 1969 г. в г. Ласса (северная Нигерия). Вирус переносится разновидностью крыс, обитающих в Африке. Распространение инфекции происходит при заражении запасов пищи мочой грызунов, описана передача и от человека к человеку.
Клинические проявления
Инкубационный период 7–18 сут. Начало заболевания постепенное с лихорадкой, ознобом, головной болью и миалгией. 4–9 дней спустя появляются анорексия, тошнота, рвота, головная боль, непродуктивный кашель (2/3 пациентов) и фарингит. При физикальном обследовании — гиперемия лица и передневерхнего отдела шеи, беловатый экссудат на небных дужках, изъязвление слизистой оболочки полости рта (у 50%) и генерализованная безболезненная лимфаденопатия (у 50%). При благоприятном течении болезни лихорадка прекращается на 2й неделе болезни. Симптоматика шока, помрачение сознания, хрипы в легких, плеврит, возбуждение, значительные судороги — признаки неблагоприятного прогноза. Летальность колеблется от 8 до 52%.
Диагностика
Основана на 4кратном повышении титра антител в сыворотке крови при в острой фазе и в период выздоровления. Заболевание маловероятно, если IgM отсутствует в сыворотке крови к 14му дню болезни.
Лечение
Симптоматическое. Были попытки применения рибавирина внутривенно. Для предупреждения распространения нозокомиальной инфекции больных следует изолировать.

Обзор
Автор
Редакторы
Обратите внимание!
Спонсоры конкурса: Лаборатория биотехнологических исследований 3D Bioprinting Solutions и Студия научной графики, анимации и моделирования Visual Science.
Эволюция и происхождение вирусов
В 2007 году сотрудники биологического факультета МГУ Л. Нефедова и А. Ким описали, как мог появиться один из видов вирусов — ретровирусы. Они провели сравнительный анализ геномов дрозофилы D. melanogaster и ее эндосимбионта (микроорганизма, живущего внутри дрозофилы) — бактерии Wolbachia pipientis. Полученные данные показали, что эндогенные ретровирусы группы gypsy могли произойти от мобильных элементов генома — ретротранспозонов. Причиной этому стало появление у ретротранспозонов одного нового гена — env, — который и превратил их в вирусы. Этот ген позволяет вирусам передаваться горизонтально, от клетки к клетке и от носителя к носителю, чего ретротранспозоны делать не могли. Именно так, как показал анализ, ретровирус gypsy передался из генома дрозофилы ее симбионту — вольбахии [7]. Это открытие упомянуто здесь не случайно. Оно нам понадобится для того, чтобы понять, чем вызваны трудности борьбы с вирусами.
Из давних письменных источников, оставленных историком Фукидидом и знахарем Галеном, нам известно о первых вирусных эпидемиях, возникших в Древней Греции в 430 году до н.э. и в Риме в 166 году. Часть вирусологов предполагает, что в Риме могла произойти первая зафиксированная в источниках эпидемия оспы. Тогда от неизвестного смертоносного вируса по всей Римской империи погибло несколько миллионов человек [8]. И с того времени европейский континент уже регулярно подвергался опустошающим нашествиям всевозможных эпидемий — в первую очередь, чумы, холеры и натуральной оспы. Эпидемии внезапно приходили одна за другой вместе с перемещавшимися на дальние расстояния людьми и опустошали целые города. И так же внезапно прекращались, ничем не проявляя себя сотни лет.
Вирус натуральной оспы стал первым инфекционным носителем, который представлял действительную угрозу для человечества и от которого погибало большое количество людей. Свирепствовавшая в средние века оспа буквально выкашивала целые города, оставляя после себя огромные кладбища погибших. В 2007 году в журнале Национальной академии наук США (PNAS) вышла работа группы американских ученых — И. Дэймона и его коллег, — которым на основе геномного анализа удалось установить предположительное время возникновения вируса натуральной оспы: более 16 тысяч лет назад. Интересно, что в этой же статье ученые недоумевают по поводу своего открытия: как так случилось, что, несмотря на древний возраст вируса, эпидемии оспы не упоминаются в Библии, а также в книгах древних римлян и греков [9]?
Строение вирусов и иммунный ответ организма

Рисунок 1. Первооткрыватель вирусов Д.И. Ивановский (1864–1920) (слева) и английский врач Эдвард Дженнер (справа).

Почти все известные науке вирусы имеют свою специфическую мишень в живом организме — определенный рецептор на поверхности клетки, к которому и прикрепляется вирус. Этот вирусный механизм и предопределяет, какие именно клетки пострадают от инфекции. К примеру, вирус полиомиелита может прикрепляться лишь к нейронам и потому поражает именно их, в то время как вирусы гепатита поражают только клетки печени. Некоторые вирусы — например, вирус гриппа А-типа и риновирус — прикрепляются к рецепторам гликофорин А и ICAM-1, которые характерны для нескольких видов клеток. Вирус иммунодефицита избирает в качестве мишеней целый ряд клеток: в первую очередь, клетки иммунной системы (Т-хелперы, макрофаги), а также эозинофилы, тимоциты, дендритные клетки, астроциты и другие, несущие на своей мембране специфический рецептор СD-4 и CXCR4-корецептор [13–15].

Одновременно с этим в организме реализуется еще один, молекулярный, защитный механизм: пораженные вирусом клетки начинают производить специальные белки — интерфероны, — о которых многие слышали в связи с гриппозной инфекцией. Существует три основных вида интерферонов. Синтез интерферона-альфа (ИФ-α) стимулируют лейкоциты. Он участвует в борьбе с вирусами и обладает противоопухолевым действием. Интерферон-бета (ИФ-β) производят клетки соединительной ткани, фибробласты. Он обладает таким же действием, как и ИФ-α, только с уклоном в противоопухолевый эффект. Интерферон-гамма (ИФ-γ) синтезируют Т-клетки (Т-хелперы и (СD8+) Т-лимфоциты), что придает ему свойства иммуномодулятора, усиливающего или ослабляющего иммунитет. Как именно интерфероны борются с вирусами? Они могут, в частности, блокировать работу чужеродных нуклеиновых кислот, не давая вирусу возможности реплицироваться (размножаться).

Причины поражений в борьбе с ВИЧ
Тем не менее нельзя сказать, что ничего не делается в борьбе с ВИЧ и нет никаких подвижек в этом вопросе. Сегодня уже определены перспективные направления в исследованиях, главные из которых: использование антисмысловых молекул (антисмысловых РНК), РНК-интерференция, аптамерная и химерная технологии [12]. Но пока эти антивирусные методы — дело научных институтов, а не широкой клинической практики*. И потому более миллиона человек, по официальным данным ВОЗ, погибают ежегодно от причин, связанных с ВИЧ и СПИДом.

Подобный вирусный механизм характерен не только для ВИЧ. Он описан и при инфицировании некоторыми другими опасными вирусами: такими, как вирусы Денге и Эбола. Но при ВИЧ антителозависимое усиление инфекции сопровождается еще несколькими факторами, делая его опасным и почти неуязвимым. Так, в 1991 году американские клеточные биологи из Мэриленда (Дж. Гудсмит с коллегами), изучая иммунный ответ на ВИЧ-вакцину, обнаружили так называемый феномен антигенного импринтинга [23]. Он был описан еще в далеком 1953 году при изучении вируса гриппа. Оказалось, что иммунная система запоминает самый первый вариант вируса ВИЧ и вырабатывает к нему специфические антитела. Когда вирус видоизменяется в результате точечных мутаций, а это происходит часто и быстро, иммунная система почему-то не реагирует на эти изменения, продолжая производить антитела к самому первому варианту вируса. Именно этот феномен, как считает ряд ученых, стоит препятствием перед созданием эффективной вакцины против ВИЧ.

Открытие биологов из МГУ — Нефёдовой и Кима, — о котором упоминалось в самом начале, также говорит в пользу этой, эволюционной, версии.

Сегодня не только ВИЧ представляет опасность для человечества, хотя он, конечно, самый главный наш вирусный враг. Так сложилось, что СМИ уделяют внимание, в основном, молниеносным инфекциям, вроде атипичной пневмонии или МЕRS, которыми быстро заражается сравнительно большое количество людей (и немало гибнет). Из-за этого в тени остаются медленно текущие инфекции, которые сегодня гораздо опаснее и коварнее коронавирусов* и даже вируса Эбола. К примеру, мало кто знает о мировой эпидемии гепатита С, вирус которого был открыт в 1989 году**. А ведь по всему миру сейчас насчитывается 150 млн человек — носителей вируса гепатита С! И, по данным ВОЗ, каждый год от этой инфекции умирает 350-500 тысяч человек [33]. Для сравнения — от лихорадки Эбола в 2014-2015 гг. (на состояние по июнь 2015 г.) погибли 11 184 человека [34].
* — Коронавирусы — РНК-содержащие вирусы, поверхность которых покрыта булавовидными отростками, придающими им форму короны. Коронавирусы поражают альвеолярный эпителий (выстилку легочных альвеол), повышая проницаемость клеток, что приводит к нарушению водно-электролитного баланса и развитию пневмонии.

Рисунок 8. Электронная микрофотография воссозданного вируса H1N1, вызвавшего эпидемию в 1918 г. Рисунок с сайта phil.cdc.gov.
Почему же вдруг сложилась такая ситуация, что буквально каждый год появляются новые, всё более опасные формы вирусов? По мнению ученых, главные причины — это сомкнутость популяции, когда происходит тесный контакт людей при их большом количестве, и снижение иммунитета вследствие загрязнения среды обитания и стрессов. Научный и технический прогресс создал такие возможности и средства передвижения, что носитель опасной инфекции уже через несколько суток может добраться с одного континента на другой, преодолев тысячи километров.
Читайте также:

