Рынок препаратов от гриппа
Обновлено: 24.04.2024
Несмотря на активное обсуждение пандемии COVID-19, из нашей действительности никуда не уходили сезонные инфекции. Об эффективности вакцин, новых методах экспресс-диагностики и актуальных разработках в терапии гриппа рассказывает д.м.н. Д.А. Лиознов
Пандемия коронавирусной инфекции своим появлением на время затмила все другие медицинские темы. Между тем, из нашей действительности никуда не уходили сезонные инфекции, в частности, вирус гриппа.
О гриппе в целом, а также о проблемах, возникших на фоне пандемии COVID-19, мы поговорили с доктором медицинских наук Лиозновым Дмитрием Анатольевичем, и.о. директора НИИ гриппа имени А.А. Смородинцева.
Научно-исследовательский институт гриппа был создан в 1967 году как головное научное учреждение СССР по проблеме гриппа и гриппоподобных заболеваний для проведения исследований в области вирусологии, иммунологии, эпидемиологии гриппа и других острых вирусных инфекций, а также разработки средств их профилактики и лечения. За время существования Института его сотрудниками внесен существенный вклад в решение фундаментальных и прикладных задач в области эволюционной изменчивости вирусов гриппа, противовирусного иммунитета; в создание средств диагностики вирусных инфекций, изучение молекулярных основ аттенуации вирусов и получение первых реассортантных вакцин. В клинике института было обосновано применение новых этиотропных и патогенетических подходов к терапии тяжелых и осложненных форм гриппа и ОРЗ, а также новые лечебные и профилактические препараты.
Целевые показатели охвата вакцинации растут с каждым годом. В 2020 году была поставлена непростая задача привить не менее 60% населения. Сложность этой задачи отчасти обусловлена наличием людей, которые относятся к вакцинации с некоторым сомнением, избирательностью или с принципиальным отрицанием. В этом же году в обществе действительно произошла смена настроений, и значительная часть населения теперь рассматривает вакцинацию против сезонного гриппа как необходимое явление.
В каком-то смысле COVID-19 сослужил хорошую службу для вакцинации?
Да, люди стали больше задумываться об инфекциях и рисках, которые они несут. На информационной волне, касающейся и коронавирусной инфекции, и гриппа, многие скептики пересматривают свое отношение по этому вопросу и все-таки приходят на вакцинацию. Мы видим значительный интерес со стороны пожилых людей, в особенности к вакцинам против гриппа и пневмококковой инфекции. Также стоит отметить удобство процедуры – вакцинация проходит в один день.
Существуют группы людей, отрицающие существование какой-либо инфекции. Например, печально известные ВИЧ-диссиденты. Сейчас нередко можно встретить людей, отрицающих наличие коронавирусной инфекции. Бывают ли похожие истории с гриппом?
Грипп-диссидентов, наверное, все-таки не бывает. Во-первых, мы знаем об этой инфекции уже слишком давно. Во-вторых, практически каждый человек в детстве или уже будучи взрослым так или иначе сталкивался с гриппоподобными состояниями. Другое дело – люди, отрицающие целесообразность применения вакцин для профилактики гриппа. Или люди, которые считают, что вакцины могут вызвать заболевание, от которого они защищают. Есть и те, кто заявляет, что вакцины не работают в принципе.
Насколько эффективны вакцины от гриппа?
В настоящее время эффективность вакцины от гриппа составляет примерно 40-60%. Конечно, мы не можем защитить всех, но половина привитого населения – это очень хороший результат.
Производители вакцин против COVID-19 заявляют об эффективности выше 90%. При этом FDA была готова одобрить даже те, эффективность которых оказалась бы хотя бы на уровне 50%. Как относиться к такой разнице?
В своих прогнозах FDA как раз-таки опиралась на примерные значения эффективности противогриппозной вакцины. Результаты, которые приводят сегодня производители вакцин против коронавирусной инфекции, говорят о соотношении людей, у которых сформировался иммунный ответ на основании исследований с краткосрочной перспективой. Но когда речь идет о вакцинных препаратах несезонного применения, т.е. рассчитанных на длительный срок, для точной оценки необходимо больше времени. Напрямую сравнивать эффективность вакцин от гриппа и COVID-19 пока рано. Все препараты показали свою эффективность, но длительность и напряженность иммунного ответа мы сможем оценить только в динамике.
Тут нет никакой тайны. Это длительно отработанная система, которой занимается Всемирная организация здравоохранения (ВОЗ) в рамках своей международной сети, в которой в том числе участвует и Россия. Все члены этой сети в течение года мониторируют возбудителей гриппа, циркулирующих на определенной территории. Возбудители выделяются у больных, и затем производится их оценка по антигенным характеристикам. Со всего мира эта информация поступает в ВОЗ, где проводится анализ доминирующих штаммов вируса гриппа. В феврале сотрудники ВОЗ предоставляют информацию для производителей вакцин в северном полушарии, где мы и находимся. Важно понимать, что в первую очередь оценка проводится на основании анализа вирусов гриппа в южном полушарии. На сегодняшний день прогноз делается в отношении 4 возбудителей – 2 вирусов гриппа A и 2 линий вируса гриппа B.
Таким образом, в феврале ВОЗ сообщает, против каких именно возбудителей следует разрабатывать трех- или четырехвалентные вакцины. После этого производители приступают к изготовлению вакцины. Фактически на это уходит полгода: выработка антигенов, подготовка самого препарата и проверка его характеристик. К осени вакцина уже выходит на рынок для массовой вакцинации.
Как часто прогноз может оказаться несостоятельным?
Это происходит практически каждый год – в среднем выявляется один или два возбудителя, которые не соответствуют заявленным рекомендациям. Куда реже мы можем наблюдать полное соответствие.
Есть ли какая-то разница в вакцинации между различными странами?
В целом создание вакцины от гриппа осуществляется по универсальному принципу на основании прогноза ВОЗ. Универсальность заключается в том, что штаммовый состав вакцин для всех стран северного полушария одинаковый. При этом стоит отметить, что не все страны могут производить вакцины. В этом плане Россия находится в весьма хорошем положении, потому что мы способны полностью обеспечить себя вакциной от гриппа. В России есть даже несколько предприятий, полностью покрывающих весь производственный цикл, а в рамках национального календаря государство бесплатно предлагает всем вакцинацию от гриппа. Не в каждой стране ведется такое обеспечение бесплатной вакцинацией. В других странах этого может и не быть – они закупают вакцины, потому что не имеют собственного производства.
Какие тенденции существуют в разработке противогриппозных вакцин?
В первую очередь – тренд на разработку универсальных вакцин, которые позволили бы избежать ежегодной вакцинации, заменив их однократной прививкой в течение 3-5 лет. Работы над этим ведутся, в том числе и в НИИ гриппа им. Смородинцева. Наша универсальная вакцина прошла 1-ю фазу клинических испытаний с участием добровольцев и сейчас находится в стадии доработки.
Экспресс-тестирование на грипп входит в стандарт оказания медицинской помощи больным с ОРВИ в Японии. Как Вы считаете, стоит ли внедрить такой же подход в нашей стране?
Какие основные принципы закладываются в терапию гриппа?
Выделяют три типа терапии: этиотропная, воздействующая непосредственно на сам возбудитель; патогенетическая, ориентированная на механизмы, которые приводят к формированию патологического процесса; и симптоматическая терапия, необходимая для купирования уже развившихся симптомов. Говоря об инфекционных болезнях, наиболее эффективным является воздействие на саму причину заболевания. В отношении гриппа имеется целый ряд противовирусных препаратов. На первом месте стоят препараты прямого действия, например, ингибиторы нейраминидазы. Два представителя этой группы рекомендованы ВОЗ в качестве препаратов для лечения гриппа. Также прямое воздействие может заключаться в ингибировании синтеза вирусных РНК, что препятствует репликации вируса. Все перечисленные группы препаратов имеют хорошую доказательную базу и включены в клинические рекомендации.
Обычно этиотропные препараты показаны в первые двое суток заболевания. В первую очередь речь идет о пациентах с риском тяжелого течения болезни и развития осложнений гриппа: пожилых, детях младшего возраста, беременных, коморбидных пациентах. В принципе это та же группа, для которой в приоритете проводится вакцинопрофилактика. Однако бывают ситуации, когда пациент не относится ни к одной из этих групп, но заболевание протекает тяжело, с риском развития осложнений. В этом случае также показано назначение противовирусных препаратов.
Устойчивость к антибиотикам сегодня является одной из наиболее серьезных проблем здравоохранения. Есть ли аналогичная проблема у вирусных инфекций – резистентность к имеющимся препаратам?
Да, конечно. Проблема резистентности характерна не только для противомикробных препаратов, но и для противовирусных. Например, препарат ремантадин, который был эффективен в течение достаточно длительного времени, в последние примерно 10 лет столкнулся с практически полной резистентностью к нему вируса гриппа. Резистентность к другим препаратам постоянно мониторируется и, к счастью, пока не наблюдается ее такого стремительного развития. Глобальные данные по использованию ингибиторов нейраминидазы показывают, что резистентность к ним находится на уровне 1,5-2%. Однако бесконтрольное и неправильное применение препаратов, конечно, ухудшает состояние проблемы и способствует распространению резистентных форм вируса.
Какие существуют меры профилактики резистентности?
В первую очередь это обучение пациентов. Препараты должны применяться в полной дозе, полным курсом и в соответствии с теми рекомендациями, которые дает врач. С этим также связано понятие приверженности к лечению. В помощь как пациенту, так и врачу идет применение препаратов, которые можно назначать в однократном режиме. Это позволяет повысить приверженность и качество жизни пациентов, а кроме того – является одним из инструментов предупреждения формирования резистентности.
Как изменились подходы к лечению гриппа за последние годы? Есть ли новые разработки в этой области?
Сокращенный вариант интервью опубликован в журнале "Лечащий врач" N12/2020


Активный рост
В 2020 году в России пациенты на покупку противовирусных препаратов потратили более 50 млрд руб., следует из данных аналитической компании AlphaRM. По сравнению с 2019 годом продажи этой группы лекарств увеличились почти в два раза в упаковках и в два с половиной раза в рублевом эквиваленте, чему способствовала пандемия коронавирусной инфекции (рис. 1).
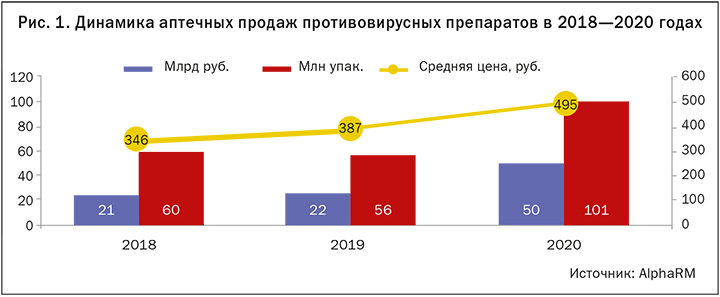
Всплески покупательской активности наблюдались весной и осенью 2020 года, когда объем продаж противовирусных препаратов в рублях относительно аналогичного месяца 2019 года увеличивался в несколько раз, к примеру, в пять раз — в октябре 2020 года.
В I квартале 2021 года в аптеках было продано около 19 млн упаковок на 9,9 млрд руб. Уменьшение рынка противовирусных препаратов относительно аналогичного периода 2020 года в рублях составило 4%, в упаковках продажи снизились на 22%. Рост средней цены в I квартале 2021 года на 22% немного замедлил снижение рынка в рублях.
![29-2.jpg (42 KB)]()
Новинки
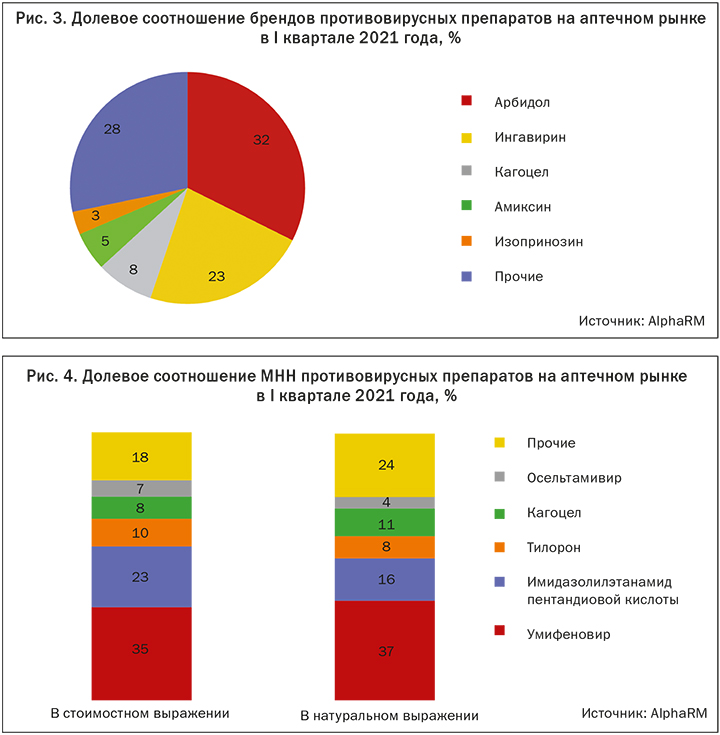
На рынке в настоящее время обращается 46 марок с 17 различными МНН (рис. 2).
Борьба с COVID-19 способствовала появлению новых противовирусных средств. В 2020 году в аптеках страны появилось около 10 торговых марок с тремя новыми действующими веществами — ремдесивир, фавипиравир, балоксавир марбоксил. Часть из них не продается в аптеках.
Первые в категории
Острые респираторные инфекции (ОРВИ) являются наиболее распространенными среди всех инфекционных заболеваний. На долю ОРВИ, а также гриппа приходится не менее 70% инфекционных заболеваний. В России ежегодно регистрируется около
Острые респираторные инфекции (ОРВИ) являются наиболее распространенными среди всех инфекционных заболеваний. На долю ОРВИ, а также гриппа приходится не менее 70% инфекционных заболеваний. В России ежегодно регистрируется около 50 млн инфекционных заболеваний, из которых до 90% случаев приходится на ОРВИ и грипп.
Почти 90% населения как минимум один раз в году переносят одну из респираторных инфекций вирусной этиологии, что в целом предопределяет высокую заболеваемость и даже влияет на показатель смертности [2].
Столь высокая частота заболеваний респираторного тракта объясняется многообразием этиологических факторов (вирусы гриппа, парагриппа, аденовирусы, риновирусы, реовирусы, респираторно-синцитиальные (РС) вирусы, микоплазмы, хламидии, бактериальные агенты), а также легкостью передачи возбудителя и высокой изменчивостью вирусов.
Дифференциальная диагностика гриппа и ОРВИ затруднена из-за сходства клинической картины этих заболеваний, но вполне возможна. Основными отличиями можно считать начальные признаки заболевания, симптомы интоксикации, характер катаральных явлений и лихорадки, тип развивающихся осложнений и др. Клинический диагноз, подтвержденный данными лабораторных анализов, и определяет выбор терапии.
Клиническая картина ОРВИ и гриппа зависит от вируса-возбудителя (см. таблицу).
Следует отметить, что осложнения при ОРВИ, особенно в период эпидемии, регистрируются в 20–30% случаев. Основными причинами осложнений являются нарушения иммунной защиты, приводящие к длительной недостаточности в работе иммунной системы. Снижение антибактериальной резистентности организма приводит к затяжным периодам реконвалесценции и обусловливает возможность осложнений в течение длительного времени. Особое место среди осложнений занимает так называемый синдром послевирусной астении (СПА), который может развиваться у 65% больных в течение 1 мес от начала заболевания. Ведущими симптомами СПА являются усталость, эмоциональные нарушения и различные психические расстройства.
Круг препаратов, используемых при лечении ОРВИ и гриппа, широк и разнообразен. Он включает живые и инактивированные вакцины, химиопрепараты этиотропного действия, а также средства, применяющиеся для иммунокорригирующей и патогенетической терапии.
Тем не менее течение гриппа и других ОРВИ по-прежнему плохо поддается контролю. Это связано не только с полиэтиологичностью данных заболеваний, но и с уникальной изменчивостью вирусов и глобальным характером эпидемий. Распространение ОРВИ в значительной степени зависит от экологической, социально-экономической ситуации, наличия у пациентов аллергических заболеваний и ряда других факторов.
Противовирусные препараты
Химиопрепараты
Механизм действия этой группы препаратов основан на избирательном подавлении отдельных звеньев репродукции вирусов, без нарушения жизнедеятельности клетки макроорганизма. При респираторных инфекциях используются две группы препаратов — блокаторы М2-каналов и ингибиторы нейроаминидазы, а также рибавирин, активный против РС-вируса.
Блокаторы М2-каналов
В 1961 г. был синтезирован симметричный амин — амантадин, а затем и ряд его производных (римантадин, мидантан, дейтифорин). В нашей стране получил широкое применение римантадин, который используется для лечения и профилактики гриппа, вызванного вирусом типа А. Эффективность этого средства составляет 70–90%.
Противовирусный эффект реализуется путем блокирования особых ионных каналов (М2) вируса, что сопровождается нарушением его способности проникать в клетки и высвобождать рибонуклеопротеид. Тем самым ингибируется важнейшая стадия репликации вирусов. Примерно в 30% случаев может развиваться резистентность к римантадину [6].
Римантадин выпускается в форме ремантадина в таблетках по 50 мг и сиропа для детей от 1 до 7 лет альгирем—2 мг/мл. С лечебной целью препарат назначается с момента регистрации первых симптомов. Длительность терапии не должна превышать 5 дней во избежание появления резистентных форм вируса. Профилактически римантадин необходимо принимать не менее 2 нед.
Ингибиторы нейроаминидазы
Препараты этой группы эффективны не только против вирусов гриппа типа А, но и против вирусов типа В.
Нейроаминидаза (сиалидаза) — один из ключевых ферментов, участвующих в репликации вирусов гриппа. При ингибировании нейроаминидазы нарушается способность вирусов проникать в здоровые клетки, снижается их устойчивость к защитному действию секрета дыхательных путей и таким образом тормозится дальнейшее распространение вируса в организме. Ингибиторы нейроаминидазы способны уменьшать продукцию цитокинов (ИЛ-1 и фактора некроза опухоли), препятствуя развитию местной воспалительной реакции и ослабляя такие системные проявления вирусной инфекции, как лихорадка, боли в мышцах и суставах, потеря аппетита [7].
Предварительные исследования показали, что эффективность такого ингибитора в качестве профилактического средства составляет 70–80%. Прием этих препаратов позволяет сократить длительность болезни на 1–1,5 дней (если препарат начать принимать не позднее, чем через 36–48 ч с момента появления первых симптомов). В начале заболевания и на ранних его стадиях средняя продолжительность репликации вируса сокращается в среднем на 3 дня, а число тяжелых форм ОРВИ и гриппа, характеризующихся повышенной температурой, — на 85%. Препараты не оказывают вредного воздействия на центральную нервную систему. Однако следует отметить, что далеко не всегда представляется возможность их применения в первые 48 ч: из-за сложностей, связанных с дифференциальной диагностикой гриппа и других ОРВИ.
Представителями ингибиторов нейроаминидазы являются озельтамивир и занамивир.
Озельтамивир (тамифлю) назначается по 75–150 мг 2 раза в день в течение 5 дней. Для профилактики — по 75 мг 1 или 2 раза в день в течение 4–6 нед. У пациентов с клиренсом креатинина менее 30 мл/мин доза снижается в 2 раза.
Занамивир (реленца) является структурным аналогом сиаловой кислоты — естественного субстрата нейроаминидазы вирусов гриппа — и, следовательно, обладает способностью конкурировать с ней за связывание с активным центром. Ингалируется с помощью специального устройства — дискхалера. С лечебной целью назначается по 10 мг 2 раза в день (с интервалом 12 ч) в течение 5 дней, для профилактики — по 10 мг 1 раз в день в течение 4–6 нед. Ингаляционный способ введения имеет преимущество, так как обеспечивает достаточно быстрый противовирусный эффект в зоне первичного очага инфекции.
Побочные реакции данной группы препаратов составляют не более 1,5% случаев. Чаще всего это головная боль, головокружение, тошнота, диарея, явления синусита. У пациентов с обструктивными бронхолегочными заболеваниями возможно развитие бронхоспазма.
Препараты, активные против других вирусов
Рибавирин (виразол, ребетол), действующий на многие РНК- и ДНК-содержащие вирусы, в аэрозольной лекарственной форме используется при лечении инфекций, вызванных РС-вирусом. Предполагается, что препарат ингибирует ранние этапы вирусной транскрипции, нарушая синтез рибонуклеопротеидов, информационной РНК, блокируя РНК-полимеразу. Применяется ингаляторно с помощью небулайзера только в условиях стационара.
При приеме рибавирина могут отмечаться бронхоспазм, сыпь, раздражение глаз, причем не только у пациентов, но и у медперсонала. В редких случаях наблюдаются лейкопения, бессонница, раздражительность. Существует риск кристаллизации препарата в дыхательных путях и интубационных трубках. Обладает тератогенным действием.
Перспективным противовирусным препаратом является недавно разработанный в США пленоконарил. В исследованиях in vitro и в экспериментах на животных выявлена его активность против энтеровирусов и риновирусов. Данные первых плацебо-контролируемых исследований свидетельствуют об эффективности препарата при респираторных инфекциях и энтеровирусном менингите [8].
В России применяются оригинальные противовирусные препараты, созданные на основе отечественных разработок. Наиболее широко известный из них — арбидол. Он оказывает ингибирующее действие на вирусы гриппа типа А и В и другие респираторные вирусы, механизм которых до конца не выяснен. Предполагают, что подобное воздействие связано и с интерферониндуцирующими и с иммуномодулирующими свойствами препарата. В частности, арбидол стимулирует активность фагоцитарных клеток. Выпускается в таблетках по 0,1 г. В лечебных целях назначается по 0,2 г 3–4 раза в день в течение 3–5 дней. С профилактической целью применяется по 0,2 г/сут в течение 10–14 дней.
Интерфероны
Интерфероны (ИФН) относятся к числу регуляторов иммуногенеза. Они продуцируются различными клетками и не только реализуют противовирусный ответ, но и регулируют иммунологические реакции. Основные эффекты интерферонов можно подразделить на антивирусные, антимикробные, антипролиферативные, иммуномодулирующие и радиопротективные.
Несмотря на разнообразие генетического материала вирусов, ИФН подавляют их репродукцию на стадии, обязательной для всех вирусов: они блокируют начало трансляции, т. е. синтез вирусспецифических белков. Этим можно объяснить универсальность антивирусного действия интерферона. Под воздействием интерферона в организме усиливается активность естественных киллеров, Т-хелперов, цитотоксических Т-лимфоцитов, фагоцитарная активность, интенсивность дифференцировки В-лимфоцитов, экспрессия антигенов МНС I и II типа [1].
Для лечения вирусных инфекций применяются α- и β-интерфероны. Хороший эффект при лечении дает комбинированное применение химиопрепаратов и препаратов ИФН.
β-интерферон (бетаферон) выпускается в форме порошка, во флаконах, содержащих по 9,5 млн ЕД ИФН. При гриппе его закапывают или распыляют в носовые ходы не менее 4–5 раз в сутки [2].
Человеческий лейкоцитарный интерферон представляет собой смесь интерферонов, синтезируемых лейкоцитами донорской крови в ответ на воздействие вирусного индуктора. Препарат вводят ингаляторно или закапывают в носовые ходы водный раствор, приготавливаемый из сухого вещества в ампуле или флаконе.
Виферон — рекомбинантный интерферон-α 2b — выпускается в форме ректальных свечей и применяется при лечении ОРВИ и гриппа. Повреждение клеточных мембран, наблюдаемое в ходе развития инфекционного процесса, является причиной снижения противовирусной активности интерферона. Токоферола ацетат и аскорбиновая кислота, входящие в состав виферона, являются мембраностабилизирующими компонентами, антиоксидантами, в сочетании с которыми противовирусная активность рекомбинантного интерферона-α 2b возрастает в 10–14 раз [1].
Особенности введения лекарственной формы обеспечивают длительную циркуляцию в крови интерферона-α 2b.
Препарат применяется как у новорожденных детей, так и у взрослых больных при ОРВИ и гриппе в возрастных дозировках. Детям до 7 лет назначается виферон-1, детям старше 7 лет и взрослым — виферон-2.
Индукторы интерферона
Амиксин — низкомолекулярный синтетический индуктор эндогенного интерферона ароматического ряда, относящийся к классу флуоренонов. Основными структурами, продуцирующими интерферон в ответ на введение амиксина, являются клетки эпителия кишечника, гепатоциты, Т-лимфоциты, гранулоциты. В лейкоцитах человека амиксин индуцирует образование интерферона, уровень в крови которого составляет 250 ЕД/мл. После приема амиксина внутрь максимум интерферона у человека определяется последовательно в кишечнике, печени, крови через 4–24 ч [2].
При лечении гриппа и ОРВИ амиксин назначается в первые часы заболевания, на курс достаточно 5–6 таблеток. С целью профилактики назначается 1 раз в неделю в течение 4–6 нед.
Циклоферон является низкомолекулярным индуктором ИФН-α , что определяет широкий спектр его биологической активности. Он быстро проникает в клетки, накапливаясь в ядре и цитоплазме. Циклоферон интеркалирует ДНК клетки, с чем связан механизм его интерферониндуцирующей активности [3].
Циклоферон быстро проникает в кровь. Отмечается низкое связывание его с белками крови и в то же время широкое распространение в различных органах, тканях, биологических жидкостях организма.
Ввиду того что циклоферон является низкомолекулярным препаратом, он легко преодолевает гематоэнцефалический барьер, вызывая образование ИФН в мозге. Циклоферон быстро выводится из организма: 99% введенного препарата элиминируется почками в неизмененном виде в течение 24 ч.
Циклоферон хорошо переносится больными и назначается с первого дня от начала заболевания в виде таблетированной формы или парентерально [4].
Ридостин — высокомолекулярный индуктор ИФН природного происхождения. Ридостин представляет собой двуспиральную РНК, полученную из лизата киллерных дрожжей Saccharamyces cervisiae.
Системное введение ридостина стимулирует продукцию раннего ИФН. Максимальное накопление ИФН в сыворотке отмечается через 6–8 ч после инъекции; через 24 ч в кровотоке не определяется [1].
Препарат проявляет выраженный иммуномодулирующий эффект. Он стимулирует Т-клеточное и гуморальное звенья иммунитета, пролиферацию стволовых клеток костного мозга и фагоцитарную активность макрофагов и нейтрофилов периферической крови. Ридостин повышает уровень кортикостероидных гормонов; применяется для лечения и профилактики гриппа и других ОРВИ.
В настоящее время незаслуженно забывают препарат дибазол, применяемый для лечения и профилактики гриппа и ОРВИ. Дибазол обладает иммуномодулирующей активностью и индуцирует выработку эндогенного интерферона. Для профилактики назначается по 1 таблетке (0,02–0,05 г) 1 раз в день — 3–4 нед, для лечения — по 1 таблетке 3 раза в день — 5 дней.
Незаменимы в лечении гриппа и ОРВИ такие комплексные препараты, как гриппостад, ринза, терафлю, фервекс, а также препараты для наружного и местного применения — мазь от простуды доктор Мом, туссамаг бальзам от простуды.
Несмотря на многообразие препаратов, представленных для лечения ОРВИ и гриппа на современном этапе, выбор лекарственного препарата остается актуальной задачей для практикующего врача. Выбор тактики назначения и ведения больного с ОРВИ или гриппом напрямую связан с тяжестью течения инфекционного процесса, формой заболевания и наличием осложнений. Успех лечения зависит от правильной оценки состояния больного и раннего начала лечения.
Интервью с Алексеем Ртищевым, к.м.н., доцентом кафедры инфекционных болезней у детей РНИМУ им. Пирогова Минздрава России, главным специалистом по инфекционным болезням у детей в ЦАО и ЮВАО города Москвы
.jpg)
Интервью с Алексеем Ртищевым, к.м.н., доцентом кафедры инфекционных болезней у детей РНИМУ им. Пирогова Минздрава России, главным специалистом по инфекционным болезням у детей в ЦАО и ЮВАО города Москвы
Да, такая формулировка правомочна в контексте текущего смягчения ограничительных мер в условиях пандемии COVID-19 и возобновления активных миграционных потоков – это безусловно увеличивает число контактов между людьми, что сказывается и на увеличении числа случаев гриппозной инфекции.
Наиболее важную роль в этом сыграли беспрецедентные строгие противоэпидемические мероприятия, которые проводились в условиях пандемии COVID-19: именно во время осеннего периода, для которого характерно начало роста заболеваемости ОРВИ, противоэпидемические мероприятия оказались наиболее серьезными. В начале прошлого сезона было предположение, что весь мир был сосредоточен именно на выявлении и борьбе с коронавирусной инфекцией, и настороженность в отношении гриппа была сравнительно низкой. Однако последующий мониторинг, активное тестирование больных с острыми респираторными инфекциями показали, что вирусы гриппа действительно практически не циркулировали. Также существует теория антагонизма некоторых респираторных вирусов. В частности, во время пандемии гриппа А(H1N1) 2009pdm было замечено, что в регионах с высокой заболеваемостью риновирусной инфекцией отмечалась более низкая заболеваемость новым вирусом гриппа. Вряде лабораторных экспериментов было продемонстрировано, аналогичное влияние риновируса и на вирус SARS-CoV-2. Но говорить об антагонизме гриппа и COVID-19 на данный момент оснований нет.
Существуют ли какие-то закономерности эпидемических процессов при гриппе?
Можно ли сравнить грипп и COVID-19 с точки зрения опасности заболевания? Существует ли достаточно данных для того, чтобы утверждать, что одна из инфекций чаще, чем другая приводит к осложнениям?
Безусловно, и то, и другое заболевание представляют определенную опасность, но особенности течения заболевания гриппозной и коронавирусной инфекцией все же отличаются.
При рассмотрении групп риска (возраст старше 60-65 лет и наличие хронических заболеваний, таких как избыточная масса тела, ожирение, сахарный диабет, артериальная гипертензия, иммунодефициты и целый ряд других состояний) и в случае гриппа, и в случае COVID-19 риск тяжелого течения, госпитализации и смертельного исхода достаточно высок. И, наконец, и для гриппа, и для COVID-19 существует риск развития отдаленных последствий, возникающих уже в период реконвалесценции, часть из которых связаны с декомпенсацией хронических заболеваний. Поэтому в текущий момент мы не можем каким-то объективным образом сравнить опасность этих двух инфекций, поскольку для этого требуется больше времени и данных.
Как устроена диагностика гриппа в условиях пандемии коронавирусной инфекции?
Стандартом ранней диагностики как в отношении гриппа, так и для COVID-19, является ПЦР-тест. Большое распространение также получили экспресс-тесты, основанные на выявлении антигена вируса — иммунохроматографический анализ (ИХА). Раннее выявление гриппа особенно важно с точки зрения назначения этиотропной терапии, на максимальную эффективность которой можно рассчитывать именно в начале заболевания.
Как меняются алгоритмы лечения гриппа в зависимости от тяжести заболевания?
Лечение любой инфекции можно разделить на 3 основных направления – этиотропная, патогенетическая и симптоматическая терапия. Стоит отметить, что грипп является единственной ОРВИ, для которой существует этиотропная терапия с доказанной клинической эффективностью. Несмотря на активные исследования в области лечения коронавирусной инфекции, для нее все же пока не существует какой-то уникальной и неоспоримой терапевтической опции.
Патогенетическая терапия является неотъемлемой частью лечения ОРВИ вне зависимости от имеющихся факторов риска. В первую очередь это дезинтоксикационная терапия, принципы которой зависят от тяжести состояния больного, Симптоматическая терапия в основном сфокусирована на применении жаропонижающих средств, самыми безопасными из которых сейчас считается парацетамол и ибупрофен. Другие методы лечения зависят от конкретных симптомов инфекции.
Является ли наличие лабораторно подтвержденной гриппозной инфекции показанием для назначения этиотропной терапии вне зависимости от имеющихся факторов риска?
В этом вопросе крайне важна ранняя этиологическая расшифровка, поскольку этиотропная терапия наиболее эффективно позволяет подавить именно раннюю репликацию вируса.
Позиция ВОЗ заключается в том, что этиотропная терапия в первую очередь должна рассматриваться у пациентов из группы риска: госпитализированные больные, возраст старше 60-65 лет, дети, беременные, коморбидные пациенты с сахарным диабетом, метаболическими нарушениями, артериальной гипертензией, бронхиальной астмой и другими заболеваниями. Также к этой группе можно отнести медицинских работников, но не столько с точки зрения тяжести заболевания, сколько со стороны распространения инфекции. В случае легкого течения гриппа прямых показаний к назначению этиотропной терапии нет.
Какова роль вакцинации в профилактике гриппа?
Безусловно, вакцинация является наиболее важным и эффективным методом профилактики гриппа, однако в ряде случаев ежегодно обновляемые вакцины могут быть неэффективными или недостаточно эффективными по отношению к отдельным циркулирующим штаммам. В этом году рекомендации Европейского регионального бюро ВОЗ в связи с возможной неэффективностью сезонных вакцин против циркулирующего штамма H3N2 предусматривают дополнительные меры по контролю заболеваемости гриппом в виде раннего начала этиотропного лечения и постконтактной профилактики.
Какие существуют направления в разработке новых методов лечения гриппа?
Первая группа препаратов имеет скорее историческое значение ввиду эффективности только против вируса гриппа А и повсеместно распространенной резистентности к нему современных циркулирующих вирусов. Ингибиторы нейраминидазы, несмотря на эпизодически выявляемые резистентныеь штаммы вирусов к этой группе препаратов, продолжают демонстрировать свою эффективность в последних эпидемиологических сезонах. Наиболее новым представителем средств с прямым противовирусным действием является балоксавир.
Чем представлена доказательная база нового противовирусного препарата, балоксавира?
Высокий уровень доказательной базы основан на результатах рандомизированных контролируемых исследований CAPSTONE-1 и CAPSTONE-2, где продемонстрирован высокий профиль безопасности, по частоте нежелательных явлений сравнимый с плацебо.
В чем заключаются преимущества балоксавира?
Терапия балоксавиром основана на однократном приеме препарата, что значительно увеличивает комплаентность пациента – практически до 100%, поскольку настолько простая схема терапии предполагает, что пациент либо принял препарат, либо его не принял.
Грипп может представлять опасность для любого возраста. Более того – дети раннего возраста, первых 5 лет жизни, относятся к группе высокого риска развития осложнений гриппа. В связи с этим, проведение исследований по эффективности и безопасности балоксавира в более младших возрастных группах являются крайне актуальными, и медицинское сообщество ждет дальнейших результатов и расширений показаний к назначению балоксавира.
Читайте также: