Сборка капсида у вируса
Обновлено: 18.04.2024
Капсид вируса. Функции капсида вирусов. Капсомеры. Нуклеокапсид вирусов. Спиральная симметрия нуклеокапсида. Кубическая симметрия капсида.
Генетический материал вирусов упакован в специальный симметричный футляр — капсид [от лат. capsa, футляр]. Капсид представлен белковой оболочкой, состоящей из повторяющихся субъединиц. Основные функции капсида — зашита вирусного генома от внешних воздействий, обеспечение адсорбции вириона к клетке, проникновение его в клетку путём взаимодействия с клеточными рецепторами.
Капсид образуют одинаковые по строению субъединицы — капсомеры, организованные в один или два слоя по двум типам симметрии — кубическому или спиральному. Симметричность капсида связана с тем, что для упаковки генома требуется большое количество капсомеров, а компактное их соединение возможно лишь при условии симметричного расположения субъединиц. Формирование капсида напоминает процесс кристаллизации и протекает по принципу самосборки. Число капсомеров строго специфично для каждого вида и зависит от размеров и морфологии вирионов. Капсомеры (морфологические единицы вирусов) образуют молекулы белка— протомеры (структурные единицы). Протомеры могут быть мономерными (содержать один полипептид) либо полимерными (включать несколько полипептидов).
Нуклеокапсид вирусов
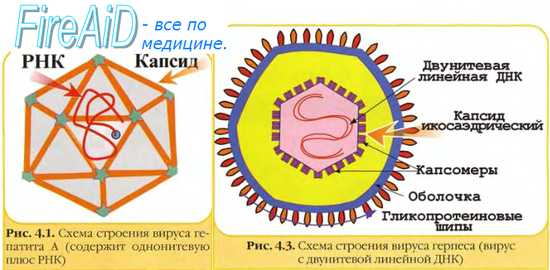
Комплекс капсида и вирусного генома называют нуклеокапсидом. Он повторяет симметрию капсида, то есть обладает спиральной либо кубической симметрией соответственно (рис. 2-2).
Спиральная симметрия. В нуклеокапсиде взаимодействие нуклеиновой кислоты и белка осуществляется по одной оси вращения. Каждый вирус со спиральной симметрией обладает характерной длиной, шириной и периодичностью нуклеокапсида. Нуклеокапсиды большинства патогенных для человека вирусов имеют спиральную симметрию (например, коронавирусы, рабдовирусы, пара- и ортомиксовирусы, буньявирусы и ареновирусы). К этой группе относят и вирус табачной мозаики. Организация по принципу спиральной симметрии придаёт вирусам палочковидную форму. При спиральной симметрии белковый чехол лучше защищает наследственную информацию, но требует большого количества белка, так как покрытие состоит из сравнительно крупных блоков.
Кубическая симметрия. У подобных вирусов нуклеиновая кислота окружена капсомерами, образующими фигуру икосаэдра— многогранника с 12 вершинами, 20 треугольными гранями и 30 углами. К вирусам с подобной структурой относят аденовирусы, реовирусы, иридови-русы, герпесвирусы и пикорнавирусы. Организация по принципу кубической симметрии придаёт вирусам сферическую форму. Принцип кубической симметрии — самый экономичный для формирования замкнутого капсида, так как для его организации используются сравнительно небольшие белковые блоки, образующие большое внутреннее пространство, в которое свободно укладывается нуклеиновая кислота.
Двойная симметрия. Некоторые бактериофаги (вирусы бактерий) имеют двойную симметрию: головка организована по принципу кубической симметрии, отросток — по принципу спиральной симметрии. Отсутствие постоянной симметрии. Для вирусов больших размеров (например, для поксвирусов) характерно отсутствие постоянной симметрии.
В состав нуклеокапсидов также входят внутренние белки, обеспечивающие правильную упаковку генома, а также выполняют структурную и ферментативную функции. Вирусные ферменты разделяют на вирионные и вирусиндуцированные. Первые входят в состав вирионов и участвуют в транскрипции и репликации (например, обратная транскриптаза), вторые закодированы в вирусном геноме (например, РНК-полимераза орто- и парамиксовирусов или ДНК-полимераза герпесвирусов). Вирионные ферменты также подразделяют на две функциональные группы: ферменты первой группы обеспечивают проникновение вирусных нуклеиновых кислот в клетку и выход дочерних популяций; ферменты второй группы участвуют в процессах репликации и транскрипции вирусного генома. В капсидах могут присутствовать ферменты обеих групп.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Репликация ДНК осуществляется ДНК-полимеразами. Для начала репликации необходим предварительный синтез короткого участка РНК на матрице ДНК, который называется затравкой. С затравки начинается синтез нити ДНК, после чего РНК быстро удаляется с растущего участка.
Репликация вирусных ДНК. Репликация генома ДНК-содержащих вирусов в основном катализируется клеточными фрагментами и механизм ее сходен с механизмом репликации клеточной ДНК.
Каждая вновь синтезированная молекула ДНК состоит из одной родительской и одной вновь синтезированной нити. Такой механизм репликации называется полуконсервативным.
У вирусов, содержащих кольцевые двунитчатые ДНК (паповавирусы), разрезается одна из нитей ДНК, что ведёт к раскручиванию и снятию супервитков на определенном участке молекулы.
При репликации однонитчатых ДНК (семейство парвовирусов) происходит образование двунитчатых форм, которые представляют собой промежуточные репликативные формы.
Репликация вирусных РНК. В клетке нет ферментов, способных осуществить репликацию РНК. Поэтому ферменты, участвующие в репликации, всегда вирусспецифические. Репликацию осуществляет тот же фермент, что и транскрипцию; репликаза является либо модифицированной транскриптазой, либо при репликации соответствующим образом модифицируется матрица.
Репликативные комплексы ассоциированы с клеточными структурами либо с предсуществующими, либо вирусиндуцируемыми. Например, репликативные комплексы пикорнавирусов ассоциированы с мембранами эндоплазматической сети, вирусов оспы — с цитоплазматическим матриксом, репликативные комплексы аденовирусов и вирусов герпеса в ядрах находятся в ассоциации со вновь сформированными волокнистыми структурами и связаны с ядерными мембранами. В зараженных клетках может происходить усиленная пролиферация клеточных структур, с которыми связаны репликативные комплексы, или их формирование из предсуществующего материала. Например, в клетках, зараженных пикорнавирусами, происходит пролиферация гладких мембран. В клетках, зараженных реовирусами, наблюдается скопление микротрубочек; в клетках, зараженных вирусами оспы, происходит формирование цитоплазматического матрикса.

В репликативных комплексах одновременно с синтезом геномных молекул осуществляется транскрипция и происходит сборка нуклеокапсидов и сердцевин, а при некоторых инфекциях — и вирусных частиц. О сложной структуре репликативных комплексов говорит, например, такой состав репликативного комплекса аденовирусов: реплицирующиеся ДНК, однонитчатые ДНК, однонитчатые РНК, ферменты репликации и транскрипции, структурные и неструктурные вирусные белки и ряд клеточных белков.
СБОРКА ВИРУСНЫХ ЧАСТИЦ
Синтез компонентов вирусных частиц в клетке разобщен и может протекать в разных структурах ядра и цитоплазмы. Вирусы, репликация которых проходит в ядрах, условно называют ядерными. В основном это ДНК-содержащие вирусы: аденовирусы, паповавирусы, парвовирусы, вирусы герпеса. Вирусы, реплицирующиеся в цитоплазме, называют цитоплазматическими. К ним относятся из ДНК-содержащих вирус оспы и большинство РНК-содержащих вирусов, за исключением ортомиксовирусов и ретровирусов. Однако это разделение весьма относительно, потому что в репродукции тех и других вирусов есть стадии, протекающие соответственно в цитоплазме и ядре.
Внутри ядра и цитоплазмы синтез вирусспецифических молекул также может быть разобщен. Так, например, синтез одних белков осуществляется на свободных полисомах, а других — на полисомах, связанных с мембранами. Вирусные нуклеиновые кислоты синтезируются в ассоциации с клеточными структурами вдали от полисом, которые синтезируют вирусные белки. При таком дисъюнктивном способе репродукции образование вирусной частицы возможно лишь в том случае, если вирусные нуклеиновые кислоты и белки обладают способностью при достаточной концентрации узнавать друг друга в многообразии клеточных белков и нуклеиновых кислот и самопроизвольно соединяться друг с другом, т. е. способны к самосборке.
В основе самосборки лежит специфическое белок-нуклеиновое и белок-белковое узнавание, которое может происходить в результате гидрофобных, солевых и водородных связей, а также стерического соответствия. Белок-нуклеиновое узнавание ограничено небольшим участком молекулы нуклеиновой кислоты и определяется уникальными последовательностями нуклеотидов в некодирующей части вирусного генома. С этого узнавания участка генома вирусными капсидными белками начинается процесс сборки вирусной частицы. Присоединение остальных белковых молекул осуществляется за счет специфичеческих белокбелковых взаимодействий или неспецифических белокнуклеиновых взаимодействий.
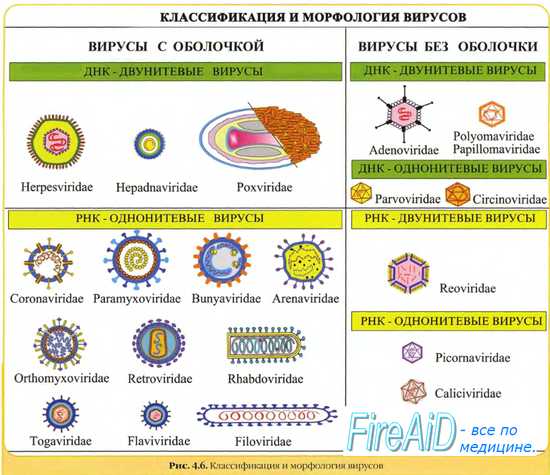
В связи с разнообразием структуры вирусов животных разнообразны и способы формирования вирионов, однако можно сформулировать следующие общие принципы сборки.
1. У просто устроенных вирусов формируются провирионы, которые затем в результате модификаций белков превращаются в вирионы. У сложно устроенных вирусов сборка осуществляется многоступенчато. Сначала формируются нуклеокапсиды или сердцевины, с которыми взаимодействуют белки наружных оболочек.
2. Сборка сложно устроенных вирусов (за исключением сборки вирусов оспы и реовирусов) осуществляется на клеточных мембранах. Сборка ядерных вирусов происходит с участием ядерных мембран, сборка цитоплазматических вирусов — с участием мембран эндоплазматической сети или плазматической мембраны, куда независимо друг от друга прибывают все компоненты вирусной частицы.
5. Сложно устроенные вирусы для построения своих частиц используют ряд элементов клетки-хозяина, например липиды, некоторые ферменты, у ДНК-геномного SV40 — гистоны, у оболочечных РНК-геномных вирусов — актин, а в составе ареновирусов обнаружены даже рибосомы. Клеточные молекулы несут определенные функции в вирусной частице, однако включение их в вирион может явиться и следствием случайной контаминации, как, например, включение ряда ферментов клеточных оболочек или клеточных нуклеиновых кислот.
Сборка РНК-содержащих вирусов. Сборка просто устроенных РНК-содержащих вирусов заключается в ассоциации вирусного генома с вирусными капсидными белками с образованием нуклеокапсида.
Все вирусные компоненты — нуклеокапсиды и суперкапсидные белки прибывают к месту сборки независимо друг от друга. Первыми к месту сборки прибывают суперкапсидные белки. Обычно этими белками являются гликопротеиды, которые синтезируются в полисомах, связанных с мембранами, и через шероховатые, а затем гладкие мембраны в результате слияния с ними везикул комплекса Гольджи транспортируются на наружную поверхность плазматических мембран или остаются в составе везикул.
Включение М-белка в клеточные мембраны является сигналом для сборки вирусной частицы: вслед за включением немедленно следует связывание нуклеокапсидов с мембранами и почкование вирусной частицы. Тем самым М-белок обладает функцией лимитирующего сборку фактора.
В результате связывания ДНК с капсидами появляется новый класс промежуточных форм, которые называются неполными формами. Помимо неполных форм с разным содержанием ДНК, существует другая промежуточная форма в морфогенезе — незрелые вирионы, отличающиеся от зрелых тем, что содержат ненарезанные предшественники полипептидов. Таким образом, морфогенез вирусов тесно связан с модификацией (процессингом) белков.
Сборка ядерных вирусов начинается в ядре, обычно — с ассоциации с ядерной мембраной. Формирующиеся в ядре промежуточные формы вируса герпеса почкуются в перинуклеарное пространство через внутреннюю ядерную мембрану, и вирус приобретает таким путем оболочку, которая является дериватом ядерной мембраны. Дальнейшая достройка и созревание вирионов происходит в мембранах эндоплазматической сети и в аппарате Гольджи, откуда вирус в составе цитоплазматических везикул транспортируется на клеточную поверхность.
ВЫХОД ВИРУСНЫХ ЧАСТИЦ ИЗ КЛЕТКИ
Выход из клетки путем взрыва связан с деструкцией клетки, нарушением ее целостности, в результате чего находящиеся внутри клетки зрелые вирусные частицы оказываются в окружающей среде. Такой способ выхода из клетки присущ вирусам, не содержащим липопротеидной оболочки (пикорна-, рео-, парво-, папова-, аденовирусы). Однако некоторые из этих вирусов могут транспортироваться на клеточную поверхность до гибели клетки.
Выход из клеток путем почкования присущ вирусам, содержащим липопротеидную мембрану, которая является дериватом клеточных мембран. При этом способе клетка может длительное время сохранять жизнеспособность и продуцировать вирусное потомство, пока не произойдет полное истощение ее ресурсов.
В зависимости от типа генетического материала (ДНК или РНК), образование дочерних копий геномов протекает по-разному.
У ДНК-геномных вирусов репликация вирусных ДНК принципиально сходна с репликацией клеточных ДНК.
Репликацию РНК-геномных вирусов осуществляют вирусные РНК-зависимые РНК-полимеразы (репликазы). Исключение составляют ретровирусы, их +РНК служит матрицей для синтеза ДНК Синтез ДНК на матрице РНК осуществляет вирусная РНК-зависимая ДНК-полимераза (обратная транскриптаза), необходимая для переписывания информации с РНК на ДНК. Синтезируемая вирусная ДНК интегрируется в клеточный геном в форме ДНК-провируса.
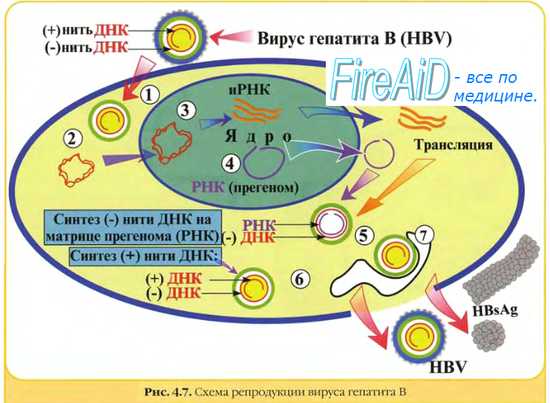
Репликация однонитевых РНК вирусов. Репликация протекает в два этапа: первый включает образование матрицы, комплементарной геному; второй — образование копий РНК с этой матрицы. При репликации +РНК-вирусов количество копий -РНК (на матрице родительской нити +РНК) строго контролируется, а количество копий +РНК (с матрицы синтезированной нити -РНК) не контролируется.
Репликация двухнитевых РНК вирусов. В качестве матрицы для синтеза +РНК вирусные репликазы используют минус-нить РНК и наоборот. Часть молекул -РНК соединяется с +РНК и образует двухнитевую молекулу РНК, а другая часть молекул -РНК функционирует как матрица для синтеза мРНК.
Сборка вирусов
У просто устроенных вирусов, состоящих из нуклеиновой кислоты и нескольких белков, сборка состоит из упорядоченного взаимодействия этих молекул. У сложно устроенных вирусов сборка дочерних популяций протекает многоступенчато.
Взаимодействие нуклеиновых кислот с внутренними и оболочечными белками приводит к образованию нуклеокапсидов, или сердцевин. В процессе образования «одетых - вирусов полные нуклеокапсиды упорядочение выстраиваются с внутренней стороны клеточной мембраны под участками, модифицированными оболочечными вирусными белками (М-белками). При нарушениях процесса самосборки могут образовываться пустые капсиды либо комплексы нуклеиновых кислот с внутренними белками.
Высвобождение дочерних вирионов из клетки
Высвобождение дочерних вирионов — конечная стадия репродуктивного цикла. Вирусы, лишённые суперкапсида, и поксвирусы обычно высвобождаются быстро; выход дочерних популяций сопровождается разрушением цитоплазматической мембраны (ЦПМ) и лизисом клетки. Вирусы, содержащие суперкапсид, высвобождаются медленнее. Модифицированные участки мембраны с заключёнными в них вирионами выпячиваются наружу и затем отпочковываются. Принцип высвобождения дочерних популяций почкованием во многом сходен с процессами, направленными на отторжение непригодного для клетки материала или обновление клеточных мембран. При высвобождении почкованием изменённая клетка иногда может сохранять жизнеспособность.
- Вернуться в оглавление раздела "Микробиология."
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Типы инфицирования клеток вирусами. Репродуктивный цикл вирусов. Основные этапы репродукции вирусов. Адсорбция вириона к клетке.
По характеру взаимодействия генома вируса с геномом клетки выделяют автономное (геном вируса не интегрирован в геном клетки) и интеграционное (геном вируса интегрирован в геном клетки) инфицирование. Особую форму составляют латентное и персистирующее инфицирование.
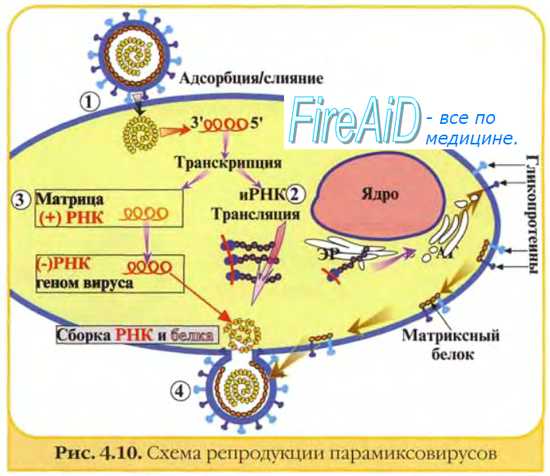
Персистирующее инфицирование клеток вирусам. Некоторые РНК-вирусы могут вызывать персистиру-ющие инфекции, проявляющиеся образованием дочерних популяций возбудителя после завершения острой фазы болезни. При этом происходит постепенное выделение вирусных частиц, но инфицированная клетка не лизируется. Нередко дочерние популяции вирионов дефектны (часто наблюдают у лиц с иммунодефицитами). Иногда такие хронические поражения протекают без клинических проявлений. В частности, вирус гепатита В способен вызывать персистирующее поражение гепатоцитов с развитием хронического гепатита; в дальнейшем возможна малигнизация клеток.
Репродуктивный цикл вирусов
Изображённые на рис. 2-3 этапы репродукции (от адсорбции вирионов до высвобождения дочерней популяции) происходят при продуктивном взаимодействии вируса с клеткой.
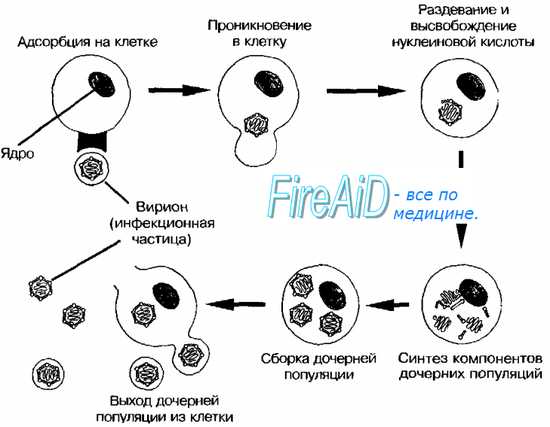
Рис. 2-3. Основные этапы репродукции вирусов.
Адсорбция вириона к клетке
• Процесс адсорбции не зависит от температуры (то есть не требует энергетических затрат) и протекает в две фазы; фаза ионного притяжения обусловлена неспецифическим взаимодействием, фаза прикрепления происходит благодаря структурной гомологии либо комплемен-тарности взаимодействующих молекул.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.

Один из возможных способов бороться с патогенными вирусами — блокировать их сборку; так они не смогут выходить из клеток и расселяться по организму. Но для этого необходимо разобраться с тем, как именно эта сборка происходит. Строение капсидов — белковых структур, внутри которых заключены молекулы нуклеиновых кислот вируса — мы уже неплохо себе представляем, а вот как именно из молекулярного раствора возникает упорядоченная симметричная конструкция, все еще неясно.
Рис Гарман (Rees Garmann) и его коллеги из Гарвардского университета изучали динамику сборки вирусного капсида. Их модельным объектом был маленький РНК-содержащий вирус, который заражает клетки кишечной палочки — бактериофаг MS2. Чтобы его рассмотреть, исследователи использовали интерферометрическую рассеивающую микроскопию: суть ее в том, что прибор собирает свет, который рассеивают объект и фон.
Исследователи зафиксировали отдельные молекулы вирусных РНК на подложке и ввели в раствор вирусные белки. Под микроскопом они обнаружили растущие темные пятна. Ученые поставили параллельный эксперимент под трансмиссионным электронным микроскопом, в котором можно было рассмотреть не только размер, но и структуру поверхности частицы. Оказалось, что это действительно капсиды. Их сборку удалось заснять на видео, в среднем она заняла около 300 секунд.

Строение капсида (А), дизайн эксперимента (В), вид в микроскоп (С) и динамика построения капсида (D).
Garman et al. / PNAS, 2019
Поэтому авторы работы предположили, что для построения вирусной частицы необходимо сначала некоторое белковое ядро, на которое потом садятся остальные молекулы. Вероятно, разница во времени объясняется именно этим: в некоторых частицах оно случайно образуется раньше, а в других — позже. После того, как частица начала расти — то есть ядро сформировалось — рост идет необратимо. Такой вывод исследователи сделали из того, что размеры частиц растут, но никогда не уменьшаются.
Затем ученые повторили свои эксперименты, изменяя концентрацию белков. Они обнаружили, что чем больше белков в растворе, тем быстрее образуются ядра капсида. Время, которое уходит на рост частицы, тоже снижается, но медленнее, чем время образования ядра. Это наблюдение позволило им объяснить аномальные формы капсидов, которые иногда встречаются у разных вирусов.

Соотношение фаз нуклеации (образования ядра) и роста в зависимости от концентрации белков (А) и образующиеся при этом структуры (В).
Читайте также:

