Снижение тромбоцитов при вирусной инфекции у ребенка
Обновлено: 25.04.2024
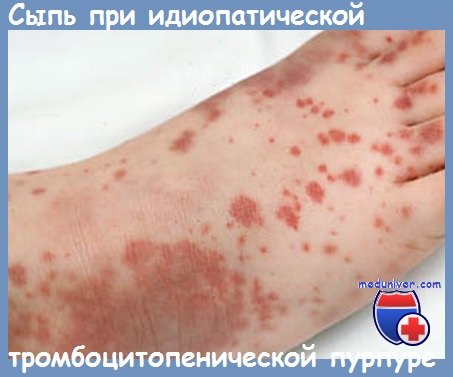
Тромбоцитопеническая пурпура после вирусных инфекций - клиника, диагностика
Эпидемиологическая анкета и специальные исследования показывают, что у детей младше 8 лет, вирусные инфекции предшествуют тромбоцитопенической пурпуре в 85% случаев и лишь 15% являются очевидно идиопатическими.
Болезнь наступает внезапно, обычно спустя 1—3 недель после вирусной инфекции, особенно дыхательных путей; бывают случаи, когда период после инфекции и до появления пурпуры продолжительнее — до 4 месяцев. Согласно McClure, вирусную этиологию можно установить по меньшей мере в 50% случаев из 413 исследованных детей.
Пурпура появилась спустя 3—6 недель, с одинаковой частотой у мальчиков и девочек, в то время как у взрослого преобладают женщины в пропорции 2/1 или даже 3/1.
Вирусная этиология была наглядно доказана у детей с тромбоцитопенической пурпурой, родившихся с краснухой (Luscher и сотр., Wallace, Svenigsen, Zinkham и сотр.), при которой обнаруживаются антивирусные антитела после состояния виремии.
Вполне возможно, что механизм тромбоцитопении происходит по поводу поражений типа III, благодаря иммунным комплексам, но не по поводу антитромбоцитарных антител. Виремия, как и при других вирусных инфекциях, находится лишь на 7 дней раньше и два дня после вирусного высыпания, следовательно задольго до пурпурного высыпания.
Вирусная этиология определяется после некоторых вирусных инфекций, проявляющих максимальную частоту в холодные времена года или в начале весны, как например различные высыпные лихорадки, корь, ветряная оспа, оспа, а также и инфекции с Pertussis. Бывают случаи и после инфекционных мононуклеозов, а также и после вирусных герпесов, инфекций с цитомегаловирусом, свинкой и даже после гепатита Боткина.
Вирусная этиология была доказана несомненно при тромбоцитопенической пурпуре после противокоревой или противооспенной вакцинации, но только в редких случаях (Alter и сотр., Oski и сотр., Bachand и сотр.). Реже можно ссылаться на иммунную этнологию после бактериальных инфекций (Clement и Diamond) или после интрадермореакций на туберкулин.
Следует обращать особое внимание на тромбоцитопеническую пурпуру, появляющиеся в разгаре септического состояния, микробного или вирусного, при котором механизм тромбоцитопении иной. В этих случаях микробные токсины, как при стрептококковых, пневмококковых, менингококковых инфекциях, а также и вследствие других граммотрицательных агентов, детерминируют появление во время септического периода синдрома с вторичной тромбоцитопенией путем явления Sanarelli-Schwartzmann.
Микробные токсины, но особенно вирусные частицы, могут прямо вызывать агглютинацию тромбоцитов и тяжелый прогрессивный синдром по поводу уничтожения тромбоцитов на уровне РЭС. Это тромбоцитопени-ческие расстройства по поводу снижения тромбоцитов на периферии, к которому добавляется однако и дефицит производства благодаря прямому поражению мегакариоцитов, которые являются очень благоприятной средой для размножения вирусов (Dalton и сотр.).
В разгаре вирусной инфекции или после вакцинации число мегакариоцитов понижается, они представляют дефекты созревания и дегенеративные поражения с вакуолями и многочисленными свободными ядрами, в то время как число тромбоцитов снижается. При тяжелых тромбоцитопениях констатируется признак разрушения тромбоцитов с повышением в сыворотке кислотных фосфатаз.
Подобные механизмы с периферическим лизисом возникают и при других инфекциях, как например лихорадка денга, токсоплазмоз, а также и при таиландской геморрагической лихорадке, вызв шной вирусом миэлодепрессивного действия (Bierman и Nelson). Эти данные смешанного патогенеза необходимы для диагностицирования известных вторичных форм путем изучения непосредственного действия инфекционных агентов, таких как вирусные агенты, антитела, иммунные комплексы, а также тромбоцитарного турновера и функций мегакариоцитов.
С клинической точки зрения, поствирусные формы у детей имеют в основном характер идиопатической тромбоцитопенической пурпуры. В обширной статистике, McClure находит, наряду с пурпурой у всех больных, эпистаксис у 30%, гематурию у 5— 10% и органиченную частоту для других кроворечений, как например гемоторакс. Внутричерепные кровоизлияния, хотя и редкие (1,2%), являются причиной смерти у 30% исследованных больных в период пурпуры.
Спленомегалии и иногда умеренные гепатомегалии появляются в 10% случаев и детерминированы скорее вирусной инфекцией, чем тромбоцитопеническим заболеванием.
С точки зрения эволюции, 50% случаев излечиваются после острого приступа за 1—2 и реже 3 месяца. В пропорции 10—20% случаев, тромбоцитопения с вариабильными значениями, с явлениями легкой или акцентуированной пурпуры персистирует от одного до нескольких лет.
У 8—10% случаев, после периода излечения, пурпура рецидивирует или принимает стойкий хронический характер, с акцентуированными приступами, детерминированными вероятно реинфекциями, которые усугубляют процесс самопродолжения путем генерирования новых иммунных комплексов или даже путем появления автоиммунного механизма после разрыва толерантности.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
На сервисе СпросиВрача доступна консультация детского гематолога по любой волнующей Вас проблеме. Врачи-эксперты оказывают консультации круглосуточно. Задайте свой вопрос и получите ответ сразу же!


Здравствуйте,после перенесенной инфекции могут снижаться тромбоциты,нужен контроль оак с подсчетом тромбоцитов вручную(часто считает анализатор),так же наблюдайте за дочкой,появление синячков,кровоточивости и т д повод обратиться срочно к врачу.

Добрый день! Если было в острое вирусное заболевание и было лечение, то скорее всего эта тромбоцитопения временное явление, от самого заболевания или терапии против него. И со временем должна самоликвидироваться. В лечениии при таких цифрах не нуждается, но надо продолжить контролировать анализ с определением количества тромбоцитов по Фонио. При прогрессирующем снижении - госпитализация в гематологический стационар для проведения специфической терапии.

Здравствуйте! Тромбоциты снижены не настолько сильно . чтоб появились клинические проявления( синяки. на теле. возникающие без особой причины). Наблюдайте за ребенком. каждые 14 дней пересдавайте кровь. Если появились синяки, значит , тромбоциты ниже 25-30тыс. тромбоцитопения не является самостоятельным заболеванием , если не снижаются другие клетки крови( лейкоциты и эритроциты). За ней наблюдают. обычно. все восстанавливается самостоятельно. но вы примите меры к скорейшему восстановления ребенка- принимайте витамин С в натуральном виде( отвар шиповника. лимон , киви, если нет противопоказаний- все по немногу, чтоб не вызвать аллергию) Также для неспецифического укрепления иммунитета пропейте курс бифидум бактерина по 3 флакона в день 21 день . Это препарат нормальной кишечной микрофлоры. И каждое лекарство проверяйте на побочное действие в виде тромбоцитопении. Вам такие нельзя. Здоровья.

Здравствуйте, Екатерина! Тромбоциты снижены всвязи с пересенным ранее заболеванием.
Нужно пересдать ОАК на фоне полного выздоровления, через 10-14 дней.
Тромбоциты должны придти в норму. Ребенок чувствует себя хорошо-это главное!
Пока требуется только наблюдение в динамике.
Не болейте!

Это не очень низкие тромбоциты. Чаще всего снижение тромбоцитов у 30% детей перенесенных перенёсших вирусную инфекцию встречается в 100% случаев, пересдайте через 2 недели, я более чем уверена что тромбоциты придут в норму. Очень часто вижу такие анализы после перенесенных вирусных инфекций и они не внушают мне никаких опасений. Всё проходит бесследно

Добрый день, розеола вызывается не энтровирусом а герпесом VI типа, необходимо сдать анализ на ДНК к этому герпесу из мочи или мазок из горла. Вирусная инфекция бывает дает такой побочный результат как снижение тромбоцитов и нейтрофилов, что мы мы и наблюдаем. Бывает и после применения некоторых лекарственных средств (ибупрофен - нурофен, антибиотики). У детей снижение тромбоцитов чаще носит временный характер, но тут необходим теперь наблюдение в динамике за общим анализом крови.

специфического лечения гематолог не может не назначить, пока не будет симптомов (синяков или частых инфекций). При повышении температуры из-за малого количества нейтрофилов, необходимо будет применение антибиотиков.
На сервисе СпросиВрача доступна консультация детского гематолога по любой волнующей Вас проблеме. Врачи-эксперты оказывают консультации круглосуточно. Задайте свой вопрос и получите ответ сразу же!

Здравствуйте. Пока переживать не стоит. Может быть на фоне инфекции снижение тромбоцитов. В этом ничего страшного нет. Также Необходим приём жидкости минимум 2 литра в сутки.
Сейчас необходимо ежедневно сдача общего анализа крови с подсчетом лейкоцитарной формулы врачом лаборантом, это очень важно. УЗИ брюшной полости +селезёнки. И если будут дальнейшие изменения, то необходим перевод в краевую больницу , где есть гематолог .
Ольга, спасибо за ответ. Сегодня сделаем УЗИ. Ещё нам назначили аскорутин. Его нужно принимать? Витамин С не разжижает кровь?

,здравствуйте! Лекарств должно быть минимум.исключите из рациона консерванты аллергены ароматизаторы( т е ,*. Магазинные полуфабрикаты готовая продукция,)обильное пить чистой воды .контроль оак с ручным подсчётом тромбоцитов .

Здравствуйте. Учитывая выраженность инфекции, тромбоциты снижены на ее фоне. Пока все это требует контроля. При положительной динамике никуда ехать не придется. Но в любом случае, обязательно пройти УЗИ селезенки и органов брюшной полости.
Виктория, спасибо за ответ. УЗИ сегодня сделаем. Нам назначили аскорутин, его стоит принимать? Где-то читала, что витаминС разжижает кровь.

Аскорутин назначается при низких тромбоцитах. Разжижать кровь глобально вит.С не способен, как аспирин, к примеру. К тому же, не за счет разрушения тромбоцитов он это пытается делать))

Здравствуйте , да, такое допустимо. Сейчас желательно отказаться от всех НПВС и внутримышечных инъекций. Тромбоциты контролировать с ручным подсчетом

Аскорутин вам как раз показан,потому что он укрепляет сосудистую стенку в условиях риска кровотечения,учитывая тромбоцитопению. Следуйте рекомендациям. Вторичная тромбоцитопения частый симптом после острых вирусных инфекций, за редким исключением с применением специфической терапии,но всегда обратима! Не волнуйтесь. Здоровья ребёнку!


Примерно половина всех тромбоцитов производится в легких.
Если там идет воспалительный процесс - это все объясняет.
Это не опасно, ибо остальные 50% рождает костный мозг и, может быть, селезенка.
Аскорутин за такие сроки никаких сосудов не укрепит, но витамины расходуются иммунной системой при воспалении в удвоенном количестве для синтеза белков (антител). Поэтому аскорутин не лишний.
Кровотечений при нормальной коагулограмме не будет.

Эритроциты
Сниженное количество эритроцитов часто встречается у пациентов с неврологическими расстройствами:, например , болезнях Паркинсона и Альцгеймера , рассеянном склерозе и ишемическом инсульте . С другой стороны и вегетативная дисфункция может быть тесно связана с эритропоэзом.
Если при болезнях Альцгеймера и Паркинсона и дисфункции вегетативной нервной системы ( ваготония ) мы встречаемся со снижением гемоглобина, то при рассеянном склерозе , мигрени, синдроме запястного канала , а главное – ишемическом инсульте – с его повышением . Однако, анемия может быть и причиной вторичных инсультов.
Анемия с относительным дефицитом эритропоэтина наблюдается у пациентов с дисфункцией вегетативной неврной системы и у некоторых пациентов с диабетом 1 типа как с тяжелой вегетативной нейропатией (АН), так и протеинурией
Неврологические нарушения после черепно-мозговой травмы прогрессируют у анемичных субъектов из-за снижения напряжения кислорода в мозге и вызванной гипоксией гибели клеток.
В одних случаях мы наблюдаем повышение гематокрита ( апноэ во сне, ишемический инсульт или инфаркт ) в других, таких как болезнь Альцгеймера или синдром беспокойных ног – напротив , снижение HCT.
При сложном регионарном болевом синдроме , синдроме запястного канала, генерализованной эпилепсии и болезни Альцгеймера мы отмечаем повышение MCV и RDW. Кроме того, последний показатель также повышен при болезни Паркинсона и синдроме хронической усталости. При инфаркте мозга часто фиксируется ускоренную ESR.
В заключении следует отметить небольшое количество исследований , посвященных MCH и MCHC при неврологических расстройствах.
Дефицит железа
В литературе имеется документальное подтверждение того, что дефицит железа связан с когнитивными нарушениями , а также со многими психоневрологическими расстройствами, такими как синдром дефицита внимания и гиперактивности (СДВГ), расстройства аутистического спектра, тревожное расстройство и биполярные аффективные расстройства. Отметим, что когнитивные способности детей с ID / IDA демонстрируют тенденцию к улучшению при лечении железом у детей в возрасте старше 2 лет
Дефицит железа является распространенным заболеванием у детей. Хотя наиболее распространенным проявлением является анемия, дефицит железа часто является источником множества неврологических расстройств, в частности , в общей детской неврологической практике. Эти расстройства включают задержку развития, инсульт, эпизоды задержки дыхания, псевдоопухоль головного мозга и паралич черепных нервов. Несмотря на то, что определение дефицита железа как части дифференциального диагноза при этих расстройствах встречается часто, оно регистрируется редко редко и обычно не лечится.

Коронавирусная болезнь 2019 (COVID-19) - это инфекционное заболевание, вызванное тяжелым острым респираторным синдромом (SARS), связанным с коронавирусом 2 (SARS-CoV-2). SARS-CoV-2 принадлежит к семейству коронавирусов, которые представляют собой оболочечные вирусы со сферической морфологией и геномом одноцепочечной РНК (оцРНК). Шипованные гликопротеины (S-белок) проходят через пеплос вируса и образуют короноподобную поверхность. Через домен связывания рецептора (RBD) , расположенный в S1 - субъединицу белка S, вирус может лигировать к рецепторной клетки - хозяина ангиотензин-превращающего фермента (2) ACE2 и вторгнуться в клетку.
Клиническая картины ковида
Во многих случаях у людей, инфицированных SARS-CoV-2, наблюдаются симптомы гриппа, такие как лихорадка, усталость и сухой кашель. Головная боль, миалгия, боль в горле, тошнота и диарея также наблюдаются у пациентов с COVID-19. В тяжелых случаях возникают одышка и гипоксемия. В критических случаях заболевание быстро прогрессирует, и у пациентов может развиться септический шок и полиорганная дисфункция. Таким образом, COVID-19 может быть системным заболеванием, поражающим несколько систем органов, включая кожу, почки, дыхательную систему, сердечно-сосудистую систему, пищеварительную систему, нервную систему и гематологическую систему. Нарушение регуляции иммунного ответа и повышение провоспалительных цитокинов, вызванных SARS-CoV-2, способствуют патогенезу заболевания и повреждению органов, что привлекло внимание к иммунорегулирующей терапии при лечении COVID-19.
Сходство ковида с аутоиммунными заболеваниями
COVID-19 имеет сходство с аутоиммунными заболеваниями по клиническим проявлениям, иммунным ответам и патогенетическим механизмам. Аутоантитела как признак аутоиммунных заболеваний также могут быть обнаружены у пациентов с COVID-19. Сообщалось, что у некоторых пациентов после заражения COVID-19 развились аутоиммунные заболевания, такие как синдром Гийена-Барре или системная красная волчанка. Предполагается, что SARS-CoV-2 может нарушать самотолерантность и вызывать аутоиммунные реакции за счет перекрестной реактивности с клетками-хозяевами.
Иммунный ответ - это палка о двух концах при COVID-19, на результаты которого влияет степень цитокинового дисбаланса и активация иммунных клеток. Избыточное производство и высвобождение провоспалительных цитокинов и хемокинов может вызвать серьезное повреждение органов в критических случаях, что также наблюдается при аутоиммунных заболеваниях. У пациентов с COVID-19 повышались провоспалительные цитокины и хемокины, включая интерлейкин (IL) -1, IL-2, IL-6, IL-8, IL-10, IL-17, IL-18, CXCL10 и CCL2. значительно и уровни экспрессии некоторых из этих цитокинов, таких как IL-1, IL-6, IL-10 и IL-18, были связаны с тяжестью заболевания. Подобно аутоиммунным заболеваниям, молекулярные паттерны, связанные с повреждениями (DAMP), также участвуют в патогенезе COVID-19 и связаны с исходом заболевания. Уровни S100A8 / A9 и HMGB1 в сыворотке крови значительно повысились у пациентов с тяжелой формой COVID-19 и значительное повышение двух DAMPs было связано с более высокой смертностью.
Активация и инфильтрация иммунных клеток участвуют в патогенезе повреждения органов у пациентов с COVID-19. Синдром активации макрофагов (MAS) может быть континуумом синдрома цитокинового шторма, приводящего к опасным для жизни осложнениям при COVID-19. В этом состоянии активированные макрофаги будут производить чрезмерное количество провоспалительных цитокинов, поляризоваться в воспалительный фенотип M1 и проявлять цитотоксическую дисфункцию. Тучные клетки, активированные SARS-CoV-2, могут выделять гистамин, повышая уровень IL-1, чтобы инициировать цитокиновый шторм и уcилить повреждение легких. Исследователи обнаружили экстрафолликулярную активацию В-клеток у пациентов с COVID-19 в критическом состоянии, аналогично тому, что наблюдалось при аутоиммунных заболеваниях. Кроме того, активация экстрафолликулярных В-клеток сильно коррелировала с производством высоких концентраций нейтрализующих антител, специфичных для SARS-CoV-2, и плохим исходом заболевания. Субпопуляции В-клеток периферической крови изменяются во время COVID-19. У пациентов с COVID-19 атипичные B-клетки памяти (CD21 lo / CD27 - / CD10 - ) значительно увеличились, в то время как классические B-клетки памяти (CD21 + / CD27 + / CD10 - ) были значительно уменьшены. Анализ иммунных профилей пациентов с тяжелой формой COVID-19 выявил повышенную долю зрелых естественных киллеров (NK) и снижение доли Т-клеток.
Подобно некоторым аутоиммунным и иммуноопосредованным тромбовоспалительным заболеваниям, включая волчанку, антифосфолипидный синдром и ANCA-ассоциированный васкулит, активация нейтрофилов и образование внеклеточной ловушки нейтрофилов (НЕТоз), по-видимому, играют патогенную роль при COVID-19.
Риск заражения ковидом пациентов с аутоиммунными заболеваниями
Было описано, что ген лейкоцитарного антигена человека (HLA) и его полиморфизм связаны с развитием различных аутоиммунных заболеваний / нарушений . В последнее время исследователи пытаются понять, как генетика человека может повлиять на распространение и заражение нынешнего вируса SARS-Cov-2. Что касается упомянутых выше доказательств связи между вирусом SARS-Cov-2 и аутоиммунитетом, неудивительно, что ученые выявили сильную связь между генетическим полиморфизмом covid-19 и HLA.
Результаты поперечного исследования, проведенного на северо-востоке Италии, показали, что пациенты с аутоиммунными заболеваниями имели схожую частоту инфицирования SARS-CoV-2 по сравнению с населением в целом. Другое итальянское исследование, проведенное в Милане, также подтвердило, что аутоиммунное заболевание не является фактором риска заражения COVID-19. Интересно, что исследование из Милана показало, что пациенты с аутоиммунными заболеваниями не имеют худшего прогноза по сравнению с людьми, не страдающими аутоиммунными заболеваниями. Однако испанское исследование показало, что госпитализированные пациенты с аутоиммунными заболеваниями имеют более тяжелое течение COVID-19.
Напротив, результаты многоцентрового ретроспективного исследования, проведенного в провинции Хубэй, Китай, показали, что пациенты с аутоиммунными заболеваниями могут быть более восприимчивыми к инфекции SARS-CoV-2 по сравнению с контрольной группой. Кроме того, в этом исследовании были изучены члены семей пациентов, которые проживали в той же среде во время вспышки, что и контрольная группа.
В настоящее время, пока не появится больше данных, крайне важно подчеркнуть важность физического дистанцирования, ношения масок и частого мытья рук для всех, особенно для наших пациентов с аутоиммунными заболеваниями. Приверженность к лекарствам также очень важна для предотвращения вспышек аутоиммунных заболеваний, которые могут привести к повреждению органов.
Аутоантитела при ковиде
Аутоантитела, встречающиеся при ряде аутоиммунных заболеваний, были обнаружены у пациентов с COVID-19. Исследователи выявили наличие антинуклеарных антител (ANA), антицитоплазматических нейтрофильных антител (ANCA) и антиантифосфолипидных (APL) антител у пациентов с COVID-19. Результаты показали, что 45% пациентов были положительными по крайней мере на одно аутоантитело, а пациенты с положительными аутоантителами имели тенденцию иметь худший прогноз и значительно более высокую частоту дыхания при поступлении. Положительный показатель для ANA составил 33%, положительный показатель для антикардиолипиновых антител (IgG и / или IgM) составил 24%, а у трех пациентов были получены положительные результаты на антитела против β2-гликопротеина-I (IgG и / или IgM) (9%). Однако ANCA был отрицательным у всех пациентов.
Коагулопатия - опасное осложнение инфекции SARS-CoV-2. Недавно в Медицинском центре Монтефиоре было проведено когортное исследование для оценки положительности антикоагулянтов при волчанке у пациентов с COVID-19. Исследователи обнаружили, что пациенты с COVID-19 имели повышенную частоту положительных результатов на антикоагулянтную волчанку по сравнению с контрольной группой, у которых был отрицательный результат с помощью ПЦР с обратной транскриптазой COVID-19. Кроме того, у пациентов с COVID-19 с положительным результатом антикоагулянта против волчанки наблюдалась повышенная частота тромбозов. Некоторые авторы также продемонстрировали более высокую частоту антител APL у пациентов с тяжелым и критическим COVID-19, и что присутствие антител APL, по-видимому, связано с гипервоспалительным состоянием с чрезвычайно высокими уровнями ферритина, С-реактивного белка и IL-6, а также при тромбоэмболии легочной артерии. Обсужденные выше данные дают возможное объяснение состояния гиперкоагуляции в тяжелых и критических случаях COVID-19 и указывают на то, что SARS-CoV-2 может вызывать аутоиммунные реакции.
Клинический аутоиммунитет после ковида
Аутоиммунные заболевания, такие как: синдром Гийена-Барре , синдром Миллера-Фишера (MFS) , антифосфолипидный синдром , иммунная тромбоцитопеническая пурпура , системная красная волчанка (SLE) и Болезнь Кавасаки - выявлялись у пациентов с инфекцией COVID-19. Кроме того, обонятельную дисфункцию можно наблюдать при ряде аутоиммунных заболеваний, таких как: SLE, рассеянный склероз и миастения (MG).
Молекулярная мимикрия инфекционных патогенов
Возможно, одним из наиболее известных примеров молекулярной мимикрии аутоиммунитета является иммунный ответ на вирус Эпштейна-Барра (EBV) у пациентов с волчанкой. Аномальный иммунный ответ на ядерный антиген-1 вируса Эпштейна-Барра (EBNA-1) может вызвать аутоиммунный ответ, нацеленный на системы аутоантигенов Sm и Ro. Также была продемонстрирована перекрестная реактивность между антителами против EBNA-1 и основным белком миелина у пациентов с рассеянным склерозом. Более того, EBNA-1 обнаружил структурное сходство с β-синуклеином, белком мозга, участвующим в рассеянном склерозе, и предположительно связывает HLA класса II DR2b (HLA-DRB1 * 15: 01). Анализ in-silico показал, что белок оболочки эндогенных ретровирусов человека (HERV) имеет сходную последовательность с тремя белками миелина, которые вызывают аутоиммунный ответ при рассеянном склерозе и, как было предсказано, связываются с HLA-DRB1 * 15: 01. Инфекция, вызванная вирусом Коксаки B3 (CVB3), может индуцировать образование аутореактивных Т-клеток в отношении множества антигенов.
Лимфоциты при ковиде
Лечение ковида препаратами для терапии аутоиммунных заболеваний
Аутоиммунные заболевания неоднородны и связаны с нарушением регуляции иммунной системы. Большинство пациентов с аутоиммунными заболеваниями получали или получают иммуномодулирующие препараты или биологические агенты. Во время пандемии COVID-19 часть пациентов с аутоиммунным заболеванием прекратила прием лекарств из-за опасений иммуносупрессивного эффекта лекарств или их отсутствия и сократила количество посещений врача из-за опасений заразной природы SARS-CoV. -2. Однако нарушение непрерывности оказания медицинской помощи и несоблюдение режима приема лекарств связаны с обострениями ревматологических заболеваний и ухудшением активности заболевания.
Некоторые лекарства, используемые для лечения аутоиммунных ревматологических заболеваний, могут оказывать терапевтический эффект у пациентов с тяжелыми вариатами инфекции COVID-19, что обращает внимание на взаимосвязь между COVID-19 и аутоиммунными заболеваниями. Риск заражения и прогноз COVID-19 у пациентов с аутоиммунными заболеваниями остаются спорными, но строго рекомендуется соблюдение пациентом режима приема лекарств для предотвращения обострений аутоиммунных заболеваний.
В тяжелых и критических случаях применялись иммуномодулирующие препараты и биологические агенты, нацеленные на провоспалительные цитокины, для сдерживания устойчивого иммунного ответа при COVID-19. Кортикостероиды, ингибиторы JAK, блокаторы IL-1 и антагонисты рецепторов IL-6, которые знакомы ревматологам, используются для лечения пациентов с COVID-19.
Вакцинация против ковида и аутоиммунные заболевания
Читайте также:

