Специфический и не специфический иммунитет при гепатите в
Обновлено: 24.04.2024
Приведенные данные убедительно доказывают то, что лямблиоз действительно угнетает иммунную систему организма, что отражается на активности основного его маркера – лизоцима. В 1-й группе пациентов, для которых характерен длительно протекающих лямблиоз и хронический вирусный гепатит В, только в 5,0 ± 2,8 % случаев наблюдается более 70 % активность лизоцима, и почти в таких же случаях она находится в пределах 61–70 % – 8,0 ± 3,5 %. Активность лизоцима на уровне 41–50 % отмечалась в 40,0 ± 6,3 % случаев. Показатели содержания специфического иммуноглобулина sIgA в ротовой жидкости свидетельствуют о нарушении в местной иммунной системе организма. Самая неблагоприятная ситуация с показателями содержания sIgA наблюдается в 1-й группе пациентов. В отличие от других групп, в этой группе очень мало случаев с нормальным содержанием sIgA. Отягчающее влияние вирусного гепатита В на иммунную функцию организма начинает проявляться при поэтапном развертывании клинической картины заболевания.

1. Бурканова JI.B. Функциональное состояние желчевыводящих путей при инфекционном гепатите в сочетании с лямблиозом и без него // Вирусный гепатит. – 2009. – № 4. – С. 1–7.
2. Быстрова Т.Н., Блохин К.В., Макарова Т.Г Динамика клинического течения гепатита А в зависимости от интенсивности эпидемического процесса // Идеи Пастера в борьбе с инфекциями: материалы конференции. – СПб., 2007. – С. 76.
3. Крамарь Л.В., Резников В.Е., Крамарь О.Г. Распространенность лямблиоза среди жителей Волгограда // Медицинская паразитология и паразитарные болезни. – 2008. – № 4. – С. 38–39.
4. Крыга Л.И., Платошина О.В. Богданов Х.У. Эпидемиологическая характеристика очагов хронических гепатитов В и С. // Идеи Пастера в борьбе с инфекциями: материалы конференции. – СПб., 2007. – С. 78.
5. Alter H.J., Holland P.V., Purcele R.H. Viral hepatitis. Light at the end of the tunnel // JAMA. – 2009. – Vol. 299, № 3. – P. 293–294.
6. Boyd William P., Bachman Barbara A. Gastrointestinal infections in the compromised host // Med. Clin. N. Amer. – 2010. – Vol. 66, № 3. – P. 743–753.
7. Вurness B.W., Beach M.J., Roberts J.M. Giardiasis surveillance United States // Morbidity& Mortality Weekly Report. – 2007. – Vol. 49, № 7. – P. l13.
8. Ganem D. Persistent infection of humans with hepatitis В virus: Mechanism and consequences // Rev. Infect. Dis. – 2008. – Vol. 4. – Р. 1026–1047.
Одно из ведущих мест в современной медицинской науке и практике занимает изучение этиологии, патогенеза и обоснование методов лечения вирусного гепатита В (ВГВ). При этом большинство работ ориентированы на изучение причин и механизмов развития этой патологии у лиц, не отягощенных паразитарными заболеваниями. Значительно меньше изучены особенности течения ВГВ на фоне кишечных паразитозов, в том числе такого распространенного, как лямблиоз [1, 2, 3]. В то же время, по данным ВОЗ, заболеваниями, сопровождающимися нарушениями метаболизма, к каковым относится лямблиоз, страдают многие миллионы людей и прогнозируется значительное увеличение данной патологии в ближайшие 10 лет.
Несмотря на небольшое число исследований по влиянию кишечных паразитозов на развитие и течение ВГВ, получены убедительные факты о многокомпонентноым воздействии этого заболевания на функциональное состояние печени. Как известно, лямблиоз возникает чаще и протекает менее благоприятно у лиц с изначальными дефектами иммунной защиты. В то же время лямблиоз относится к заболеваниям, сопровождающимся нарушениями иммунореактивности, и к факторам риска развития и неблагоприятного течения ВГВ [4, 5, 6, 7. 8]. Поэтому изучение спектра воздействия ВГВ на иммунные функции организма приобретает актуальное значение, так как без устранения последствий подобного воздействия лечение ВГB практически обречено на неудачу.
Целью исследования явилось изучение спектра влияния вирусного гепатита В на иммунные функции организма
Материалы и методы исследования
В соответствии с решаемыми задачами были отобраны три группы наблюдения: 1-я группа наблюдения – 59 пациентов, с развернутой, длительно протекающей клинической формой лямблиоза и с наличием хронического вирусного гепатита В, 2-я группа наблюдения ‒ 48 пациентов без лямблиоза и наличием ранних, начальных стадий , и контрольная группа наблюдения – 45 пациентов, не имеющих ВГВ и лямблиоза, практически здоровое население. Для характеристики состояния местного иммунитета организма обследуемых пациентов использовали методы по определению лизоцима секреторного иммуноглобулина sIgA, которые наиболее информативны в иммунологическом отношении. В основу количественного определения иммуноглобулинов положено измерение кольца преципитации, образующегося после внесения исследуемого субстрата в лунки, вырезанные в слое агара, в котором предварительно диспертирована моноспецифическая сыворотка. В стандартных условиях опыта диаметр кольца преципитации прямо пропорционален концентрации исследуемого иммуноглобулина sIgA. Концентрацию иммуноглобулина определяли по калибровочному графику с точностью до 0,003 г/л. В норме уровень sIgA в ротовой жидкости находится в пределах 50–60 г/л. Статистический анализ данных осуществлялся с помощью программы электронных таблиц Microsoft Excel, которые были сформированы в соответствии с запросами проводимого исследования.
Результаты исследования и их обсуждение
Лизоцим – фермент класса гидролаз, разрушающий оболочки бактериальных клеток, является первым и надежным антимикробным барьером организма. Присутствием его в ротовой жидкости и нейтрализацией агрессивных патогенных микроорганизмов во многом обусловлено процветание человечества. Снижение уровня активности лизоцима (обычно это бывает при менее 70 %) является серьезным сигналом сбоя иммунологической функции организма. Приведенные нами исследования по определению активности лизоцима в ротовой жидкости разных групп пациентов дали следующие результаты (табл. 1).
Данные по активности лизоцима в ротовой жидкости в разных группах обследованных пациентов
Что такое гепатит Б? Причины возникновения, диагностику и методы лечения разберем в статье доктора Александрова Павла Андреевича, инфекциониста со стажем в 14 лет.
Над статьей доктора Александрова Павла Андреевича работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Вирусный гепатит В (Б) — острое и хроническое инфекционное заболевание, вызываемое вирусом гепатита В, с гемоконтактным механизмом передачи (через кровь), протекающее в различных клинико-морфологических вариантах, и возможным развитием цирроза печени и гепатоцеллюлярной карциномы. Всего в мире, по самым скромных оценкам, инфицировано более 250 млн человек.
Этиология
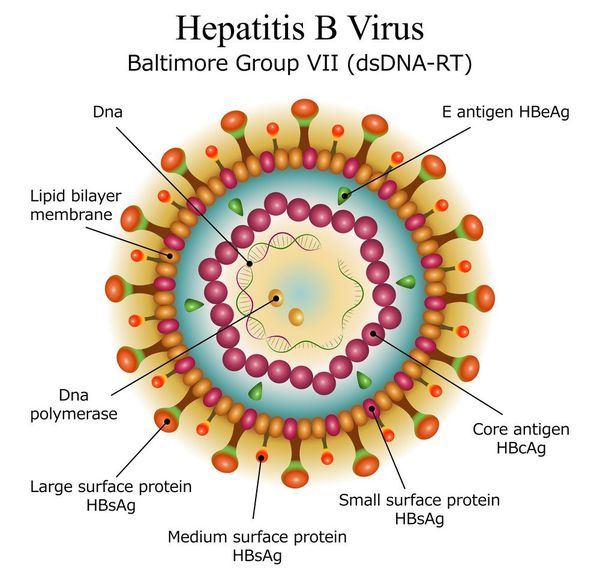
вид — вирус гепатита В (частица Дейна)
Развитие вируса гепатита Б происходит в гепатоцитах (железистых клетках печени). Он способен к интеграции в ДНК человека. Имеются 9 генотипов вируса с различными подтипами — генетическая изменчивость позволяет вирусу образовывать мутантные формы и ускользать от действия лекарств.
Имеет ряд собственных антигенов:
- поверхностный HbsAg (австралийский). Появляется за 15-30 дней до развития болезни, свидетельствует об инфицировании (не всегда). Антитела к HbsAg выявляются через 2-5 месяцев от начала заболевания, а сам HbsAg исчезает из крови (при благоприятном течении процесса);
- сердцевинный HbcorAg (ядерный, коровский). Появляется в инкубационном периоде и совместно с ним появляются антитела (HbcorAb). Длительное присутствие HbcorAg в крови свидетельствует о вероятной хронизации процесса (неадекватный иммунный ответ);
- антиген инфекциозности и активного размножения вируса (HbeAg). Появляется совместно с HbsAg и отражает степень инфицированности. Его продолжительная циркуляция в крови является свидетельством развития хронизации процесса, а антитела к нему являются благоприятным прогностическим признаком (не всегда, но по меньшей мере указывают на возможность более благоприятного процесса, срок их циркуляции после выздоровления окончательно не определён, но не более пяти лет после благоприятного разрешения процесса);
- HbxAg — регулятор транскрипции, способствует развитию гепатокарциномы.
Вирус гепатита В чрезвычайно устойчив к действию всевозможных естественных факторов окружающей среды, инактивируется при 60 °C за 10 часов, при 100 °C за 10 минут, при оптимальной температуре сохраняется до 6 месяцев, при автоклавировании погибает за 5 минут, в сухожаровом шкафу — через 2 часа, 2% раствор хлорамина убивает вирус за 2 часа. [1] [3]
Эпидемиология
Источник инфекции — только человек, больной острой или хронической формой инфекции.
Механизм передачи: гемоконтактный и вертикальный (от матери к ребёнку), не исключается трансмиссивный механизм передачи (например, при укусах комаров в результате раздавливания и втирания инфицированного тела комара в поврежденную ткань человека).
Пути передачи: половой, контактно-бытовой, гемотрансфузионный (например, при переливании крови или медицинских манипуляциях). Восприимчивость всеобщая. Заболеваемость — 30-100 человек на 100 тысяч населения (зависит от страны). Летальность от острых форм — до 2%. После перенесённого острого заболевания при условии выздоровления иммунитет стойкий, пожизненный.
Для заражения характерна малая заражающая доза (невидимые следы крови). [1] [2]
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
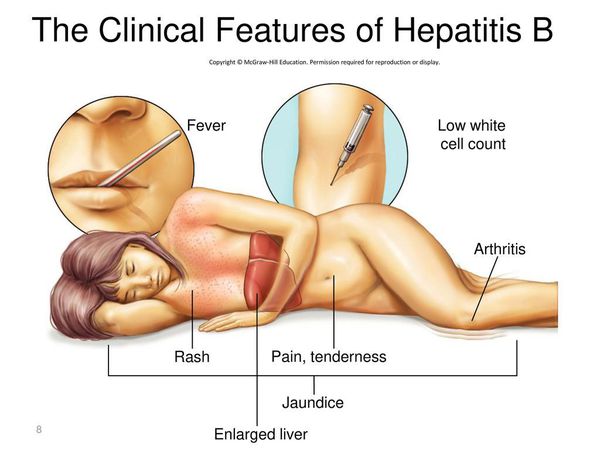
Симптомы гепатита Б
Инкубационный период гепатита В длится от 42 до 180 дней (следует иметь в виду, что наличие клинической симптоматики характеризует лишь незначительную долю всех случаев заболевания).
Начало постепенное. Характерные синдромы:
- общей инфекционной интоксикации (проявляется как астеноневротический синдром);
- холестатический (нарушение секреции желчи);
- артрита;
- нарушения пигментного обмена (появление желтухи при уровне общего билирубина свыше 40 ммоль/л);
- геморрагический (кровоточивость кровеносных сосудов);
- экзантемы;
- отёчно-асцитический (скопление жидкости в брюшной полости);
- гепатолиенальный (увеличение печени и селезёнки).
При первых признаках гепатита B нужно обратиться к доктору.
Первые признаки гепатита B
Начальный (преджелтушный) период продолжается 7-14 дней. Чаще протекает по многообразному типу с болевыми ощущениями в различных суставах по ночам и утром, уртикарными высыпаниями, астеновегетативными проявлениями (снижение аппетита, апатия, нервозность, слабость, разбитость, повышенная утомляемость). Изредка развивается синдром Джанотти-Крости — симметричная, яркая пятнисто-папулёзная сыпь. Не исключены умеренные диспептические явления (расстройства пищеварения). К концу периода происходит потемнение мочи, обесцвечивание кала.
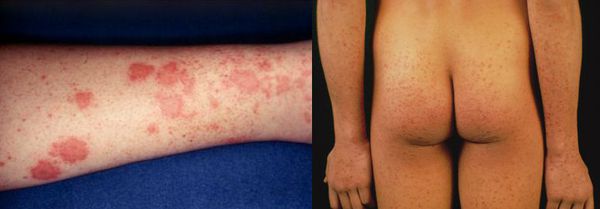
Желтушный период
Этот период продолжительностью около одного месяца характеризуется возникновением желтушного окрашивания кожи (различных оттенков) на фоне продолжающегося или ухудшающегося общего состояния. Характерна длительность и стойкость симптоматики. Появляется тяжесть и болезненность в правом подреберье, горечь во рту, тошнота, выражённый зуд кожи (практически не снимаемый никакими средствами). На фоне усиления астеноневротического компонента появляются геморрагические проявления, урежение пульса, гипотензия, отёки (отражает степень интоксикации и нарушения функций печени).
Выздоровление
Следующим этапом в развитии болезни является нормализации общего состояния, спадение желтухи и реконвалесценция, которая в зависимости от конкретной ситуации и состояния иммунной системы может закончиться как выздоровлением, так и движением развития заболевания в хроническое течение, характеризующееся маловыраженой неусточивой симптоматикой, преимущественно в виде слабости, периодического дискомфорта в правом подреберье, бурно сигнализирующим лишь на стадии цирроза и полиорганных осложнений.
- гепатиты другой этиологии;
- желтухи другой этиологии (например, гемолитическая болезнь, токсическое поражение, опухоли);
- малярия; ;
- лептоспироз;
- ревматоидный артрит.
Гепатит В у беременных
Острый гепатит характеризуется более тяжёлым течением у беременной, возникновении повышенного риска преждевременных родов, аномалий развития плода на ранних сроках и кровотечений. Вероятность передачи при острой форме зависит от сроков беременности: в первом триместре риск 10% (но более тяжёлые проявления), в третьем триместре — до 75% (чаще бессимптомное течение после родов). У большинства детей при заражении во внутриутробном и постнатальном периодах происходит хронизация инфекции. [1] [3] [6]
Патогенез гепатита Б
С движением кровяной массы вирус попадает в печеночную ткань, где локализуется в гепатоцитах и теряет свою протеиновую сферу в лизосомах. Происходит выход вирусной ДНК с последующим ресинтезом аномальных протеинов LSP, а параллельно образование новых частиц Дейна.
В процессе эволюции вирусчеловеческого взаимодействия возможно развитие двух вариантов:
При репликативном пути происходит следующее: белки LSP совместно с HbcorAg вызывают увеличение продукции гамма-интерферона, что приводит к активации главного комплекса гисотсовместимости (HLA), проистекает преобразование молекул гистосовместимости 1 и 2 классов, в результате чего клетка становиться для организма враждебной в антигенном формате.
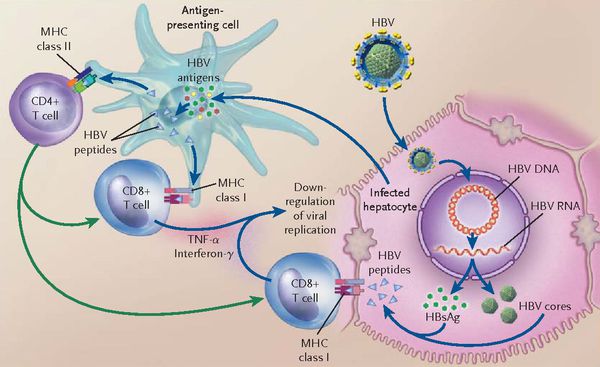
Антигенпрезентирующие макрофаги содействуют изменению В-лимфоцитов в плазматические клетки и экспрессии ими агрессивных белков-антител к посторонним антигенам. В итоге на поверхности печёночных клеток формируются вирусспецифические иммунные комплексы (антиген + антитело + фракция комплемента С3в).
В динамике может реализоваться два сценария:
- в первом варианте запуск каскада комплимента ведёт к появлению в составе иммунных комплексов агрессивной фракции С9 (мембранатакующий комплекс) — наблюдается значительный некроз гепатоцитов без участия лимфоцитов (молниеносная форма гепатита В);
- при альтернативной варианте (наблюдающимся в большинстве случаев) каскад комплемента в силу иммуноиндивидуалистических свойств не активируется — тогда идёт умеренное разрушение Т-киллерами меченых антителами заражённых вирусом гепатоцитов. Образуются ступенчатые некрозы с образованием на месте гибели гепатоцитов соединительной ткани — рубцов (то есть острый гепатит В при плохом иммунном ответе постепенно переходит в хронический).
Непременным атрибутом патогенеза является формирование иммунопатологического процесса. Гибель гепатоцитов, инфицированных вирусом гепатита В, следует за счёт иммунокомпетентных частиц, Т-киллеров и макрофагальных элементов.
Серьёзным значением является нарушение свойств мембраны клеток печени, что сопровождается экскрецией (выделением) лизосомальных ферментов, разрушающих гепатоциты. Сообразно этому, гибель гепатоцитов происходит за счёт иммунокомпетентных клеток, лизосомальных ферментов и противопечёночных гуморальных аутоантител, то есть острая болезнь наступает (и благоприятно заканчивается) только при хорошем иммунитете, а при плохом идёт хронизация.
При тяжёлом цитолитическом синдроме (массивные некрозы гепатоцитов) возникает гипокалиемический алкалоз, острая печёночная недостаточность, печёночная энцефалопатия (ПЭП), церебротоксическое действие, нарушение функции обмена нервной ткани. [2] [3] [6]
Классификация и стадии развития гепатита Б
По цикличности течения:
- острый;
- острый затяжной;
- хронический.
По клиническим проявлениям:
- субклинический (инаппарантный);
- клинически выраженный (желтушный, безжелтушный, холестатический, фульминантный).
По фазам хронического процесса:
Группы риска хронического гепатита B
Хроническим гепатитом чаще страдают дети младше шести лет. При заражении в первый год жизни он развивается в 80–90 % случаев, от года до шести лет — в 30–50 %, у взрослых без сопутствующих заболеваний — менее чем в 5 %. [7]
Осложнения гепатита Б
Чем опасен гепатит Б
Заболевание может привести к острой печёночной недостаточности (синдрому острой печеночной энцефалопатии).
Выделяют четыре стадии болезни:
Диагностика гепатита Б
Многообразие форм, тесная взаимосвязь с иммунной системой человека и зачастую достаточно высокая стоимость исследований часто затрудняют принятие конкретного решения и диагноза в стационарный отрезок времени, поэтому во избежание роковых (для больного) ошибок следует подходить к диагностике с учётом всех получаемых данных в динамическом наблюдении:
- общеклинический анализ крови с лейкоцитарной формулой (лейкопения, лимфо- и моноцитоз, уменьшение СОЭ, тромбоцитопения);
- общий анализ мочи (появление уробилина);
- биохимический анализ крови (гипербилирубинемия в основном за счёт связанной фракции, повышение уровня АЛТ и АСТ, ГГТП, холестерина, щелочной фосфатазы, снижение протромбинового индекса, фибриногена, положительная тимоловая проба);
- маркеры гепатита В: HbsAg, HbeAg, HbcorAg, HbcorAb IgM и суммарные, HbeAb, anti-Hbs, ПЦР в качественном и количественном измерении);
- УЗИ органов брюшной полости, КТ и МРТ диагностика;
- фиброскан (применяется для оценки степени фиброза). [3][4]
Скрининг при хроническом гепатите
Пациентам с хроническим гепатитом В рекомендуется не реже чем раз в полгода проходить обследование: УЗИ органов брюшной полости, клинический анализ крови, АЛТ, АСТ, тест на альфа-фетопротеин. Скрининг позволяет вовремя заметить обострение болезни и начать специфическую терапию.
Лечение гепатита Б
Лечение острых форм гепатита В должно осуществляться в стационаре (учитывая возможность быстрых и тяжёлых форм болезни), хронических — с учётом проявлений.
Диета и режим при гепатите В
В острый период показан постельный режим, печёночная диета (№ 5 по Певзнеру): достаточное количество жидкости, исключение алкоголя, жирной, жареной, острой пищи, всё в мягком и жидком виде.
Медикаментозная терапия
При лёгкой и средней тяжести острого гепатита этиотропная противовирусная терапия (ПВТ) не показана. При тяжёлой степени и риске развития осложнений назначается специфическая противовирусная терапия на весь период лечения и возможно более длительное время.
В лечении хронических форм гепатита показаниями к назначению ПВТ является наличие уровня DNA HBV более 2000 МЕ/мл (при циррозе печении независимо от уровня), умеренное и высокое повышение АЛТ/АСТ и степени фиброза печёночной ткани не менее F2 по шкале METAVIR, высокая вирусная нагрузка у беременных женщин. В каждом конкретном случае показания определяются индивидуально, в зависимости от выраженности процесса, временной тенденции, пола, планирования беременности и другого.
Существует два пути противовирусного лечения:
- терапия пегилированными интерферонами (имеет ряд существенных противопоказаний и серьёзных побочных эффектов — не менее 12 месяцев);
- нуклеозидно-аналоговой терапии NA (используются препараты с высоким порогом резистентности вируса, длительно — не менее пяти лет, удобство применения, хорошая переносимость).
В отдельных случаях может рассматриваться применение комбинированной терапии.
Из средств патогенетической терапии в острый период используются внутривенно вводимые растворы 5% глюкозы, дезинтоксикантов, антиоксидантов и витамины. Показан приём энтеросорбентов, ферментных препаратов, при выраженном холестазе применяются препараты Урсодезоксихолевой кислоты, при тяжёлом течении — глюкокортикостероиды, методы аппаратного плазмофереза.
В хронической стадии заболевания при наличии соответствующей активности процесса и невозможности назначения ПВТ может быть показан приём групп гепатопротекторов и антиоксидантов. [1] [3]
Прогноз. Профилактика
Основное направление профилактики на сегодняшний день — это проведение профилактической вакцинации против гепатита В в младенческом возрасте (в том числе усиленная вакцинация детей, рождённых от матерей с гепатитом В) и далее периодические ревакцинации раз в 10 лет (или индивидуально по результатам обследования). Достоверно показано, что в странах, где была введена вакцинация, резко сократилось количество вновь выявленных случаев острого гепатита В.
Вторая составляющая стратегии профилактики включает обеспечение безопасности крови и её компонентов, использование одноразового или стерилизованного инструментария, ограничение числа половых партнёров и использование барьерной контрацепции. [1] [2]
JANGU BANATVALA 1 , PIERRE VAN DAMME 2 , STEPHAN OEHEN 3
1 Department of Microbiology, John Radcliffe Hospital, Oxford, UK
2 Centre for Evaluation of Vaccination, Department of Epidemiology, University of Antwerp, Antwerp, Belgium
3 University Hospital Zurich, Institute for Experimental Immunology, Zurich, Switzerland Продолжительный иммунитет к НВV-инфекции - в этом заинтересован каждый человек, врачи и медицинский персонал, занимающиеся вакцинацией, менеджеры, органы управления здравоохранением.
Продолжительный иммунитет означает, что в популяции будет поддерживаться иммунная защита от инфекции на достаточно высоком уровне, а также отпадет необходимость в проведении каких-либо промежуточных бустерных вакцинаций. В результате снижения заболеваемости и смертности от HBV-инфекции, снижения расходов на лечение заболевания и, конечно, снижения стоимости бустерных вакцинаций значительно возрастает экономическая выгода, связанная с существованием длительного иммунитета к инфекции.
Благодаря тому, что общедоступными становятся результаты долговременных исследований эффективности НВ-вакцин, а также накапливаются данные о взаимосвязи между иммуногенными свойствами вакцины, клеточным иммунитетом и иммунологической памятью, появилась возможность идентифицировать факторы, которые влияют на формирование иммунологической памяти к HBV-инфекции.
Иммуногенность первичной вакцинации позволяет прогнозировать и первичный и вторичный, анамнестический, ответ на НВ. Возможно, это имеет отношение и к иммунологической памяти и, как следствие, эффективности долговременной защиты от инфекции. Таким образом, напрашивается вывод, что использование высокоиммуногенных НВ вакцин создаст оптимальные условия для полноценного формирования иммунологической памяти и продолжительного иммунитета к HBV-инфекции.
Положение с НВ-вакцинацией в настоящее время
Финансовые проблемы заметно ограничивают использование НВ-вакцин. Несмотря на то, что снижение цены на НВ-вакцину в развивающихся странах с 20 USD до 3,0-5,0 USD за одну дозу сделало возможным массовое использование этой вакцины в детских иммунизационных программах, она по-прежнему остается дороже большинства других вакцин. В настоящее время во многих странах рекомендуется проводить периодические бустерные вакцинации даже иммунокомпетентных лиц, кроме того, бустерные дозы предусмотрены для иммунокопромитированных субъектов в случае снижения титра антител против поверхностного антигена HBV (анти-HBs) ниже 10 mlU/ml. Однако результаты научных исследований не подтверждают необходимости рутинной бустерной вакцинации для поддержания долговременной иммунологической защиты в этих популяциях. Как следствие были предложены новые рекомендации, суммированные в таблице 1. Они ограничивают круг лиц, нуждающихся в бустерной НВ-вакцинации, до иммунокомпромитированных групп риска, таких как пациенты, которым проводится гемодиализ, страдающие хронической почечной недостаточностью или заболеваниями печени и ВИЧ-позитивные субъекты. Повсеместное распространение новой концепции приведет к существенной экономии средств и в развитых, и, что наиболее важно, в развивающихся странах. Однако наряду с признанием отсутствия необходимости в бустерной вакцинации важно учитывать и те соображения, которые позволят оптимизировать первичный курс вакцинации.
Существуют также данные о возможности снижения числа доз первичного курса иммунизации с трех до двух без какого-либо ослабления эффективности НВ вакцинации. Такое сокращение количества доз, наряду с экономией, связанной с повышением доступности комбинированных вакцин, включающих НВ, окажет важнейшее влияние на расширение охвата прививками населения, необходимого для достижения цели глобального искоренения HBV-инфекции.
Медицинские работники и другие служащие с профессиональным риском заражения
Группы повышенного риска
Что означает иммунитет к HBV?
Важно провести разграничение между защитой от субклинической и клинически выраженной инфекции. Клинически выраженная инфекция, которая может быть идентифицирована путем определения HBsAg и приводящая к клиническому заболеванию, после вакцинации не наблюдалась. Так называемая скрытая, или субклиническая, инфекция приводит к сероконверсии с появлением анти-HBs (антитела к ядерному НВ-антигену), протекает с транзиторной виремией и без выраженных симптомов, а также без заболевания. У индивидуумов, которые были ранее вакцинированы, но содержание анти-HBs значительно снизилось (до неопределяемого уровня), может произойти анамнестическое повышение содержания специфических антител за период менее 4 дней с момента вирусной "атаки". В то время, когда инфекция еще ограничивается небольшим количеством гепатоцитов, быстрое образование антител В-клетками памяти позволяет предотвратить распространение вируса и пресекает инфекцию до того, как появляется риск развития хронического вирусоносительства.
Иммунный ответ при естественном заражении HBV
Течение HBV-инфекции определяется сложным взаимодействием между различными составляющими антивирусного иммунного ответа хозяина. Гуморальный иммунный ответ, в ходе которого появляются нейтрализующие антитела к поверхностному антигену HBV (HBsAg), является необходимым условием эффективного клиренса вируса. Нейтрализующие антитела синтезируются активированными В-клетками. После заражения HBV невакцинированного человека протективные антитела появляются на 50-150-й день, в то время как цитопатические вирусы вызывают более быструю ответную реакцию (6-14-й день).
Клеточный иммунный ответ играет решающую роль в клиренсе HBV из инфицированных гепатоцитов. Вплоть до недавнего времени считалось, что это происходит исключительно в результате деструкции гепатоцитов цитотоксическими Т-клетками (CTL). Однако Т-хелперные клетки-индукторы вирус-специфических CTL играют еще и другую роль, состоящую в секреции нецитотоксических цитокинов: y-интерферона (IFNg) и фактора некроза опухолей-а (TNF-а), которые способны подавлять экспрессию вирусных генов и таким образом "лечить" инфицированные клетки.
Иммунный ответ, индуцированный НВ-вакцинацией
Большинство работ в этой области характеризует иммунный ответ на HBsAg, используемый в производстве рекомбинантных НВ-вакцин. Основные рекомбинантные НВ-вакцины, которые успешно используются с момента их внедрения в 1986 году, содержат дрожжевой HBsAg. Введение вакцины приводит к презентации HBsAg по классической схеме, то есть от антиген-презентирующих клеток (АПК) - Т-хелперным лимфоцитам (CD4), которые распознают антиген в комплексе с молекулами II класса МНС на АПК. Т-хелперные клетки запускают дифференцировку HBsAg-специфических В-лимфоцитов в быстро пролиферирующие анти-HBsAg иммуноглобулин (IgG)-продуцирующие клетки. Антиген-специфические В-клетки ответственны за продукцию анти-HBs (IgG). Вслед за первичным иммунным ответом образуются В- и Т-клетки памяти, которые способствуют стремительному протеканию последующих анамнестических реакций.
Влияние антигена на формирование иммунологической памяти:
- персистенция антигена играет важную роль в образовании антител-продуцирующих В-клеток памяти и, следовательно, в поддержания протективного уровня антител;
- персистенция антигена зависит от введенной дозы и возрастает с ее увеличением;
- нереплицирующиеся антигены с наиболее высоким числом повторов индуцируют наиболее сильный В-клеточный ответ
Зависимость гуморального иммунного ответа от Т-клеток привела к появлению работ, исследующих взаимосвязь между уровнем антител и лимфопролиферацией. Эксперименты с использование спот-фермент-связанного иммуносорбентного анализа (spot-ELISA), метода определения in vitro способности циркулирующих В-лимфоцитов продуцировать анти-HBs, продемонстрировали тесную корреляцию между продукцией анти-HBs IgG in vitro и иммунологической памятью (характеризуемой частотой В-клеток памяти). Статистически достоверная корреляция также была обнаружена между кинетикой и нарастанием содержания антител in vivo и Т-клеточным иммунным ответом in vitro.
Иммунологическая память
Механистической основой иммунологической памяти являются селективная экспансия и дифференцировка клонов антиген-специфических В- и Т-лимфоцитов. В то время как В-клеточный ответ - основной фактор иммунологической памяти, общепризнанным является факт, что наличие Т-клеток способствует В-клеточной персистенции и что "память" формируется в результате сложных взаимодействий В-, Т-, CTL-клеток памяти и комплексов антиген-антитело. Формирование иммунологической памяти - ключевая особенность специфического иммунного ответа, эту функцию выполняют В- и Т-лимфоциты памяти, синтезируемые в результате первичной антигенной стимуляции. Эти клетки сохраняют способность к быстрой пролиферации, дифференцировке и, в случае В-клеток памяти, быстрой продукции специфических антител при последующей встрече с идентичным антигеном. Иммунологическая память, таким образом, может рассматриваться как адаптивный иммунный ответ на антиген, который уже знаком иммунной системе. В обычных условиях вторичный иммунный ответ подразумевает продукцию сывороточных антител в более высокой концентрации и через более короткий промежуток времени по сравнению с первичным, кроме того, синтезируемые антитела обладают более высокой связывающей способностью. Для того чтобы понять, какие факторы оказывают воздействие на вакцин-индуцированную иммунологическую память, мы должны рассмотреть следующие иммунологические механизмы.
Персистенция иммунологической памяти к HBV
В ходе испытания вакцин, а также в результате долговременных наблюдений за вакцинированными было показано, что иммунологическая память к НВ сохраняется в течение, по крайней мере, 5-12 лет.
Так как основная задача вакцинации в детском или подростковом возрасте состоит в формировании как можно более длительного иммунитета, используемая вакцина должна обладать оптимальными иммуногенными свойствами. Исследования вакцин-индуцированного иммунитета к НВ показывают, что вакцинация приводит к формированию иммунитета к инфекции и он сохраняется даже в том случае, когда антитела в крови уже не определяются. Предположение о том, что у адекватно вакцинированных лиц имеет место иммунологическое праймирование, подтверждается данными о том, что HBsAg-специфические лимфоциты памяти циркулируют в периферической крови вакцинированных людей, даже если у них к тому времени уже не обнаруживаются специфические антитела. Однако было показано, что гуморальный ответ на завершенный первичный курс вакцинации тесно коррелирует с будущей реакцией на ревакцинацию. Иммуногенность первичной вакцинации, таким образом, является ключевым фактором, определяющим силу последующего анамнестического ответа. Так как анамнестический гуморальный ответ зависит от В-клеток памяти, есть основания считать, что более сильный вторичный иммунный ответ является индикатором более мощного потенциала В-клеток памяти, который, в свою очередь, отражает иммуногенность первичного курса иммунизации.
Взаимодействие антигена, гуморального и клеточного иммунного ответа в формировании иммунологической памяти (упрощенная схема)
Исследования, в которых иммунологическая память оценивалась путем проведения бустерной вакцинации, не только демонстрируют наличие иммунологической памяти, но подтверждают последние рекомендации об отсутствии необходимости и бустерной дозы для поддержания иммунитета.
Перспективы
Дальнейшее изучение вопросов, связанных с проблемой иммунологической памяти, в будущем, несомненно, окажет влияние на политику вакцинации против HBV. Проведенные в этом направлении исследования уже позволили сделать выводы о том, что В-клетки обеспечивают существование долговременной иммунологической памяти и о синергии Т- и В-клеточных реакций, которые, безусловно, внесут свой вклад в понимание механизмов формирования долговременной иммунологической памяти. Необходимо продолжать наблюдения за группами вакцинированных против гепатита В людей, анализируя и клеточный, и гуморальный иммунитет. Также следует оценить эффект объединения НВ-вакцины с другими детскими вакцинами в комбинированных препаратах.
Существующие на сегодняшний день представления о роли первичного иммунного ответа в формировании иммунологической памяти подчеркивают важность гарантии полноценного иммунного ответа на первичный курс вакцинации. Это тем более важно в плане снижения количества доз вводимой вакцины.
В настоящее время вакцинопрофилактика вирусного гепатита В является основным методом борьбы с этой инфекцией. С момента начала широкомасштабной кампании вакцинации против гепатита В во многих странах мира прошло не так много времени (6-12 лет), поэтому многие проблемы, связанные с напряженностью и длительностью иммунного ответа на введение вакцины, остаются пока нерешенными. Крайне важно их решение не только для определения тактики и стратегии вакцинопрофилактики гепатита В, но и развития фундаментальной иммунологии. Так, до сих пор, окончательно не принято решение о необходимости и кратности ревакцинации против этой инфекции. В настоящее время Комитетом по профилактике вирусного гепатита В Европейского бюро ВОЗ проведение ревакцинации не рекомендовано. Введение бустерных доз вакцины считается оправданным только для иммунокомпрометированных пациентов (лиц находящихся на гемодиализе, носителей ВИЧ, больных хронической почечной и печеночной недостаточностью) [1]. Введение дополнительных доз вакцины против гепатита В (в рамках первичного курса вакцинации) показано только тогда, когда концентрация антител к HBs-антигену у пациента не достигла защитного уровня (10 МЕ/л). В таких случаях вводят дополнительные дозы вакцинного препарата с интервалом в три месяца, с последующим серологическим контролем [1].
Специфический иммунный ответ на вирус гепатита В имеет особенности, которые характерны не cтолько для иммунопротективной, сколько для иммунопатологической защитной реакции. Это обусловлено тем, что вирус гепатита В относится к инфекционным агентам, не обладающим прямым цитопатическим действием. При инфекции такими вирусами цитолиз инфицированных клеток осуществляют цитотоксические Т-лимфоциты. Иммунная реакция развивается постепенно, с поздним (50-150 день после заражения) накоплением антител к HBs-антигену. Для сравнения, антитела к вирусам с цитопатическим действием вырабатываются на 6-14 день после заражения. Обязательным условием эффективности иммунопатологических механизмов защиты является минимально необходимая интенсивность иммунного ответа, в частности реакции Т-клеток. Это соответствует общим закономерностям иммуногенеза вирусных инфекций, возбудители которых, как и вирус гепатита В, лишены прямого цитопатического действия. При инфекции такими вирусами существует комплексное взаимодействие между различными компонентами гуморального и клеточного иммунного ответа организма.
Безусловно, гуморальный иммунный ответ, при котором образуются вируснейтрализующие антитела к HBs-антигену (продукты активированных В-лимфоцитов), необходим для выведения вируса из организма. Клеточный иммунный ответ только частично важен для выведения вируса гепатита В из инфицированных гепатоцитов. До недавнего времени считалось, что в этом процессе участвуют только цитотоксические Т-лимфоциты, разрушающие зараженные вирусом гепатоциты. Однако показано, что вирусоспецифические цитотоксические Т-лимфоциты, индуцированные Т-хелперами, могут играть и другую роль, а именно: подавлять экспрессию вирусных генов, секретируя нецитотоксические цитокины (g-интерферон и фактор некроза опухоли) и таким образом освобождать клетки от вируса. При этом, относительно небольшое количество цитотоксических лимфоцитов способно элиминировать вирус из большого числа гепатоцитов без их разрушения [2].
Еще одним важным фактором, влияющим на продолжительность иммунной памяти к антигенам вируса гепатита В, является количество циркулирующих (в момент первичной вакцинации) комплексов антиген-антитело, которое прямо зависит от количества антигена, вводимого при вакцинации. Персистирующие на клетках ретикулоэндотелиальной системы комплексы стимулируют пролонгированную пролиферацию В-лимфоцитов и, следовательно, постоянную продукцию антител. Таким образом, вакцины с более высоким содержанием HBs-антигена, имеют преимущество не только по иммуногенности, но и по длительности сохранения формируемого ими иммунитета. Очень большое значение для формирования иммунной памяти при вакцинации имеет и природа антигена. Известно, что живые вакцины в отличие от убитых или белковых препаратов дают более продолжительный иммунный ответ. Однако, недавние исследования показали, что такие жесткие и многократно повторяющиеся белковые структуры, к которым относится используемый в современных субъединичных вакцинных препаратах рекомбинантный HBs-антиген из неинфекционных частиц, индуцируют сильный В-клеточный ответ независимый от Т-лимфоцитов. Таким образом, сила и длительность иммунного ответа при вакцинации против гепатита В зависит от комплекса взаимодействий Т- и В-клеток памяти, комплексов антиген-антитело, дозы и природы вводимого антигена.
В настоящее время является подтвержденным сохранение иммунной памяти после вакцинации против вирусного гепатита В в течение по крайней мере 12 лет [4]. Однако, учитывая тот факт, что первые рекомбинантные вакцины против этой инфекции стали широко доступны только 14 лет назад, этот показатель вряд ли можно считать окончательным и потребуются дополнительные наблюдения для того, чтобы оценить предельные значения длительности иммунитета после вакцинации. Дальнейшее изучение взаимодействия между Т- и В-клеточным ответом поможет понять механизм развития длительной иммунной памяти и позволит в дальнейшем совершенствовать тактику и стратегию вакцинации против гепатита В.
Вирусные гепатиты В и С, антропонозные инфекции с заражением через поврежденные кожные покровы и слизистые оболочки, относятся к числу повсеместно распространенных болезней и по праву занимают одно из ведущих мест в инфекционной патологии человека. Эти инфекции характеризуются тяжелым клиническим течением, являясь частой причиной хронического гепатита, цирроза и первичного рака печени.
Этиология. Возбудитель гепатита В - ДНК-содержащий вирус (HBV) из группы Hepadnaviridae. Известны 3 вирусоспецифических антигена HBV: один из них входит в состав оболочки - поверхностный антиген (HBsAg), 2 других - внутренние (HBeAg и HBcAg). HBcAg (сердцевинный антиген) играет важную роль в репликации вируса и при инфекционном процессе выявляется только в ядрах гепатоцитов. HBeAg обнаруживается не только в "сердцевине" вируса, но и циркулирует в крови в свободном виде или в соединении с иммуноглобулином. Его определяют как антиген инфекционности. HBsAg (поверхностный антиген) свидетельствует о длительной персистенции вируса в организме и характеризуется относительно низкой иммуногенностью, термостабильностью и устойчивостью к протеазам и детергентам. Известно несколько подтипов HBsAg, отличающихся субдетерминантами: adw, adr, ayw, ayr. Общей антигенной детерминантой является а-детерминанта, поэтому поствакцинальный иммунитет является протективным по отношению к любому субтипу вируса. В России регистрируются, в основном, субтипы ayw и adw. Клинические проявления болезни не зависят от субтипа вируса. HBV чрезвычайно устойчив во внешней среде (в цельной крови и ее препаратах сохраняется годами). Антиген обнаруживают на постельных принадлежностях, медицинских и стоматологических инструментах, иглах, загрязненных кровью, в течение нескольких месяцев при комнатной температуре.
Вирус гепатита С (HCV) отнесен к РНК-содержащим вирусам семейства Flaviviridae. Он обладает способностью к длительной персистенции в организме, что обуславливает высокий уровень хронизации инфекции (50-80%). HCV при размножении образует квазиштаммы, иммунологически различающиеся антигенные варианты, которые обладают значительными возможностями адаптации и избегают иммунного надзора. Известно 6 основных генотипов и более чем 90 субтипов вируса. Инфекции, вызванные генотипом 1b, характеризуются более тяжелым течением заболевания, более высоким содержанием РНК HCV в сыворотке крови, худшим ответом на лечение противовирусными препаратами и большей вероятностью рецидива болезни.
Естественная восприимчивость населения - всеобщая и в большой степени определяется инфицирующей дозой. Постинфекционный иммунитет при гепатите В длительный, возможно пожизненный. Повторные случаи заболевания наблюдаются исключительно редко. При гепатите С постинфекционный иммунитет мало изучен. В экспериментах на обезьянах показана возможность повторного заболевания.
Механизм передачи. Выделение вируса с различными биологическими секретами (кровь, слюна, моча, желчь, слезы, грудное молоко, сперма и др.) определяет множественность путей передачи инфекции. Однако только кровь, сперма и, возможно, слюна представляют реальную эпидемиологическую опасность, так как в других жидкостях концентрация вируса очень мала. Заболевание передается, главным образом, парентеральным путем при переливаниях крови и кровезаменителей, при использовании медицинских инструментов после недостаточно эффективной стерилизации. Удельный вес посттрансфузионного гепатита В и С в последние годы значительно уменьшился. Сохраняющийся минимальный риск связан, главным образом, с возможным наличием у донора острого периода инфекции, который не диагностируется с помощью экспресс-методов обнаружения антител к вирусу гепатита С (anti-HCV). В то же время риск передачи ВГС с единичной случайной инъекцией, выполненной медицинским персоналом, незначителен, что объясняется низкой концентрацией вируса в небольших объемах крови.
К группам повышенного риска относятся больные, многократно получающие кровь и ее препараты (например, препараты факторов свертывания, плазма, альбумин, иммуноглобулины и т.д.), а также лица, имеющие в анамнезе массивные медицинские вмешательства, пересадку органов от доноров с ВГС-положительной реакцией и многократные парентеральные манипуляции, особенно при повторном использовании нестерильных шприцев и игл. Распространенность вирусного гепатита С среди наркоманов очень высока - 70-90%. Этот путь передачи представляет собой наибольшую опасность в распространении ВГС.
Из естественных механизмов передачи реализуется контактный (половой) путь, а также передача посредством контаминированных вирусом различных предметов обихода (бритвы, зубные щетки, полотенца и т.д.), при проникновении возбудителя в организм при микротравмах кожи и слизистых оболочек. Заражение происходит также в результате нанесения татуировки, прокола мочек ушей и при других парентеральных манипуляциях. Возможна также и вертикальная передача возбудителя. Обычно заражение происходит во время родов. Опасность передачи гепатита В возрастает в десятки раз при наличии у женщины не только HBsAg, но и HBeAg. Если не проводят специальных профилактических мероприятий, вирусным гепатитом В инфицируется до 90% детей, родившихся от матерей-вирусоносителей. Роль половых контактов в передаче ВГС незначительна и составляет около 5-10%, в то время, как при гепатите В - 30-35%.
В России наблюдается устойчивая тенденция к росту заболеваемости гепатитом В - от 17,9 на 100 тыс. населения в 1991 г. до 43,5 в 1999 г. (42,1 в 2000 г.), что значительно отличается от такового во многих странах Западной Европы и США (в которых в эти годы регистрировали всего 1-4 случая ОГВ на 100 тыс. жителей). На многих административных территориях показатели заболеваемости превышают среднефедеративный в 1,5-2,5 раза (Иркутская обл., Таймырский автономный округ, Москва и др.). Наряду с ростом заболеваемости из года в год увеличивается число выявленных носителей вируса ГВ.
Гепатит С является одной из основных причин развития хронических диффузных заболеваний печени и гепатоцеллюлярной карциномы (первичного рака печени). Отличительной особенностью ВГС является многолетнее латентное или малосимптомное течение по типу так называемой медленной вирусной инфекции. В таких случаях заболевание большей частью долго остается нераспознанным и диагностируется на далеко зашедших клинических стадиях, в том числе на фоне развития цирроза печени и первичной гепатоцеллюлярной карциномы. По данным ВОЗ в конце 90-х годов вирусом гепатита С инфицировано около 1% населения мира. В Европе и Северной Америке распространенность инфекции составляет 0,5-2,0%, в ряде регионов Африки она составляет 4% и выше. В России заболеваемость гепатитом С продолжает расти (в 1999 г. -16,7, а в 2000 г. - 19,0 на 100 тыс. населения, носительство возбудителя составило соответственно 83,3 и 95,9). Самый высокий уровень заболеваемости ВГС отмечается в Санкт-Петербурге, Тюменской области и др. С момента начала регистрации в Москве отмечается неуклонный рост заболеваемости населения вирусным гепатитом С. За последние 5 лет показатель возрос более чем в 15 раз.
В эпидемический процесс гепатита В и С интенсивно вовлекается молодое трудоспособное население: среди заболевших преобладают лица в возрасте от 15 до 30 лет, на долю которых приходится около 90% заболевших. Такой возрастной состав заболевших гепатитом обусловлен тем, что в структуре путей инфицирования доминирует "наркозависимый" и половой пути передачи инфекции. Молодые люди в возрасте до 30 лет, употреблявшие наркотики, составляют (по данным формы Госстатучета №2) 80% умерших от гепатита В. Значительная часть летальных исходов (до 42%) обусловлена одновременным инфицированием HBV, HCV и HDV. Сегодня у нас в стране проблема парентеральных гепатитов из медицинской превращается в социальную.
Профилактические мероприятия. В комплексе профилактических мероприятий первостепенное значение имеют меры, направленные на предупреждение заражений при переливаниях крови и проведении лечебно-диагностических парентеральных манипуляций. Все доноры подвергаются комплексному клинико-лабораторному обследованию на наличие маркеров гепатита В и С. В России с 1994 г. введена обязательная регистрация всех случаев ВГС. С этого же периода начато обязательное обследование доноров на анти-HCV, что явилось серьезным шагом на пути снижения заболеваемости посттрансфузионным гепатитом С. От донорства отстраняются лица, перенесшие вирусный гепатит В, независимо от срока давности, а также контактировавшие с больными в течение последних 6 мес. К сдаче крови не допускаются лица, страдающие хроническим гепатитом (в том числе неясной этиологии) и подвергшиеся за последние годы гемотрансфузии. Перспективным является внедрение аутогемотрансфузий, когда больному переливают его же кровь, заготовленную до плановой операции. Неспецифическая профилактика парентеральных гепатитов достигается применением одноразовых инструментов при манипуляциях, связанных с повреждением кожных покровов и слизистых, тщательной стерилизацией медицинского инструментария, а также жесткого контроля по обнаружению вирусных антигенов у доноров. Первостепенное значение имеет повсеместное внедрение и улучшение централизованной стерилизации изделий медицинского назначения. Прерывание естественных путей передачи вируса ГВ и ГС обеспечивается санитарно-гигиеническими мерами: индивидуализация всех предметов личной гигиены и раздельное их хранение (бритвенные приборы, зубные щетки, мочалки, расчески и др.), выполнение правил личной гигиены, предупреждение микротравм в быту и на производстве. Профилактика полового пути передачи инфекции предусматривает необходимость избегать случайных половых связей и использовать механические контрацептивные средства. Предупреждение профессиональных заражений в лечебно-профилактических учреждениях достигается неукоснительным соблюдением правил противоэпидемического режима, особенно в гемодиализных, хирургических, лабораторных и других отделениях, в которых персонал часто имеет контакт с кровью. При выполнении любых парентеральных вмешательств и процедур обязательно использование резиновых перчаток.
Учитывая многообразие путей передачи вируса гепатита В и большое число источников инфекции, наиболее перспективным средством профилактики этого заболевания является вакцинация. Именно она является единственным средством профилактики гепатита В у новорожденных. Это первая вакцина, которая предотвращает раковое заболевание печени. Более 75 стран включили в свои программы вакцинации рутинную иммунизацию против гепатита В новорожденных и/или подростков. В настоящее время во многих странах Европы и Америки проводят сочетанную вакцинацию против гепатита В в рамках расширенной программы иммунизации детей. Вакцинация против гепатита В в России введена в национальный календарь профилактических прививок. Специфическая профилактика гепатита В осуществляется с помощью использования одной из вакцин, разрешенных к применению в Российской Федерации. К ним относятся вакцины HBVax-II (США), Engerix-В (Бельгия), Rec-HBsAg (Куба), Эувакс В (Южная Корея), Комбиотех (Россия) и Шанвак Б (Индия).
Вакцинации подлежат также медицинские работники из групп высокого риска заражения вирусным гепатитом В, выпускники медицинских ВУЗов и техникумов; новорожденные, родившиеся от матерей-носителей HBs-антигена и женщин, переболевших гепатитом В в III триместре беременности; дети и персонал детских домов и специнтернатов, пациенты, находящиеся в отделениях с высоким риском заражения гепатитом В, а также лица, соприкасавшиеся с больными гепатитом В в очагах заболевания по месту жительства.
В настоящее время предполагается, что длительность поствакцинального иммунитета составляет примерно 15 лет. Накопленный опыт свидетельствует, что проведение вакцинации приводит к снижению заболеваемости в 10-12 раз и носительства HBsAg в популяции с 9-12% до 1%.
К сожалению, в виду недостаточного финансирования закупок вакцин прививки в стране проводятся в крайне низких объемах. В 1998 г. в России против вирусного гепатита В были привиты 323 702 человека в 65 административных территориях. Среди медицинских работников привито всего лишь около 10%. Еще меньше охват прививками студентов медицинских вузов и училищ. В тех местах, где проводилась вакцинация медиков, произошло заметное снижение заболеваемости гепатитом В среди этого контингента. Различия в заболеваемости медицинских работников и совокупного населения г. Москвы составили в последние годы 4-5 раз. Наиболее существенное снижение заболеваемости произошло среди хирургов и анестезиологов-реаниматологов.
Более половины всех случаев заболеваний ГB среди медицинских работников приходится на первые 5 лет от начала работы, а основная их часть - при стаже от 1 до 5 лет. Это свидетельствует о необходимости обязательной вакцинации против гепатита В медработников до начала их профессиональной деятельности.
Однако иммунизация только групп риска (медицинские работники, имеющие "кровяные контакты", новорожденные от носителей и больных, персонал и дети домов ребенка) не обеспечивает эффективного снижения заболеваемости. Активно повлиять на эпидемический процесс и добиться существенного снижения заболеваемости гепатитом В возможно лишь перейдя от вакцинации лиц, составляющих "группы риска", к иммунизации всех подростков и новорожденных детей. Следует отметить приоритетность этой инфекции и с точки зрения ее экономической значимости, определяемой сочетанием очень высокой "стоимости" одного острого случая заболевания (уступающей только полиомиелиту и столбняку) и широкого и все возрастающего распространения среди населения.
Создание ВГС-вакцины затрудняется наличием большого количества геномных подтипов (более 90) и мутантных разновидностей ВГС, а также кратковременностью эффекта нейтрализующих антител.
В осуществлении эпидемиоло-гического надзора важное значение имеет определение удельного веса гепатитов В и С среди всех гепатитов, регистрация и учет хронических форм болезни. Анализ заболеваемости должен проводиться с учетом активности действия тех или иных путей заражения, определяющих социально-возрастную структуру заболевших. Осуществление оценки эпидемиологической эффективности вакцинации против гепатита B и других мер профилактики против гепатита C среди различных групп населения, их социально-экономической значимости обеспечивает снижение заболеваемости гепатитами B и C.
Читайте также:

