Сыпь при противовирусной терапии
Обновлено: 25.04.2024
19.05.2020 Владимир Адаскевич, заведующий кафедрой дерматовенерологии ВГМУ, председатель Белорусской общественной организации дерматовенерологов и косметологов, профессор, д.м.н. 07.09.2020 !-->
В конце марта 2020 года итальянский врач прислал письмо редактору журнала Европейской академии дерматологии и венерологии с описанием состояний кожи, наблюдаемых у 20 % из 88 пациентов с COVID-19 в Ломбардии — наиболее пострадавшем от заболевания регионе Италии. У большинства развивалась красная сыпь на туловище, у некоторых появлялись высыпания по типу крапивницы или пузырьки, напоминающие ветряную оспу.
В начале апреля французское дерматологическое общество, включающее более 400 специалистов, опубликовало заявление, что у пациентов с вероятным COVID-19 отмечались крапивница, красная сыпь и очаги на конечностях, напоминающие картину обморожений. И наконец, в середине апреля поступило письмо редактору журнала Американской академии дерматологии от группы итальянских врачей с описанием высыпаний по типу ветряной оспы как редкого, но специфически ассоциированного с COVID-19 проявления. Однако затруднительно определить, действительно ли эти кожные симптомы вызваны вирусом SARS-CoV-2 или являются побочным эффектом применяемых для лечения вируса лекарственных средств.
Понятно, что у пациентов с подтвержденным COVID-19 проявления на коже не являются главной проблемой, но оказание дерматологической помощи необходимо для облегчения дискомфорта. В таких случаях специалисты применяют типичную местную терапию. Но некоторые предварительные исследования показывают, что у пациентов с COVID-19 высыпания могут развиваться из-за нарушения кровотока, что уже более серьезно: небольшие сгустки крови в коже могут говорить о наличии подобных в других участках организма.
Китайские исследователи, исходя из данных о 140 пациентах, инфицированных новым коронавирусом, идентифицировали в качестве кожных проявлений лекарственную гиперчувствительность у 11,4 % и крапивницу у 1,4 % больных.
Британские врачи описали первый случай нового воспалительного состояния по типу болезни Кавасаки у 6-месячного ребенка с симптомами, включавшими лихорадку, стойкую красную сыпь на руках и ногах; сухие потрескавшиеся губы, бугорки на языке, отекшие кисти, конъюнктивит. Проведенный тест на коронавирусную инфекцию оказался положительным.
Синдром, похожий на болезнь Кавасаки, предположительно вызванный COVID-19, стал причиной смерти 12 детей в Великобритании. Однако некоторые исследователи не уверены в связи данных летальных исходов с коронавирусной инфекцией.
Пока еще неизвестно, могут ли очаги на коже и нарушение кожного барьера способствовать передаче SARS-CoV-2 при непрямом контакте. Предстоит определить, ассоциируются ли с коронавирусной инфекцией специфические очаги на слизистых и коже, хотя некоторые неопубликованные наблюдения указывают на случаи транзиторной оспенноподобной экзантемы в ранней фазе заболевания.
Экспертная оценка данных приведенного ниже исследования опубликована в конце апреля в Британском журнале дерматологии. Испанские специалисты описали кожные высыпания, которые они наблюдали у 375 больных коронавирусной инфекцией в течение 2 недель. Выявлено 5 разновидностей сыпи: акральные участки эритемы-отека с везикулами или пустулами (псевдообморожение) (19 % случаев); другие везикулезные высыпания (9 %); уртикарные очаги (19 %); другие макулопапулы (47 %); ливедо или некроз (6 %).
- Акральные участки эритемы-отека с везикулами или пустулами (псевдообморожение). Эти очаги, поражающие кисти и стопы, могут напоминать обморожения (небольшие зудящие отечности на коже) с мелкими красными или лиловыми пятнышками, вызванными подкожными кровоизлияниями. Высыпания обычно асимметричные. Они ассоциируются с молодыми пациентами, длятся в среднем 12,7 дня, развиваются в позднем течении COVID-19 и наблюдаются при менее тяжелом заболевании. Высыпания иногда вызывают боль (32 %) или зуд (30 %).
- Другие везикулезные высыпания. Проявлялись внезапным развитием пузырьков на туловище, которые могли также поражать конечности. Пузырьки иногда были наполнены кровью и становились более крупными или распространенными. Они ассоциируются с пациентами среднего возраста, длятся в среднем 10,4 дня, чаще появляются (15 %) до возникновения других симптомов и наблюдаются при средней тяжести заболевания. Зуд частый (68 %).
- Уртикарные очаги. Представляют собой розовые или белые припухлости кожи, напоминающие обычно зудящие волдыри при крапивнице. Высыпания в основном развивались на туловище или распространялись по всему телу. В нескольких случаях наблюдались на ладонях.
- Другие макулопапулы. Маленькие, плоские и приподнятые красные выпуклости. В некоторых случаях располагались вокруг волосяных фолликулов, отмечалась также разная степень шелушения. Некоторые из элементов описывались похожими на розовый лишай. Пятнышки крови под кожей также могут присутствовать либо в форме крапинок/точек, либо более крупных участков. Такие высыпания ассоциируются с меньшей продолжительностью (6,8 дня в среднем для уртикарных очагов и 8,6 для макулопапулезных), обычно появляются вместе с другими симптомами и наблюдаются при более тяжелом течении COVID-19 (2 % смертность в выборке). Зуд очень частый при уртикарных очагах (92 %), при макулопапулезных отмечается в 57 % случаев.
- Ливедо или некроз. Ливедо является результатом нарушения циркуляции в кровеносных сосудах кожи, отчего на поверхности появляется сосудистый рисунок в форме красной или синей сетки. Некроз означает преждевременную гибель кожной ткани. Эти два симптома отражают разную степень окклюзии сосудов с сужением или блокировкой артерий, ограничивающих кровоток в отдельных участках тела (в данном случае на туловище или конечностях). Такие высыпания ассоциируются с пожилыми пациентами и более тяжелым течением болезни (смертность 10 %). Однако данные проявления COVID-19 более вариабельны, включая транзиторное ливедо у пациентов, которым не требовалась госпитализация.

Исследователи обратили внимание, что некоторые из кожных проявлений, ассоциированных с COVID-19, являются распространенными и могут иметь много причин. Это касается, в частности, макулопапул и уртикарных очагов. Сами по себе они не помогают в постановке диагноза. Ливедо и некроз, с другой стороны, достаточно редки, и чаще всего они появлялись у пожилых и тяжелых пациентов. Однако трудно сказать, вызваны ли они непосредственно COVID-19 или являются индикатором осложнений.
Группа дерматологов в Нью-Йорке изучает связь между COVID-19 и уже имеющимися воспалительными кожными заболеваниями, такими как экзема и псориаз. Для этого в медицинской школе Icahn госпиталя Mount Sinai набирают профильных пациентов, проходящих лечение, в надежде изучить, насколько они восприимчивы к COVID-19 по сравнению с другими. А поскольку многие лекарства, применяемые у данной категории, нацелены на снижение воспаления в организме, врачи предполагают, что эти препараты могут также улучшать способность иммунной системы бороться с SARS-CoV-2. Результаты исследования из Mount Sinai и все данные о дерматологических реакциях на COVID-19 пока предварительные. Американские дерматологи предлагают пациентам с необычными кожными высыпаниями воспользоваться возможностями телемедицины для консультации со специалистом, который поможет выяснить, связаны ли эти проявления с COVID-19, и обосновать причину для самоизоляции.
Важным является заявление Европейской целевой группы по атопическому дерматиту (ETFAD). Пациенты с тяжелым течением атопического дерматита часто получают иммуномодулирующие системные препараты, которые влияют также на тяжесть коморбидной патологии (бронхиальная астма, ХОБЛ, эозинофильный эзофагит, болезни почек и аллергии).
Резкое прекращение стабильной системной терапии может привести к обострению всех указанных заболеваний. Если же ее нужно приостановить, пациенты должны быть обеспечены достаточной местной терапией вкупе с рекомендациями по объему, необходимому для предотвращения обострений, до возобновления системного лечения. Вместе с тем требуется мониторинг и лечение таких коморбидных состояний, как бронхиальная астма. При тяжелом и осложненном течении нужна госпитализация в специализированный лечебный центр.
Тяжелый и нелеченый атопический дерматит известен как фактор риска диссеминированного вирусного кожного заболевания. С другой стороны, многие традиционные системные иммуномодулирующие препараты, такие как циклоспорин, могут взаимодействовать с защитными механизмами организма против вирусной инфекции. Пока еще неизвестно, как SARS-CoV-2 влияет на пациентов с атопическим дерматитом, в том числе получающих иммуномодулирующую терапию.
Диссеминированная кожная вирусная инфекция (герпетическая экзема, опоясывающий лишай или сезонный назофарингит), наблюдаемая при атопическом дерматите, может служить потенциальной моделью для оценки лечения COVID-19 у пациентов, получающих системную терапию. Но выводы в этом случае очень ограничены. Считается, что целевая терапия, селективно воздействующая на воспаление 2-го типа, в частности, применение биологических препаратов, не повышает риски вирусных инфекций и в условиях пандемии может быть предпочтительнее традиционных иммуносупрессивных препаратов.
В повседневной практике педиатру часто приходится сталкиваться с различными изменениями на коже пациентов. По статистике, различные поражения кожи являются причиной почти 30% всех обращений к педиатру. Иногда это только дерматологические проблемы, иногда высыпания являются проявлениями аллергической или соматической патологии, но в последнее время существенно вырос процент дерматологических проявлений инфекционных заболеваний. Иными словами, синдром инфекционной экзантемы прочно входит в нашу практику и требует определенной осведомленности, так как порой он является одним из главных диагностических признаков, позволяющих своевременно поставить диагноз и избежать тяжелых последствий.
Экзантемы являются одним из наиболее ярких и значимых в диагностическом и дифференциально-диагностическом отношении симптомов. Они встречаются при многих инфекционных заболеваниях, которые даже получили название экзантематозных (корь, краснуха, скарлатина, брюшной и сыпной тифы, ветряная оспа, герпетические инфекции). При них сыпь - обязательный компонент клинической картины заболевания, вокруг нее как бы разворачивается диагностический процесс, на нее опирается и дифференциальный диагноз. Существует также группа инфекций, при которых сыпь встречается, но она непостоянна и эфемерна. Такого рода экзантемы возможны при многих вирусных инфекциях (энтеро- и аденовирусных, ЦМВ, ЭБВ и др.). В этих случаях диагностическая ценность экзантем невелика.
Экзантема почти всегда сосуществует с энантемой, причем последняя обычно появляется за несколько часов или 1-2 дня до экзантемы. Например, обнаружение розеол или петехий на небе у больного с симптомами ОРВИ позволит доктору заподозрить герпетическую инфекцию, сыпной тиф или лептоспироз, а пятна Филатова - Коплика являются единственным по-настоящему патогномоничным симптомом кори. Это лишний раз доказывает чрезвычайную важность тщательного осмотра не только кожи, но и слизистых оболочек.
Единой классификации инфекционных экзантем в настоящее время не существует. Наиболее удобно их разделять на генерализованные и локализованные. Классическими называют экзантемы потому, что заболевания, относящиеся к данной группе, всегда протекают с синдромом экзантемы. Атипичные же заболевания сопровождаются высыпаниями часто, но не всегда (рис. 1, 2).
В статье речь пойдет о генерализованных вирусных атипичных экзантемах.
Рис. 1. Классификация экзантем
Рис. 2. Генерализованные экзантемы
Экзантема при парвовирусной инфекции постепенно исчезает в течение 5-9 дней, но при воздействии провоцирующих факторов, таких как солнечное облучение, горячая ванна, холод, физическая нагрузка и стресс, могут персистировать недели и даже месяцы. Исчезает сыпь бесследно.
У части больных на фоне сыпи или после ее исчезновения может отмечаться поражение суставов. Характерно симметричное поражение преимущественно коленных, голеностопных, межфаланговых, пястно-фаланговых суставов. Болевой синдром зависит от тяжести заболевания и может быть слабым или сильным, затрудняющим самостоятельное передвижение, суставы опухшие, болезненные, горячие на ощупь. Течение полиартритов доброкачественное.
В анализе крови в высыпной период выявляется легкая анемия, низкое содержание ретикулоцитов, в ряде случаев - нейтропения, тромбоцитопения, повышенная СОЭ [6]. Для более точной диагностики возможно использовать ПЦР (сыворотка, ликвор, пунктат костного мозга, биоптат кожи и т. д.) для определения ДНК парвовируса. Также применяется метод ИФА с определением в сыворотке крови уровня специфических антител: IgM в сыворотке крови пациента обнаруживаются одновременно с появлением симптомов заболевания (на 12-14-й день после заражения), их уровень достигает максимума на 30-й день, затем снижается в течение 2-3 месяцев. Через 5-7 дней от момента клинических проявлений парвовирусной инфекции появляются IgG, которые сохраняются в течение нескольких лет [7].
Специфической этиотропной терапии парвовирусной инфекции не существует. В зависимости от клинической формы проводится посиндромная терапия.
Внезапная экзантема
Внезапная экзантема (син.: розеола детская, шестая болезнь) - это острая детская инфекция, вызывающаяся вирусом герпеса 6-го типа, реже 7-го типа и сопровождающаяся пятнисто-папулезной экзантемой, возникающей после снижения температуры тела. Вирус герпеса типа 6 был впервые выделен и идентифицирован в 1986 году у больных с лимфопролиферативными заболеваниями, а в 1988 году было доказано, что данный тип вируса является этиологическим агентом внезапной экзантемы. Инфекция, вызванная вирусом герпеса человека типа 6, является актуальной проблемой современной педиатрии, что связано с ее широкой распространенностью: почти все дети инфицируются в возрасте до 3 лет и сохраняют иммунитет на всю жизнь [8, 9]. При данном заболевании четко выражена сезонность - чаще внезапная экзантема регистрируется весной и осенью.
После снижения температуры тела, реже за день до или через сутки после, появляется экзантема. Высыпания вначале появляются на туловище и затем уже распространяются на шею, верхние и нижние конечности, редко - лицо. Представлены округлыми пятнами и папулами до 2-5 мм в диаметре, розового цвета, окруженными белым венчиком, бледнеющими при надавливании. Элементы сыпи редко сливаются и не сопровождаются зудом. Продолжительность высыпаний - от нескольких часов до 3-5 дней, после чего они исчезают бесследно [10, 11]. Особенностью заболевания является то, что, несмотря на болезнь, самочувствие ребенка страдает не сильно, может сохраняться аппетит и активность. В клиническом анализе крови отмечаются лейкопения и нейтропения, лимфоцитоз, могут обнаруживаться атипичные мононуклеары и тромбоцитопения. Течение внезапной экзантемы доброкачественное, склонное к саморазрешению.
Заболевание склонно к саморазрешению и в подавляющем большинстве случаев не требует специфического лечения.
Инфекционный мононуклеоз
Инфекционный мононуклеоз - это острое инфекционное заболевание, вызываемое вирусами группы герпесов, наиболее часто ЭБВ, и характеризующееся лихорадочным состоянием, ангиной, увеличением лимфатических узлов, печени и селезенки, лимфоцитозом, появлением атипичных мононуклеаров в периферической крови [13].
ЭБВ повсеместно распространен среди человеческой популяции, им поражено 80-100% населения земного шара [14, 15]. Большинство детей инфицируется к 3 годам, а все население - к совершеннолетию. Максимальная заболеваемость отмечается в 4-6 лет и подростковом возрасте. Выражена сезонность -с весенним пиком и незначительным подъемом в октябре. Характерны подъемы заболеваемости каждые 6-7 лет.
Инкубационный период составляет от 2 недель до 2 месяцев. Основной симптомокомплекс включает следующие ведущие симптомы:
Заболевание в большинстве случаев начинается остро, с подъема температуры тела до высоких цифр. Обычно весь симптомокомплекс разворачивается к концу первой недели. Наиболее ранними клиническими проявлениями являются: повышение температуры тела; припухание шейных лимфатических узлов; наложения на миндалинах; затруднение носового дыхания. К концу первой недели от начала заболевания у большинства больных уже пальпируются увеличенная печень и селезенка, в крови появляются атипичные мононуклеары.
Помимо основного симптомокомплекса, при инфекционном мононуклеозе часто отмечаются различные изменения кожи и слизистых оболочек, появляющиеся в разгар заболевания и не связанные с приемом лекарственных препаратов. Практически постоянным симптомом является одутловатость лица и отечность век, что связано с лимфостазом, возникающем при поражении носоглотки и лимфатических узлов. Также нередко на слизистой оболочке полости рта появляются энантема и петехии. В разгар заболевания часто наблюдаются различные высыпания на коже. Сыпь может быть точечной (скарлатиноподобной), пятнисто-папулезной (кореподобной), уртикарной, геморрагической. Сыпь появляется на 3-14-й день заболевания, может держаться до 10 дней и разрешается бесследно. Отличительной чертой является ее большая интенсивность на акральных участках, где она обычно сливается и дольше держится. Экзантема не зудит и проходит бесследно.
Нельзя не упомянуть еще об одном очень характерном проявлении инфекционного мононуклеоза - появлении сыпи после назначения антибиотиков пенициллинового ряда [16]. Сыпь возникает, как правило, на 3-4-й день от начала приема антибиотиков, располагается преимущественно на туловище, представлена пятнисто-папулезной сливающейся экзантемой (кореподобный характер). Некоторые элементы сыпи могут быть более интенсивно окрашены в центре. Сыпь разрешается самостоятельно без шелушения и пигментации. Важным моментом является то, что данная экзантема не является проявлением аллергической реакции на лекарственный препарат: пациенты как до, так и после ЭБВ-инфекции могут хорошо переносить антибактериальные препараты пенициллинового ряда. Эта реакция до конца не изучена и на данный момент рассматривается как взаимодействие вируса и лекарственного препарата. Отличительными чертами такой сыпи являются следующие:
Инфекционный мононуклеоз в большинстве случаев протекает гладко, без осложнений. Заболевание заканчивается через 2-4 недели. В некоторых случаях по истечении этого срока сохраняются остаточные проявления болезни.
Этиотропнаятерапия инфекционногомононуклеоза окончательно не разработана. При среднетяжелой и тяжелой формах можно использовать препараты рекомбинантного интерферона (виферон), индукторы интерферона (циклоферон), иммуномодуляторы с противовирусным эффектом (изопринозин) [17, 18]. В основном применяется патогенетическая и симптоматическая терапия [19, 20].
Энтеровирусная экзантема может быть вызвана различными типами энтеровирусов, а в зависимости от этиологии различается и симптоматика. Выделяют три вида энтеровирусных экзантем:
Кореподабная экзантема возникает преимущественно у детей раннего возраста. Заболевание начинается остро, с подъема температуры тела, головной боли, мышечных болей. Практически сразу появляются гиперемия ротоглотки, инъекция склер, нередко в начале болезни бывают рвота, боли в животе, возможен жидкий стул. На 2-3-й день от начала лихорадочного периода одномоментно появляется обильная распространенная экзантема на неизмененном фоне кожи. Сыпь располагается всегда на лице и туловище, реже на руках и ногах, может быть пятнистой, пятнисто-папулезной, реже петехиальной, размеры элементов - до 3 мм. Сыпь сохраняется 1-2 дня и исчезает бесследно. Примерно в это же время снижается температура тела.
Розеолоформная экзантема (бостонская болезнь) начинается также остро, с повышения температуры до фебрильных цифр. Лихорадка сопровождается интоксикацией, першением и болью в горле, хотя при осмотре ротоглотки никаких существенных изменений, кроме усиления сосудистого рисунка, нет. В неосложненных случаях лихорадка держится 1-3 дня и резко падает до нормы. Одновременно с нормализацией температуры появляется экзантема. Она имеет вид округлых розовато-красных пятен размером от 0,5 до 1,5 см и может располагаться по всему телу, но наиболее обильной бывает на лице и груди. На конечностях, особенно на открытых участках, сыпь может отсутствовать. Сыпь сохраняется 1-5 дней и бесследно исчезает [22].
Генерализованная герпетиформная экзантема возникает при наличии иммунодефицита и характеризуется наличием мелкой везикулезной сыпи. Отличием от герпетической инфекции является отсутствие сгруппированности везикул и помутнения их содержимого.
Одним из локальных вариантов энтеровирусной экзантемы является заболевание, протекающее с поражением кожи рук и ног, слизистой оболочки полости рта - так называемая болезнь рук, ног и рта (син.: ящуроподобный синдром, вирусная пузырчатка конечностей и полости рта). Наиболее частыми возбудителями данного заболевания служат вирусы Коксаки А5, А10, А11, А16, В3 и энтеровирус типа 71 [23, 24].
Заболевание встречается повсеместно, болеют преимущественно дети до 10 лет, однако отмечаются случаи заболеваний и среди взрослых, особенно молодых мужчин. Так же как и при других энтеровирусных заболеваниях, встречается чаще летом и осенью.
Инкубационный период короткий, от 1 до 6 дней, продромальный - невыразительный или отсутствует вовсе. Заболевание начинается с незначительного повышения температуры тела, умеренной интоксикации. Возможны боли в животе и симптомы поражения респираторного тракта. Практически сразу на языке, слизистой щек, твердом небе и внутренней поверхности губ появляется энантема в виде немногочисленных болезненных красных пятен, которые быстро превращаются в везикулы с эритематозным венчиком. Везикулы быстро вскрываются с формированием эрозий желтого или серого цвета. Ротоглотка не поражается, что отличает заболевание от герпангины [25]. Вскоре после развития энантемы у 2/3 пациентов появляются аналогичные высыпания на коже ладоней, подошв, боковых поверхностей кистей и стоп, реже - ягодиц, гениталий и лице. Так же как и высыпания во рту, они начинаются как красные пятна, которые превращаются в пузырьки овальной, эллиптической или треугольной формы с венчиком гиперемии. Высыпания могут быть единичными или множественными [26].
Заболевание протекает легко и разрешается самостоятельно без осложнений в течение 7-10 дней. Однако необходимо помнить, что вирус выделяется до 6 недель после выздоровления [27, 28].
Диагностика энтеровирусных экзантем носит комплексный характер и предусматривает оценку клинических симптомов заболевания совместно с данными эпидемиологического анамнеза и обязательного лабораторного подтверждения (выделение энтеровируса из биологических материалов, нарастание титра антител) [29].
Лечение носит в большинстве симптоматический характер. Применение рекомбинантных интерферонов (виферон, реаферон), интерфероногенов (циклоферон, неовир), иммуноглобулинов с высоким титром антител может потребоваться только при лечении больных тяжелыми формами энтеровирусного энцефалита [30].
Таким образом, проблема инфекционных заболеваний, сопровождающихся экзантемами, остается актуальной по сей день. Высокая распространенность данной патологии среди населения требует повышенного внимания от врачей любой специальности.
Вирус герпеса третьего типа varicella zoster (VZV) вызывает два клинически обособленных заболевания - ветряную оспу и опоясывающий герпес (Баринский И.Ф. и др., 1986; Haanpaa M., 2001). Оба заболевания, прежде всего, характеризуются везикулярной сыпью. Первичная инфекция манифестирует в форме ветряной оспы (ветрянки), а реактивация латентного VZV обусловливает появление локализованных высыпаний - опоясывающего лишая (Хахалин Н.Н., 2002). Мысль о связи между ветрянкой оспой и опоясывающим лишаем впервые была высказана в 1888 венским врачом Яношом Бокеем (von Bokay J., 1909).
Эпизод ветряной оспы в детстве способствует формированию специфической клеточной и гуморальной иммунной защиты. Считается, что рецидив инфекции у таких пациентов может развиться только на фоне недостаточности иммунной защиты, вследствие снижения активности специфических натуральных киллеров, Т-киллеров и системы интерферонов (Fleming D.M. et al., 2004). После первичной инфекции излюбленным местом персистенции VZV являются ганглий тройничного нерва и спинномозговые ганглии чувствительных корешков грудного отдела спинного мозга, где VZV находится в латентном состоянии. В течение этого времени вирус не размножается и не проявляет патогенных свойств. По-видимому, время латентного состояния вируса определяется уровнем специфических антител к VZV. Снижение их количества ведет к реактивации вируса, вирусной репликации (размножению), что на клиническом уровне и проявляется в виде опоясывающего лишая (Arvin A., 2005). Данный вывод подтверждается высокой корреляцией между вероятностью возникновения опоясывающего лишая у людей пожилого возраста и возрастным ослаблением активности клеточного звена иммунитета (Gilden et al., 2000)., На это также указывают данные, свидетельствующие о более высокой заболеваемости опоясывающим герпесом среди лиц, инфицированных вирусом иммунодефицита человека (Gilson I.H. et al., 1989), однако точные механизмы, лежащие в основе перехода вируса из латентного состояния в активное неизвестны.
В случае реактивации VZV ганглии чувствительных нервов становятся местами репликации вируса, именно в них обнаруживаются наиболее выраженные дегенеративные повреждения нейронов (Zerboni L. et al., 2005; Reichelt M. et al., 2008). В результате развивается ганглионит, сопровождаемый распространением инфекции вниз по нервным аксонам к коже. Каким образом происходит транспортировка вируса в поврежденных аксонах неизвестно. Инфекция также может распространяться центрально, приводя к воспалению оболочек в области передних и задних рогов спинного мозга (Gray F. et al. 1994). Отдельные патолого-анатомические наблюдения также свидетельствуют о наличии воспалительных изменений и в контралатеральных спинномозговых ганглиях (Miller S. E. et al., 1997), отмечается снижение количества нейронов и наличие воспалительных инфильтратов в ганглиях, периферических нервах, и спинномозговых корешках (Gowrishankar K. et al., 2007). В некоторых случаях отмечается выраженные некротические изменения в спинномозговых ганглиях. Большинство изменений в периферическом нерве протекает по типу Валлериановской дегенерации, имеющей место, как в толстых, так и в тонких волокнах. (Denny-Brown et al., 1944).
Острая VZV инфекция клинически характеризуется стадией продрома и стадией везикулярных высыпаний (Arvin A., 2005).
Сыпь обычно локализуется в одном или нескольких смежных дерматомах и сопровождается развитием острой невропатической боли. У 50% больных сыпь встречается на туловище, у 20% - на голове, у 15% - на руках, и у 15% - на ногах (Arani R.B. et al., 2001).
Клинический диагноз опоясывающего лишая в типичных случаях достаточно прост. Однако иногда требуется проведение лабораторной диагностики с целью идентификации вируса. Наиболее быстрым и высокочувствительным методом является полимеразная цепная реакция.
В остром периоде болезни или после него возможно развитие осложнений, захватывающих различные системы организма. Наиболее серьезными считаются неврологические осложнения. В структуре неврологических расстройств ведущее место занимает поражение периферической нервной системы. При данном заболевании воспалительный процесс затрагивает региональные, чувствительные ганглии с развитием ганглиолитов. Наличие у больных корешковых болей, парастезий, сегментарных нарушений чувствительности отмечается практически у каждого больного (Stankus S. et al., 2000; Thyregod H. G. et al., 2007). Болевой синдром имеет выраженную вегетативную окраску в виде жгучих, приступообразных, резких болей, усиливающихся в ночное время. В головном мозге при опоясывающем герпесе могут быть обнаружены явления отека, выраженная диффузная инфильтрация подпаутинного пространства, геморрагии в белом веществе, базальных ганглиях (Sissoko D. et al., 1998). Следует заметить, что осложнения со стороны головного и спинного мозга в настоящее время встречаются редко. В случаях развития VZV-инфекции в области тройничного нерва часто наблюдаются осложнения со стороны глаз - кератит, ирит, ретинит, офтальмит. Ранее, при отсутствии специфической противогерпетической терапии, к частым осложнениям VZV-инфекции относились пневмонии, энцефалиты или гепатиты, иногда приводившие к летальному исходу.
Вместе с тем, из всех перечисленных осложнений VZV инфекции самым распространенным считается постгерпетическая невралгия (Dworkin R.H., Portenoy R.K., 1996).
Различают острую герпетическую невралгию (в течение 30 дней после начала заболевания) и постгерпетическую невралгию (Choo P. et al.,1997). К ПГН относят упорные боли в областях, затронутых герпесной инфекцией после заживления кожи (Dworkin R. et al. 2003). Наиболее хорошо установленными факторами риска для ПГН являются пожилой возраст, большая распространенность высыпаний на коже и выраженная боль перед везикулярной сыпью (Desmond R.A. et al., 2002; Fleming D.M. et al., 2004). Все эти факторы находятся во взаимосвязи, поэтому пациенты 50 лет и старше в большинстве случаев испытывают тяжелую, нестерпимую боль и значительные кожные высыпания, что гораздо чаще приводит к развитию ПГН. У пациентов со всеми этими факторами риск развития ПГН превышает 50-75 % (Gnann J., Whitley R. 2002; Jung B.F., 2004). Постгерпетическая невралгия может развиться в любом возрасте, однако для нее характерна прямая корреляция частоты встречаемости и длительности ПГН с возрастом. Более 50% всех пациентов с ПГН - старше 60 лет, 75% больных с указанной патологией приходится на возрастную группу старше 75 лет (Nurmikko T.J., 2001). Половина всех пациентов с ПГН старше 60 лет испытывает постоянную боль более 6 месяцев, в то время как в возрастной группе 30-50 лет ПГН более 6 месяцевь наблюдается у 10% больных (Whitley R. et al. 1996). В США ежегодно регистрируется 100-200 тыс. новых случаев ПГН (Nurmikko T.J., 2001). Однако, истинная распространенность ПГН не известна, не только потому, что эпидемиологические данные недостаточны, но также из-за отсутствия конценсусса по определению ПГН. Некоторые авторы относят к ПГН боли, возникающие в любой период герпесной инфекции, другие считают, что ПГН - это боль, сохраняющаяся спустя 3 месяца после заживления кожи. В первом случае определения ПГН ее распространенность составляет 8%, во втором - 4,5% (Choo P. et al. 1997). Постоянную боль в течение 1 мес после сыпи испытывают до 15% пациентов и около 4% пациентов от общего количества перенесших опоясывающий лишай отмечают сохранение боли в течение года (Lancaster T. et al. 1995).
Классическое проспективное исследование, проведенное Hope-Simpson (1975), продемонстрировало, что из 321 пациента с опоясывающим лишаем 10 % имеют выраженную боль спустя 3 месяца после острой герпетической инфекции, а 4 % - и через 12 месяцев. Подобные результаты были получены и в других проспективных исследованиях (Helgason S. et al. 1996; 2000; Scott F.T. et al., 2006), в которых также было показано, что наибольший риск пролонгации болевого синдрома после перенесенного опоясывающего лишая имеют пациенты в возрасте около 60 лет.
Постгерпетическая невралгия занимает третье место по частоте встречаемости среди различных типов невропатической боли и уступает только болям в нижней части спины и диабетической невропатии (Montero H.J. et al., 2005; Breivik H. et al, 2006; Torrance N. et al., 2006).
Локализация болевого синдрома практически всегда соответствует зоне кожных высыпаний. Интенсивность болевого синдрома как правило высокая. Кроме глубоких ноющих и стреляющих болей очень характерны поверхностные жгучие боли и наличие стимулозависимых болей - динамической гипералгезии и аллодинии (Baron R., 2004).
При клиническом осмотре в зоне болей выявляются нарушения поверхностной чувствительности. Качество боли в острый период опоясывающего лишая и при ПГН различно. Вместе с тем, несмотря на разный выбор дескрипторов из МакГилловского болевого вопросника, пациенты с опоясывающим лишаем и ПГН для описания своих болевых ощущений выбирают похожие по смыслу слова, например, горячая и жгучая боль или пронзающая и простреливающая боль (Bennett M., 2001).
Схожие проявления наблюдаются и при описании вызванной боли пациентами с опоясывающим лишаем и ПГН. И те, и другие отмечают наличие схожих типов гипералгезии и аллодинии (Haanpaa M. et al., 2000; Berry J.D., Rowbotham M.C., 2004).
У большинства пациентов боль, связанная с ПГН, уменьшается в течение первого года. Однако у части больных она может сохраняться годами и даже в течение всей оставшейся жизни, причиняя немалые страдания (Cunningham A.L., Dworkin R.H., 2000). Затяжной, тяжелый характер заболевания с длительным, выраженным болевым синдромом способствует формированию расстройств психики (Dworkin R.H., et al., 1992). У таких пациентов выявляются тревожно-депрессивные расстройства, когнитивные нарушения - снижение активного внимания, памяти, затруднения осмысления происходящего, отмечается некритичность, нетерпеливость, неряшливость, страх боли, неуверенность в завтрашнем дне, отмечается снижение социальной активности (Haythornthwaite J.A. et al., 2003). ПГН оказывает значительное отрицательное влияние на качество жизни и функциональный статус пациентов особенно пожилого возраста (Lydick E. et al., 1995). У пациентов с ПГН отмечается хроническая усталость, снижение массы тела, физической активности, нарушения сна (Morin C.M., Gibson D., Wade J., 1998).
В основе боли, связанной с ПГН, лежат воспалительные изменения или повреждения ганглиев задних корешков спинного мозга и периферических нервов в пораженных зонах тела. Такие боли относят к невропатическим болям, их выделяют в отдельную самостоятельную группу и определяют как боли, возникающие вследствие первичного повреждения соматосенсорной нервной системы (Treede R.D. et al., 2008).
Патофизиологической основой невропатических болевых синдромов являются нарушения генерации и проведения ноцицептивного сигнала в нервных волокнах, а также механизмов контроля возбудимости ноцицептивных нейронов в структурах спинного и головного мозга (Кукушкин М.Л., Хитров Н.К., 2004; Baron R. 2000).
Лечебная тактика при опоясывающем лишае включает два основных направления: противовирусная терапия и купирование невропатической боли, как в острый период заболевания, так и в стадии постгерпетической невралгии. Результаты нескольких рандомизированных контролируемых испытаний свидетельствуют о том, что раннее начало лечения простого герпеса может предотвратить развитие постгерпетической невралгии или способствовать ее скорейшему разрешению (Исаков В.А. и др., 2004; Helgason S. et al., 1996; Jackson J.L. et al., 1997 ; Volmink J. et al., 1996).
Наиболее широкое применение нашли такие специфические противогерпетические препараты, как ацикловир, фамцикловир и валацикловир, которые, являясь нуклеозидными аналогами, блокируют вирусную репликацию (Романцев М.Г., 1996; Beutner K. et al., 1995; Bruxelle J., 1995). Важно, что противовирусное лечение проявляет наивысшую активность, если назначено в течение 72 ч от начала герпетических высыпаний (Johnson R., 2001; Johnson R., Dworkin R.H., 2003). В ряде исследований доказана высокая эффективность ацикловира в уменьшении тяжести, продолжительности острой герпесной инфекции и профилактике ПГН, особенно при его раннем назначении. Оценка эффективности фамцикловира также продемонстрировала уменьшение времени до разрешения сыпи (Dworkin R.H. et al., 1998). В сравнительном исследовании ацикловира и валацикловира показана эквивалентная эффективность в сокращении продолжительности невропатической ПГН (Beutner K. et al. 1995). В другом клиническом испытании установлена терапевтическая эквивалентность фамцикловира и валацикловира для неосложненного герпеса (Tyring S. et al. 2000). Возможно также сочетанное использование противовирусной терапии и глюкокортикостероидов (Whitley R. et al. 1999). Выявлено, что такая комбинация эффективнее монотерапии противовирусными препаратами, особенно для лечения острой боли и коррекции различных аспектов качества жизни пациентов. Комбинация ацикловир+преднизолон значительно быстрее купирует острую невралгию и возвращает пациента к обычной жизнедеятельности, но существенно не влияет на течение ПГН, то есть она наиболее показана в остром периоде в старших возрастных группах для терапии острого болевого синдрома. Доказано, что хотя преднизолон является иммуносупрессором, его использование не увеличивает частоты развития ПГН и в этом смысле его действие сравнимо с влиянием плацебо, то есть данная комбинация может быть спокойно использована в старших возрастных группах. Для некупируемых тяжелых случаев ПГН некоторые исследователи рекомендуют интратекальное введение метилпреднизолона (Kost R., Straus S., 1996).
В настоящее время в США делается акцент на профилактику герпетической инфекции. С 1995 г. в США проводится всеобщая вакцинация от ветряной оспы, особенно пожилых лиц, и с 1999 г. отмечается резкое снижение заболеваемости (Hambleton S., Gershon A., 2005; Oxman M.N. et al., 2005).
При постгерпетической невралгии препаратами с доказанной эффективностью (класс А - терапия первой линии) являются: пластины с 5% лидокаином, габапентин, прегабалин, трициклические антидепрессанты, трамадол (Attal et al., 2006).
На сегодняшний день эффективность применения пластин с 5% лидокаином (Версатис, Grunenthal Gmbh) убедительно доказана при лечении ПГН. Так, в нескольких рандомизированных клинических исследованиях установлено, что применение пластин с 5% лидокаином статистически достоверно более значимо облегчает проявления болевого синдрома у пациентов с постгерпетической невралгией по сравнению с плацебо (Rowbotham M.C., 1996; Galer B.S., 1999, 2002). На основании полученных данных FDA одобрило применение данного препарата в качестве стартовой терапии у пациентов с постгерпетической невралгией. (Richard L. et al., 2004)
Версатис - это топический анальгетик, который действует непосредственно там, где болит. Он выпускается в виде мягких пластин размером 10х14 см, которые наклеиваются на неповрежденную кожу без признаков воспаления. Медленно высвобождающийся из пластины лидокаин создает более или менее значительную концентрацию лишь в поверхностных слоях кожи, где проходят тонкие волокна, обеспечивающие болевую и температурную чувствительность (Gammaitoni AR, Davis MW. 2002.). Лидокаин лишь в незначительной степени проникает в более глубокие слои кожи, где проходят кровеносные сосуды, поэтому его попадание в системный кровоток сведено к минимуму. У пациентов, использовавших пластины Версатис, не наблюдалось никаких известных системных эффектов лидокаина (влияние на деятельность ЦНС и сердечно-сосудистой системы). Таким образом, важнейшим преимуществом пластин Версатис служит отсутствие системного действия, что гарантирует безопасность лечения. Практически полное отсутствие системного эффекта позволяет назначать Версатис совместно с любыми другими препаратами для лечения нейропатической боли.
Механизм лечебного эффекта препарата Версатис не ограничивается только действием высвобождающегося из них лидокаина. Важное значение имеет также то, что пластина выполняет роль механического барьера, препятствуя раздражению участка кожи с измененной чувствительностью (аллодиния), а также оказывает не него легкое охлаждающее действие (Galer BS, Gammaitoni AR, Oleka N et al., 2004)
Пластины Версатис рекомендуется прикреплять на 12 ч в течение суток, затем следует 12-часовой перерыв. Обезболивающий эффект часто начинается в течение 30 мин после прикрепления пластины, но может проявляться и позже, нарастает в течение 4 ч и затем поддерживается в течение длительного времени, пока пластина прикреплена к коже. Более того, он может сохраняться и после ее удаления.
Для объективной оценки эффективности каждого из препаратов при лечении ПГН используется показатель NNT (number needed to treat - количество больных, которых нужно пролечить, чтобы получить у одного 50% снижение боли). Чем ниже NNT, тем более эффективен препарат при данной патологии. NNT для пластин с 5% лидокаином при лечении пациентов с ПГН составляет 2,0; для амитриптилина - 2,6; габапентина - 4,4; прегабалина - 4,6 (Wu C.L., Raja S.N., 2008); для трамадола - 3,9 (Kalso E., 2006).
Кроме того, в клинической практике очень важен показатель NNH (number needed to harm - число пациентов, которых необходимо пролечить данным препаратом, чтобы получить развитие 1 случая неблагоприятной побочной реакции, приводящей к отмене препарата). Он показывает, насколько безопасен данный препарат при его использовании. Величина NNH для трамадола, рассчитанная по результатам нескольких клинических исследований, составила 9.0, для ТЦА 14.7, для габапентина 26.1. Рассчитать показатель NNH для пластин с 5% лидокаином не представляется возможным в связи благоприятным профилем безопасности препарата, сравнимым с плацебо.
Таким образом, оценка препарата Версатис с позиций доказательной медицины делает его препаратом выбора при лечении постгерпетической невралгии, что подтверждено в соответствующих рекомендациях.
СПИСОК ЛИТЕРАТУРЫ

Жанна Жданович, врач-дерматовенеролог, заведующая консультативно-методическим отделением Минского областного кожно-венерологического диспансера. Все уже вроде бы хорошо знают симптомы COVID-19. Но есть среди симптомов и те, что не особенно известны широкой публике.
Да, это так. COVID-19 — это острое инфекционное вирусное заболевание, характеризующееся воспалением дыхательных путей, интоксикацией. Это, конечно, знают все. У больных часто повышается температура, появляются кашель, утомляемость.
У некоторых инфицированных людей могут наблюдаться боль в горле, головная боль, различные другие болевые ощущения, диарея, а также сыпь на коже или изменение цвета кожи на пальцах рук или ног, покраснение или раздражение глаз.
То есть кожные проявления — это следствие основного заболевания. А могут ли высыпания возникать на фоне лечения COVID-19, из-за лекарственных препаратов?
Да, кожные высыпания при коронавирусной инфекции могут быть как начальными симптомами заболевания (вирусная экзантема по типу ветряной оспы, острая крапивница), так и возникать в результате лечения (крапивница, токсидермия, аллергические дерматиты).
Крапивница , например, проявляется в виде внезапно возникающих на коже волдырей, которые могут появляться и исчезать в течение нескольких часов, дней.
Токсидермии , аллергические дерматиты обусловлены токсико-аллергическими реакциями на принимаемые в процессе лечения лекарственные препараты и проявляются пятнами, папулами красного, розового цвета.
Нередко на коже ладоней, подошвенной поверхности стоп, пальцах кистей и стоп появляются мелкие внутриэпидермальные пузырьки, которые в процессе разрешения начинают шелушиться. Это дисгидроз кистей и стоп.
В результате повреждения внутрикожных капилляров могут возникать петехии — мелкие точечные округлые пятна с различной окраской: красной, коричневой или фиолетовой.
Какие еще кожные проявления у переболевших COVID-19 вы наблюдаете?
К этой группе кожных проявлений можно отнести телеангиэктазии — стойкое расширение мелких сосудов кожи (артериол, венул, капилляров) невоспалительной природы в виде сосудистых звездочек или сеточки. К сожалению, эти проблемы сами не исчезают, требуется вмешательство косметологов. Но обычно такие проявления не обширные, занимают небольшую площадь.
В результате отложения избыточного количества гемосидерина в дерме, поражения капиллярной и прекапиллярной сети кровеносных сосудов дермы возможно появление пятен гемосидероза. Это пятна желтоватого и желтовато-буроватого цвета, а также папулезно-геморрагические, иногда сливающиеся высыпания, небольшой зуд. Чаще всего гемосидероз развивается на коже верхних и нижних конечностей.
Еще один момент: нередко васкулопатии имеют клиническую картину акродерматитов, псевдообморожений .
Некоторые пациенты на фоне COVID-19 предъявляют жалобы на сухость губ, появление чешуек на губах. Обычно этот симптом развивается ближе к концу болезни.
Встречаются и папуло-сквамозные высыпания на коже, характеризующиеся появлением красных, розовых пятен, папул, шелушения. К этой группе заболеваний можно отнести псориаз, красный плоский лишай, розовый лишай Жибера, острый парапсориаз и другие.
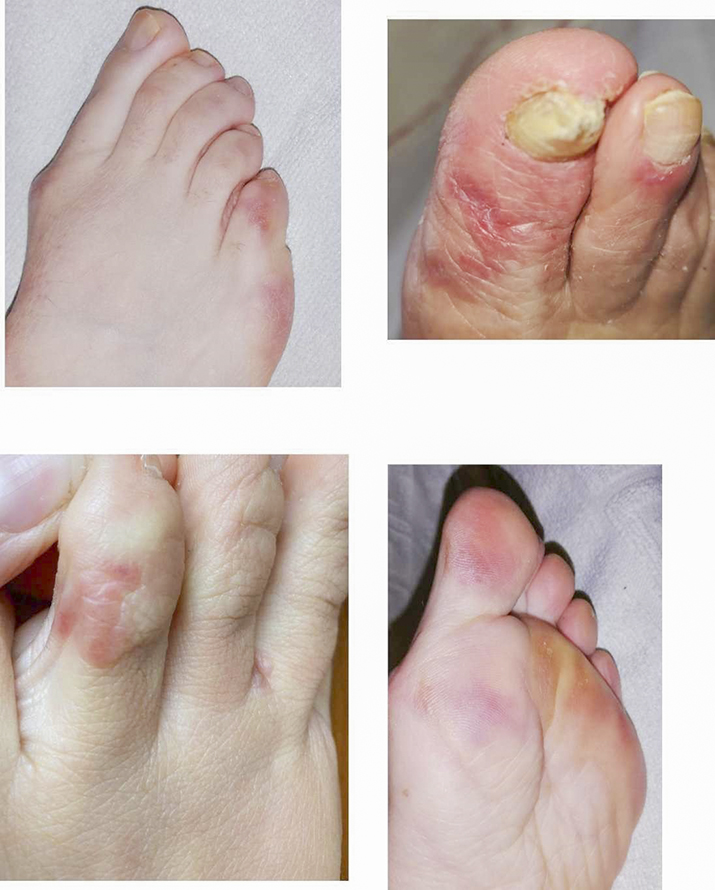
Возможные кожные проявления у пациентов, перенесших COVID-19.
Различается ли частота кожных проявлений у пациентов разного возраста, пола, веса?
На кожные проявления практически не оказывают влияние возраст, пол, вес. Единственное — у женщин могут значительно чаще появляться стойкие ливедо-синюшные пятна различной величины и очертаний, образующие причудливую петлистую сеть в области нижних конечностей, реже — на предплечьях, кистях, лице и туловище.
А как на инфекцию реагируют пациенты с хроническими кожными патологиями?
Кроме острых кожных проявлений при коронавирусной инфекции возможно обострение любой хронической кожной патологии (атопический дерматит, экзема и другие).
Кстати, псориаз, красный плоский лишай, атопический дерматит, другие кожные патологии могут как обостряться у хронических больных, так и возникать остро. Например, причина развития псориаза неизвестна, но мы знаем, что среди предрасполагающих факторов — стрессы, острые инфекции и обострение хронических заболеваний. Если бы не коронавирус, то, возможно, у человека никогда бы и не проявилось то или иное кожное заболевание.
Профилактика COVID-19, таким образом, лучшее средство от перечисленных и других кожных проявлений, возникающих или обостряющихся из-за этой инфекции…
Несомненно. Своим пациентам мы всегда напоминаем, что лечение и восстановление после коронавирусной инфекции длительное и сложное. Поэтому необходимо предпринять все меры предосторожности, чтобы избежать заражения. А меры эти широко известны и просты: стараемся не посещать мест массового скопления людей, избегаем контактов с людьми с симптомами респираторных заболеваний; используем одноразовые медицинские маски; моем руки с мылом, обрабатываем антисептическими средствами. Нужно также стараться не касаться глаз, рта и носа руками, если они не вымыты или не обработаны антисептиком.
Я не случайно перечисляю известные меры профилактики COVID-19, так как некоторые из них могут вызвать определенные проблемы с кожей. Так, дерматиты кистей рук мы особенно часто наблюдали в первую волну коронавируса, когда некоторые люди очень уж рьяно использовали для обработки антисептики и прочие, в том числе спиртосодержащие, средства.
А постоянное ношение маски может вызвать контактные, контактно-аллергические дерматиты на лице, что особенно касается медиков, которые работают в красных зонах. Но обычным людям чаще всего не нужно носить маски не снимая — здесь, как и во всем, важен разумный подход. Сейчас, кстати, кожных проявлений из-за постоянного ношения масок и обработки рук антисептическими средствами мы видим меньше — люди привыкли жить в новой реальности.
Лечение пациентов с кожными проявлениями после перенесенного COVID-19 такое же, как у других пациентов?
В общем, да. Как лечить острые кожные заболевания, мы знаем, как помочь пациентам с хронической кожной патологией — тоже, но, конечно учитывается состояние человека после коронавирусной инфекции, подход должен быть всегда индивидуальный. Количество пациентов с приходом эпидемии выросло и у дерматовенерологов, но мы отнюдь не беспомощны. Главное, чтобы люди не занимались самолечением и обращались к специалистам.
Читайте также:

