Температура при противовирусной терапии гепатита с
Обновлено: 18.04.2024
Отмечены осложнения лечения препаратами прямого действия при наличии гепатита В, что выражается в обострении процесса со всеми ярко выраженными проявлениями обострения вирусного гепатита В (желтуха, значительное повышение печеночных ферментов в крови, температура).
Поэтому до начала терапии необходимо провести исследование маркеров гепатита В: HBsAg, anti-HBcor, anti-HBs.
При выявлении HBsAg обязательно обследование на ДНК вируса гепатита В, на антитела к гепатиту D - anti-HDV и РНК HDV методом ПЦР.
В ходе противовирусного лечения хронического гепатита С у пациентов с anti-HBcor+, а также в периоде наблюдения после завершения терапии, следует проводить контроль ДНК HBV и при необходимости назначать противовирусное лечение хронического гепатита В.
2. Степень фиброза и лечение пациентов с циррозом печени
Опасность вирусного заболевания печени обусловлена тем, что активный вирус при размножении разрушает печень необратимо и при этом вместо разрушенной печени формируются участки повышенной плотности, состоящие из соединительной ткани. Оставшаяся здоровая часть печени компенсирует функции уже разрушенной ее части и обеспечивает, таким образом, жизнедеятельность пациента, часто без всяких симптомов и даже отклонений в биохимическом анализе крови.
Однако, при длительном процессе разрушения может сложиться ситуация, при которой оставшаяся здоровая часть печени не достаточна для компенсации – эта стадия заболевания называется цирроз, а при далеко зашедшем процессе его нельзя вылечить, так как при назначении ПППД возможно обострение цирроза, которое невозможно остановить.
Поэтому важнейшим вопросом при назначении противовирусной терапии является оценка степени поражения печени (степени фиброза). Из всех существующих в настоящее время методом оценки фиброза наиболее информативным признана эластометрия на аппарате фиброскан. В результате измерения таким образом плотности печени мы получаем ее значение в килопаскалях кПа (физические единицы измерения плотности). Начиная с 12,5 кПа мы ставим 4-ю, последнюю стадию, которая может ассоциироваться с циррозом.
Основное и самое опасное последствие уплотнения печени – это вызванное им повышение давления в портальной вене – портальная гипертензия, которая возникает из-за увеличения сопротивления кровотоку и может закончиться разрывом сосуда и несовместимым с жизнью кровотечением.
Портальная гипертензия чаще всего проходит бессимптомно и первым клиническим проявлением является увеличение селезенки и в связи с этим снижение уровня тромбоцитов. Клиническое значение портальной гипертензии заключается в угрозе кровотечения из расширенных вен пищевода и желудка, развития асцита (жидкость в брюшной полости), бактериального перитонитом и энцефалопатии.
Измерение плотности печеночной ткани на аппарате Фиброскан точно определяет степень ее фиброза, повышение которой и вызывает портальную гипертензию. Пороговый уровень плотности, ассоциирующийся с циррозом и портальной гипертензией, является 25 кПа.
Поскольку плотность печеночной ткани связана с портальной гипертензией, то сочетание уровня тромбоцитов и выраженности фиброза в килопаскалях, дает нам предварительную информацию для выбора тактики лечения и возможности назначения ПППД. Плотность меньше или равная 20 кПа и количество тромбоцитов больше 150, позволяют считать процесс компенсированным и назначать противовирусную терапию с учетом рекомендаций по лечению цирроза класса А.
Клиническая декомпенсация является противопоказанием для назначения ПППД. Для принятия решения о назначении терапии значимыми являются следующие показатели, характеризующие угрозу кровотечений: индекс LSPS, включающий плотность печеночной ткани по данным эластометрии, размеры селезенки и уровень тромбоцитов. Пороговым является значение больше 6,5 и плотность печеночной ткани больше 21 кПа.
В зависимости от прогностических показателей, в том числе плотности печеночной ткани, могут быть назначены разные схемы лечения ПППД, обязательно с учетом противопоказаний и сопутствующих заболеваний. В схему лечения как правило добавляется рибавирин и длительность терапии может быть увеличена до 24 недель.
При наблюдении пациентов с циррозом печени класса В обязательно наблюдение у опытного гепатолога или в специализированном гепатологическом центре. До начала противовирусного лечения крайне важно исключить наличие гепато-целлюларной карциномы (ГКЦ). При наличии ГЦК сначала проводится лечение рака печени, а затем вирусного гепатита С. В ряде случаев противовирусная терапия ПППД может быть назначена совместно с химиотерапией.
Что такое гепатит Б? Причины возникновения, диагностику и методы лечения разберем в статье доктора Александрова Павла Андреевича, инфекциониста со стажем в 14 лет.
Над статьей доктора Александрова Павла Андреевича работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Вирусный гепатит В (Б) — острое и хроническое инфекционное заболевание, вызываемое вирусом гепатита В, с гемоконтактным механизмом передачи (через кровь), протекающее в различных клинико-морфологических вариантах, и возможным развитием цирроза печени и гепатоцеллюлярной карциномы. Всего в мире, по самым скромных оценкам, инфицировано более 250 млн человек.
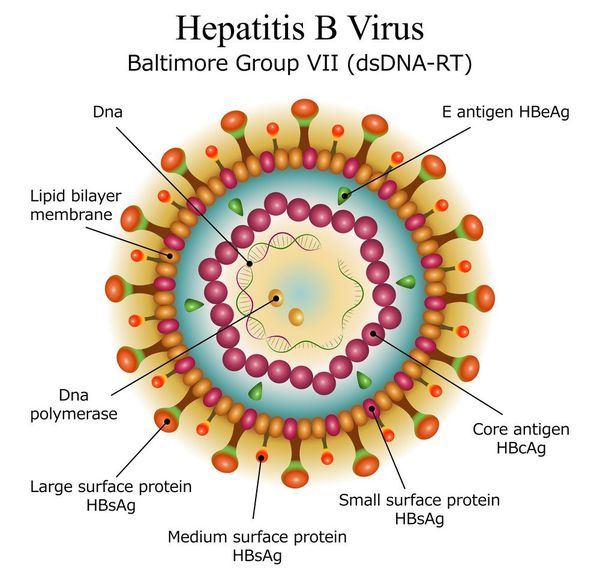
Этиология
вид — вирус гепатита В (частица Дейна)
Развитие вируса гепатита Б происходит в гепатоцитах (железистых клетках печени). Он способен к интеграции в ДНК человека. Имеются 9 генотипов вируса с различными подтипами — генетическая изменчивость позволяет вирусу образовывать мутантные формы и ускользать от действия лекарств.
Имеет ряд собственных антигенов:
- поверхностный HbsAg (австралийский). Появляется за 15-30 дней до развития болезни, свидетельствует об инфицировании (не всегда). Антитела к HbsAg выявляются через 2-5 месяцев от начала заболевания, а сам HbsAg исчезает из крови (при благоприятном течении процесса);
- сердцевинный HbcorAg (ядерный, коровский). Появляется в инкубационном периоде и совместно с ним появляются антитела (HbcorAb). Длительное присутствие HbcorAg в крови свидетельствует о вероятной хронизации процесса (неадекватный иммунный ответ);
- антиген инфекциозности и активного размножения вируса (HbeAg). Появляется совместно с HbsAg и отражает степень инфицированности. Его продолжительная циркуляция в крови является свидетельством развития хронизации процесса, а антитела к нему являются благоприятным прогностическим признаком (не всегда, но по меньшей мере указывают на возможность более благоприятного процесса, срок их циркуляции после выздоровления окончательно не определён, но не более пяти лет после благоприятного разрешения процесса);
- HbxAg — регулятор транскрипции, способствует развитию гепатокарциномы.
Вирус гепатита В чрезвычайно устойчив к действию всевозможных естественных факторов окружающей среды, инактивируется при 60 °C за 10 часов, при 100 °C за 10 минут, при оптимальной температуре сохраняется до 6 месяцев, при автоклавировании погибает за 5 минут, в сухожаровом шкафу — через 2 часа, 2% раствор хлорамина убивает вирус за 2 часа. [1] [3]
Эпидемиология
Источник инфекции — только человек, больной острой или хронической формой инфекции.
Механизм передачи: гемоконтактный и вертикальный (от матери к ребёнку), не исключается трансмиссивный механизм передачи (например, при укусах комаров в результате раздавливания и втирания инфицированного тела комара в поврежденную ткань человека).
Пути передачи: половой, контактно-бытовой, гемотрансфузионный (например, при переливании крови или медицинских манипуляциях). Восприимчивость всеобщая. Заболеваемость — 30-100 человек на 100 тысяч населения (зависит от страны). Летальность от острых форм — до 2%. После перенесённого острого заболевания при условии выздоровления иммунитет стойкий, пожизненный.
Для заражения характерна малая заражающая доза (невидимые следы крови). [1] [2]
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы гепатита Б
Инкубационный период гепатита В длится от 42 до 180 дней (следует иметь в виду, что наличие клинической симптоматики характеризует лишь незначительную долю всех случаев заболевания).
Начало постепенное. Характерные синдромы:
- общей инфекционной интоксикации (проявляется как астеноневротический синдром);
- холестатический (нарушение секреции желчи);
- артрита;
- нарушения пигментного обмена (появление желтухи при уровне общего билирубина свыше 40 ммоль/л);
- геморрагический (кровоточивость кровеносных сосудов);
- экзантемы;
- отёчно-асцитический (скопление жидкости в брюшной полости);
- гепатолиенальный (увеличение печени и селезёнки).
При первых признаках гепатита B нужно обратиться к доктору.
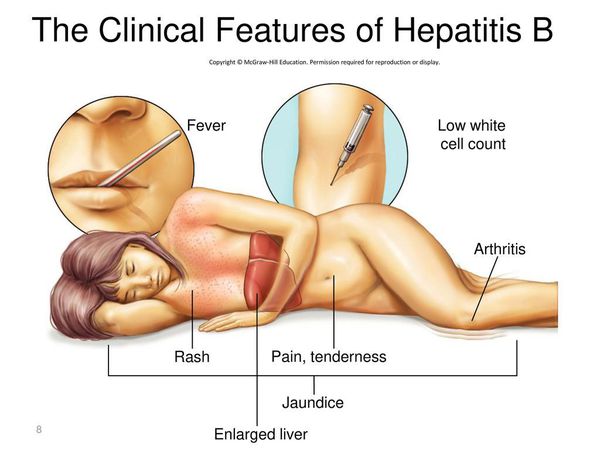
Первые признаки гепатита B
Начальный (преджелтушный) период продолжается 7-14 дней. Чаще протекает по многообразному типу с болевыми ощущениями в различных суставах по ночам и утром, уртикарными высыпаниями, астеновегетативными проявлениями (снижение аппетита, апатия, нервозность, слабость, разбитость, повышенная утомляемость). Изредка развивается синдром Джанотти-Крости — симметричная, яркая пятнисто-папулёзная сыпь. Не исключены умеренные диспептические явления (расстройства пищеварения). К концу периода происходит потемнение мочи, обесцвечивание кала.
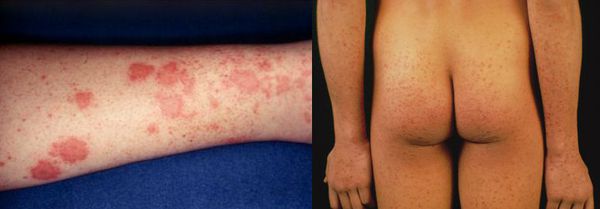
Желтушный период
Этот период продолжительностью около одного месяца характеризуется возникновением желтушного окрашивания кожи (различных оттенков) на фоне продолжающегося или ухудшающегося общего состояния. Характерна длительность и стойкость симптоматики. Появляется тяжесть и болезненность в правом подреберье, горечь во рту, тошнота, выражённый зуд кожи (практически не снимаемый никакими средствами). На фоне усиления астеноневротического компонента появляются геморрагические проявления, урежение пульса, гипотензия, отёки (отражает степень интоксикации и нарушения функций печени).
Выздоровление
Следующим этапом в развитии болезни является нормализации общего состояния, спадение желтухи и реконвалесценция, которая в зависимости от конкретной ситуации и состояния иммунной системы может закончиться как выздоровлением, так и движением развития заболевания в хроническое течение, характеризующееся маловыраженой неусточивой симптоматикой, преимущественно в виде слабости, периодического дискомфорта в правом подреберье, бурно сигнализирующим лишь на стадии цирроза и полиорганных осложнений.
- гепатиты другой этиологии;
- желтухи другой этиологии (например, гемолитическая болезнь, токсическое поражение, опухоли);
- малярия; ;
- лептоспироз;
- ревматоидный артрит.
Гепатит В у беременных
Острый гепатит характеризуется более тяжёлым течением у беременной, возникновении повышенного риска преждевременных родов, аномалий развития плода на ранних сроках и кровотечений. Вероятность передачи при острой форме зависит от сроков беременности: в первом триместре риск 10% (но более тяжёлые проявления), в третьем триместре — до 75% (чаще бессимптомное течение после родов). У большинства детей при заражении во внутриутробном и постнатальном периодах происходит хронизация инфекции. [1] [3] [6]
Патогенез гепатита Б
С движением кровяной массы вирус попадает в печеночную ткань, где локализуется в гепатоцитах и теряет свою протеиновую сферу в лизосомах. Происходит выход вирусной ДНК с последующим ресинтезом аномальных протеинов LSP, а параллельно образование новых частиц Дейна.
В процессе эволюции вирусчеловеческого взаимодействия возможно развитие двух вариантов:
При репликативном пути происходит следующее: белки LSP совместно с HbcorAg вызывают увеличение продукции гамма-интерферона, что приводит к активации главного комплекса гисотсовместимости (HLA), проистекает преобразование молекул гистосовместимости 1 и 2 классов, в результате чего клетка становиться для организма враждебной в антигенном формате.
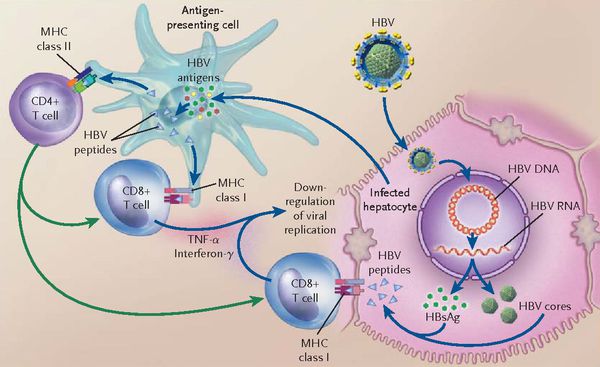
Антигенпрезентирующие макрофаги содействуют изменению В-лимфоцитов в плазматические клетки и экспрессии ими агрессивных белков-антител к посторонним антигенам. В итоге на поверхности печёночных клеток формируются вирусспецифические иммунные комплексы (антиген + антитело + фракция комплемента С3в).
В динамике может реализоваться два сценария:
- в первом варианте запуск каскада комплимента ведёт к появлению в составе иммунных комплексов агрессивной фракции С9 (мембранатакующий комплекс) — наблюдается значительный некроз гепатоцитов без участия лимфоцитов (молниеносная форма гепатита В);
- при альтернативной варианте (наблюдающимся в большинстве случаев) каскад комплемента в силу иммуноиндивидуалистических свойств не активируется — тогда идёт умеренное разрушение Т-киллерами меченых антителами заражённых вирусом гепатоцитов. Образуются ступенчатые некрозы с образованием на месте гибели гепатоцитов соединительной ткани — рубцов (то есть острый гепатит В при плохом иммунном ответе постепенно переходит в хронический).
Непременным атрибутом патогенеза является формирование иммунопатологического процесса. Гибель гепатоцитов, инфицированных вирусом гепатита В, следует за счёт иммунокомпетентных частиц, Т-киллеров и макрофагальных элементов.
Серьёзным значением является нарушение свойств мембраны клеток печени, что сопровождается экскрецией (выделением) лизосомальных ферментов, разрушающих гепатоциты. Сообразно этому, гибель гепатоцитов происходит за счёт иммунокомпетентных клеток, лизосомальных ферментов и противопечёночных гуморальных аутоантител, то есть острая болезнь наступает (и благоприятно заканчивается) только при хорошем иммунитете, а при плохом идёт хронизация.
При тяжёлом цитолитическом синдроме (массивные некрозы гепатоцитов) возникает гипокалиемический алкалоз, острая печёночная недостаточность, печёночная энцефалопатия (ПЭП), церебротоксическое действие, нарушение функции обмена нервной ткани. [2] [3] [6]
Классификация и стадии развития гепатита Б
По цикличности течения:
- острый;
- острый затяжной;
- хронический.
По клиническим проявлениям:
- субклинический (инаппарантный);
- клинически выраженный (желтушный, безжелтушный, холестатический, фульминантный).
По фазам хронического процесса:
Группы риска хронического гепатита B
Хроническим гепатитом чаще страдают дети младше шести лет. При заражении в первый год жизни он развивается в 80–90 % случаев, от года до шести лет — в 30–50 %, у взрослых без сопутствующих заболеваний — менее чем в 5 %. [7]
Осложнения гепатита Б
Чем опасен гепатит Б
Заболевание может привести к острой печёночной недостаточности (синдрому острой печеночной энцефалопатии).
Выделяют четыре стадии болезни:
Диагностика гепатита Б
Многообразие форм, тесная взаимосвязь с иммунной системой человека и зачастую достаточно высокая стоимость исследований часто затрудняют принятие конкретного решения и диагноза в стационарный отрезок времени, поэтому во избежание роковых (для больного) ошибок следует подходить к диагностике с учётом всех получаемых данных в динамическом наблюдении:
- общеклинический анализ крови с лейкоцитарной формулой (лейкопения, лимфо- и моноцитоз, уменьшение СОЭ, тромбоцитопения);
- общий анализ мочи (появление уробилина);
- биохимический анализ крови (гипербилирубинемия в основном за счёт связанной фракции, повышение уровня АЛТ и АСТ, ГГТП, холестерина, щелочной фосфатазы, снижение протромбинового индекса, фибриногена, положительная тимоловая проба);
- маркеры гепатита В: HbsAg, HbeAg, HbcorAg, HbcorAb IgM и суммарные, HbeAb, anti-Hbs, ПЦР в качественном и количественном измерении);
- УЗИ органов брюшной полости, КТ и МРТ диагностика;
- фиброскан (применяется для оценки степени фиброза). [3][4]
Скрининг при хроническом гепатите
Пациентам с хроническим гепатитом В рекомендуется не реже чем раз в полгода проходить обследование: УЗИ органов брюшной полости, клинический анализ крови, АЛТ, АСТ, тест на альфа-фетопротеин. Скрининг позволяет вовремя заметить обострение болезни и начать специфическую терапию.
Лечение гепатита Б
Лечение острых форм гепатита В должно осуществляться в стационаре (учитывая возможность быстрых и тяжёлых форм болезни), хронических — с учётом проявлений.
Диета и режим при гепатите В
В острый период показан постельный режим, печёночная диета (№ 5 по Певзнеру): достаточное количество жидкости, исключение алкоголя, жирной, жареной, острой пищи, всё в мягком и жидком виде.
Медикаментозная терапия
При лёгкой и средней тяжести острого гепатита этиотропная противовирусная терапия (ПВТ) не показана. При тяжёлой степени и риске развития осложнений назначается специфическая противовирусная терапия на весь период лечения и возможно более длительное время.
В лечении хронических форм гепатита показаниями к назначению ПВТ является наличие уровня DNA HBV более 2000 МЕ/мл (при циррозе печении независимо от уровня), умеренное и высокое повышение АЛТ/АСТ и степени фиброза печёночной ткани не менее F2 по шкале METAVIR, высокая вирусная нагрузка у беременных женщин. В каждом конкретном случае показания определяются индивидуально, в зависимости от выраженности процесса, временной тенденции, пола, планирования беременности и другого.
Существует два пути противовирусного лечения:
- терапия пегилированными интерферонами (имеет ряд существенных противопоказаний и серьёзных побочных эффектов — не менее 12 месяцев);
- нуклеозидно-аналоговой терапии NA (используются препараты с высоким порогом резистентности вируса, длительно — не менее пяти лет, удобство применения, хорошая переносимость).
В отдельных случаях может рассматриваться применение комбинированной терапии.
Из средств патогенетической терапии в острый период используются внутривенно вводимые растворы 5% глюкозы, дезинтоксикантов, антиоксидантов и витамины. Показан приём энтеросорбентов, ферментных препаратов, при выраженном холестазе применяются препараты Урсодезоксихолевой кислоты, при тяжёлом течении — глюкокортикостероиды, методы аппаратного плазмофереза.
В хронической стадии заболевания при наличии соответствующей активности процесса и невозможности назначения ПВТ может быть показан приём групп гепатопротекторов и антиоксидантов. [1] [3]
Прогноз. Профилактика
Основное направление профилактики на сегодняшний день — это проведение профилактической вакцинации против гепатита В в младенческом возрасте (в том числе усиленная вакцинация детей, рождённых от матерей с гепатитом В) и далее периодические ревакцинации раз в 10 лет (или индивидуально по результатам обследования). Достоверно показано, что в странах, где была введена вакцинация, резко сократилось количество вновь выявленных случаев острого гепатита В.
Вторая составляющая стратегии профилактики включает обеспечение безопасности крови и её компонентов, использование одноразового или стерилизованного инструментария, ограничение числа половых партнёров и использование барьерной контрацепции. [1] [2]
Актуальность. Проблема этиотропного лечения хронического вирусного гепатита С (ХВГС), несмотря на большое количество исследований, по-прежнему остается актуальной и до конца не решена.
Эффективность лечения по данным разных исследователей не превышает 46-51% у больных ХВГС с 1-м генотипом и 70-80% у больных ХВГС с не 1-м генотипом 3. Так же ограничивают их применение высокая стоимость препаратов и большое количество побочных эффектов от проводимой терапии. Целью проведения этиотропной терапии ХВГС является подавление вирусной репликации, эрадикация вируса из организма и, соответственно, прекращение инфекционного процесса. Даже отсутствие вирусологического эффекта при специфической терапии приводит к замедлению прогрессирования заболевания, стабилизации или регрессии патологических изменений в печени, предупреждению формирования цирроза печени и первичной гепатоцеллюлярной карциномы, а также повышению качества жизни.
Оценку эффективности специфического лечения осуществляют на основании нескольких критериев: вирусологического (исчезновение рибонуклеиновой кислоты (РНК) вируса из сыворотки крови), биохимического (стойкая нормализация уровня ферментов печени) и морфологического (уменьшение индекса гистологической активности и стадии фиброза).
В целом около 5% больных [1,5] вынуждены отказаться от специфического противовирусного лечения в начале курса из-за многочисленных побочных эффектов, а 20% не доводят его до конца.
Побочные эффекты интерферона (ИФН) и рибавирина иногда вынуждают временно или постоянно снижать их дозы или отменять препараты. Некоторыми исследователями [5] показано, что для достижения устойчивого вирусологического ответа (УВО) необходимо получение не менее 2/3 дозы ИФН и рибавирина, поэтому эффективность комбинированной противовирусной терапии (КПВТ) напрямую зависит от наличия побочных эффектов и возможностью их коррекции.
Некоторые побочные эффекты не требуют медикаментозной терапии, так как носят легкий или среднетяжелый характер, другие - тяжелый и угрожающий жизни характер, при этом необходима специфическая коррекция. Как правило, после окончания терапии большинство побочных эффектов полностью исчезает без применения симптоматической терапии.
Проблема побочных эффектов на фоне проводимой КПВТ остается до конца не изученной, несмотря на проведенные многочисленные исследования.
Основными побочными явлениями, описанными в литературе, являются: гематологические изменения; гриппоподобный, диспепсический, неврологический и астеновегетативный синдромы; аутоиммунные поражения; снижение массы тела; выпадение волос; огрубение кожи; аллергические реакции различной степени выраженности; местная реакция в области введения интерферонов.
Таким образом, проблема побочного действия комбинированного противовирусного лечения ХВГС, его влияние на достижение УВО является актуальной в настоящее время.
Целью данного исследования было изучение побочных явлений КПВТ в зависимости от схемы лечения, сопутствующих заболеваний, влияние на достижение УВО. Для достижения поставленной цели были сформулированы следующие задачи: оценить переносимость КПВТ пациентами с различными схемами терапии, выявить частоту побочных эффектов КПВТ и взаимосвязь их с достижением УВО.
Материалы и методы. В исследование были включены 50 пациентов с установленным диагнозом ХВГС, которые получали КПВТ. Диагноз был подтвержден согласно общепринятым методикам.
Из исследования исключались пациенты с микст-инфекцией (вирусный гепатит В, ВИЧ-инфекция) а так же наличием сопутствующей патологии печени (первичный билиарный цирроз, болезнь Вильсона-Коновалова, синдром Бадда-Киари, гемохроматоз, аутоиммунный гепатит, дефицит альфа-1 антитрипсина) и предшествующего специфического противовирусного лечения по поводу ХВГС, больные с наличием любого из общепринятых противопоказаний для проведения КПВТ.
Продолжительность лечения составила 48 недель для пациентов, инфицированных генотипом 1в вирусного гепатита С или при наличии у больного цирроза печени; 24 недели для пациентов, инфицированных генотипом 2 и 3а. Согласно рекомендациям по ведению пациентов с ХВГС, КПВП включала комбинацию стандартного (Интрон или Альтевир 3 млн МЕ 3 раза в неделю) или пегилированного (ПегИнтрон 120 мкг или Пегасис 180 мкг в неделю) ИФН и рибавирина в дозировке 800-1200 мг в зависимости от массы тела.
Устойчивый вирусологический ответ (УВО) определялся как отсутствие РНК вируса в сыворотке крови спустя 24 недели после окончания КПВТ. Больные находились под наблюдение в течение терапии на базе Воронежской областной клинической инфекционной больницы и поликлиник Воронежа. Все пациенты были разделены на 2 группы: получающие в составе КПВТ стандартные ИФН – 52,0% (26 человек) или пегилированные ИФН – 48,0% (24 человек). Пациенты были сопоставимы по возрасту и полу: средний возраст составил 40,3 ±10,4, количество мужчин - 57,1%, женщин 42,9%. Распределение по группам показано в табл. 1.
Таблица 1. Характеристика пациентов в исследуемых группах

При анализе полученных результатов использовались описательные методы математической статистики с применением пакета программ Microsoft Excel 2010. Достоверность различий оценивалась методами непараметрической статистики, статистически значимыми считались различия результатов при р≤0,05.
Результаты. При анализе эпидемиологических данных выяснено, что в большинстве случаев (34% случаев) ХВГС выявлен случайно, без клинических проявлений. Одинаковое количество пациентов (по 8 человек - 19,2%) обследовались по поводу диспепсических жалоб и длительного повышения печеночных ферментов. У 30 % пациентов в анамнезе отмечались неоднократные операции или переливание крови; употребление внутривенных наркотиков - у 16% человек. Длительность заболевания до начала противовирусной терапии составила в 1 группе 3±1,4 лет, во 2 группе 5±3,4лет. Степень фиброза по Metavir в среднем составил в 1 группе 1±0,85 балла, во второй группе выше - 1,9±1,5 баллов.
Соотношение генотипов вируса гепатита С, определенных до начала КПВТ, показано в табл. 2.
Таблица 2. Соотношение генотипов вирусного гепатита С

Среди всех пациентов УВО определялся в большинстве случаев - 80,0%, при применении обоих видов терапии, но при этом достоверных различий между группами по этому признаку не выявлено. Эффективность терапии в 1 группе составила 75,1%, во 2 группе - 78,2%. Отсутствие вирусологического ответа в половине случаев связано с отменой препаратов из-за развития выраженных побочных эффектов (прогрессирование неврологической симптоматики с развитием энцефалопатии в 1 группе, длительная некупируемая лихорадка во 2 группе).
Частота побочных эффектов в общей выборке была достаточно высокой - 72,3% среди всех пациентов, при этом в 1 и 2 группе нежелательные явления встречались с одинаковой частотой (69,1% и 73% соответственно).
На протяжении всей терапии у большинства пациентов встречался астеновегетативный синдром в виде выраженной слабости, усталости, нарушения сна, при этом значительно чаще эти проявления отмечали пациенты 2 группы - принимающие пегилированные ИФН (30,7%), что в 2,1 раза чаще, чем во 1 группе (66,6%). Снижение настроения, появление раздражительности, неконтролируемой агрессии при опросе отмечали 23,0% пациентов 1 группы и 25,0% пациентов 2 группы. Данные жалобы чаще встречались на 24±2 неделе терапии. Описанная в литературе депрессия, индуцированная КПВТ, среди данной выборки не встречалась. Для выявления депрессии у всех пациентов применялся опросник Цунга в начале и при завершении КПВТ.
Гриппоподобный синдром, проявляющийся лихорадкой до 38±0,85?С, миалгией, артралгией, выявлен достоверно чаще в у пациентов 1 группы (38,4%), чем у 2 группы (30,1%). Длительность лихорадки составляла в среднем 14±2 недель, первый подъем температуры всегда сопровождал начало КПВТ. Лихорадка купировалась применением препаратов НПВС в стандартных дозировках.
Жалобы со стороны желудочно-кишечного тракта в виде снижения аппетита, тошноты, периодической диареи, боли, вздутия в животе отмечались у 34,6% пациентов 1 группы, что в 2,08 раза чаще, чем во 2 группе (16,6%) .Желтуха на фоне КПВТ встречалась у 2 человек в каждой группе (по 8,3% и 7,6% соответственно).
Снижение веса в среднем на 10,5±5,1 кг, регистрируемое к концу КПВТ, встречалась в 2,3 раза чаще у пациентов 1 группы (19,2%) чем у пациентов среди пациентов 2 группы (8,3%).
Выпадение волос, жалобы на сухость кожи, зуд кожи регистрировались редко: в 1 группе у 2 человек (7,6%среди группы), во 2 группе чаще - у 3 человек(12,5%).
Обострение имеющихся сопутствующих соматических заболеваний встречались в обеих группах приблизительно с одинаковой частотой (30,1% и 27,6% соответственно). Чаще всего встречались обострения хронического панкреатита, язвенной болезни желудка, сахарного диабета.
Частота манифестации впервые выявленных соматических заболеваний на фоне проведения КПВТ имеет прямую корреляционную связь с используемыми препаратами, то есть значительно чаще выявляется при применении ИФН короткого действия, чем пролонгированных форм. При этом в 1 группе на фоне КПВТ манифестировали псориаз (7,6%), аутоиммунный тиреодит (15,3%). А во 2 группе выявлялись гипотиреоз и сахарный диабет (по 4,1% пациентов).
Гематологические осложнения встречались в обеих группах. Анемия, регистрируемая в виде снижения гемоглобина ниже 110г/л, встречалась чаще всего в середине терапии (24±3недели КПВТ). Во второй группе анемия выявлена достоверно чаще – в 2,4раза чаще (38,4%случаев), чем в 1 группе (16% случаев). Эритропоэтин для коррекции анемии применялся в 4 случаях (8%), у остальных коррекции анемии не требовалось.
Среди пациентов обеих групп при наличии анемии УВО встречается в 49,7% случаев, при отсутствии анемии достоверно реже (в 1,35 раз) - у 36,6% пациентов. Таким образом, наличие анемии, в сочетании с другими факторами можно считать предиктором эффективности КПВТ.
Напротив, частота тромбоцитопении на фоне КПВТ коррелировала с отсутствием УВО. Пациенты со снижением уровня тромбоцитов в 1,8 раз реже достигали УВО. Среди всех пациентов тромбоцитопения встречалась только у 8,0% пациентов, что реже, чем по литературным данным. В обеих группах частота данного побочного действия была одинаковой.
Выводы
1. Эффективность терапии с применением препаратов пегилированных или стандартных интерферонов оказалась сходной.
2. Гематологические нежелательные эффекты выявлены достоверно чаще при использовании пегилированных ИФН в составе противовирусной терапии.
3. Гриппоподобный на фоне КПВТ встречались достоверно чаще у пациентов, получающих стандартные ИФН.
5. Выявлена зависимость между достижением устойчивого вирусологического ответа и величиной снижения уровня гемоглобина.
Список использованных источников:
1. Беляева Н.М., Турьянов М.Х., Рабинович Э.З. Комбинированная терапия гепатита С рибавирином и альфа-интерфероном: Пособие для врачей. - М.: РМАПО. – 2002.
2. Громова Н.И. и Богомолов Б.П. Клиническая эффективность этиотропной терапии хронического вирусного гепатита С// Клин. мед. - 2003.-№1. - С.48.
3. Ивашкин В.Т. Комбинированное лечение хронического гепатита В// Российский журнал гастроэнтерологии, гепатологии, колопроктологии. 1998. №5. С. 57-60.
4. Ferenci P., Fried M., Shiffman M. et al. Predicting sustained virological responses in chronic hepatitis C patients treated with peginterferon alfa-2a// J. Hepatol. – 2005. – Vol. 43. – P. 425–433.
5. Fried M.W. Side effects of therapy of hepatitis C and their management. Hepatology. 2002. - P.237-244
6. Князькина О.В., Каган Ю.Д., Скачков М.В. Микробиоценоз кишечника у больных хроническим вирусным гепатитом С и его лечение// Врач-аспирант, №3.4(52), 2012. – С.579-586.
7. Пирогова И.Ю., Пышкин С.А. Неинвазивная диагностика стадии фиброза у пациентов с хроническими гепатитами В и С// Врач-аспирант, №2(45), 2011. – С. 21-27.
8. Попов С.С., Попов С.Ф. Динамика биохимических показателей гепато-билиарной системы рабочих основных цехов металлургического завода, инфицированных вирусами гемоконтактных гепатитов В и С// Врач-аспирант, №6(55), 2012. – С.55-61.
9. Рихсиева Г.М. Особенности клинико-иммунологических показателей детей, больных острыми вирусными гепатитами А и В, родившихся от матерей, злоупотребляющих алкоголем// Врач-аспирант, №4.4(47), 2011. – С. 675-681.
10. Рюмин А.М., Корочкина О.В., Соболевская О.Л. Закономерности естественного течения хронического гепатита В// Врач-аспирант, №4.1(53), 2012. – С. 214-223.
Подписано в печать: 01.02.2013
Доступность и широкое использование в клинической практике антиретровирусной терапии (АРВТ) для борьбы с вирусом иммунодефицита человека (ВИЧ) снизили частоту развития синдрома приобретенного иммунодефицита (СПИДа) и оппортунистических инфекций [1, 2, 3, 4]. Сдерживание этих заболеваний продлило жизнь ВИЧ-инфицированных, и они стали доживать до срока развития печеночной недостаточности в исходе хронического гепатита С (ХГС) [5, 6]. Есть сведения, что после внедрения АРВТ, смертность от болезней печени у ВИЧ-инфицированных увеличилась с 5-12% до 35-50% [7].
В Росийской Федерации по данным Федерального научно-методического центра по профилактике и борьбе со СПИДом в структуре летальных исходов среди больных ВИЧ-инфекцией терминальная стадия поражений печени в исходе хронических вирусных гепатитов до 2009 г. уже составляла существенную долю - 13,5-14,5%. В 2009 г. этот показатель вырос до 15,7%, хотя общая смертность среди ВИЧ-инфицированных снизилась с 3,4% (2008 г.) до 3% (2009 г.) [8].
Неблагоприятное течение гепатита С при наличии ВИЧ-инфекции, увеличение смертности от заболеваний печени, повышение риска гепатотоксического действия лекарственных препаратов - аргументы, указывающие на необходимость лечения гепатита С у больных ВИЧ-инфекцией [10, 11, 12].
Целью настоящего исследования явилось изучение эффективности противовирусной терапии (ПВТ) ХГС при моно- и коинфекции с ВИЧ.
Курс противовирусной терапии соответствовал рекомендуемым стандартам: при коинфекции ВИЧ/ХГС – 48 недель, независимо от генотипа вируса гепатита С (ВГС), при моноинфекции ХГС – 24-48 недель в зависимости от генотипа. У 5 (4,6%) больных коинфекцией ВИЧ/ХГС, в связи с поздней элиминацией РНК ВГС из сыворотки крови (к 24 неделе лечения), продолжительность терапии составила 72 недели. В исследование не были включены пациенты: ранее получавшие ПВТ, с микст-гепатитами, c серьезными хроническими сопутствующими заболеваниями, с компенсированным и декомпенсированным циррозом печени, принимающие алкоголь и наркотики, с уровнем СД4+ лимфоцитов менее 350 клеток/мкл.
Вирусологический мониторинг РНК ВГС методом полимеразной цепной реакции (ПЦР) проводился согласно рекомендациям Федерального научно-методического центра по профилактике и борьбе со СПИДом (2007 г.) на сроках 4 недели и в последующем каждые 12 недель. После завершения ПВТ больные обследовались в течение 2–х лет (1 раз в 6 месяцев). У всех больных коинфекцией определяли уровень CD4+лимфоцитов каждые 12/24 недели на протяжении курса наблюдения.
Высокую вирусную нагрузку РНК ВГС (более 2 млн. копий/мкл) имели 69 больных (63,3%) с коинфекцией ВИЧ/ХГС и 9 больных (36,0%) с моноинфекцией ХГС. Генотип 1 ВГС был обнаружен у 55 пациентов (50,5%) с коинфекцией и у 17 (68,0%) с моноинфекцией ХГС.
В соответствии с клинической классификацией ВИЧ-инфекции В.И. Покровского (2002г.) 48 больных (44,0%) коинфекцией ВИЧ/ХГС находились на субклинической стадии (3 стадия) ВИЧ-инфекции, 60 (55,0%) – на стадии 4А и 1 больной на стадии 4Б в фазах ремиссии. На момент начала противовирусной терапии 32 (29,4%) пациента получали антиретровирусную терапию.
Схемы АРВТ у 31 (96,9%) пациента включали бустированные ритонавиром ингибиторы протеазы (ИП): у 19 – лопинавир, у 6 – дарунавир, у 4-х – реатаз, по одному пациенту получали – телзир и саквинавир. Схему с ненуклеозидным ингибитором обратной транскриптазы (ННИОТ) – эфавирензом принимал один пациент (3,1%). Из нуклеозидных/нуклеотидных аналогов (НИОТ) пациенты получали ламивудин в сочетании с абакавиром - 90,6% (29 пациентов), либо с фосфазидом – 9,4% (3 пациента).
Статистическая обработка полученных результатов проводилась с помощью программного обеспечения Microsoft Excel и STATISTICA. При этом использовались параметрические методы оценки результатов – вычисление средней арифметической, среднеквадратического отклонения, средней ошибки средней арифметической. Оценка различий между сопоставляемыми группами по избранным критериям осуществлялась по критерию Стьюдента. Достоверность изменений признавалась при вероятности ошибки ρ меньшей или равной 0,05.
В группе больных моноинфекцией ХГС БВО наблюдался у 11 (44 %) больных: с 1-м генотипом у 5-ти (29,4%), с генотипом 2 и 3 – у 6-ти пациентов (75%). РВО был отмечен у 21 (84%) больного: с 1-м генотипом - у 13 (76,5%), с генотипом 2 и 3 – у 8 (100%) больных.
Из 109 коинфицированных ВИЧ/ХГС пациентов 63 (57,8%) человека прошли полный курс терапии. У 16 (14,7%) пациентов отсутствовал вирусологический ответа на фоне ПВТ, поэтому 11 человек из их завершили лечение в 24 недели, остальные 5 пациентов, в ввиду высокой приверженности, прошли 48–ми недельный курс. ПВТ была прекращена у 4 (3,7%) пациентов из-за вирусологического прорыва на сроках 24-36 недель и у 6 (5,5%) - из-за осложнений на сроках 22-47 недель. Отказались от продолжения лечения на сроках 33-38 недель 20 (19,2%) пациентов (все имели отрицательные результаты ПЦР-детекции РНК-ВГС на момент завершения ПВТ). Из них 17 пациентов сохранили устойчивый вирусологический ответ (УВО), у 3-х - через 6 месяцев после лечения наблюдался рецидив заболевания.
В группе больных ХГС моноинфекцией полный курс прошел 21(84,0%) пациент. Из 4-х пациентов (16,0%), у которых не снижалась вирусная нагрузка до 24 недель ПВТ, 2 - завершили лечение в 24 недели; 2 - продолжили курс до 48 недель.
Таким образом, завершили лечение с получением непосредственного вирусологического ответа 89 пациентов (81,7%) с коинфекцией ВИЧ/ХГС и 21 пациент (84,0%) с моноинфекцией ХГС. Не получен вирусологический ответ у 20 пациентов (18,3%) с ВИЧ/ХГС и у 4 (16,0%) - с моноинфекцией ХГС. Все пациенты, не ответившие на терапию, были инфицированы генотипом 1 ВГС.
В ходе исследования выявлено, что частота УВО у больных ВИЧ/ХГС коинфекцией составила 67,0%/73: с генотипом 1 – у 43,6%/24, с генотипом 2 и 3 – у 90,7%/49. Среди больных с моноинфекцией ХГС частота УВО составила 76,0%/19: с генотипом 1 – у 64,7%/11, с генотипом 2 и 3 в 100% случаев (n=8).
Рецидив заболевания (через 6 месяцев после окончания терапии) возник у 16 (14,7%) пациентов с ВИЧ/ХГС (с генотипом 1 – 11 человек и генотипом 2,3 – 5 человек) и у 2 (8,0%) с моноинфекцией (с 1 генотипом).
Таким образом, БВО у больных инфицированных ВГС генотипом 2, 3 прогнозировал более высокий процент УВО как при ко-, так и при моноинфекции. При генотипе 1 ВГС в обеих группах была низкая частота БВО – 23,6% и 29,4% соответственно, и частота УВО в этих группах была ниже. Лучший результат в достижении УВО при генотипе 1 наблюдался у больных моноинфекцией - 64,7% относительно 43,6% больных при коинфекции.
Как известно, при составлении прогноза эффективности лечения ХГС, традиционно, учитываются следующие факторы: возраст, стаж инфицирования ВГС и наличие фиброза, генотип ВГС и уровень вирусной нагрузки, а так же наличие быстрого клиренса РНК ВГС в ответ на ПВТ (БВО) [13, 14, 15]. Мы проанализировали данные критерии при сравнении групп больных в зависимости от достижения УВО. У больных коинфекцией дополнительно рассматривались показатели по ВИЧ-инфекции: уровень СД4+ лимфоцитов и прием антиретровирусных препаратов (табл. 1).
На рис. 1 представлены результаты по достижению УВО в зависимости от генотипа ВГС и проведения АРВТ.
Таблица 1. Сравнительная характеристика больных ВИЧ/ХГС в зависимости от достижения УВО (%).


Рис. 1. Устойчивый вирусологический ответ в зависимости от генотипа у пациентов, получавших и не получавших АРВТ: *р

Рис. 2. Динамика активности АлАТ у больных коинфекцией ВИЧ/ХГС в зависимости от результата УВО (ЕД/л)
Как известно, ПЕГ-ИФН и рибавирину свойственны разнообразные нежелательные явления. Нами проводился сравнительный анализ частоты выявления нежелательных явлений у пациентов с ВИЧ/ХГС коинфекцией и ХГС моноинфекцией. Выявлено, что нежелательные явления в обеих группах были однотипными и не отличались от ранее описанных в литературе [21, 23-25]. Кроме того, нами было замечено, что характер и выраженность нежелательных явлений зависят от сроков проведения ПВТ. Гриппоподобный синдром (подъем температуры до фебрильных цифр, озноб, головная боль, миалгия, артралгия) наблюдался на 1-2–й неделе лечения у 75,2% больных с ВИЧ/ХГС коинфекцией и был более выражен у больных ХГС моноинфекцией - 92% (р<0,02). В последующем температурная реакция снижалась, но начинали нарастать астенический синдром (слабость, недомогание, повышенная утомляемость, снижение работоспособности), чаще наблюдавшийся у больных коинфекцией - 89% против 60% больных с моноинфекцией, и диспепсический синдром (тошнота, сухость во рту, снижение аппетита).
На 4-12 неделе ПВТ в обеих группах регистрировались кожный зуд, сухость, гиперемия в местах инъекций. На 12-24-й неделе лечения отмечались усиление выпадения волос у 52 (47,7%) больных ВИЧ/ХГС и 11 (44,0%) - в группе ХГС и нейропсихические расстройства (раздражительность, снижение памяти и внимания, плаксивость, беспокойство, бессонница, апатия, плохое настроение) - у 47,7% больных ВИЧ/ХГС коинфекцией и 40% - ХГС. Коррекция депрессивных состояний осуществлялась при активном участии психиатра и психолога, в редких случаях назначались антидепрессанты. По литературным данным около 20% больных не доводят лечение до конца из-за непереносимости побочных реакций [26]. В нашем исследовании 18,3% больных ВИЧ/ХГС коинфекцией досрочно прекратили терапию на сроке 33-38 недель. Однако, несмотря на укорочение курса лечения, большинство из них - 85% имели УВО.
Как известно, терапия α-интерфероном и рибавирином часто вызывает гематологические нарушения. Среди наблюдаемых нами пациентов – 51,5 % имели снижение гематологических показателей (анемия, тромбоцитопения, нейтропения). Отмены противовирусной терапии не было ни в одном случае, что позволило закончить терапию с УВО у 37,6% больных с ВИЧ/ХГС коинфекцией и у 32% больных ХГС.
Нами проанализирован уровень СД4+ лимфоцитов у больных ВИЧ/ХГС коинфекцией во время проведения ПВТ в зависимости от наличия УВО (рис. 3).
Как видно из рис. 3, ни на одном этапе наблюдения нами не выявлено достоверных различий между исследуемыми группами.
В обеих группах в ходе терапии происходило снижение абсолютного количества СД4+ лимфоцитов: число больных с уровнем ниже 350 клеток/мкл составило 40,4%/44. Из них больше половины - 68,2%/30 достигли УВО. Среди 65 пациентов, у которых на фоне лечения уровень СД4+ сохранялся выше 350 клеток/мкл частота УВО составила 63,1%/41 (р>0,65).

Рис. 3. Динамика уровня СД4 лимфоцитов в зависимости от результата УВО на разных этапах ПВТ (кл/мкл)
Несмотря на то, что снижение СД4-лимфоцитов у большинства не сопровождалось развитием клинической симптоматики вторичных заболеваний, у 6 (5,5%) пациентов терапия была прекращена в связи с развитием осложнений (табл. 2). У всех был получен УВО: 4 пациента с 1 генотипом, 3 – с 3 генотипом.
Таким образом, укорочение курса ПВТ даже при наличии осложнений, явившихся причиной ее отмены, не повлияло на эффективность ПВТ.
Таблица 2. Осложнения на фоне ПВТ у больных ВИЧ/ХГС коинфекцией (n=6)

В группе больных моноинфекцией осложнений не наблюдалось.
Заключение
1. Противовирусная терапия ВГС-инфекции показывает высокую эффективность в плане достижения УВО у больных коинфекцией ВИЧ/ХГС преимущественно при генотипах 2,3 вируса.
2. Частота нежелательных явлений при проведении ПВТ у больных коинфекцией ВИЧ/ХГС не является критерием отмены лечения.
3. Сочетание антиретровирусной и противовирусной терапии ХГС снижает частоту УВО у больных коинфекцией преимущественно с 1 генотипом ВГС.
4. Снижение уровня СД4+ лимфоцитов на фоне проведения ПВТ не влияет на частоту УВО.
Список использованных источников:
1. Блохина Н.П. Клинические аспекты гепатита С у ВИЧ-инфицированных// Вирусные гепатиты: достижения и перспективы. Информ.- 2001.- № 2 (12). – С. 3-7.
2. Покровский В.В. и др. ВИЧ-инфекция и СПИД. - М.: ГЭОТАР-Медиа, 2010. - 192 с.
3. Murphy E., Collier A., Kalish L. et al. Highly active antiretroviral therapy decreases mortality and morbidity in patients with advanced HIV disease// Ann Intern Med. – 2001.- Vol. 135. – Р. 17–26.
4. Kakinami L., Block R.C., Adams M.J. et al. Risk of cardiovascular disease in HIV, hepatitis C, or HIV/hepatitis C patients compared to the general population// Int J Clin Pract. – 2013. - Vol. 67(1). – Р. 6-13.
5. Хоффман К., Рокштро Ю.К. Лечение ВИЧ-инфекции 2009.- М.: Р.Валент. - 2010.- С. 476-486.
6. George S., Gebhardt J., Klinzman D. et al. Hepatitis C viremia in HIV-infected individuals with negative ВГС antibody tests//J. Acquir Immun Defic Syndr. – 2002. - Vol. 31. – Р. 154–162.
7. Scott J., Kitahata M., van Rompaey S. et al. Hepatitis C virus co-infection is associated with higher risk of death due to HIV and liver-related diasease among an HIV-infected cohort// Program and abstracts of the 13th Conference on retroviruses and opportunistic infections; Febr. 5-8, 2006; Denver, Colorado.- Denver. - 2006. - Abstract 865.
8. Голиусов А.Т., Дементьева Л.А. Эпидемическая ситуация по ВИЧ-инфекции в Российской Федерации в 2009 г.// Журн. микробиол.- 2010. - №6. - С.31-34.
9. Бобкова М.Р., Самохвалов Е.И., Кравченко А.В. и др. Генетические варианты вируса гепатита С у ВИЧ-инфицированных наркоманов// Вопр. вирусол. - 2002. - Т. 47, №3.- С. 15-20.
10. Soriano V., Barreiro P. and Nunez M. Management of chronic hepatitis B and C in HIV-coinfected patients// Journal of Antimicrobial Chemotherapy.- 2006.- Vol. 57. – Р. 815–818.
11. Bambha K., Pierce C., Cox C. et al. Assessing mortality in women with hepatitis C virus and HIV using indirect markers of fibrosis// AIDS. – 2012. - Vol. 26(5). – Р. 599-607.
12. Bani-Sadr F., Krastinova E., Fromentin D. et al. Severe transaminitis after interferon-ribavirin therapy in HIV/ВГС-coinfected patients: influence of a sustained ВГС response// J Viral Hepat. – 2012. - Vol. 19(6). – Р. 431-435.
13. Лопаткина Т.Н. Возможности противовирусной терапии хронического гепатита С у больных, злоупотребляющих алкоголем// Гепатологический форум. - 2005. - №4. - С. 28.
14. Еналеева Д.Ш., Фазылов В.Х., Созинов А.С. Хронические вирусные гепатиты В и С. Что нужно знать о болезни? – М.: МЕДпресс-Информ, 2003. - 144 с.
15. Kenneth E Sherman et al. Sustained long-term antiviral maintenance therapy in ВГС/HIV сoinfected рatients (SLAM-C)// J. Acquir Immune Defic Syndr. – 2010. - Vol. 55(5). – Р. 597–605.
16. Solmone M., Girardi E., Lalle E. et al.. Evolution of HVR-1 quasispecies after 1-year treatment in HIV/ВГС-coinfected patients according to the pattern of response to highly active antiretroviral therapy// Antivir Ther. – 2006. - Vol. 11(1). – Р. 87-94.
17. Abbate I., Lo Iacono O., Di Stefano R. et al. J. HVR-1 quasispecies modifications occur early and are correlated to initial but not sustained response in ВГС-infected patients treated with pegylated- or standard-interferon and ribavirin// Hepatol. – 2004. - Vol. 40(5). – Р. 831-836.
18. Poizot-Martin I., Marimoutou C., Benhaim S. et al. Efficacy and tolerance of ВГС treatment in HIV-ВГС coinfected patients: the potential interaction of PI treatment// HIV Clin. Trials. – 2003. – Vol. 4(4). – Р. 262-268.
19. Кравченко А.В., Канестри В.Г., Ганкина Н.Ю. и др. Усиленные ритонавиром нгибиторы протеазы ВИЧ в составе схем первой линии АРВТ// Эпидемиология и инфекционные болезни, 2010.- №3.- С.22-27.
20. Poordad F.F., Flamm S.L. Virological relapse in chronic hepatitis C// Antivir Ther. - 2009. - Vol.14(3). – Р. 303-313.
21. Soriano V., Vispo E., Labarga P. et al. Uptate on HIV and ВГС coinfection// Hot Topics Viral Hep. – 2010. - Vol. 6(17). – Р. 17-22.
22. Канестри В.Г., Кравченко А.В. Особенности вирусного гепатита у больных ВИЧ-инфекцией.// Медицинская помощь. - 2001. - № 2. - С. 21-24.
23. Максимов С.Л. Клиническое течение, исходы и лечение вирусных гепатитов у больных ВИЧ-инфекцией: Автореф. дис. … д-ра мед. наук. – М., 2010. - 46 с.
24. Ивашкин В.Т. Диагностика, лечение и ведение пациентов с гепатитом С// Клин. микробиол. антимикроб. химиотер.- 2006, т. 8, №2. – С. 102-129.
25. Soriano V., Barreiro P. and Nunez M. Management of chronic hepatitis B and C in HIV-coinfected patients// Journal of Antimicrobial Chemotherapy.- 2006.- Vol. 57. – Р. 815–818.
26. Апросина З.Г., Игнатова Т.М., Козловская Л.В. Хронический вирусный гепатит/ Под ред. В.В. Серова, З.Г. Апросиной. - М.: Медицина, 2004.- 384 с.
Подписано в печать: 02.07.2013
Диагностическим тестом при гепатите С служит определение антител к вирусу методом ИФА (анти-HCV). Если антитела к HCV обнаружены, необходимо определять РНК HCV чувствительным методом молекулярной диагностики.
В случае положительного результата на антитела и отрицательного результата определения РНК-HCV необходимо выполнять повторные исследования для подтверждения выздоровления.
Цель лечения вирусного гепатита С
Цель лечения – полное удаление вируса и предупреждение заболеваний печени и внепеченочных заболеваний, включая воспалительно-дегенеративные поражения, фиброз, цирроз, рак печени и тяжелые внепеченочные проявления.
Контрольный показатель эффективности лечения
Устойчивый вирусологический ответ (УВО) – отсутствие вируса (определяемой РНК-HCV) через 12 и 24 недели после окончания лечения. Исследование необходимо проводить чувствительным методом молекулярной диагностики с нижним порогом определения 15 МЕ/мл и менее.
Результаты исследований с долгосрочным наблюдением показали, что УВО соответствует окончательному излечению от гепатита в 99% случаев.
У пациентов с циррозом и выраженным фиброзом исследования РНК-HCV следует продолжать и после получения УВО.
Обследование перед началом терапии (подробнее. )
Исключение других причин поражения печени
Прежде всего необходимо исключить другие факторы, влияющие на течение заболевания: наличие гепатотропных вирусов – гепатита В, ВИЧ, алкоголизма, аутоиммунного заболевания печени, поражение печени генетическими и метаболическими заболеваниями: гемахроматоз, сахарный диабет или ожирение, токсическое поражение печени и другие.
Оценка степени поражения печени.
Поскольку от стадии фиброза зависит вероятность выздоровления, прежде всего, необходимо выявление цирроза или выраженного фиброза. В настоящее время убедительно показана возможность оценки степени фиброза не инвазивными методами:
эластометрия / эластография (на аппарате фиброскан),
фибромакс и фибротест (по показателям крови)
Наиболее информативным является совместное определение степени фиброза (по крови и на аппарате фиброскан), что полностью заменяет биопсию.
Пациентам с циррозом необходимо исключать гепатоцеллюлярную карциному (первичный рак печени), а также осложнение цирроза – выраженную портальную гипертензию с расширением вен пищевода и желудка. С этой целью важно до начала терапии провести ЭГДС (гастроскопию).
Для оценки состояния печени проводится биохимическое обследование крови с определением структурных (АЛТ, АСТ, ГГТ) и функциональных показателей (альбумин, общий белок, белковые фракции, фракции липидов), а также общий клинический анализ крови.
Определение характеристик вируса.
Для назначения противовирусной терапии необходимо определить вирусную нагрузку и генотип вируса.
Количественное определение вируса должно проводиться чувствительным методом.
Генотипы устанавливаются методами, позволяющими достоверно определить подтип вируса (например, 1а и 1в), так как они влияют на выбор терапии.
Определение генетических характеристик пациента.
Определение генотипа интерлейкина 28В не потеряло своего прогностического значения.
Противопоказания для применения препаратов прямого противовирусного действия.
Абсолютных противопоказаний к применению препаратов прямого противовирусного действия нет.
Следует соблюдать меры предосторожности при лечении препаратом софосбувир пациентов с заболеваниями почек и сердца.
Пациентам с декомпенсированным циррозом класса В и С противопоказана комбинация препаратов Викейра Пак.
Продолжается исследование безопасности препарата симепревир для пациентов с декомпенсированным циррозом.
Показания к лечению: кого следует лечить?
Все пациенты с компенсированным и декомпенсированным хроническим гепатитом С являются кандидатами на лечение, если они не имеют противопоказаний.
Не имеет значения, получали они ранее терапию или нет.
Приоритет в лечении определяется стадией фиброза. В первую очередь следует назначать терапию пациентам с фиброзом F3-F4 по шкале METAVIR.
Пациентам с декомпенсированным циррозом (класс В и С по шкале Чайлд-Пью) лечение должно быть назначено незамедлительно. Желательно проводить его в условиях отделения трансплантологии.
К группе высокого приоритета относятся также пациенты, коинфецированные ВИЧ и гепатитом В, а также с клинически значимыми внепеченочными проявлениями, такими как васкулит, сопровождающийся криоглобулинемией.
Пациентам с умеренным фиброзом F2 назначение лечения оправдано, однако при необходимости оно может быть отложено (например, по материальным соображениям).
Время начала терапии у пациентов без проявлений или с легким течением заболевания (F0-1) и без внепеченочных симптомов определяется индивидуально.
Препараты прямого противовирусного действия, доступные в Европе.
СОФОСБУВИР – следует принимать в дозе 400 мг (1 таблетка) один раз в сутки.
Софосбувир выводится в основном (80%) почками с мочой, поэтому назначение его требует осторожности у пациентов с заболеваниями почек.
Возможны межлекарственные взаимодействия с многими препаратами, поэтому следует внимательно относиться к сопутствующим заболеваниям и корректировать прием препаратов, назначенных для лечения этих заболеваний.
ЛЕДИПАСВИР – доступен в комбинации с софосбувиром (400 мг софосбувира и 90 мг ледипасвира). Доза для приема – 1 таблетка в день независимо от приема пищи.
Так как ледипасвир может взаимодействовать с другими лекарственными препаратами, следует соблюдать меры предосторожности, с частым контролем функции почек. Кроме того, важно учитывать прием пациентом статинов и препаратов в схеме антиретровирусной терапии.
СИМЕПРЕВИР – следует принимать 1 капсулу 150 мг 1 раз в сутки. Пациентам, принимающим симепревир, противопоказаны некоторые препараты, в том числе антиретровирусные.
ДАКЛАТАСВИР – 1 таблетка 60 мг 1 раз в сутки. Многочисленные лекарственные взаимодействия даклатасвира требуют внимательного отношения при его назначении и соответственно контроля при его применении.
ВИКЕЙРА ПАК – комплексный препарат, включающий 4 действующих вещества (ритонавир, усиливающий действие паритапревира, омбитасвир и дасабувир).
Рекомендуемая дозировка 1 раз в сутки во время еды 2 таблетки ритонавира/паритапревира/омнитасвира, а также дасабувир 2 раза в сутки. При назначении следует учитывать многочисленные лекарственные взаимодействия и класс цирроза.
Варианты лечения различных групп пациентов.
Для лечения хронического гепатита С противовирусными препаратами прямого действия существует несколько различных схем, эффективность и безопасность которых проверена во многих клинических испытаниях.
Выбор комбинаций лекарственных средств осуществляется врачом и зависит от генотипа и подтипа вируса, тяжести заболевания печени, результатов предшествующей терапии.
Длительность терапии зависит от степени поражения печени и наличия компенсированного или декомпенсированного цирроза. Стандартный курс терапии – 12 недель, при циррозе может быть увеличен до 24 недель.
Возможно назначение дополнительно к схеме лечения препарата рибавирин у пациентов с циррозом и с отрицательными прогностическими факторами ответа на лечение, например, при содержании тромбоцитов менее 75х10^3/мкл.
Для лечения пациентов с генотипом 1 (1а и 1в) существует 4 рекомендованные схемы препаратов прямого противовирусного действия:
Для лечения пациентов с генотипом 2 существует только одна безинтерфероновая схема: софосбувир+даклатасвир в течение 12 недель.
Пациентов с циррозом, ранее уже получавших или не получавших терапию, следует лечить также 12 недель.
Для лечение пациентов, инфицированных HCV генотипа 3, пока существует только одна схема безинтерфероновой терапии: софосбувир +даклатасвир. Ледипасвир в отношении HCV генотипа 3 значительно менее эффективен, чем даклатасвир, поэтому схемы с применением ледипасвира для этого генотипа не рекомендованы.
Пациентам с HCV генотипа 3 с циррозом, получавшим или не получавшим ранее терапию, следует назначать эту схему лечения с добавлением рибавирина и длительностью курса 24 недели.
Контроль лечения
В процессе лечения необходимо контролировать эффективность и безопасность (побочные нежелательные эффекты).
Контроль эффективности лечения основан на регулярном определении уровня РНК HCV с использованием чувствительных количественных методов.
РНК HCV следует определять до начала терапии, через 2 недели, а затем через 4, 8 и 12 недель, а также через 12 и 24 недели после окончания курса лечения.
Прекращение терапии вследствие ее бесперспективности при лечении препаратами прямого противовирусного действия правилами НЕ предусмотрено.
Контроль безопасности лечения
Схемы лечения препаратами прямого противовирусного действия хорошо переносятся. Случаи выраженных нежелательных явлений, требующих отмены препаратов, отмечены редко.
Однако, во время терапии необходимо контролировать проявления токсичности других препаратов, применяемых для лечения сопутствующих заболеваний, а также проявления лекарственных взаимодействий. При лечении схемами, содержащими софосбувир, необходимо контролировать состояние почек.
Наиболее часто отмечаются утомляемость и головная боль.
Лечение следует безотлагательно прекратить при обострении гепатита (АЛТ выше нормы в 10 раз).
Тактика лечения пациентов с ожирением и метаболическим синдромом
При выявлении у пациентов с HCV сопутствующего поражения печени в результате метаболического синдрома (неалкогольная жировая болезнь печени - стеатоз) необходимо провести дополнительное обследование на показатели обменных и гормональных нарушений, характерных для этого заболевания.
Рекомендуется для оценки степени поражения печени использовать исследование крови – Фибромакс, которое дает возможность оценить отдельно степень поражения печени вирусом и отдельно метаболическим синдромом.
Тактика лечения зависит от степени поражения печени в целом, и отдельно каждым повреждающим фактором. Лечение противовирусными препаратами может быть назначено сразу, а дальнейшее лечение метаболического синдрома после получения УВО.
Если степень поражения печени вирусом значительно меньше, чем метаболическим синдромом, возможно начинать противовирусную терапию после лечения метаболического синдрома.
В случаях наличия сопутствующих заболеваний печени необходимо ставить целью лечения не только получение УВО, но и сохранение и восстановление печени, пострадавшей от других патологических факторов.
Читайте также:

