Тест система иммуноферментная для выявления антител к вирусу гепатита в дс ифа
Обновлено: 24.04.2024
Характеристика и принцип работы набора
2.1 Состав набора:
Положительный контрольный образец (К + )
Отрицательный контрольный образец (К – )
Слабоположительный контрольный образец (Ксл + )
Раствор для разведения конъюгата №1 (РР-К1)
2 флакона по 6 мл
Раствор для разведения конъюгата №2 (РР-К2)
2 флакона по 6 мл
Буферный раствор для субстрата (БРС)
2 флакона по 13 мл
25-кратный концентрат фосфатно-солевого буферного раствора с твином (ФСБ-Т×25)
2 флакона по 28 мл
Комплект ванночки для реагентов с наконечниками для многоканальных пипеток
2.2 Основные компоненты набора "ИФА-HBsAg" – иммуносорбент, конъюгат №1 и конъюгат №2.
Иммуносорбент представляет собой полистирольный планшет, в лунках которого сорбированы поликлональные антитела к HВs-антигену.
Конъюгат №1 представляет собой меченые биотином моноклональные антитела к HBs-антигену.
Конъюгат №2 представляет собой стрептавидин, конъюгированный с пероксидазой хрена.
Положительный контрольный образец – сыворотка крови человека, содержащая НВs-антиген, не содержащая антитела к ВИЧ-1, ВИЧ-2 и вирусу гепатита С, инактивированная прогреванием в течение 3 ч при температуре 56 ºC.
Отрицательный контрольный образец – сыворотка крови человека, не содержащая НВs-антиген, антитела к ВИЧ-1, ВИЧ-2, вирусу гепатита С, инактивированная прогреванием в течение 3 ч при температуре 56 ºC.
Слабоположительный контрольный образец – лиофилизированный препарат сыворотки крови человека, содержащей рекомбинантный НВs-антиген с концентрацией 0,25 нг/мл, не содержащей антитела к ВИЧ-1, ВИЧ-2, вирусу гепатита С и НВs-антиген, инактивированной прогреванием в течение 3 ч при температуре 56 ºC.
Принцип работы набора. При внесении в лунки планшета конъюгата №1 и образцов сывороток (плазмы) инфицированной крови HВs-антиген связывается как с поликлональными антителами к HВs-антигену, сорбированными на твердой фазе, так и с моноклональными антителами к HBs-антигену, входящими в состав конъюгата №1, образуя комплексы антитело-антиген-конъюгат. Иммунные комплексы антитело-антиген-конъюгат выявляются конъюгатом №2. После отмывания несвязавшихся компонентов связавшийся конъюгат №2 выявляют, добавляя в лунки планшета раствор субстрата пероксидазы (перекись водорода) и хромогена ТМБ.
Пероксидазную реакцию останавливают, добавляя стоп-реагент (0,9 М раствор серной кислоты), и интенсивность окрашивания раствора в лунках измеряют на спектрофотометре как величину оптической плотности (ОП) при длине волны 450 нм.
Величина ОП прямо пропорциональна концентрации HВs-антигена в образце сыворотки или плазмы крови человека. Чем выше содержание HВs-антигена в образце сыворотки, тем выше интенсивность окрашивания.
2.3 Набор рассчитан на проведение 24 постановоки ИФА: 1 постановка – 1 стрип (8 лунок). Всего – 192 определения, включая контрольные образцы.
3.1 Все компоненты набора в используемых концентрациях являются нетоксичными. Однако работа со всеми исследуемыми образцами сыворотки (плазмы) крови человека, которые следует рассматривать как потенциально инфицированные, способные сохранять и передавать ВИЧ, вирус гепатита В или любой другой возбудитель вирусной инфекции, с отработанными растворами и жидкостями, различным оборудованием, которое может быть загрязнено в процессе анализа, требует определенных мер безопасности при использовании набора:
- работу необходимо проводить в специально оборудованном помещении;
- работать необходимо с применением средств индивидуальной защиты и с соблюдением мер предосторожности в соответствии с требованиями [1], [2], и [3].
3.2 Стоп-реагент, содержащий серную кислоту, обладает раздражающим действием. При попадании на кожу и слизистые немедленно промыть большим количеством воды.
3.3 При работе с набором рабочие места должны быть обеспечены приточно-вытяжной вентиляцией.
3.4 Все лица, работающие в лаборатории с наборами, должны проходить обязательный медицинский осмотр в соответствии с требованиями [4].
3.5 Утилизация медицинских отходов и/или неиспользованных наборов с истекшим сроком годности должна производиться в соответствии с требованиями [5].
4.1 Для исключения ложных результатов исследуемые образцы необходимо готовить и хранить в условиях, предотвращающих бактериальный пророст. Необходимо осветлять образцы сывороток, содержащие агрегированные компоненты сыворотки или осадок, при помощи центрифугирования в течение 15 мин при скорости вращения 3000 об/мин. Образцы сывороток можно хранить при температуре (2-8) °С не более 7 суток. Замороженные образцы (желательно до температуры не менее минус 20 °С) можно хранить не более 6 месяцев. Необходимо избегать повторных циклов замораживания-оттаивания образцов.
Необходимо помнить, что образцы с гемолизом, гиперлипидемией, бактериальным проростом, а также длительно хранившиеся без замораживания не пригодны для анализа.
Надежность результатов зависит от выполнения следующих правил:
- не допускается использование набора после окончания срока годности, а также смешивание компонентов наборов разных серий;
- для приготовления каждого реагента должна использоваться отдельная емкость;
- всю используемую для приготовления реагентов посуду не обрабатывать дезрастворами и моющими средствами. В случае необходимости промыть водой питьевой проточной, а затем пять раз ополоснуть дистиллированной водой;
- для работы с хромогеном ТМБ необходимо использовать отдельные емкости для растворов, наконечники для пипеток, посуду.
- необходимо обратить внимание на тщательное перемешивание реагентов;
- при внесении в лунки стрипов раствора Кг-1 в рабочем разведении или раствора Кг-2 в рабочем разведении нельзя касаться наконечником пипетки поверхности планшета и раствора, находящегося в лунках во избежание случайного заноса образца из одного стрипа в другой через наконечники;
- время между заполнением и опорожнением лунок планшета растворами и реагентами должно быть не менее 30 с. Не допускается подсыхание лунок на всех этапах постановки ИФА;
- при использовании промывателя следить за состоянием емкости для раствора для промывания планшета и соединительных шлангов: в них не должно быть признаков бактериального или грибкового роста;
- необходимо использовать пипетки автоматические со сменными наконечниками, аттестованные по значению средней дозы и сходимости результатов пипетирования (погрешность не более 3 %);
- дозаторы и рабочие поверхности обрабатывать раствором с объемной долей спирта этилового 70 %. Не использовать хлорамин и другие хлорсодержащие вещества;
- для работы с исследуемыми сыворотками и контрольными образцами рекомендуется использовать одноразовые наконечники для пипеток. Каждый образец сыворотки, а также реагенты набора необходимо отбирать отдельным наконечником.
- во время проведения анализа следует избегать попадания прямых солнечных лучей на рабочую поверхность.
4.2 При вскрытии и растворении лиофилизированных компонентов необходимо следить, чтобы на крышке и стенках флаконов не оставалось сухого вещества.
5.1 Спектрофотометр вертикального сканирования, позволяющий проводить измерения оптической плотности растворов в лунках планшета при длине волны 450 нм;
- полу- или автоматическое устройство для промывания планшетов (вошер);
- суховоздушный термостат типа ТС-80 М2, поддерживающий температуру (37±1) °С, или аналогичный ему по характеристикам;
- пипетки одноканальные автоматические со сменными наконечниками, позволяющие отбирать объемы жидкости от 0,02 до 5,0 мл;
- мерный цилиндр вместимостью 1000 мл;
- колба лабораторная вместимостью 1000 мл;
- флаконы стеклянные вместимостью 20 мл;
- ванночки для реагентов или чашки Петри (диаметр 100 мм);
- вата медицинская гигроскопическая;
- перчатки резиновые хирургические;
- раствор с объемной долей спирта этилового 70 %;
- раствор с массовой долей перекиси водорода 6 %;
- вода деионизированная или дистиллированная;
- контейнер для сбора твердых отходов;
- контейнер для слива жидких отходов.
Содержимое флаконов с реагентами, входящими в состав набора, и все образцы исследуемых сывороток (плазмы) крови человека перед проведением анализа тщательно перемешать.
Расход реагентов набора для постановки анализа, который определяется количеством используемых стрипов, приведен в таблице А.1 Приложения А.
6.2 Подготовка иммуносорбента
Иммуносорбент готов к использованию.
Открыть пакет и установить на рамку необходимое количество стрипов. Оставшиеся стрипы хранить в плотно закрытом пакете с влагопоглотителем при температуре (2-8) °С в не более 3 месяцев.
6.3 Приготовление раствора для промывания планшета
Внимание! Раствор для промывания планшета готовить за 15 мин до начала проведения анализа!
Если флакон с ФСБ-Т×25 содержит осадок, его необходимо прогреть перед использованием при температуре (37±1) °С до полного растворения осадка.
В мерный цилиндр вместимостью 1000 мл внести содержимое флакона с ФСБ-Т×25, затем добавить дистиллированной воды до метки 700 мл и аккуратно перемешать раствор.
В случае использования одного или несколько стрипов содержимое флакона с ФСБ-Т×25 интенсивно встряхнуть в течение (20-30) с, отобрать необходимый объем раствора (таблица A.1 Приложения А) в мерный стакан или цилиндр, добавить необходимое количество дистиллированной воды и перемешать раствор.
Неиспользованный ФСБ-Т×25 можно хранить в плотно закрытом флаконе при температуре (2-8) °С в течение срока годности набора.
6.4 Подготовка К + , К – , РР-К1, РР-К2, БРС и стоп-реагента
К + , К – , РР-К1, РР-К2, БРС и стоп-реагент готовы к использованию.
Неиспользованные РР-К1, РР-К2, БРС и стоп-реагент после вскрытия флаконов можно хранить в плотно закрытых флаконах при температуре (2-8) °С в течение срока годности набора.
Остаток К + и К - после вскрытия флаконов можно хранить в плотно закрытых флаконах при температуре (2-8) °С в течение срока годности набора.
6.5 Приготовление раствора Ксл +
Внимание! Раствор Ксл + готовить за 15 мин до начала проведения анализа!
Восстановленный Ксл + можно хранить в закрытом флаконе при температуре (2-8) °С не более 1 месяца , при температуре минус 20 °С – в течение шести месяцев. Допускается однократное замораживание-оттаивание восстановленного Ксл + .
6.6 Приготовление раствора Кг-1 в рабочем разведении
Из флакона с Кг-1 отобрать указанный в таблице А.1 Приложения А объем и перенести во флакон с РР-К1. Содержимое флакона тщательно перемешать, не допуская образования пены.
В случае использования одного или несколько стрипов в чистый флакон отобрать необходимое количество РР-К1, добавить Кг-1 в соответствии с таблицей А.1 Приложения А и перемешать раствор, не допуская образования пены.
Остаток Кг-1 можно хранить в плотно закрытом флаконе при температуре (2-8) °С в течение срока годности набора.
6.7 Приготовление раствора Кг-2 в рабочем разведении
Из флакона с Кг-2 отобрать указанный в таблице А.1 Приложения А объем и перенести во флакон с РР-К2. Содержимое флакона тщательно перемешать, не допуская образования пены.
В случае использования одного или несколько стрипов в чистый флакон отобрать необходимое количество РР-К2, добавить Кг-2 в соответствии с таблицей А.1 Приложения А и перемешать раствор, не допуская образования пены.
Остаток Кг-2 можно хранить в плотно закрытом флаконе при температуре (2-8) °С в течение срока годности набора.
6.8 Приготовление рабочего раствора субстрата
Флакон с хромогеном ТМБ необходимо прогреть перед использованием в течение (3-5) мин при температуре (37±1)° С до полного растворения кристаллов.
Из флакона с хромогеном ТМБ отобрать указанный в таблице А.1 Приложения А объем и перенести во флакон с БРС. Содержимое флакона тщательно перемешать, не допуская образования пены.
В случае использования одного или несколько стрипов в чистый флакон из темного стекла или пластика (прозрачный флакон обернуть флакон) отобрать необходимое количество БРС, добавить хромоген ТМБ в соответствии с таблицей A.1 Приложения А и перемешать раствор, не допуская образования пены.
Раствор необходимо предохранять от попадания света и контакта с металлами или ионами металлов. Перед использованием раствор субстрата должен быть бесцветным. Посуду, которая будет в ходе реакции контактировать с раствором субстрата, отмывать без применения синтетических моющих средств. Использовать только новую ванночку для реагентов и новые наконечники!
Остаток хромогена ТМБ можно хранить в плотно закрытом флаконе при температуре (2-8) °С в течение срока годности набора.
- на всех этапах промывания необходимо контролировать заполнение всех лунок и полное удаление (аспирацию) жидкости из них;
- необходимо при каждом промывании во все лунки планшета вносить не менее 380 мкл раствора для промывания планшета;
- необходимо выдерживать лунки, заполненными раствором для промывания планшета, в течение 30 с;
- при каждой аспирации тщательно удалять остатки жидкости из лунок постукиванием рамкой со стрипами в перевернутом положении по сложенной в несколько раз фильтровальной бумаге, положенной на лист полиэтилена;
- некачественное промывание планшета приводит к получению некорректных результатов.
8.1 В лунки, предназначенные для контрольных образцов внести:
- в две лунки планшета – по 0,1 мл (100 мкл) К + ;
- в две лунки планшета – по 0,1 мл (100 мкл) Ксл + ;
- в две лунки планшета – по 0,1 мл (100 мкл) К – .
Во все остальные лунки планшета внести по 0,1 мл (100 мкл) исследуемых образцов сыворотки (плазмы) крови человека.
Внести во все лунки планшета по 0,05 мл (50 мкл) раствора Кг-1 в рабочем разведении (п 6.6).
Внимание! При постановке ИФА на одном или двух стрипах допускается использовать для К – – две лунки, для К + – одну лунку, для Ксл + – одну лунку.
Внимание! Время внесения контрольных и исследуемых образцов не должно превышать (5-10) мин! Каждый образец необходимо отбирать одноразовым наконечником!
Содержимое лунок перемешать осторожным постукиванием по краю планшета
8.2 Планшет заклеить пленкой или закрыть крышкой и инкубировать при температуре (37±1) °С в течение 60 мин в термостате.
Внимание! За (1-2) мин до окончания инкубации приготовить раствор Кг-2 в рабочем разведении (п 6.7).
8.3 По окончании инкубации внести во все лунки планшета по по 0,05 мл (50 мкл) раствора Кг-2 в рабочем разведении (п 6.7). Содержимое лунок перемешать осторожным постукиванием по краю планшета
8.4 Планшет заклеить пленкой или закрыть крышкой и инкубировать при температуре (37±1) °С в течение 30 мин в термостате.
8.5 Удалить содержимое лунок, затем промыть лунки планшета раствором для промывания планшета (п 6.3) семь раз. Для этого во все лунки планшета необходимо внести не менее 380 мкл раствора для промывания планшета, а затем удалить содержимое лунок в емкость с дезраствором.
По окончании промывания тщательно удалить остатки жидкости из лунок, активно постукивая планшетом в перевернутом положении (лунками вниз) по сложенной в несколько раз фильтровальной бумаге, положенной на лист полиэтилена.
8.6 Во все лунки планшета внести по 0,1 мл (100 мкл) рабочего раствора субстрата (п 6.8). При приготовлении рабочего раствора субстрата (п.6.8) флакон с хромогеном ТМБ необходимо прогреть перед использованием в течение (3-5) мин при температуре (37±1)° С до полного растворения кристаллов
8.7 Планшет заклеить пленкой или закрыть крышкой и инкубировать в термостате при температуре (37±1) °С в защищенном от света месте в течение 15 мин.
Внимание! По окончании инкубации в лунках с образцами сывороток, содержащими HBs-антиген, произойдет изменение окраски раствора различной интенсивности в зависимости от концентрации HBs-антигена в исследуемом образце сыворотки: от бесцветной до голубой.
8.8 Остановить пероксидазную реакцию путем внесения во все лунки по 0,05 мл (50 мкл) стоп-реагента.
Внимание! В лунках с образцами сывороток, содержащими HBs-антиген, произойдет изменение окраски раствора: с голубой на желтую.
8.9 Не позже чем через 10 мин после остановки реакции определить значение ОП раствора в лунках в двухволновом режиме: 450 нм относительно (620-700) нм. Допускается измерение ОП в одноволновом режиме при длине волны 450 нм.
Современная диагностика гепатита В. Выявление HBsAg
Серологическая диагностика гепатита В в настоящее время строится на основании определения маркеров НВ-вирусной инфекции, как правило, с помощью имуноферментного анализа, то есть антигенов вируса гепатита В или антител к ним в биологических субстратах, главным образом, в сыворотке крови. В качестве основных маркеров гепатита В, имеющих самостоятельное значение для серологической диагностики, сегодня признаны:
HBsAg (поверхностный антиген вируса гепатита В) — основной маркер, свидетельствующий о наличии вируса гепатита В. При остром гепатите В HBsAg можно обнаружить еще в продромальном периоде, и длительность его персистенции при неосложненном течении составляет до 10 недель;
HBeAg — показатель высокой степени активности инфекционного процесса. Маркер репликации HBeAg определяется, как правило, при наличии HBsAg, однако циркулирует в крови менее продолжительное время — в среднем 4 недели;
anti-HBc класса IgM — показатель острого инфекционного процесса или, при хронических формах гепатита В, косвенный показатель активной репликации HBV. Возможна их длительная циркуляция;
anti-HBe — не являются показателем, характеризующим какое-либо конкретное состояние при гепатите В. Эти антитела могут быть и в конце острого гепатита В и при хроническом гепатите и в случаях, так называемого здорового носительства HBsAg.
Хронический гепатит В: в фазу обострения наблюдается следующий профиль маркеров: HBsAg, HBeAg, DNA HBV, anti-HBc IgM и суммарные. В период стихания процесса обнаруживаются HBsAg, anti-HBc IgG (суммарные), возможна сероконверсия HBeAg на anti-HBe.
В основе всей серологигеской диагностики гепатита В: как острых, так и хронигеских форм—лежит определение HBsAg. Современные иммуноферментные тест-системы позволяют выявлять HBsAg в концентрациях до 0,1 нг/мл. Схема определения у разных тест-систем, как правило, одна и та же. В качестве иммуносорбента используются антитела к HBsAg. Как правило, применяются моноклональные антитела.
Именно они обеспечивают строгую специфичность применяемых в настоящее время диагностических наборов.
ПЦР (полимеразная цепная реакция) в диагностике гепатита В
Метод полимеразной цепной реакции используют для подтверждения НВ-вирусной инфекции, наличия репликации вируса при остром и хроническом гепатите В, а также определения эффективности курса лечения. Наибольшей чувствительностью обладает двойной нестед-метод, который предполагает использование двух пар праймеров. Чувствительность нестедметода весьма высока и позволяет выявлять несколько копий DNA HBV в образце, что существенно превосходит возможности ИФА.
Сегодня разработаны соответствующие технологии производства отечественные тест-системы для детекции DNA HBV с помощью ПЦР, которые активно применяются в практическом здравоохранении. Высокая чувствительность ПЦР-диагностики при гепатите В расширила возможности раннего определения вируса гепатита В при острой инфекции. Длительность инкубационного периода при гепатите В достигает 6 месяцев, а в ряде случаев и больше. В это время вирус попадает в кровь, проникает в клетки печени, запускается механизм репликации, и в результате размножение приобретает устойчивый характер.
Эти процессы не затрагивают в значительной степени жизнедеятельность печени и других органов в течение длительного времени. В этот период эффекторные реакции иммунной системы организма не задействованы. Число вирусных частиц резко возрастает к концу инкубационного периода и становятся максимальными. В этот период методом ПЦР можно обнаружить в крови вирус гепатита В, тогда как остальные маркеры НВ-вирусной инфекции, главным образом серологические, ещё отсутствуют. Таким образом, с помощью полимеразной цепной реакции стала возможной более ранняя диагностика острого гепатита В.
Белки и антигены вируса гепатита С. Диагностика ВГС
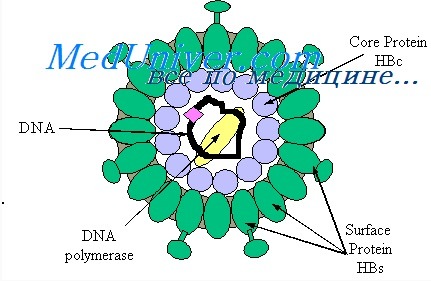
Сегодня известно минимум 10 структурных и неструктурных белков, кодируемых геномом HCV. К структурным белкам относят core, envelop 1 и envelop 2. Белок core является белком нуклеокапсида, тогда как envelop 1 и envelop 2 — гликопротеины внешней оболочки вируса. В структурной зоне кодируется также белок р7, функция которого не ясна, однако аналогия с другими представителями семейства Flaviviridae позволяет предположить, что его функция связана с высвобождением вириона из инфицированной клетки.
Этот белок отщепляется клеточной пептидазой от envelop 2, но не во всех случаях, что обусловливает существование envelop 2 в виде двух форм более и менее протяженной.
Неструктурная область генома HCV кодирует 6 белков — NS2, NS3, NS4A, NS4B, NS5A и NS5B. Белок NS2 является вирусной металлозависимой протеиназой. Белок NS4A действует как эффектор или кофактор для NSЗ-протеолитической активности в NS4A/NS4B, NS4B/NS5A, NS5A/NS5B сайтах нарезания полипротеина вируса.
В настоящее время фрагменты структурных и неструктурных белков, полученных генноинженерным путем (рекомбинантные белки) или с помощью химического синтеза, используют в качестве антигенов при конструировании иммуноферментных тест-систем. Первое поколение иммуноферментных тест-систем появилось на рынке в 1989 году и было основано на прямом ИФА. В качестве иммуносорбента были использованы фрагменты двух белков, NS3 и NS4, обозначаемых как 5-1-1 и С100-3.
Одновременно были разработаны и подтверждающие тесты на основе иммуноблота с рекомбинантными белками (RIBA). Чувствительность этих тест-систем первого поколения составляла только 64% для ИФА и 55% для иммуноблота. Тест-системы второго поколения появились на рынке в 1991 году. В качестве антигенов, сорбированных на твердой фазе, в этих тест-системах использовали капсидные белки (фрагмент с22-3) и антигены неструктурных регионов NS3 (фрагменты с200 и сЗЗс) и NS4, что позволило повысить чувствительность и специфичность исследований. Поскольку гуморальный иммунный ответ на капсидные антигены (структурные белки) нагинается быстрее, гем на неструктурные белки, период от инфицирования до выявляемой сероконверсии удалось уменьшить до двух месяцев.
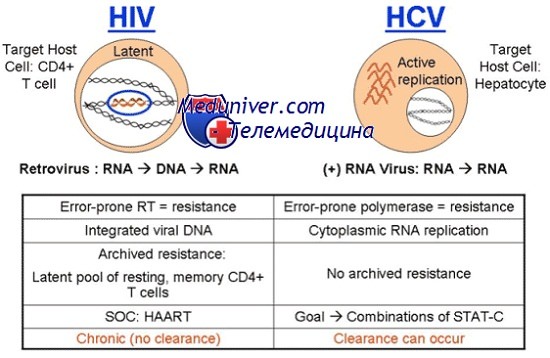
Подтверждающие тест-системы на основе иммуноблота позволяли идентифицировать участвующие в реакции антигены. Результаты, полученные при помощи этих тест-систем, интерпретировали как положительные лишь при реакции антител, находящихся в исследуемом субстрате, по крайней мере, с двумя антигенами, тогда как при наличии реакции лишь с одним из антигенов результат считали неопределенным. Было установлено, что специфичность второго поколения тест-систем зависела от источника антигенов. В 1993 году на рынке появилось третье поколение тест-систем. В дополнение к вышеупомянутым антигенам в этих тест-системах используются также антигены, аминокислотная последовательность которых соответствует иммунодоминантным участкам NS5 белков.
В тест-системах первого, второго и третьего поколений в качестве антигенов использовались или рекомбинантные, или синтетические пептиды. В настоящее время можно выделить также тест-системы четвертого поколения, в которых в качестве иммуносорбента используют сочетания рекомбинантных и синтетических пептидов.
Опыт применения тест-систем различных поколений в мире очень большой. Было установлено, что если с помощью тест-систем первого или второго поколения у больных с острым вирусным гепатитом С антитела выявляли на 10-16, а в ряде случаев и 25-30 неделе от начала заболевания, то диагностикумы третьего поколения позволяли сократить этот срок до 2-3 недель. Согласно обобщенным данным чувствительность тест-систем первого, второго и третьего поколений составляет соответственно 70-80%, 92-95% и 97%.
В то же время, по данным С. Colin, 2001, чувствительность тест-систем третьего поколения составила 98,9% у пациентов с хроническими заболеваниями печени и 97,2% на специальных контрольных панелях сывороток. Достижение высокой чувствительности иммуноферментных тест-систем 3 и 4 поколения сопряжено с некоторыми проблемами в обеспечении специфичности исследований, что в ряде случаев может приводить к появлению ложноположительных результатов. В литературе имеются данные о возможных погрешностях в специфичности ELISA 3 тест-систем. Они являются общими для всех ELISA тест-систем, включая тест-системы для диагностики СПИДа.
Ложнопозитивные результаты могут быть следствием повышенного содержания в образцах гамма-глобулинов (сыворотки пациентов африканской расы, миеломная болезнь, ревматоидные факторы), заболеваний печени (цирроз, рак), аутоиммунных заболеваний (коллагенозы, аутоиммунные гепатиты), других вирусных инфекций (ВИЧ, гепатит В) и длительного хранения сывороток в меняющихся температурных условиях. Проведение какой-либо иммунизации также может сопровождаться повышением частоты ложнопозитивных реакций. Рекомендуемые в настоящее время меры по устранению этой проблемы следующие: а) повторная постановка образца в этой же ИФТС; б) повторная детекция anti-HCV в другой ИФТС; в) использование подтверждающих тестов на основе ИФА и иммуноблота.
Однако использование предлагаемых способов подтверждения результатов зачастую приводят к расхождениям в их итоговой трактовке, что показано исследованиями российских и зарубежных исследователей.
В настоящее время производители ИФТС для детекции anti-HCV достигают высокой чувствительности или за счет более полного выявления антител к NS3 или антител к антигенам core. Сравнительные исследования, выполненные на различных группах риска и специальных контрольных панелях показали, что тест-системы, лучше выявлявшие антитела к NS3, оказались несколько более чувствительными, чем тест-системы, лучше выявлявшие антитела к антигенам core. Их чувствительность составляла, соответственно 99,9% и 98,6%.

На нашем YouTube-канале опубликована серия видео по ИФА-диагностике респираторных инфекций. Подробнее
Новый набор для дифференциального выявления IgG к S- и N-белкам SARS-CoV-2. Подробнее
HBsAg-ИФА-БЕСТ (комплект 1/авто)
Набор реагентов для иммуноферментного выявления HBs-антигена вируса гепатита В.
Срок годности: 12 месяцев
HBsAg-ИФА-БЕСТ (комплект 2)
Набор реагентов для иммуноферментного выявления HBs-антигена вируса гепатита В.
Срок годности: 12 месяцев
HBsAg-ИФА-БЕСТ (комплект 3)
Набор реагентов для иммуноферментного выявления HBs-антигена вируса гепатита В.
Срок годности: 12 месяцев
HBsAg-подтверждающий-ИФА-БЕСТ
Набор реагентов для иммуноферментного подтверждения присутствия HBs-антигена вируса гепатита В.
Срок годности: 12 месяцев
Вектогеп B-HBs-антиген-авто (комплект 1)
Набор реагентов для иммуноферментного выявления HBsAg для автоматических ИФА анализаторов.
Вектогеп B-HBs-антиген-авто (комплект 2/Чароит)
Набор реагентов для иммуноферментного выявления HBsAg для автоматических ИФА анализаторов.
Вектогеп B-HBs-антиген (комплект 1)
Набор реагентов для иммуноферментного выявления HBsAg. Одностадийная постановка.
Срок годности: 24 месяцев
Вектогеп B-HBs-антиген (комплект 2)
Набор реагентов для иммуноферментного выявления HBsAg. Одностадийная постановка.
Срок годности: 24 месяцев
Вектогеп B-HBs-антиген (комплект 3)
Набор реагентов для иммуноферментного выявления HBsAg. Одностадийная постановка.
Срок годности: 24 месяцев
Вектогеп B-HBs-антиген (комплект 4)
Набор реагентов для иммуноферментного выявления HBsAg. Одностадийная постановка.
Срок годности: 24 месяцев
Вектогеп В-HBs-антиген-подтверждающий тест (комплект 1)
Набор реагентов для иммуноферментного подтверждения наличия HBsAg. Одностадийная постановка.
Срок годности: 24 месяцев
Вектогеп В-HBs-антиген-подтверждающий тест (комплект 2)
Набор реагентов для иммуноферментного подтверждения наличия HBsAg. Одностадийная постановка.
Срок годности: 24 месяцев
HBsAg-ИФА-БЕСТ-количественный
Набор реагентов для иммуноферментного количественного определения HBs-антигена вируса гепатита В в сыворотке (плазме) крови
Диапазон измерений: 0 - 10 МЕ/мл (нг/мг)
ВектоHBsAg-антитела
Набор реагентов для иммуноферментного качественного и количественного определения антител к HBs-антигену вируса гепатита В в сыворотке (плазме) крови.
ВектоHBcAg-IgМ
Набор реагентов для иммуноферментного выявления иммуноглобулинов класса М к core-антигену вируса гепатита В.
ВектоHBcAg-антитела
Набор реагентов для иммуноферментного выявления суммарных антител к core-антигену вируса гепатита В.
ГепаБест анти-HBc-IgG
Набор реагентов для иммуноферментного выявления иммуноглобулинов класса G к core-антигену вируса гепатита В в сыворотке (плазме) крови.
ВектоHBe-антиген
Набор реагентов для иммуноферментного выявления E-антигена вируса гепатита В в сыворотке (плазме) крови.
ВектоHBe-IgG
Набор реагентов для иммуноферментного выявления иммуноглобулинов класса G к HВe-антигену вируса гепатита В.
Набор для внутрилабораторного контроля качества ИФА "Сыворотка, содержащая НВsАg".
HBsAg-стандартная панель сывороток
Набор образцов сывороток крови, содержащих разные субтипы и мутантные формы HBsAg вируса гепатита В.
Читайте также:

