Токсический гепатит диффузный токсический зоб
Обновлено: 25.04.2024
Московский областной НИИ акушерства и гинекологии
Московский областной НИИ акушерства и гинекологии
Московский областной НИИ акушерства и гинекологии
Московский областной НИИ акушерства и гинекологии
Московский областной НИИ акушерства и гинекологии
Московский областной НИИ акушерства и гинекологии
Московский областной НИИ акушерства и гинекологии
Московский областной НИИ акушерства и гинекологии
Течение беременности и перинатальные исходы при диффузном токсическом зобе
Журнал: Российский вестник акушера-гинеколога. 2010;10(1): 35‑39
Шидловская Н.В., Логутова Л.С., Петрухин В.А., Бурумкулова Ф.Ф., Башакин Н.Ф., Троицкая М.В., Жученко Л.А., Котов Ю.Б. Течение беременности и перинатальные исходы при диффузном токсическом зобе. Российский вестник акушера-гинеколога. 2010;10(1):35‑39.
Shidlovskaia NV, Logutova LS, Petrukhin VA, Burumkulova FF, Bashakin NF, Troitskaia MV, Zhuchenko LA, Kotov IuB. The course of pregnancy and perinatal outcomes in diffuse toxic goiter. Russian Bulletin of Obstetrician-Gynecologist. 2010;10(1):35‑39. (In Russ.).
Московский областной НИИ акушерства и гинекологии
Изучены особенности течения беременности и лечения 92 беременных с диффузным токсическим зобом (ДТЗ), а также перинатальные исходы у них. Установлено, что частота и тяжесть гестационных осложнений у беременных с ДТЗ зависит от длительности компенсации основного заболевания, при этом продолжительность компенсации является дополнительным критерием прогноза течения беременности и перинатальных исходов у этих больных. При наступлении беременности на фоне декомпенсации ДТЗ высока частота развития первичной плацентарной недостаточности. Женщинам репродуктивного возраста с ДТЗ, планирующим беременность, необходима прегравидарная подготовка с целью достижения эутиреоидного состояния.
Московский областной НИИ акушерства и гинекологии
Московский областной НИИ акушерства и гинекологии
Московский областной НИИ акушерства и гинекологии
Московский областной НИИ акушерства и гинекологии
Московский областной НИИ акушерства и гинекологии
Московский областной НИИ акушерства и гинекологии
Московский областной НИИ акушерства и гинекологии
Московский областной НИИ акушерства и гинекологии
Заболевания щитовидной железы (ЩЖ), сопровождающиеся нарушением ее функции, оказывают выраженное отрицательное действие на процессы эмбриогенеза, плацентации и течение беременности, ухудшая перинатальные исходы. Наиболее частой причиной тиреотоксикоза при беременности (в 80-90% наблюдениях) является диффузный токсический зоб (ДТЗ) [4].
ДТЗ - органспецифическое аутоиммунное заболевание, обусловленное избыточной секрецией тиреоидных гормонов диффузно увеличенной щитовидной железой [1]. Большинство авторов считают, что частота развития ДТЗ во время беременности не превышает 0,2% [4, 7, 8, 12]. Несмотря на сравнительно невысокую заболеваемость беременных данной патологией, тяжелые осложнения беременности и родов, а также высокие перинатальная заболеваемость и смертность у данной категории пациенток превращают ее в серьезную акушерскую проблему. Нелеченый ДТЗ приводит к высокой частоте развития осложнений у матери и плода [3, 10], которая достигает 55% [2]. При неадекватном лечении ДТЗ возрастает частота самопроизвольного выкидыша, преждевременных родов, рождения новорожденного с малой массой тела, гестоза, отслойки плаценты [2, 3, 5, 10, 11]. Неадекватное лечение ДТЗ увеличивает риск роста материнской и перинатальной смертности [9]; так, в случае декомпенсированного течения ДТЗ 50% детей рождаются мертвыми [12]. При неудовлетворительном лечении ДТЗ возрастает частота развития тиреотоксического криза [5]; при этом тиреотоксический криз, развившийся во время родов, служит причиной гибели матери и плода.
Нарушения функции ЩЖ у детей, родившихся у матерей с ДТЗ, достигают 12% [6], частота аномалий развития плода (пороки сердца, дефекты лицевого черепа, грыжи передней брюшной стенки, а также полидактилия и трахеопищеводные свищи) составляют 6% (D. Wing и соавт., 1994). В литературе описаны также атрезия ануса, аплазия кожи, атрезия хоан и так называемый синдром Поттера, или аплазия почек [13]. Роды у данной категории пациенток характеризуются высокой частотой осложнений - до 46% [2, 3].
К сожалению, в отечественной литературе имеется лишь небольшое число работ, посвященных изучению течения беременности и родов, а также гормональной функции фетоплацентарного комплекса (ФПК) и морфологии плаценты при ДТЗ. Не разработан комплексный подход к прогнозированию акушерских осложнений, дисфункции ФПК, состояния плода и новорожденного. Известно, что ДТЗ часто рецидивирует в послеродовом периоде, однако до сих пор существуют рекомендации отмены тиреостатической терапии после родов. Это побудило нас к более углубленному изучению данного заболевания у беременных.
Целью нашего исследования явилось улучшение перинатальных исходов у беременных с ДТЗ путем разработки методов профилактики гестационных осложнений, ранней диагностики и коррекции нарушений функции ФПК.
Материал и методы исследования
Проблемой родоразрешения больных тиреотоксикозом МОНИИАГ занимается в течение 10 лет. За этот период родоразрешены 142 беременные с ДТЗ. Диагностика данного заболевания основывалась на характерной клинической картине заболевания, результатах гормональных исследований и УЗИ ЩЖ. Гормональные методы исследования функции ЩЖ и ФПК проводились с помощью стандартных радиоиммунологических наборов отечественного и зарубежного производства. Общеклинические исследования включали клинические анализы крови и мочи, коагулограмму, биохимический анализ крови. Для объективного анализа роста и развития плода, гормональной функции ФПК использовалась оценка в перцентилях (П) полученных показателей, что позволило четко определить степень их отклонения от характерных для популяции.
Результаты исследования и обсуждение
В процессе выполнения работы были тщательно обследованы 92 беременные, страдающие ДТЗ, и их новорожденные.
В зависимости от степени компенсации ДТЗ до беременности все пациентки ретроспективно были разделены на 3 группы.
1-ю группу составили 24 пациентки, у которых беременность наступила на фоне ремиссии или медикаментозной компенсации заболевания, 2-ю группу - 29 больных, у которых беременность наступила на фоне декомпенсации ДТЗ, в том числе у 11 больных заболевание было впервые диагностировано только во время беременности, в 3-ю группу были включены 39 пациенток, у которых заболевание ДТЗ во время беременности имело рецидивирующее течение.
Длительность заболевания до наступления беременности составила от 6 мес до 17 лет. Рецидив ДТЗ до наступления беременности отмечен у 6 (15,4%) пациенток, в I триместре зафиксирован рецидив ДТЗ в 22 (56,4%) наблюдениях, во II триместре - в 9 (23,1%), в III триместре - у 2 (5,1%) беременных (на фоне самовольной отмены тиреостатических препаратов). Не получали тиреостатических препаратов в связи с ремиссией заболевания 16 пациенток. Тиреостатическая терапия проводилась 76 беременным, из них находились на монотерапии пропилтиоурацилом в дозе от 25 до 150 мг/сут 35 беременных, только тиамазолом в дозе от 2,5 до 20 мг/сут - 25. У 16 больных в процессе беременности проводилась смена препаратов по медицинским показаниям или материальным соображениям.
К моменту родов 86 беременных были в состоянии клинического и биохимического эутиреоза. Побочных эффектов терапии или аллергических проявлений не было отмечено ни у одной пациентки. Не удалось достигнуть компенсации заболевания в связи с ограниченным временем лечения у 6 больных. Эти беременные поступили в отделение интенсивной терапии, из них 4 не получали тиреостатическую терапию до госпитализации (т.е. до III триместра), в 2 наблюдениях тиреостатическая терапия была назначена в конце II триместра до поступления в стационар.
При анализе течения беременности у больных 2-й и 3-й групп обнаружено, что частота и тяжесть гестационных осложнений, а также перинатальные исходы значительно отличались и зависели от продолжительности компенсации ДТЗ.
При ретроспективном математическом анализе была выявлена минимальная продолжительность компенсации ДТЗ, при которой течение беременности и перинатальные исходы были оптимальными. В связи с этим пациентки из данных групп были разделены на подгруппы:
- в подгруппах А продолжительность компенсации ДТЗ во время данной беременности была в течение 20 нед и более,
- в подгруппах В продолжительность компенсации ДТЗ во время данной беременности была менее 20 нед.
По возрасту, соматическому анамнезу, гинекологическим заболеваниям и паритету группы были сопоставимы. Течение данной беременности было осложненным практически у всех беременных с ДТЗ, причем во всех случаях осложнения были сочетанными. Самыми частыми гестационными осложнениями были угроза прерывания беременности - 49,0% наблюдений, гестоз - 60,9% и фетоплацентарная недостаточность (ФПН) - 64,5%, особенно в группах с декомпенсированным течением заболевания. Значительно чаще, чем в популяции, беременность протекала на фоне анемии - 60,9%.

При анализе осложнений беременности в подгруппах выявлено, что угроза преждевременных родов осложняла течение беременности чаще в подгруппах 2В и 3В (с недостаточной продолжительностью компенсации ДТЗ), достоверно чаще развивался гестоз (50 и 64,7% соответственно), а в 3В подгруппе - и ФПН, которая диагностирована у всех беременных (рис. 1). Рисунок 1. Гестационные осложнения у беременных с ДТЗ. * - различие показателей достоверно при сравнении таковых у пациенток подгрупп 2В и 3В с показателями у беременных 1-й группы и подгрупп 2А, 3А (р<0,05).
При анализе времени манифестации гестоза в подгруппах выявлено, что в случае продолжительности компенсации ДТЗ более 20 нед (подгруппы 2А и 3А) симптомы гестоза отмечены в сроке беременности, максимально приближенном к доношенному или в доношенном (36 нед и более).

Напротив, при компенсации основного заболевания продолжительностью меньше 20 нед (подгруппы 2В и 3В) гестоз манифестировал до 31-й недели гестации. Выявлена корреляционная зависимость между продолжительностью компенсации ДТЗ у беременных и тяжестью гестоза. Так, при продолжительности компенсации ДТЗ меньше 20 нед течение беременности осложнилось гестозом средней и тяжелой степени (рис. 2). Рисунок 2. Тяжесть гестоза в зависимости от продолжительности компенсации ДТЗ. * - различия показателей достоверны при сравнении таковых у пациенток без гестоза и с гестозом средней и тяжелой степени (р<0,01).
При анализе уровней гормонов в подгруппах при различной продолжительности компенсации основного заболевания наиболее критическое состояние ФПК выявлено в подгруппе 2В, а также в обеих подгруппах у беременных с рецидивирующим течением ДТЗ (3А и 3В). Уровни основных гормонов соответствовали таковым меньше 10-го перцентиля.
У 92 беременных с ДТЗ родились 94 новорожденных (две двойни), из них доношенными 88 (93,6%) детей. В 1-й группе недоношенных детей не было. Наибольшее число недоношенных новорожденных было в 3-й группе - 4 (10,0%) (одна двойня), во 2-й группе их было двое (6,7%) также при многоплодной беременности.

В связи с нарушением функции ФПК в каждой группе были новорожденные с задержкой внутриутробного роста плода (ЗВУР), однако наиболее часто это осложнение встречалось в подгруппах 2В и 3В, причем разница по числу таких детей у беременных с рецидивирующим течением заболевания и недостаточной продолжительностью компенсации ДТЗ (подгруппа 3В) была достоверна по сравнению со всеми остальными группами (рис. 4). Рисунок 4. ЗВУР плода в зависимости от продолжительности компенсации ДТЗ во время беременности. * - различия показателей достоверны по сравнению с таковыми у пациенток 1-й группы и подгрупп 2А, 2В и 3А (р<0,05).
В раннем неонатальном периоде повышенный уровень ТТГ (более 20,0 МЕ/мл) выявлен у 8 (8,7%) детей: у 2 (8,3%) из 1-й группы, у 4 (16,7%) из 2-й группы и у 2 (8,3%) из 3-й группы. К первому месяцу жизни уровень ТТГ нормализовался без лечения, что позволило считать эти изменения транзиторными. Повышенный уровень тироксина (Т4) более 190,0 нмоль/л (или более 40,0 пмоль/л для свободного Т4) отмечен у 11 (12%) детей, он также нормализовался без лечения, клинических проявлений тиреотоксикоза у этих новорожденных не было. Только у одного ребенка из подгруппы 3В имелись гормональные и клинические проявления транзиторного неонатального тиреотоксикоза (умеренная тахикардия, возбудимость), купировавшиеся к 2 мес жизни без назначения тиреостатической терапии.
Таким образом, частота врожденных аномалий у детей, родившихся у матерей с ДТЗ, получавших тиреостатическую терапию во время беременности, незначительно превышает популяционную (по данным МОНИИАГ - 4,3-5,3%), в то же время не установлено достоверных различий по тератогенному влиянию антитиреоидных препаратов. Возможно, на возникновение аномалий развития у плода может оказывать влияние декомпенсация ДТЗ, особенно при несвоевременном начале терапии и, соответственно, более поздних сроках наступления компенсации ДТЗ.

Состояние новорожденных не зависело от способа родоразрешения, так как частота самопроизвольных родов и кесарева сечения в группах были практически одинаковыми. Анализируя осложнения родового процесса, мы отметили высокую частоту аномалий сократительной деятельности матки, особенно при декомпенсированном течении заболевания, в структуре аномалий превалировала слабость родовой деятельности, причем в 3-й группе с рецидивом ДТЗ зафиксирована исключительно первичная слабость родовой деятельности (см. таблицу).
Показания к кесареву сечению были различны. Основными из них послужили нарастание степени тяжести гестоза и прогрессирующая ФПН (40%), упорная слабость родовой деятельности (20%) и острая гипоксия плода на фоне ФПН (8%). Только в 3-й группе основными показаниями к абдоминальному родоразрешению были нарастание степени тяжести гестоза и прогрессирующая ФПН (66,7%), что обусловило и более высокую частоту досрочного родоразрешения у пациенток с рецидивом ДТЗ. У новорожденных, находящихся на грудном вскармливании, не выявлено патологических клинических и лабораторных изменений, связанных с приемом кормящей матерью тиреостатических препаратов в средних терапевтических дозировках (пропилтиоурацил 50-100 мг/сут, тиамазол - 5-15 мг/сут).
Выводы
1. Частота и тяжесть гестационных осложнений у беременных с ДТЗ находятся в прямой корреляционной зависимости от длительности компенсации основного заболевания: при компенсации ДТЗ не менее 20 нед частота гестационных осложнений минимальна, а перинатальные исходы - оптимальны.
2. С продолжительностью компенсации ДТЗ коррелируют морфологические и функциональные нарушения плаценты, которые обусловливают высокую частоту ЗВУР. При этом в случае наступления беременности на фоне декомпенсации ДТЗ высока частота развития первичной плацентарной недостаточности, морфологически выражающейся в глубоких метаболических изменениях (фиброз стромы, незрелость ворсинчатого дерева, а также дефицит массы плаценты), а функционально - в снижении концентрации ПЛ, прогестерона, АФП.
3. Особенностью гестоза у беременных с декомпенсированным ДТЗ являются раннее его начало (до 28 нед гестации) и тяжелое течение.
4. Дополнительным критерием прогноза течения беременности и перинатальных исходов является продолжительность компенсации ДТЗ во время гестации.
5. Женщинам репродуктивного возраста с ДТЗ, планирующим беременность, необходима прегравидарная подготовка, целью которой является достижение эутиреоидного состояния, а тиреостатическая терапия у беременных с ДТЗ должна быть перманентной на протяжении всего периода гестации и после родов.
Что такое зоб диффузный токсический (Базедова болезнь)? Причины возникновения, диагностику и методы лечения разберем в статье доктора Родионова Е. А., терапевта со стажем в 14 лет.
Над статьей доктора Родионова Е. А. работали литературный редактор Елена Бережная , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Диффузный токсический зоб — это аутоиммунное поражение щитовидной железы.
Диффузный токсический зоб впервые был описан в трудах Роберта Джеймса Грейвса и Карла Адольфа фон Базедова в середине ХIХ века. Кроме данного заболевания, тиреотоксикоз может встречаться и при других заболеваниях щитовидной железы (тиреоидит, токсическая аденома и др.), что требует дифференциальной диагностики, так как лечение этих состояний не является однотипным, а осложнения из-за отсутствия или неправильного лечения могут привести к необратимым патологическим изменениям. [1] , [2]
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
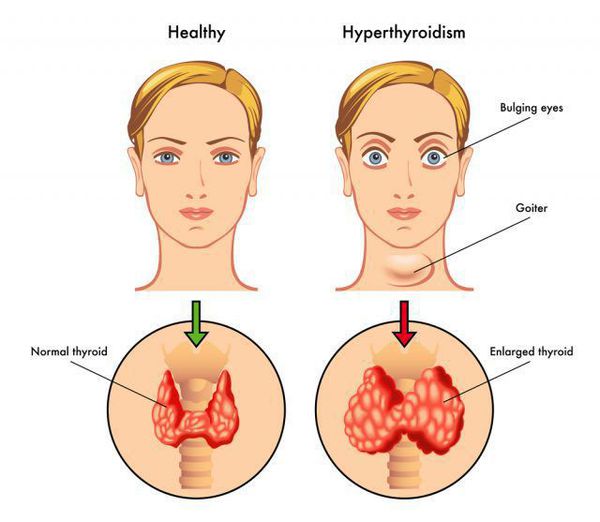
Симптомы диффузного токсического зоба
Некоторые авторы в развитии диффузного токсического зоба выделяют четыре стадии:
- Невротическая (вегетативный невроз и незначительное увеличение или нормальные размеры щитовидной железы);
- Нейрогормональная (увеличенные размеры щитовидной железы и клиническая картина тиреотоксикоза);
- Висцеропатическая (нарушение функции органов);
- Кахектическая (тиреотоксические кризы и общая дистрофия). [4]
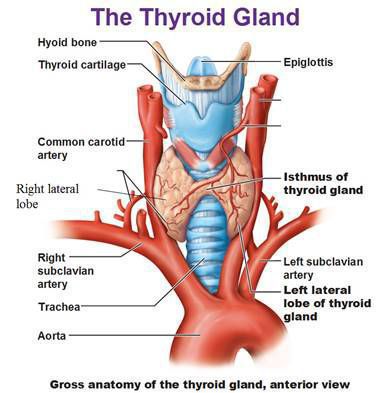
Патогенез диффузного токсического зоба
Кроме генетических факторов, есть предположения о роли стресса и инфекции в развитии болезни Грейвса, а также действия токсических веществ. [4] Из-за иммунологических нарушений, происходит инфильтрация щитовидной железы лимфоцитами, выработка антител к различным её компонентам, главным образом — к рецепторам ТТГ, что приводит к стимуляции выработки ТГ и пролиферации тироцитов. Эти антитела также называют тиреостимулирующими иммуноглобулинами. Избыточное действие ТГ в организме приводит к развитию тиреотоксикоза, с признаками которого больные диффузным токсическим зобом обычно обращаются к врачу. [1] , [2]
Классификация и стадии развития диффузного токсического зоба
Согласно классификации тиреотоксикоза по Фадееву В.В. и Мельниченко Г.А., выделяется:
- субклинический;
- манифестный;
- осложнённый.
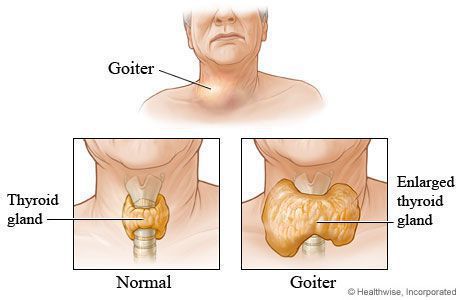
Также существует классификация зоба (патологического увеличения щитовидной железы), в которой выделяется три степени зоба, в зависимости от данных осмотра и пальпации щитовидной железы.
Классификация зоба, рекомендованная ВОЗ (2001)
- 0 cтепень: зоба нет (объём каждой доли не превышает объёма дистальной фаланги большого пальца руки обследуемого);
- I степень: зоб пальпируется, но не виден при нормальном положении шеи, или же имеются узловые образования, не приводящие к увеличению щитовидной железы;
- II степень: зоб чётко виден при нормальном положении шеи. [4] , [5]
Патоморфологическая классификация диффузного токсического зоба (три варианта заболевания) опирается на данные гистологического исследования биоптата или удалённой щитовидной железы. [4] , [5]
Осложнения диффузного токсического зоба
Развившийся при диффузном токсическом зобе тиреотоксикоз поражает все системы организма. Если надлежащим образом не лечить это заболевание, то оно грозит тяжёлой инвалидизацией, а аритмии и сердечная недостаточность даже могут привести к летальному исходу.
Наиболее опасным осложнением болезни Грейвса является тиреотоксический криз, развитие которого связывают с неблагоприятными факторами (стресс, различные заболевания, выраженная физическая нагрузка, операция и др.). Появляется резкое возбуждение, температура повышается до 40 о С, частота сердечных сокращений достигает 200 ударов в минуту, может развиться фибрилляция предсердий, усиливаются явления диспепсии (тошнота, рвот, понос, жажда), повышается пульсовое артериальное давление. Затем могут появиться признаки недостаточности надпочечников (гиперпигментация, нитевидный пульс, нарушение микроциркуляции). Состояние ухудшается за несколько часов. Это ургентная ситуация, требующая неотложных мер, направленных на снижение концентрации ТГ, борьбу с надпочечниковой недостаточностью, дегидратацией, гипертермией, метаболическими нарушениями и недостаточностью кровообращения. В/в вводится гидрокортизон, проводится дезинтоксикационная и тиреостатическая терапия. К осложнениям диффузного токсического зоба также можно отнести осложнения хирургического его лечения: гипопаратиреоз, повреждение n. laryngeus recurrens (при повреждении одного нерва появляется осиплость голоса, при повреждении двух может возникнуть асфиксия), кровотечения, аллергические реакции на препараты. Об осложнениях тиреостатической терапии будет сказано ниже. [5]
Диагностика диффузного токсического зоба
При наличии у пациента признаков тиреотоксикоза ему определяют уровень тиреотропного гормона (ТТГ) высокочувствительным методом (чувс. 0,01 мЕд/л). Если уровень ТТГ меньше нормы, то исследуют концентрацию св. Т4 (тетрайодтиронин, тироксин) и Т3 (трийодтиронин). Существует понятие о так называемом субклиническом тиреотоксикозе, когда уровни Т4 и Т3 оказываются в норме. Среди антител наибольшее клиническое значение имеет уровень антител к рецепторам ТТГ (АТ-рТТГ). Высокие их титры с большой долей вероятности указывают на то, что мы имеем дело именно с болезнью Грейвса. Другие антитела, такие, как антитела к тиреоидной пероксидазе и тиреоглобулину (АТ-ТПО и АТ-ТГ), выявляются и при других состояниях, поэтому имеют значение только в комплексной оценке, и их определение может помочь в некоторых ситуациях.
Лечение диффузного токсического зоба
Лечение болезни Грейвса может проводиться эндокринологом или терапевтом. К сожалению, в настоящее время лечение диффузного токсического зоба направлено только на орган-мишень, то есть щитовидную железу, а не на выработку антител, являющуюся непосредственной причиной развития болезни. Даже после удаления щитовидной железы продолжают синтезироваться антитела к рецепторам тиреотропного гормона, хотя тиреотоксикоза уже не возникает (при адекватной заместительной терапии). [9]
Итак, существует три способа лечения диффузного токсического зоба:
- консервативное лечение;
- радиойодтерапия;
- оперативное лечение.
Выбор метода зависит от возраста, сопутствующих заболеваний, степени увеличения щитовидной железы, желания пациента и возможностей лечебного учреждения. Консервативный метод лечения диффузного токсического зоба заключается в назначении тиреостатиков. В некоторых случаях (до 30%) курс такого лечения способен привести к стойкой ремиссии, в некоторых — является подготовкой к использованию другого, более радикального метода (хирургическое лечение или терапия йодом-131). Считается, что консервативная терапия неэффективна при выраженном увеличении щитовидной железы (более 40 см 3 ) и с признаками сдавления окружающих тканей, при наличии крупных узлов в ней, а также при наличии осложнений (фибрилляция предсердий, остеопороз и др.). При рецидиве после курса терапии тиреостатиком, повторный длительный курс не назначается. [5] В подобных случаях проводится курс медикаментозной подготовки к радиойодтерапии или операции.
Важным условием адекватного проведения консервативного лечения является приверженность пациента к лечению и доступность лабораторного контроля. Тиреостатики блокируют синтез тиреоидных гормонов и купируют тиреотоксикоз. По прошествии 4-6 недель тиреостатической терапии, при наступлении эутиреоидного состояния, обычно к лечению добавляют левотироксин. [4] В период тиреотоксикоза (до нормализации Т4) также целесообразно назначение препаратов из группы β-адреноблокаторов: они подавляют тканевое превращение Т4 в Т3, снижают частоту сердечных сокращений. Критерием адекватности лечения является нормальный уровень Т4 и ТТГ. Курс лечения продолжается 12-18 месяцев. Во время лечения необходимо контролировать показатели общего анализа крови. Это необходимо для контроля грозных осложнений тиреостатической терапии — агранулоцитоза и тромбоцитопении, требующих немедленной отмены препаратов. Симптомы агранулоцитоза: лихорадка, боль в горле, жидкий стул. [4] При их появлении пациенту необходимо экстренно сдать кровь на общий анализ и прекратить приём тиреостатиков до получения результатов анализа. Рецидив чаще всего наступает в первые 12 месяцев после завершения курса.
Под хирургическим лечением подразумевается удаление всей или большей части щитовидной железы. [8] Операция проводится только в состоянии эутиреоза. В настоящее время удаление этого органа не является фатальным для человека, так как имеются все возможности адекватной и недорогой заместительной терапии левотироксином. С другой стороны, при оставлении даже небольшого фрагмента железы, сохраняется вероятность рецидива заболевания, это орган-мишень для антитиреоидных антител, выделяемых иммунной системой. Таким образом, послеоперационный гипотиреоз теперь не рассматривается в качестве осложнения операции, а является её целью. Доза левотироксина после операции подбирается индивидуально и обычно составляет 1,7 мкг/кг в сутки.
В России радиойодтерапия мало распространена, что связано с дефицитом йода-131. Противопоказанием к радиойодтерапии является только беременность и период кормления грудью. Даже детский возраст не является помехой к её проведению. [6] Данный метод заключается в приёме внутрь предварительно рассчитанной дозы йода-131, который накапливается в щитовидной железе, распадается в выделением β-частиц, что приводит к лучевой деструкции тироцитов. Радиойодтерапия по сути является нехирургическим методом удаления ткани щитовидной железы. [1] , [5] , [7]
Прогноз. Профилактика
Прогноз при своевременной диагностике и надлежащем лечении благоприятный. Не рекомендуется приём лекарств, побочным эффектом которых является влияние на выработку тиреоидных гормонов, например амиодарона. Диффузный токсический зоб в большинстве случаев успешно лечится и не является приговором. Благодаря общедоступной и относительно недорогой заместительной терапии, удаётся добиться нормализации метаболических процессов и исчезновения клинических проявлений. Однако осложнения болезни Грейвса способны привести к необратимым патологическим изменениям в организме. Профилактика диффузного токсического зоба у прямых родственников больных чётко не разработана, однако можно рекомендовать отказ от курения, йод-содержащих лекарств, соблюдение оптимального режима дня для минимизации стрессовых ситуаций и регулярный контроль ТТГ. Чёткой связи между поступлением йода с пищей и болезнью Грейвса не выявлено, в регионах с недостаточным содержанием йода диффузный токсический зоб встречается не чаще; в отличие от функциональной автономии, которая в этих областях становится основной причиной тиреотоксикоза. [3] , [7]
Что такое тиреотоксикоз (гипертиреоз)? Причины возникновения, диагностику и методы лечения разберем в статье доктора Курашова О. Н., эндокринолога со стажем в 28 лет.
Над статьей доктора Курашова О. Н. работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Тиреотоксикоз (гипертиреоз) — гиперметаболический процесс, вызванный избытком тиреоидных гормонов в организме и их токсическим воздействием на различные органы и ткани. Клинически характеризуется увеличением щитовидной железы и поражением других систем и органов. [3] [5] [11]
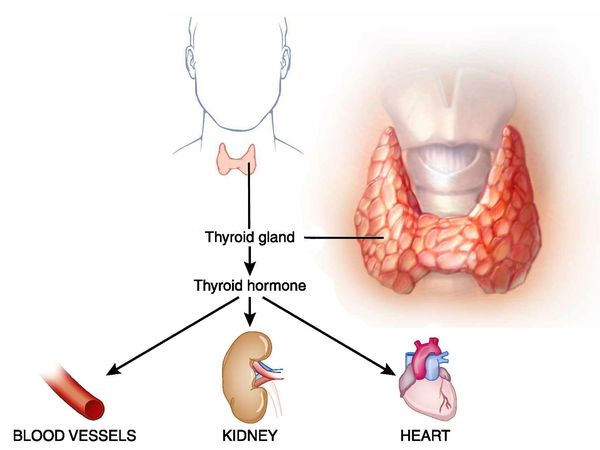
Первые описания этой патологии были найдены в работах персидского врача Джурджани, созданных в 1100 году. [5] [11]
Данный синдром встречается как у женщин (до 2%), так и у мужчин (до 0,2%). Чаще он возникает у людей в возрасте 20-45 лет.
Причин возникновения тиреотоксикоза множество. К основным относятся:
- повышение продукции гормонов щитовидной железой вследствие различных заболеваний (диффузно-токсический, узловой зоб и другие);
- избыточный приём препаратов, содержащих гормоны щитовидной железы (нарушение назначенной схемы лечения).
Провоцирующим фактором синдрома является дополнительное количество йода, поступающее в организм при самостоятельном использовании йодных добавок.
Состояние тиреотоксикоза при диффузно-токсическом зобе является аутоиммунным заболеванием. Обычно оно развивается в результате избыточной выработки антител к рецептору тиреотропного гормона (ТТГ), производимого гипофизом.
Возникновение тиреотоксического состояния возможно при возникновении функциональной автономии уже существующего узла щитовидной железы — одно- и многоузлового зоба. Это заболевание развивается достаточно долго, в основном у людей, старше 45 лет. Так, в отсутствие воздействия ТТГ — основного физиологического стимулятора [7] [8] — узлы синтезируют количество тиреогормонов, превышающее потребность организма. [5] [6] [11]
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы тиреотоксикоза (гипертиреоза)
При опросе пациентов с подозрением на повышенную функцию щитовидной железы выявляются:
Эмоциональные расстройства сочетаются с двигательно-волевыми: появляется необходимость в постоянном движении и хореоподобные подёргивания. Причём тремор конечностей и тела - типичный симптом тиреотоксикоза. [2] [3] [5] [11]
Журнал: Проблемы эндокринологии. 2017;63(1): 46‑50
Заболевания печени у больных гипертиреозом могут выступать в трех ипостасях: лекарственные гепатиты, развивающиеся в ответ на прием тиреостатиков, сопутствующие аутоиммунные заболевания печени и, наконец, гепатопатии как непосредственное проявление тиреотоксикоза [4—6]. Гепатотоксичность тиреостатиков проявляется менее чем в 0,5% случаев [4] и чаще бывает связана с применением пропилтиоурацила, чем метимазола, в основном метаболизирующегося почками. Отмечены случаи токсического гепатита и на фоне лечения радиоактивным йодом [7]. Универсальная аутоиммунная природа патологического процесса объясняет случаи сочетания болезни Грейвса с аутоиммунным гепатитом [4, 5, 8] и первичным билиарным циррозом [6].
Из трех вариантов поражения печени при тиреотоксикозе лишь последний, очевидно, может рассматриваться в контексте патогенного влияния тиреоидных гормонов. В уже упомянутой статье D. Mazo и соавт. [4] из 8 описанных случаев 2 было представлено аутоиммунным гепатитом, еще 3 — лекарственным гепатитом, индуцированным пропилтиоурацилом, и лишь оставшиеся 3 случая — собственно отражением тиреотоксикоза. Механизм развития тиреотоксического гепатита объясняется диспропорцией между кровоснабжением и метаболическими затратами печени, развивающейся в условиях повышенного сердечного выброса [6, 9]. Правожелудочковая сердечная недостаточность, вызванная тиреогенной миокардиодистрофией, может усугубить повреждение печени [4, 9]. Концепция прямого токсического действия избытка гормонов щитовидной железы на печень убедительного подтверждения не нашла [9], хотя и продолжает обсуждаться [5].
Описание клинического случая
Больной М., 56 лет, поступил в городскую клиническую больницу с жалобами на желтуху, потемнение мочи, слабость, одышку при незначительной физической нагрузке, отеки ног, увеличение живота, похудание. Из анамнеза выяснилось, что последние 5 лет у больного наблюдается постоянная форма мерцательной аритмии (попытки восстановления синусового ритма не предпринимались), а 6 мес назад был установлен диагноз цирроза печени. Самочувствие больного ухудшилось в течение последних 2 мес, когда появились и усилились вышеуказанные жалобы.
При поступлении состояние расценено как тяжелое. Больной истощен (после устранения отеков: рост 176 см, масса тела 52 кг, индекс массы тела 16,8 кг/м 2 ), кожа и склеры интенсивно желтушны. Границы сердца расширены влево, тоны аритмичные 98 в минуту, на верхушке сердца и у основания мечевидного отростка систолический шум. Живот равномерно увеличен за счет асцита. Печень плотная, с гладкой поверхностью, чувствительная при пальпации, выступает из-под края реберной дуги на 5 см.
Общий анализ крови документировал легкую анемию (гемоглобин 108 г/л, эритроциты 3,5´10 12 /л), которая сопровождалась сниженным уровнем железа (8,6 мкмоль/л) и достаточно высоким уровнем ферритина (230 мкг/л). Отмечены гипербилирубинемия (общий билирубин 279,2 мкмоль/л, прямой билирубин 224,6 мкмоль/л, непрямой билирубин 54,6 мкмоль/л), повышение уровня трансаминаз (АСТ 101,4 Ед/л, АЛТ 58 Ед/л), низкие значения фибриногена (1,02 г/л) и общего холестерина (1,87 г/л), диспротеинемия (альбумины 40,7%, γ-глобулины 33,1%), уробилинурия. Маркеры вирусных гепатитов В и С оказались отрицательными.
УЗИ установило повышенную эхогенность печени и умеренную гепатомегалию — косовертикальный размер 167 мм (норма до 150 мм). Зафиксировано увеличение диаметра воротной вены — 13,5 мм (норма до 12 мм) и нижней полой вены — 21 мм (норма до 15—16 мм). Диаметры желчных протоков, размер селезенки в пределах нормы. Подтверждено значительное количество жидкости в брюшной полости.
Эзофагогастродуоденоскопия существенных изменений не выявила.
ЭКГ подтвердила наличие фибрилляции предсердий с частотой активации желудочков 78—136 в минуту, признаки гипертрофии левого желудочка.
Таким образом, заболевание было представлено желтухой, гепатомегалией, нарушением ритма по типу фибрилляции предсердий, сердечной недостаточностью, отечно-асцитическим синдромом. Отклонения лабораторных показателей укладывались в цитолитический, мезенхимально-воспалительный и гепатодепрессивный (гипоальбуминемия, гипофибриногенемия, гипохолестеринемия) синдромы. С учетом выявленного диффузного поражения печени и неизмененных желчных протоков наиболее вероятным признано предположение о печеночном характере желтухи. Стандартное лечение сердечной недостаточности (ингибиторы ангиотензин-превращающего фермента, диуретики, β-адреноблокаторы, сердечные гликозиды) в сочетании с препаратом урсодезоксихолевой кислоты привели к быстрому устранению отеков и асцита, значительному уменьшению одышки; желтуха тем не менее сохранялась.
Выполненная для уточнения диагноза магнитно-резонансная томография констатировала отсутствие изменений формы, размеров, структуры и плотности печени и селезенки, просвета внутрипеченочных протоков, лимфоузлов брюшной полости и забрюшинного пространства; диаметры воротной и нижней полой вен на фоне проведенного лечения приобрели нормальные значения, свободной жидкости в брюшной полости не отмечалось.
Отрицательные маркеры вирусных гепатитов, отсутствие холедохоэктазии и структурных изменений печеночной ткани не давали оснований говорить о первичном поражении печени и желчевыводящей системы. Мерцательная аритмия, тотальная сердечная недостаточность, кардиомегалия в сочетании с систолическим шумом свидетельствовали о возможном пороке сердца. В подобных обстоятельствах желтуха и гепатомегалия могли рассматриваться как проявление кардиального фиброза печени, однако в эту версию не укладывался высокий и стойкий уровень билирубина и выраженные лабораторные признаки гепатодепрессии.
Проведенная эхокардиография выявила признаки легочной гипертензии и легочного сердца: дилатацию полостей предсердий (левое 4,3 см, правое 6,9×5,0 см) и правого желудочка (3,0 см), увеличение диаметра легочной артерии 2,8 см, трикуспидальную регургитацию II степени. Клапанные створки оказались интактны, нарушений локальной сократимости миокарда не отмечено, фракция выброса составила 65%.
В круг болезней с одновременным вовлечением сердца с развитием фибрилляции предсердий и печени входят поражения щитовидной железы, протекающие с явлениями гипертиреоза. При целенаправленном осмотре больного были выявлены положительные глазные симптомы Дельримпля и Штельвага, выраженный блеск глаз, тремор тела и конечностей, экзофтальм. Ультразвуковое исследование установило пониженную эхогенность и увеличение объема щитовидной железы до 26,2 см 3 . Признаки манифестного тиреотоксикоза были документированы уровнем гормонов: Т4 свободный 45,0 пмоль/л (норма 10,0—23,2 пмоль/л), Т4 общий 37,0 нмоль/л (норма 52—155 нмоль/л), Т3 0,4 нг/мл (норма 0,8—2,8 нг/мл), ТТГ 0 мкМЕ/мл (норма 0,23—3,4 мкМЕ/мл).
Лабораторные и клинические признаки тиреотоксикоза дали основание к назначению тиамазола, что привело к уменьшению желтухи и быстрой положительной динамике лабораторных показателей. При контрольном лабораторном исследовании отмечено значительное снижение гипербилирубинемии и нормализация уровня трансаминаз: общий билирубин 55,6 мкмоль/л, прямой билирубин 50,9 мкмоль/л, АСТ 35,4 Ед/л, АЛТ 35,1 Ед/л. Уровень тиреоидных гормонов составил: Т4 свободный 19,6 пмоль/л; Т4 общий 58,0 нмоль/л, Т3 0,99 нг/мл, ТТГ 0,1 мкМЕ/мл.
Окончательный диагноз: диффузный токсический зоб I степени (по ВОЗ), тиреотоксикоз тяжелой степени. Тиреогенная миокардиодистрофия, кардиомегалия, постоянная форма фибрилляции предсердий, СН IIБ стадии. Тиреотоксический гепатит тяжелого течения, гипербилирубинемический криз, отечно-асцитический синдром. Анемия хронических заболеваний легкой степени. Недостаточность питания II степени.
Заключение
Интенсивная желтуха при тяжелом течении тиреотоксикоза описывалась в публикациях, относящихся еще к 20—40-м годам прошлого века. Однако ошибочно считать, что в настоящее время при современном уровне диагностики и лечения проблема поражений печени при заболеваниях щитовидной железы перестала быть актуальной.
Комментируя приведенный случай, хотелось бы обратить внимание на изолированное повышение концентрации свободного Т4 при исходно пониженных уровнях общего Т4 и Т3. Очевидно, выраженное снижение белково-синтетической функции (факт гепатодепрессии подтвержден лабораторно) привело к снижению синтеза белков-переносчиков тиреоидных гормонов, и только уровень свободного (не связанного с белками) Т4 оказался информативным. Показательно, что на фоне лечения концентрации общего Т4 и Т3 возросли, что косвенно свидетельствовало о нормализации функции печени.
В завершение сошлемся на приведенный в работе D. Mazo и соавт. [4] алгоритм ведения пациента с поражением печени, связанным с гипертиреозом (см. рисунок).

Алгоритм ведения пациентов с поражением печени на фоне гипертиреоза [4].
Информация о финансировании и конфликте интересов
Авторы декларируют отсутствие явных и потенциальных конфликтов интересов, связанных с публикацией настоящей статьи.
Проведенная поисково-аналитическая работа по подготовке рукописи проведена на личные средства членов авторского коллектива.
Медицинские сведения о пациенте публикуются с его письменного согласия.
Участие авторов: концепция и дизайн исследования — Д.В. Пикулев, А.В. Клеменов; сбор и обработка материалов — Д.В. Пикулев, А.В. Клеменов; анализ полученных данных, написание текста — А.В. Клеменов, Д.В. Пикулев; редактирование текста — А.В. Клеменов.
Читайте также:

