Токсический гепатит жидкость в брюшной полости
Обновлено: 17.04.2024
Асцит - накопление жидкости в брюшной полости. Наиболее часто синдром встречается при циррозе печени. Слово "асцит" образовалось от греческого ascos,что означает "мешок" или "сумка". Асцит известен врачам со времен Гиппократа. Единственным способом терапии асцита вплоть до XX в. был парацентез.
Что провоцирует / Причины Отечно-асцитического синдрома:
Асцит может возникнуть неожиданно или развиваться медленно, в течение нескольких недель или месяцев. Внезапное возникновение асцита характерно для проявления печеночно-клеточной недостаточности на фоне геморрагического синдрома, шока, интоксикации и др. Постепенное развитие асцита обусловлено наличием длительно текущего, далеко зашедшего патологического процесса, часто При отсутствии определенного причинного фактора. При асците наблюдается увеличение в объеме живота, появление метеоризма, одышки. При большом количестве асцитической жидкости (15-20 л) появляются дополнительные симптомы: пупочные и паховые грыжи, геморроидальных вен, смещение диафрагмы вверх, верхушечного толчка - вверх и влево, повышение давления в яремной вене, набухание шейных вен. У таких больных могут определяться диафрагмальная грыжа, желудочно-пищеводный рефлюкс.
В 6-7 % случаев у больных циррозом печени развивается правосторонний гидроторакс.
Патогенез (что происходит?) во время Отечно-асцитического синдрома:
Патогенез асцита у больных циррозом печени является многофакторным. Портальная гипертензия и связанный с ней застой в системе воротной вены являются пусковыми факторами развития асцита. Кроме того, развитию асцита способствует каскад нейрогормональных, гемодинамических и вводно-электролитных сдвигов. В настоящее время патогенез асцита рассматривается как индивидуальное сочетание многочисленных патогенетических факторов прогрессирования основного патологического процесса, которые условно разделены на местные (регионарные) и общие (системные).
К местным регионарным факторам относятся повышение печеночного сосудистого сопротивления вследствие взаимодействия комплекса органических и функциональных нарушений. По преимущественной локализации поражения при ХЗП можно выделить преси-нусоидальный, синусоидальный и постсинусоидальный уровни блока. В зависимости от обратимости изменений выделяют необратимые, или органические, поражения и потенциально обратимые, или функциональные, изменения.
Внутрипеченочный блок оттока приводит к усиленному лимфообразованию. При этом лимфа может просачиваться через лимфатические сосуды глиссоновой капсулы прямо в брюшную полость или поступать в области ворот печени в грудной лимфатический проток. В результате развивающегося лимфатического застоя происходит пропотевание жидкости в брюшную полость.
Одним из важных моментов патогенеза асцита является накопление у больных в циркулирующей крови нерасщепленных эндогенных вазодилататоров (глюкагон и др.), способствующих расширению мелких периферических артерий, а также открытию артериовенозных шунтов в органах и тканях, что помогает снижению кровенаполнения артерий, увеличению сердечного выброса, гиперволемии, повышению скорости портального кровотока и портальной гипертензии. Кроме того, следует помнить, что накопление асцитической жидкости сопровождается снижением эффективного кровотока в результате депонирования значительной части объема плазмы в сосудах брюшной полости. Эффект вазодилататоров повышается на фоне недостатка синтеза оксида азота, что способствует усилению вазоконстрикции в синусоидах и мелких разветвлениях воротной вены. Аналогичным образом действует значительная гиперпродукция эндотелинов набухшими эндотелиоцитами.
Установлено, что асцит в первую очередь формируется внутрипеченочно, внутри печеночных синусоидов. Стенки эндотелиальной выстилки синусоидов имеют относительно большие поры-финестры, необходимые для обеспечения легкого доступа плазмы к гепатоцитам в пространстве Диссе. В перипортальной области имеются выстланные эндотелием, слепо начинающиеся лимфатические капилляры, благодаря чему жидкость из пространства Диссе может попасть в лимфатические капилляры, проходя эндотелиальную стенку. При формировании блока оттока из печени возникает синусоидальная гипертензия. В соответствии с законом Старлинга, повышение синусоидального давления является фактором, усиливающим проникновение элементов плазмы через стенку синусоида в перисинусоидальное пространство Диссе, а затем в лимфатические сосуды, которые компенсируют синусоидальную гипертензию за счет возрастания оттока лимфы из печени.
К системным факторам, способствующим формированию ПГ, можно отнести гипоальбуминемию, активизацию симпатической нервной системы, повышение секреции компонентов ренин-ангиотензиналь-достероновой системы, антидиуретического гормона, предсердного натрийуретического пептида, снижение продукции простагландинов.
Наряду с вышеуказанными изменениями важную роль в формировании асцита играет гиперальдостеронизм, природа которого довольно сложна и включает в себя следующие механизмы:
- активизация РААС, приводящая к увеличению уровня альдостерона;
- развитие вторичного гиперальдостеронизма;
- повышение чувствительности канальцев почек к действию альдостерона.
Известно, что концентрация альбумина в сыворотке крови является ведущим фактором, определяющим онкотическое давление. По мере прогрессирования патологического процесса, проявляющегося на морфологическом уровне дистрофически-некротическими процессами в паренхиме и синусоидах, нарушается синтез альбуминов и, как следствие, изменяется проницаемость синусоидального эндотелия. При этом значение гипоальбуминемии и сопутствующих ей изменений онкотических градиентов возрастает.
У большинства больных хроническими гепатитами на цирротической стадии выявлены признаки активации симпатической нервной системы. Повышение уровня катехоламинов в сыворотке крови обнаружено у 60 % пациентов Считается, что снижение эффективного внутрисосудистого объема и гипоальбуминемия способствуют повышению секреции катехоламинов в целях поддержания важнейших го меостатических показателей.
Секреция ренина в почках является одной из важнейших компенсаторных реакций в условиях гиповолемии. Выброс ренина происходит вследствие как гиповолемии, так и гипонатриемии. Ренин вызывает увеличение синтеза ангиотензина, являющегося мощным вазоконстриктором, и стимулирует секрецию альдостерона. Увеличение уровня альдостерона приводит к повышению реабсорбции натрия и воды в почках
Снижение внутрисосудистого объема - сигнал к синтезу антидиуретического гормона опосредованно через волюморецепторы, предположительно расположенные в предсердиях. Физиологическим эффектом антидиуретического гормона является повышение объема циркулирующей плазмы.
Большинство авторов сообщает о повышении уровня предсердного натрийуретического пептида при циррозе печени с асцитом. По-видимому, повышение концентрации натрийуретического пептида и увеличение задержки натрия при циррозе могут объясняться снижением чувствительности почек к данному гормону
Одним из возможных участников патогенеза асцита рассматривается простагландин Ег, синтезирующийся, в частности, в почках и обладающий вазодилататорным действием. Считается, что степень задержки натрия может быть вызвана снижением продукции этого вазодилататора. При этом простагландины оказываются патогенетически связующим звеном между изменениями гемодинамики на локальном уровне и системными гуморальными реакциями.
Следовательно, в развитии асцита при заболеваниях печени важную роль играют гемодинамические и метаболические факторы, проявляющиеся на фоне морфологической перестройки печени Появление асцита обусловлено выраженной задержкой натрия. Суточная экскреция натрия с мочой при асците не превышает 5 ммоль.
Согласно теории "недостаточного наполнения сосудистого русла", задержка натрия и воды почками вторична и обусловлена расширением сосудистого русла внутренних органов. Причиной указанных явлений считается активизация ренин-ангиотензин-альдостероновой системы, симпатической нервной системы, простагландина Ег, способствующая изменению функции почек. При этом натрийуретическому фактору отводится второстепенная роль.
Теория "избыточного наполнения сосудистого русла" предусматривает первичную задержку натрия с дальнейшим увеличением объема циркулирующей плазмы и переходом жидкости в межклеточное пространство.
Важная роль отводится активному переносу жидкости через мембрану капилляров брюшины. Кроме того, формированию асцита способствуют повышение давления внутри синусоидов, что наблюдается ПРИ циррозе, усиленное образование лимфы при обструкции синусоидов, печеночных вен.
Диагностика Отечно-асцитического синдрома:
Большое скопление жидкости в брюшной полости можно обнаружить обычными клиническими методами. При перкуссии выявляется притупление звука в боковых отделах живота. Перемещение больных на левый или правый бок вызывает смещение тупости к соответствующему фланку. При наличии осумкованной жидкости в брюшной полости, при слипчивом перитоните туберкулезной этиологии, кисте яичника перемена положения пациента тимпанит не изменяет. Асцитическую жидкость объемом менее 1,5 л определить клиническими методами не удаегся. В подобных случаях асцит можно определить с помощью УЗИ. Минимальное количество асцитической жидкости, определяемое указанным методом, составляет 200 мл. УЗИ в ряде случаев позволяет выявить заболевание, явившееся причиной развития асцита (цирроз печени, новообразование органов брюшной полости, панкреатит и др.). После клинического обнаружения асцига в неясных случаях показано проведение диагностического парацентеза с биохимическим и цитологическим исследованиями полученной жидкости. При парацентезе с помощью тонкой иглы получают 50-250 мл асцитической жидкости.
Показаниями для проведения диагностического парацентеза являются;
- впервые выявленный асцит,
- подозрение на злокачественную опухоль,
- исключение спонтанного бактериального перитонита.
В асцитической жидкости определяют уровень общего белка, альбумина, глюкозы, холестерина, триглицеридов, билирубина, активности амилазы, производят подсчет количества лейкоцитов, эритроцитов, атипических клеток, окраску бактерий по Граму, посев жидкости на микрофлору с определением чувствительности к антибиотикам В. A Runyon предлагает определять в асцитической жидкости сывороточно-асцитический альбуминовый градиент (СААГ).
СААГ = (альбумин сыворотки) - (альбумин асцитической жидкости), СААГ 1,1 может свидетельствовать о том, что причиной асцита является портальная гипертензия, обусловленная циррозом печени.
Лечение Отечно-асцитического синдрома:
Лечение отечно-асцитического синдрома при циррозе печени. При лечении асцита необходимо установить этиологию цирроза печени, выявить факторы, лежащие в основе его декомпенсации Выделяют базисную и диуретическую терапию.
Мероприятия, проводимые в рамках базисной терапии, включают постельный режим, уменьшение потребления поваренной соли, ограничение приема жидкости, соблюдение диеты. Для поддержания натриевого баланса целесообразно ограничить поступление хлористого натрия до 500 мг в сутки Проведение диуретической терапии предусматривает ежедневный контроль ряда параметров.
Все блюда готовят без добавления соли Целесообразно дополнить рацион белковой пищей с низким содержанием натрия. Энергетическая ценность диеты, содержащей 70 г белка (22 ммоль натрия в сутки - 500 мг NaCl), составляет 1500-2000 ккал/сут. Больным необходимо ограничивать прием жидкости до 750-1000 мг в сутки. Назначение постельного режима основано на том, что горизонтальное положение влияет на выработку ренина, ангиотензина и тонус симпатической нервной системы Вертикальное положение ведет к стимуляции симпатической нервной системы, уменьшению гломерулярной фильтрации, увеличению абсорбции натрия в канальцах. Начальный клинический эффект общих мероприятий оценивается после 4-го дня лечения.
Терапия диуретиками проводится по ступенчатому принципу. Прием диуретиков можно осуществлять при отсутствии тяжелых электролитных сдвигов и нарушений функции почек. Диуретики подавляют факторы, вызывающие задержку натрия, и повышают экскрецию натрия и воды. В лечении больных асцитом чаще используют две группы диуретиков. В первую группу входят петлевые диуретики* фуросемид, буметанид, этакриновая кислота. Ко второй группе относятся спиронолактон, триамтерен, амилорид
Больной с асцитом и отеками на фоне эффективной терапии должен терять не более 1 кг массы тела, при наличии асцита без отеков - не более 500 г в сутки. Монотерапия фуросемидом больных циррозом печени и асцитом нецелесообразна ввиду выраженных электролитных изменений Переход к следующей, более высокой ступени показан при потере массы тела больного на фоне лечения менее 1,5 кг за 4 дня терапии.
Тактика при длительном лечении больных циррозом печени с асцитом.После ликвидации асцита возникает вопрос о длительном лечении указанной категории лиц. Больные должны придерживаться рекомендованной бессолевой диеты, проводить регулярный контроль за количеством выпитой жидкости и выделенной мочи, измерять массу тела. Доза диуретического препарата зависит от тяжести и стадии заболевания. При этом чаще используются 100-200 мг/сут спиронолактона и через день 40-80 мг/сут фуросемида в сочетании с препаратами калия. Один раз в месяц нужно исследовать содержание электролитов, азота, мочевины, проводить функциональные пробы печени, определять содержание белка в крови.
Рефрактерный (ригидный) асцит. Термин "рефрактерный к лечению асцит" используется в том случае, когда при терапии, проводимой по всем правилам, масса тела не снижается. Если диуретическая терапия, проводимая, как минимум, в течение 4 нед, оказывается неэффективной и исключаются все причины, способные вызывать мнимую рефрактерность к лечению, можно думать о рефрактерном асците.
Причинами данного синдрома чаще являютсядалеко зашедший патологический процесс в печени, большие поступления натрия в организм (с пищей, лекарственными препаратами), отсутствие ограничения приема жидкости, нарушение функции почек, не связанное с заболеванием печени, происхождение асцита (злокачественные новообразования, воспаление асцитической жидкости) и др.
Эффективным методом лечения рефрактерного асцита является парацентез, при проведении которого удаляется 5-10 л жидкости на фоне введения бессолевого альбумина: по 6 г на 1 л удаляемой жидкости. В качестве симптоматической терапии таким больным показаны методы экстракорпоральной гемокоррекции: ультрафильтрация и реинфузия асцитической жидкости, перитонеовенозное шунтирование, имплантация TIPS, трансплантация печени.
К каким докторам следует обращаться если у Вас Отечно-асцитический синдром:
Вас что-то беспокоит? Вы хотите узнать более детальную информацию о Отечно-асцитического синдрома, ее причинах, симптомах, методах лечения и профилактики, ходе течения болезни и соблюдении диеты после нее? Или же Вам необходим осмотр? Вы можете записаться на прием к доктору .
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Гепатит С: причины появления, классификация, симптомы, диагностика и способы лечения.
Определение
Гепатит С – это вирусное инфекционное заболевание, которое вызывает воспаление печени, зачастую приводя к ее серьезным повреждениям. Вирус гепатита С распространяется через зараженную кровь.
До недавнего времени лечение гепатита С требовало еженедельных инъекций и приема пероральных препаратов, которые многие люди, инфицированные вирусом, не могли использовать из-за других проблем со здоровьем или серьезных побочных эффектов.
Сегодня ситуация изменилась – разработаны лекарства нового поколения, и с их помощью хронический гепатит С поддается терапии.
Тем не менее около половины людей с гепатитом С не подозревают о том, что инфицированы, поскольку часто болезнь протекает бессимптомно.
Поэтому скрининг гепатита С необходимо проходить регулярно, особенно при наличии факторов риска заражения.
Причины появления гепатита С
Заболевание обычно распространяется, когда кровь человека, зараженного вирусом гепатита С, попадает в организм незараженного. Особенно часто это происходит в среде наркоманов.
В группе риска находятся люди, которым часто переливают кровь, и длительное время находящиеся на гемодиализе.
Заражению подвержены новорожденные дети, если их мать больна гепатитом С.
Кроме того, существуют редкие, но все же возможные ситуации инфицирования вирусом:
- Совместное использование предметов личной гигиены, которые могли соприкасаться с кровью больного человека (бритвы, ножницы или зубные щетки).
- Половой контакт с человеком, зараженным вирусом гепатита С.
- Татуировки или пирсинг, выполненные в ненадлежащих санитарных условиях.
Вирус гепатита С не передается при совместном использовании столовых приборов, кормлении грудью, объятиях, поцелуях, при держании за руку, кашле или чихании, через укусы насекомых. Также он не распространяется через еду или воду.
- Острый гепатит С – это ранняя стадия, когда гепатит длится менее шести месяцев.
- Хронический гепатит С – это долгосрочный тип, когда заболевание длится больше шести месяцев.
- Минимальная активность (печеночные трансаминазы (АЛТ и АСТ) в биохимическом анализе крови повышены не более, чем на 3 нормы)).
- Умеренная активность (3–10 норм печеночных трансаминаз).
- Высокая активность (> 10 норм).
В течение первых 6 месяцев от начала заболевания человек может даже не подозревать, что болен, ощущая лишь необъяснимую усталость, плохой аппетит, тяжесть в правом подреберье, регулярную головную боль и головокружение.
В этот же период может меняться цвет кала (от светлого вплоть до белого) и мочи (от темно-желтой до коричневой). Некоторые пациенты говорят, что у них болят суставы.
По мере прогрессирования заболевания к первоначальным симптомам присоединяются спонтанные кровотечения (носовые, маточные, кровотечения из десен), желтушность кожных покровов, склонность к образованию гематом, зуд, накопление свободной жидкости в брюшной полости (асцит), отеки ног. Кроме того, пациенты начинают терять вес, снижается память, появляются проблемы со зрением, на коже формируются сосудистые звездочки.
У мужчин может отмечаться гинекомастия (увеличение грудных желез), снижение либидо, уменьшение размера яичек.
Симптомы острого гепатита С включают желтуху, усталость, тошноту, жар и мышечные боли. Они появляются через 1-3 месяца после инфицирования вирусом и продолжаются от двух недель до трех месяцев.
Диагностика гепатита С
Диагноз ставится на основании жалоб больного и анамнеза. При подозрении на вирусный гепатит С врач обязательно выясняет, были ли в течение жизни переливания крови, хирургические манипуляции, не употреблял ли пациент инъекционные наркотики, делал ли татуировки и пирсинг, имели ли место незащищенные половые контакты.
Для уточнения диагноза могут понадобиться следующие обследования:
-
Клинический анализ крови с развернутой лейкоцитарной формулой.
Синонимы: Общий анализ крови, ОАК. Full blood count, FBC, Complete blood count (CBC) with differential white blood cell count (CBC with diff), Hemogram. Краткое описание исследования Клинический анализ крови: общий анализ, лейкоформула, СОЭ См. также: Общий анализ – см. тест № 5, Лейкоцит.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Жидкость в брюшной полости: причины появления, при каких заболеваниях возникает, диагностика и способы лечения.
Определение
Состояние, при котором накапливается жидкость в брюшной полости, называется асцитом. Очень небольшое количество жидкости присутствует в полости брюшины всегда. Эта жидкость – следствие естественного процесса фильтрации крови через кровеносные сосуды.
Однако при некоторых заболеваниях жидкость либо начинает вырабатываться в избыточном количестве, либо перестает всасываться. В результате она постепенно накапливается в брюшине и давит на внутренние органы, серьезно нарушая их работу.
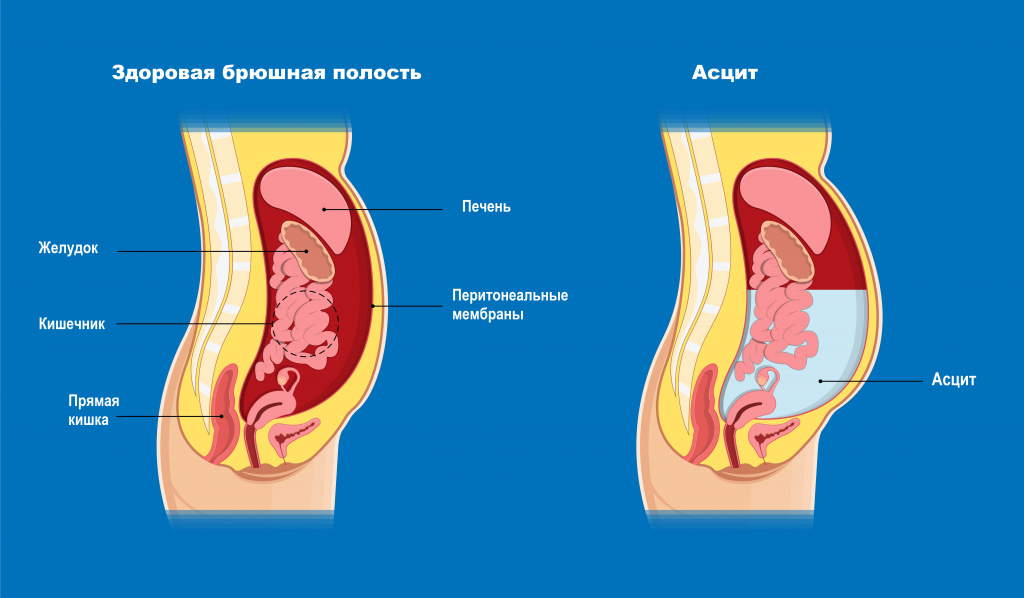
Разновидности асцита
По объему жидкости:
- небольшое количество;
- умеренное количество;
- значительное количество.
- стерильное содержимое (отсутствие бактериальной составляющей);
- инфицированное содержимое (может быть связано с прободением кишечника или желудка, а также с травмой живота и проникающим ранением);
- спонтанный бактериальный перитонит.
- асцит, поддающийся медикаментозной терапии;
- рефрактерный асцит – то есть не поддающийся лекарственной терапии или возвращающийся вновь спустя короткое время после лечения.
Онкологические процессы в организме также способны стать причиной асцита. Однако, как и в случае с заболеваниями печени, жидкость в брюшной полости появляется лишь по мере прогрессирования болезни. В первую очередь, следует обращать внимание на такие симптомы, как снижение массы тела, аппетита, повышенную утомляемость, болевой синдром, нарушение работы кишечника.
Хронические заболевания сердечно-сосудистой системы приводят к застою крови в левом круге кровообращения, вследствие чего внутрибрюшная жидкость начинает вырабатываться интенсивнее. Появлению асцита всегда предшествует длительная история сердечно-сосудистого заболевания.
Ухудшение состояния происходит постепенно и не очень заметно для больного, поэтому важно не нарушать врачебные предписания и обращаться за врачебной помощью своевременно.
Больного должна насторожить нарастающая слабость, появление или усиление одышки, ночного кашля, изменение привычных цифр артериального давления, появление или увеличение отеков на ногах, которые сначала становятся более выраженными к вечеру, а затем не проходят совсем.
Механизм данного процесса объясняется массивной потерей белка из-за неправильной работы почек и, соответственно, ухудшением всасывания жидкости. Кроме того, отечность присутствует на лице, шее, нижних конечностях, жидкость может скапливаться в грудной полости и полости сердца.
Асцит сопровождает ряд инфекционно-воспалительных заболеваний. По-прежнему довольно часто во врачебной практике встречается туберкулез, течение которого связано с поражением лимфатических узлов брюшной полости, что приводит к сдавливанию внутренних органов, в результате чего наблюдается скопление внутрибрюшной жидкости. Туберкулез обычно начинается с жалоб пациента на повышенную утомляемость, чрезмерную потливость, особенно в ночное время, снижение аппетита и похудение, длительное повышение температуры тела в пределах 37,3–38,3°С. У части больных наблюдаются несильные боли в животе без четкой локализации. Появление таких симптомов требует скорейшего обращения к врачу.
Хронический панкреатит иногда сопровождается асцитом. Такое состояние особенно характерно для людей, злоупотребляющих алкоголем. Накоплению жидкости в брюшной полости предшествуют интенсивные боли в животе.
Длительное голодание может приводить к появлению жидкости в брюшной полости за счет снижения уровня белка и нарушения процесса всасывания жидкости.
В этом случае объем жидкости будет небольшим, однако появление подобного симптома говорит о серьезных нарушениях в работе всего организма. Данное состояние потребует в дальнейшем проведения серьезного и длительного лечения под тщательным контролем множества лабораторных показателей.
Заболевания, приводящие к асциту
Некоторые онкологические заболевания.
Болезни поджелудочной железы.
Недоедание и истощение.
Заболевания эндокринной системы.
Гинекологические заболевания (эндометриоз, кисты и опухоли яичников).
К каким врачам обращаться при асците
Появление жидкости в брюшной полости является симптомом заболеваний, как правило, требующих госпитализации и длительного лечения. Постановкой диагноза и назначением терапии занимаются следующие специалисты: врач-гастроэнтеролог , онколог, кардиолог, эндокринолог, нефролог, пульмонолог, хирург, гинеколог.
Диагностика и обследования при асците
Тщательный сбор анамнеза с учетом всех жалоб пациента, осмотр и проведение дополнительной диагностики помогают установить правильный и своевременный диагноз.
-
Клинический анализ крови с развернутой лейкоцитарной формулой (для выявления воспалительных изменений при различных инфекционно-воспалительных заболеваниях.
Синонимы: Общий анализ крови, ОАК. Full blood count, FBC, Complete blood count (CBC) with differential white blood cell count (CBC with diff), Hemogram. Краткое описание исследования Клинический анализ крови: общий анализ, лейкоформула, СОЭ См. также: Общий анализ – см. тест № 5, Лейкоцит.
Токсический гепатит – поражение печени промышленными, сельскохозяйственными и бытовыми химическими веществами, гепатотропными ядами, приводящее к воспалительной реакции и некрозу гепатоцитов, изменению реактивности печени. Клинически проявляется гепатомегалией и болью в правом подреберье, желтухой, диспепсическими явлениями, энцефалопатией, асцитом, анорексией. Диагностика включает клинический и биохимический анализы крови, УЗИ, КТ либо МРТ печени и допплерометрию ее сосудов, биопсию, радиоизотопное исследование. Лечение направлено на прерывание контакта с токсическим веществом, выведение его из организма, проведение симптоматической терапии, трансплантации печени.
Общие сведения
Токсический гепатит – поражение печени острого, подострого либо хронического характера, развивающееся в результате попадания в организм токсических веществ, которые губительно воздействуют на клетки печени, вызывая их некроз. Токсическое поражение печени встречается не так уж часто – не более 1-2 случаев на 100 тысяч населения в год. Среди всех госпитализированных в отделения гастроэнтерологии в РФ токсические гепатозы, вызванные приемом гепатотропных ядов, выявляются примерно у 3% пациентов. Среди причин формирования печеночной недостаточности данная патология занимает второе место после алкогольного гепатита. Изучением гепатотоксичности различных химических веществ занимаются ведущие гепатологи, гастроэнтерологи и токсикологи всего мира.

Причины токсического гепатита
В зависимости от строения все гепатотоксичные химические вещества подразделяются на несколько групп. К первой группе относят хлорированные углеводороды – хлороформ, дихлорэтан, четыреххлористый углерод, хлористый метил, этилхлорид и другие. Эти вещества применяются в производстве автомобилей, самолетов, огнетушителей, в машиностроении, при пошиве обуви, в химчистках, для дезинфекции, дезинсекции и дегельминтизации, в качестве растворителей жиров. В организм проникают через кожу, при дыхании и употреблении внутрь. Выделяются легкими, почками, кишечником. Четыреххлористые углеводороды воздействуют на эндоплазматический ретикулум, разрушая ферментативные системы гепатоцита; усиливают переокисление ненасыщенных жирных кислот в клеточных мембранах.
Вторая группа веществ включает дифенилы и хлорированные нафталины – они используются в оболочках электропроводов, в электроконденсаторах, могут применяться в качестве аналогов воска, смолы, каучука. Третья группа состоит из бензола и его производных: анилина, толуола, тринитротолуола и др. Эти соединения в последние годы активно эксплуатируются в промышленности при производстве взрывчатых веществ, органических красок. В кровоток попадают после контакта с кожей, слизистыми оболочками, при приеме внутрь.
В четвертой группе находятся металлоиды и металлы – золото, фосфор, мышьяк, олово, ртуть, свинец. В настоящее время данные химические элементы в промышленности используются редко, производители стараются найти им более безопасную замену. Тяжелые металлы связываются с сульфгидрильными группами, блокируя активность печеночных ферментов. В отдельную группу выносят природные гепатотропные яды (ядовитые грибы, семена гелиотропа опушенного), сельскохозяйственные и бытовые инсектициды.
Все химические вещества, попадающие в организм, подвергаются разрушению либо связыванию. Основную роль в этих процессах играет печень. Некоторые вещества и их производные, образующиеся при биотрансформации, могут оказывать токсическое действие на гепатоциты. При этом гепатотоксичность может быть истинной (возникает у всех людей при введении определенной дозы вещества в организм) либо проявляться идиосинкразией (индивидуальная гиперчувствительность организма к данному соединению). Механизм действия гепатотропного яда зависит от его химического строения и дозы, однако результатом в любом случае будет разрушение клеток печени и сбой обменных процессов в ней.
Разрушающее влияние перечисленных токсических веществ значительно усиливается, если в прошлом гепатоциты подвергались воздействию больших доз алкоголя, гепатотоксичных лекарственных препаратов, вирусов и бактерий. Также токсический гепатит быстрее развивается у людей, страдающих истощением и дефицитом белка в организме.
Симптомы токсического гепатита
Для всех токсических гепатитов характерно наличие двух групп симптомов: признаков поражения непосредственно печени (желтуха, гепатомегалия, боли в правом подреберье) и признаков токсического воздействия на другие органы (зависят от химического строения отравляющего вещества).
Острое поражение четыреххлористыми углеводородами манифестирует симптомами повреждения головного мозга: угнетение сознания вплоть до комы в пределах одних-двух суток, головная боль, выраженная слабость. Затем присоединяются желтуха, тошнота, рвота, понос, повышение температуры до субфебрильных цифр, затрудненное дыхание, синюшный цвет кожи, желудочно-кишечные кровотечения. Смерть от острой печеночной недостаточности может наступить в течение нескольких дней – двух недель (в зависимости от дозы токсина). Хроническое отравление данными химическими веществами проявляется головной болью, болью в области печени, диспепсическими явлениями, слабостью. Постоянный контакт с четыреххлористыми углеводородами может привести к развитию цирроза печени на протяжении нескольких месяцев.
Для отравления производными бензола характерен токсический гепатит, которому сопутствуют апластическая анемия, поражение головного мозга, катаракта. Постоянный контакт с бензолом приводит к развитию хронического токсического гепатита, сопровождающегося геморрагическим синдромом, асцитом, циррозом печени.
Отравление мышьяком клинически проявляется желтухой, увеличением размеров печени, нарушением функции почек и периферических нервов. Для поражения фосфором, кроме симптомов токсического гепатита, характерны повышенная кровоточивость, гипогликемия. Токсический гепатит при воздействии меди развивается только в случае попадания в организм более одного грамма этого химического элемента, смерть – при превышении дозы в 10 грамм. Симптомы отравления медью – острая боль в области желудка, тошнота, рвота, профузный понос, кровотечения, уменьшение объема мочи. Смерть наступает от фульминантной почечной и печеночной недостаточности. Токсическое поражение печени железом напоминает отравление медью.
При употреблении ядовитых грибов клиническая картина токсического гепатита развивается в течение ближайших двадцати часов. Также поражаются почки, центральная нервная система. Пациенты предъявляют жалобы на желтушность кожных покровов, тошноту, рвоту, сильные боли в животе, диарею. Выраженная дегидратация и дисэлектролитемия приводят к сбоям в работе сердечно-сосудистой системы (нарушения ритма вплоть до остановки сердца) и головного мозга (судорожный синдром, угнетение сознания). Острый некроз печени приводит к прекращению ее белково-синтезирующей функции, что проявляется массивным геморрагическим синдромом. Каждый второй больной погибает от печеночной энцефалопатии, уремии, сердечно-сосудистых нарушений; у остальных формируется цирроз печени.
Употребление злаков, зараженных семенами гелиотропа, чаще всего приводит к хронической интоксикации, проявляющейся симптомами токсического поражения печени и вено-окклюзионной болезни (желтуха, гепатомегалия, боли в правом подреберье, асцит, ожирение).
При отравлении инсектицидами данные химические соединения накапливаются в жировых клетках печени и других органов, что ведет к формированию полиорганной недостаточности: токсического гепатита, миокардита, нефрита, поражения центральной нервной системы, развития агранулоцитоза. При хроническом поражении инсектицидами, помимо клинической картины токсического поражения печени, пациент отмечает появление полирадикулопатий, болей в сердце, нарушения функций почек; в анализах выявляют анемию и лейкопению. После прекращения воздействия инсектицида на организм данные патологические изменения быстро регрессируют.
Диагностика
Лабораторная диагностика токсического гепатита не позволяет выявить специфичные признаки данной патологии. Следует помнить, что у 3% здоровых людей печеночные пробы могут быть изменены, еще примерно у 5% их изменение никак не связано с поражением печени. И наоборот, примерно в 10% случаев токсического гепатита лабораторные показатели будут находиться в границах нормы. Оценка тяжести поражения печени проводится на основании исследования уровней общего билирубина и его фракций, трансаминаз, ферментов (ЩФ, ГГТП, ЛДГ), альбумина и протромбина. Для выявления некоторых гепатотоксичных веществ возможно проведение специальных лабораторных тестов. Обязательно проводят исследования на вирусные гепатиты, ВИЧ.
Из инструментальных методов в диагностике токсического гепатита используют УЗИ, КТ и МРТ печени, допплерометрию печеночных сосудов, эластографию, радиоизотопное исследование гепатобилиарной системы. Перечисленные методики не дают возможности определить этиологию гепатита, но позволят подтвердить поражение печени. Наиболее точным способом оценки морфологических изменений при токсическом гепатите является биопсия печени с последующим гистологическим исследованием биоптатов.
Токсический гепатит следует дифференцировать с поражением печени алкоголем, медикаментами, бактериями, вирусами и паразитами; с желчнокаменной болезнью, раком печени и другими опухолями данной локализации, аутоиммунным гепатитом, пороками развития печени и ЖВП, болезнями обмена веществ, острым панкреатитом, реактивным гепатитом.
Лечение токсического гепатита
Основное направление лечения токсического гепатита любой этиологии – прекращение контакта с химическим агентом, обезвреживание и быстрое выведение его из организма. При отравлении тяжелыми металлами антидотами являются унитиол, тиосульфат натрия (для ртути, мышьяка, свинца); дефероксамин (для железа); бензиламин, глюкокортикостероиды (для меди). Всем пациентам обязательно назначают витамины группы В, фолиевую, никотиновую и аскорбиновую кислоты. Если на фоне токсического гепатита развилась тяжелая печеночная и/или почечная недостаточность, проводят гемодиализ. При формировании фульминантной печеночной недостаточности может потребоваться трансплантация печени.
Прогноз и профилактика
В большинстве случаев проявления токсического гепатита регрессируют после прекращения контакта с ядовитым веществом, наступает полное выздоровление. После тяжелого токсического поражения печени с массивным некрозом гепатоцитов развивается цирроз печени, в редких случаях – рак печени.
Профилактика токсического гепатита заключается в строгом соблюдении техники безопасности при контакте с токсичными веществами, проведении регулярных медицинских осмотров всего контингента контактирующих с токсинами рабочих (для своевременного выявления лиц с патологией печени и недопущения их к работе с токсическими химическими соединениями), налаживании здорового питания с достаточным количеством белка, борьбе с алкоголизмом.
Читайте также:

