Триггерная роль вирусов в этиологии опухолей
Обновлено: 19.04.2024
ДНК-вирусы как причина развития рака - вирусный канцерогенез
В канцерогенезе также могут участвовать ДНК-содержащие вирусы. Наиболее крупные ДНК-содержащие вирусы принадлежат к группе герпесвирусов. Первым вирусом, выделенным из культуры опухолевых клеток, был вирус Эпштейна-Баррра (ЭБВ).
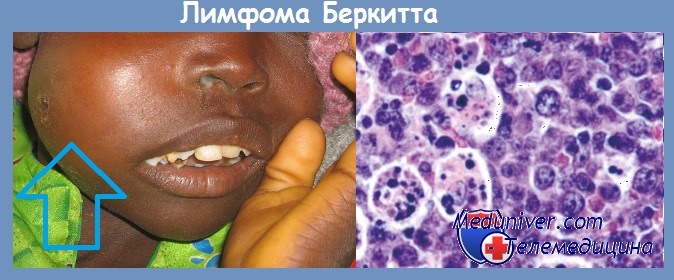
Вирус был получен из культуры опухолевых клеток больных лимфомой Беркита. В культуре in vitro ЭБВ вызывает бесконечную пролиферацию человеческих В-лимфоцитов. Вирусные гены, встраиваясь в геном этих клеток, инициируют пролиферацию путем активации клеточных генов-регуляторов роста (онкогенов).
В крови больных лимфомой Беркита обнаруживается более высокий, чем у здоровых людей, титр антител к антигенам вирусной оболочки и к мембранным антигенам. В то же время в африканских странах среди множества детей, инфицированных этим вирусом, лимфома развивается только в единичных случаях.
Механизм онкогенеза этого заболевания не может быть объяснен только вирусным заражением. К тому же, за пределами африканского континента регистрируются случаи заболевания лимфомой Беркита, абсолютно не связанные с инфицированием вирусом ЭБВ. По-видимому, ЭБВ также может принимать участие в патогенезе карциномы носоглотки, так как клетки этой опухоли экспрессируют вирусные антигены EBNA-1.
При исследованиях саркомы Капоши, развивающейся у больных СПИДом, в 1994 г. из ее клеток был выделен новый герпесвирус. Первоначально вирус получил название герпес-вируса саркомы Капоши (ГСК), впоследствии он был переименован в герпесвирус человека серотип 8 (ГВЧ 8). Вирус обнаруживается в веретеновидных клетках саркомы Капоши практически при всех случаях заболевания.
ГВЧ 8 был также найден в опухолевых клетках первичной эффузионной лимфомы и в клетках многоочаговой болезни Кастлемана. Данный вирус кодирует синтез циклина, который является промотором клеточного деления, чем и объясняется высокая пролиферативная активность инфицированных клеток.
Человеческие папилломавирусы (ПВЧ) вызывают кожные бородавки и ряд доброкачественных папиллом. Это весьма обширный класс вирусов, и некоторые его представители могут в той или иной степени участвовать в развитии злокачественных опухолей. Большинство вирусов вызывает лишь ограниченную пролиферацию клеток, но ряд серотипов может вызвать и развитие злокачественных новообразований.
Наибольшую опасность с точки зрения онкологии представляют серотипы 16, 18, 31 и 33. Более 90% опухолей карциномы шейки матки in situ обнаруживают в своих клетках генные последовательности вирусов ПВЧ. Эти вирусы также играют значительную роль в возникновении инвазивных и многоочаговых плоскоклеточных раков кожи, которые часто развиваются у больных после долгосрочных курсов иммуносупрессивной терапии.
Механизмы вирусного канцерогенеза в этом случае изучены недостаточно. В исследованиях доказано, что существует вероятность включения вирусной ДНК в клетки базального эпителия. Обычно в клеточную ДНК внедряются восемь ранних и два поздних гена. Ранние гены Е6 и Е7 вызывают пролиферацию клеток.
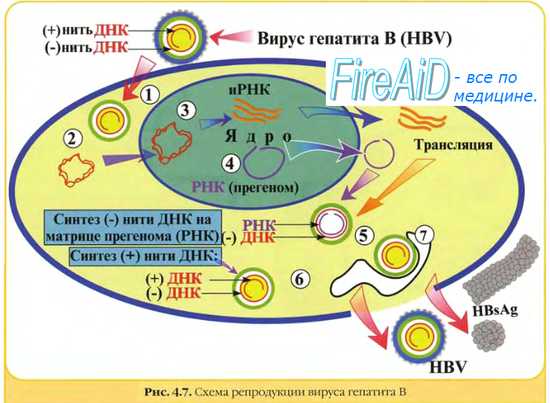
Вирус гепатита В четко связывают с развитием печеночно-клеточного рака. Риск развития этого заболевания у инфицированных вирусом в 200 раз превышает таковой у неинфицированных людей. Механизмы зарождения рака не до конца понятны: считается, что вирус вызывает бесконечную пролиферацию клеток, хотя зараженные вирусом клетки уничтожаются иммунной системой организма. Возможно, что пролиферирующие клетки становятся чувствительными к другим канцерогенам, например к афлатоксину.
Подытоживая вышесказанное, можно заключить, что основным механизмом канцерогенного воздействия является повреждение молекул ДНК и нарушения процессов ее репарации. Если не происходит исправления первичных повреждений ДНК, ошибки со временем начинают накапливаться, что ведет к дестабилизации структуры хромосом и к соматическим мутациям. Большинство таких мутаций летальны для клетки.
Однако, если часть клеток выживает, происходит постепенное накопление клеточной массы с опухолевым фенотипом, что в итоге приводит к клиническим проявлениям. Большой вклад в понимание этого процесса внесли современные исследования механизмов регулировки клеточного цикла и недавнее открытие регуляторных белков, которые запрещают клетке делиться, если ее геном сильно поврежден.
Для развития опухоли может быть недостаточно единичных мутаций в генах-регуляторах деления, но накопление массы ошибок в регуляторных генах может привести к фатальным последствиям. Особенно критичны мутации в генах, регулирующих клеточное деление, так называемых онкогенах. Очень опасны также мутационная инактивация генов, подавляющих клеточное деление — генов-подавителей опухоли, и мутации в генах, кодирующих белки, запрещающие деление при повреждении клеточного генотипа.
Накопление числа жизнеспособных мутаций по одному или нескольким из этих генов приводит к общей клеточной дезорганизации и к потере контроля над клеточным делением. В следующем разделе мы рассмотрим механизмы действия онкогенов и наиболее важные моменты контроля над клеточным циклом.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Рак – бич человечества. По смертности он занимает второе место после сердечно-сосудистых заболеваний, по страху, который внушает людям – первое. Тысячи исследователей стремятся понять его причины, найти пути к его профилактике и лечению. Десятки институтов и сотни лабораторий во всем мире работают над этой проблемой, пытаясь достичь успеха в ее понимании и прогресса в профилактике и лечении этого заболевания.
Современной науке известны некоторые факторы, вызывающие развитие злокачественных опухолей и, вместе с тем, ученые вынуждены констатировать, что основная часть злокачественных опухолей возникает спонтанно, то есть без видимой связи с индуцирующими агентами. К факторам, способным вызывать развитие опухоли, относятся: различные канцерогенные вещества, наследственная предрасположенность, ионизирующее излучение и опухолеродные вирусы.
Вирусно-генетическая теория возникновения опухолей, предложенная еще в 40-х годах ХХ века Л.И. Зильбером, получила за прошедшие годы многочисленные подтверждения. В настоящее время, очевидно, что хотя вирусы и не являются единственной причиной рака, но они играют большую роль в возникновении злокачественных заболеваний как у человека, так и у животных. Характерной особенностью опухолевых заболеваний, ассоциированных с вирусами, является длительный латентный период, от момента инфекции до проявления заболевания могут пройти годы и даже десятилетия.
Согласно современным данным, этиологическими агентами около 15% опухолевых новообразований человека являются вирусы. К таким вирусам относятся: вирус Т-клеточного лейкоза/лимфомы (human T-leukemia/lymphoma virus), вирус иммунодефицита человека (ВИЧ), вирус папилломы человека (ВПЧ), вирусы гепатита В и С, вирус Эпштейна-Барр (ВЭБ) и другие. Важно отметить, что некоторые вирусы ассоциированы с опухолями только одной локализации, тогда как другие — с разными злокачественными новообразованиями, что, вероятно, обусловлено тропизмом вирусов к клеточным системам определенного типа.
Вирус Т-клеточного лейкоза/лимфомы (HTLV-1). HTLV-1 – это онкогенный вирус, способный вызывать Т-клеточный лейкоз/лимфому у взрослых, а также тропический спастический парапарез и ряд других неонкологических заболеваний.
Существуют 3 основных пути передачи инфекции от инфицированных лиц:
- с молоком матери;
- при половом контакте;
- с переливаемой кровью при гемотрансфузиях.
Основными методами диагностики вирусов гепатита В и С являются методы иммуноферментного анализа и полимеразной цепной реакции.
Вирус папилломы человека (ВПЧ, human papilloma virus). В середине 70-х гг. прошлого века было высказано предположение, что вирус папилломы человека является этиологическим агентом рака шейки матки, и эта область онкологии и вирусологии получила стремительное развитие. Действительно, к настоящему моменту роль ВПЧ в развитии рака шейки матки не вызывает сомнений. Многочисленные исследования доказали, что не менее 95% злокачественных опухолей шейки матки содержат разновидности ВПЧ, принадлежащие к так называемым типам "высокого онкогенного риска" (ВПЧ 16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59 типов). Среди них максимальной онкогенной активностью обладают ВПЧ 16 и 18 типов. Действительно, ВПЧ достаточно часто (примерно в 30% случаев) выявляется у абсолютно здоровых женщин. Однако не у всех женщин, зараженных вирусом папилломы человека, возникает дисплазия шейки матки и рак шейки матки. Примерно у 80% женщин иммунная система организма в течение 2 лет после инфицирования сама избавляется от вируса. Таким образом, носительство этих вирусов свидетельствует не о злокачественном процессе как таковом, а о многократно повышенном риске его возникновения.
Диагностика ВПЧ-инфекции обладает очень высокой клинической значимостью. Она позволяет выявить тех пациенток, для которых жизненно необходимы активные, комплексные меры, направленные на профилактику и раннюю диагностику рака шейки матки. Самым надежным диагностическим тестом по выявлению всех 12 онкогенных типов вируса папилломы человека в настоящее время является метод полимеразной цепной реакции в режиме реального времени.
Вирус Эпштейна-Барр (ВЭБ). Известен широкий спектр патологических состояний, представленный опухолями лимфоидного и эпителиального происхождения, в возникновении которых ВЭБ принимает непосредственное участие. Доказано, что этот вирус причастен к возникновению не только лимфомы Беркитта, но и ряда других злокачественных и доброкачественных новообразований, таких, как рак носоглотки, лимфома Ходжкина, инфекционный мононуклеоз и многие другие.
Согласно некоторым исследованиям, ВЭБ широко циркулирует среди населения, о чем свидетельствует высокий процент людей, имеющих в крови антитела к ВЭБ - 50% детей и 85% взрослых. Но поскольку инфекция, как правило, протекает бессимптомно, сложилось ошибочное мнение о невысокой заболеваемости ВЭБ-инфекцией.
Вирус герпеса человека 8 типа (HHV-8). В настоящее время считается доказанной его роль в возникновении саркомы Капоши, выпотной лимфомы полостей тела и болезни Кастельмана. В геноме HHV-8 содержится ряд генов, продукты которых играют важную роль в регуляции размножения и жизнеспособности клеток; повышение их активности приводит к возникновению опухоли.
Следует понимать, что HHV-8 является всего лишь фактором риска развития вышеуказанных заболеваний. Если человек инфицирован HHV-8, то это не означает, что у него обязательно разовьётся саркома Капоши или лимфома.
Сам по себе вирус герпеса 8 типа опасности для здорового человека практически не представляет. Большинство людей с нормальным иммунитетом, инфицированных этим вирусом, не отмечают каких-либо проявлений, и он не оказывает на них никакого вредного влияния.
Свое негативное действие HHV-8 может проявить только в случае стойкого снижения иммунитета (иммунодепрессии), и то лишь у больных СПИДом (зараженных вирусом ВИЧ) или при длительном лечении, снижающем иммунитет (после пересадки органов и тканей, лучевой терапии). По данным статистики у 45% людей, имеющих HHV-8 и ВИЧ в течение 10 лет развилась саркома Капоши. У людей с нормальным иммунитетом вирус герпеса человека никак себя не проявляет. Он не влияет на состояние здоровья.
Таким образом, несмотря на различную организацию онкогенных вирусов человека они обладают рядом общих биологических свойств, а именно:
- вирусы лишь инициируют патологический процесс, усиливая процессы деления клеток и генетическую нестабильность инфицированных ими клеток;
- у инфицированных онкогенными вирусами лиц возникновение опухоли, как правило, событие нечастое: один случай новообразования возникает среди сотен, иногда тысяч инфицированных;
- от момента инфицирования до возникновения опухоли имеет место продолжительный латентный период, длящийся годами, иногда десятилетиями;
- у большинства инфицированных лиц возникновение опухоли не является обязательным, но они могут составить группу риска, с более высокой вероятностью ее возникновения;
- для злокачественной трансформации инфицированных клеток необходимы дополнительные факторы и условия, приводящие к прогрессированию наиболее агрессивного опухолевого клона.
Такими дополнительными факторами, играющими роль сопутствующих канцерогенов, могут быть: злоупотребление алкоголем, табакокурение, коинфекция генитальным герпесом, малярия, нитрозамины в продуктах питания, пестициды.
На сегодняшний день основными методами лабораторной диагностики являются метод иммуноферментного анализа (ИФА) и метод полимеразной цепной реакции (ПЦР). Первый позволяет выявить белок вируса либо антитела к нему, которые выделяет организм в ответ на инфицирование. При помощи метода ПЦР мы можем выявить генетический материал самого вируса.
Метод иммуноферментного анализа является стандартным методом лабораторной диагностики.
Следует также отметить, что не всегда возможно определение вирусных белков в плазме крови. В таких случаях методом ИФА можно диагностировать только наличие антител в плазме крови пациента. Однако, важно помнить, что антитела могут вырабатываться в довольно длительный срок. Так, например, при инфицировании ВИЧ антитела вырабатываются в течение 6 месяцев, в случае гепатита С этот период может длиться до года, а антитела к вирусу Эпштейна-Барр (иммуноглобулины класса G) присутствуют у большого количества практически здоровых людей и их диагностика обладает низкой прогностической значимостью.
Полимеразная цепная реакция (ПЦР) — метод молекулярной биологии, позволяющий обнаружить возбудителя заболевания на основе его генетической информации.
ПЦР диагностика дает возможность существенно ускорить и облегчить диагностику различных заболеваний, в частности, вирусов гепатита В, С, D, цитомегаловирусной инфекции, вируса Эпштейна-Барр, вируса простого герпеса, а также хламидиоза, микоплазмоза, уреаплазмоза и т.п. При помощи данного метода вирусные инфекции можно обнаружить уже через 5–7 дней после заражения, за недели или месяцы до того, как появятся антитела или первые симптомы. Метод ПЦР позволяет выявить даже единичные клетки возбудителя, благодаря многократному увеличению последовательностей ДНК.
Полимеразная цепная реакция - это один из самых точных методов лабораторной диагностики. Его чувствительность составляет 95–99%, а специфичность достигает 100%.
Таким образом, достижения науки в области онкологии внесли определенную ясность в понимание механизмов возникновения некоторых злокачественных новообразований и все же большую часть из них не удается увязать с инфицированностью тем или иным вирусом, что создает большое поле деятельности современным онкологам в направлении дальнейшего изучения механизмов развития онкологических заболеваний.
Все вышеуказанные методы диагностики существуют у нас в РНПЦ онкологии и медицинской онкологии им. Н.Н.Александрова. В лаборатории клинической молекулярной генетики и иммунологических методов диагностики можно пройти обследование на вирусы герпеса,цитомегаловируса, Эпштена-Барра, вирусы гепатита В и С, а также пройти обследование на инфицирование вирусом папилломы человека, данные исследования может пройти любой человек обратившийся в центр.
Основным направлением деятельности онкологическом отделении (вирусологии) является проведение молекулярно-биологических исследований с использованием метода полимеразной цепной реакции (ПЦР) в режиме реального времени и иммуноферментного анализа для выявления вирусного и бактериального инфицирования.
Диагностика вирусных и бактериальных инфекций позволяет:
- Выявить вирусное и бактериальное инфицирование на ранней стадии;
- Провести эффективное лечение на раннем этапе;
- Осуществлять мониторинг проводимого лечения;
- Оценивать эффективность проведённого лечения.
Вирусный канцерогенез

Молекулярно-генетические исследования с использованием методов полимеразной цепной реакции (ПЦР), позволяют диагностировать ДНК/РНК вирусных и бактериальных агентов, которые имеют немаловажное значение в преобразовании нормальной клетки в злокачественную.
Внедрение опухолеродного вируса в геном клетки, приводящее к нарушению контроля клеточного деления, является одним из инициирующих шагов многоступенчатого процесса канцерогенеза. При этом заражение онкогенным вирусом не означает однозначно, что в последующем образуется злокачественная опухоль, но сформируется вероятность ее появления.
В настоящее время можно считать установленным, что на долю опухолей, ассоциированных с вирусами, приходится около 20% всех опухолей человека. Онкогенные вирусы, принадлежащие к разным семействам, используют во многом сходную стратегию для инициации канцерогенеза.
Среди этих общих свойств можно назвать нарушения работы клеточных сигнальных путей, контролирующих пролиферацию, дифференцировку, целостность генома, миграцию клеток, апоптоз, иммунный ответ.
Механизмы реализации онкогенного потенциала вирусов включают:
- взаимодействие вирусных белков с клеточными белками – компонентами сигнальных путей;
- встраивание генома вируса в геном клетки (интеграция);
- влияние на эпигенетические механизмы регуляции экспрессии генов.
Исследования последних лет позволяют предположить, что все онкогенные вирусы успешно используют ограничение транскрипции своих генов, накладываемые метилированием ДНК, репрессивными модификациями гистонов и клеточными микроРНК, для ухода от иммунологического контроля, что способствует персистенции вирусного генома в клетке хозяина.
В настоящее время выявлено несколько групп вирусов, предрасполагающих к развитию опухолей у человека.
Опухоли человека, ассоциированные с вирусами
| Вирус | Опухоль |
|---|---|
| Вирусы папиллом (HPV) типов 3, 6, 11, 32, 72, 73 | Доброкачественные: папилломы, кондиломы кожи и слизистых |
| Вирусы папиллом (HPV) типов 16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59, 70 | Злокачественные: рак шейки матки, рак анального канала |
| Вирус гепатита В (HBV) | Первичный рак печени |
| Вирус гепатита С (HСV) | Первичный рак печени |
| Вирус Т-клеточной лейкемии человека (HTLV-1) | Т-клеточный лейкоз у взрослых |
| Вирусы герпеса: вирус Эпштейна-Барр (EBV) вирус герпеса 8 типа (HSV-8) | Лимфомы, рак носоглотки, рак желудка Саркома Капоши (на фоне иммуносупрессии) |
Рак шейки матки (РШМ)
Рак шейки матки (РШМ) – одно из наиболее распространенных онкологических заболеваний, занимающее второе место по частоте встречаемости среди женщин в мире. Ежегодно регистрируется около 600 тыс. новых случаев РШМ и свыше 95% РШМ ассоциировано с вирусами папилломы человека (HPV) высокого онкогенного риска.
Эпидемиологические исследования показали, что заболевание могут вызывать 18 типов вируса, из которых наиболее часто (в 94 % случаев) встречаются двенадцать: 16, 18, 31, 33, 35, 39, 45, 52, 56, 58, 59, 66.
Инфицированность HPV достаточно высока: геном вируса определяется у 46% женщин и 33% мужчин. Максимальный риск заражения отмечен в возрасте от 16 до 25 лет. Однако не у всех женщин развиваются дисплазия и рак шейки матки – примерно у 80% иммунная система организма в течение 2 лет после инфицирования сама избавляется от вируса. Таким образом, носительство этих вирусов свидетельствует не о злокачественном процессе как таковом, а многократном повышении риска его возникновения. Диагностика HPV-инфекции необходима для отбора пациенток, которым показано проведение комплексных мероприятий, направленных на профилактику и раннюю диагностику рака шейки матки.
Заболеваемость раком анального канала также тесно связано с инфицированием HPV – геном вируса определяется в 80-85% случаев.
В настоящее время доказано участие и других вирусных агентов (вирусов гепатита В и С, вируса Т-клеточной лейкемии человека, вируса Эпштейна-Барр, вируса герпеса 8 типа) в развитии злокачественных опухолей различных локализаций.
Вирусные гепатиты
Инфицирование вирусными гепатитами ведет к увеличению риска развития первичного рака печени. Во всем мире хронические вирусные гепатиты В и С, зачастую имея бессимптомное течение, являются самыми значимыми факторами риска развития цирроза и рака печени.
Своевременная диагностика вирусных гепатитов позволяет не только выявить заболевание на ранней стадии, тем самым предотвратив возникновение осложнений, но и исключить возможное инфицирование окружающих Вас людей. Кроме печени вирусы гепатитов способны поражать лимфатическую ткань, вызывая развитие неходжкинских лимфом, селезенку, почки, слюнные железы и др.

Важным открытием было обнаружение сходства продукта экспрессии онкогена с нормальным белковым фактором роста кровяных пластинок. Это позволило предположить, что злокачественная трансформация клеток онкогеном может осуществляться путём избыточного производства продукта, в норме стимулирующего рост. Если, как указывает И.Ф. Сейц (1984), такая закономерность будет установлена, то причину злокачественной трансформации нужно будет искать не в качественных, а в количественных изменениях механизмов, регулирующих рост на нормальной физиологической основе.
Прямая этиологическая роль вирусов в возникновении злокачественных опухолей человека доказана пока лишь в единичных случаях (это Т-клеточный лейкоз взрослых и, вероятно, африканская лимфома Беркитта). В свое время выдвигались концепции о едином механизме канцерогенеза, осуществляемом за счет гипотетических провирусов или протовирусов. В настоящее время вирусный канцерогенез рассматривается лишь как частный случай канцерогенеза, а общим звеном в возникновении опухолей любой этиологии считается активация, превращение собственных клеточных генов (протоонкогенов) в онкогены.
Если хромосомные мутации возникают в половых клетках, то они затем обнаруживаются и во всех соматических клетках нормальных тканей, и в опухолевых клетках. При злокачественных новообразованиях, не связанных с мутациями половых клеток, нормальные ткани сохраняют нормальный кариотип, а хромосомы опухолевых клеток могут быть изменены, причем эти изменения могут быть специфическими только для данной опухоли. Впервые специфические изменения кариотипа в опухолях были обнаружены в I960 г. в клетках хронического миелоидного лейкоза (ХМЛ) так называемой филадельфийской (Ph´) хромосомы, возникновение которой обусловлено транслокацией длинного плеча хромосомы 22 на длинное плечо хромосомы 9. Это нарушение отмечают у 70-90 % больных, у остальных Ph´-хромосомы не обнаруживают, причём клиническое течение болезни у них также несколько отлично, равно как и реакция на терапевтическое вмешательство. Рh´-хромосома, как и многие другие хромосомные маркёры, не связанные с мутацией в половых клетках, является приобретённым, а не наследуемым признаком.
Большая работа по идентификации канцерогенов человека проводится IARC, созывающего для этого комиссии экспертов из разных стран, которые обсуждают результаты опубликованных эпидемиологических исследований.
Вирусные болезни как причина онкологических заболеваний - рака

Вирусные инфекции ответственны за развитие примерно 10-15% всех онкологических заболеваний у человека. Значимость вирусных инфекций в онкологии значительно возросла с возникновением эпидемии синдрома приобретенного иммунодефицита (СПИД), так как при этом заболевании смертность от рака преобладает в общем числе смертных случаев.
Механизмы вирус-индуцированного канцерогенеза будут обсуждаться в отдельной статье на сайте. Среди вирусов, наиболее часто ассоциируемых с онкологическими заболеваниями, находятся вирус Эпштейна-Барра (ВЭБ), герпесвирус саркомы Капоши ((ГСК) или герпесвирус человека серотипа 8 (ГВЧ8)) и вирус человеческой папилломы. Вирус ВЭБ вызывает лимфому Беркита и рак носоглоточной полости у небольшого процента зараженных им людей.
Лимфома наиболее часто встречается в районах Африки, прилегающих к пустыне Сахара, и в районах с эндемическими очагами малярии. Распространение саркомы Капоши также в основном характерно для близлежащим к Сахаре регионов и в большой степени этому заболеванию подвержены евреи, проживающие в средиземноморском регионе. Известно, что инфицированность ГВЧ8 тесно связана с риском развития саркомы в ходе течения связанных со СПИДом заболеваний.
ГВЧ8 также увеличивает риск развития многоцентровой болезни Каслемана и первичной эффузионной лимфомы. У жителей Италии и Северной Африки отмечается повышенное в сравнении с жителями Великобритании или США содержание антител к вирусу ГВЧ8 (ГСК).
Существенным фактором риска при развитии рака шейки матки являются папилломавирусы. Среди более 100 разновидностей этих вирусов наибольшую опасность представляют серотипы 16, 18, 31 и 33 (несколько менее опасны серотипы 6 и 11).
Рак могут вызывать и представители семейства ретровирусов. Наиболее общеизвестный пример — вирус Т-клеточной лейкемии, серотип 1 (ВТКЛ-1) который является эндемической инфекцией в южной Японии и на Карибском море. У жителей этих регионов опухоли развиваются только у незначительной части инфицированных. Вирус может передаваться от матери к ребенку во время беременности через плаценту, а также с молоком при кормлении. Возможна передача вируса через сперму.
ДНК-Содержащий вирус гепатита В передается через кровь или при половых контактах и вызывает гепатит и цирроз печени. Среди людей, пораженных таким вирусом, печеночно-клеточная карцинома встречается в 100 раз чаще, чем у неинфици-рованных. РНК-Содержащий вирус гепатита С также вызывает хронический гепатит и значительно повышает риск заболеваемости печеночно-клеточной карциномой.
Оба вируса широко распространены по всему миру, но особенно часто встречаются у жителей Китая и Тайваня, а также среди лиц, принимающих наркотики внутривенно. Эти два вируса являются основной причиной смертности от заболеваний раком печени.
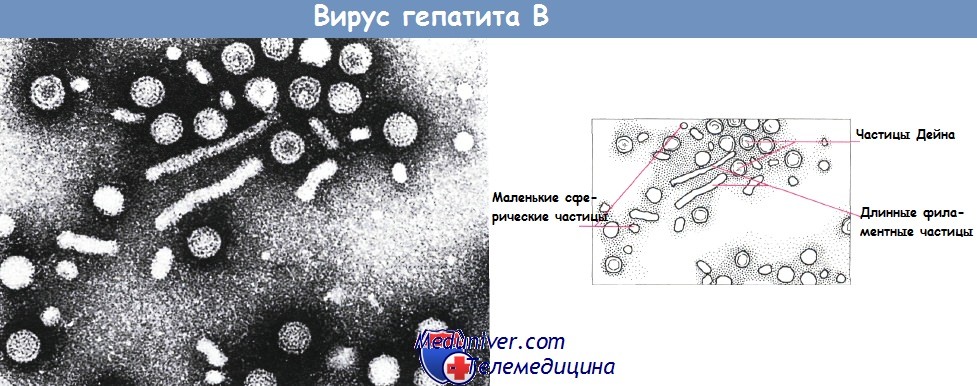
Электронная микрофотография вируса гепатита В.
На срезе видны мелкие сферические частицы с диаметром 28 нм (HBsAg); более крупные сферические двумембранные частицы Дейна (42 нм), продолговатые филаментозные частицы.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Читайте также:

