Тромбоцитопения у детей при гриппе
Обновлено: 15.04.2024
Лечение идиопатической тромбоцитопенической пурпуры. Эффективность спленэктомии
Терапевтические показания в настоящее время проще, после длительного опыта различных терапевтических попыток. Лечение идиопатической тромбоцитопенической пурпуры назначается в соответствии с клинико-гематологической формой, определяемой посредством специальных тестов и состоит, для излечимых форм, в кортикотерапии, в некоторых случаях в спленэктомии и в особых случаях в иммуносуппрессивпой терапии. Первым условием лечения с точным показанием является правильный диагноз идиопатической тромбоцитопенической пурпуры, с устранением вторичных форм, которые, наряду с лечением пурпурового синдрома, нуждаются в лечении этиологического характера.
У детей и вообще у молодых младше 20 лет, эволюция идиопатической тромбоцитопенической пурпуры, будучи более легкой, геморрагический синдром ограничивается острой фазой, которая продолжается 3—4 недели. Случаи с внутричерепными геморрагиями бывают редко (1—1,5%) и неизвестно, можно или невозможно их предупреждать посредством лечения кортикоидами (McClure). Поэтому, по крайней мере для этой группы больных рекомендуется лишь надзор и покой, до тех пор пока число тромбоцитов начинает повышаться и геморрагии проходят.
Терапия кортикоидами идиопатической тромбоцитопенической пурпуры была эскпериментирована долгое время. На больших группах больных, которым не применялось лечение преднисоном, в 85% случаев эволюция была хорошей, а у леченных предни-соном эволюция оказалась подобной первой, без статистической разницы между группами (Choi и McClure, McClure).
Если пурпура затягивается, как это часто бывает у взрослого, назначается кортикотерапия в вариабильных дозах. Высокие дозы — 1,5—2 мг/кг веса тела показаны только в устойчивых на малые дозы случаях, когда тромбоциты составляют менее 20 000. Нельзя забывать, что длительное лечение высокими дозами может снижать медуллярный тромбоцитопоэз (Shulmann). При формах, которых не излечиваются спонтанно на 3—4 недели, но число тромбоцитов варьирует между 25—50 000 и более, следует применять дозы в 0,5—1 мг/кг веса тела, которые следует приостанавливать когда рост тромбоцитов приближается к 100 000. В основном 60% больных отвечают на дозы в 1—1,5 мг/кг веса тела или меньше и лишь 10% нуждаются в более высоких дозах (Baldini).
Согласно McClure у 75% больных тромбоцитопения персистирует после 3 месяцев эволюции, нуждаясь в продолжении кортикотерапии в высоких дозах. У половины из них ремиссии не происходит, так что необходимо прибегать к спленэктомии или к другому лечению.


Эффект кортизона по-видимому имеет скорее симптоматический характер, благоприятствуя устойчивости капилляров и сокращая таким образом эволюцию пурпуры, даже если число тромбоцитов не возрастает в таком же темпе. Однако признано, что тромбоцитарный лизис уменьшается и возрастает число тромбоцитов благодаря действию кортизона, его свойству ингибировать тромбоцитофагию в гепатоспленической макрофаговой системе. Исследования Harrington показали однако, что эффект уменьшается со временем, при этом тромбоцитофагия сокращается, а также и титр антител благодаря иммунодепрессивному, лимфоцитотоксическому действию кортизона. АКТГ, рекомендуемый в некоторых резистентных случаях, повидимому не оказывает лучшего действия ни на одной из фаз при тяжелой эволюции.
Следовательно, кортизоновое лечение имеет ограниченное показание, в молодом возрасте, когда спонтанная ремиссия происходит в большинстве случаев.
У взрослого, особенно после 50-летнего возраста, эволюция острых форм тяжелее, геморрагии более суровые, а риск хроницизации, по некоторым статистикам, составляет 25—35%. В этих случаях необходима кортикотерапия в высоких дозах. Однако следует иметь в виду, что многие из форм у взрослого, с хронической эволюцией, могут возникать по поводу сенсибилизации к медикаментам и меньше в виде первичных форм идиопатической тромбоцитопенической пурпуры.
В хроницизированных формах у взрослого и особенно у женщин пурпура затягивается но становится менее тяжелой. Если пурпура умеренная и только кожная, больные могут вести почти нормальный образ жизни с минимальным числом тромбоцитов, варьирующим между 30 000 и 70 000. Кортикотерапия назначается с целью излечения в случаях с тяжелыми рецидивами, с увеличением доз и с продолжением лечения в течение 2—3 месяцев. Если не достигается излечения, следует рекомендовать спленэктомию. Если последняя представляет некоторый риск или существуют другие патологические состояния ее противопоказывающие, можно сокращать дозы в известных пределах с тем, чтобы сохранять оптимальное число тромбоцитов. Сочетание гормонального лечения у женщины с применением в особенности тестостерона может привести к излечению или к значительному улучшению.


Беременной женщине с идиопатической тромбоцитопенической пурпурой назначается кортикотерапия, особенно в течение последней трети беременности, когда пурпура отягощается. Хронические формы переносятся лучше, в то время как острые формы, возникающие во время беременности, могут быть тяжелыми и нуждаются в высоких дозах кортизона. Все авторы согласны, что идиопатической тромбоцитопенической пурпура, как и кортикотерапия, не отягощает беременность для матери; однако 60% детей рождаются с пурпурой, а из них умирают до 10%.
Вполне вероятно, что лечение кортизоном в последние 3 месяца, благодаря сокращению антител, улучшает пурпуру у новорожденного или даже вообще предотвращает ее появление (Baldini, Schenker и сотр.).
Несмотря на то, что в основном беременность эволюирует нормально, в течение последних трех месяцев все-таки происходят внутриматочные кровотечения с преждевременным отторжением плаценты и преждевременными родами. В тех случаях, на которые кортикотерапия не повлияла, следует производить трансфузии тромбоцитов до тех пор пока не прекратится геморрагия постпартум.
В лечении идиопатической тромбоцитопенической пурпуры трансфузия тромбоцитов необходима лишь при серьезных геморрагических осложнениях и особенно при внутричерепных геморрагиях. Не известно, в какой мере на их эволюцию и на предупреждение, при сильном сокращении тромбоцитов, оказывают влияние очень высокие дозы кортизона и трансфузии тромбоцитов. Известно, что при острой форме, в которой происходят геморрагии, жизнь трансфузированных тромбоцитов продолжается лишь несколько часов, так что их эффект весьма мимолетный.
Трансфузии тромбоцитов могут давать хороший эффект при хронических формах, устойчивых к кортикотерапии, и когда больных надо подготовить к спленэктомии.
Количество трансфузированных тромбоцитов надо рассчитать в зависимости от числа имеющихся у больного тромбоцитов в момент перфузии, с целью получения нарастания до 30—50 000 тромбоцитов. Для этого рекомендуются концентрированные свежие тромбоциты, взятые из 2—6 единиц крови. Практически, это рекомендуется только для спленэктомии за 1—2 часа до вмешательства. Жизнеспособность и гемостатический эффект сохраняются только для тромбоцитов, взятых самое большее за 24 часа до использования (Baldini и сотр.). Использование тромбоцитов, сохраняемых после замораживания, пока еще изучается и вполне вероятно, что оно сможет дать хорошие результаты (Iercan и сотр.).
Спленэктомия считается специфической терапией при идиопатической тромбоцитопенической пурпуре наряду с кортикотерапией и иммуносупрессией; она является как бы интермедиарным методом между первыми двумя. Если показание целесообразно, результаты спленэктомии хорошие в 80—90% случаев, но существуют значительные вариации в разных группах больных, находившихся под наблюдением за прошлые 25 лет (Dameshek и сотр., Gardner). Повидимому высокий процент хороших результатов — до 85% — (McGlure) получается за счет спленэктомий у детей при острых формах, но вполне вероятно, что можно было получать излечения и с помощью долговременной кортикотерапии; у взрослого, с преобладанием хронических форм, хорошие результаты за последние годы не превышают 65%, то есть как это было 30 лет тому назад (Harrington). Впрочем, даже у детей при хронических формах, по другим статистикам, излечения не превышали 60% (Chioi и McGlure). У взрослых старше 50 лет, ремиссия после спленэктомий не превышает 50% случаев (Aster).
Наш опыт на более чем 20 случаев идиопатической тромбоцитопенической пурпуры показал, что правильно показанная спленэктомия дает полные или частичные ремиссии в 85% случаев (Butoianu и сотр.). Несомненно хорошие результаты получаются у больных, отвечающих на кортизон, но зависимых от этого медикамента, так что существует показание спленэктомии.

Согласно собственному опыту и из литературы вытекает, что спленэктомия показана при формах с рецидивами или при хронических формах, устойчивых к лечению кортизоном в высоких дозах — 1,5—2 мг/кг веса гела, в течение 3—6 месяцев. Неизбежное вмешательство можно производить под защитой высокими дозами кортизона в тот момент когда число тромбоцитов составляет 20—25 000; в случаях с висцеральными кровотечениями, увеличиваются дозы кортизона и производится перфузия тромбоцитов за 1—2 часа до вмешательства; перфузия повторяется после вмешательства если не получилось быстрого и немедленного нарастания. При хорошей дооперационной подготовке смертность не превышает 1% оперированных больных.
Как мы уже указывали, возможно предвидеть хороший эффект спленэктомии в случаях с максимальной секвестрацией в селезенке, хотя существуют показания и противоположных результатов: максимальная секвестрация в печени и все-таки хорошие эффекты после спленэктомий (Najean и сотр.). Изъятие селезенки имеет и эффект биологической иммуносуппрессии, так как устраняется главный очаг производства автоагглютининов. Не подтверждается однако соотношение между эффектом спленэктомии и титром антител. Во всяком случае интенсивность секвестрации в печени или селезенке не является более важным критерием для показания спленэктомий (Aster и Кеепа, Baldini, Najean и Ardailan).
Один из критериев предсказания результатов спленэктомий — немедленный ответ после спленэктомий. Если в течение 1—3 дней тромбоциты достигают высоких цифр, более 500 000, они сохранятся в дальнейшем в нормальных пределах, с клиническими излечениями в 84% случаев (Orringer, Najean и Ardailan). Если нарастание достигает лишь 100—200 000, получаются излечения только в 25% случаев, а у 85% тромбоциты спадают спустя несколько недель до прежних цифр и возобновляются пурпуровые явления. Патогенетическая гипотеза, согласно которой спленэктомия удаляет максимальный очаг секвестрации (Shulmann и сотр., Aster и Keena, Najean и Ardailan) и производства антител (McMillan и сотр., Karpatkin и сотр.) не подтверждается благодаря непостоянным результатам спленэктомии.
Антитела исчезают в некоторых исследованных случаях, но часто они персистируют и тромбоциты остаются пониженными, а в некоторых случаях повышаются до нормальных цифр (Berceanu и сотр.). Несмотря на это, опыт показал, что больные, которые не ремиттируются полностью после спленэктомии нуждаются в более низких дозах кортизона и цитостатических медикаментов. В некоторых исследованных нами случаях кортикотерапия непрерывно примененная в случае неудачи после спленэктомии привела к ряду окончательныу излечений. Однако неизвестно если эти излечения не произошли бы и без спленэктомии.
Показания терапии с иммуносуппрессивными медикаментами должны делаться только в случаях крайней необходимости, лишь в тех случаях, когда спленэктомия не дала результатов и когда персистирует эволюция тяжелой хронической формы. Как указывалось ранее, кортикотерапия при идиопатической тромбоцитопенической пурпуре имеет иммуносупрессивный эффект лишь вторично и неопределенно, не контролируя автоиммунный процесс, что создает необходимость использовать другие медикаменты твердо доказанного иммуносуппрессивного действия. До сих пор использовался главным образом имуран (азотиоприн), который давал результаты в 65% случаев хронических форм у взрослого, но и у ребенка (Goebel и сотр.).
Согласно другим, хорошие результаты не превышают 20—30% случаев устойчивых к кортикотерапии или к спленэктомии, где показание иммуносуппрессии является первостепенным.
Использовались и другие медикаменты с антиметаболическим действием, как 6-метил-пурин, тиогуанин, имеющие близкое к имурану фармакодинамическое действие. Используемые дозы известны, соответственно 2,5—3 мг/кг веса тела для 6 MP и имурана и несколько меньше, 2 мг/кг веса тела для тиогуанина.
Попытки лечения эндоксаном, обычно перорально, 50—100 мг, дают приблизительно такие же результаты или лучшие (Finch и сотр.), но с более значительными вторичными токсическими эффектами. Как и при любой иммуносуппрессивной терапии, лечение должно продолжаться несколько месяцев и прекращаться, когда тромбоциты приближаются к нормальной цифре.
В некоторых кортикозависящих случаях, применение иммуносуппрессивного медикамента ведет к уменьшению дозы кортизона у больных, леченных долгое время этим медикаментом и проявляющих явные признаки терапевтического гиперкортицизма.
Не существует обширного опыта в связи с использованием актиномицина С, который на небольшом числе случаев, повидимому дал спектакулярные результаты (Baldini). Однако очень важные вторичные токсические эффекты ограничивают показание этого медикамента (Martin и сотр.).
За последнее время в терапию резистентных форм идиопатической тромбоцитопенической пурпуры проникли производные Vinca rosea, винбластин и в особенности винкристин (Marmont и сотр., Harrington). Они применяются в несколько меньших дозах, чем при злокачественных заболеваниях, а именно 1/20 мг/кг веса тела винбластина и 0,5 мг/м2 винкристина через каждые 2 или даже 3—4 недели. В некоторых случаях с длительной резистентностью к другим методам, были получены полные или даже частичные ремиссии, с сокращением тромбоцитов и полным исчезновением клинических признаков пурпуры. Если после 2—3 инъекций не появляются признаки ремиссии следует отказаться от этих медикаментов. Фармакодинамическое действие, детерминирующее рост тромбоцитов является темой дискуссий. Вполне вероятно, что оба медикамента имеют иммуносуппрессивный эффект, но винкристин поводимому оказывает добавочно стимулирующий эффект на центральный тромбоцитопоэз.
Имея в виду хорошие результаты, полученные нами и в случаях дисглобулинемических пурпур, следует признать иммуносушгрессивный эффект, влияющий на воспалительные поражения сосудистой стенки.
Согласно некоторым более новым данным (Finch и сотр.), наилучшие результаты получаются в хронических случаях, эволюция которых продолжается более 4 месяцев; но если до 8 месяцев еще возможно получать хорошие результаты, после 12 месяцев результаты редко бывают хорошими или посредственными, а после 18 месяцев отмечаются в основном только неудачи.
Недавно в Бухарестской Клинике Гематологии была сделана попытка прицельной иммуносуппрессии, с целью уничтожения макрофаго в посредством тромбоцитов загруженных in vitro Винкристином или Винбластином. В случаях где применялся этот метод были получены явные но мимолетные результаты, причем в хронических формах снова возникали рецидивы.
Кроме этих трех главных методов лечения, которые под правильной последовательностью и правильным применением дают эффективные результаты в большинстве форм идиопатической тромбоцитопенической пурпуры, в некоторых случаях, устойчивых ко всем этим методам, делались попытки других лечений, которые были затем отвергнуты. Так например, лечение гепарином или дикумаролом (Cohen) принятое в силу гипотезы, что оно убавляет эффект реакций антиген-антитело, особенно благодаря антикомплементарному действию гемарина, было отвергнуто тем более, что известны случаи тромбоцитопений после гепаринотерапии (Natelson и сотр., Fratantoni и сотр.); антикоагулирующая терапия может давать кое-какие эффекты в тех случаях, когда возникает и процесс диссеминированной внутрисосудистой тромбоцитопенизирующей коагуляции.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021

Гематологические осложнения часто наблюдаются при системной красной волчанке (СКВ). Сюда входят гемолитическая анемия с ретикулоцитозом, лейкопения (
Анемия, лейкопения и тромбоцитопения могут возникать в результате недостаточности костного мозга или чрезмерного разрушения периферических клеток, оба из которых могут быть иммуноопосредованными. Другие частые причины - наркотики , включая психотропные препараты, и инфекция. Несмотря на то, что многим пациентам не требуется специфического лечения цитопении при системной красной волчанке , CS остаются основой лечения. Другие традиционные методы лечения включают AZA, CYC и нормальный иммуноглобулин человека. Совсем недавно MMF стал играть роль агента, сохраняющего CS и CYC.
Лейкопения
Нейтропения
Нейтропения также является частым признаком СКВ с распространенностью порядка 47%, и это может быть опосредовано антинейтрофильными антителами. Нарушение функции мононуклеарной фагоцитарной системы, позволяющей сенсибилизированным клеткам оставаться в кровотоке, может частично компенсировать это. Уровни G-CSF обычно повышены у пациентов с СКВ с нейтропенией. Это может отражать сниженную чувствительность миелоидных клеток к G-CSF или присутствие антител против G-CSF иммуноглобулина G (IgG) и иммуноглобулина M (IgM). Увеличение сывороточного TNF-связанного лиганда, индуцирующего апоптоз при СКВ, также может способствовать нейтропении из-за чрезмерного апоптоза нейтрофилов.
Хотя аутоиммунитет является наиболее вероятным объяснением нейтропении при СКВ, другие патологии, такие как миелофиброз, также могут иногда иметь значение. Как и лимфопения, нейтропения в легкой форме часто не имеет клинических последствий, но иногда может быть связана с опасным для жизни сепсисом . Нейтропения при СКВ также часто связана с приемом лекарств и, в отличие от тромбоцитопении, не связана с повышенной смертностью.
Тромбоцитопения
Сообщается, что тромбоцитопения имеет распространенность от 7 до 30% в большой группе пациентов с СКВ. Повышенная периферическая деструкция тромбоцитов, связанная с наличием антитромбоцитарных антител, является наиболее вероятным патогенетическим механизмом. Также могут быть задействованы aPL, наряду с антителами против тромбопоэтина (TPO) , рецептора TPO c-Mpl и CD40L. Также сообщалось о повышенных уровнях TPO. Тромбоцитопения при СКВ может быть острой в начале и чрезвычайно тяжелой. Это проявление обычно связано с активным заболеванием в других системах органов и, как правило, реагирует на CS. Также распространена более хроническая форма, менее связанная с активностью заболевания, и обычно менее поддается лечению CS. Иммунная тромбоцитопения может предшествовать СКВ у 16% пациентов, появляясь за 10 лет до того, как СКВ становится клинически очевидной.
В дополнение к терапии высокими дозами кортикостероидов (CS), тромбоцитопения является независимым фактором риска повышенной смертности при СКВ. ретроспективном исследовании 126 пациентов с СКВ поздняя тромбоцитопения была связана с повышенной смертностью. Не было обнаружено связи с aPL, и увеличение смертности не было связано с тромбоэмболическими событиями. Более недавнее ретроспективное исследование 632 пациентов выявило особенно высокую распространенность тромбоцитопении, которая присутствовала у 58% на момент постановки диагноза [ 38 ]. Была очевидна связь с активностью заболевания, повышенной смертностью и гипокомплементемией.
Тромбоцитопения может также возникать в других контекстах при СКВ, например, как осложнение лекарственной терапии, например, иммунодепрессантами, такими как АЗА и редко HCQ. Тромботическая тромбоцитопеническая пурпура (ТТП) также хорошо известна, но, к счастью, встречается редко. Сообщается также о тромботической микроангиопатической гемолитической анемии в сочетании с СКВ [ 41 ], характеризующейся тромбоцитопенией, микроангиопатической гемолитической анемией, лихорадкой, неврологическими симптомами и поражением почек.
Тромбоцитопения и анемия
Тромбоцитопения при СКВ часто связана с гемолитической анемией, наличием других цитопений и aPLs. Хотя может наблюдаться связь между антителами к дцДНК и гемолитической анемией, эта связь не очевидна в случаях тромбоцитопении.
Оценка причин цитопении при системной красной волчанке
Подробная история приема лекарств при лечении системной красной волчанки очень важна. При этом следует учитывать как препараты, назначаемые непосредственно для лечения этого патологического состояния, так и препараты для лечения его осложнений, такие как статины, антибиотики и ингибиторы АПФ. Лейкопения и тромбоцитопения могут осложнять лечение СКВ с помощью AZA, MTX и, реже, CSA, MMF или HCQ. Нейтропения может следовать за импульсным CYC, с надиром, обычно возникающим на 10-й день после инфузии, что частично зависит от дозы.
Выявление морфологии лимфоцитов может быть диагностикой конкретных лимфопролиферативных заболеваний. Сопутствующая анемия требует анализа крови, количества ретикулоцитов и прямого теста Кумба. Другие соответствующие исследования включают лактатдегидрогеназу (ЛДГ) в сыворотке крови, функциональные тесты печени, иммуноглобулины и электрофорез белков сыворотки. Исследования перестройки гена периферической крови (гена тяжелой цепи иммуноглобулина или перестройки гена рецептора Т-клеток) следует рассматривать, если есть высокий индекс подозрения на лимфопролиферативное заболевание.
Измерение антитромбоцитов и других антител в рутинной клинической практике является более спорным. Доступен ряд анализов для измерения антител к тромбоцитам, в основном направленных против гликопротеинов IIb / IIIa и Ib / IX. Из-за их стоимости, ограниченной доступности и времени, необходимого для получения результата, измерение антител к тромбоцитам с использованием таких методов, вероятно, не является необходимым. Однако их использование следует рассматривать в случаях тяжелой тромбоцитопении, особенно если они не поддаются лечению. Есть некоторые свидетельства того, что их уровень может коррелировать с активностью заболевания. Когда уровень тромбоцитов нормализуется у пролеченных пациентов, антитела к тромбоцитам могут значительно снизиться или стать неопределяемыми . Однако отсутствие антитромбоцитарных антител не исключает аутоиммунную этиологию тромбоцитопении у отдельного пациента с СКВ.\
IgG и IgM антинейтрофильные и антилимфоцитарные антитела также могут быть измерены с помощью IIF с использованием проточной цитометрии. Это определит клеточную специфичность и класс иммуноглобулинов антитела. Специфичность антител против лимфоцитов может быть дополнительно исследована с помощью ELISA на антитела HLA класса I. Тест хемилюминесценции нейтрофилов также используется некоторыми лабораториями. Он измеряет ответ человеческих моноцитов на опсонизированные антителами нейтрофилы пациента, положительный результат подтверждает наличие антител, реагирующих с нейтрофилами. Ограничения анализов, используемых для измерения антинейтрофильных антител у пациентов с нейтропенией, недавно были пересмотрены. APL также могут быть связаны с тромбоцитопенией и гемолитической анемией и обычно измеряются в большинстве лабораторий. Другие антитела, которые могут иметь патогенетическое значение при цитопении, связанной с волчанкой, например, против G-CSF и рецептора TPO , обычно не измеряются.
Исследование костного мозга
Аспирацию костного мозга (КМ) и трепан следует рассматривать во всех случаях тяжелой или стойкой лейкопении или тромбоцитопении у пациентов с СКВ. Точно так же обследование костного мозга важно в случаях панцитопении, особенно если пациент получает миелотоксическую терапию, такую как AZA, MMF или CYC. В костном мозге могут присутствовать специфические признаки, указывающие на миелотоксичность, вызванную лекарственными средствами. Например, AZA может вызывать апластическую анемию, гипоплазию эритроидов и мегалобластные изменения. Исследование BM также может выявить злокачественные гематологические заболевания и гемофагоцитоз. Посев на BM показан при лихорадке неизвестного происхождения у пациентов с подавленным иммунитетом и СКВ. Общие аномалии костного мозга у пациентов с СКВ включают увеличение предшественников гемопоэза, что свидетельствует о периферической деструкции или, альтернативно, гипоцеллюлярности, вызванной СКВ. Некроз BM с изменениями стромы также является частым. У пациентов с тромбоцитопенией может наблюдаться ряд аномалий мегакариоцитов. Эти клетки могут быть сгруппированными, гиполобулированными и пикнотическими и могут иметь оголенную цитоплазму.. Это подтверждает гипотезу о том, что костный мозг может быть органом-мишенью при болезни и что нормальные механизмы клиренса дефектны и / или подавлены при СКВ
Лечение цитопении при системной красной волчанке
Лейкопения и тромбоцитопения при СКВ часто протекают в легкой форме и не требуют специальной лекарственной терапии.
Кортикостероиды
Азатиоприн и др.
АZA традиционно используется в качестве стероидсберегающего средства при лечении тромбоцитопении при СКВ. Однако рандомизированных контролируемых испытаний его использования в этом контексте не проводилось. CSA является альтернативным иммунодепрессивным препаратом при лечении цитопении, связанной с волчанкой. В открытом исследовании с участием 16 пациентов с СКВ уровни тромбоцитов и лейкоцитов вернулись к норме у пациентов с тромбоцитопенией или лейкопенией, получавших CSA 3-5 мг / кг / день в течение среднего периода лечения 30 месяцев. Однако не рекомендуют использовать эти дозы из-за риска нефротоксичности и предпочитаем дозы до 2,5 мг / кг / день с тщательным контролем функции почек и артериального давления. . Кроме того, другие рекомендовали использовать еще более низкие дозы. Недавно сообщалось о его успехе в качестве стероидсберегающего средства при тромбоцитопении, связанной с волчанкой, с минимальными побочными эффектами . Несмотря на это, ассоциация гипертонии и почечных осложнений с циклоспорином предполагает, что его следует использовать с осторожностью и тщательно наблюдать за пациентами. Комбинация преднизолона и HCQ может быть адекватной альтернативой для контроля тромбоцитопении у многих пациентов.
Спленэктомия
Если лечение тромбоцитопении преднизолоном или стероидсберегающими препаратами оказалось безуспешным, следует рассмотреть возможность спленэктомии. Ответ на спленэктомию при тромбоцитопении, связанной с волчанкой, обычно благоприятен. Учитывая важную роль селезенки в клиренсе иммунных комплексов, после спленэктомии при СКВ предполагался риск обострения активности заболевания, но на практике это обычно не подтверждается .Важность соответствующих профилактических мер против инфицирования после спленэктомии при СКВ невозможно переоценить. Это включает использование вакцин против пневмококка, гемофильного гриппа типа B, менингита C и гриппа, а также профилактических антибиотиков, таких как пенициллин V, особенно у пациентов с дополнительной хронической гипокомплементемией. Пневмококковая вакцинация может потребоваться повторить через 5 л
Иммуноглобулинемия G
IVIG может быть очень эффективным у некоторых пациентов с тромбоцитопенией, связанной с волчанкой. Кроме того, при иммунной тромбоцитопении , IVIG может как блокировать активирующие, так и повышать ингибирующие рецепторы Fcγ. Даназол - еще один вариант специфического лечения тромбоцитопении при СКВ. Как правило, это безопасно и хорошо переносится, и в этом контексте можно применять IVIG в отличие от даназола во время беременности. Терапевтическая доза IVIG при тяжелой тромбоцитопении, осложняющей СКВ, составляет 2 г / кг, обычно вводимая пятью последовательными ежедневными дозами по 400 мг / кг. Также сообщалось о поддержании ремиссии с помощью повторных доз IVIG при тяжелой тромбоцитопении, осложняющей СКВ.
Механизм действия IVIG при системной красной волчанке , вероятно. мультмодален и включает в себя: понижающую регуляцию продукции аутоантител нейтрализацию патогенных аутоантител, антиидиопатическими антителами , ингибирование комплемент - опосредованного повреждения модулояцию продукции цитокинов , индукцию апоптоза лимфоцитов и моноцитов , модуляцию функции В - и Т - лимфоцитов.
Рефрактерные цитопении
Лечение тяжелой цитопении и апластической анемии при СКВ может потребовать лечения более сильными цитотоксическими средствами, включая CYC. Терапия CYC (назначается из расчета 0,75–1,0 г / м 2 площади поверхности тела или 10–15 мг / кг), вводимая внутривенно каждый месяц в течение не менее 4 месяцев, оказывается полезной при лечении тяжелой тромбоцитопении, связанной с волчанкой, не поддающейся стандартным методам лечения . Более низкие дозы, применяемые чаще, например, каждые 2 недели, все чаще используются в некоторых учреждениях для улучшения переносимости без потери эффективности. Сбалансировать риски и преимущества такой терапии может быть сложно, особенно при наличии тяжелой нейтропении. Однако сообщалось об успешном использовании высоких доз CYC в / в при лечении апластической анемии, осложняющей СКВ. Анализ BM перед терапией особенно полезен в этой ситуации, поскольку повышенное количество предшественников эритроцитов или лейкоцитов в костном мозге предполагает, что ответ на терапию более вероятен. Кроме того, одновременное использование рекомбинантного человеческого G-CSF (rhG-CSF) и антибиотиков снижает риск этой формы подхода.
MMF
Иммуноаблативная доза CYC и трансплантация стволовых клеток
ечение тяжелых и особенно рефрактерных аутоиммунных заболеваний было несколько улучшено за счет введения интенсивной иммуноаблативной иммуносупрессии с использованием трех различных подходов. Это аллогенная трансплантация гемопоэтических стволовых клеток (HSCT), аутологичная HSCT (с использованием костного мозга или периферической крови) и иммуноаблативная иммуносупрессия высокими дозами без поддержки стволовых клеток. Испытания при СКВ, включая пациентов с тяжелыми гематологическими проявлениями, и при других аутоиммунных заболеваниях показывают, что иммуносупрессивная терапия высокими дозами с поддержкой аутологичных гематопоэтических стволовых клеток или без нее может вызвать ремиссию ранее резистентного заболевания
Таким образом, альтернативным подходом является использование высоких доз CYC без трансплантации стволовых клеток. Это успешно применялось при апластической анемии и других аутоиммунных заболеваниях, включая СКВ
Анти-В-клеточная терапия
Центральная роль В-клеток в патогенезе СКВ дает основание для использования моноклонального антитела против CD20 ритуксимаба в его лечении. CD20 экспрессируется на промежуточных стадиях развития В-клеток, но теряется на терминальных стадиях и отсутствует в плазматических клетках. Ритуксимаб представляет собой химерное моноклональное антитело против CD20 человека, которое быстро истощает CD20-положительные В-клетки периферической крови за счет опосредованной комплементом и антителозависимой клеточной цитотоксичности. Хотя изначально ритуксимаб использовался для лечения рецидивов В-клеточной фолликулярной неходжкинской лимфомы низкой степени злокачественности, впоследствии он успешно применялся при лечении хронической иммунной тромоцитопении. Было показано, что у пациентов с СКВ ритуксимаб истощает популяции аутореактивных В-клеток и снижает продукцию аутоантител плазматическими клетками. При введении с использованием протокола повышения дозы от разовой дозы 100 мг / м 2 до четырех еженедельных доз 375 мг / м 2ритуксимаб приводил к истощению В-клеток, что коррелировало со снижением проявлений заболевания. Ритуксимаб также успешно применялся при лечении аутоиммунной гемолитической анемии, осложняющей СКВ.
Альтернативный подход включает аутореактивный стимулятор B-лимфоцитов фактора выживания B-клеток (BLyS). BLys - цитокин, связанный с TNF, может быть нацелен несколькими способами, например, через рецепторы-ловушки и моноклональные антитела против BLyS. LymphoStat-B (белимумаб) - полностью человеческое моноклональное антитело, которое связывается с BLyS с высокой аффинностью и нейтрализует биоактивность BLyS человека in vitro и in vivo. У пациентов, получавших белимумаб, наблюдалось более длительное время до обострения болезни по сравнению с плацебо, и наблюдалось снижение титров анти-дцДНК. В анализе подгрупп пациенты с серологически активным заболеванием значительно лучше ответили на терапию белимумабом. Хотя его влияние на цитопении при СКВ еще не известно, оно может представлять собой дополнительный терапевтический подход к их лечению. Abetimus (LJP 394), который индуцирует толерантность В-клеток к антителам против дцДНК, до сих пор исследовался только для предотвращения почечных обострений при волчанке.
Даназол
Ингибитор продукции гонадотропных гормонов. Вызывает обратимое подавление продукции ЛГ и ФСГ гипофизом у мужчин и женщин. Не обладает эстрогенной и гестагенной активностью. Обладает слабой андрогенной активностью с сопутствующим анаболическим эффектом. Подавляет пролиферацию и вызывает атрофию нормальной и эктопической ткани эндометрия. Уменьшает потерю менструальной крови, механизм данного действия окончательно не установлен. Ингибирует овуляцию и уменьшает уровень 17β-эстрадиола в плазме крови. Остается неясным, является ли ингибирование пролиферации эндометрия следствием уменьшения уровня эстрадиола или прямого влияния даназола на эстрогеновые рецепторы эндометрия. После отмены даназола овуляция обычно возобновляется в течение 5 недель, что сопровождается характерным резким повышением ЛГ и небольшим повышением ФСГ. Стандартны показания к назначению даназола : эндометриоз с сопутствующим бесплодием, доброкачественные новообразования молочной железы (фиброзно-кистозная мастопатия), первичные меноррагии, предменструальный синдром, гинекомастия; наследственный ангионевротический отек. Противопоказания : тяжелые нарушения функции печени и/или почек, хроническая сердечная недостаточность, порфирия, тромбоэмболические нарушения (в т.ч. в анамнезе), андрогенозависимые опухоли, вагинальное кровотечение неясного генеза, рак молочной железы, карцинома, беременность, период лактации, повышенная чувствительность к даназолу. Не рекомендуется применять даназол у детей и у лиц с заболеванием почек.
Новаторские подходы
Элтромбопаг - это агонист рецепторов тромбопоэтина на поздних стадиях развития для лечения тромбоцитопении. Недавно были опубликованы испытания фазы II, изучающие его роль в иммунной тромбоцитопении и в тромбоцитопении, связанной с инфекцией гепатита С. В исследовании ITP элтромбопаг вводили перорально в дозе 30, 50 или 75 мг в день 118 пациентам с количеством тромбоцитов 50 × 10 9 / л на 43-й день. Это было достигнуто в 28, 70 и 81% в трех группах дозировки элтромбопага, соответственно, по сравнению с 11% в группе плацебо. Среднее количество тромбоцитов на 43-й день составляло 26 × 10 9 / л, 126 × 10 9./ л, 183 × 10 9 / л и 16 × 10 9 / л соответственно.
Ромиплостим (AMG 531) - еще один агонист рецепторов ТПО, который в настоящее время лицензирован для лечения хронической рефрактерной иммунной тромбоцитопении. Он состоит из компонента Fc IgG 1, связанного с пептидным доменом с четырьмя сайтами связывания для Mpl, рецептора ТРО. В отличие от рекомбинантного фактора роста и развития мегакариоцитов первого поколения, ромиплостин не имеет гомологии последовательности с ТПО, следовательно, существует меньший риск выработки антител против эндогенного ТПО. Он имеет высокое сродство к рецептору ТПО и увеличивает дифференцировку мегакариоцитов. Его вводят в виде еженедельных подкожных инъекций, и ответ зависит от дозы, достигая пика на 12-15 дни
Тромбоцитопеническая пурпура после вирусных инфекций - клиника, диагностика
Эпидемиологическая анкета и специальные исследования показывают, что у детей младше 8 лет, вирусные инфекции предшествуют тромбоцитопенической пурпуре в 85% случаев и лишь 15% являются очевидно идиопатическими.
Болезнь наступает внезапно, обычно спустя 1—3 недель после вирусной инфекции, особенно дыхательных путей; бывают случаи, когда период после инфекции и до появления пурпуры продолжительнее — до 4 месяцев. Согласно McClure, вирусную этиологию можно установить по меньшей мере в 50% случаев из 413 исследованных детей.
Пурпура появилась спустя 3—6 недель, с одинаковой частотой у мальчиков и девочек, в то время как у взрослого преобладают женщины в пропорции 2/1 или даже 3/1.
Вирусная этиология была наглядно доказана у детей с тромбоцитопенической пурпурой, родившихся с краснухой (Luscher и сотр., Wallace, Svenigsen, Zinkham и сотр.), при которой обнаруживаются антивирусные антитела после состояния виремии.
Вполне возможно, что механизм тромбоцитопении происходит по поводу поражений типа III, благодаря иммунным комплексам, но не по поводу антитромбоцитарных антител. Виремия, как и при других вирусных инфекциях, находится лишь на 7 дней раньше и два дня после вирусного высыпания, следовательно задольго до пурпурного высыпания.
Вирусная этиология определяется после некоторых вирусных инфекций, проявляющих максимальную частоту в холодные времена года или в начале весны, как например различные высыпные лихорадки, корь, ветряная оспа, оспа, а также и инфекции с Pertussis. Бывают случаи и после инфекционных мононуклеозов, а также и после вирусных герпесов, инфекций с цитомегаловирусом, свинкой и даже после гепатита Боткина.
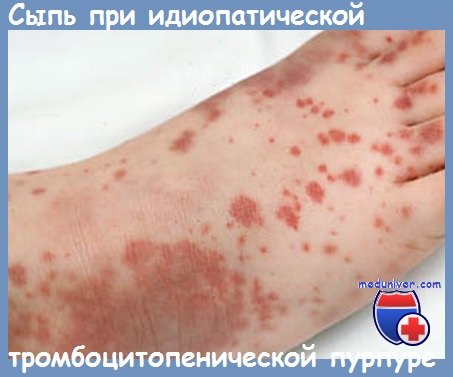
Вирусная этиология была доказана несомненно при тромбоцитопенической пурпуре после противокоревой или противооспенной вакцинации, но только в редких случаях (Alter и сотр., Oski и сотр., Bachand и сотр.). Реже можно ссылаться на иммунную этнологию после бактериальных инфекций (Clement и Diamond) или после интрадермореакций на туберкулин.
Следует обращать особое внимание на тромбоцитопеническую пурпуру, появляющиеся в разгаре септического состояния, микробного или вирусного, при котором механизм тромбоцитопении иной. В этих случаях микробные токсины, как при стрептококковых, пневмококковых, менингококковых инфекциях, а также и вследствие других граммотрицательных агентов, детерминируют появление во время септического периода синдрома с вторичной тромбоцитопенией путем явления Sanarelli-Schwartzmann.
Микробные токсины, но особенно вирусные частицы, могут прямо вызывать агглютинацию тромбоцитов и тяжелый прогрессивный синдром по поводу уничтожения тромбоцитов на уровне РЭС. Это тромбоцитопени-ческие расстройства по поводу снижения тромбоцитов на периферии, к которому добавляется однако и дефицит производства благодаря прямому поражению мегакариоцитов, которые являются очень благоприятной средой для размножения вирусов (Dalton и сотр.).
В разгаре вирусной инфекции или после вакцинации число мегакариоцитов понижается, они представляют дефекты созревания и дегенеративные поражения с вакуолями и многочисленными свободными ядрами, в то время как число тромбоцитов снижается. При тяжелых тромбоцитопениях констатируется признак разрушения тромбоцитов с повышением в сыворотке кислотных фосфатаз.
Подобные механизмы с периферическим лизисом возникают и при других инфекциях, как например лихорадка денга, токсоплазмоз, а также и при таиландской геморрагической лихорадке, вызв шной вирусом миэлодепрессивного действия (Bierman и Nelson). Эти данные смешанного патогенеза необходимы для диагностицирования известных вторичных форм путем изучения непосредственного действия инфекционных агентов, таких как вирусные агенты, антитела, иммунные комплексы, а также тромбоцитарного турновера и функций мегакариоцитов.
С клинической точки зрения, поствирусные формы у детей имеют в основном характер идиопатической тромбоцитопенической пурпуры. В обширной статистике, McClure находит, наряду с пурпурой у всех больных, эпистаксис у 30%, гематурию у 5— 10% и органиченную частоту для других кроворечений, как например гемоторакс. Внутричерепные кровоизлияния, хотя и редкие (1,2%), являются причиной смерти у 30% исследованных больных в период пурпуры.
Спленомегалии и иногда умеренные гепатомегалии появляются в 10% случаев и детерминированы скорее вирусной инфекцией, чем тромбоцитопеническим заболеванием.
С точки зрения эволюции, 50% случаев излечиваются после острого приступа за 1—2 и реже 3 месяца. В пропорции 10—20% случаев, тромбоцитопения с вариабильными значениями, с явлениями легкой или акцентуированной пурпуры персистирует от одного до нескольких лет.
У 8—10% случаев, после периода излечения, пурпура рецидивирует или принимает стойкий хронический характер, с акцентуированными приступами, детерминированными вероятно реинфекциями, которые усугубляют процесс самопродолжения путем генерирования новых иммунных комплексов или даже путем появления автоиммунного механизма после разрыва толерантности.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Тромбоцитопении у детей: причины, диагностика, лечение
Тромбоцитопения — состояние, при котором количество тромбоцитов ниже 150х109/л. Риск кровотечений зависит от количества тромбоцитов.
• Тяжёлая тромбоцитопения (количество тромбоцитов • Умеренная тромбоцитопения (количество тромбоцитов 20-50х109/л) — риск избыточного кровотечения во время операций или при травме, но невысокий риск спонтанных кровотечений.
• Лёгкая тромбоцитопения (количество тромбоцитов 50-150х109/л) — низкий риск кровотечения во время операций или при травме. Тромбоцитопения может приводить к формированию кровоподтёков, петехиям, пурпуре и кровотечениям из слизистых (например, носовым, из дёсен при чистке зубов). Обширное кровотечение в форме тяжёлого желудочно-кишечного кровотечения, гематурии и внутричерепного кровоизлияния встречается намного реже.
Хотя пурпура может обозначать тромбоцитопению, она также происходит при нормальном количестве тромбоцитов вследствие дисфункции тромбоцитов и сосудистых нарушений.
Иммунная тромбоцитопения
Иммунная тромбоцитопения (также называемая тромбоцитопенической пурпурой) — наиболее распространённая причина тромбоцитопении в детском возрасте. Распространенность её составляет около 4 на 100 000 детей в год.
Она возникает в результате иммуноопосредованной деструкции циркулирующих тромбоцитов под действием антитромбоцитарных антител. Снижение количества тромбоцитов сопровождается компенсаторным увеличением мегакариоцитов в костном мозге.
Клинические признаки иммунной тромбоцитопении у детей
У большинства детей клинические признаки появляются в возрасте между 2 и 10 годами, часто с началом заболевания спустя 1-2 нед после перенесённой вирусной инфекции. Анамнез обычно короткий, занимает дни или недели. У поражённых детей развиваются петехии, пурпура и поверхностные кровоподтёки. Также могут развиться носовое и другие кровотечения из слизистых, однако профузные кровотечения нетипичны, несмотря на тот факт, что количество тромбоцитов обычно снижается до 10х109/л.
Внутричерепные кровоизлияния — серьёзные, но редкие осложнения, происходят в 0,1-0,5% случаев в основном у тех, у кого тяжёлая тромбоцитопения присутствует в течение длительного периода.
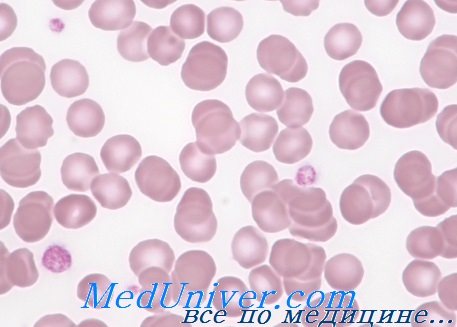
Диагностика иммунной тромбоцитопении у детей
Иммунная тромбоцитопения — диагноз исключения, поэтому необходимо уделить большое внимание анамнезу, клиническим особенностям и мазку крови для того, чтобы быть уверенным, что ни один более тяжёлый диагноз не был пропущен. У детей младшего возраста необходимо предположить врождённые причины (такие как синдромы Вискотта-Олдрича или Бер-нара-Сулье). Любые атипичные клинические проявления, как, например, наличие гепатоспленоме-галии или выраженной лимфаденопатии, требуют немедленного исследования костного мозга для исключения острой лейкемии или апластической анемии.
Необходимо провести исследование костного мозга, если планируется лечение ребёнка глюкокортикоидами, поскольку эта терапия может временно маскировать эти заболевания. Также необходимо предположить СКВ. Однако если имеются характерные клинические симптомы при отсутствии изменений в крови, за исключением низкого количества тромбоцитов, и нет намерения проводить лечение, то исследование костного мозга не требуется.
При иммунной тромбоцитопении, за исключением выразительных кожых проявлений и значительно сниженного количества тромбоцитов, состояние хорошее и у большинства пациентов происходит быстрая ремиссия без каких-либо вмешательств.
Ведение детей с иммунной тромбоцитопенией
Приблизительно у 80% детей болезнь протекает остро, доброкачественно и обычно спонтанно разрешается в течение 6-8 нед. Большинству детей помощь может оказываться на дому, госпитализация и не требуется. Подход к лечению противоречивый. Большинству детей не требуется никакая терапия, даже если количество тромбоцитов составляет менее 10х109/л, однако необходимо начать лечение, если есть признаки массивного кровотечения (например, внутричерепного или желудочно-кишечного) или продолжающееся небольшое кровотечение (например, постоянная кровоточивость ротовой полости).
Для лечения используется преднизолон внутрь или иммуноглобулин внутривенно, однако оба они имеют значительные побочные эффекты и не влияют на шанс достижения полной ремиссии. Инфузии иммуноглобулина обычно приводят к более быстрому увеличению числа тромбоцитов, чем глюкокортикоиды. Трансфузии тромбоцитарной массы оставляют для жизнеугрожающих кровотечений, поскольку они поднимают уровень тромбоцитов лишь на несколько часов. Преднизолон должен применяться лишь короткими курсами независимо от числа тромбоцитов. У родителей должен быть свободный 24-часовой доступ в клинику.
Ребёнок должен избегать травм, насколько это возможно, и контактных видов спорта до тех пор, пока сохраняется очень низкое число тромбоцитов.
Хроническая иммунная тромбоцитопения у детей
У 20% детей количество тромбоцитов остаётся низким через 6 мес после установления диагноза, это известно как хроническая иммунная тромбоцитопения у детей. Никакое лечение не проводится до тех пор, пока не произойдет массивное кровотечение. Как и при острой иммунной тромбоцитопении у детей, не должны применяться длительные курсы глюкокортикоидной терапии. Поэтому терапия в основном поддерживающая, ребёнок должен избегать контактных видов спорта, однако должен стимулироваться для продолжения нормальной жизнедеятельности, в том числе посещения школы.
Как и при острой иммунной тромбоцитопении у детей, родителям необходим 24-часовой доступ к медицинской помощи. Семье может пойти на пользу общение с группой поддержки родителей детей, страдающих иммунной тромбоцитопенией. У большинства детей наступает выздоровление в течение 3 лет или стабилизация с сохранением умеренной асимптомной тромбоцитопении. Случаи профузных кровотечений являются редкими и требуют помощи специалистов. Спленэктомия является, вероятно, наиболее эффективным лечением в этой группе пациентов, но приводит к значительному увеличению заболеваемости и в 25% случаев может оказаться бесполезным. Если иммунная тромбоцитопения у ребёнка переходит в хроническую форму, требуется проведение регулярных обследований на наличие СКВ, поскольку тромбоцитопения может предшествовать появлению маркёров этого заболевания.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Читайте также:

