Удаляют ли вич инфицированным селезенку
Обновлено: 24.04.2024
ВИЧ (VIH), или вирус иммунодефицита человека, поражает различные органы организма человека (пищеварительной, нервной и других систем), но преимущественно воздействует на иммунную систему. В результате развития ВИЧ-инфекции иммунная система теряет способность реагировать даже на самые безобидные инфекции, с которыми легко справляется здоровый организм. Формируется синдром приобретенного иммунодефицита, или СПИД (AIDS). По сути, СПИД является терминальной (завершающей) стадией развития ВИЧ-инфекции, как правило, с летальным исходом. При этом смертельно опасным является не сам СПИД или начальное звено в развитии СПИДа, то есть ВИЧ-инфекция, а заболевания, которые развиваются на фоне измененного иммунного статуса, — так называемые оппортунистические заболевания. К ним относятся различные инфекционные, онкологические или аутоиммунные заболевания (заболевания, при которых иммунная система человека воспринимает собственные клетки организма как чужеродные и повреждает их).
Симптомы ВИЧ-инфекции/СПИДа
Первые симптомы ВИЧ-инфекции могут появиться в конце инкубационного периода (через 2 недели — 6 месяцев после заражения) или чуть позже.
У многих людей данный период протекает бессимптомно, или симптомы могут пройти самостоятельно, даже при отсутствии терапии; заболевание в дальнейшем может никак не проявлять себя в течение нескольких лет.
Для острой фазы заболевания характерны:
- повышенная температура тела;
- увеличенные лимфатические узлы (различных групп: паховые, шейные, подмышечные и др.);
- эритрематозная сыпь (покраснение, вызванное расширением капилляров) и макулопаппулезная сыпь (сыпь в виде плотных выпуклых элементов размером до 10 мм — от телесного до фиолетового оттенков) на лице, туловище, конечностях;
- боли в мышцах и суставах;
- возможны диарея (понос), тошнота, рвота;
- возможно увеличение печени и селезенки.
Далее развивается бессимптомная стадия.
Бессимптомная стадия может протекать как при отсутствии клинических симптомов, так и с развитием персистирующей лимфаденопатии (множественного увеличения лимфатических узлов).В исключительных случаях болезнь минует бессимптомную фазу, прогрессирует вплоть до развития терминальной стадии, СПИДа. Бессимптомный период может длиться до нескольких лет.
Для персистирующей лимфаденопатии характерно:
- увеличение, как минимум, двух групп лимфатических узлов (от 1 см ) в течение 3-х месяцев;
- наиболее часто увеличены шейные, затылочные, подмышечные лимфатические узлы;
- увеличение печени, селезенки.
За бессимптомным периодом следует симптоматическая хроническая фаза ВИЧ-инфекции, характеризующаяся развитием различных вирусных, бактериальных, грибковых заболеваний.
Данная фаза является переходной между бессимптомным периодом развития заболевания и СПИДом, в среднем ее длительность составляет 3-7 лет и более.
- повышенная температура тела;
- повышенное потоотделение в ночное время;
- диарея (понос);
- потеря веса.
Как правило, заболевание на данном этапе сопровождается частыми заболеваниями верхних дыхательных путей и ЛОР-инфекциями:
- отитами (воспаление среднего уха);
- синуситами (воспалением носовых пазух);
- трахеитами (воспалением трахеи);
- тонзиллитами (ангинами).
О переходе ВИЧ-инфекции в терминальную (завершающую) стадию, то есть СПИД (синдром приобретенного иммунодефицита), указывает появление заболеваний у больного человека, которые в норме у здоровых людей встречаются достаточно редко. К ним относятся следующие заболевания.
Грибковые поражения легких:
- воспаление легких, вызванное вирусами герпеса или грибками, чаще рода Сandida;
- пневмоцистная пневмония (вызываемая возбудителем Pneumocystis jirovecii). Заболевание часто наблюдается у ВИЧ-инфицированных и остается одним из первых признаков, по которым ставится подозрение на СПИД (наличие ВИЧ-инфекции).
Поверхностные поражения кожи и слизистых.
- Частые эпизоды опоясывающего лишая.
- Различные грибковые заболевания кожи (в основном вызванные грибами рода Candida – отсюда название кандидоз).
Сопровождается образованием белого налета на видимых частях тела и слизистых оболочках, зудом.
На фоне ВИЧ-инфекции грибок часто поражает внутренние органы (пищевод, легкие и даже головной мозг).
Снаружи грибковое поражение имеет нетипичную локализацию (глаза, сфинктер прямой кишки).
Опухолевые процессы, редко встречающиеся у здоровых людей.
Поражения нервной системы.
- Токсоплазменное поражение головного мозга (вызывается одноклеточным паразитом Toxoplasma gondii, который может инфицировать головной мозг, стать причиной развития энцефалита (воспалительного процесса в веществе головного мозга)).
- Криптококковый менингит — инфекционное заболевание, поражающее мозговые оболочки, вызываемое грибом Cryptococcus neoformans. Сопровождается высокой температурой тела, головной болью, усталостью, тошнотой, рвотой, припадками.
- Прогрессивная мультифокальная лейкоэнцефалопатия — заболевание, при котором постепенно разрушается миелиновый слой, покрывающий длинные отростки нервных клеток (аксоны), в результате нарушается проведение нервных импульсов, что может стать причиной развития параличей, нарушения функции слуха, зрения и других тяжелых неврологических нарушений.
Причиной болезни является полиомавирус. Вирус присутствует в организме большинства абсолютно здоровых людей и никак не проявляет себя. Активация вируса происходит на фоне сниженного иммунитета. Человек умирает в течение нескольких месяцев после появления первых симптомов.
Диагностика
Ранняя диагностика ВИЧ-инфекции осложняется тем, что первоначальные симптомы встречаются и при других различных заболеваниях и не являются характерными непосредственно для ВИЧ-инфекции. Тем не менее подозрение на ВИЧ ставится при следующей симптоматике:
Подозрение на ВИЧ-инфекцию возникает при следующих состояниях:
- пневмоцистная пневмония (воспаление легких грибкового характера), грибковое поражение нервной системы и внутренних органов;
- подтвержденная саркома Капоши у лиц моложе 60 лет;
- токсоплазмоз мозга (инфекция мозга, вызванная токсоплазмой);
- опоясывающий герпес у лиц моложе 50 лет.
Лабораторная диагностика.
На начальных этапах болезни антитела к ВИЧ, как правило, не обнаруживаются, потому основным диагностическим методом является ПЦР (полимеразно-цепная реакция) — метод обнаружения РНК вируса.
ИФА (иммуноферментный анализ) на определение антител к ВИЧ. Антитела, как правило, определяются через 3 месяца с момента заражения.
Иммуноблоттинг (метод применяется после положительного результата ИФА). Суть заключается в определении специфических антител к 3-м основным антигенам оболочки вируса.
Осложнения и последствия
По сути, осложнения и последствия ВИЧ-инфекции являются ничем иным, как признаками развития СПИДа.
ВИЧ-инфекция — один из факторов, который во много раз повышает вероятность развития рака. Выяснили, какие именно онкозаболевания чаще всего могут возникать при положительном ВИЧ-статусе, как их вовремя обнаружить, и на какие факторы риска еще нужно обратить внимание людям, живущим с ВИЧ.
Мишень вируса
Главная мишень вируса — CD4-Т-лимфоциты. Они передают сигнал другим клеткам, которые защищают организм от рака. В результате вмешательства вируса количество CD4-T-лимфоцитов постепенно уменьшается. Критически низкий уровень этих клеток - одна из причин отсутствия согласованной работы между звеньями иммунитета и главный механизм, приводящий к развитию СПИДа.
СПИД-индикаторные опухоли
Иммунитет человека с ВИЧ-инфекцией перестает контролировать процессы избыточного клеточного деления и злокачественной трансформации клеток. Вместе с уменьшением количества CD4-T-лимфоцитов происходит накопление раковых клеток. В результате у человека развиваются несколько видов опухолей, которые называют СПИД-индикаторными: появление такого вида рака с очень большой вероятностью означает наличие у человека СПИДа.
Однако повышается риск появления не только СПИД-индикаторных опухолей, но и тех видов рака, которые развиваются из-за потери иммунного контроля над несколькими онкогенными инфекциями: вирусом герпеса человека 8 типа (ВГЧ-8), вирусом папилломы человека (ВПЧ), вирусами гепатита В и С (ВГВ, ВГС), вирусом Эпштейна-Барр (ВЭБ) и другими.
Все эти состояния развиваются у людей с ВИЧ-инфекцией преимущественно на фоне снижения количества CD4-T-лимфоцитов до уровня менее 200 клеток/мкл (при разбросе в норме от 500 до 1100 клеток), но также могут возникать при нормальном или близком к нормальному уровню CD4-T-лимфоцитов.
Саркома Капоши
Саркома Капоши (СК) — СПИД-индикаторная опухоль, при которой происходит злокачественная трансформация клеток лимфатических и кровеносных сосудов. Риск развития СК у пациентов с ВИЧ-инфекцией увеличивается в несколько сотен раз. Различные белки ВИЧ-1 способны усиливать воспаление и нарушать регуляцию в эндотелиальных клетках. Это приводит к тому, что саркома Капоши может развиться до того, как уровень CD4-T-лимфоцитов упадет ниже 200 клеток/мкл. Еще одно обязательное условие для возникновения СК — наличие в организме вируса герпеса человека 8 типа.
Саркома Капоши развивается в виде папулы, пятна, узелка, бляшки коричневого, розового, красного или темно-красного цвета от нескольких миллиметров до нескольких сантиметров в диаметре. Обычно высыпания концентрируются на ногах, голове, шее, на слизистой оболочке — в области неба, десен, конъюнктивы.
До эры внедрения лекарств от ВИЧ — антиретровирусной терапии (АРТ) 5-летняя выживаемость (с момента диагностики опухоли) пациентов с саркомой Капоши составляла менее 10%. Применение АРТ значительно улучшило ситуацию — сейчас речь идет о 74%, — а также позволило снизить риск развития СК.
Более половины случаев СК (56%) диагностируются сейчас в локальной форме — до того, как опухоль распространится на лимфатические узлы, слизистую ЖКТ, печень, селезенку и другие органы. Прием антиретровирусной терапии помогает значительно замедлить прогрессию болезни и предотвратить распространение СК по всему организму.
Однако, человеку с ВИЧ и его амбулаторному врачу-инфекционисту необходимо учитывать несколько факторов риска развития этой опухоли:
- Этническая принадлежность: люди еврейского или средиземноморского происхождения, а также экваториальные африканцы;
- Мужской пол;
- Иммунодефицит: Люди с уровнем CD4-клеток менее 200 кл/мкл, те, кто перенес трансплантацию органов или костного мозга или постоянно принимает глюкокортикостероиды;
- Сексуальная ориентация: мужчины, имеющие секс с мужчинами(МСМ), подвержены более высокому риску развития СК.
Опухоли, связанные с ВПЧ
К онкологическим заболеваниям, ассоциированным с вирусом папилломы человека, относятся инвазивный рак шейки матки (ИРШМ), сквамозный (чешуйчатый) рак головы/шеи, рак анального канала, вульвы и влагалища. СПИД-индикаторной из них является только ИРШМ.
Распространенность генитальной онкогенной инфекции ВПЧ среди женщин, живущих с ВИЧ, в целом выше, чем у остального населения.
Вирус папилломы человека способен к самопроизвольной элиминации — исчезновению из организма. У ВИЧ-положительных женщин этот процесс занимает больше времени, что увеличивает вероятность появления патологических изменений в шейке матки.
Продолжительный прием АРТ приводит к более низкой распространенности ВПЧ высокого риска и поражений шейки матки и даже предотвращает новые случаи ИРШМ.
Раннее начало антиретровирусной терапии, приверженность лечению обеспечивают снижение вирусной нагрузки — количества вируса в крови. Эти меры очень эффективны в отношении местного иммунитета слизистой оболочки и профилактики ИРШМ.
Скрининг ИРШМ заключается в проведении ПАП-теста и ВПЧ-теста (ПЦР). Женщины с ВИЧ-инфекцией в возрасте от 21 до 29 лет должны пройти ПАП-тест во время первичной диагностики ВИЧ, затем — через 12 месяцев, если анализ не показал патологии. Некоторые эксперты рекомендуют делать следующий ПАП-тест через 6 месяцев после первого. Если результаты трех последовательных мазков без отклонений, повторные тесты следует проводить каждые 3 года. ВПЧ-тест не рекомендуется подключать к ПАП-тесту до 30 лет — высока вероятность положительного результата, при этом оснований для активных действий нет. Лечения ВПЧ не существует, а для развития РШМ требуется, как правило, от 10 лет.
Также для предотвращения ИРШМ девочкам с сопутствующей ВИЧ-инфекцией старше 9 лет и до 26 лет крайне рекомендуется вакцинация от ВПЧ-инфекции (вакцины: 2-валентный Церварикс, 4-валентный Гардасил, в Европе/США - 9-валентный Гардасил-9). Кроме ИРШМ и дисплазии вульвы и влагалища у женщин, вакцинация предотвращает развитие рака анального канала. У ВИЧ+ гетеросексуальных мужчин и МСМ риск этого вида рака возрастает в 19 раз.
О чем еще нужно знать
У пациентов с ВИЧ-инфекцией повышается риск развития:
Гепатоцеллюлярная карцинома
К факторам риска развития ГЦК у пациентов с ВИЧ относятся: цирроз печени, ожирение, диабет, возраст старше 60 лет, мужской пол.
Скрининг ГЦК проводится с помощью анализа крови на альфа-фетопротеин (АФП), который может продуцироваться раковыми клетками, или инструментальных методик диагностики — УЗИ, КТ, МРТ.
В последние годы всё чаще используется фиброскан для оценки стадии фиброза и близости к циррозу, независимому фактору риска ГЦК.
Предотвратить появление гепатоцеллюлярной карциномы можно с помощью своевременной вакцинации и ревакцинации от вирусного гепатита В и контроля вирусной нагрузки.
Неходжкинские лимфомы (НХЛ)
Несмотря на появление АРТ, НХЛ остаются актуальной проблемой для людей, длительное время живущих с ВИЧ. Хотя в большом количестве случаев неходжкинские лимфомы являются СПИД-индикаторными, они способны развиваться при нормальном уровне CD4-клеток и являются одной из наиболее частых причин смерти среди ВИЧ-положительных.
Общая выживаемость у пациентов с этим диагнозом низкая: более половины умирают в течение пяти лет от момента постановки диагноза
Отсюда возникают факторы риска развития НХЛ при ВИЧ-инфекции:
- наличие ко-инфекции вирусными гепатитами В, C, H.pylori;
- наличие вирусной нагрузки вируса Эпштейна-Барр или цитомегаловируса;
- наличие аутоиммунных заболеваний до постановки диагноза ВИЧ-инфекция;
- наличие специфических изменений в протеинограмме до или во время ВИЧ-инфекции;
- наличие минимальной вирусной нагрузки ВИЧ, несмотря на АРТ;
- снижение CD4-Т-лимфоцитов.
К скринингу неходжкинских лимфом относятся мониторинг вирусной нагрузки ВЭБ, ВГС, ВГВ и проведение инструментальной диагностики (КТ, МРТ, УЗИ, ФГДС).
С помощью контроля факторов риска и своевременного скрининга можно не только найти опухоль на ранней стадии, но и предотвратить заболевание.
Если рак все же обнаружили, ни в коем случае нельзя прерывать антиретровирусную терапию — она проводится по жизненным показаниям, что означает высокую вероятность неблагоприятного исхода противоопухолевой терапии без сопутствующего противовирусного лечения.
Несмотря на огромное количество статей и исследований о ВИЧ, в обществе до сих пор гуляет множество мифов и заблуждений об этом заболевании, а люди, столкнувшиеся с ВИЧ, — стигматизируются. Добавляет масла в огонь новость о всемирной ВИЧ-эпидемии. В результате — общество в неведении и панике. Резидент Высшей школы онкологии и химиотерапевт Татьяна Бобровицкая помогает нам снизить накал страстей и рассказывает, что современная медицина уже знает о ВИЧ-инфекции.
Неутешительная статистика: 1 млн россиян болеет ВИЧ
На первом месте в списке регионов-лидеров по количеству смертей от ВИЧ находится Кемеровская область: с 2018 года коэффициент смертности здесь вырос на 11% и составил 65,1. На втором месте находится Иркутская область с коэффициентом 42,4, что на 1% ниже показателей прошлого года (за год снизился на 1%). Третье место заняла Свердловская область, где коэффициент смертности вырос на 10% и составил 38,1.
АРТ снижает смертность от ВИЧ и СПИДа на 38%
К концу 2017 года 21,7 млн человек с ВИЧ-инфекцией получали пожизненную АРТ по всему миру. По оценкам экспертов, только 75% носителей этого заболевания знают свой статус.
- 90 % всех людей с ВИЧ должны знать о своем статусе;
- 90 % ВИЧ-инфицированных должны стабильно получать АРТ;
- у 90 % людей, получающих АРТ, должна наблюдаться вирусная супрессия (ограничение или полное подавление любой физиологической активности вируса — прим. ред.)

АРТ способна уничтожить ВИЧ в крови
ВИЧ невозможно вылечить, но благодаря использованию антиретровирусных препаратов (АРВ) его можно контролировать и, следовательно, предотвращать передачу. АРТ блокирует выработку новых вирусов в активных клетках CD4, инфицированных ВИЧ. Если терапия подошла пациенту, вирусная нагрузка снижается на 90% через несколько недель после начала терапии, а через несколько месяцев — уже на 99%.
Люди с ВИЧ, принимая терапию, могут иметь здоровых детей
АРТ охватывает порядка 80% беременных и кормящих грудью женщин по всему миру. По данным исследования Роланда Тубиана, Джерома Ле Шенадек Кристины Розиу и др. риск передачи ВИЧ типа 1 от матери к ребенку составляет всего 0,5% у не кормящих матерей, которые родили в срок, получая АРТ. Методология и результаты исследования опубликованы в журнале Clinical Infectious Diseases в феврале 2010 года.
Ученые пришли к выводу, что непрерывный контроль вирусной нагрузки на ранних стадиях уменьшает остаточный риск передачи ВИЧ-инфекции от матери к ребенку. При этом, для принятия решения о времени начала АРТ во время беременности важно учитывать не только количество CD4 (+) Т-клеток и риск преждевременных родов, но и также ВИЧ-нагрузку.
Сегодня существует множество доказательств влияния АРТ на распространение ВИЧ-инфекции. Инфицированный человек с неопределяемым уровнем вирусной нагрузки не может передавать заболевание. С 2007 по 2016 годы ученые провели три крупных исследования передачи ВИЧ половым путем при участии пар (как гомо-, так и гетеросексуальных), в которых один из партнеров — с ВИЧ-положительным статусом, принимающий АРТ.
В ходе исследований авторы не зафиксировали ни одного случая передачи вируса. Тем не менее, авторы UNAIDS Explainer настаивают на проведении тестов для уверенности в том, что у носителя подавлена вирусная нагрузка.
Как правило, человек с ВИЧ-положительным статусом, не принимающий АРВ-препараты, живет не более 10 лет. Продолжительность жизни при этом сильно зависит от ряда факторов: образа жизни, иммунитета и т. д. — некоторые не проживают и 3 лет с момента заражения. При этом, человек умирает не от СПИДа, а от оппортунистических (сопутствующих) заболеваний.
Препараты, созданные для борьбы с ВИЧ, уже объединены в отдельный класс. Они снижают вирусную нагрузку и блокируют распространение вируса. Благодаря этому, уровень лимфоцитов в крови повышается, поддерживая нормальный уровень иммунной защиты.
Если человек принимает терапию, то продолжительность жизни приближается к средней в популяции. В развитых странах ожидаемая продолжительность жизни — 60 лет с момента постановки диагноза.
Туберкулез — главная причина смерти людей с ВИЧ
Ежедневно от туберкулеза умирает около 4,4 тыс людей с инфекционными заболеваниями. Количество смертей от этой болезни среди ВИЧ-инфицированных людей в 2017 году составило 300 тыс. человек.
Страны-участники ООН в Политической декларации ООН об искоренении СПИДа взяли на себя обязательство к 2020 году снизить уровень смертности от туберкулеза среди носителей ВИЧ-инфекции на 75 %.
Риск развития онкологии при ВИЧ без АРТ увеличивается до 20 раз
У ВИЧ-инфицированных женщин переход нелеченной эрозии шейки матки в рак шейки матки (РШМ) происходит намного быстрее, чем у здоровых из-за поражения иммунной системы: при отсутствии терапии риск развития РШМ увеличивается в 5 раз, а по некоторым данным — в 13 раз.
Так, женщина с ВИЧ должна проходить цитологический скрининг не реже 1 раза полгода, а также тестирование на вирус папилломы человека (ВПЧ).
Важно знать, что, наряду с риском РШМ, увеличивается риск развития лимфом, злокачественного опухолевого заболевания лимфатической системы, в 20 раз, а также саркомы Капоши — множественных злокачественные новообразований кожи, которые в 95% случаев встречаются только людей с ВИЧ.

Как не заболеть?
Уже есть схемы терапии, позволяющие предотвратить инфицирование. Это доконтактная и постконтактная профилактика для пар с разным или неизвестным ВИЧ-статусом, а также для людей, практикующих частую смену половых партнеров.
В результате исследователи выявили несколько побочных эффектов: боли в месте инъекции (88% у активной группы и 49% — в группе плацебо), боли в животе и диарея, повышение уровня аспартат-аминотрансферазы (АсАт, молекулы белка, способствующей активизации биохимических процессов в организме), головокружение и общее недомогание.
Чтобы проверить иммуногенность вакцины (способность антигена вызывать иммунный ответ), ученые вакцинировали обезьян, а затем инфицировали их комбинированным вирусом SHIV (simian-human immunodeficiency virus). Выяснилось, что Ad26.Mos.HIV с gp140 защищает от инфекции лучше всего: даже после шестикратного введения вируса ⅔ животных остались здоровы. Сейчас проект находится в фазе испытаний 2b для оценки эффективности вакцины на 2600 женщинах с высоким риском заражения в Южной Африке.
Безусловно, ВИЧ-инфекция — серьезное и опасное заболевание, от которого никто не застрахован. Однако, благодаря труду врачей и ученых по всему миру, оно больше не приравнивается к смертному приговору. Для человека с ВИЧ-положительным статусом существует лишь одно ограничение — необходимость АРТ. В остальном носитель вируса сегодня может жить полноценной жизнью: ходить на работу, получать медицинскую помощь, иметь детей, с любовью и ответственностью относиться к себе, своему здоровью и здоровью своих близких.
Авторами проведен ретроспективный анализ историй болезни, диагностики и результатов лечения пострадавших с повреждениями селезенки с сопутствующей ВИЧ инфекцией и вирусоносительством гепатита В или С, а также их сочетанием, и представлены два клинических наблюдения. Патологические изменения в селезенке при данных инфекциях увеличивают риск ее повреждения. При оперативном вмешательстве у данных пациентов должны строго соблюдаться инструкции работы хирургов в операционной. При повреждении селезенки тактический подход оперативного лечения в каждом конкретном случае должен быть индивидуальным.
Features diagnosis and treatment of patients with damage spleen and concomitant HIV infection, hepatitis B, C
The authors conducted a retrospective analysis of medical records, diagnosis and results of treatment of patients with injuries of the spleen with human immunodeficiency virus infection and infection with hepatitis B or C, as well as a combination of both, and present two clinical cases. Pathological changes in the spleen in these infections increase the risk of damage. Surgical intervention in these patients should be strictly followed the instructions of the surgeons in the operating room. If damaged spleen tactical approach of surgical treatment in each case must be individualized.
Вирусные гепатиты — одна из наиболее актуальных проблем современной медицины во всем мире, возбудителями вирусных гепатитов ежегодно заражаются сотни миллионов людей, а более миллиона человек умирают каждый год от этих заболеваний. Считается, что в тот или иной период жизни вирусом гепатита В инфицированы около 2 млрд. человек, а постоянными носителями вируса являются около 350 млн. жителей земного шара. Стремительный рост количества ВИЧ инфицированных в мире и в России влечет за собой повышение риска профессионального заражения ВИЧ для медицинских работников. При этом следует знать, что официальные сведения о носителях не соответствуют их действительному числу из-за сложностей организации и проведения обследований.
Эти обстоятельства привели к тому, что произошло значительное увеличение числа ВИЧ и гепатит инфицированных больных среди пострадавших с закрытой травмой живота и повреждением селезенки. Нельзя не отметить тот факт, что сами по себе эти инфекции приводят к патологическим изменениям в селезенке, что увеличивает риск ее повреждений даже при минимальной травме.
Из неинвазивных методов наиболее часто применяли УЗИ (18 больных), при этом у 8 пострадавших выявлена свободная жидкость в брюшной полости и выполнен лапароцентез. У пострадавших с тяжелой сочетанной ЧМТ (6 человек) параллельно проводили РКТ головного мозга и брюшной полости. У пострадавших с нестабильной гемодинамикой чаще всего в условиях приемного покоя выполняли лапароцентез одновременно с реанимационными мероприятиями. Диагностическую лапароскопию выполняли в сомнительных случаях у 4 пострадавших со стабильной гемодинамикой. При диагностике внутрибрюшного кровотечения выполняли экстренную лапаротомию. Дополнительные сложности в диагностике возникли у 1-го ВИЧ инфицированного больного и у 2-х с гепатитами В и С, так как у них отсутствовали клинические признаки повреждения селезенки, был сомнительный анамнез травмы.
Клиническое наблюдение 1.
Рисунок 1. По данным УЗИ и клинической картины — абсцесс нижнего полюса селезенки

Диагноз: Абсцесс нижнего полюса селезенки. Показано оперативное лечение. Под наркозом левым подреберным разрезом произведена лапаротомия. При ревизии брюшной полости выявлена увеличенная в размерах багрового цвета, пастозная на ощупь селезенка, в нижней и средней трети которой обнаружен абсцесс, содержащий 200 мл грязно-серого цвета гной с неприятным запахом. Выполнена спленэктомия, санация и дренирование брюшной полости.
В послеоперационном периоде у пациентов после спленэктомии повышается число тромбоцитов, наблюдается длительная гипертермия. В нашем наблюдении у больного наблюдался значительный тромбоцитоз с тенденцией постоянного роста (710х10 3 /mm 3 на 6 сутки после операции), гипертермия до 39 0 С. На 12 сутки с момента операции выписан в удовлетворительном состоянии.
Клиническое наблюдение 2.
Рисунок 3. Попкасульная гематома селезенки

Рисунок 4. Вид после опорожнения гематомы

Послеоперационное течение гладкое. Тромбоцитоза и гипертермии не наблюдалось. Выписан в удовлетворительном состоянии на 10 сутки.
Таким образом в современных условиях с увеличением пациентов с ВИЧ и гепатитом В, С, вероятность числа пациентов с повреждения селезенки существенно возрастает. При оперативном вмешательстве у данных пациентов должны строго соблюдаться инструкции работы хирургов в операционной. При повреждении селезенки тактический подход к оперативному лечению в каждом конкретном случае должен быть индивидуальным.
Р.А. Ибрагимов, В.Ф. Чикаев, А.Ю. Анисимов, Ю.В. Бондарев
Казанский государственный медицинский университет
Больница скорой медицинской помощи №1, г. Казань
Ибрагимов Ринат Абдулкабирович — кандидат медицинских наук, ассистент кафедры травматологии ортопедии и ХЭС
Случилась непредвиденное…Сирены машин, мигалки, люди в белых халатах и свет ламп в операционной. Пришел в себя и услышал диагноз – вам удалена селезенка. Другой случай – плановый. Но также грустный диагноз, врач рекомендует пройти спленэктомию. Целый список с анализами, госпитализация, лампы, наркоз, реанимация. Суть одна – удалена селезенка, какие последствия этого?
Что это за орган? Какие функции выполняет в организме? Как жить дальше и каковы последствия, прогноз операции? Эти вопросы задает себе и лечащему врачу пациент. Попробуем разобраться в этом вопросе.
За что отвечает этот орган в теле человека
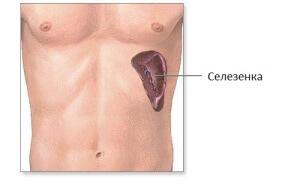
Селезенка располагается в левом подреберье в промежутке между 9 и 11 парой ребер.
Селезенка долгое время считалась второстепенным органом человека. Существовало даже мнение, что другие органы следует беречь, а этот не жалко. Это продолжалось до тех пор, пока не были изучены ее функции и строение.
Селезенка насыщена кровеносными сосудами. Кровь, попадая в этот орган, получает свежую порцию развивающихся лейкоцитов – клеток, ответственных за иммунную защиту организма.
В селезенке происходит утилизация отживших клеток крови, вирусов, инородных частиц, попавших в кровеносную систему. Кроме этого, орган отвечает за кроветворение и процессы коагуляции крови.
Располагается этот орган в левом подреберье в промежутке между 9 и 11 парой ребер. На внешний вид селезенка походит на кофейное зерно. Жить без нее можно. Человек продолжает вести активный образ жизни и не становится инвалидом.
Зачем удалять селезенку? Показания к проведению операции
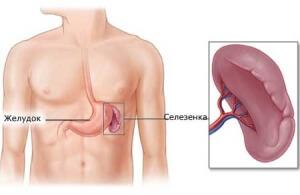
Селезенка удаляется при повреждении кровеносных сосудов в самом органе.
В человеческом теле нет лишних или ненужных органов. И поэтому селезенку удаляют только по жизненно важным показаниям, а не подчиняясь желаниям пациента. Операция спленэктомии проводится в следующих случаях:
- Травмы органа, несовместимые с дальнейшим выполнением его функций.
- Разрыв селезенки, несмотря на причины его вызвавшие. Это может быть травма, прием лекарственных средств, острая интоксикация, опухоли и инфекционные заболевания, такие как мононуклеоз.
- Повреждение кровеносных сосудов в селезенке. Внутреннее кровотечение.
- ВИЧ-инфекция.
- Миелофиброз – замещение тканей костного мозга фиброзными тяжами.
- Лейкемия, опухоли органа различной этиологии.
- Патологическое увеличение селезенки.
Хирургическое вмешательство бывает экстренным – как правило, вследствие травмы – и плановым.
Спленэктомия, как проходит операция
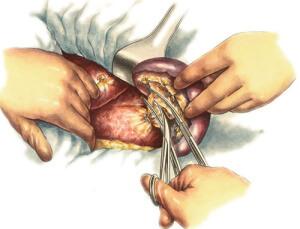
Спленэктомия — хирургическая операция по удалению селезенки.
В XX веке удаление селезенки проходило под общим наркозом. Это была широкополосная операция с длительным периодом восстановления.
Современные методики позволяют спасти орган, наложить швы. Иногда небольшие участки уже удаленной ткани селезенки подшивают к стенке брюшины.
Они способны прирастать и увеличиваться в размерах. При достижении объема в 1 см ткань способна выполнять функции изъятого органа. В настоящее время спленэктомия с полным доступом проводится в исключительных случаях:
- Увеличение линейных размеров селезенки
- Ожирение пациента с большим жировым слоем в операционной области.
Во всех других случаях спленэктомию проводят при помощи лапароскопа. Сама процедура длится от 45 минут до 1 часа под общим наркозом. После операции орган направляется на гистологическое исследование.
Если вмешательство прошло без осложнений, то на 4 день после операции пациент покидает хирургическое отделение. Полное восстановление происходит в течение 1–1,5 месяцев. Это зависит от причин, вызвавших хирургическое вмешательство – была ли это травма, экстренная операция или плановая, диагноз пациента.
Последствия

Боли в левом подреберье после операции должны насторожить пациента.
Все последствия условно делятся на ближайшие, которые могут произойти сразу после вмешательства или в период реабилитации, и отдаленные. И в том, и в другом случае многое зависит от поведения пациента. Ближайшие последствия спленэктомии:
Все эти патологии считаются ближайшими и особенно опасными в течение 2 лет после хирургического вмешательства. Что должно насторожить пациента в этот период:
- Сильные боли в прооперированной области
- Любые признаки инфекции – боли, жжение, гнойные выделения, повышение температуры тела, озноб
- Кровотечение или любые другие выделения из места введения инструментов
- Кашель
- Тошнота, рвота, прочие диспепсические расстройства
- Отдышка
Возникновение любого из этих симптомов является поводом для срочного визита к врачу. Снизить риск развития ближайших осложнений помогут следующие действия:
- Лапароскопия – это щадящая методика. Но вы должны помнить, что у вас удалили орган. Поэтому никаких трудовых подвигов сразу после выписки.
- Уточните у врача, когда вам можно принимать душ, купаться. Прием горячей ванны временно откладывается, так как повышается риск кровотечения.
- Не переохлаждайтесь. Это та ситуация когда лучше вспотеть, чем замерзнуть.
- Не садитесь за руль в течение 1,5 месяцев после операции.
- Не посещайте места большого скоплению людей. У вас снижен иммунитет, и любой вирус может перерасти в серьезное заболевание.
- Не принимайте обезболивающие препараты, содержащие аспирин.
- Не поднимайте тяжести, легкая атлетика также временно под запретом.
- Принимайте назначенные врачом препараты.
- На любом приеме сообщайте врачу о том, что у вас удалена селезенка.
Жизнь после спленэктомии
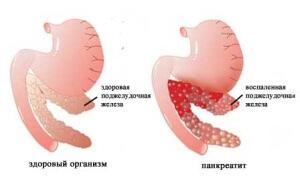
Последствием удаления селезенки может быть развитие панкреатита.
Отдаленные последствия возникают и развиваются в течение жизни после реабилитационного периода.
Удаление любого органа наносит удар по иммунитету, а при спленэктомии убирают именно орган, участвующий в формировании защиты нашего организма. Отдаленные последствия резекции селезенки:
- Снижение иммунитета, и как следствие риск инфицирования повышается
- Образование тромбов в сосудах печени
- Развитие панкреатита
- Ателектаз легких – спадание или безвоздушность альвеол органа
Снизить вероятность развития отдаленных осложнений могут следующие рекомендации:
- Вакцинация в осенне-зимний период от гриппа.
- Избегать появляться в людных местах в период эпидемий. Не стоять в очередях, не передвигаться в общественном транспорте, по возможности не посещать лечебные учреждения.
- Перед поездкой в экзотические страны обязательно сделать все рекомендуемые прививки.
- Периодически проходить профилактический осмотр и УЗИ системы ЖКТ, сдавать анализы мочи, крови – общий и печеночные пробы.
- Не желательны поездки в страны, где можно получить малярию.
- Не забывать про личную гигиену. После посещения общественных учреждений обязательно мыть руки. Это убережет вас от гепатита.
- Вести здоровый образ жизни и правильно питаться.
- Не применять лекарственные препараты без назначения врача и показаний.
- При простуде или других инфекционных заболеваниях сразу обращаться к врачу.
Придерживаться этих правил легко. И не только после спленэктомии, но и пациентам с полным комплектом органов. И риск возникновения отдаленных осложнений будет стремиться к нулю.
Рекомендации по питанию

Жирную и острую пищу следует убрать из рациона после удаления селезенки.
Природа умна. И если по какой-то причине человек теряет орган, то другие органы начинают выполнять часть его функций, компенсируя тем самым недостачу. В случае спленэктомии за иммунную защиту организма начинает отвечать лимфатическая система и печень.
Поэтому важно придерживаться щадящей диеты. В реабилитационном периоде она направлена на снижение нагрузки на печень, травмированную брюшину и другие органы ЖКТ. В дальнейшем рекомендуется придерживаться принципов здорового питания. Из рациона следует убрать:
- Тяжелые и жирные блюда
- Острые приправы и маринад
- Жирное мясо
- Блюда, приготовленные в большом количестве жира, во фритюре
- Жирные наваристые костные бульоны и блюда на их основе
- Крепкий кофе и спиртные напитки
- Сигареты и наркотические препараты
Что можно есть после удаления селезенки:
- Врачи рекомендуют ввести в рацион большое количество овощей, как сырых, так и приготовленных
- Фрукты в любом количестве – свежие и приготовленные
- Жидкость из расчета 30 г на 1 кг веса пациента
- Крупяные блюда
- Молочные и кисломолочные продукты с небольшим процентом жирности
- Рыба, мясо – выбирайте нежирные сорта или куски. В первое время после операции готовьте на пару или в духовке
- Лекарственные травы, улучшающие отток желчи и функции печени, следует пропивать периодически курсами по рекомендации врача
Прогноз для пациента после спленэктомии
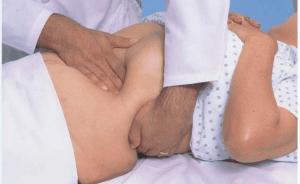
Удаление селезенки не является критической ситуацией для организма.
Как будет жить пациент после операции, возникнут ли осложнения, зависит от нескольких факторов:
- Причина, по которой была назначена операции – травма, опухоли и какого генеза, инфекции, критическое увеличение в размерах. При злокачественных новообразованиях прогноз неблагоприятный
- Как проходило вмешательство – методика проведения, процент кровопотери, травмы соседних органов.
- Состояние пациента после спленэктомии – как быстро пришел в себя после наркоза, состояние в реанимации
- Постоперационный период – скорость заживления, отсутствие воспалительных или инфекционных процессов в местах введения инструментов.
- Дальнейшее поведение пациента в течение жизни.
Удаление селезенки не является критической ситуацией для организма. В целом прогноз благоприятный, так как функции органа компенсируются. Длительность и качество жизни пациента зависят от поведения человека на этапе реабилитации и в дальнейшем.
Подробно о селезенке расскажет видеоматериал:
Читайте также:

