Уровень железа в крови при гепатите с
Обновлено: 22.04.2024
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Дефицит железа в организме: причины появления, симптомы, диагностика и способы лечения.
Определение
Дефицит железа в организме, или железодефицитная анемия – это патологическое состояние, для которого характерно снижении уровня железа в организме, приводящее к уменьшению концентрации эритроцитов и гемоглобина в крови. По данным ВОЗ, более 2 миллиардов людей в мире имеют недостаток железа в организме.
Причины появления железодефицитной анемии
Наиболее частой причиной возникновения дефицита железа с последующим развитием анемии является неправильное или несбалансированное питание.
Основную группу риска составляют вегетарианцы, люди, придерживающиеся жестких диет с ограниченным набором продуктов в рационе питания, а также пожилые люди - из-за снижения способности кишечника к усвоению железа. Кроме того, нарушение всасывания железа в желудочно-кишечном тракте может наблюдаться после резекции желудка или тонкого кишечника, в результате атрофии слизистой желудка, снижения секреции соляной кислоты, а также в результате целиакии (врожденного заболевания, связанного с непереносимостью глютена), ожирения. Колонизация желудка Helicobacter pylori приводит к увеличению потери железа и снижает его всасывание. Негативное влияние на процессы пищеварения оказывают гельминты, затрудняя, в том числе, всасывание железа.
Железодефицитная анемия нередко диагностируется у детей, подростков и беременных женщин, поскольку у них ежедневная потребность в железе выше, чем в среднем в популяции.
На втором месте среди причин железодефицитной анемии стоит кровопотеря - как острая, так и хроническая. После тяжелых травм, обильных носовых и маточных кровотечений, кровохарканья развивается дефицит железа в связи с потерей большого количества эритроцитов, содержащих железо, и некоторых белков плазмы крови, которые связывают железо в крови.
К менее очевидным причинам потери железа вследствие кровопотери относятся:
- нарушение правил донорства;
- частые необоснованные заборы крови для обследования;
- обильные менструации;
- кровопотери при язвенной болезни желудка и двенадцатиперстной кишки, воспалительных заболеваниях кишечника (болезни Крона и неспецифическом язвенном колите);
- кровотечение из расширенных геморроидальных вен.
У детей первого года жизни возможной причиной хронической кровопотери может стать использование для искусственного вскармливания цельного молока (коровьего, козьего и др.) и неадаптированных молочных смесей в виде разведенного молока и кефира.
Доказано, что при длительном применении такого питания у младенцев развиваются диапедезные кровотечения кишечника (повышенная проницаемость мелких сосудов) с потерей железа.
Классификация железодефицитной анемии
Клиническая классификация железодефицитной анемии:
- Постгеморрагическая анемия – развивается на фоне регулярных (возможно и небольших) кровопотерь (носовых кровотечений, кровянистых выделений из мочевого пузыря и т.д.) или как следствие значительной кровопотери.
- Анемия, связанная с патологиями ЖКТ, - развивается после резекции кишечника, гастроэктомии и связана с нарушением функции всасывания железа.
- Анемия у беременных и кормящих женщин – развивается в результате недостаточного поступления железа, необходимого для развития эмбриона.
- Ювенильная анемия – развивается, как правило, у подростков женского пола и связана с гормональной перестройкой организма.
- Вторичные анемии – развиваются на фоне воспалительных, инфекционных и онкологических процессов вследствие большой потери железа при распаде опухолевых тканей или повышения потребности в железе в очагах воспаления.
- Эссенциальная (идиопатическая) анемия – диагностируется в тех случаях, когда точно установить причину нехватки железа не удается.
- Алиментарная анемия - к факторам алиментарного порядка относят вегетарианство, диеты с ограниченным потреблением мяса, снижение абсорбции или транспорта железа.
- анемия легкой степени тяжести, когда уровень гемоглобина составляет от 90 до 120 г/л;
- анемия средней степени тяжести, когда уровень гемоглобина составляет от 70 до 89 г/л;
- тяжелая анемия, когда уровень гемоглобина опускается ниже 70 г/л.
Железодефицитную анемию классифицируют по стадиям протекания:
1-я стадия. Потеря железа больше, чем его поступление, в результате чего его запасы в организме снижаются, а всасывание в кишечнике увеличивается.
2-я стадия. Истощение запасов железа, количество эритроцитов начинает снижаться.
3-я стадия. Развивается легкая степень анемии.
4-я стадия. Развивается выраженная анемия с явным снижением насыщения эритроцитов гемоглобином.
5-я стадия. Тяжелая анемия с циркуляторными нарушениями и тканевой гипоксией.
Симптомы железодефицитной анемии
Железодефицитная анемия является заболеванием крови и проявляется многочисленными симптомами, которые объединены в два основных синдрома: анемический и сидеропенический.
При длительном течении и медленном развитии железодефицитной анемии возможна компенсация и отсутствие субъективных неприятных симптомов.
Внешне человек, страдающий железодефицитной анемией, бледен, губы и слизистые полости рта бледно-розовые, артериальное давление может быть снижено, при исследовании пульса наблюдается его учащение.
Сидеропенический синдром заключается в дефиците железа во многих тканях организма. Это проявляется сухостью кожных покровов, шелушением кожи и трещинами в уголках рта (заедами, или ангулярным стоматитом). Иногда возникают жалобы на сухость во рту, боль или жжение языка. Ногти теряют прочность и начинают слоиться. Ногтевая пластина принимает вогнутый, ложкообразный внешний вид (койлонихия).

Волосы становятся ломкими, усиленно выпадают. Очень характерным признаком является изменение вкусовых предпочтений и извращенное обоняние. Люди с железодефицитной анемией неожиданно начинают употреблять в пищу необычные или непригодные для еды вещества и предметы (самый яркий пример – поедание мела или земли), им нравятся запахи краски, бензина, ацетона. В тяжелых случаях развивается мышечная слабость вплоть до недержания мочи и нарушения функции глотания.
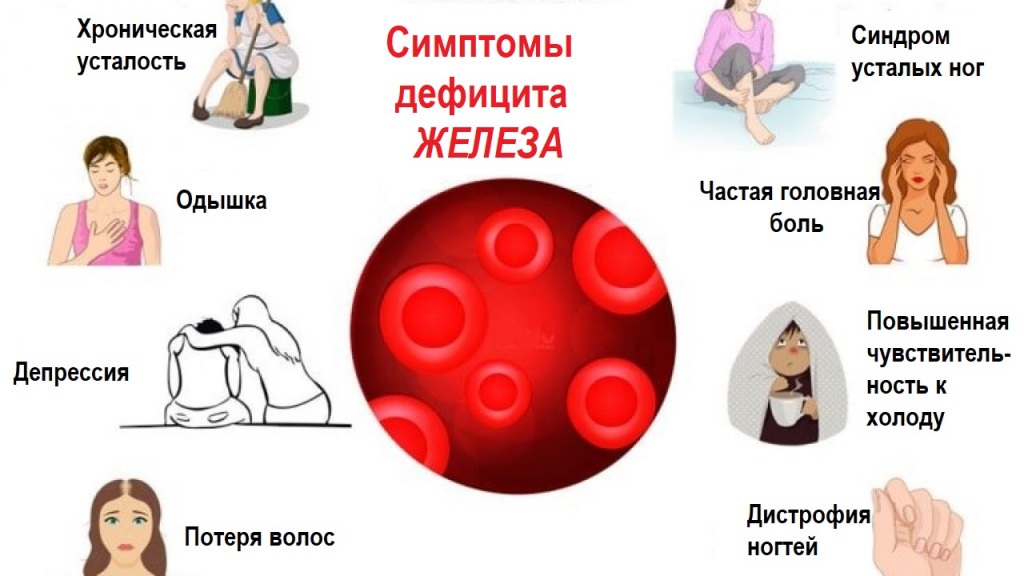
Для детей железодефицитная анемия опасна замедлением психомоторного развития.
Младенцы часто срыгивают пищу, у детей постарше наблюдается необъяснимая рвота, расстройства стула, плохая прибавка веса.
Диагностика железодефицитной анемии
Для диагностики железодефицитной анемии могут быть назначены следующие лабораторные и инструментальные обследования:
-
клинический анализ крови (определение уровня гемоглобина, количества эритроцитов, их размера, насыщения гемоглобином, формы, уровня гематокрита, скорости оседания эритроцитов, количества тромбоцитов и подсчет лейкоцитарной формулы);
Синонимы: Общий анализ крови, ОАК. Full blood count, FBC, Complete blood count (CBC) with differential white blood cell count (CBC with diff), Hemogram. Краткое описание исследования Клинический анализ крови: общий анализ, лейкоформула, СОЭ См. также: Общий анализ – см. тест № 5, Лейкоцит.
С-реактивный белок – белок острой фазы, чувствительный индикатор повреждения тканей при воспалении, некрозе, травме. Синонимы: Анализ крови на СРБ; С-реактивный белок сыворотки крови. C-reactive Protein (CRP), quantitative; C-reactive protein test; CRP test. Краткое описание опред.
Аланинаминотрансфераза − внутриклеточный фермент, участвующий в метаболизме аминокислот. Тест используют в диагностике поражений печени, сердечной и скелетных мышц. Синонимы: Глутамат-пируват-трансаминаза; Глутамат-пируват-трансаминаза в сыворотке; СГПТ. Alanine aminotransferase; S.
Синонимы: Глутамино-щавелевоуксусная трансаминаза; Глутамат-оксалоацетат-трансаминаза сыворотки крови (СГОТ); L-аспартат 2-оксоглутарат аминотрансфераза; ГЩТ. Aspartateaminotransferase; Serum Glutamicoxaloacetic Transaminase; SGOT; GOT. Краткая характеристика определяемого вещества АсАТ .
Определение концентрации железа в сыворотке крови в комплексе с другими тестами (см. белки, участвующие в обмене железа) используют в диагностике железодефицитных анемий и контроле применения препаратов железа. Синонимы: Анализ крови на железо; Сывороточное железо. Serum Iron; Serum Fe; Iron; F.
Синонимы: Анализ крови на ферритин; Депонированное железо; Индикатор запасов железа. Serum ferritin. Краткая характеристика определяемого вещества Ферритин Ферритин – это основная форма внутриклеточного депонирования железа в организме. Состоит ферритин из белковой оболочки (апофер.
Синонимы: Переносчик железа; Сидерофилин. Siderophilin, Transferrin; Tf. Краткая характеристика определяемого вещества Транферрин Транферрин – плазменный белок, гликопротеин, основной переносчик железа. Синтез трансферрина осуществляется в печени и зависит от ее функцио.
Исследование слизистой оболочки верхнего отдела желудочно-кишечного тракта с возможностью выполнения биопсии или эндоскопического удаления небольших патологических образований.
Эндоскопическое исследование толстого кишечника для поиска участков патологии, проведения биопсии и удаления небольших полипов и опухолей.
Лечебно-диагностический метод исследования толстого кишечника, во время которого при необходимости может быть проведено малое хирургическое вмешательство (биопсия, удаление полипа до 1 мм).
Сканирование внутренних органов брюшной полости для оценки его функционального состояния и наличия патологии.
Исследование функциональных возможностей сердца – быстро, безболезненно и информативно.
Расшифровка ЭКГ с заключением, выполненная квалифицированным кардиологом ИНВИТРО.
ЭКГ представляет собой исследование, в основе которого - регистрация биопотенциалов сердца. Применяется для диагностики функциональной активности миокарда.
При появлении слабости, сонливости, повышенной чувствительности к низким температурам и других симптомах, характерных для недостатка железа в организме, необходимо обратиться к врачу-педиатру или к терапевту .
Врач составит индивидуальный план диагностики и лечения, а также при необходимости назначит консультации узких специалистов.
Лечение железодефицитной анемии
Лечение железодефицитной анемии назначается врачом после обследования и включает сбалансированную диету и терапию заболевания или состояния, которое привело к развитию дефицита железа, а также восполнение запасов железа в организме.
Препараты двухвалентного и трехвалентного железа назначаются курсом не менее 1,5-2 месяцев, затем, если удалось нормализовать уровень гемоглобина, их дозировку уменьшают в два раза, но продолжают принимать еще минимум 4-6 недель.
При тяжелых состояниях прибегают к гемотрансфузионной терапии.
Осложнения железодефицитной анемии
Легкая степень железодефицитной анемии обычно не вызывает серьезных осложнений, однако длительный дефицит железа может негативно влиять на умственное и физическое развитие ребенка.
Тяжелые степени железодефицитной анемии способны привести к нарушениям работы сердца: аритмиям, снижению сократительной способности сердца и даже к инфаркту миокарда и сердечной недостаточности.
Для беременных железодефицитная анемия опасна изменением тонуса мускулатуры матки, а также задержкой развития плода.
Профилактика железодефицитной анемии
Профилактика железодефицитной анемии заключается в решении основной проблемы развития дефицита железа – недостаточного поступления железа в организм. Важно придерживаться адекватного и сбалансированного питания. Ежедневная потребность взрослого человека в железе составляет около 1–2 мг, ребенка от 0,5 до 1,2 мг в сутки. Полноценное питание при отсутствии заболеваний способно восполнять естественные потери железа, причем важно не количество железа в продукте, а его доступность для всасывания в кишечнике.
Лучше всего всасывается гемовое железо, или иначе – железо животного происхождения. Основными источниками гемового железа являются говядина, баранина, печень, в меньшей степени – рыба и творог.
Железо, содержащееся в продуктах растительного происхождения, имеет сниженную биодоступность (хуже усваивается организмом) и поэтому может рассматриваться лишь как дополнение к мясным продуктам.

Усиливает всасывание железа витамин С, поэтому рекомендуется одновременно употреблять продукты, содержащие железо и витамин С: например, можно приготовить блюдо, в котором будет присутствовать и говядина, и красный болгарский перец. Всасывание железа ухудшается при употреблении большого количества чая, кофе и некоторых лекарственных препаратов, например, антацидов.
Для профилактики дефицита железа у детей разработаны рекомендации по дополнительному введению железа с 4-месячного возраста и до введения прикорма – каш, обогащенных железом. На искусственном вскармливании все дети до 12 месяцев должны получать адаптированные молочные смеси, обогащенные железом.
В рамках профилактики важно вовремя проходить обследование и лечить заболевания, приводящие к хронической кровопотере.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Актуальную проблему в ранней диагностике и лечении функциональной недостаточности печени при наследственных аномалиях крови представляет инфицированность больных вирусом гепатита С. С этой целью у 82 пациентов с α и β талассемией, а также с поздней кожной порфирией было изучено влияние хронического гепатита С на метаболизм железопорфиринового комплекса. У инфицированных больных установлена взаимосвязь между тяжестью функциональных нарушений печени и изменениями в обмене железа и порфиринов. Полученные результаты имеют значение в дифференциальной диагностике различных форм порфирий и наследственных аномалий крови. На основании полученных данных предложен алгоритм обследования пациентов с наследственными заболеваниями крови, осложненными хроническим гепатитом С, который, наряду с рутинными биохимическими тестами, определением маркеров вирусных гепатитов и биопсией печени, включает исследование показателей железопорфиринового комплекса.

Инфицирование вирусом гепатита С (HCV) является основной причиной развития посттрансфузионного гепатита и цирроза печени и потому представляет актуальную проблему для больных с наследственными аномалиями крови [7, 10, 11]. Для этой патологии характерны повсеместное распространение, высокий уровень заболеваемости и смертности. Столь выраженная способность HCV вызывать персистирование инфекции связана с высокой частотой мутаций и образованием множественных квазивидов, незначительно отличающихся друг от друга геномами [6].
Инфицирование вирусом гепатита С пациентов с наследственной патологией крови возникает из-за регулярно проводимой гемотрансфузионной терапии, являющейся основным методом лечения больных. Поэтому пациентов с α и β талассемией причисляют к группе риска по заражению гемотрансмиссивными инфекциями. При гомозиготной форме β-талассемии (гомоз. β-th) HCV инфекция по частоте распространения является второй после гемохроматоза [12]. Возникший хронический гепатит С (ХГС) нередко протекает бессимптомно, под маской основной патологии. Поражается орган, который в норме поддерживает метаболитический гомеостаз и от функционального состояния которого во многом зависят течение и исход основного заболевания. При ХГС изменения в печени представляют собой постоянный, необратимый процесс и характеризуются длительным течением. Манифестация уже на поздней стадии болезни с высокой частотой внутри и внепеченочных проявлений, в том числе развитием анемического синдрома и портального цирроза печени, существенно усложняет лечебно-диагностический процесс [9].
Печень участвует в обмене железа, метаболизме порфиринов и образовании ферментов, необходимых для в синтеза молекул гема. При низких концентрациях сывороточного железа гепатоциты способны отдавать железо в кровь для нужд эритропоэза [6]. С развитием гемосидероза в печени возрастает тяжесть фиброзных изменений. Присоединение ХГС к наследственной патологии крови увеличивает функциональную недостаточность печени. По сравнению с HBV роль HCV инфекции в генезе поражения печени при гомоз. β-th, гемоглобинопатии Н (Hbpat.H) и поздней кожной порфирии (ПКП) представляется более значительной, в связи с частотой его выявления. У больных с ПКП обнаружена связь аккумуляции железа в печени с обострением ХГС [9]. HCV инфекция и железо увеличивают кислородный стресс на гепатоциты, способствуя окислению уропорфириногена в уропорфирин, который не метаболизируется ферментом уропорфириноген-декарбоксилазой, а накапливается в печени и оказывает токсическое влияние на жизненно важные органы и системы [1-5, 8].
В доступной литературе мы не встретили специальных работ, посвященных изучению обмена железа и порфиринов у больных с наследственными аномалиями крови, инфицированных вирусом гепати-
та С. Остаются малоизученными особенности течения ХГС у пациентов с талассемией и поздней кожной порфирией, не определены подходы к неинвазивной диагностике стадии патологического процесса, этиопатогенетической терапии и динамическому наблюдению за данной категорией больных.
Исходя из вышеизложенного целью исследования явилось изучение влияния хронического гепатита С на метаболизм железопорфиринового комплекса и результаты проводимой терапии у больных с гомозиготной формой β-талассемии, гемоглобинопатией Н и поздней кожной порфирией.
Материалы и методы исследования
Под наблюдением находилось 82 пациента с наследственной патологией крови, в возрасте 6-33 лет (медиана - 21 год, женщин - 38, мужчин - 44), проходивших обследование и лечение в АзНИИ гематологии и трансфузиологии. Все больные были разделены на 3 группы: 1-ю составили 32 пациента с гомоз. β-th без и с ХГС (по 16 больных), 2-ую - 30 пациентов с Hbpat.H без и в сочетании с ХГС (по 15 больных) и 3-ю - 20 больных с ПКП без ХГС - 4 случая и с ХГС - 16 пациентов. Во 2-й группе без ХГС 15 пациентов наблюдались после спленэктомии в анамнезе.
Из анамнеза больных следовало, что инфицирование вирусом гепатита С произошло в различные периоды времени, а причиной тому в 89 % случаев была гемотрансфузионная терапия. Заражению в одинаковой степени были подвержены лица обоих полов и различных возрастных групп. Обладая высоким хроногенным потенциалом, HCV инфекция была основной причиной развития ХГС, с переходом в 36 случаях в портальный цирроз печени. Диагноз ХГС подтверждался с помощью клинико-эпидемиологических, лабораторно-инструментальных и морфологических данных, обнаружения в крови антител к вирусу гепатита С, а также путем качественного определения вирусной РНК, методом ПЦР, что имело существенное значение для оценки контагиозности и мониторинга результатов лечения. Маркер HCV исследовался имунноферментным анализом (ИФА). У инфицированных больных основными генотипами HCV были 1в (40 %) и 3а (20 %). С диагностической целью применялась пункционная биопсия печени. В биоптате печени больных обнаружены некрозо-воспалительные и фиброзные изменения, что служило показанием для начала этиотропной терапии. Лечение таких больных включало курсы специфической противовирусной терапии препаратами α-интерфероном и рибавирином.
Результаты исследования и их обсуждение
Нарушения в работе печени при талассемиях и поздней кожной порфирии (ПКП) регистрировались при первичной диагностике заболеваний в 85-97 % случаев. Общее состояние 46 пациентов после присоединения к основной патологии хронического персистирующего гепатита (ХГ) и ХГС оценивалось как средней тяжести, субкомпенсированное, а 36 больных с портальным циррозом печени - тяжелое, декомпенсированное (табл. 1). На течение заболевания оказывали влияние тяжесть анемии и нарушения в обмене железа и порфиринов. Жалобы больных сводились к нарастающей общей слабости, утомляемости, одышке, тяжести в эпигастральной области, выявлялись иктеричности склер и видимых слизистых оболочек. При портальном циррозе печени у 5 больных на коже передней брюшной стенки определялись характерные сосудистые звездочки, а у 19 отмечались диспептические явления с потерей массы тела и желтуха, как результат гемолиза и нарушенной функции гепатоцитов. Гепатомегалия выявлена у 77, а спленомегалия с синдромом гиперспленизма - у 47 больных 1-й и 2-й групп и у 8 пациентов с ПКП. В 26 случаях наблюдались отеки и асцит. У 6 пациентов определялись признаки печеночной энцефалопатии. У 30 больных рентгенологически обнаружено варикозное расширение вен пищевода с кровотечением у 10.
Таблица 1
Распределение ХГ, ХГС и цирроза печени среди больных
с наследственной патологией крови
В настоящее время проблемой хронической HCV-инфекции интересуются как врачи-специалисты, так и люди, никак не связанные с медициной. От гепатита С во всем мире страдают по меньшей мере 200 млн человек.
В настоящее время проблемой хронической HCV-инфекции интересуются как врачи-специалисты, так и люди, никак не связанные с медициной.
От гепатита С во всем мире страдают по меньшей мере 200 млн человек. Последствиями перенесенного заболевания могут быть хронический гепатит, цирроз и первичный рак печени.
Эпидемиология
Распространенность хронической HCV-инфекции на земном шаре варьирует от 0,5 до 2%. Существуют регионы, для которых характерна более высокая распространенность этого заболевания: 6% в Заире и Саудовской Аравии, 16% в изолированных поселениях в Японии. В России наблюдается рост заболеваемости гепатитом С (3,2 на 100 тыс. населения в 1994 году и 19,3 в 1999 году). Источниками заражения вирусным гепатитом C служат больные острыми и хроническими формами HCV-инфекции, причем в основном это люди, у которых отсутствует желтуха и наблюдается бессимптомное или малосимптомное течение заболевания.
В настоящее время HCV чаще всего инфицируются молодые люди, преимущественно мужчины в возрасте около 20 лет, примерно 40% из них заражаются при внутривенном введении наркотиков. Основным путем инфицирования HCV является парентеральный. Так, у 6,1% больных, которым производилось переливание крови и ее компонентов во время кардиохирургических операций, развивался острый вирусный гепатит C, у 60% из них гепатит принимал хроническую форму.
Существует и риск заражения гепатитом C половым путем, однако он невелик (5-8%). Возможна передача HCV от матерей с острой или хронической формой инфекции; это также редкое явление, встречается не чаще чем в 5-6% случаев. Риск заражения вышеуказанными путями уступает таковому при гепатите В.
Приблизительно у половины больных путь инфицирования HCV установить не удается.
Вирус гепатита С
Вирус гепатита С относится к семейству флавивирусов. Геном вируса представлен однонитевой РНК протяженностью около 10 000 нуклеотидов. Вирус гепатита С вызывает заболевание только у человека. В экспериментальных условиях воспроизвести инфекцию можно у высших обезьян.
Определение генотипов вируса гепатита С имеет большое значение для практической медицины. Хотя до сих пор не установлено четкой корреляции между генотипами и уровнем виремии, характеристиками пациента, тяжестью течения заболевания, большинство исследователей соглашаются с выводами о значении генотипов вируса как важного фактора, влияющего на эффективность противовирусной терапии.
Вакцину против гепатита С создать пока не удалось из-за высокой изменчивости вируса гепатита С (ВГС).
Патогенез
Считают, что вирус оказывает прямое цитопатическое действие и вызывает иммуноопосредованное повреждение гепатоцитов. Высокая степень хронизации вирусного гепатита С обусловлена некоторыми особенностями действия вируса:
- возможностью внепеченочной репликации вируса, включая иммунокомпетентные клетки (клетки, предшественники гемопоэза, лимфоциты и моноциты периферической крови, миофибробласты);
- гетерогенностью генотипов и частыми мутациями генома вируса;
- индукцией каскада иммунопатологических реакций;
- активизацией процессов перекисного окисления липидов в печени.
В течении хронической HCV-инфекции может происходить нейтрализация мажорного варианта вируса, но тогда генерируются минорные варианты. Квазивиды HCV представляют собой движущуюся мишень, которую ограничивает иммунная система хозяина. Появление нового мажорного квазивида сопровождается повышением виремии и увеличением титра Ig M антител к вирусным белкам. Постепенно и этот новый мажорный вариант заменяется. Такой процесс приводит к периодической волнообразной виремии, сопровождающейся обострением хронического гепатита С (ХГС) и повышением уровня антител.
Возможно, антивирусному Т-клеточному ответу отведена центральная роль в элиминации ВГC, так как нейтрализующие антитела, по-видимому, очень часто оказываются неэффективными. Т-хелперные (Th) лимфоциты распознают вирусные антигенные пептиды, представленные HLA-комплексом II класса на поверхностной мембране антиген-презентирующих клеток. В зависимости от типа цитокинового профиля Th-клетки делятся на две группы: Th1 и Th2. Первые продуцируют IFNg и IL2, стимулируя Т-клеточный ответ и цитотоксическую Т-лимфоцитную активность, а вторые продуцируют IL4 и IL10, стимулируя В-клеточный ответ. Таким образом, Тh-лимфоциты играют существенную роль в регуляции иммунного ответа. У пациентов, у которых болезнь перешла в хроническую стадию, в острой фазе вирус-специфический Th ответ был ниже и преобладали цитокины типа Th2.
У хронически ВГC-инфицированных пациентов значительно увеличено содержание вирусоспецифических Th2-клеток и их цитокинов. Нарушение баланса Th1/Th2 цитокиновой продукции может играть важную роль в иммунопатогенезе хронической ВГC-инфекции. Показано снижение уровня IFNg и IL12 при ХГС. Этот дефицит является следствием повышенного уровня IL10, предполагаемого отрицательного регулятора для IFNg. Повышенное содержание Th2-клеток при ХГС может снижаться при комбинированной терапии рибавирином и IFNa. Обнаружено, что у пациентов с клинико-биохимическим улучшением после лечения IFNa произошло увеличение уровня Th1-цитокинов.
Цитотоксические лимфоциты (CTL) играют, по-видимому, некоторую роль в ограничении репликации ВГС. Этот ответ недостаточен для полной элиминации вируса при хронической инфекции и, кроме того, может вызывать повреждение печени. Известно, что CTL способны быстро опознавать и направленно лизировать клетки, несущие ВГC-антигены, не провоцируя значительного воспаления, с помощью перфоринового, FasL- и TNFα-базируемых механизмов.
ТNF, как предполагается, индуцируют апоптоз клеток, опосредуя высвобождение свободных радикалов из митохондриальных электронно-транспортных путей и модуляцию синтеза некоторых белков. Взаимодействие нуклеокапсидного белка ВГC с внутрицитоплазматической частью рецептора TNFb, вероятно, представляет собой эволюционно-отобранный механизм, с помощью которого вирус препятствует преждевременному апоптозу клетки-хозяина. В отсутствие доступных модельных клеточных культур прямая цитопатичность вируса гепатита С не может быть исследована в полном объеме.
В подавляющем большинстве случаев острого гепатита С иммунной системе не удается элиминировать вирус. До сих пор нет ясного представления о том, почему это происходит. Очевидно, ВГС обладает эволюционно-закрепленными способностями, обеспечивающими ему персистенцию.
Однако иммунная система может оказывать существенное влияние на ВГC-инфекцию. В 15% случаев острого гепатита С она эффективно уничтожает вирус, а у хронически ВГC-инфицированных обеспечивает умеренное ограничение инфекции в течение почти 20 лет. Возможно, ослабление какого-либо звена антивирусных иммунных механизмов позволяет вирусу активно воздействовать на иммунную систему. Длительная ВГC-персистенция может привести к развитию В-клеточных лимфопролиферативных нарушений, таких, как смешанная криоглобулинемия, злокачественная не-Ходжкинская лимфома и появление органоспецифических и неспецифических аутоантител. Таким образом, хроническую ВГC-инфекцию следует рассматривать как мультисистемное заболевание.
Диагностика
Лабораторная диагностика гепатита С основана на выявлении специфических маркеров инфицирования ВГС (анти-ВГС-IgM/G, РНК ВГС) и должна проводиться разрешенными МЗ РФ к применению диагностическими препаратами отечественного или зарубежного производства в лабораториях, имеющих лицензию на проведение данного вида лабораторных исследований.
HCV RNA — самый ранний маркер репликации вируса, определяемый с помощью полимеразной цепной реакции (ПЦР) спустя несколько недель после заражения. Для выявления анти-ВГС применяют иммуноферментный анализ (ИФА). В настоящее время используют тест-системы третьего поколения ELISA-3. Подтверждающим методом является рекомбинантный иммуноблотинг (RIBA). У 60% больных анти-ВГС определяются в острой фазе, у 35% они появляются спустя 3-6 месяцев после инфицирования, у 5% инфицированных лиц анти-ВГС не определяются.
Болезнь может протекать бессимптомно. Наиболее распространенным симптомом является слабость. Целенаправленный опрос больных часто помогает выявить такие факторы риска, как переливание крови, внутривенное введение наркотиков, хронический гемодиализ и др. Кроме слабости больной может жаловаться на быструю утомляемость, тяжесть в правом подреберье, боли в правом верхнем квадранте живота, диспепсические явления.
Критериями постановки диагноза являются увеличение печени и селезенки, гиперферментемия и анти-ВГС в крови в течение не менее 6 месяцев.
Гепатоспленомегалия выявляется не более чем у 50% обратившихся за помощью больных, активность сывороточных трансаминаз редко превышает верхнюю границу нормы в 6 раз. Следует обратить внимание на то, что активность сывороточных трасаминаз не отражает степени изменений в печени: она может быть нормальной, несмотря на значительные морфологические изменения. Концентрация РНК ВГС в сыворотке имеет существенное значение для определения контагиозности и для мониторинга результатов лечения. При наличии в крови HCV-РНК биопсия печени, как правило, выявляет ряд изменений. Концентрация HCV-РНК в сыворотке, превышающая 105 молекулярных эквивалентов (копий) в 1 мл, наблюдается в активной фазе заболевания и совпадает с пиками активности трансаминаз.
Наличие или отсутствие РНК ВГС, как правило, не является диагностическим критерием хронического гепатита С и определяет фазу процесса (активный, неактивный).
Для раннего выявления ГЦК у больных циррозом печени, особенно у мужчин старше 40 лет, каждые 6 месяцев определяют уровень сывороточного α-фетопротеина и выполняют УЗИ печени.
Естественное течение и прогноз
Инфицирование ВГС приводит к развитию острого гепатита С, протекающего в манифестной (желтушной) или чаще в латентной (безжелтушной) формах, которые развиваются в соотношении 1:6. Около 17-25% больных острым гепатитом С выздоравливают спонтанно, у остальных 75-83% развивается хронический гепатит С. Большинство больных с биохимическими и иммунологическими признаками хронического гепатита имеют слабовыраженную или умеренную степень воспалительно-некротического поражения печени и минимально выраженный фиброз. Примерно у 26-35% больных хроническим гепатитом С в течение 10-40 лет развивается фиброз печени и может наступить смерть от цирроза печени и его осложнений. У 30-40% больных с циррозом печени высок риск заболевания раком печени.
Считается, что не более чем у 30% больных ВГС с минимальной морфологической активностью через 20 лет возможно развитие цирроза печени. Таким образом, больные, у которых при гистологическом исследовании биоптата печени выявляется наличие минимального воспаления и минимального фиброза, нуждаются в динамическом наблюдении.
Если персистенция РНК ВГС сохраняется более 6 месяцев, то спонтанное разрешение хронической HCV-инфекции маловероятно.
Клиническая картина
У большинства больных с хроническим гепатитом С заболевание протекает бессимптомно. Если жалобы существуют, то это чаще всего слабость, тупые боли в правом подреберье, тошнота, снижение аппетита, кожный зуд, артралгии и миалгии. Физикальный осмотр пациента помогает установить диагноз зачастую только на стадии цирроза печени.
Внепеченочные проявления HCV-инфекции
Ассоциация хронического гепатита С с различными внепеченочными проявлениями — хорошо известный врачам факт. Наиболее вероятным для большинства заболеваний и синдромов, наблюдаемых при HCV-инфекции, представляется иммунный патогенез, хотя конкретные механизмы во многом еще не выяснены. Доказанные и предполагаемые иммунные механизмы включают:
- моно- или поликлональную пролиферацию лимфоцитов;
- образование аутоантител;
- отложение иммунных комплексов;
- секрецию цитокинов.
Частота иммуноопосредованных заболеваний и синдромов у больных хроническим гепатитом С достигает 23%. Наиболее характерны аутоиммунные проявления для больных с гаплотипом HLA DR4, который ассоциируется с внепеченочными проявлениями при аутоиммунном гепатите. Этот факт подтверждает гипотезу о триггерной роли вируса в инициации аутоиммунных процессов у генетически предрасположенного индивидуума.
Заболевания, ассоциированные с HCV-инфекцией
Ассоциированные с продукцией или отложением иммуноглобулинов:
- Криоглобулинемия
- Лейкоцитокластерный васкулит
- Мембранозно-пролиферативный гломерулонефрит
- В-клеточная лимфома
- Плазмоцитома
- MALTома
- Тиреоидит
- Синдром Шегрена
- Гемолитическая анемия
- Тромбоцитопения
- Красный плоский лишай
Ассоциированные с неизвестным механизмом:
Выявление сывороточных аутоантител отражает наиболее частый феномен аутоиммунизации при HCV-инфекции, который диагностируют у 40-65% больных. Спектр аутоантител достаточно широк и включает ANA (до 28%), SMA (до 11%), анти-LKM-1 (до 7%), антифосфолипидные (до 25%), антитиреоидные (до 12,5%), ревматоидный фактор, анти-ASGP-R и др. Чаще всего титры этих антител не достигают диагностических значений, показательных для той или иной аутоиммунной патологии.
Анти-GOR являются антителами, специфичными для HCV-инфекции, и их выявляют не менее чем у 80% больных. Эпитоп, распознаваемый анти-GOR, локализуется на пока неидентифицированном ядерном белке, гиперэкспрессию которого наблюдают при гепатоцеллюлярной карциноме. Выработка анти-GOR ассоциирована только с HCV-инфекцией, но не с АИГ.
Аутоиммунные расстройства наблюдаются в среднем у 23% больных хроническим гепатитом С. Наиболее часто встречаются патология щитовидной железы.
Гистологическое исследование печени
Гистологическая картина не является патогномоничной, при этом достаточно часто выявляются характерные изменения. Отличительная особенность ее — лимфоидные агрегаты или фолликулы в портальных трактах, которые могут быть как изолированными, так и частью воспалительных изменений портальных трактов. По клеточному составу эти агрегаты напоминают первичные лимфоидные фолликулы в лимфатических узлах. Жировая дистрофия обнаруживается в 75% случаев. Кроме того, выявляются следующие характерные изменения: негнойный холангит с лимфоидной и плазмоклеточной инфильтрацией стенок протоков; лимфогистиоцитарная инфильтрация перипортальной зоны; слабовыраженные ступенчатые некрозы; мостовидные некрозы (обнаруживаются редко), пролиферация и активация сателлитных клеток печени, пролиферация эпителия желчных канальцев.
Отмечено, что индекс гистологической активности (ИГА) и индекс фиброза (ИФ) у больных хроническим гепатитом С с наличием жировой дистрофии достоверно выше, чем у пациентов без сопутствующей жировой дистрофии. У 93% больных с жировой дистрофией в гепатоцитах обнаруживался Core-протеин ВГС, при отсутствии жировой дистрофии — лишь у 39%. Этим фактом подчеркивается роль Core-протеина в развитии жировой дистрофии гепатоцитов.
Биопсия печени играет существенную роль в уточнении диагноза и оценке активности и стадии заболевания.
РНК ВГС можно определить в ткани печени методом ПЦР.
Лечение
Основная цель лечения — предотвратить прогрессирование заболевания.
Режим отдыха, диета и прием витаминов не оказывают лечебного действия.
Отбор пациентов для лечения. Показанием к назначению терапии интерфероном служит умеренное (но не минимальное) либо тяжелое воспаление и/или фиброз. Решение о лечении пациентов с циррозом печени принимают индивидуально в каждом конкретном случае. Больные, у которых гистологическая активность минимальна, должны находиться под динамическим наблюдением, так как они имеют хороший жизненный прогноз без лечения и очень низкий риск развития цирроза печени через 10-20 лет.
Факторы, связанные с благоприятным эффектом противовирусной терапии при хронической HCV-инфекции:
- Возраст моложе 45 лет
- Женский пол
- Отсутствие ожирения
- Срок инфицирования менее 5 лет
- Отсутствие коинфекции HBV
- Отсутствие иммунодепрессии
- Отсутствие алкоголизма
- Умеренное повышение АЛТ
- Отсутствие цирроза
- Низкое содержание железа в печени
- Низкий уровень HCV RNA в сыворотке
- Генотип 2 или 3
- Однородность популяции вируса
Больным с нормальным уровнем АЛТ и положительным тестом на HCV RNA без результатов гистологического исследования противовирусное лечение проводить не рекомендуется.
Основной препарат, эффективность которого в лечении гепатита С доказана, — это интерферон альфа (ИФα).
В настоящее время принята оптимальная схема монотерапии ИФ: разовая доза составляет 3 млн МЕ, ее вводят подкожно или внутримышечно 3 раза в неделю в течение 3 месяцев. Через 3 месяца необходимо исследовать РНК ВГС. Если результаты ПЦР положительные схему лечения меняют. Если же РНК не выявляется, лечение продолжают до 12 месяцев. Стойкий положительный ответ в этом случае регистрируется у 15-20% больных.
Оптимальная схема лечения хронического гепатита С в настоящее время — это комбинация ИФa и рибавирина.
- в течение 6 месяцев - при генотипах 2 и 3;
- в течение 6 месяцев - при генотипе 1 и низком уровне виремии;
- в течение 12 месяцев - при генотипе 1 и высоком уровне виремии.
Стойкий положительный ответ при комбинированном лечении ИФa с рибавирином наблюдается в 40-60% случаев.
Суточная масса рибавирина составляет 1000-1200 мг в зависимости от массы тела.
В последние годы для повышения эффективности интерферона применяют пегилирование, которое заключается в присоединении к молекуле интерферона полиэтиленгликоля. В итоге образуется ПЭГ-интерферон, имеющий более длительный период полураспада. Предварительные данные свидетельствуют о большей эффективности такого лечения по сравнению с терапией интерфероном альфа.
Другие противовирусные препараты в лечении хронического гепатита С
Имеются данные, свидетельствующие о положительном действии таких препаратов, как ремантадин, урсодеоксихолевая кислота, пегилированные интерфероны, препараты глициризиновой кислоты, однако эта информация нуждается в дальнейшей проверке.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Гепатит С: причины появления, классификация, симптомы, диагностика и способы лечения.
Определение
Гепатит С – это вирусное инфекционное заболевание, которое вызывает воспаление печени, зачастую приводя к ее серьезным повреждениям. Вирус гепатита С распространяется через зараженную кровь.
До недавнего времени лечение гепатита С требовало еженедельных инъекций и приема пероральных препаратов, которые многие люди, инфицированные вирусом, не могли использовать из-за других проблем со здоровьем или серьезных побочных эффектов.
Сегодня ситуация изменилась – разработаны лекарства нового поколения, и с их помощью хронический гепатит С поддается терапии.
Тем не менее около половины людей с гепатитом С не подозревают о том, что инфицированы, поскольку часто болезнь протекает бессимптомно.
Поэтому скрининг гепатита С необходимо проходить регулярно, особенно при наличии факторов риска заражения.
Причины появления гепатита С
Заболевание обычно распространяется, когда кровь человека, зараженного вирусом гепатита С, попадает в организм незараженного. Особенно часто это происходит в среде наркоманов.
В группе риска находятся люди, которым часто переливают кровь, и длительное время находящиеся на гемодиализе.
Заражению подвержены новорожденные дети, если их мать больна гепатитом С.
Кроме того, существуют редкие, но все же возможные ситуации инфицирования вирусом:
- Совместное использование предметов личной гигиены, которые могли соприкасаться с кровью больного человека (бритвы, ножницы или зубные щетки).
- Половой контакт с человеком, зараженным вирусом гепатита С.
- Татуировки или пирсинг, выполненные в ненадлежащих санитарных условиях.
Вирус гепатита С не передается при совместном использовании столовых приборов, кормлении грудью, объятиях, поцелуях, при держании за руку, кашле или чихании, через укусы насекомых. Также он не распространяется через еду или воду.
- Острый гепатит С – это ранняя стадия, когда гепатит длится менее шести месяцев.
- Хронический гепатит С – это долгосрочный тип, когда заболевание длится больше шести месяцев.
- Минимальная активность (печеночные трансаминазы (АЛТ и АСТ) в биохимическом анализе крови повышены не более, чем на 3 нормы)).
- Умеренная активность (3–10 норм печеночных трансаминаз).
- Высокая активность (> 10 норм).
В течение первых 6 месяцев от начала заболевания человек может даже не подозревать, что болен, ощущая лишь необъяснимую усталость, плохой аппетит, тяжесть в правом подреберье, регулярную головную боль и головокружение.
В этот же период может меняться цвет кала (от светлого вплоть до белого) и мочи (от темно-желтой до коричневой). Некоторые пациенты говорят, что у них болят суставы.
По мере прогрессирования заболевания к первоначальным симптомам присоединяются спонтанные кровотечения (носовые, маточные, кровотечения из десен), желтушность кожных покровов, склонность к образованию гематом, зуд, накопление свободной жидкости в брюшной полости (асцит), отеки ног. Кроме того, пациенты начинают терять вес, снижается память, появляются проблемы со зрением, на коже формируются сосудистые звездочки.
У мужчин может отмечаться гинекомастия (увеличение грудных желез), снижение либидо, уменьшение размера яичек.
Симптомы острого гепатита С включают желтуху, усталость, тошноту, жар и мышечные боли. Они появляются через 1-3 месяца после инфицирования вирусом и продолжаются от двух недель до трех месяцев.
Диагностика гепатита С
Диагноз ставится на основании жалоб больного и анамнеза. При подозрении на вирусный гепатит С врач обязательно выясняет, были ли в течение жизни переливания крови, хирургические манипуляции, не употреблял ли пациент инъекционные наркотики, делал ли татуировки и пирсинг, имели ли место незащищенные половые контакты.
Для уточнения диагноза могут понадобиться следующие обследования:
-
Клинический анализ крови с развернутой лейкоцитарной формулой.
Синонимы: Общий анализ крови, ОАК. Full blood count, FBC, Complete blood count (CBC) with differential white blood cell count (CBC with diff), Hemogram. Краткое описание исследования Клинический анализ крови: общий анализ, лейкоформула, СОЭ См. также: Общий анализ – см. тест № 5, Лейкоцит.
Проблема вирусных гепатитов сохраняет актуальность уже на протяжении многих десятилетий. Инфицирование вирусами гепатита В, С, D в большинстве случаев регистрируется среди лиц трудоспособного возраста и у части пациентов может приводить к хронизации процесса. При гепатитах любого генеза нарушаются все виды обмена веществ. Не является исключением в этом отношении и обмен микроэлементов [2]. В литературных источниках описывается нарушение обмена железа при хроническом вирусном гепатите в виде перегрузки железом [4]. Изменения метаболизма железа при хронических вирусных гепатитах рассматриваются как неблагоприятные для течения и прогноза заболевания, а также эффективности противовирусной терапии [5, 6].
Изучение обмена железа при вирусных гепатитах представляет значительный интерес и диктуется необходимостью поиска новых тестов, отражающих направленность патологического процесса, влияния на него применяемой терапии, решения вопросов дифференциальной диагностики и трудовой экспертизы.
Цель исследования: Выявить закономерности изменения уровня железа в сыворотке крови при вирусных гепатитах в динамике патологического процесса.
Пациенты обследованы в соответствии со стандартами оказания специализированной помощи больным вирусными гепатитами. Все отобранные больные имели среднетяжелое течение инфекции с индикацией маркеров вирусных гепатитов методами ИФА, ПЦР. По анамнестическим данным больные поступали в стационар на 5-7 сутки от начала заболевания. По клиническим и лабораторным показателям группы пациентов были сопоставимы.
Все больные получали только базисную терапию, входящую в стандарты оказания специализированной медицинской помощи, которая включала полупостельный режим, стол № 5, симптоматическую и патогенетическую терапию, внутривенную инфузионную терапию (5%-ный раствор глюкозы, раствор Рингера).
Уровень железа определялся при поступлении, в динамике заболевания (чаще на 14 день пребывания в стационаре) и перед выпиской (на 21-28 день пребывания в стационаре).
Статистическую обработку результатов исследования проводили путем вычисления средней арифметической (M) и ошибки средней (m). Для установления статистической достоверности различий в сравниваемых величинах мы использовали математический метод построения динамических рядов и параметрический критерий Стьюдента. За уровень достоверности принималась вероятность различия = 95% (p
ГОРОДА: Москва, Санкт-Петербург, Новосибирск, Екатеринбург, Нижний Новгород, Казань, Самара, Челябинск, Омск, Ростов-на-Дону, Уфа, Красноярск, Пермь, Волгоград, Воронеж, Владивосток, Ярославль, Обнинск, Калининград, Орел, Тюмень, Томск, Тамбов, Тверь, Улан-Удэ, Смоленск, Саранск, Сочи, Ставрополь, Сыктывкар, Рязань, Пенза, Оренбург, Набережные Челны, Новгород Великий, Новороссийск, Магадан, Магнитогорск, Липецк, Калуга, Кемерово, Краснодар, Ижевск, Иваново, Иркутск, Забайкальск, Владимир, Вологда, Белгород, Брянск
Инновационный Центр Развития Образования и Науки © 2013 - 2022 гг. Все права защищены
Использование материала сайта разрешено только при наличии активной ссылки на источник.
Читайте также:

