В состав вирусов обязательно входит днк да или нет
Обновлено: 24.04.2024
Химический состав вирусов. Вирусные геномы. Виды вирусных геномов.
Химический состав вирусов отличается от других форм жизни необычайной простотой. Кроме геномной ДНК или РНК вирусы позвоночных содержат белки, масса которых составляет 57—90% массы вириона. Количество вирионных белков может колебаться в широких пределах в зависимости от сложности строения вируса. Среди белков, кодируемых вирусным геномом, различают структурные и неструктурные вирусспецифические белки. Первые входят в структуру вириона, вторые не входят. Структурными белками являются капсидные белки, белки оболочки и в некоторых случаях белки тегумента и ферменты.
У многих вирусов некоторые структурные вирусные белки не являются первичными продуктами генов, а образуются в результате посттрансляционного расщепления полипептида-предшественника вирусспецифическими и клеточными протеазами.
Неструктурными вирусными белками являются белки, кодируемые вирусным геномом, но не являющиеся составными частями вириона. Одни из них участвуют в репликации вирусных компонентов, другие — в сборке вирионов, третьи нарушают нормальный клеточный синтез. Они включают различные типы репликаз, связанные с репликацией ДНК, транскриптазы, транскрибирующие мРНК на геномной дцДНК или дцРНК или (-)оцРНК, вирусные протеазы, геликазы и лигазы. У ретро- и гепаднавирусов найдена обратная транскриптаза, транскрибирующая ДНК на матрице РНК. У ретровирусов найден уникальный фермент, участвующий в интеграции ДНК-продукта в хромосомальную ДНК клетки. Вирусы оспы, которые размножаются в цитоплазме и имеют много уникальных ферментов для процессинга РНК-транскриптов и репликации вирусной ДНК, мало зависят от метаболизма клетки. Вирусные белки имеют молекулярную массу 5-200 кД. Наиболее просто устроенные вирусы (вирусы-сателлиты, дефектные вирусы) кодируют синтез только одного белка, многие патогенные вирусы кодируют синтез 5—10 белков, крупные вирусы, такие как вирусы оспы, герпесвирусы, кодируют синтез до 200 белков. Хотя это немного по сравнению с клетками прои эукариотов (кодируют соответственно более 5000 и 100000 белков).
Разные вирусы демонстрируют различные варианты стратегии экспрессии своих генов и репликации геномов.
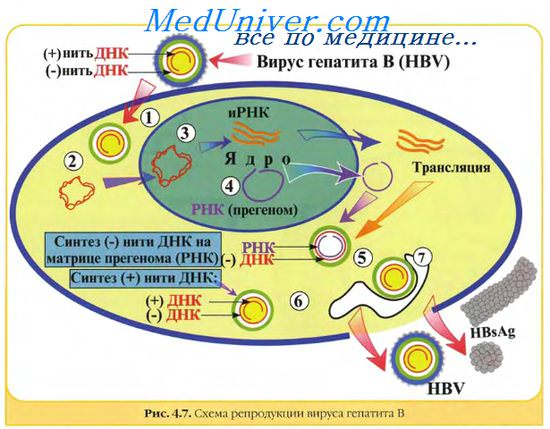
Вирусные геномы. Виды вирусных геномов.
Все вирусные геномы являются гаплоидными, т.е. содержат одну копию каждого гена. Исключение составляют ретровирусы, которые обладают диплоидным геномом. Геномы ДНК-вирусов позвоночных представлены одной двуспиральной молекулой за исключением парво- и цирковирусов.
Геномы полиома-, папиллома-, гепадна- и цирковирусов представлены кольцевой ДНК. ДНК гепаднавирусов частично двуспиральная, частично односпиральная. ДНК вирусов полиомы и папилломы является суперспиральной. Большинство линейных вирусных ДНК обладает способностью приобрести циркулярную конфигурацию, которая требуется для репликации по вращающемуся кольцевому механизму. Две цепи ДНК вируса оспы ковалентно связаны своими концами и при денатурации образуют большое одноцепочечное кольцо. У некоторых ДНК-вирусов (так же как у РНК-ретровирусов) имеются концевые повторяющиеся последовательности. Инвертированные концевые повторы обнаружены у адено- и парвовирусов. У адено-, гепадна- и парвовирусов, так же как у некоторых РНК-вирусов (пикорна- и калицивирусов), с 5'-концом генома ковалентно связан белок, играющий важную роль в его репликации.
Все РНК-вирусы позвоночных за исключением рео- и бирнавирусов имеют одноцепочечные геномы. Геном некоторых РНК-вирусов состоит из нескольких (2-12) уникальных фрагментов, каждый из которых кодирует, как правило, один белок. РНК-вирусы с односпиральным геномом могут иметь различную полярность. Если они имеют ту же полярность, что и мРНК, то они могут прямо индуцировать синтез вирусного белка и считаются положительно (+) полярными.
Если геномная нуклеотидная последовательность комплементарна мРНК, то они считаются отрицательно (—) полярными. К ним относятся: парамиксо-, рабдо-, фило-, ортомиксо-, арена- и буньявирусы. Все они имеют вирионную РНК-зависимую полимеразу (транскриптазу), которая в инфицированной клетке транскрибирует положительно-полярную РНК на матрице геномной вирусной РНК. У аренавирусов, по крайней мере, у одного рода буньявирусов, один из РНК-сегментов является двуполярным. Обычно у (+)полярных РНК-вирусов З'-конец имеет polyA-последовательность, а 5'-конец имеет кэп-структуру.
Размер геномов РНК-вирусов (одноцепочечных 1,7—21 т.н.; двуцепочечных — 18—27 т.п.н.) значительно меньше размера генома многих ДНК-вирусов. Поэтому РНК-вирусы, как правило, кодируют меньше белков, чем ДНК-вирусы. Масса генома различных вирусов находится в пределах от 1 % (орто- и пара-миксовирусы) до 32% (парвовирусы) от массы вириона.
Различные семейства вирусов позвоночных значительно различаются по структуре и функции генома. Основные типы вирусных геномов можно представить следующим образом:
1) двуцепочечной линейной молекулой ДНК с открытыми (герпесвирусы, аденовирусы, иридовирусы) или ковалентно связанными концами (вирусы оспы, асфаровирусы);
2) одноцепочечной линейной молекулой ДНК (парвовирусы);
3) одноцепочечной кольцевой молекулой ДНК (цирковирусы);
4) двуцепочечной кольцевой молекулой ДНК (папилломавирусы, полиомавирусы);
5) частично двуцепочечной кольцевой незамкнутой молекулой ДНК (гепаднавирусы);
6) одноцепочечной молекулой РНК, являющейся мРНК (положительно-геномные вирусы: пикорнавирусы, тогавирусы, флавивирусы, астровирусы, калицивирусы, коронавирусы, артеривирусы, нодавирусы);
7) одноцепочечной единой (рабдовирусы, парамиксовирусы, филовирусы, бор-навирусы) или фрагментированнои (ортомиксовирусы) линейной молекулой РНК, комплементарной мРНК — отрицательно-геномные вирусы;
8) одноцепочечной фрагментированнои кольцевой ковалентно несвязанной отрицательной или двуполярной РНК (буньявирусы, аренавирусы);
9) двуцепочечной линейной фрагментированнои молекулой РНК (реовирусы, бирнавирусы);
10) двумя идентичными линейными молекулами плюс-РНК, являющимися матрицами для синтеза ДНК (ретровирусы).
Молекулярная масса ДНК различных вирусов позвоночных варьирует в широких пределах: от 0,7—1,5 МД у цирковирусов и парвовирусов, до 150—200 МД у вирусов оспы. Молекулярная масса генома у РНК вирусов колеблется менее значительно - от 2,0 до 20,0 МД.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
ДНК-вирусы. Этапы репликации вирусов с ДНК геномом.
Оспо-, асфаро- и иридовирусы имеют вирионную транскриптазу (ДНК-зависимую РНК-полимеразу) и размножаются в цитоплазме. Их очень большие геномы кодируют многочисленные ферменты, которые делают их репликацию независимой от клеточного ядра. Моноцистронные мРНК транскрибируются непосредственно на вирусной ДНК.
После разрушения наружной оболочки вириона клеточными ферментами на вирусной ДНК с помощью вирионной ДНК-зависимой РНК-полимеразы синтезируются ранние мРНК. Они транслируются в вирусные белки с помощью которых вирионная ДНК полностью освобождается от белка и реплицируется по полуконсервативному механизму. Вначале синтезируются фрагменты ДНК (фрагменты Оказаки), которые затем соединяются с образованием зрелых вирусных ДНК.
Поздние моно- и полицистронные мРНК транскрибируются после начала репликации вирусной ДНК и кодируют синтез структурных белков вириона. Иридовирусы и асфаровирусы, по-видимому, обладают сходной с вирусами оспы стратегией репликации.
Герпес-, адено-, папиллома и полиомавирусы в одном отношении имеют общую стратегию репликации: вирусная ДНК транскрибируется в ядре клеточной ДНК-зависимой РНК-полимеразой II. В течение определенного промежутка времени проходит два или более циклов транскрипции различных генных единиц (групп генов под контролем одного промотора). Субгеномные полицистронные РНК-транскрипты подвергаются расщеплению и сплайсингу, превращаясь в моноцистронные мРНК.
У папиллома- и полиомавирусов транскрипционная программа состоит по крайней мере из двух циклов (ранние и поздние мРНК), а у герпес- и аденовирусов по крайней мере из трех (сверхранние, ранние и поздние мРНК). В каждом случае вирионные полипептиды синтезируются на мРНК, появляющейся в последнем цикле транскрипции (поздние мРНК). ДНК аденовирусов, папиллома- и полиомавирусов может встраиваться в геном клетки-хозяина, реплицироваться вместе с ним, передаваться дочерним клеткам и транслироваться с образованием вирусных белков.
Парво- и цирковирусы, обладающие оцДНК, реплицируются в ядре. Эти вирусы используют клеточные ДНК-полимеразы для синтеза двуспиральной ДНК, которая затем транскрибируется в ядре клеточной ДНК-зависимой РНК-полимеразой II. Синтезированные транскрипты подвергаются сплайсингу и превращаются в мРНК.
Вирионная ДНК служит матрицей для синтеза (+) и (-)ДНК. Последние включаются в вирионы в качестве генома.
Различают недефектные (автономные) и дефектные парвовирусы. Первые размножаются самостоятельно, тогда как вторые реплицируются только в присутствии вируса-помощника, которым является любой аденовирус или вирус простого герпеса. В связи с этим дефектные парвовирусы называют аденоассоциированными вирусами (ААВ). В вирионах недефектных парвовирусов содержится односпиральная линейная (+)ДНК. Дефектные парвовирусы являются уникальными в мире вирусов, поскольку комплементарные плюс- и минус-ДНК входят в различные вирионы.
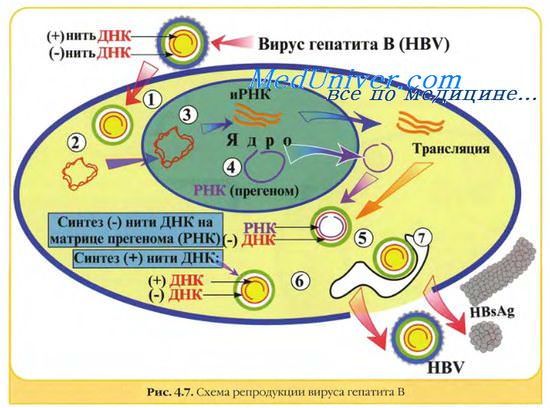
Гепаднавирусы. Частично двуцепочечная ДНК генома гепаднавирусов с помощью вирионной ДНК-полимеразы превращается в суперспирализованную двуцепочечную ДНК. Затем с помощью клеточной РНК-полимеразы II образуются мРНК для вирусных белков, в том числе для обратной транскриптазы, и полноразмерная (+)РНК, которая служит матрицей для обратной вирусной транскрипции с образованием (-)ДНК, на которой в свою очередь синтезируется частично двуцепочечная ДНК. мРНК транскрибируется на двуцепочечной ДНК, стартуя от различных промоторов.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.

Обзор
Автор
Редакторы
Обратите внимание!
Спонсоры конкурса: Лаборатория биотехнологических исследований 3D Bioprinting Solutions и Студия научной графики, анимации и моделирования Visual Science.
Эволюция и происхождение вирусов
В 2007 году сотрудники биологического факультета МГУ Л. Нефедова и А. Ким описали, как мог появиться один из видов вирусов — ретровирусы. Они провели сравнительный анализ геномов дрозофилы D. melanogaster и ее эндосимбионта (микроорганизма, живущего внутри дрозофилы) — бактерии Wolbachia pipientis. Полученные данные показали, что эндогенные ретровирусы группы gypsy могли произойти от мобильных элементов генома — ретротранспозонов. Причиной этому стало появление у ретротранспозонов одного нового гена — env, — который и превратил их в вирусы. Этот ген позволяет вирусам передаваться горизонтально, от клетки к клетке и от носителя к носителю, чего ретротранспозоны делать не могли. Именно так, как показал анализ, ретровирус gypsy передался из генома дрозофилы ее симбионту — вольбахии [7]. Это открытие упомянуто здесь не случайно. Оно нам понадобится для того, чтобы понять, чем вызваны трудности борьбы с вирусами.
Из давних письменных источников, оставленных историком Фукидидом и знахарем Галеном, нам известно о первых вирусных эпидемиях, возникших в Древней Греции в 430 году до н.э. и в Риме в 166 году. Часть вирусологов предполагает, что в Риме могла произойти первая зафиксированная в источниках эпидемия оспы. Тогда от неизвестного смертоносного вируса по всей Римской империи погибло несколько миллионов человек [8]. И с того времени европейский континент уже регулярно подвергался опустошающим нашествиям всевозможных эпидемий — в первую очередь, чумы, холеры и натуральной оспы. Эпидемии внезапно приходили одна за другой вместе с перемещавшимися на дальние расстояния людьми и опустошали целые города. И так же внезапно прекращались, ничем не проявляя себя сотни лет.
Вирус натуральной оспы стал первым инфекционным носителем, который представлял действительную угрозу для человечества и от которого погибало большое количество людей. Свирепствовавшая в средние века оспа буквально выкашивала целые города, оставляя после себя огромные кладбища погибших. В 2007 году в журнале Национальной академии наук США (PNAS) вышла работа группы американских ученых — И. Дэймона и его коллег, — которым на основе геномного анализа удалось установить предположительное время возникновения вируса натуральной оспы: более 16 тысяч лет назад. Интересно, что в этой же статье ученые недоумевают по поводу своего открытия: как так случилось, что, несмотря на древний возраст вируса, эпидемии оспы не упоминаются в Библии, а также в книгах древних римлян и греков [9]?
Строение вирусов и иммунный ответ организма

Рисунок 1. Первооткрыватель вирусов Д.И. Ивановский (1864–1920) (слева) и английский врач Эдвард Дженнер (справа).

Почти все известные науке вирусы имеют свою специфическую мишень в живом организме — определенный рецептор на поверхности клетки, к которому и прикрепляется вирус. Этот вирусный механизм и предопределяет, какие именно клетки пострадают от инфекции. К примеру, вирус полиомиелита может прикрепляться лишь к нейронам и потому поражает именно их, в то время как вирусы гепатита поражают только клетки печени. Некоторые вирусы — например, вирус гриппа А-типа и риновирус — прикрепляются к рецепторам гликофорин А и ICAM-1, которые характерны для нескольких видов клеток. Вирус иммунодефицита избирает в качестве мишеней целый ряд клеток: в первую очередь, клетки иммунной системы (Т-хелперы, макрофаги), а также эозинофилы, тимоциты, дендритные клетки, астроциты и другие, несущие на своей мембране специфический рецептор СD-4 и CXCR4-корецептор [13–15].

Одновременно с этим в организме реализуется еще один, молекулярный, защитный механизм: пораженные вирусом клетки начинают производить специальные белки — интерфероны, — о которых многие слышали в связи с гриппозной инфекцией. Существует три основных вида интерферонов. Синтез интерферона-альфа (ИФ-α) стимулируют лейкоциты. Он участвует в борьбе с вирусами и обладает противоопухолевым действием. Интерферон-бета (ИФ-β) производят клетки соединительной ткани, фибробласты. Он обладает таким же действием, как и ИФ-α, только с уклоном в противоопухолевый эффект. Интерферон-гамма (ИФ-γ) синтезируют Т-клетки (Т-хелперы и (СD8+) Т-лимфоциты), что придает ему свойства иммуномодулятора, усиливающего или ослабляющего иммунитет. Как именно интерфероны борются с вирусами? Они могут, в частности, блокировать работу чужеродных нуклеиновых кислот, не давая вирусу возможности реплицироваться (размножаться).

Причины поражений в борьбе с ВИЧ
Тем не менее нельзя сказать, что ничего не делается в борьбе с ВИЧ и нет никаких подвижек в этом вопросе. Сегодня уже определены перспективные направления в исследованиях, главные из которых: использование антисмысловых молекул (антисмысловых РНК), РНК-интерференция, аптамерная и химерная технологии [12]. Но пока эти антивирусные методы — дело научных институтов, а не широкой клинической практики*. И потому более миллиона человек, по официальным данным ВОЗ, погибают ежегодно от причин, связанных с ВИЧ и СПИДом.

Подобный вирусный механизм характерен не только для ВИЧ. Он описан и при инфицировании некоторыми другими опасными вирусами: такими, как вирусы Денге и Эбола. Но при ВИЧ антителозависимое усиление инфекции сопровождается еще несколькими факторами, делая его опасным и почти неуязвимым. Так, в 1991 году американские клеточные биологи из Мэриленда (Дж. Гудсмит с коллегами), изучая иммунный ответ на ВИЧ-вакцину, обнаружили так называемый феномен антигенного импринтинга [23]. Он был описан еще в далеком 1953 году при изучении вируса гриппа. Оказалось, что иммунная система запоминает самый первый вариант вируса ВИЧ и вырабатывает к нему специфические антитела. Когда вирус видоизменяется в результате точечных мутаций, а это происходит часто и быстро, иммунная система почему-то не реагирует на эти изменения, продолжая производить антитела к самому первому варианту вируса. Именно этот феномен, как считает ряд ученых, стоит препятствием перед созданием эффективной вакцины против ВИЧ.

Открытие биологов из МГУ — Нефёдовой и Кима, — о котором упоминалось в самом начале, также говорит в пользу этой, эволюционной, версии.

Сегодня не только ВИЧ представляет опасность для человечества, хотя он, конечно, самый главный наш вирусный враг. Так сложилось, что СМИ уделяют внимание, в основном, молниеносным инфекциям, вроде атипичной пневмонии или МЕRS, которыми быстро заражается сравнительно большое количество людей (и немало гибнет). Из-за этого в тени остаются медленно текущие инфекции, которые сегодня гораздо опаснее и коварнее коронавирусов* и даже вируса Эбола. К примеру, мало кто знает о мировой эпидемии гепатита С, вирус которого был открыт в 1989 году**. А ведь по всему миру сейчас насчитывается 150 млн человек — носителей вируса гепатита С! И, по данным ВОЗ, каждый год от этой инфекции умирает 350-500 тысяч человек [33]. Для сравнения — от лихорадки Эбола в 2014-2015 гг. (на состояние по июнь 2015 г.) погибли 11 184 человека [34].
* — Коронавирусы — РНК-содержащие вирусы, поверхность которых покрыта булавовидными отростками, придающими им форму короны. Коронавирусы поражают альвеолярный эпителий (выстилку легочных альвеол), повышая проницаемость клеток, что приводит к нарушению водно-электролитного баланса и развитию пневмонии.

Рисунок 8. Электронная микрофотография воссозданного вируса H1N1, вызвавшего эпидемию в 1918 г. Рисунок с сайта phil.cdc.gov.
Почему же вдруг сложилась такая ситуация, что буквально каждый год появляются новые, всё более опасные формы вирусов? По мнению ученых, главные причины — это сомкнутость популяции, когда происходит тесный контакт людей при их большом количестве, и снижение иммунитета вследствие загрязнения среды обитания и стрессов. Научный и технический прогресс создал такие возможности и средства передвижения, что носитель опасной инфекции уже через несколько суток может добраться с одного континента на другой, преодолев тысячи километров.

Обзор
Человеческая Т-клетка (синий), атакованная ВИЧ (желтый). Вирус ориентирован на Т-клетки, которые играют важную роль в иммунной реакции организма против вторжений, таких как бактерии и вирусы.
Автор
Редакторы

Вопрос о происхождении вирусов
Существует три основные теории возникновения вирусов:
Зарождение жизни. Идея последнего универсального общего предка: каким он мог бы быть и что ему предшествовало?

Рисунок 1. Схема трехдоменной классификации, предложенная Вёзе. В основании этой схемы должен находиться последний универсальный общий предок (англ. last universal common ancestor, LUCA).
Самый сильный аргумент в пользу существования LUCA — сохранившаяся общая система экспрессии генов (передачи наследственной информации от гена с образованием РНК или белков), одинаковая для всех живущих организмов. Все известные клеточные формы жизни используют один и тот же генетический код из 20 универсальных аминокислот и стоп-сигналов, закодированных в 64 кодонах (единицах генетического кода). Трансляция генетической информации в процессе синтеза белков по заданной матрице выполняется рибосомами, состоящими из трех универсальных молекул РНК и примерно 50 белков, из которых 20 так же одинаковы для всех организмов.
В 2010 году американский биохимик Даглас Теобальд математически проверил вероятность существования LUCA [6]. Он выбрал 23 белка, встречающихся у организмов из всех трех доменов, но имеющих разную структуру у различных видов. И исследовал эти белки у 12 различных видов (по четыре из каждого домена), после чего использовал компьютерное моделирование различных эволюционных сценариев, чтобы понять, при каком из них наблюдаемая картина будет наиболее вероятной. Оказалось, что концепция, включающая существование универсального предка, значительно вероятнее концепций, где его нет. Еще более вероятна модель, основанная на существовании общего предка, но допускающая обмен генами между видами [7].
Предположение о том, что LUCA был прокариотической клеткой, похожей на современные, часто принимается по умолчанию. Однако мембраны архей и бактерий имеют разное строение (рис. 2). Получается, что общий предок должен был обладать комбинаторной мембраной. Новая информация о мембранах LUCA появилась в 2012 году, когда несколько групп ученых подробно проанализировали историю генов всех ферментов биосинтеза компонентов липидов у бактерий, архей и эукариот [8].

Рисунок 2. Строение мембранных липидов бактерий (справа) и архей (слева)
Родственными у архей и бактерий оказались ферменты для синтеза терпеновых спиртов и пришивания полярных голов к спиртам. Значит, эти реакции мог проводить и LUCA. Проще всего было предположить, что липиды LUCA состояли из одного остатка терпенового спирта, остатка фосфата и полярной группы (серина или инозитола). Подобные липиды были синтезированы искусственно. Образующиеся из них мембраны обладают высокой подвижностью по сравнению с современными мембранами, хорошо пропускают ионы металлов и малые органические молекулы. Это могло позволять древним протоклеткам поглощать готовую органику из внешней среды даже без транспортных белков.
Реконструкции LUCA методами сравнительной геномики указывают на то, что это должен быть сложный организм без обширного ДНК-генома (геном, состоящий из нескольких сотен РНК-сегментов или ДНК провирусного типа). Но даже если считать возможность существования общего предка доказанной, остается загадкой, в какой среде он мог бы появиться.

Рисунок 3. Сценарий вирусного мира в гипотезе доклеточного происхождения вирусов подпись
Предполагается, что идеальные условия для формирования жизни существовали вблизи термальных геоисточников (морских или наземных) в виде сети неорганических ячеек, обеспечивающих градиенты температуры и рН, способствующих первичным реакциям, и предоставляющих универсальные каталитические поверхности для примитивной биохимии [10].
Эти отсеки могли быть населены разнородной популяцией генетических элементов. Вначале сегментами РНК. Затем более крупными и сложными молекулами РНК (один или несколько белок-кодирующих генов). А позднее и сегментами ДНК, которые постепенно увеличивались (рис. 3).
Такие простейшие генетические системы использовали неорганические соединения из раствора и продукты деятельности других генетических систем. Сначала они должны были подчиняться индивидуальному отбору ввиду большого разнообразия. Но ясно, что важным фактором такого отбора была способность передавать генетическую информацию, то есть, копировать себя. Присутствие одновременно в одной ячейке молекул, способных копировать РНК, кодировать полезные белки и управлять синтезом новых молекул, давало больше шансов выживать в каждой отдельной ячейке. И в такой системе рано или поздно должны были появиться паразитирующие элементы. А если это так, то вирусные элементы стоят у самых истоков эволюции [11].
Возникновение паразитов — неизбежное последствие эволюционного процесса

Рисунок 4. Схематическое представление структуры модели эволюции РНК-подобной системы. На втором этапе цепочки последовательностей начинают соединяться комплементарными связями сами с собой. В результате у двух видов (cat-C и cat-A) возникает вторичная структура молекулы, которая обладает каталитическим свойством. Она ускоряет собственную репликацию (или репликацию несвернувшихся соседей). Два вида при этом приобретают паразитические свойства (par-G и par-U). Пояснения в тексте.
Таким образом, паразитарные репликаторы способствуют эволюции разнообразия, вместо того, чтобы мешать этому разнообразию. Это также делает существующую систему репликатора чрезвычайно стабильной при эволюции паразитов.
Согласно гипотезе Черной Королевы, чтобы поддержать свое существование в постоянно эволюционирующем мире, вид должен реагировать на эти эволюционные изменения и должным образом приспосабливаться к среде. Поэтому, если мы говорим о вирусах как о паразитах, мы обязаны представлять себе взаимоотношения вируса с хозяином. В борьбе с вирусом хозяева развивают новые защитные механизмы, а паразиты отвечают, развивая механизмы для атаки и взлома защиты. Этот процесс может длиться бесконечно либо до вымирания одной из противоборствующих сторон. Так множественные системы защиты составляют существенную часть геномов всех клеточных организмов, а взлом защиты — одна из основных функций генов у вирусов с большими геномами .
Механизмы клеточной защиты против вирусов
Механизмы защиты от вирусов стандартны, поскольку все вирусы уникальны, и приспособиться к каждому не представляется возможным. Это такие механизмы как:
- Деградация РНК (вирусных и клеточных) — РНК-интерференция;
- Угнетение синтеза белков (вирусных и клеточных);
- Ликвидация зараженных клеток — апоптоз (программируемая клеточная смерть);
- Воспаление.
Получается, что клетка борется с вирусом, нарушая собственные обмен веществ и/или структуру. Защитные реакции клетки — это в основном самоповреждающие механизмы.
Вирус заражает конкретную клетку потому, что его механизмы нападения направлены именно против данного типа клеток. Это такие механизмы как:
- Угнетение синтеза клеточной РНК;
- Угнетение синтеза клеточных белков;
- Нарушение клеточной инфраструктуры и транспорта;
- Подавление/включение апоптоза и других видов клеточной смерти.
Схемы защитных приемов клетки и противозащиты вирусов во многом идентичны. Вирусы и клетки применяют одни и те же приемы. Для подавления синтеза вирусных белков клетка использует интерферон, а чтобы подавить образование интерферона, вирус угнетает синтез белков.
Поскольку узнавание вируса неспецифическое, клетка не может знать намерения конкретного вируса. Она может бороться с вирусом лишь стандартными приемами, поэтому ее оборонные действия часто могут быть чрезмерными.
Понятие о вирусном геноме, типы вирусных генов, концепция генов-сигнатур
В исследовании, проведенном вирусологом Евгением Куниным и его коллегами [16], анализ последовательностей вирусных геномов выявил несколько категорий вирусных генов, принципиально отличающихся по происхождению. Можно обсуждать, какая степень дробности классификации оптимальна, но четко различаются пять классов, укладывающихся в две более крупные категории.
Гены с четко опознаваемыми гомологами у клеточных форм жизни:
- Гены, присутствующие у узких групп вирусов (обычно это гены, гомологичные генам хозяев этих вирусов).
- Гены, консервативные среди большой группы вирусов или даже нескольких групп и имеющие относительно отдаленные клеточные гомологи.
Таким образом, отличительные особенности генов-сигнатур:
- Происхождение из первичного пула генов;
- Наличие лишь очень отдаленных гомологов среди генов клеточных форм жизни, из чего можно сделать вывод, что они никогда не входили в геномы клеточных форм;
- Необходимость для репродукции вирусов.
Из всего вышесказанного следует, что эти гены переходили от вируса к вирусу (или к элементу, подобному вирусу) на протяжении четырех миллиардов лет эволюции жизни, а вирусные геномы появились благодаря перемешиванию и подгонке друг к другу генов в гигантской генетической сети, которую представляет собой мир вирусов. Многочисленные гены клеточных форм жизни также пронизывают эту сеть, прежде всего благодаря геномам крупных вирусов, таких как NCDLV и крупным бактериофагам, которые позаимствовали множество генов от своих хозяев на разных этапах эволюции. Однако большинство заимствованных генов сами по себе не критичны для репликации и экспрессии вирусного генома (исключая некоторые случаи возможного неортологичного замещения генов-сигнатур); обычно эти гены участвуют во взаимодействии между вирусом и хозяином. Таким образом, несмотря на интенсивный взаимообмен генами с хозяевами, вирусы всегда происходят от других вирусов.
Вирусы, встроенные в геном, и горизонтальный перенос генов
В процессе эволюции многие вирусы встроились в геномы клеточных форм жизни путем горизонтального переноса генов (ГПГ). Впервые горизонтальный перенос был описан в 1959 году, когда ученые продемонстрировали передачу резистентности к антибиотикам между разными видами бактерий. В 1999 году Рави Джайн, Мария Ривера и Джеймс Лейк в своей статье писали о произошедшей значительной передаче генов между прокариотами [17]. Этот процесс, по-видимому, оказал некоторое влияние также и на одноклеточные эукариоты. В 2004 году Карл Вёзе опубликовал статью, в которой утверждал, что между древними группами живых организмов происходил массивный перенос генетической информации. В древнейшие времена преобладал процесс, который он называет горизонтальным переносом генов. Причем, чем дальше в прошлое, тем это преобладание сильнее [18].
Горизонтальный перенос генов — процесс, в котором организм передаёт генетический материал другому организму, не являющемуся его потомком. Горизонтальная передача генов реализуется через различные каналы генетической коммуникации — процессы конъюгации, трансдукции, трансформации, переноса генов в составе плазмидных векторов, вирусов, мобильных генетических элементов (МГЭ).
Трансдукция — перенос бактериофагом (агентами переноса генов, АПГ) в заражаемую клетку фрагментов генетического материала клетки, исходно содержавшей бактериофаг [19]. Такой бактериофаг обычно переносит лишь небольшой фрагмент ДНК хозяина от одной клетки (донор) к другой (реципиент). В зависимости от типа трансдукции — неспецифической (общей), специфической или абортивной, геном фага или хозяина-бактерии может быть изменен тем или иным образом:
- При неспецифической трансдукции (рис. 5) ДНК клетки-хозяина включаются в частицу фага (дополнительно к его собственному геному или вместо него);
- При специфической трансдукции гены фага замещаются генами хозяина;
- При абортивной трансдукции внесённый фрагмент ДНК донора не встраивается в ДНК хозяина-реципиента, а остаётся в цитоплазме и не реплицируется. Это приводит к тому, что при клеточном делении он передаётся только одной из дочерних клеток и затем теряется в потомстве.

Рисунок 5. Схема общей трансдукции
Наиболее известным примером специфической трансдукции служит трансдукция, осуществляемая фагом λ. Поскольку этот фаг при переходе в состояние профага включается в хромосому бактерий между генами, кодирующими синтез галактозы и биотина, именно эти гены он может переносить при трансдукции.
Вот несколько примеров важных эволюционных событий, связанных с молекулярным одомашниванием:
- Ферменты теломеразы, служащие для восстановления концевых участков хромосом, возможно, ведут свое происхождение от обратных транскриптаз, кодируемых ретровирусами и ретротранспозонами [22];
- Белки RAG, играющие ключевую роль в системе адаптивного иммунитета, по-видимому, происходят от прирученных транспозаз — ферментов, кодируемых транспозонами;
- Ген Peg10, необходимый для развития плаценты, был позаимствован древними млекопитающими у ретротранспозона (рис. 6) [23].

Рисунок 6. Роль гена Peg10 в эмбриональном развитии. Ученые под руководством Рюичи Оно из Токийского медицинского университета Японии показали, что у мышей с выключенным геном Peg10 нарушается развитие плаценты, от чего эмбрион погибает через 10 дней после зачатия [24].
В 2008 году в ходе целенаправленного поиска неиспорченных вирусных генов в геноме человека исследователи нашли два очень похожих друг на друга ретровирусных гена (их назвали ENVV1 и ENVV2), которые, по всей видимости, находятся в рабочем состоянии [25]. Это гены белков оболочки ретровируса. Каждый из них входит в состав своего эндогенного ретровируса (ЭРВ), причем все остальные части этих ЭРВ давно не функционируют.
Вирусные гены ENVV1 и ENVV2 у человека и обезьян работают в плаценте и, скорее всего, выполняют следующие функции:
Таким образом, как минимум три полезных применения нашли себе вирусные гены в плаценте приматов. Это показывает, что генетические модификации, которым ретровирусы подвергают организмы, в долгосрочной перспективе могут оказаться полезными или даже определить развитие вида. И с учетом всего вышесказанного древо доменов должно выглядеть как на схеме ниже (рис. 7).

Рисунок 7. Горизонтальный перенос генов в рамках трехдоменного дерева
Заключение
Возникновение паразитов — обязательная черта эволюционирующих систем репликаторов, а соревнование хозяев и паразитов движет эволюцию тех и других. Любой организм является результатом миллионов лет борьбы клеток с невероятно разнообразным миром вирусов. Их действия и их эволюция пронизывают всю историю клеточной эволюции, и сейчас меняется само наше представление о них. Когда-то вирусы считали деградировавшими клетками, но чем больше мы узнаем о вирусах, тем очевиднее, что их роль в общей эволюции значительна. И невероятно много нам еще предстоит узнать.
Читайте также:

