Вакцинация или противовирусные препараты
Обновлено: 15.04.2024
Классификация вирусных вакцин. Типы вирусных вакцин.
Современной науке известны сотни видов патогенных вирусов, относящихся к 26 семействам, избирательно поражающим различные системы организма человека и животных. Природное многообразие вирусных болезней вызывало необходимость наряду с санитарно-гигиеническими мерами прибегнуть к специфической профилактике с использованием широкого круга вакцинных препаратов.
Вакцинопрофилактика занимает ведущее место в борьбе со многими вирусными заболеваниями человека и животных. Несмотря на большое разнообразие вирусов и вызываемых ими заболеваний, имеются общие принципы приготовления и применения вирусных вакцин. Однако в настоящее время не все вирусные болезни в одинаковой степени удается контролировать с помощью вакцинации.
Вакцинация должна сопровождаться развитием иммунологической памяти. В идеале, это поддержание специфических антител в высокой концентрации в сыворотке крови и на месте внедрения вируса. В тоже время Т-клетки, ответственные за специфический клеточный иммунитет, должны находиться в состоянии готовности быстро синтезировать свои летальные продукты (т.е. гранзимы и перфорины), когда происходит инфицирование. Все существующие на сегодня вакцины можно разделить на три общие группы: инактивированные (убитые), живые (аттенуированные) и компонентные (субъединичные) вакцины. Каждая из этих категорий вакцин имеет свои преимущества и недостатки.
В зависимости от технологии изготовления различают несколько типов вирусных вакцин:
1. Живые реплицирующиеся вакцины:
— вакцины из природно ослабленных или гетерологичных вирусов;
— вакцины из вирусов, аттенуированных пассажами в гетерологичных организмах или в культурах клеток при обычной или пониженной температуре, или реассортацией вирусных генов.

2. Нереплицирующиеся вакцины, содержащие природные вирусные антигены:
- вакцины из инактивированных целых вирионов и неструктурных вирусных белков;
- вакцины из нативных вирусных субъединиц.
3. Вакцины, полученные с помощью рекомбинантной ДНК или других новых технологий:
- вакцины, полученные путем делеции гена (генов) или точечного мутагенеза;
- вакцины на основе вирусных белков, экспрессированных in vitro в клетках эукариотов или прокатиотов;
- вакцины из вирусных белков, собранных в вирусоподобные частицы;
- вакцины, экспрессирующие вирусные антигены с помощью вирусных векторов;
- вакцины на основе вирусных химер;
- ДНК-вакцины.
4. Синтетические полипептидные вакцины.
Живые вакцины содержат авирулентные штаммы вирусов, аттенуированные разными способами, и отличаются способностью размножаться в привитом организме (реплицирующиеся антигены). Остальные типы вакцин готовят из инактивированных вирусов или их антигенных и иммуногенных компонентов (нереплицирующиеся антигены).
Используя другие принципы классификации, вакцинные препараты можно разделить на две большие группы: цельновирионные и компонентные (субъединичные). Причем к первой группе относятся как традиционные живые, так и инактивированные вакцины. Живые гомологичные вакцины, в свою очередь, могут различаться способом получения и быть представленными природно аттенуированными или искусственно ослабленными штаммами, включая рекомбинантные и реассортантные, а также штаммы, аттенуированные цельнонаправленными изменениями генома биотехнологическими методами.
К компонентным (субъединичным) вакцинам можно отнести все, которые не входят в рубрику цельновирионных вакцин. Прежде всего, сюда относятся вакцины, полученные из компонентов вирионов или вирус-инфицированных клеток после их разрушения. Кроме них к этой категории относятся субъединичные вакцины, приготовленные из вирусных белков, экспрессируемых клонированными вирусными генами в эукариотических или прокариотических системах. Сюда же можно отнести живые рекомбинантные вакцины, которые по своей сути являются реплицирующимися субъединичными вакцинами. Клонированные гены, реплицируясь в составе вирусного вектора, обеспечивают экспрессию белков, ответственных за индукцию специфического иммунитета.
Вакцины на основе вирусспецифических пептидов, получаемых синтетическим путем, в известном смысле, тоже можно отнести к разряду субъединичных (эпитопных) вакцин.
Анализ имеющихся данных свидетельствует о достаточно высокой эффективности многих вирусных вакцин, применяемых в медицинской и ветеринарной практике. Это, прежде всего, относится к живым вакцинам, применяемым для контроля таких массовых и опасных заболеваний человека, как полиомиелит, желтая лихорадка, корь, эпидемический паротит, краснуха и др. Аналогичным примером из практики ветеринарной медицины могут служить живые вакцины против чумы свиней, крупного рогатого скота и плотоядных, против ньюкаслской болезни и другие. Примером инактивированных вакцин могут служить вакцины против полиомиелита, гриппа, ящура и многих других болезней.
Некоторые из живых вакцин (оспа человека, полиомиелит, желтая лихорадка, корь, чума крупного рогатого скота, классическая чума свиней и др.) отвечают требованиям безопасности (генетическая стабильность, отсутствие реверсии, слабая реактогенность), обеспечивают длительный напряженный иммунитет и могут служить образцом для вновь создаваемых вакцинных препаратов.
Возбудители многих вирусных заболеваний (полиомиелит, грипп, ящур, катаральная лихорадка овец, чума лошадей и др.) существуют в виде нескольких антигенных типов. Поскольку иммунизация против одного из этих типов не защищает от заражения другими, эффективная профилактика возможна только при вакцинации поливалентной вакциной, содержащей антигены нескольких антигенных типов данного вируса. Вакцины, содержащие антигены более чем одного вида возбудителя, называют комбинированными (ассоциированными).
Большинство применяемых в настоящее время вакцин содержит антигены, идентичные или подобные антигенам вирулентного вируса, против которого предполагается создать иммунитет. Такие вакцины называют гомологичными. В некоторых случаях для приготовления вакцин используют гетерологичные вирусы, содержащие перекрестно-реагирующие антигены и создающие достаточный иммунитет. Такие вакцины называются гетерологичными.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Нужно ли лечить ОРВИ у детей? Препараты для повышения иммунитета
Почти 90% всех инфекционных заболеваний это - острые респираторные вирусные инфекции (ОРВИ), к которым также относится и грипп. Особенно таким простудным заболеваниям подвержены дети, они заболевают простудой в 4 раза чаще, чем взрослые. В среднем ежегодно от острых респираторных заболеваний (ОРЗ), в том числе ОРВИ и гриппа, страдает порядка 40 млн. населения России, и эта цифра не сильно изменяется из года в год. Однако можно смело предположить, что число заболевших на деле гораздо выше, ведь очень многие предпочитают лечиться дома и не посещать врача. Некоторые и вовсе принимают ОРЗ за обычную аллергию.
В частой заболеваемости детей ОРВИ есть определенная тенденция, и она сложилась не случайно. Как правило, дети до 9 месяцев практически не болеют, особенно, если они получают материнское молоко. На самом деле иммунитет ребенка пока слаб, но сказывается его поддержка в виде особых защитных белков иммунной системы матери, которые малыш получил, еще будучи в утробе. Кроме того, некоторые защитные белки попадают в организм ребенка из материнского молока. Таким образом, то, что иммунная система пока не в состоянии получить сама, приходит к ребенку от мамы. Однако срок жизни этих защитный белков ограничен, и с момента их гибели ребенок становится уязвим для инфекционных агентов.
Также риск развития ОРВИ значительно возрастает, если ребенок находится на искусственном вскармливании, если он родился недоношенным, при беременности с осложнениями. К сожалению, сегодня все это перестало быть редкостью.
Склонность детей к ОРВИ является причиной того, что их организм только "знакомится" с бактериями и вирусами. "Знакомство" это и есть простуда, и происходит оно повсеместно: дома, в детском саду, на улице, в транспорте, в школе. Поэтому оградить ребенка от бактерий и вирусов, вызывающих ОРЗ, просто невозможно, да это и не нужно, ведь в скором времени иммунитет ребенка будет знаком со многими из них и сможет давать адекватный ответ, защищая организм от этих инфекций.

Повышение иммунитета как метод лечения ОРВИ у детей

Лечение ОРВИ, безусловно, комплексное. В него входят методы борьбы с интоксикацией - обильное питье, приём витамина С для того, чтобы защитить сосуды от негативных влияний вируса. Возможно применение и некоторых противовирусных препаратов, однако это эффективно в первые часы заболевания, когда вирус еще не успел размножиться в клетках и разрушить их. Отдельное место в терапии ОРВИ отводится иммуномодуляторам - лекарствам, которые стимулируют работу иммунной системы. Они заслуживают внимательного рассмотрения.
Стимулировать иммунитет способны препараты на растительной основе, такие как элеутерококк, женьшень, боярышник, "Иммунал", содержащий экстракт эхинацеи. Последний препарат проходил множество клинических исследований, показал отличные результаты при отсутствии побочных эффектов и нежелательных реакций у пациентов, переносящих ОРВИ. Он показан для применения с четырехлетнего возраста. Все эти препараты стоят недорого, поэтому доступны и безвредны благодаря своему натуральному происхождению. Их можно использовать для профилактики или уже в первые часы болезни. Хорошим иммуностимулирующим эффектом обладает также прополис. Помните, что профилактический прием средств, стимулирующих работу иммунной системы, необходимо начинать за несколько недель до начала сезона заболеваний, так как иммунитету требуется определенное время на выработку защитных клеток и белков.
Довольно широко при ОРВИ применяются лекарства, в состав которых входит интерферон - белок, вырабатываемый клетками человека в ответ на вторжение вируса. Интерфероны защищают организм от вирусных атак, поэтому при бактериальной инфекции прием этих препаратов лишается смысла. В аптеках продаются лекарства, содержащие уже готовый интерферон, полученный от донора ("Лейкинферон", "Виферон", "Гриппферон"). Особенно приятно, что они универсальны в борьбе с любыми вирусами, чего не скажешь о многих противовирусных препаратах. Для детей старшего возраста (примерно с 3 лет) разрешается применение стимуляторов выработки собственного интерферона ("Арбидол", "Кагоцел", "Циклоферон").
Стоит ли делать прививки ребенку, если он часто болеет?
- Вернуться в оглавление раздела "Профилактика заболеваний"
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Вакцины. Виды антигенов вакцин. Классификация вакцин. Виды вакцин. Живые вакцины. Ослабленные ( аттенуированные ) вакцины. Дивергентные вакцины.
Вакцины — иммунобиологические препараты, предназначенные для активной иммунопрофилактики, то есть для создания активной специфической невосприимчивости организма к конкретному возбудителю. Вакцинация признана ВОЗ идеальным методом профилактики инфекционных заболеваний человека. Высокая эффективность, простота, возможность широкого охвата вакцинируемых лиц с целью массового предупреждения заболевания вывели активную иммунопрофилактику в большинстве стран мира в разряд государственных приоритетов. Комплекс мероприятий по вакцинации включает отбор лиц, подлежащих вакцинации, выбор вакцинного препарата и определение схемы его использования, а также (при необходимости) контроль эффективности, купирование возможных патологических реакций и осложнений. В качестве Аг в вакцинных препаратах выступают:
• цельные микробные тела (живые или убитые);
• отдельные Аг микроорганизмов (наиболее часто протективные Аг);
• токсины микроорганизмов;
• искусственно созданные Аг микроорганизмов;
• Аг, полученные методами генной инженерии.
Большинство вакцин разделяют на живые, инактивированные (убитые, неживые), молекулярные (анатоксины) генно инженерные и химические; по наличию полного или неполного набора Аг — на корпускулярные и компонентные, а по способности вырабатывать невосприимчивость к одному или нескольким возбудителям — на моно- и ассоциированные.
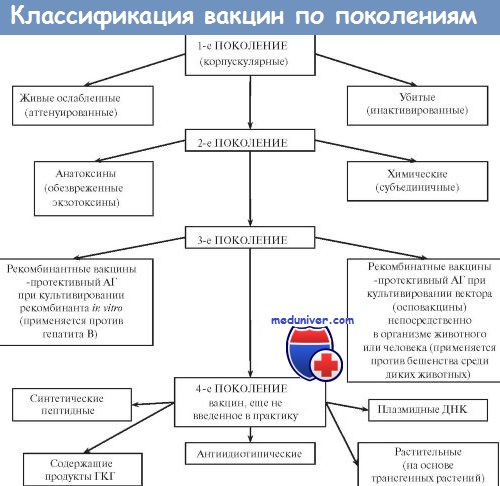
Живые вакцины
Живые вакцины — препараты из аттенуированных (ослабленных) либо генетически изменённых патогенных микроорганизмов, а также близкородственных микробов, способных индуцировать невосприимчивость к патогенному виду (в последнем случае речь идёт о так называемых дивергентных вакцинах). Поскольку все живые вакцины содержат микробные тела, то их относят к группе корпускулярных вакцинных препаратов.
Иммунизация живой вакциной приводит к развитию вакцинального процесса, протекающего у большинства привитых без видимых клинических проявлений. Основное достоинство живых вакцин— полностью сохранённый набор Аг возбудителя, что обеспечивает развитие длительной невосприимчивости даже после однократной иммунизации. Живые вакцины обладают и рядом недостатков. Наиболее характерный — риск развития манифестной инфекции в результате снижения аттенуации вакцинного штамма. Подобные явления более типичны для противовирусных вакцин (например, живая полиомиелитная вакцина в редких случаях может вызвать полиомиелит вплоть до развития поражения спинного мозга и паралича).
Ослабленные ( аттенуированные ) вакцины
Ослабленные (аттенуированные) вакцины изготавливают из микроорганизмов с пониженной патогенностью, но выраженной иммуногенностью. Введение вакцинного штамма в организм имитирует инфекционный процесс: микроорганизм размножается, вызывая развитие иммунных реакций. Наиболее известны вакцины для профилактики сибирской язвы, бруцеллёза, Ку-лихорадки, брюшного тифа. Однако большая часть живых вакцин — противовирусные. Наиболее известны вакцина против возбудителя жёлтой лихорадки, противополи-омиелитная вакцина Сэйбина, вакцины против гриппа, кори, краснухи, паротита и аденовирусных инфекций.
Дивергентные вакцины
В качестве вакцинных штаммов используют микроорганизмы, находящиеся в близком родстве с возбудителями инфекционных болезней. Аг таких микроорганизмов индуцируют иммунный ответ, перекрёстно направленный на Аг возбудителя. Наиболее известны и длительно применяются вакцина против натуральной оспы (из вируса коровьей оспы) и БЦЖ для профилактики туберкулёза (из микобактерий бычьего туберкулёза).
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Правительство Великобритании собрало рабочую группу, чтобы к осени получить препараты от COVID-19 в таблетках или капсулах. Инвестиционный аналитик объясняет, почему подобные лекарства все еще не появились. Ученые рассуждают, почему заболеваемость в Индии бьет антирекорды. Об этом — в обзоре зарубежных СМИ
Правительство Великобритании создало рабочую группу, которая должна сделать так, чтобы к осени появились хотя бы два лекарства для лечения COVID-19 на ранней стадии в виде таблеток или капсул. Об этом пишет The Guardian.
Самые эффективные лекарства, что есть сейчас, не убивают вирус, а сдерживают иммунную систему человека. Их назначают, когда болезнь перешла в тяжелую форму, и обычно вводят через шприц или капельницу. Хотя эти препараты заметно снизили смертность, было бы здорово иметь средства, которые можно принимать дома и которые помогают выздороветь без госпитализации. Что-то такое и попытаются найти среди существующих или разработать с нуля в Великобритании, готовясь к новой волне пандемии.
The Guardian считает, что усилия сосредоточат на моноклональных антителах — белках наподобие тех, которые вырабатывает наш организм в ответ на инфекцию, но произведенных в биореакторах с запрограммированными для этого клетками. Правда, такие препараты получаются дорогими, к тому же есть опасения, что они не справятся с новыми вариантами коронавируса.
Почему все еще нет ни одного противовирусного препарата, справляющегося с SARS-CoV-2
За несколько дней до того, как правительство Великобритании объявило о своих планах, STAT обсудил поиски и разработки лекарств от COVID-19 с руководителем отдела биотехнологий консалтинговой компании Evercore ISI Джошем Шиммером. Поводом послужил его скептический отчет.
Шиммер с самого начала прогнозировал, что клинические исследования пойдут со скрипом. За все время на рынке появилось очень мало противовирусных препаратов. Наука по-прежнему плохо понимает взаимодействие вирусов с иммунной системой — достаточно вспомнить, что одни умирают от COVID-19, а другие переносят инфекцию вообще без симптомов.

Трудность с лекарствами заключается в том, что большинство людей с COVID-19 выздоравливает, причем обычно очень быстро. Когда набор данных маленький, сложно понять, помогло ли лекарство или все было бы хорошо и без него.
В отличие от вакцин, которые защищают как минимум месяцами, противовирусные препараты нужно назначить в строго определенный момент. Вскоре после этого они становятся бесполезными. Их не станешь принимать для профилактики каждый день, к тому же большинству людей они вообще не понадобятся. Все это надо как-то учесть, продумывая клиническое исследование, чтобы получить ясный и убедительный ответ.
Поскольку биологические процессы во время коронавирусной инфекции во многом остаются загадкой, компании испытывают самые разные средства и надеются, что какое-то сработает. А компаний появилось так много, что распознать действительно эффективный препарат становится еще труднее. Вдобавок фармацевтические компании, собирая и позже презентуя данные, намеренно или невольно их искажают. С COVID-19 отличить сигнал от шума чрезвычайно тяжело.
Клинические исследования можно было бы централизовать (в Великобритании так поступили еще в прошлом году, и именно там выявили самые действенные на сегодняшний день препараты для лечения COVID-19 — прим. ТАСС). Но централизованная система плохо сочетается с рыночным подходом, а этот подход в прошлом давал самые лучшие результаты. В такой системе будет меньше попыток, зато каждая даст более надежные данные. Возможно, нужен компромисс.
Почему вторая волна в Индии стала кошмарной
После прошлогодней вспышки COVID-19 в Индии думали, что худшее позади. Но в марте стала подниматься новая волна. На этой неделе число случаев, выявленных за сутки, превысило 300 тыс. — это больше, чем где-либо за все время, и примерно втрое превышает осенний пик. О возможных причинах пишет Nature.
По расчетам, сделанным зимой, в некоторых районах крупных индийских городов переболело больше половины жителей, а всего по стране — около 271 млн человек, или пятая часть населения. Казалось, следующая волна не поднимется выше первой. Вот только оценка, возможно, получилась заниженной.
Число переболевших вывели из тестов на антитела, не учтя, что коронавирус мог распространяться неравномерно. Ученые, опрошенные Nature, предполагают, что в прошлом году болели в основном городские бедняки. Люди побогаче изолировались, а теперь потеряли бдительность и стали заражаться. Впрочем, вряд ли дело только в этом.
Почему с вирусами нельзя бороться антибиотиками? А чем можно? Почему разработать эффективный противовирусный препарат так сложно? А вакцина — это лекарство? Разбираем популярные вопросы, мифы и сомнения
Вирусы отличаются от бактерий и по строению, и по способу размножения. Одинаковые препараты не применяются для тех и других.
Самым эффективным средством против вирусов остается наш собственный иммунитет, но если он ослаблен — могут быть назначены препараты, подавляющие вирусную нагрузку.
Созданию эффективных препаратов мешают изменчивость вирусов и их способность захватывать наши собственные клетки.
Вакцина — не лекарство, а скорее "обучающий курс" для нашего собственного иммунитета. В идеале вакцина лучше, но для некоторых болезней ее нет — а вот лекарства есть.
Почему вирус нельзя убить антибиотиком?
Антибиотики часто выписывают при инфекционных заболеваниях. Из-за этого может сложиться представление, что их нужно пить при любых инфекциях. На самом деле они действуют только против бактерий. Хотя у бактериальных и вирусных болезней симптомы часто похожи (жар, насморк, кашель, слабость), у их возбудителей разная природа. Они отличаются и по строению, и по способу выживания.
Бактерии — одноклеточные организмы, которые размножаются примерно так же, как и человеческие клетки. Антибиотик может нарушить целостность бактериальной клетки (например, вмешаться в процесс формирования клеточной стенки) или сбить механизм её размножения. Важный момент: препарат должен действовать именно на чужеродные клетки, не затрагивая наши.
Вирусы устроены иначе. У них нет собственной клетки, они живут и размножаются за счет чужих — захватывая их и используя как фабрики по производству своих копий. Созревшие вирусные частицы вырываются наружу, разрушая клетку и заражая ее соседей. Но антибиотик, заточенный под взаимодействие с бактериальной клеткой, не причинит вреда ни отдельной вирусной частице, ни уже зараженной ею человеческой клетке.
Как тогда с ним бороться?
Обычно с этим справляется сам организм, и помощь ему не требуется. Но бывает, что иммунитет ослаблен, и болезнь изначально развивается по тяжелому сценарию — либо вирус умеет обходить защиту (например, поражает сами иммунные клетки, как это делает ВИЧ). Тогда врачи назначают препараты, которые действуют непосредственно на вирусные частицы.
Часть препаратов, попадая в кровь, связываются с белками на поверхности вируса, которые он использует для прикрепления к клетке, и блокируют их. Если вирус уже попал в клетку, можно попытаться нарушить механизм его размножения. В этом случае используют вещества, близкие по структуре к фрагментам вирусного генетического кода (нуклеотидам). Когда они проникают в зараженную клетку, то заменяют собой нормальные части вирусной ДНК, из-за чего ему не удается создавать свои копии.
Как разрабатывают противовирусные препараты?
Чтобы создать работающее лекарство, ученым нужно изучить вирус — его строение, принцип заражения, химические процессы, которые его сопровождают. Препарату всегда нужна мишень, на которую он будет действовать. Например, у вирусов гриппа такими мишенями служат белки гемагглютинин, нейраминидаза (на них указывают буквы H и N в названиях штаммов) и M2. Каждая группа препаратов действует только на один тип белков — точнее, даже на их составные части.
Вещества, которые ученые сочли перспективными, сначала тестируются in vitro — в пробирке, на культуре клеток. Но даже если результаты показали, что концентрация вирусной ДНК снижается, результаты могут не подтвердиться в живых организмах. Вещество может плохо всасываться в кровь или изменять свою структуру, попадая в желудок или кровь. Точно установить причины плохих результатов в клинических испытаниях не всегда удается.
Почему эффективных препаратов так мало?
За 60 лет регулирующие органы разных стран одобрили несколько десятков препаратов, но лишь против 5% всех известных человеческих вирусов. Это вирусы гриппа, ветряной оспы, папилломы человека, герпеса, респираторно-синцитиальный вирус, вирусы гепатита С и B, а также ВИЧ. Но и среди них большинство не способны полностью изгнать вирус из организма, а могут только остановить или затормозить его распространение.
Одна из сложностей в том, что вирусы очень быстро размножаются и мутируют. Фармакологи могут долго подбирать соединение, которое свяжется с вирусным белком определенной структуры, — но в ходе мутации его структура может измениться, и вирус приобретет устойчивость к препарату. Именно это произошло с первыми лекарствами от вируса гриппа, которые были заточены под белок M2. Оказалось, что ген, который кодирует этот белок, склонен к частым мутациям. Сейчас эти препараты не рекомендуют применять без поддержки других.
У некоторых вирусов (например, того же гриппа) отдельные частицы имеют очень разные форму и размеры, с разным числом белков на поверхности. Молекулы препарата могут не закрепиться на мелких или нестандартных частицах, и они все равно найдут способ проникнуть в клетки и заразить их. Эффект от лечения будет, но хуже ожидаемого.
Некоторые вирусы трудно "выкурить" из захваченных ими клеток. Например, ВИЧ проникает в Т-лимфоциты — иммунные клетки, благодаря которым организм защищает себя от инфекций. Вирус встраивается в их геном, и в результате клетки производят уже зараженные копии самих себя. Сегодня антивирусные препараты могут блокировать воспроизведение генома вируса, мешать ему встраиваться в ДНК клеток, предотвращают сборку новых копий — но достать его внутри клеток они не могут.
Чем лекарство отличается от вакцины? Что лучше?
Вакцина стимулирует выработку собственного иммунитета у человека: знакомит иммунную систему с вирусом, а дальше сама вырабатывает защиту — антитела и клетки-киллеры, которые в будущем могут дать отпор настоящему вирусу. При этом вирус в вакцине может быть как живым, но ослабленным, так и мертвым. А в ряде случаев используют только белки этого вируса.
Антитела, в отличие от препаратов, вырабатываются естественным путем. Это белковые молекулы, которые подходят к вирусным белкам, как ключ к замочной скважине. В каком-то смысле можно сказать, что организму виднее, как именно ему бороться с инфекцией. Он сам распознает патоген, сам запускает защитную реакцию — и все это происходит быстрее, чем мы поймем, что заражены.
Но в некоторых случаях вакцину оказывается разработать сложнее, чем лекарство. Например, вакцины от ВИЧ до сих пор нет, а вот существующие препараты (если их начать принимать как можно раньше и делать это регулярно) позволяют вести полноценную жизнь. Также пока нет и вакцины от гепатита С — зато современные препараты позволяют изгнать вирус из организма почти в 100% случаев.
Читайте также:

